הבדלים בין גרסאות בדף "מדריך לשימוש בנוגדי הקרישה החדשים - NOACS בפרפור פרוזדורים על פי הנחיות האיגוד האירופאי לקרדיולוגיה מ-2012"
| שורה 153: | שורה 153: | ||
===התערבות כירורגית או אבלציה=== | ===התערבות כירורגית או אבלציה=== | ||
| − | כרבע מהמטופלים הזקוקים לטיפול נוגד קרישה צריכים לבצע הפסקה זמנית של הטיפול תוך שנתיים מתחילת הטיפול. בעת ההחלטה מתי להפסיק ולהתחיל מחדש את התרופה, יש לקחת בחשבון הן את מאפייני המטופל (תפקוד כליות, גיל, היסטוריה של סיבוכי דימום ותרופות נלוות) והן גורמים כירורגיים. טבלה 3 מסכמת את המידע הזה עבור תרופות ה-NOACs השונות. | + | כרבע מהמטופלים הזקוקים לטיפול נוגד קרישה צריכים לבצע הפסקה זמנית של הטיפול תוך שנתיים מתחילת הטיפול. בעת ההחלטה מתי להפסיק ולהתחיל מחדש את התרופה, יש לקחת בחשבון הן את מאפייני המטופל (תפקוד כליות, גיל, היסטוריה של סיבוכי דימום ותרופות נלוות) והן גורמים כירורגיים. טבלה 3 מסכמת את המידע הזה עבור תרופות ה-NOACs השונות. ההמלצה הינה לפתח הנחיות מוסדיות ומדיניות לכלל בתי החולים באשר לניהול ניגוד הקרישה לאחר ניתוח במסגרות כירורגיות שונות, שתופץ באופן נרחב ותהיה נגישה בקלות. |
אף על פי שניתן לבצע התערבויות נפוצות ללא סיכון משמעותי לדימום (כגון, הליכים דנטליים מסוימים או התערבויות ל[[קטרקט]] או ל[[גלאוקומה]]) בזמן רמות השפל של ה-NOACs (כלומר, 12 או 24 שעות לאחר הנטילה האחרונה, בהתאם למשטר מינון של פעמיים ביום או של פעם ביום), ייתכן שיהיה מעשי יותר לקבוע את מועד ההתערבות ל-24-18 שעות לאחר הנטילה האחרונה, ולאחר מכן להתחיל את התרופה מחדש 6 שעות לאחר מכן, כלומר, לדלג על מנה אחת של NOAC הניטלת פעמיים ביום. כשמדובר על הליכים עם סיכון שולי לדימום, מומלץ להפסיק את תרופות ה-NOACs {{כ}}24 שעות לפני ההליך האלקטיבי בקרב מטופלים עם תפקוד כליות תקין, וכשמדובר על הליכים עם סיכון לדימום משמעותי, יש ליטול את ה-NOAC האחרונה 48 שעות לפני כן. | אף על פי שניתן לבצע התערבויות נפוצות ללא סיכון משמעותי לדימום (כגון, הליכים דנטליים מסוימים או התערבויות ל[[קטרקט]] או ל[[גלאוקומה]]) בזמן רמות השפל של ה-NOACs (כלומר, 12 או 24 שעות לאחר הנטילה האחרונה, בהתאם למשטר מינון של פעמיים ביום או של פעם ביום), ייתכן שיהיה מעשי יותר לקבוע את מועד ההתערבות ל-24-18 שעות לאחר הנטילה האחרונה, ולאחר מכן להתחיל את התרופה מחדש 6 שעות לאחר מכן, כלומר, לדלג על מנה אחת של NOAC הניטלת פעמיים ביום. כשמדובר על הליכים עם סיכון שולי לדימום, מומלץ להפסיק את תרופות ה-NOACs {{כ}}24 שעות לפני ההליך האלקטיבי בקרב מטופלים עם תפקוד כליות תקין, וכשמדובר על הליכים עם סיכון לדימום משמעותי, יש ליטול את ה-NOAC האחרונה 48 שעות לפני כן. | ||
גרסה מ־00:28, 19 באוקטובר 2015
|
| ||
|---|---|---|
| מדריך לשימוש בנוגדי הקרישה החדשים בפרפור פרוזדורים | ||
| [[File:|250px]]Property "Image page" (as page type) with input value "File:" contains invalid characters or is incomplete and therefore can cause unexpected results during a query or annotation process. | ||
| הוועדה המקצועית | האיגוד הקרדיולוגי בישראל | |
| עריכה | פרופ' דורון זגר | |
| תחום | קרדיולוגיה | |
| תאריך פרסום | מאי 2015 | |
| הנחיות קליניות מתפרסמות ככלי עזר לרופא/ה ואינן באות במקום שיקול דעתו/ה בכל מצב נתון | ||
לערכים נוספים הקשורים לנושא זה, ראו את דף הפירושים – פרפור פרוזדורים
תרגום סיכום המלצות האיגוד האירופאי לקרדולוגיה לשנת 2012
פרפור פרוזדורים הוא הפרעת קצב ששכיחותה נמצאת בעליה מתמדת עם הזדקנות האוכלוסייה. הפרעה זו כרוכה בתחלואה ותמותה ניכרות, בעיקר בשל הסיכון הכרוך בה לאירועים מוחיים. בשנים האחרונות עלתה מאוד המודעות לצורך בטיפול נוגד קרישה בחולים הסובלים מפרפור פרוזדורים. במקביל, נכנסו לשימוש שלוש תרופות נוגדות קרישה חדשות המהוות תחליף לטיפול המסורתי בנוגדי קרישה פומיים (OAC, Oral anticoagulant) כדוגמת Coumadin (Warfarin sodium).
מבחינת היעילות והבטיחות בהשוואה ל-Coumadin הוכיחו התרופות שוויון, ולעתים קרובות עליונות והן מהוות מהפיכה של ממש בטיפול בחולים אלה. עם זאת, נוגדי הקרישה החדשים מציגים בפני הרופא המטפל אתגרים באשר לבחירת התרופה והמינון המתאימים לכל חולה, כמו גם ניהול אירועים דוגמת ניתוח או דימום. האיגוד האירופי לקרדיולוגיה (ESC, European Society of Cardiology) הוציא שני מסמכים העוסקים בטיפול בפרפור פרוזדורים: עדכון של קווי ההנחיה משנת 2012 ומדריך מעשי לרופא המטפל המתאר את נוגדי הקרישה החדשים ועוסק בהיבטים השונים של הטיפול בתרופות חדשות אלה[1],[2].
מכיוון שמדובר במסמך אירופי יתכנו אי התאמות לגבי חלק מהתרופות בישראל. מסמך זה אינו מהווה תחליף לעיון בעלון לרופא של התרופות המוזכרות בו.
הבעיה העיקרית בטיפול נוגד קרישה בחולי פרפור פרוזדורים היא העובדה שחולים רבים הזקוקים לטיפול חשוב זה אינם מקבלים אותו, ואילו מבין אותם חולים שעדיין מקבלים Coumadin, רבים אינם מאוזנים כראוי.
נוגדי קרישה פומיים חדשים (NOACs, New oral anticoagulants) הופיעו כחלופה לאנטגוניסטים לויטמין K (VKAs, vitamin K antagonists) למניעת אירועים תרומבואמבוליים בקרב מטופלים עם פרפור פרוזדורים שאינו ממקור מסתמי. על מנת לממש את ההבטחה הגדולה הטמונה בתרופות אלו מבחינות רבות (השפעה ניתנת לחיזוי ללא צורך בניטור, אינטראקציות מעטות יותר עם מזון ותרופות, מחצית חיים קצרה יותר בפלסמה ויחס תועלת/בטיחות טוב יותר), יצריך השימוש הנכון ב-NOACs גישות חדשות בהיבטים יומיומיים רבים.
נקודות מפתח
- ל-NOACs יש יעילות, בטיחות ונוחות טובות יותר לעומת אנטגוניסטים לויטמין K ויש על כן להעדיף את אחת מה-NOACs - מעכב תרומבין ישיר [Pradaxa (Dabigatran etexilate)] או מעכב פומי של פקטור Xa [למשל Xarelto (Rivaroxaban) או Eliquis (Apixaban)] - במקום אנטגוניסטים לויטמין K בקרב רוב המטופלים עם פרפור פרוזדורים
- אין די ראיות להמלצה על NOAC אחד לעומת האחר, אף על פי שייתכן כי חלק ממאפייני המטופל, ההיענות לתרופה, הסבילות והעלות עשויות להוות שיקולים חשובים בעת בחירת התכשיר
- היעילות של אספירין במניעת שבץ מוחי היא חלשה, עם פוטנציאל לנזק, מאחר שהסיכון לדימום משמעותי (ולדימום תוך-גולגולתי) עם אספירין אינו שונה באופן מובהק מהסיכון עם תרופות נוגדות קרישה פומיות, במיוחד בקרב קשישים
- יש להגביל את השימוש בטיפול נוגד טסיות (טיפול משולב באספירין וב-Clopidogrel או, ביעילות פחותה, אספירין בלבד) למניעת שבץ מוחי בפרפור פרוזדורים לאותו מיעוט של מטופלים שמסרבים לכל צורה של תרופות נוגדות קרישה פומיות
- ציון CHA2DS2-VASc טוב יותר בזיהוי מטופלים עם פרפור פרוזדורים עם "סיכון נמוך מאד" והוא טוב באותה מידה (אם לא יותר) מציונים כגון ה-CHADS2, בזיהוי מטופלים שילקו בשבץ ובתרומואמבוליזם
- ציון HAS-BLED מאפשר לקלינאים לבצע הערכה מושכלת באשר לסיכון לדימום, וחשוב עוד יותר, הוא גורם להם לחשוב על גורמי סיכון לדימום שניתן לתקנם. בקרב מטופלים עם ציון HAS-BLED של 3 או יותר, מומלץ לנהוג בזהירות ולקיים בדיקות שגרתיות, וכן להשתדל לפעול לתיקון גורמי הסיכון שבאופן פוטנציאלי הם הפיכים. אין להשתמש בציון HAS-BLED גבוה כשלעצמו כדי להימנע מטיפול נוגד קרישה
הערכת סיכון לשבץ ולדימום
מקובל לחלק את פרפור הפרוזדורים למקרים שהם על רקע מסתמי או שהם על רקע לא מסתמי. במסמך זה, המונח "פרפור פרוזדורים על רקע מסתמי" מתייחס לפרפור על רקע מחלה מסתמית ריאומטית (בעיקר היצרות של המסתם המיטראלי) או למסתמי לב תותבים.
הנחיות האיגוד האירופי לקרדיולוגיה מדגישות את הצורך בריבוד הסיכון לשבץ, תוך דגש מיוחד על זיהוי מטופלים ב"סיכון נמוך מאד", שאינם זקוקים לשום טיפול אנטיתרומבוטי ומפרטות את הראיות לשימוש בתרופות נוגדות הקרישה הפומיות החדשות כחלופות לטיפול באנטגוניסטים לויטמין K.
הסיכון לשבץ עולה בצורה רצופה ככל שמתרבים גורמי הסיכון. עד לאחרונה, התרופות נוגדות הקרישה הפומיות הזמינות היחידות היו התרופות ממשפחת אנטגוניסטים לויטמין K (למשל, Coumadin), ועל אף מגבלותיהן, רופאים רבים טיפלו באנטגוניסטים לויטמין K באופן נרחב, ללא קשר לרמת הסיכון. במקרים בהם לא נעשה שימוש באנטגוניסטים לויטמין K, לעיתים קרובות ניתן במקום זאת אספירין.
ההוכחות למניעה יעילה של שבץ באמצעות אספירין בקרב מטופלים עם פרפור פרוזדורים הן חלשות, וקיים פוטנציאל לנזק, כיוון שהסיכון לדימום בכלל או דימום תוך-גולגולתי עם אספירין אינו שונה באופן מובהק מזה שעם נוגדי קרישה פומיים, במיוחד בקרב קשישים. שילוב של אספירין ו-Clopidogrel יעיל יותר מאשר אספירין לבדו אך כרוך גם בסיכון מוגבר לדימום. בהתחשב בזמינות של NOACs, יש להגביל את השימוש בטיפול נוגד טסיות (כגון אספירין עם או בלי Clopidogrel) למניעת שבץ בקרב מטופלים עם פרפור פרוזדורים לאותה קבוצה קטנה של מטופלים שמסרבים לכל צורה של נוגדי קרישה. במקרים אלה יש להעדיף שילוב של Clopidogrel ואספירין על פני אספירין לבדו.
הנחיות אלה מדגישות מאוד פרקטיקה שמתמקדת בזיהוי מטופלים עם פרפור פרוזדורים המצויים ב"סיכון נמוך מאד" (כלומר, "מתחת לגיל 65 ועם Lone AF") שאינם זקוקים לשום טיפול אנטיתרומבוטי, במקום לנסות לזהות מטופלים "בסיכון גבוה".
למטופלים עם AF שיש להם גורם סיכון אחד או יותר לשבץ מומלץ לקבל טיפול יעיל למניעת שבץ, שהינו למעשה נוגד קרישה פומי עם טיפול יעיל באנטגוניסטים לויטמין K (2-3 INR), עם אחוז גבוה של זמן בטווח הטיפולי (TTR, Time in Therapeutic Range), או באחד מה-NOACs.
בעוד שציון CHADS2 [אי ספיקת לב, יתר לחץ דם, גיל 75 או יותר, סוכרת, שבץ (מוכפל)] הוא פשוט, הרוב מסכימים כיום שהוא אינו כולל גורמי סיכון נפוצים מאד לשבץ.
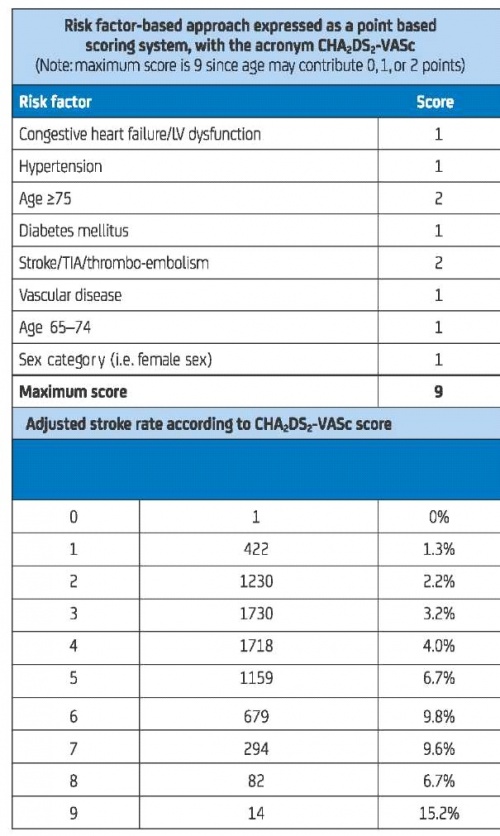
ציון CHA2DS2-VASc כולל את גורמי הסיכון הנפוצים ביותר לשבץ בפרקטיקה הקלינית היומיומית (תמונה מס' 1). היסטוריה של אי ספיקת לב בפני עצמה אינה מוגדרת באופן עקבי כגורם סיכון, וה-"C" ב-CHA2DS2 VASc מתייחס לירידה בינונית - קשה בתפקוד הסיסטולי או למטופלים עם אי ספיקת לב חריפה הזקוקים לאשפוז. השתייכות למגדר הנשי מעלה באופן בלתי תלוי את הסיכון לשבץ, למעט נשים מתחת לגיל 65 שאין להן כל גורם סיכון נוסף שאז השתייכות למגדר הנשי אינה מעלה את הסיכון לשבץ. לכן, מטופלות שמינן בלבד הוא גורם הסיכון היחיד (עדיין ציון CHA2DS2-VASc של 1) לא יזדקקו לטיפול אנטי טרומבוטי.
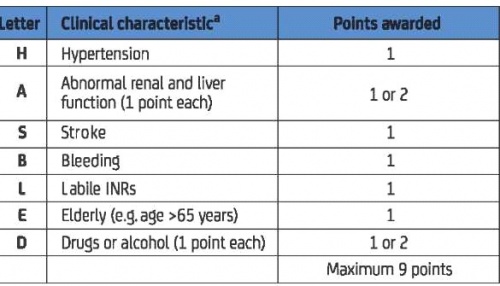
הנחיות האיגוד האירופי לקרדיולוגיה וההנחיות הקנדיות ממליצות על השימוש בציון HAS-BLED להערכת הסיכון לדימום (תמונה מס' 2). ציון HAS-BLED אומת במספר מחקרים בלתי תלויים, ויש לו מתאם טוב עם הסיכון לדימום תוך גולגולתי. שיעור הדימום תוך גולגולתי (או הדימומים המשמעותיים) בקרב מטופלים הנוטלים אספירין, עם ציון HAS-BLED נתון, היה דומה לשיעורו בקרב אלו שנוטלים Coumadin.
הערכה פורמלית של הסיכון לדימום מומלצת בקרב כל המטופלים עם פרפור פרוזדורים, ובמטופלים עם ציון HAS BLED של 3 או יותר, נכון לנהוג בזהירות ולהשתדל לפעול לתיקון גורמי הסיכון ככל שניתן.
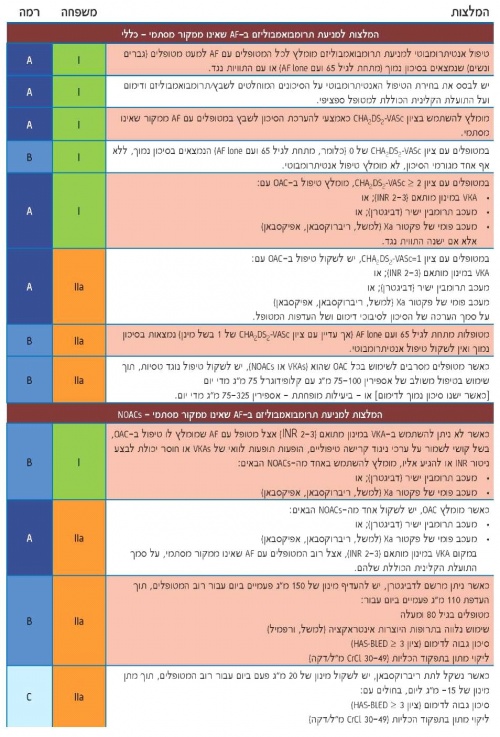
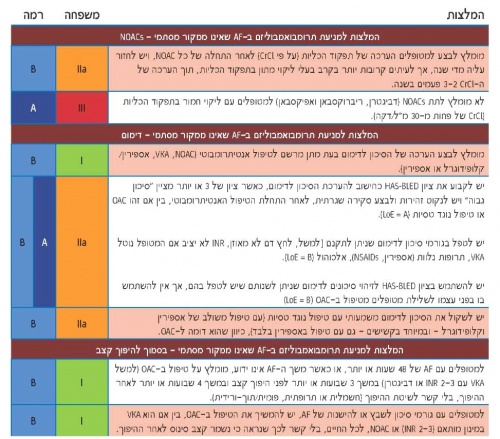
המלצות האיגוד האירופי לקרדיולוגיה להחלטה על טיפול אנטיתרומבוטי בחולי פרפור פרוזדורים מסוכמות בתמונה מס' 3 וביתר פירוט בטבלה מס' 4.
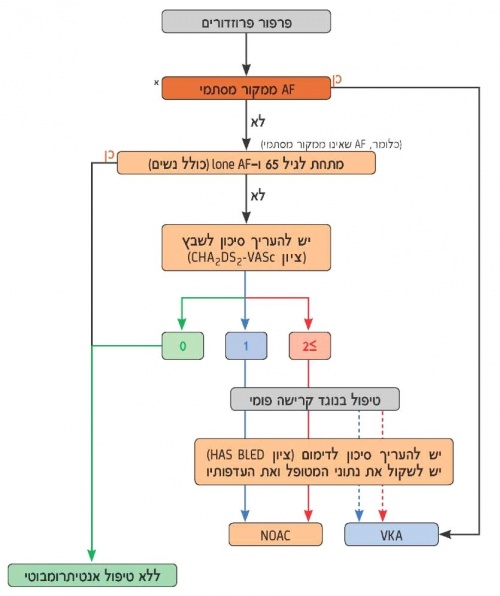
יש לשקול טיפול נוגד טסיות של אספירין עם Clopidogrel, או - ביעילות פחותה - אספירין בלבד, רק במטופלים שמסרבים לכל נוגד קרישה פומי.
אם ישנן התוויות נגד לנוגדי קרישה פומיים או לטיפול נוגד טסיות, ניתן לשקול סגירה או כריתה של אוזנית העלייה השמאלית.
צבע: CHA2DS2-VASc; ירוק = 0, כחול = 1, אדום ≤2.
קו: רציף = האפשרות הטובה ביותר; מקווקו = אפשרות חלופית.
AF = פרפור פרוזדורים; CHA2DS2-VASc = ראה טקסט; HAS-BLED = ראה טקסט; NOAC = נוגד קרישה פומי חדש; OAC = נוגד קרישה פומי; VKA = אנטגוניסט לוויטמין K.
א כולל מחלה מסתמית ריאומטית ומסתמים תותבים - ראה פירוט נייר עמדה של האיגוד הקרדיולוגי הישראלי
נוגדי קרישה פומיים חדשים
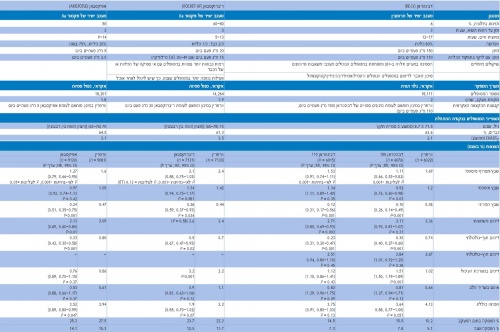
AF = פרפור פרוזדורים; b.i.d. = פעמיים ביום; CHADS2 = אי ספיקת לב גדשתית, יתר לחץ דם, גיל 75 או יותר, סוכרת, שבץ/שבץ איסכמי חולף (מוכפל); CI = confidence interval, רווח בר סמך; creatinine clearance CrCl (פינוי קריאטינין); HR = hazard ratio, יחס סיכונים; ITT = intention-to-treat, כוונה לטפל; o.d. = פעם ביום; RR = relative risk, סיכון יחסי; SD = סטייה סטנדרטית; TIA = שבץ איסכמי חולף; VKA= אנטגוניסט לוויטמין K.
Pradaxa (Dabigatran etexilate)
מחקר ה-RE-LY היה מחקר שלב III, פרוספקטיבי, אקראי וגלוי, שהשווה בקרב 18,113 מטופלים בין שני מינונים סמויים של Pradaxa [110 מיליגרם (מ"ג) פעמיים ביום (D110) או 150 מ"ג פעמיים ביום (D150)] לבין Coumadin גלוי במינון שהותאם להגיע ל-INR של 2.0-3.0 (טבלה 1). בנקודת הסיום הראשונית ליעילות (שבץ או תסחיף סיסטמי), הייתה ל-D150 עליונות אל מול Coumadin, ללא הבדל מובהק בדימומים משמעותיים. D110 היה בלתי נחות (Non inferior) במדד היעילות מ-Coumadin אך בטוח ממנו, עם ירידה של 20% בשיעור הדימומים המשמעותיים. שיעורי השבץ ההמורגי היו נמוכים יותר עם שני המינונים של Pradaxa מאשר עם Coumadin, אך שיעור הדימומים במערכת העיכול היה גבוה באופן מובהק עם D150. שני המינונים של Pradaxa היו כרוכים בעליה של 28% בשיעורי אוטם בשריר הלב, עליה שלא הייתה מובהקת סטטיסטית. עם D150 הייתה ירידה מובהקת בשיעורי השבץ האיסכמי, וכן ירידה גבולית בתמותה הכוללת (0.051 = P) וירידה מובהקת בתמותה מסיבות וסקולריות (0.04 = P). החששות באשר לעלייה הקטנה בשיעורי מקרי האוטם עם Pradaxa הובילו לאנליזה מפורטת של המחקר בה לא נמצאה עליה בצורך באשפוזים או צורך קליני ברה-וסקולריזציה בקרב המטופלים שטופלו ב-Pradaxa. התמותה הקרדיו-וסקולרית וה-Net clinical benefit היו לטובת Pradaxa.
Xarelto (Rivaroxaban)
מחקר ROCKET-AF כפול הסמיות חילק באופן אקראי 14,264 מטופלים עם פרפור פרוזדורים בסיכון גבוה לטיפול ב-Xarelto 20 מ"ג ביום (15 מ"ג ליום לבעלי GFR של 30-49 מ"ל/דקה) או לטפול ב-Coumadin (טבלה 1). אוכלוסיית מחקר זה היתה בסיכון גבוה יותר לשבץ מאשר האוכלוסיה שנכללה במחקרי ה-NOAC האחרים. Xarelto התברר כבלתי נחות לעומת Coumadin בנקודת הסיום הראשונית של שבץ ותסחיפים סיסטמיים. ניתוח הנתונים על פי הטיפול שניתן בפועל (ולא על פי Intention to treat), הצביע על כך ש-Xarelto השיג עליונות לעומת Coumadin בנקודת הסיום הראשונית עם הפחתה יחסית בסיכון (Relative risk reduction) של 21%, 0.015=P. לא הייתה ירידה בשיעורי התמותה או השבץ האיסכמי, אך נראתה ירידה מובהקת בשבץ המורגי ובדימום תוך-גולגולתי. נקודת הסיום הראשונית לבטיחות הייתה מורכבת מדימום משמעותי ומדימום לא משמעותי בעל רלוונטיות קלינית, ולא הייתה שונה במידה מובהקת בין Xarelto ל-Coumadin. עם Xarelto הייתה ירידה מובהקת בדימומים הקטלניים, כמו גם עלייה בדימומים במערכת העיכול ובדימומים שהצריכו עירוי.
Eliquis (Apixaban)
מחקר AVERROES שיבץ באופן כפול סמיות ואקראי 5,599 מטופלים עם פרפור פרוזדורים, שלא היו מועמדים מתאימים לטיפול באנטגוניסטים לויטמין K או לא הסכימו ליטול טפול זה, לאספירין או ל-Eliquis (5 מ"ג פעמיים ביום עם התאמת מינון ל-2.5 מ"ג פעמיים ביום בקרב מטופלים שמילאו שנים מהקריטריונים הבאים: גיל 80 ומעלה, משקל 60 ומטה וקריאטינין של 1.5 מ"ג/ד"ל או יותר). לאחר מעקב ממוצע של כשנה הופסק המחקר מוקדם מהצפוי, בשל ירידה מובהקת של 55% בנקודת הסיום הראשונית של שבץ או תסחיפים סיסטמיים עם Eliquis בהשוואה לאספירין, ללא הבדל מובהק בין הקבוצות בשיעורי הדימומים המשמעותיים או דימום תוך גולגולתי.
מחקר ARISTOTLE היה מחקר שלב III, אקראי, כפול סמיות, שהשווה בין Eliquis (במינון זהה לזה שניתן ב-AVERROES) ל-Coumadin במינון שהותאם לשמירת INR של 3.0-2.0, ב-18,201 מטופלים עם פרפור פרוזדורים לא מסתמי (טבלה 1). המחקר מצא ירידה מובהקת של 21% בתוצאת היעילות הראשונית של שבץ או תסחיפים סיסטמיים עם Eliquis בהשוואה ל-Coumadin, כמו גם ירידה של 31% בשיעור הדימומים המשמעותיים וירידה מובהקת של 11% בתמותה הכוללת (אך לא בתמותה ממחלות לב וכלי דם). שיעורי השבץ ההמורגי ודימום תוך גולגולתי - אך לא של השבץ האיסכמי - היו נמוכים באופן מובהק בקרב המטופלים שטופלו ב-Eliquis לעומת אלו שטופלו ב-Coumadin. שיעור הדימומים במערכת העיכול היה דומה בין זרועות הטיפול. Eliquis נסבלה טוב יותר מ-Coumadin, עם שיעור מעט נמוך יותר של הפסקות מוקדמות (25.3% לעומת 27.5%).
שיקולים מעשיים
ה-NOACs שנבדקו במחקרים קליניים הראו כולם אי נחיתות בהשוואה לאנטגוניסטים לויטמין K, עם בטיחות טובה יותר, תוך הקטנה עקבית של שיעור הדימום התוך גולגולתי. על סמך ממצאים אלה, ישנה המלצה על תכשירים אלה כעדיפים באופן כללי על פני אנטגוניסטים לויטמין K ברוב המטופלים עם פרפור פרוזדורים שאינו מסתמי, כאשר משתמשים בהם כפי שהיה במחקרים הקליניים שבוצעו. מאחר שהניסיון עם תכשירים אלה מוגבל יש לדבוק באופן קפדני בהתוויות שאושרו ומומלץ מאוד לקיים פיקוח זהיר על התוצאות לאחר השיווק.
בהיעדר מחקרים של השוואות ישירות לא נכון לומר בוודאות איזה מה-NOACs הוא הטוב ביותר, בהתחשב בהטרוגניות של המחקרים השונים. ניתוחי השוואה עקיפים אינם מרמזים על הבדלים מהותיים בנקודות הסיום ליעילות בין ה-NOACs, אך נראה כי שיעור הדימומים המשמעותיים נמוך יותר עם Pradaxa 110 מ"ג פעמיים ביום ועם Eliquis. ייתכן כי מאפייני המטופלים, הסבילות לתרופה והעלות עשויים להיות שיקולים חשובים. לכל ה-NOACs פורסמו נתונים המצביעים על פרופיל עלות-תועלת משביע רצון ברוב המטופלים.
לאף אחת מהתרופות החדשות אין עדיין תרופת נגד (Antidote) ספציפי אך תכשירים כאלה מצויים בשלבי פיתוח מתקדמים וצפויים להיות זמינים בקרוב (נכון לשנת 2012); חשוב לזכור כי גם לתרופות אלו ישנן אינטראקציות בין תרופתיות מסוימות. מטופלים עם ליקוי חמור בתפקוד הכליות לא נכללו במחקרים, ובאופן ספציפי, הפינוי הכלייתי של Pradaxa הוא גבוה במיוחד.
סכמת מעקב טיפול
לפני מתן מרשם ל-NOACs למטופל עם פרפור פרוזדורים, יש לבצע ניתוח סיכון-תועלת מבחינת טיפול נוגד קרישה בכלל ומבחינת נוגד הקרישה הספציפי, על סמך ההתוויות המאושרות ועל פי העדפת המטופל לאחר דיון באפשרויות השונות. באשר לבחירה של NOAC מסוים, חשוב לשקול גם את הפרופיל הקליני של המטופל ואת התרופות הנלוות שלו. בדומה למשתמשים באנטגוניסטים לויטמין K, חשוב גם שאלו שהמטופלים ב-NOACs יישאו פרטים על הטיפול נוגד הקרישה שלהם, על מנת להתריע בפני כל גורם (פרא-)רפואי על הטיפול בהם. תמונה 4 מתארת את עקרונות תחילת הטיפול והמעקב אחר חולים המקבלים NOAC.
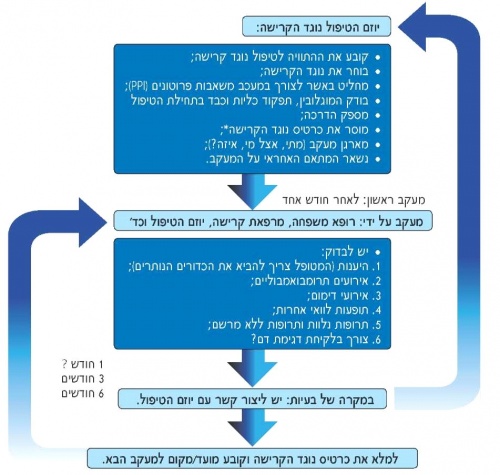
*כרטיס נוגד הקרישה, מיועד לתיעוד כל ביקור מתוכנן, כל השגחה או בדיקה רלוונטית וכל שינוי בתרופה, כדי שלכל אדם העוקב אחר המטופל יהיה את כל המידע. בנוסף, נדרשת התקשרות כתובה בין השחקנים ה(פרא-) רפואיים השונים, על מנת ליידע אותם באשר לתכנית המעקב וביצועה.
חובה לבצע מעקב מובנה אחר מטופלים הנוטלים את נוגדי הקרישה הפומיים החדשים על מנת להבטיח נטילה בטוחה ויעילה של התרופה.
מדידת השפעה נוגדת קרישה
NOACs אינם מצריכים ניטור שגרתי של הקרישה: אין צורך לשנות שום מינון או מרווח בין מינונים בתגובה לשינויים בפרמטרים המעבדתיים הנוגעים לקרישה. עם זאת, ייתכן שבמקרי חירום יהיה צורך לבצע הערכה כמותית של החשיפה לתרופה ושל ההשפעה נוגדת הקרישה.
בעת פענוח תבחין קרישה של מטופל המקבל NOAC חשוב לדעת בדיוק מתי נלקח ה-NOAC ביחס למועד נטילת דגימת הדם.
ה-aPTT (activated Partial Thromboplastin Time) עשוי לספק הערכה איכותנית באשר לנוכחות של Pradaxa אם רמת ה-aPTT 24-12 שעות לאחר הנטילה עדיין עולה על פי 2 מגבול הנורמה העליון, ייתכן שניתן לקשר זאת לסיכון גבוה יותר לדימום וייתכן שהיא מחייבת זהירות, במיוחד בקרב מטופלים עם גורמי סיכון לדימום. זמן הפרותרומבין (PT, Prothrombin Time) עשוי לספק הערכה איכותנית באשר לנוכחותם של מעכבי פקטור Xa. בדומה לקשר בין aPTT ל-Pradaxa, בדיקות אלה אינן רגישות להערכה כמותית של השפעת ה-NOAC. קיימות אמנם בדיקות כמותיות לתרופות המעכבות תרומבין באופן ישיר (DTI, Direct Thrombin Inhibitors) ולמעכבי FXa (בדיקת זמן תרומבין מדוללת ותבחינים כרומוגניים, בהתאמה), אך חשוב לציין שאין נתונים על ערכי הסף של בדיקות אלה, שמתחת להם ניתוח הוא "בטוח", ולפיכך לא ניתן בשלב זה להמליץ על השימוש בבדיקות אלה לצורך זה. אין להשתמש בבדיקת INR בקרב מטופלים הנוטלים NOACs.
אינטראקציות בין-תרופתיות ופרמקוקינטיקה
על אף הציפיות הגבוהות לאינטראקציות מעטות יותר בין מזון לבין ה NOACs יהיו הרופאים חייבים לשקול את ההשפעות הפרמקוקינטיות של תרופות נלוות ושל מחלות נלוות בעת מתן מרשם ל-NOACs, במיוחד כאשר ישנו שילוב של גורמים מפריעים. למידע מפורט ועדכני על האינטראקציות הבין תרופתיות של כל אחת מהתרופות יש לעיין בעלון המתאים לרופא כפי שאושר על ידי משרד הבריאות הישראלי.
מאחר שלצריכת מזון ישנה השפעה על הספיגה ועל הזמינות הביולוגית של Xarelto יש ליטול תרופה זו עם האוכל. לתרופות NOACs אחרות אין אינטראקציה רלוונטית עם מזון. כמו כן, שימוש נלווה במעכבי משאבות פרוטונים (PPI, Proton-Pump Inhibitor) ובחוסמי H2 אינו מהווה התוויית נגד לאף NOAC .
מעבר בין נוגדי קרישה
כאשר עוברים מאנטגוניסטים לויטמין K ל-NOACs יש להפסיק תחילה את הטיפול באנטגוניסטים לויטמין K ולעקוב אחר ה-INR. רק לאחר ירידת ה-INR אל מתחת ל-2.0 יש להתחיל במתן ה-NOAC. מעבר מ-NOAC לאנטגוניסטים לויטמין K דורש חפיפה מסויימת והפסקת ה-NOAC רק לאחר שה-INR התייצב בין 2.0 ל-3.0.
היענות
ההשפעה נוגדת הקרישה של NOACs מתפוגגת 24-12 שעות לאחר הנטילה האחרונה. לפיכך, היענות קפדנית לטיפול חיונית להשגת הגנה מתאימה. על הרופאים לפתח דרכים לשיפור ההיענות, שידוע כי היא עומדת על 80% או פחות ברוב התרופות הנמצאות בפרקטיקה היומיומית. יש מעט נתונים בנוגע להיענות בפועל ל-NOACs בחיי היום יום. עם זאת, יש לשקול את כל האמצעים הקיימים לצורך שיפור ההיענות. אמצעים אלה כוללים בחירה במשטר מינון צריכה של פעם ביום או של פעמיים ביום; חזרה על ההדרכה למטופל ולבני משפחתו; לוח זמנים ברור למעקב עם רופא משפחה וקרדיולוג, אפשרות שימוש בעזרים טכנולוגיים, כגון קופסאות של תרופות ואפליקציות סמארטפון ומאגר נתונים של בתי מרקחת.
טעויות במינון
שאלות הקשורות לטעויות במינון נפוצות מאוד בפרקטיקה היומיומית. על מנת למנוע מצבים כגון אלו המתוארים להלן, יש לעודד במידת האפשר את המטופלים הנוטלים NOACs להשתמש במיכלי הכדורים השבועיים שבהם יש מקומות נפרדים לכל מנה.
במקרה של החמצת מנה, אין ליטול מנה כפולה כדי לפצות על המנות הבודדות שהוחמצו. עם זאת, ניתן ליטול את המנה שנשכחה עד מחצית מפרק הזמן שבין המנות (למשל, עד 12 שעות, כאשר המינון הוא פעם ביום). אם לא ניתן לעשות זאת יותר, יש לדלג על המנה וליטול את המנה הבאה במועדה.
במקרה שבטעות ניטלה מנה כפולה, ניתן לבחור לוותר על המנה המתוכננת הבאה. לעיתים, המטופל אינו בטוח אם מנה ניטלה או לא. במשטר NOACs של נטילת מנה פעמיים ביום, ניתן להמשיך במינון המתוכנן, כלומר, החל מהמנה הבאה בתום מרווח הזמן של 12 שעות. במשטר NOACs של נטילת מנה פעם אחת ביום, ניתן ליטול כדור נוסף ואז להמשיך במשטר המינון המתוכנן.
במקרה של מינון יתר, בהתאם לכמות החשודה של מינון היתר, יש להציע אשפוז לצורך ניטור או להציע נקיטת צעדים דחופים.
ניהול סיבוכי דימום
בשל היעדרן של תרופות נגד ספציפיות ל-NOACs, האסטרטגיות לסתירת ההשפעות נוגדות הקרישה הן מוגבלות. סתירת ההשפעה של אנטגוניסטים לויטמין K באמצעות מתן ויטמין K מתחיל לאט (כלומר, לאחר 24 שעות לפחות), אך מתן פלסמה קפואה טרייה או גורמי קרישה משקם את הקרישה מהר יותר. עם זאת, במקרה של NOACs, הכמות הרבה של התרופה בפלסמה עלולה לחסום גם את גורמי הקרישה החדשים שניתנים. מצד שני, מחקרים הראו כי פרופיל הדימום של ה NOACs, במיוחד זה של דימום תוך-גולגולתי ושל דימומים מסכני חיים, עדיף על זה של Coumadin. עם זאת ככל שיותר מטופלים יתחילו להשתמש באחת מתרופות ה-NOAC, מספר האירועים הקשורים לדימומים צפוי לעלות. כיום, ההמלצות לטיפול בדימום אינן מבוססות ברובן על ניסיון קליני, אלא משקפות יותר את דעות המומחים ואת שינוי ערכי המעבדה. בהתחשב בכך שזמני מחצית החיים של ה-NOACs הם קצרים יחסית עד לסילוקן, זמן הוא תרופת הנגד הטובה ביותר של תרופות אלה. דבר זה מדגיש את חשיבות האנמנזה המפורטת אודות משטר המינון שבו נעשה שימוש, הזמן המדויק של הנטילה האחרונה, גורמים המשפיעים על הריכוז בפלסמה (למשל, טיפול ב-P-gp, מחלת כליות כרונית ואחרים) וגורמים אחרים המשפיעים על עצירת הדימום (כגון שימוש נלווה בתרופות נוגדות טסיות).
על סמך נתונים קליניים מועטים, ניתן לשקול מתן PCC (Prothrombin Complex Concentrate) או aPCC (activated Prothrombin Complex Concentrate) למטופל עם דימום מסכן חיים, אם נדרשת תמיכה מיידית לעצירת הדימום (תמונה 5). בעת ההמתנה לנתונים נוספים על היעילות הקלינית של אסטרטגיות אלה, הבחירה עשויה להיות תלויה בזמינותם ובניסיון במרכז הטיפול. מקומו של פקטור VIIa משופעל רקומביננטי זקוק להערכה נוספת. ישנה המלצה על התייעצות בין קרדיולוגים, מומחי קרישה ורופאי רפואת חירום על מנת לפתח מדיניות לכלל בתי החולים באשר לטיפול בדימום. מדיניות כזו צריכה להיות מועברת היטב ולהיות נגישה בקלות (למשל, באתר אינטרנט או בעלוני כיס). החברה הישראלית לקרישת הדם והאיגוד הישראלי לרפואה דחופה פרסמו פרוטוקול לטיפול בדימום בחולים הנוטלים את נוגדי הקרישה החדשים.
בעת כתיבת מסמך זה נמצאים בשלבי פיתוח שונים תרופות נגד כלפי נוגדי הקרישה החדשים. תכשירים אלה צפויים להיות זמינים בעתיד הלא רחוק ולהקל במידה רבה על הטיפול במקרים של דימום תחת NOACs.
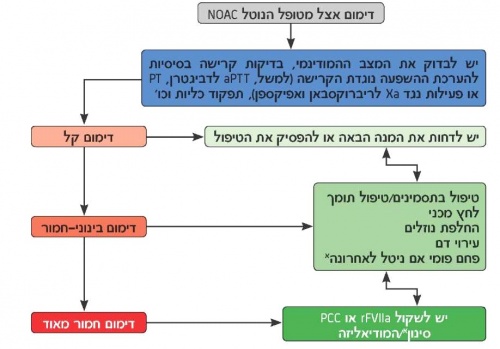
aPTT = activated partial thromboplastin time, זמן תרומבופלסטין חלקי משופעל; NOAC = נוגד קרישה פומי חדש; = PCC Prothrombin complex concentrate, תרכיז קומפלקס פרותרומבין; PT = זמן פרותרומבין; rFVIIa = activated recombinant factor VII , פקטור VII רקומביננטי משופעל. א עם דביגטרן.
קו-מורבידיות
מחלת כליות כרונית
מחלת כליות כרונית (CKD, chronic kidney disease) מהווה גורם סיכון הן לאירועים תרומבואמבוליים והן לדימום בקרב מטופלי פרפור פרוזדורים. ממצאים מעלים את האפשרות כי פינוי קריאטינין של פחות מ-60 מ"ל/דקה אף עשוי להיות גורם מנבא בלתי תלוי לשבץ ולתסחיפים סיסטמיים. טיפול באנטגוניסטים לויטמין K נקשר להפחתה משמעותית בסיכון לשבץ או לאירועים תרומבואמבוליים בקרב חולי מחלות כליות כרונית, אך במקביל הסיכון לדימום עולה במידה משמעותית. אם כן, יש להעריך בזהירות את ההשפעה הקלינית הכוללת של הטיפול באנטגוניסטים לויטמין K במטופלים אלה. מטופלים רבים עם מחלת כליות כרונית בדרגה מתונה עד חמורה גויסו לניסויים על NOAC, עם הפחתות מינון שהוגדרו מראש. בהקשר של הטיפול עם NOAC, הפינוי קריאטנין מוערך בצורה הטובה ביותר באמצעות שיטת קוקרופט (Cockroft), כיוון שזו השיטה שבה נעשה שימוש ברוב הניסויים עם NOAC. אין נתונים באשר NOACs במטופלים עם מחלת כליות כרונית מתקדמת (פינוי קריאטנין של פחות מ-30 מ"ל/דקה), וההנחיות הנוכחיות של האגודה האירופית לקרדיולוגיה ממליצות נגד השימוש ב-NOACs במטופלים אלו. יתר על כן, ישנם מעט מאד נתונים על מטופלי דיאליזה או שקרובים לטיפול בדיאליזה (GFR של פחות מ-15 מ"ל/דקה, CKD בשלב V), הן מניסויים והן מהניסיון הקליני. בהיעדר ניסיון שכזה, אף אחת מתרופות ה-NOACs אינה מאושרת לשימוש במטופלי דיאליזה.
נראה כי נוגדי הקרישה הפומיים החדשים מהווים אפשרות סבירה לטיפול נוגד קרישה בקרב מטופלי פרפור חדרים עם מחלת כליות כרונית בדרגה מתונה עד חמורה. נראה כי יחס התועלת/סיכון של NOACs לעומת אנטגוניסטים לויטמין K דומה בחולי מחלת כליות כרונית ליחס שבחולים ללא הפרעה כליתית, וישנן עדויות לכך שהעלייה בשיעור הדימום בקרב חולי מחלת כליות כרונית הייתה פחותה באופן משמעותי לעומת שיעורה עם אנטגוניסטים לויטמין K.
אין מחקרים שהשוו בין הסיכונים של מחלת כליות כרונית עם ה-NOACs השונות. לפיכך, ייתכן כי איזון זהיר בין היתרונות לסיכונים של כל תרופה (ושל התאמת המינון שלה) מצדיק את הבחירה הזו. עם זאת, בקרב חולי מחלת כליות כרונית נדרש מעקב זהיר אחר תפקוד הכליות עם כל התרופות, מאחר שכולן מפונות במידה זו או אחרת דרך הכליות. ניטור תפקוד הכליות רלוונטי במיוחד ל-Pradaxa, שעיקר הפינוי שלו הוא כלייתי (ראו גם "התחלה מעשית וסכמת מעקב למטופלים הנוטלים נוגדי קרישה פומיים חדשים"). מחלה חריפה לעיתים קרובות משפיעה באופן זמני על תפקוד הכליות (זיהומים, אי ספיקת לב חריפה וכדומה), ולפיכך עליה להוביל להערכה עדכנית של התפקוד הכלייתי. במטופלי פרפור פרוזדורים הזקוקים להמודיאליזה יש להימנע מטיפול בנוגדי הקרישה הפומיים החדשים וייתכן כי אנטגוניסטים לויטמין K הינם חלופות מתאימות יותר.
התערבות כירורגית או אבלציה
כרבע מהמטופלים הזקוקים לטיפול נוגד קרישה צריכים לבצע הפסקה זמנית של הטיפול תוך שנתיים מתחילת הטיפול. בעת ההחלטה מתי להפסיק ולהתחיל מחדש את התרופה, יש לקחת בחשבון הן את מאפייני המטופל (תפקוד כליות, גיל, היסטוריה של סיבוכי דימום ותרופות נלוות) והן גורמים כירורגיים. טבלה 3 מסכמת את המידע הזה עבור תרופות ה-NOACs השונות. ההמלצה הינה לפתח הנחיות מוסדיות ומדיניות לכלל בתי החולים באשר לניהול ניגוד הקרישה לאחר ניתוח במסגרות כירורגיות שונות, שתופץ באופן נרחב ותהיה נגישה בקלות.
אף על פי שניתן לבצע התערבויות נפוצות ללא סיכון משמעותי לדימום (כגון, הליכים דנטליים מסוימים או התערבויות לקטרקט או לגלאוקומה) בזמן רמות השפל של ה-NOACs (כלומר, 12 או 24 שעות לאחר הנטילה האחרונה, בהתאם למשטר מינון של פעמיים ביום או של פעם ביום), ייתכן שיהיה מעשי יותר לקבוע את מועד ההתערבות ל-24-18 שעות לאחר הנטילה האחרונה, ולאחר מכן להתחיל את התרופה מחדש 6 שעות לאחר מכן, כלומר, לדלג על מנה אחת של NOAC הניטלת פעמיים ביום. כשמדובר על הליכים עם סיכון שולי לדימום, מומלץ להפסיק את תרופות ה-NOACs 24 שעות לפני ההליך האלקטיבי בקרב מטופלים עם תפקוד כליות תקין, וכשמדובר על הליכים עם סיכון לדימום משמעותי, יש ליטול את ה-NOAC האחרונה 48 שעות לפני כן.
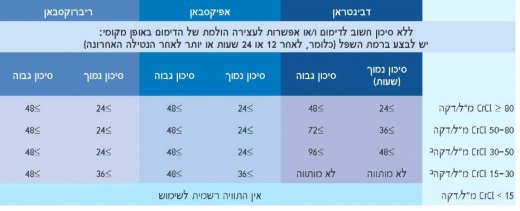
סיכון נמוך, ניתוח עם סיכון נמוך לדימום; סיכון גבוה, ניתוח עם סיכון גבוה לדימום. CrCl, פינוי קריאטינין. ב. רבים מהמטופלים האלה עשויים להיות על המינון הנמוך יותר של Pradaxa (כלומר, 110 מ"ג פעמיים ביום) או של Eliquis (כלומר, 2.5 מ"ג פעמיים ביום), או שהם חייבים להיות על המינון הנמוך יותר של Xarelto (15 מ"ג ביום).
התערבות כירורגית דחופה
אם נדרשת התערבות חירום, יש להפסיק את ה-NOAC. יש לדחות את הניתוח או את ההתערבות, אם ניתן, עד שיעברו לפחות 12 שעות, ובאופן אידיאלי - 24 שעות, לאחר המנה האחרונה. ניתן לשקול הערכה של בדיקות הקרישה הנפוצות (aPTT ל-PT; DTI רגיש למעכבי FXa) או בדיקת קרישה ספציפית (dTT ל-DTI; תבחינים כרומוגניים למעכבי FXa), אם ישנו חשש באשר לדעיכה פרמקוקינטית של ההשפעה נוגדת הקרישה (למשל, אי ספיקת כליות ו/או מצבים נלווים). בכל אופן, אסטרטגיה כזו מעולם לא הוערכה ולפיכך לא ניתן להמליץ עליה ואין להשתמש בה באופן שגרתי.
מחלת לב כלילית
השילוב של פרפור פרוזדורים עם מחלת לב כלילית הוא שכיח. זהו מצב מורכב מבחינת אופן ההתמודדות עם הטיפול נוגד הקרישה ונוגד הטסיות, והוא נקשר לשיעורי תמותה גבוהים באופן משמעותי. לרוע המזל, אין די נתונים זמינים על מנת להדריך באופן מיטבי את הפרקטיקה הקלינית במצבים אלו. יתר כל כן, חומרים נוגדי טסיות חדשים נכנסו לשוק בתסמונות כליליות חריפות ובכך הוסיפו אי וודאות באשר לשימוש בהם בשילוב עם אנטגוניסטים לויטמין K או עם NOACs כאשר למטופל יש הן מחלת לב כלילית חריפה (ACS, Acute Coronary Syndrome) והן פרפור פרוזדורים. לשם הבהירות, נבחרו שלושה תרחישים קליניים עם תרחישי משנה רבים ושונים והוצעו הוראות מעשיות לכל אחד מהם:
- ניהול מחלת לב כלילית חריפה במטופל עם פרפור פרוזדורים הנוטל NOAC;
- ניהול מטופל עם מחלת לב כלילית חריפה לאחרונה (פחות משנה) המפתח פרפור פרוזדורים חדש;
- התפתחות פרפור פרוזדורים במטופל עם היסטוריה של מחלת לב כלילית, אך ללא מחלת לב כלילית חריפה במהלך השנה האחרונה, ללא השתלה אלקטיבית של תומכן חשוף (Bare metal stent) במהלך החודש האחרון או תומכן מפריש תרופה (Drug eluting stent) במהלך 6 החודשים האחרונים ("מחלת לב כלילית יציבה").
יש להתאים באופן מאוד אישי את הסוג ואת הרמה של נוגד הקרישה, כמו כן את הטיפול נוגד הטסיות, יחיד לעומת כפול, בשילוב עם NOAC, ואת משכו, על סמך הסיכון האתרותרומבוטי, הסיכון הקרדיואמבוליי והסיכון לדימום. מומלץ מאוד להעריך את הסיכון באופן רשמי באמצעות כלים מתוקפים, כגון ציוני GRACE, CHA2DS2-VASc ו-HAS-BLED. במסמך גם ישנה רשימה של הנתונים המדעיים המרכזיים המהווים בסיס להנחיה. נתונים חדשים, הנחוצים ביותר, עשויים לשנות את אפשרויות הניהול.
המלצות טיפול
AF = פרפור פרוזדורים; b.i.d. = פעמיים ביום; CHA2DS2-VASc= אי ספיקת לב גדשתית, יתר לחץ דם, גיל 75 או יותר (מוכפל), סוכרת, שבץ (מוכפל), מחלה וסקולרית, גיל 65-74, מין (נשים); CrCl = פינוי קריאטינין; HAS-BLED = יתר לחץ דם, תפקוד חריג של הכליות/כבד (נקודה אחת לכל אחד), שבץ, נטייה לדימום, INR לא יציב עם Coumadin, קשיש (כלומר, מעל גיל 65), אלכוהול/תרופות (אספירין, NSAIDs וכדומה) נלווים (נקודה אחת לכל אחד); INR = יחס בינלאומי מתוקנן; i.v. = תוך-ורידי; OAC = נוגד קרישה פומי; NOAC = נוגד קרישה פומי חדש; NSAID = תרופה נוגדת דלקת שאינה סטרואידית; VKA = אנטגוניסט לוויטמין K.


 כניסה
כניסה  עקבו אחרינו בפייסבוק
עקבו אחרינו בפייסבוק