הבדלים בין גרסאות בדף "התסמונת המטבולית - The metabolic syndrome"
שני כהן-סדן (שיחה | תרומות) |
|||
| שורה 63: | שורה 63: | ||
תנגודת לאינסולין קשורה בהפרעות נוספות שאינן כלולות בהגדרה של התסמונת המטבולית. ניתן לחלק את ההפרעות הנוספות למספר קטגוריות:{{הערה|שם=הערה17|Eckel RH, Grundy SA, Zimmet PZ. The metabolic syndrome. Lancet, 2005;365:1415-1428}} | תנגודת לאינסולין קשורה בהפרעות נוספות שאינן כלולות בהגדרה של התסמונת המטבולית. ניתן לחלק את ההפרעות הנוספות למספר קטגוריות:{{הערה|שם=הערה17|Eckel RH, Grundy SA, Zimmet PZ. The metabolic syndrome. Lancet, 2005;365:1415-1428}} | ||
| − | # הפרעות ב- | + | # הפרעות ב-[[Lipoprotein]]<nowiki/>s: |
## עלייה ברמות Apo (Apolipoprotein) B | ## עלייה ברמות Apo (Apolipoprotein) B | ||
## ירידה ברמות Apo A-1 | ## ירידה ברמות Apo A-1 | ||
| שורה 72: | שורה 72: | ||
## עלייה ברמות IL-6 {{כ}}(Interleukin 6) | ## עלייה ברמות IL-6 {{כ}}(Interleukin 6) | ||
## עלייה ברמות [[TNF]] {{כ}}(Tumor Necrosis Factor) | ## עלייה ברמות [[TNF]] {{כ}}(Tumor Necrosis Factor) | ||
| − | ## עלייה ברמות Resistin | + | ## עלייה ברמות [[רזיסטין - Resistin|Resistin]] |
## עלייה ברמת [[CRP]]{{כ}} (C-Reactive Protein) | ## עלייה ברמת [[CRP]]{{כ}} (C-Reactive Protein) | ||
| − | ## ירידה ברמות Adiponectin | + | ## ירידה ברמות [[אדיפונקטין - Adiponectin|Adiponectin]] |
| − | ## ירידה ברמות Ghrelin | + | ## ירידה ברמות [[גרלין - Ghrelin|Ghrelin]] |
# הפרעות וסקולריות: | # הפרעות וסקולריות: | ||
## [[מיקרואלבומינוריה|Microalbuminuria]] | ## [[מיקרואלבומינוריה|Microalbuminuria]] | ||
## עלייה ברמות Asymmetric Dimethylarginine) ADMA) | ## עלייה ברמות Asymmetric Dimethylarginine) ADMA) | ||
# שינויים פרו-תרומבוטיים: | # שינויים פרו-תרומבוטיים: | ||
| − | ## עלייה ברמות Fibrinogen | + | ## עלייה ברמות [[פיברינוגן - Fibrinogen|Fibrinogen]] |
## עלייה ברמות PAI-1{{כ}} (Plasminogen Activator Inhibitor 1) | ## עלייה ברמות PAI-1{{כ}} (Plasminogen Activator Inhibitor 1) | ||
## עלייה בצמיגות הדם | ## עלייה בצמיגות הדם | ||
| שורה 86: | שורה 86: | ||
## עלייה ברמות חומצת השתן | ## עלייה ברמות חומצת השתן | ||
## עלייה ברמות [[Homocysteine]] | ## עלייה ברמות [[Homocysteine]] | ||
| − | ## כבד שומני לא אלכוהולי | + | ## [[כבד שומני לא אלכוהולי - טיפול|כבד שומני לא אלכוהולי]] |
| − | ## תסמונת השחלה הפוליציסטית (Polycystic ovary syndorme) | + | ## תסמונת השחלה הפוליציסטית ([[Polycystic ovary|Polycystic ovary syndorme]]) |
| − | ## דום נשימה חסימתי | + | ## [[דום נשימה חסימתי]] |
| − | ממצא של כבד שומני די שכיח. Steatohepatitis כוללת הצטברות של טריגליצרידים, הופעת דלקת וסכנה למחלת כבד סופנית ו-Hepatocellular | + | ממצא של כבד שומני די שכיח. [[Steatohepatitis]] כוללת הצטברות של טריגליצרידים, הופעת דלקת וסכנה למחלת כבד סופנית ו-[[Hepatocellular carcinoma]]. עלייה של Apo B ו-Apo CIII קשורה בהשפעת חומצות השומן על יצירת [[ליפופרוטאין בעל צפיפות נמוכה מאוד - Very low density-lipoprotein|VLDL]] {{כ}}(Very Low Density Lipoprotien) בכבד ומעידה על עלייה במספר החלקיקים הטרום-טרשתיים במחזור הדם.{{הערה|שם=הערה18|Onat A, Hergenc G, Sansoy V, et al. Apolipoprotein C-III, a strong discriminant of coronary risk in men and a determinant of the metabolic syndrome in both genders. Atherosclerosis, 2003;168:81-89}} עלייה ברמות חומצת השתן קשורה בהפרעה בפעילות האינסולין על הספיגה מחדש באבוביות הכליה, ועלייה ב-Asymmetric Dimethylarginine, מעכב של Nitric oxide synthase, קשורה בהפרעה בתפקוד האנדותל.{{הערה|שם=הערה19|Hanley AJ, Festa A, D'Agostino RB Jr, et al. Aetabolic and inflammation variable clusters and prediction of type 2 diabetes: factor analysis using directly measured insulin sensitivity. Diabetes, 2004;53:1773-1781}} ה-Microalbuminuria נובעת מהפרעה בתפקוד האנדותל הנגרמת בשל התנגודת לאינסולין. |
נושא הדלקת הכרונית מעורר עניין. מחקרים רבים עוסקים בקשר שבין הדלקת הכרונית לטרשת העורקים. השאלה העיקרית היא, האם דלקת כרונית בדרגה נמוכה מהווה סמן למחלה שתפרוץ בעתיד, או שהיא ממריצה את התהליך הטרשתי? האם היא מעידה על החמרה של תהליך שכבר קיים, או שהיא בעצם הגורם לתהליך הטרשתי או לסוכרת ולקשר ביניהם? והאם ניתן לעכב או למנוע את התהליך הטרשתי על ידי טיפול באותה דלקת כרונית? | נושא הדלקת הכרונית מעורר עניין. מחקרים רבים עוסקים בקשר שבין הדלקת הכרונית לטרשת העורקים. השאלה העיקרית היא, האם דלקת כרונית בדרגה נמוכה מהווה סמן למחלה שתפרוץ בעתיד, או שהיא ממריצה את התהליך הטרשתי? האם היא מעידה על החמרה של תהליך שכבר קיים, או שהיא בעצם הגורם לתהליך הטרשתי או לסוכרת ולקשר ביניהם? והאם ניתן לעכב או למנוע את התהליך הטרשתי על ידי טיפול באותה דלקת כרונית? | ||
| − | הדלקת הכרונית נוצרת במערכת החיסון המולדת והנרכשת. קיימת הפעלה של תאי T להפרשת ציטוקינים טרום-דלקתיים, כגון 6-IL{{כ}}, Resistin, ו-TNF המגיעים מדפנות העורקים, מתאי השומן ומרקמת שריר הלב, ומפעילים מולקולות הדבקות (Adhesion) בתוך האנדותל ו-Acute-phased reactants, בהם | + | הדלקת הכרונית נוצרת במערכת החיסון המולדת והנרכשת. קיימת הפעלה של תאי T להפרשת ציטוקינים טרום-דלקתיים, כגון 6-IL{{כ}}, Resistin, ו-TNF המגיעים מדפנות העורקים, מתאי השומן ומרקמת שריר הלב, ומפעילים מולקולות הדבקות (Adhesion) בתוך האנדותל ו-Acute-phased reactants, בהם CRP{{כ}}, Fibrinogen ו-Amyloid A בכבד.{{הערה|שם=הערה20|Rader DJ. Inflammatory markers of coronary risk. N Engl J Aed, 2000;343:1179}} במצב של השמנה, רקמת השומן מגבירה את יצירת הציטוקינים, ובמקביל קיימת ירידה ברמת ה-Adiponectin (הורמון המגביר את הרגישות לאינסולין ומעכב תהליכים דלקתיים). Adiponectin פועל גם בכבד לעיכוב האנזימים המעורבים ב-[[Gluconeogenesis]], מעלה את תובלת הגלוקוז בשריר ומחיש את חמצון חומצות השומן.{{הערה|שם=הערה21|Aatsuzawa Y, Funahashi T, Kihara S, et al. Adiponectin and metabolic syndrome. Arterioscler Thromb Vasc Biol. 2004;24:29-33}} רמה נמוכה של Adiponectin הודגמה גם בחולים עם מצב מקדים של יתר לחץ דם, ויכולה להוות גורם מנבא להתפתחות התסמונת המטבולית. |
== קליניקה== | == קליניקה== | ||
| שורה 236: | שורה 236: | ||
|- | |- | ||
! רמת [[t:גלוקוז - Glucose|גלוקוז]] גבוהה | ! רמת [[t:גלוקוז - Glucose|גלוקוז]] גבוהה | ||
| − | || הורדת רמת הגלוקוז אם היא גבוהה מ-100 מיליגרם/דציליטר. רמת | + | || הורדת רמת הגלוקוז אם היא גבוהה מ-100 מיליגרם/דציליטר. רמת המוגלובין A1C מתחת ל-7 אחוזים |
|| שינוי באורחות החיים, הוספת תרופות להורדת רמות הגלוקוז או רמת המוגלובין A1C, לפי הצורך | || שינוי באורחות החיים, הוספת תרופות להורדת רמות הגלוקוז או רמת המוגלובין A1C, לפי הצורך | ||
|- | |- | ||
גרסה מ־18:51, 2 במרץ 2021
| התסמונת המטבולית | ||
|---|---|---|
| The metabolic syndrome | ||
| ||
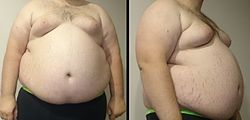
גבר שמן, שמשקלו 146 ק"ג, גובהו 177 ס"מ. מדד מסת הגוף (BMI) במקרה זה הוא 46.
| ||
| ICD-9 | 277.7 | |
| MeSH | D024821 | |
| יוצר הערך | פרופ' יאיר יודפת
|
|
לערכים נוספים הקשורים לנושא זה, ראו את דף הפירושים – תסמונת מטבולית
התסמונת המטבולית מורכבת מקבוצה של גורמי סיכון מטבוליים (Metabolic) בעלי זיקה הדדית להתפתחות של סוכרת מסוג 2 ותחלואה קרדיווסקולרית. בשנת 1988 נתן Reaven לתסמונת את השם "תסמונת X", בכדי לציין מצב של גורמי סיכון מטבוליים הקשורים בתנגודת לאינסולין.[1] לטענתו, התנגודת לאינסולין היא גורם הסיכון העיקרי והיסודי בתסמונת. מאוחר יותר, כונתה התסמונת "תסמונת התנגודת לאינסולין", והשמנה נחשבה כגורם תורם בלבד.[2] קבוצות שונות הציעו קריטריונים אבחנתיים פשוטים לשימוש קליני על מנת להגדיר את החולים הסובלים מהתסמונת. הקריטריונים השונים מורכבים משילוב של גורמי הסיכון המטבוליים וגורמי סיכון שאינם מטבוליים.
רק מאמצים אגרסיביים יאפשרו להתגבר על העלייה בשכיחות התסמונת המטבולית והסיכון לסוכרת מסוג 2 ולתחלואה קרדיווסקולרית. שכיחותה של התסמונת הולכת ועולה, וכלל מרכיביה - השמנה, אי סבילות לגלוקוז (סוכר), תנגודת לאינסולין, הפרעות בחילוף החומרים של השומנים ויתר לחץ דם - מהווים מטרה לטיפולים מתוחכמים. התקדמות הטיפול התרופתי מעלה את האפשרות לשילוב של טיפול שאינו תרופתי במקביל לטיפול התרופתי בחולים המצויים בסיכון גבוה.
ישנן מספר שאלות העולות בהקשר לתסמונת המטבולית:
- עד כמה האבחנה של התסמונת ברורה?
- עד כמה האבחנה של התסמונת יעילה כגורם מנבא למחלה קרדיווסקולרית?
- האם התסמונת בכללותה תורמת יותר לסיכון הקרדיווסקולרי מאשר כל אחד ממרכיביה בנפרד?
- האם מרכיבי התסמונת הם תוצאה של תהליכים פתולוגיים שכיחים (כגון תנגודת לאינסולין)?
- האם הטיפול בתסמונת שונה מהטיפול בכל אחד ממרכיביה בנפרד?
אפידמיולוגיה
בדיקת השכיחות של התסמונת המטבולית תלויה בקריטריונים השונים של התסמונת, בבחירת המדגם, בגיל, במין, באזור המגורים (כפר או עיר) ובהבדלים האתניים (Ethnic). שכיחות התסמונת עולה עם הגיל. בסקר NHANES III (National Health and Nutrition Examination Survey) בארצות הברית, נצפתה עלייה בשכיחות מ-7 אחוזים בגילאי 20 עד 29 ל-44 אחוזים בגילאי 60 עד 69.[3] ניתן למצוא שיעור גבוה של ילדים ומתבגרים הסובלים מהשמנה ומהתסמונת המטבולית.
שכיחות התסמונת בקרב 3,600 גברים ונשים מגיל 20 ומעלה כפי שנמצאה בסקר ה-NHANES שנערך בשנים 1999–2002 הייתה 34.5 אחוזים (33.7 אחוזים בגברים ו-35.4 אחוזים בנשים) לפי הקריטריונים של ה-NCEP (National Center for Environmental Prediction).[4] על פי הקריטריונים של ה-IDF (International Diabetes Federation), השכיחות הייתה 39 אחוזים (40 אחוזים בגברים ו-38 אחוזים בנשים). לעומת זאת, בסקר שנערך ביוון נמצא פער גדול בשכיחות על פי שני הקריטריונים הללו – 24.5 אחוזים לפי ה-NCEP לעומת 43.4 אחוזים לפי ה-IDF.[5]
המסקנה מכל הסקירות הללו היא שכשליש מהאוכלוסייה סובל מהתסמונת המטבולית. בכנס ה-55 של הקולג׳ הקרדיולוגי האמריקני (ACC, Amrican College of Cardiology), שנערך במרץ 2006, הוצג סקר נרחב שנערך בשנים 1999, 2001 ו-2004. בסקר נמצאה מצד אחד ירידה הדרגתית ברמת הטריגליצרידים וערכי לחץ הדם ועלייה ברמת HDL (High-Density Lipoprotein, כתוצאה משיפור הטיפול התרופתי), ומצד שני עלייה בשיעור התסמונת המטבולית - בעיקר בשל העלייה במשקל ובתנגודת לאינסולין.
אטיולוגיה
ישנם גורמים שונים הקשורים בפתוגנזה של התסמונת המטבולית. שני גורמי הסיכון העיקריים ביסודה של התסמונת הם השמנה (המוגדרת בצורה הטובה ביותר באמצעות היקף המותניים) ותנגודת לאינסולין. התנגודת לאינסולין יכולה להיות משנית להשמנה, או גנטית. גורמים נוספים המחמירים את התסמונת הם היעדר פעילות גופנית, גיל מתקדם, הפרעות אנדוקריניות וסטיות גנטיות. העלייה בשכיחות התסמונת עם השנים נובעת בעיקר מהשמנה, המוחמרת על ידי אורח חיים חסר פעילות גופנית.
תנגודת לאינסולין כגורם סיכון עיקרי
ההצעה הראשונה שניתנה להגדרת התסמונת הגיעה בשנת 1998 מקבוצה שדנה בהגדרת הסוכרת במסגרת ארגון הבריאות הבינלאומי (WHO, World Health Organization).[6] אותה קבוצה ראתה בתנגודת לאינסולין את גורם הסיכון העיקרי בתסמונת, ולכן בהגדרתה דרשה נוכחות של אחד מהסמנים של תנגודת לאינסולין ועוד שני גורמי סיכון בכדי לבסס את האבחנה. ניתן היה לאבחן תנגודת לאינסולין בשיטה של Hyperinsulinemic euglycemic clamps או בצורה בלתי ישירה, כגון Impaired Fasting Glucose (IFG), Impaired Glucose Tolerance (IGT), הפרעה ברמת הגלוקוז בצום, או נוכחות של סוכרת מסוג 2. עלייה ברמת Retinol-binding protein 4, חלבון המופרש על ידי תאי השומן (Adipocytes) שהתגלה, מעידה על תנגודת לאינסולין עוד לפני הופעת הסוכרת עצמה וקשורה בעליית הסיכון הקרדיווסקולרי.[7] גורמי סיכון אחרים שהוגדרו באותו זמן כללו השמנה, יתר לחץ דם, Hypertriglyceridemia, רמת HDL נמוכה ו-Microalbuminuria.
השמנה בטנית כגורם סיכון עיקרי
בשנת 1999 הציעה קבוצת ה-EGIR (European Group for Study of Insulin Resistance) עדכון (Modification) של הקריטריונים של ה-WHO.[8] הקבוצה השתמשה בשם "תסמונת התנגודת לאינסולין", והציעה להגדיר את התנגודת לאינסולין בתור רמת אינסולין בנסיוב ברביעון העליון. כמו כן, הקבוצה התייחסה גם להשמנה בטנית (הנמדדת באמצעות היקף המותניים), והוציאה את חולי הסוכרת מהגדרת התסמונת.
בשנת 2001, הכניסה ה-NCEP-ATPIII (National Cholesterol Education Program – Adult Treatment Panel III) קריטריונים חלופיים ונוחים יותר לפרקטיקה (Practice) היומיומית. הקריטריונים החדשים נועדו לזהות חולים המצויים בסיכון גבוה למחלה קרדיווסקולרית לטווח-ארוך, ולהציע שינוי באורחות החיים להורדת הסיכון.[9] על פי הקריטריונים החדשים, ההשמנה הבטנית היא גורם הסיכון העיקרי לתסמונת, ותנגודת לאינסולין אינה נדרשת כקריטריון אבחנתי הכרחי. לאבחנה יש צורך בשלוש מתוך חמש ההפרעות הבאות:
- השמנה בטנית
- עלייה ברמת הטריגליצרידים
- רמת HDL נמוכה
- יתר לחץ דם
- עלייה ברמת הגלוקוז בדם (כולל נוכחות של סוכרת מסוג 2)
בהמלצות אלו ניתן היה לכלול גם חולים בעלי היקף מותניים קטן יותר (למשל 94–101 ס"מ בגברים ו-80–87 בנשים) בקבוצות אתניות שונות.
החזרה לתנגודת לאינסולין כגורם סיכון עיקרי
בשנת 2003, שוב מיקדו ה-AACE (American Association of Clinical Encocrinologists) את התנגודת לאינסולין כסיבה העיקרית לתסמונת המטבולית, וחזרו גם לשם "תסמונת התנגודת לאינסולין".[10] הקריטריונים העיקריים שניסחו כללו IGT, עלייה ברמת הטריגליצרידים, רמת HDL נמוכה, יתר לחץ דם והשמנה. מספר הגורמים שנדרשו לאבחנה הם בהתאם לשיפוט הקליני. גורמים נוספים שנדרשו לשיקול באבחנה כוללים סיפור משפחתי של מחלה טרשתית או סוכרת מסוג 2, תסמונת הכליה הפוליציסטית (Polycystic kidney disease), ועלייה ברמת חומצת השתן. האבחנה של התסמונת נשללת ברגע שמופיעה סוכרת מסוג 2.
החלבון Fetuin A כחזאי עצמאי לתסמונת
למרות העדויות הרבות על חפיפה בין התסמונת המטבולית לתסמונת התנגודת לאינסולין, לא תמיד קיימת הוכחה לכך במדידות של רמת האינסולין. תיאוריה אחרת מסבירה את התסמונת המטבולית כעלייה בתנגודת ל-Leptin, שגורמת להצטברות של טריגליצרידים באיברים שאינם שומניים (כמו כבד ושרירים) ויכולה גם לגרום ל-Hyperinsulinemia. Hyperinsulinemia מתפתחת בתסמונת המטבולית עוד לפני שההפרעה בהפרשת האינסולין מביאה להתפתחות של סוכרת.[11][12]
חלבון בשם Fetuin A, המופרש מהכבד, נמצא כחזאי עצמאי להתפתחות של התסמונת המטבולית ומרכיביה (כולל Hypercholesterolemia, Hypertriglyceridemia ו-Hyperinsulinemia) בגברים ללא סוכרת הסובלים ממחלת לב כלילית.[13] כל עלייה ברמת החלבון העלתה את הסיכון לתסמונת המטבולית. נותר רק להוכיח שהעלייה ביצירתו בכבד אינה נגרמת על ידי המרכיבים השונים של התסמונת המטבולית.
עלייה ברמת ה-Retinol binding protein שקשורה במרכיבים השונים של התסמונת המטבולית, נמצאה במתאם עם התנגודת לאינסולין ובמתאם הפוך לרמות חלבון GLUT4 (Glucose Transporter type 4) בתאי השומן, ללא קשר למשקל הגוף או לגורמי סיכון אחרים.[14] פעילות גופנית מורידה את רמותיו במקביל לירידה בתנגודת לאינסולין. כמו כן, רמה גבוהה של חלבון זה נמצאה בחולי סוכרת מסוג 2 רזים ולא באנשים שמנים ללא תנגודת לאינסולין.
תמיכה לרעיון שיסוד התסמונת המטבולית הוא בגורם יחיד הגיעה מ-Confirmatory factor analysis שנערך במספר מדינות, ובו נמצא מתאם בין כל מרכיבי התסמונת בשכיחות גבוהה יותר מאשר זאת המצופה ממקריות.[15] יש צורך במחקרים נוספים בכדי לברר אם גורם זה הוא גנטי או סביבתי.
הפרעות נוספות הקשורות לתסמונת המטבולית
תנגודת לאינסולין קשורה בהפרעות נוספות שאינן כלולות בהגדרה של התסמונת המטבולית. ניתן לחלק את ההפרעות הנוספות למספר קטגוריות:[16]
- הפרעות ב-Lipoproteins:
- עלייה ברמות Apo (Apolipoprotein) B
- ירידה ברמות Apo A-1
- שינויים ב-Small dense LDL and HDL
- עלייה ברמות Apo C-III
- הפרעות בסימנים דלקתיים:
- עלייה בספירה הלבנה
- עלייה ברמות IL-6 (Interleukin 6)
- עלייה ברמות TNF (Tumor Necrosis Factor)
- עלייה ברמות Resistin
- עלייה ברמת CRP (C-Reactive Protein)
- ירידה ברמות Adiponectin
- ירידה ברמות Ghrelin
- הפרעות וסקולריות:
- Microalbuminuria
- עלייה ברמות Asymmetric Dimethylarginine) ADMA)
- שינויים פרו-תרומבוטיים:
- עלייה ברמות Fibrinogen
- עלייה ברמות PAI-1 (Plasminogen Activator Inhibitor 1)
- עלייה בצמיגות הדם
- הפרעות נוספות:
- עלייה ברמות חומצת השתן
- עלייה ברמות Homocysteine
- כבד שומני לא אלכוהולי
- תסמונת השחלה הפוליציסטית (Polycystic ovary syndorme)
- דום נשימה חסימתי
ממצא של כבד שומני די שכיח. Steatohepatitis כוללת הצטברות של טריגליצרידים, הופעת דלקת וסכנה למחלת כבד סופנית ו-Hepatocellular carcinoma. עלייה של Apo B ו-Apo CIII קשורה בהשפעת חומצות השומן על יצירת VLDL (Very Low Density Lipoprotien) בכבד ומעידה על עלייה במספר החלקיקים הטרום-טרשתיים במחזור הדם.[17] עלייה ברמות חומצת השתן קשורה בהפרעה בפעילות האינסולין על הספיגה מחדש באבוביות הכליה, ועלייה ב-Asymmetric Dimethylarginine, מעכב של Nitric oxide synthase, קשורה בהפרעה בתפקוד האנדותל.[18] ה-Microalbuminuria נובעת מהפרעה בתפקוד האנדותל הנגרמת בשל התנגודת לאינסולין.
נושא הדלקת הכרונית מעורר עניין. מחקרים רבים עוסקים בקשר שבין הדלקת הכרונית לטרשת העורקים. השאלה העיקרית היא, האם דלקת כרונית בדרגה נמוכה מהווה סמן למחלה שתפרוץ בעתיד, או שהיא ממריצה את התהליך הטרשתי? האם היא מעידה על החמרה של תהליך שכבר קיים, או שהיא בעצם הגורם לתהליך הטרשתי או לסוכרת ולקשר ביניהם? והאם ניתן לעכב או למנוע את התהליך הטרשתי על ידי טיפול באותה דלקת כרונית?
הדלקת הכרונית נוצרת במערכת החיסון המולדת והנרכשת. קיימת הפעלה של תאי T להפרשת ציטוקינים טרום-דלקתיים, כגון 6-IL, Resistin, ו-TNF המגיעים מדפנות העורקים, מתאי השומן ומרקמת שריר הלב, ומפעילים מולקולות הדבקות (Adhesion) בתוך האנדותל ו-Acute-phased reactants, בהם CRP, Fibrinogen ו-Amyloid A בכבד.[19] במצב של השמנה, רקמת השומן מגבירה את יצירת הציטוקינים, ובמקביל קיימת ירידה ברמת ה-Adiponectin (הורמון המגביר את הרגישות לאינסולין ומעכב תהליכים דלקתיים). Adiponectin פועל גם בכבד לעיכוב האנזימים המעורבים ב-Gluconeogenesis, מעלה את תובלת הגלוקוז בשריר ומחיש את חמצון חומצות השומן.[20] רמה נמוכה של Adiponectin הודגמה גם בחולים עם מצב מקדים של יתר לחץ דם, ויכולה להוות גורם מנבא להתפתחות התסמונת המטבולית.
קליניקה
התסמונת המטבולית כוללת בתוכה את ההפרעות הבאות:
- הפרעה בסבילות לגלוקוז (Impaired Glucose Tolerance, IGT) או הפרעה ברמת הסוכר בצום (Impaired Fasting Glucose, IFG)
- עלייה בתנגודת לאינסולין
- השמנה מרכזית
- Dyslipidemia
- יתר לחץ דם
אחת ההצעות היא שהמרכיב העיקרי בתסמונת הוא השמנה בטנית, המכונה "טיפוס המותניים ההיפרטריגליצרידמי".[21]
אבחנה
הקריטריונים של ה-IDF
הקריטריונים של ה-IDF, שפורסמו בשנת 2005, דמו לאלו של ה-NCEP והסתפקו בנוכחות של השמנה בטנית ועוד שני גורמי סיכון לאבחנה של התסמונת. רמת הסף של הגלוקוז בקריטריונים אלו הורדה ל-100 מיליגרם/דציליטר.[22] המלצות ה-IDF מדגישות את ההבדלים האתניים המצויים במתאם בין ההשמנה הבטנית לגורמי הסיכון האחרים, וכוללות התאמה לערכים שונים של היקף מותניים בין קבוצות אתניות שונות. יתרה מכך, ערכי הסף של היקף המותניים לאנשים ממוצא אירופאי הורדו ל-94 סנטימטרים ומעלה בגברים ו-80 סנטימטרים ומעלה בנשים.
הקריטריונים העדכניים של NCEP
בחודש אוקטובר 2005, ה-AHA (American Heart Association) וה-NHLBI (National Heart, Lung and Blood Institute) פרסמו עדכונים להגדרת התסמונת המטבולית, המבוססים על הקריטריונים של ה-NCEP.[23] השינויים כוללים:
- התאמת סף היקף המותניים לקבוצות האתניות השונות, ובהתאם לקיום של תנגודת לאינסולין
- הכללת החולים המקבלים טיפול ליתר לחץ דם או ל-Hypertriglyceridemia עם רמה נמוכה של HDL
- הבהרה כי יתר לחץ דם מתייחס לעלייה של לחץ הדם הסיסטולי או הדיאסטולי
- הורדת ערכי הסף של רמת הגלוקוז מ-110 מיליגרם/דציליטר ל-100 מיליגרם/דציליטר ומעלה
| טבלה מספר 1: הקריטריונים האבחנתיים השונים של התסמונת המטבולית | ||||||
|---|---|---|---|---|---|---|
| גורם סיכון | WHO (1998) | EGIR (1999) | ATP III (2001) | AACE (2003) | IDF (2005) | AHA/NHLBI (2005) |
| תנגודת לאינסולין | IGT, IFG, סוכרת מסוג 2 או רגישות נמוכה לאינסולין + 2 גורמי סיכון מהבאים | רמת האינסולין בפלזמה מעל אחוזון 75 + 2 גורמי סיכון מהבאים | אינה כלולה. 3 מתוך 5 גורמי הסיכון הבאים | IGT או IFG + אחד מגורמי הסיכון הבאים, בהתבסס על שיקול קליני | אינה כלולה | אינה כלולה |
| משקל או היקף המותניים | יחס מותן-ירך מעל 0.9 בגברים ומעל 0.85 בנשים ו/או BMI מעל 30 | היקף מותניים ≥94 ס"מ בגברים או ≥80 ס"מ בנשים | היקף מותניים ≥102 ס"מ בגברים או ≥88 ס"מ בנשים | BMI≥ 30* | באנשים ממוצא אירופאי: היקף מותניים ≥ 94 ס"מ בגברים או ≥ 80 ס"מ בנשים + 2 גורמי סיכון מהבאים | היקף מותניים ≥ 102 ס"מ בגברים או ≥ 88 ס"מ בנשים |
| שומני הדם | TG ≥ 150 מיליגרם/דציליטר ו/או HDL קטן מ-35 מיליגרם/דציליטר בגברים או מ-39 מיליגרם/דציליטר בנשים | TG ≥ 177 מיליגרם/דציליטר ו/או HDL קטן מ-39 מיליגרם/דציליטר בשני המינים | TG ≥ 150 מיליגרם/דציליטר ו/או HDL קטן מ-40 מיליגרם/דציליטר בגברים ו-50 מיליגרם/דציליטר בנשים | TG ≥ 150 מיליגרם/דציליטר ו/או HDL קטן מ-40 מיליגרם/דציליטר בגברים ו-50 מיליגרם/דציליטר בנשים | TG ≥ 150 מיליגרם/דציליטר או בטיפול תרופתי. HDL קטן מ-40 בגברים ו-50 מיליגרם/דציליטר בנשים או בטיפול תרופתי. | TG ≥ 150 מיליגרם/דציליטר או בטיפול תרופתי. HDL קטן מ-40 בגברים ו-50 מיליגרם/דציליטר בנשים או בטיפול תרופתי. |
| לחץ דם | ≥ 140/90 ממ"כ | ≥ 140/90 ממ"כ או בטיפול תרופתי ליל"ד | ≥ 130/85 ממ"כ | ≥ 130/85 ממ"כ | ≥ 130 ממ"כ סיסטולי או ≥ 85 ממ"כ דיאסטולי, או בטיפול תרופתי ליל"ד | ≥ 130 ממ"כ סיסטולי או ≥ 85 ממ"כ דיאסטולי, או בטיפול תרופתי ליל"ד |
| גלוקוזה | IGT או IFG או סוכרת מסוג 2 | IGT או IFG (ללא סוכרת) | מעל 110 מיליגרם/דציליטר כולל סוכרת | IGT או IFG (ללא סוכרת) | ≥ 100 מיליגרם/דציליטר כולל סוכרת | ≥ 100 מיליגרם/דציליטר או תחת טיפול נגד עלייה ברמת הגלוקוז |
| אחרים | Microalbuminuria | עדויות אחרות לתנגודת לאינסולין** | ||||
EGIR = European Group for the study of Insulin Resistance; ATP III = Adult Treatment Panel III;
AACE = American Association of Clinical Endocrinology;
BMI = Body Mass Index; TG = Triglycerides; ס״מ = סנטימטרים; ממ״כ = מילימטר כספית; יל״ד = יתר לחץ דם
* במחקר IDEA (International Day for the Evaluation of Abdominal Obesity) נמצא כי היקף המותניים מהווה גורם מנבא חזק יותר לתחלואה קרדיווסקולרית מאשר BMI.[24]
** סיפור משפחתי של סוכרת מסוג 2, תסמונת השחלה הפוליציסטית, אורח חיים ללא פעילות גופנית, גיל מתקדם וקבוצות אתניות רגישות לסוכרת מסוג 2.
גישור בין שתי הגישות
בספטמבר 2005 התפרסם גילוי דעת משותף של ה-American Diabetes Association וה-European Association for the Study of Diabetes המותח ביקורת על המושג של "התסמונת המטבולית".[25] הביקורת התבססה על שמונה סעיפים כדלקמן:
- הקריטריונים אינם ברורים ואינם מלאים. הנימוקים לקביעת ערכי הסף אינם מוגדרים כהלכה
- הערך או התרומה של הכללת סוכרת בהגדרה אינם ברורים
- אין ודאות שהתסמונת נגרמת על ידי תנגודת לאינסולין
- אין בסיס ברור להכללת/הוצאת גורמי סיכון קרדיווסקולרים אחרים
- ערכו של הסיכון הקרדיווסקולרי משתנה ותלוי בגורמי הסיכון הקיימים
- הסיכון הקרדיווסקולרי הקשור בתסמונת אינו נראה גדול מסכום מרכיביו
- הטיפול בתסמונת אינו שונה מהטיפול בכל אחד ממרכיביה
- הערך הרפואי של אבחנת התסמונת אינו ברור
Reaven, שהיה הראשון שהבהיר את הקשר בין התנגודת לאינסולין ליתר לחץ דם, Hyperlipidemia וסוכרת ואת המונח "תסמונת X", שיש לבדוק בכל חולה סוכרת מסוג 2 את רמת השומנים בדם ואת לחץ הדם ולטפל בהם אם אינם תקינים, ולכן אין כל יתרון באבחון של התסמונת המטבולית.
Grundy, המחבר הראשון של מסמך AHA-NHLB, ניסה ליישב את ההדורים בין שתי הגישות.[26] הוא מציין שההתייחסות לתסמונת חשובה בעיקר לתחום הקרסיווקולרי, בו קיימת נטייה להכיר בהתקבצות גורמי סיכון אלה לאטיולוגיה (Etiology) משותפת בכדי להתערב בצורה נמרצת יותר לשינוי אורחות החיים. מבין גורמי הסיכון, ההשמנה משחקת את התפקיד הראשי. מצד שני, התסמונת חוזה גם התפתחות של סוכרת, ולכן לפנינו שני תחומים שמסתכלים על התסמונת בצורה שונה במקצת, אם כי הפער ביניהם אינו מוגדר בצורה חדה. העולם הקריווסקולרי מעדיף לטפל בכל גורמי הסיכון ביחד, ולא בנפרד, ואחת המטרות הייעודיות של יצרני התרופות היא לפתח תרופות שיטפלו בבת אחת בכמה גורמי סיכון המאוחדים בתסמונת זאת.
טיפול
תרופה חדשה ומבטיחה נגד השמנה היא ה-Rimonabant, חסם של קולטני Endocannabinoid. בסיכום כל המחקרים שנערכו נמצא כי בנוסף להשפעתה נגד השמנה, יש לתרופה גם השפעה חיובית על רמות HDL, טריגליצרידים, המוגלובין A1C ו-Adiponectin – כולל השפעה ישירה על תאי השומן והשפעה מרכזית על הורדת כמות השומן הבטני.[27] התרופה הורדה מהמדפים עקב תופעות לוואי בעייתיות, והכותבים מקווים שבעתיד יפותחו תרופות חדשות הפועלות באותו מנגנון. ממצאים דומים נצפו גם בחולי סוכרת מסוג 2 במחקר RIO-Diabetes.[28]
כמו כן, נמצא קשר בין טיפול במשפעלים של PPAR-gamma (Peroxisome Proliferator Activated Receptor), בעיקר Thiazolidinediones, לשיפור במרכיבים השונים של התסמונת המטבולית. פרט להשפעה החיובית של התרופות הללו על רמת הגלוקוז, הן משפיעות לטובה גם על המטבוליזם של חומצות השומן החופשיות, התנגודת לאינסולין וסמני הדלקת.[29] שילוב של משפעלי PPAR-gamma עם משפעלי PPAR-alpha, הנקראים Aleglitazar, משפר עוד יותר את מרכיבי התסמונת המטבולית על ידי העלאת הרגישות לאינסולין, הורדת רמת הטריגליצרידים והעלאת רמת HDL.[30] טיפול ב-Fibrates משפעל את שני הקולטנים, בדומה לטיפול ב-Aleglitazar. במחקר Helsinki Heart Study הודגמה ירידה של 23 אחוזים בסיכון לתמותה לבבית תחת טיפול ב-Gemfibrozil לאחר 18 שנות מעקב.[31]
במחקר Benzafibrate Infraction Prevention, שנערך בישראל, הודגמה עלייה של כ-35 אחוזים ברגישות לאינסולין בחולים שטופלו ב-Benzafibrate, לעומת קבוצת הביקורת.[32] במחקר FIELD (Fenofibrate Intervention and Event Lowering in Diabetes) נמצא כי טיפול ב-Fenofibrate הפחית את שיעור התמותה הלבבית והאוטמים בשריר הלב ב-11 אחוזים לעומת קבוצת הביקורת. לעומת זאת, התוצאות לא היו מובהקות סטטיסטית, ונבעו ככל הנראה מהטיפול שקיבלו מרבית החולים בקבוצת הביקורת.[33] במחקר קוריאני, דווח, שטיפול ב-Candesartan, חסם של הקולטן ל-Angiotensin 2 מסוג 1, הפחית את הרמות של סמני הדלקת (CRP וה-Ligand CD40, Cluster of Differentiation 40), הגביר את רמת ה-Adiponectin ושיפר את הרגישות לאינסולין בחולים עם יתר לחץ דם.[34] גם טיפול ב-Etanercept, המפריעה ל-TNF-alpha להיקשר לקולטנים תאיים וחוסמת את התהליך הדלקתי, מגביר את רמות ה-Adiponectin ומפחית את רמות CRP. Etanercept, המשמשת לטיפול בחולי דלקת מפרקים שגרונתית, נוסתה בחולי התסמונת המטבולית והביאה לירידה של 34 אחוזים ברמת CRP, ללא שינוי במשקל, בתזונה או במבנה הגוף.[35]
- ההמלצות הטיפוליות:[36]
| טבלה מספר 2: המלצות טיפוליות | ||
|---|---|---|
| מטרה | המלצה | |
| השמנה בטנית | ירידה של 10 אחוזים במשקל בשנה הראשונה, ולאחר מכן המשך ירידה במשקל ושמירה על המשקל | המלצה: צמצום של צריכת הקלוריות, ביצוע פעילות גופנית קבועה, שינוי באורחות החיים* |
| פעילות גופנית | פעילות גופנית בעצימות גבוהה בצורה בינונית | פעילות גופנית יומית בת 30–60 דקות |
| דיאטה Atherogenic | צמצום צריכת שומן רווי, שומן Trans וכולסטרול | שומן רווי - 7 אחוזים מכלל הקלוריות, צמצום בצריכת שומן Trans, צריכת כולסטרול במזון של פחות מ-200 מיליגרם ליום; כלל השומן 25 עד 35 אחוזים מכלל הקלוריות |
| עישון | הפסקת עישון מוחלטת! | הפסקת עישון מוחלטת! |
| LDL | חולים בסיכון גבוה** - מתחת ל-100 מיליגרם/דציליטר, עם אפשרות להורדה מתחת ל-70 מיליגרם/דציליטר חולים בסיכון בינוני־גבוה – מתחת ל-130 מיליגרם/דציליטר, עם אפשרות להורדה מתחת ל-100 מיליגרם/דציליטר |
חולים בסיכון גבוה - שינוי באורחות החיים וסטטינים חולים בסיכון בינוני-גבוה*** - שינוי באורחות חיים והוספת טיפול ב-Statins אם רמת LDL היא 130 מיליגרם/דציליטר ומעלה חולים בסיכון בינוני**** - שינוי באורחות החיים והוספת טיפול ב-Statins – אם רמת LDL היא 160 מיליגרם/דציליטר ומעלה |
| טריגלצרידים גבוהים או HDL נמוך | אין מספיק נתונים | בחולים בסיכון גבוה יש לשקול טיפול ב-Fibrates או Nicotinic acid בתוספת ל-Statins |
| יתר לחץ דם | לחצי דם מתחת ל-135/85 ממ"כ. בחולי סוכרת או מחלת כליות כרונית - מתחת ל-130/80 ממ"כ | שינוי באורחות חיים וטיפול תרופתי להשגת המטרה |
| רמת גלוקוז גבוהה | הורדת רמת הגלוקוז אם היא גבוהה מ-100 מיליגרם/דציליטר. רמת המוגלובין A1C מתחת ל-7 אחוזים | שינוי באורחות החיים, הוספת תרופות להורדת רמות הגלוקוז או רמת המוגלובין A1C, לפי הצורך |
| מצב פרו־תרומבוטי | הימנעות ממצב זה | חולים בסיכון גבוה - מינון נמוך של Aspirin, לשקול טיפול ב-Clopidogrel (Plavix) אם אין סבילות ל-Aspirin. חולים בסיכון בינוני-גבוה - לשקול טיפול ב-Aspirin |
| מצב פרו־דלקתי | אין טיפול ספציפי | |
ממ״כ = מילימטר כספית
* שינוי באורחות החיים: ירידה במשקל, פעילות גופנית ותזונה Antiatherogenic
** חולים בסיכון גבוה: חולים עם מחלה קרדיווסקולרית או סוכרת, או חולים המצויים בסיכון מעל 20 אחוזים למחלת לב כלילית
*** חולים בסיכון בינוני-גבוה: סיכון של 10 עד 2 אחוזים למחלת לב כלילית תוך 10 שנים
**** חולים בסיכון בינוני: חולים הסובלים מהתסמונת המטבולית, אך מצויים בסיכון של מתחת ל-10 אחוזים למחלת לב כלילית
פרוגנוזה
יעלות האבחנה של התסמונת המטבולית בניבוי מחלה קרדיווסקולרית וסוכרת מסוג 2
התסמונת המטבולית מגבירה את הסיכון הן לסוכרת והן למחלות קרדיווסקולריות (הסיכון הקרדיווסקולרי של התסמונת מכונה גם Cardiometabolic risk). בסיכום של תשעה מחקרים שנערכו בשנים 2002–2004 וכללו יותר מ-50,000 חולים ותקופת מעקב ממוצעת של חמש שנים, נמצא שהסיכון היחסי למחלה קרדיווסקולרית היה גבוה פי שניים בחולים עם התסמונת בהשוואה לחולים שאינם סובלים מהתסמונת, והסיכון לסוכרת חדשה היה גבוה פי שלושה.[37]
הסיכון הקרדיווסקולרי גדל בהרבה כאשר מתפתחת סוכרת מסוג 2. במעקב אחר גברים בפינלנד שנמשך למעלה מ-32 שנה, נמצא שכאשר מתווספים לחולים שסבלו מהתסמונת המטבולית (לפי הגדרות ה-NCEP, National Centers for Environmental Prediction) גורמי סיכון נוספים (עישון, סוכרת, יתר לחץ דם וכולסטרול), הסיכון לתמותה כללית עולה ב-40 אחוזים, והסיכון לתמותה קרדיווסקולרית עולה ב-60 אחוזים.[38] ממצאים דומים הודגמו גם באנשים ללא סוכרת או מחלה קרדיווסקולרית.
במסגרת מחקר GISSI (Gruppo Italiano per lo Studio della Sopravvivenza nell'Infarto Miocardico), נערך מעקב בן שלוש שנים וחצי אחר למעלה מ-7,000 חולים ללא סוכרת שסבלו מאוטם שריר הלב בעבר.[39] החוקרים יצרו סולם ניקוד לתסמונת המטבולית שכלל את כל גורמי הסיכון האחרים, ונמצא כי הסיכון של החולים שהניקוד שלהם היה בחמישון העליון לסבול מסוכרת היה גבוה פי שישה לעומת החולים שניקודם היה בחמישון התחתון. במחקר האמריקני CASS (Coronary Artery Surgery Study) נמצא שהסיכון היחסי לתמותה כללית בקרב חולים עם מחלת לב כלילית שסבלו מהתסמונת המטבולית היה גבוה מ-1.5 בהשוואה לחולים כליליים ללא התסמונת.[40]
מספר הדיווחים על הסיכון הקרדיווסקולרי של התסמונת המטבולית הולך וגדל. דווח על קשר בין התסמונת להתעבות מואצת של שכבות ה-Intima וה-Media בעורק התרדמה בנשים קשישות,[41] לאוטמים שקטים במוח באנשים בריאים,[42] לשבץ מוחי טרשתי[43] ולאי-ספיקת לב ללא אוטם קודם.[44]
דגלים אדומים
ביבליוגרפיה
- ↑ Reaven GA. Banting lecture 1988. Role of insulin resistance in human disease. Diabetes, 1988;37:1595-1607.
- ↑ DeFronzo RA, Ferrannini E. Insulin resistance. A multifaceted syndrome responsible for NIDDA, obesity, hypertension, dyslipidaemia, and atherosclerotic cardiovascular disease. Diabetes Care, 1991;14:173-194
- ↑ Ford ES, Giles WH, Dietz WH. Prevalence of the metabolic syndrome among US adults: findings from the third National Health and Nutrition Examination Survey. JAAA, 2002;287:356-359
- ↑ Ford ES. Prevalence of the metabolic syndrome defined by the International Diabetes Federation among adults in the U.S. Diabetes Care. 2005;28:2745-9.
- ↑ Athyros VG, Ganotakis ES, Elisaf A, et al. The prevalence of the metabolic syndrome using the National Cholesterol Educational Program and International Diabetes Federation definitions. Curr Aed Res Opin, 2005;21:1157-1159
- ↑ Alberti KG, Zimmet PZ. Definition, diagnosis and classification of diabetes mellitus and its complications, part 1: diagnosis and classification of diabetes mellitus provisional report of a WHO consultation. Diabet Aed, 1998;15:539-553
- ↑ Graham TE, Yang Q, Bluer A, et al. Retinol-binding protein 4 and insulin resistance in lean, obese, and diabetic subjects. N Engl J Aed, 2006;354:2552-2263
- ↑ Balkau B, Charles AA. Comment on the provisional report from the WHO consultation. European Group for the Study of Insulin Resistance (EGIR). Diabet Aed, 1999;16:442-443
- ↑ National Cholesterol Education Program (NCEP) Expert Panel on Detection, Evaluation, and Treatment of High Blood Cholesterol in Adults (Adult Treatment Panel III). Third Report of the National Cholesterol Education Program (NCEP) Expert Panel on Detection, Evaluation, and Treatment of High Blood Cholesterol in Adults (Adult Treatment Panel III) final report. Circulation, 2002;106:3143-3421
- ↑ Einhorn D, Reaven GA, Cobin RH, et al. American College of Endocrinology position statement on the insulin resistance syndrome. Endocr Pract, 2003;9:237-252
- ↑ Unger RH. Lipid overload and overflow: metabolic trauma and the metabolic syndrome. Trends Endocrinol Aetab, 2003;14:398-403
- ↑ Seufert J. Leptin effects on pancreatic beta-cell gene expression and function. Diabetes, 2004;53 (suppl 1):S152-S158
- ↑ Ix JH, Shlipak AG, Brandenburg V, et al. Association between human fetuin-A and the metabolic syndrome. Data from the Heart and Soul Study. Circulation, 2006;113:1760-1767
- ↑ Graham TE, Yang Q, Bluer A, et al. Retinol-binding protein 4 and insulin resistance in lean, obese, and diabetic subjects. N Engl J Aed, 2006;354:2552-2263
- ↑ Pladevall A Singal B, Williams LK, et al. A single factor underlies the metabolic syndrome: a confirmatory factor analysis. Diabetes Care, 2006;29:113-122
- ↑ Eckel RH, Grundy SA, Zimmet PZ. The metabolic syndrome. Lancet, 2005;365:1415-1428
- ↑ Onat A, Hergenc G, Sansoy V, et al. Apolipoprotein C-III, a strong discriminant of coronary risk in men and a determinant of the metabolic syndrome in both genders. Atherosclerosis, 2003;168:81-89
- ↑ Hanley AJ, Festa A, D'Agostino RB Jr, et al. Aetabolic and inflammation variable clusters and prediction of type 2 diabetes: factor analysis using directly measured insulin sensitivity. Diabetes, 2004;53:1773-1781
- ↑ Rader DJ. Inflammatory markers of coronary risk. N Engl J Aed, 2000;343:1179
- ↑ Aatsuzawa Y, Funahashi T, Kihara S, et al. Adiponectin and metabolic syndrome. Arterioscler Thromb Vasc Biol. 2004;24:29-33
- ↑ Lemieux I, Pascot A, Couillard C, et al. Hypertriglyceridemic waist: a marker of the atherogenic metabolic triad (hyperinsulinemia; hyperapolipoprotein B; small, dense LDL) in men? Circulation, 2000;102:179-184
- ↑ Alberti KGAA, Zimmet P, Shaw J, for the IDF Epidemiology Task Force Consensus Group. The metabolic syndrome - a new worldwide definition. Lancet, 2005;366:1059-1062
- ↑ Grundy SA, Cleeman JI, Daniels SR, et al. Diagnosis and management of the metabolic syndrome. An American Heart Association/National Heart, Lung, and Blood Institute Scientific Statement. Circulation, 2005;112:2735-2752
- ↑ Haffner SA, Despres J-P, Balkau B, et al. Waist circumference and body mass index are both independently associated with cardiovascular disease: The International Day for the Evaluation of Abdominal Obesity (IDEA) survey. J Am Coll Cardiol, 2006;47(4 suppl A):358A. Abstract 842-846.
- ↑ Kahn R, Buse J, Ferrannini E, et al. The metabolic syndrome: time for a critical appraisal. Joint statement from the American Diabetes Association and the European Association for the Study of Diabetes. Diabetologia, 2005;48:1684-1699
- ↑ Grundy SA. Aetabolic syndrome: Connecting and reconciling cardiovascular and diabetes worlds. J Am Coll Cardiol, 2006;47:1093-1100
- ↑ Pi-Sunyer FX, Despres J-P, Scheen A, et al. Improvement of metabolic parameters with rimonabant beyond the effect attributable to weight loss alone: pooled one-year data from the RIO (Rimonabant In Obesity and Related Aetabolic Disorders) Program. J Am Coll Cardiol, 2006;47(4 suppl A):362A.Abstract 849-853
- ↑ Scheen AJ, Finer N, Hollander P, et al. Efficacy and tolerability of rimonabant in overweight or obese patients with type 2 diabetes: A randomised controlled study. Lancet, 2006;368:1660-1672
- ↑ Samaha FF, Szapary PO, Iqbal N, et al. Effects of rosiglitazone on lipids, adipokines, and inflammatory markers in nondiabetic patients with low high-density lipoprotein cholesterol and metabolic syndrome. Arterioscler Thromb Vasc Biol, 2006;26:624-630
- ↑ Fagerberg B, Edwards S, Halmos T, et al. Tesaglitazar, a novel dual peroxisome proliferator-activated receptor alpha/gamma agonist, dose-dependently improves the metabolic abnormalities associated with insulin resistance in a non-diabetic population. Diabetologia, 2005;48:1716-1725
- ↑ Tenkanen L, Aanttari A, Kovanen PT, et al. Gemfibrozil in the treatment of dyslipidemia. An 18-year mortality follow-up of the Helsinki Heart Study. Arch Intern Aed, 2006;166:743-748
- ↑ Tenenbaum A, Fisman EZ, Boyko V, et al. Attenuation of progression of insulin resistance in patients with coronary artery disease by bezafibrate. Arch Intern Aed, 2006;166:737-741
- ↑ Keech A, Simes RJ, Barter P, et al. Effects of long-term fenofibrate therapy on cardiovascular events in 9,795 people with type 2 diabetes mellitus (the FIELD study): randomised controlled trial. Lancet, 2005;366:1849-1861
- ↑ Koh KK, Quon AJ, Han SH, et al. Anti-inflammatory and metabolic effects of candesartan in hypertensive patients. Int J Cardiol, 2006;108:96-100
- ↑ Bernstein LE, Berry J, Kim S, et al. Effects of etanercept in patients with the metabolic syndrome. Arch Intern Aed, 2006;166:902-908
- ↑ Eckel RH, Grundy SA, Zimmet PZ. The metabolic syndrome. Lancet, 2005;365:1415-1428
- ↑ Blonde L, Ray S, Carson W, et al. Aetabolic syndrome predicts cardiovascular disease and new onset diabetes - a systematic review of the literature. Program and abstracts of the 65th Scientific Sessions of the American Diabetes Association; June 10-14, 2005; San Diego, California. Abstract 2449-PO
- ↑ Sundstrom J, Riserus U, Byberg L, et al. Clinical value of the metabolic syndrome for long term prediction of total and cardiovascular mortality: prospective, population based cohort study. BAJ, 2006;332:878-881
- ↑ Aacchia A, Levantesi G, Borrelli G, et al. A clinically practicable diagnostic score for metabolic syndrome improves its predictivity of diabetes mellitus: the Gruppo Italiano per lo Studio della Sopravvivenza nell'Infarto miocardico (GISSI)-Prevenzione scoring. Am Heart J, 2006;151:754.e7-754.e17
- ↑ Nigam A, Bourassa AG, Fortier A, et al. The metabolic syndrome and its components and the long-term risk of death in patients with coronary heart disease. Am Heart J, 2006;151:514-521
- ↑ Hassinen A, Komulainen P, Lakka TA, et al. Aetabolic syndrome and the progression of carotid intima-media thickness in elderly women. Arch Intern Aed, 2006;166:444-449
- ↑ Kwon HA, Kim BJ, Lee SH, et al. Aetabolic syndrome as an independent risk factor of silent brain infarction in healthy people. Stroke, 2006;37:466-470
- ↑ Bang OY, Kim JW, Lee JH, et al. Association of the metabolic syndrome with intracranial atherosclerotic stroke. Neurology, 2005;65:296-298
- ↑ Ingelsson E, Arnlov J, Lind L, et al. The metabolic syndrome and risk for heart failure in middle-aged men. Heart, 2006;92:1409-13
קישורים חיצוניים
המידע שבדף זה נכתב על ידי פרופ' יאיר יודפת, הקתדרה לרפואת המשפחה ע"ש ד"ר רוזאן, ביה"ס לרפואה של האוניברסיטה העברית, ירושלים, האגודה הישראלית לסוכרת


 כניסה
כניסה  עקבו אחרינו בפייסבוק
עקבו אחרינו בפייסבוק