סרטן ריאה - Lung Cancer
| סרטן ריאה | ||
|---|---|---|
| Lung Cancer | ||
| ||
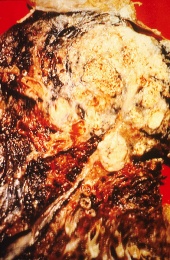
חתך רחבי של ריאת אדם; השטח הלבן באונה העליונה הוא סרטן, והאזורים השחורים הם שינויי צבע שנגרמו עקב עישון.
| ||
| ICD-10 | Chapter C 33. Chapter C 34. |
|
| ICD-9 | 162 | |
| MeSH | D002283 | |
| יוצר הערך | ד"ר מיה גוטפריד וד"ר דודניק אליזבטה | |
לערכים נוספים הקשורים לנושא זה, ראו את דף הפירושים – סרטן ריאה
אפידמיולוגיה
שיעור התחלואה מסרטן ריאה נמצא בעלייה מתמדת, ונכון לשנת 2011 הוא גורם התמותה מסרטן מספר אחד בגברים והשלישי אצל הנשים. לפי הערכות סטטיסטיות מבוססת על נתוני עבר, במהלך שנת 2020 בארצות הברית, 228,820 אנשים יאובחנו עם סרטן ריאה וכ-135.720 ימותו כתוצאה מהמחלה [1]. בישראל, לפי נתוני הרישום הלאומי לסרטן, מאובחנים מדי שנה כ- 2500 מקרים חדשים של שאת ריאה [2].
תמונה 1. סרטן ריאה בישראל - מגמת התחלואה בעשור האחרון
פתולוגיה - סיווג
- סרטן ריאה נחלק לשני סוגים עיקריים
- Non-Small Cell Lung Cancer (NSCLC) (סרטן ריאה של התאים הלא קטנים) - מהווה כ-85 אחוזים מכלל מקרי סרטן ריאה. קיימים שלושה סוגים של סרטן ריאה מסוג NSCLC:
- Squamous cell carcinoma (סרטן ריאה מסוג התאים הקשקשיים)
- Adenocarcinoma (סרטן ריאה מסוג אדנוקרצינומה)
- Large cell (Anaplastic) carcinoma (סרטן ריאה מסוג התאים הגדולים)
- Small Cell Lung Cancer (SCLC) (סרטן ריאה של התאים הקטנים) - מהווה כ-15 אחוזים מכלל מקרי סרטן ריאה
אבחנה
התסמינים המביאים את החולה להיבדק הם בדרך כלל: שיעול, קוצר נשימה, כיח דמי (Hemoptysis), כאבים בחזה ודלקות ריאה נשנות. לעיתים הגידול מתגלה במקרה בצילום חזה שמבוצע מסיבה אחרת.
אבחון סרטן ריאה כולל: בדיקה גופנית, ספירת דם מלאה וכימיה, צילום חזה, CT (Computed Tomography) חזה, ברונכוסקופיה (Bronchoscopy) או ניקור מחטי (Needle biopsy) לאישור האבחנה הפתולוגית (Pathology).
בדיקות נוספות להערכת מידת התפשטות המחלה: PET-CT, CT (Positron-Emission Tomography) מוח במידת הצורך.
שלבי המחלה (Staging)
- נקבע לפי TNM (Tumor, Nodes, Metastasis)
T - גודל הגידול
- T1 - גידול מתחת ל-3 סנטימטרים
- T2 - גידול מעל ל-3 סנטימטרים
- T3 - גידול חודר לדופן החזה או לפלאורת המיצר (Mediastinal pleura)
- T4 - גידול חודר ללב, כלי דם גדולים, וושט, תפליט פלאורלי (Pleural effusion)
N - מעורבות בלוטות
- N1 - מעורבות בלוטות בשער הריאה או תוך ריאתיות (Eneropulmonary)
- N2 - בלוטות במיצר באותו צד של הגידול
- N3 - בלוטות במיצר בצד הנגדי של הגידול או בלוטות על בריחיות
M - גרורות מרוחקות
- M0 - ללא גרורות מרוחקות
- M1 - ישנן גרורות מרוחקות, האתרים השכיחים הם: בלוטת יותרת הכיליה (Adrenal), כבד, עצמות, ריאה שנייה או פיזור ריאתי, מוח
- Stage I
T1 N0 M0
T2 N0 M0 - Stage II IIA
T1 N1 M0 - Stage II IIB
T2 N1 M0
T3 N0 M0 - Stage IIIA
T1 N2 M0
T2 N2 M0
T3 N1 M0
T3 N2 M0 - Stage IIIB
Any T N3 M0
T4 Any N M0 - Stage IV
Any T Any N M1
פרוגנוזה
הפרוגנוזה נקבעת על פי מידת התפשטות המחלה. בדרך כלל התסמינים מופיעים רק בשלב מתקדם של המחלה, כך שמרבית המקרים מתגלים כשהמחלה מפושטת וסיכויי הריפוי נמוכים.
גילוי מוקדם
באוקטובר 2006 התפרסמו לראשונה תוצאות מחקר רב היקף (מעל 30,000 אנשים) שבדק על יעילות CT במינון קרינה נמוך, כבדיקת סקר לגילוי מוקדם של סרטן ריאה באוכלוסייה בסיכון גבוה. תוצאות המחקר מצביעות על יעילות השיטה: כ-85 אחוזים ממקרי סרטן הריאה במחקר התגלו בשלב I והחיות ל-10 שנים הייתה 92 אחוזים. אולם בשלב זה יש צורך בנתונים נוספים על מנת להמליץ על CT במינון קרינה נמוך כבדיקה שגרתית לגילוי מוקדם.
מתוך 100 חולים חדשים 70 יהיו בלתי מנותחים עקב מחלה מפושטת, ו-30 יהיו מנותחים, כאשר: 20 יהיו בשלב מוקדם של המחלה, 10 יהיו בשלב מחלה מתקדמת בבית החזה.
טיפול
Staging
ההחלטה על טיפול בסרטן הריאה נעשית בעיקר לפי דרגת התפשטות המחלה (Staging).
Stage I + Stage II
ניתוח רדיקלי (Radical) באם מצבו של החולה מאפשר זאת (מבחינת תפקודי ריאה ולב)
ניתוחים – כריתת אונה (Lobectomy), כריתת ריאה מלאה
פחות מכריתת אונה - ניתוח לא מספיק השוני ביניהם הוא אחוז תמותה בניתוח ותחלואה - שניהם גבוהים יותר בכריתת ריאה מלאה
- טיפול משלים
- קרינה - אין הצדקה לטיפול קרינתי משלים באופן שגרתי אחרי כריתה מלאה. מטה אנליזה (Metaanalysis) של Port שהתפרסמה ב-1998 הוכיחה שתוספת קרינה לאחר כריתה מלאה לא משפרת את שיעורי ההישרדות לחמש שנים. יש לתת קרינה אם הכריתה הכירורגית (Surgical) לא הייתה שלמה ו/או אם החתך הניתוחי עובר דרך הגידול
- טיפול כימי משלים - נעשו שש עבודות אקראיות שבדקו יעילות של טיפול כימותרפי (Chemotherapy) משלים לאחר ניתוח כריתה מלא. כל העבודות למעט אחת הראו יתרון ברור בהיוותרות בחיים בזרוע שטופלה בכימותרפיה. לכן טיפול כימי משלים מהווה חלק מהטיפול השגרתי לאחר ניתוח כריתה מלא והשילוב המקובל הוא Cisplatin ו-Navelbine
Stage III
- Stage III A - קבוצת חולים בעלי פוטנציאל ניתוחי - בשלב זה של המחלה יש מעורבות של בלוטות במיצר. לאבחנה דרושה הוכחה פתולוגית מ-Mediastinoscopy (PET בעצמו לא מספק מכיוון שיש לפחות 8 אחוזים False Positive).
לקבוצת חולים זו נהוג להציע טיפול משולב הכולל לפחות שני סוגי טיפולים: כימותרפיה Neo adjuvant וניתוח ו/או כימותרפיה, קרינה וניתוח
- Stage IIIB - שלב מחלה מתקדמת מקומית – בדרך כלל מחלה לא נתיחה. הטיפול היעיל ביותר הוא שילוב של כימותרפיה וקרינה. ההמלצה: טיפול כימי בהתחלה ואחר כך שילוב בו-זמני של כימותרפיה וקרינה (בדרך כלל שילוב של תרופות Radio sensitizing)
Stage IV
מחלה גרורתית.
נכון לשנת 2011, בשלב זה ניתן בדרך כלל טיפול סיסטמי פליאטיבי (Systemic palliative) אשר מטרתו שיפור חיי החולה על ידי הפחתה או העלמה של התסמינים (שיעול, חולשה, קוצר נשימה) והארכת חיים עם טיפול כימותרפי משולב ההישרדות החציונית היא 8–10 חודשים וכ-40 אחוזים יחיו מעל שנה. לעומת זה, בטיפול תומך ההישרדות החציונית היא 4–5 חודשים בלבד ורק 10 אחוזים ייוותרו בחיים כעבור שנה.
סוג הסרטן
בנוסף לדרגת התפשטות המחלה, מאפיין חשוב נוסף לטיפול הוא סוג הסרטן:
NSCLC
הטיפול הראשוני נקבע על ידי שלב המחלה.
לחולים שאובחנו בשלב מוקדם של המחלה, טיפול ניתוחי מקנה אפשרות ריפוי, כאשר טיפול משולב כימותרפי-קרינתי מועדף בחולים עם מחלה מפושטת יותר; תוך-חזית (Intrathoracic). לעומתם, חולים עם מחלה מתקדמת מטופלים פליאטיבית בטיפול מערכתי (Systemic) ו/או טיפול מקומי פליאטיבי[3].
SCLC
כימותרפיה מערכתית היא מרכיב חשוב בטיפול, מאחר שכבר בעת האבחנה, ברוב החולים, ה-SCLC יהיה כבר מפושט. בחולים עם מחלה מוגבלת, הטיפול יהיה משולב; קרינתי עם כימותרפיה. תכופות, יעשה טיפול מניעתי קרינתי לגולגולת, למניעת גרורות מוחיות והארכת תוחלת החיים. טיפול מניעתי קרינתי גולגולתי ושל בית החזה יכול להיות מועיל בחולים עם תגובה חלקית או מלאה לטיפול כימותרפי ראשוני[1].
טיפול תרופתי
כימותרפיה
יש מספר תרופות שהוכיחו יעילות בטיפול בסרטן ריאה:
- תרופות הדור הישן: Carboplatin, Cisplatin
- תרופות הדור החדש: Gemcitabine, Navelbine, Taxol (Paclitaxel), Taxotere, Alimta
בדרך כלל נהוג לטפל בחולים במצב תפקודי טוב 0 או 1 Performance status) PS) על ידי שילוב של שתי תרופות (אחת מהדור החדש ואחת מהדור הישן) במשך 4–6 מחזורי טיפול - לדוגמה שילוב של Taxotere עם Cisplatin או Navelbine עם Carboplatin וכדומה. מספר עבודות מבוקרות הראו שהשילובים השונים נבדלים בעיקר ברעילות ולא ביעילות. במשך שנים נעשו ניסיונות לשפר את יעילות הטיפול על ידי הוספת תרופה כימותרפית שלישית אבל, למרות שיפור בשיעורי התגובה, השילובים המשולשים לא השיגו שיפור בהארכת חיים והיו כרוכים ברעילות מרובה. לחולים במצב תפקודי ירוד, 2 PS ומעלה, נהוג לתת טיפול בתרופה בודדת מאחר שהטיפול המשולב כרוך ברעילות לא מבוטלת, ומטרת הטיפול היא להאריך חיים תוך שמירה במידת האפשר על איכות החיים.
טיפולים מכווני מטרה בסרטן ריאה
Tarceva
Tarceva היא טיפול ממוקד כנגד הקולטן לגורם הגדילה EGFR אשר מצוי על קרום התא ומשחק תפקיד מרכזי בהתפתחות הגידול הסרטני. Tarceva מעכבת את פעולתו של אנזים מסוג Tyrosine Kinase שאחראי על הפעלת שרשרת התגובות שמתרחשת בעקבות הפעלת הקולטן. חסימת הפעלת הקולטן באמצעות עיכוב האנזים גורמת עיכוב בתהליכי הגדילה והחלוקה של התא הסרטני.
Tarceva היא התרופה היחידה הפועלת כנגד המסלול של HER1/EGFR שהביאה להארכת חיים בחולי סרטן ריאה. יעילותה של Tarceva הודגמה במחקר פאזה שלישית שכלל 731 חולים שנכשלו על טיפול כימי קודם, והשווה טיפול ב-Tarceva לטיפול תומך. המחקר הראה שמתן Tarceva שיפר משמעותית את כל מדדי המחלה: שיעור התגובה, עיכוב הזמן עד התקדמות המחלה, שיפור בתסמיני המחלה והארכת חיים: בהשפעת Tarceva התארכה ההישרדות החציונית ב-43 אחוזים.
על בסיס מחקר זה, נרשמה Tarceva ברחבי העולם כולל בישראל לטיפול בסרטן ריאה גרורתי מסוג NSCLC לאחר כישלון של טיפול כימי אחד לפחות (קו שני ומעלה). בנוסף, Tarceva היא התרופה היחידה שהוכיחה יעילות בקו טיפולי שלישי במחקר פאזה III מבוקר.
ל-Tarceva פרופיל בטיחותי גבוה, השונה מזה של כימותרפיה תופעות הלוואי העיקריות של Tarceva הן פריחה ושלשול המופיעות בדרך כלל בדרגה קלה וניתנות לשליטה. יתרון נוסף ב-Tarceva הוא העובדה שהיא ניתנת כטבלייה אחת ליום ולא כעירוי תוך ורידי.
ניתן לטפל ב-Tarceva גם בחולים במצב תפקודי ירוד שאינם יכולים לקבל כימותרפיה ולא קיבלו טיפולים כלשהם למחלתם. משרד הבריאות הישראלי אישר התוויה נוספת לטרסבה - כקו טיפולי ראשון בסרטן לבלב גרורתי (בשילוב עם Gemcitabine).
Avastin
Avastin היא תרופה ביולוגית הפועלת כנגד תהליך יצירת כלי הדם של הגידול (Angiogenesis). Avastin היא נוגדן ספציפי לגורם הגדילה של כלי דם (Vascular Endothelial Growth Factor ,VEGF). על ידי קישור ל-VEGF היא מונעת את יצירת כלי הדם לגידול וכתוצאה מעכבת את צמיחת הגידול והתפשטותו.
Avastin רשומה בישראל לטיפול קו ראשון בשילוב עם כימותרפיה בסרטן מעי גס גרורתי.
ביוני 2005 פורסמו לראשונה תוצאות מחקר פאזה שלישית רב-מרכזי, מבוקר E4599 שבדק האם תוספת Avastin למשלב כימותרפי של Carboplatin ו-Taxol משפרת את יעילות הטיפול. במחקר השתתפו 878 חולי סרטן ריאה מפושט מסוג תאים קטנים לא קשקשיים (Non Squamous NSCLC) שלא קיבלו טיפול קודם למחלתם. המחקר הראה כי בחולים שטופלו ב-Avastin בשילוב עם כימותרפיה הייתה הפחתה של 20 אחוזים בסיכון לתמותה במשך כל זמן המחקר, בהשוואה לחולים שקיבלו כימותרפיה בלבד, וההישרדות החציונית של החולים שטופלו ב-Avastin התארכה (12.3 לעומת 10.3 חודשים). על בסיס תוצאות מחקר זה Avastin נרשמה על ידי ה-FDA (Food and Drug Administration) באוקטובר 2006 לטיפול בסרטן ריאה גרורתי מסוג תאים קטנים לא קשקשיים בשילוב עם כימותרפיה (Carboplatin/Taxol) והיא הוגשה לרישום גם באירופה.
נכון לשנת 2011 ישנן תרופות ביולוגיות נוספות מקבוצת מעכבי VEGF ומעכבי VEGF ו- EGFR הנמצאות עדיין בשלבי מחקר קליני מתקדם.
מצבים מיוחדים
חולים מבוגרים (מעל גיל 70)
שתי עבודות אירופאיות שנעשו עם Navelbine הוכיחו כי מתן טיפול כימי סל תרופה בודדת Navelbine טוב יותר בשיעורי התגובה, באיכות החיים ואף באורך החיים לעומת טיפול תומך. כמו כן, ניתוח של עבודות שבדקו יעילות שילובים בקו ראשון הראה שלא היה הבדל ביעילות הטיפול בין חולים צעירים למבוגרים (מעל 70).
עבודה שהתפרסמה בשנת 2010 הראתה כי Taxotere הדגים שיעורי תגובה ואורך חיים טובים יותר בהשוואה ל-Navelbine. היום ניתן להציע לחולים מעל גיל 70 טיפול ב-Navelbine או ב-Taxotere. הגישה המקובלת היום היא להתייחס לגיל הביולוגי ולא הכרונולוגי ולהציע גם לחולים מבוגרים טיפול כימותרפי, בתרופה בודדת או בשילוב, אם מצבם התפקודי מאפשר זאת. הטיפולים הכימותרפיים פועלים באופן לא ספציפי ופוגעים גם בתאים בריאים ולכן מלווים בתופעות לוואי רבות. בדרך כלל Dose limiting toxicity היא דיכוי מח עצם. בשילובים של שתי תרופות, תופעות הלוואי השכיחות הנוספות הן נשירת שיער, בחילות, חולשה, סחרחורת, הפרעה במערכת העיכול ורעילות של מערכת העצבים ההיקפית. לכן יש להעריך בכל פגישה עם החולה, בנוסף ליעילות, את רעילות הטיפול ולשקול המשך טיפול בהתאם. בחולים במצב כללי ותפקודי טוב אשר נכשלו על קו טיפולי כימי ראשון ניתן להציע קו טיפולי שני. בעבר הייתה רק תרופה אחת שיעילותה הוכחה בקו טיפולי שני - Taxotere. נוספו אפשרויות טיפוליות נוספות לקו שני: Alimta שהיא כימותרפיה עם יעילות דומה ל-Taxotere אבל עם פרופיל בטיחותי טוב יותר, ו-Tarceva תרופה מכוונת מטרה (Targeted therapy) כנגד המסלול של EGFR (Epidermal Growth Factor Receptor) הטיפול בקו שני נותן כ-9 אחוזים שיעור תגובה עם הישרדות חציונית של כ-8 חודשים.
גרורות למוח
בהתפתחות גרורות מוחיות בשלב מחלה מתקדם, האופציה הטיפולית היא קרינה לכל המוח (WBRT, Whole Brain RadioTherapy). במקרה של גרורה בודדת: ניתוח ו/או Radiosurgery ואחר כך לשקול קרינה לכל המוח. יש לזכור כי הקרינה מורידה שכיחות של גרורות מוחיות, אך אינה משפיעה על אורך החיים.
ראו גם
למידע נוסף ועדכני ראו:
ביבליוגרפיה


 כניסה
כניסה  עקבו אחרינו בפייסבוק
עקבו אחרינו בפייסבוק