דלקת כבד נגיפית מסוג C - טיפול - 2017 - Hepatitis C - treatment
ערך זה נמצא בבדיקה ועריכה על ידי מערכת ויקירפואה, וייתכן כי הוא לא ערוך ומוגה.
| דלקת כבד נגיפית מסוג C - טיפול - 2017 | ||
|---|---|---|
| 2017 - Hepatitis C - treatment | ||
| ||
וירוס ההפטיטיס C
| ||
| שמות נוספים | פשטות הטיפול בהפטיטיס HCV) C) -האם יש בידינו את ה- "Perfectovir"? | |
| יוצר הערך | פרופסור אלי צוקרמן | |
לערכים נוספים הקשורים לנושא זה, ראו את דפי הפירושים: – הפטיטיס#C, סל תרופות 2018
נגיף דלקת הכבד מסוג C (HCV) הוא נגיף הפטוטרופי הגורם לדלקת כבד כרונית העשויה להימשך עשרות שנים ולגרום לפיברוזיס משמעותית ולשחמת הכבד על כל סיבוכיה (מיימת, אנצפלופתיה, דימום מדליות בוושט או בקיבה, התפתחות של סרטן כבד ראשוני בכ-20% מהחולים, אי ספיקת כבד ומוות).
מספר החולים בהפטיטיס C בעולם מוערך בכ-200-180 מיליון ובישראל בכ-2% (כלומר כ 150,000-120,000 נשאים). מסתבר שיותר מ-60% מחולי HCV בישראל הם עולים מברית המועצות לשעבר והגנוטיפ השכיח הוא גנוטיפ 1 (67%) (גנוטיפ 3 - 22%, גנוטיפ 2 - 7%, גנוטיפ 4 - 3%). עד 2011, הטיפול שהיה מבוסס על אינטרפרון אלפא (בזריקה תת-עורית) וריבוירין במשך 48 שבועות בגנוטיפ 1 (24 שבועות בגנוטיפ 2 ו-3), היה כרוך בתופעות לוואי רבות עם 50%-45% הצלחה בלבד (SVR - sustained virological response) שמשמעותה סילוק הנגיף, שיפור היסטולוגי במרבית המקרים והפחתת הסיכון להופעת HCC (hepatocellular carcinoma).
ב-2012 אושר השילוב המשולש של אינטרפרון (IFN), ריבוירין (RBV) ומעכבי הפרוטיאז מהדור הראשון (Boceprevir או Telaprevir) שנכלל בסל הבריאות בישראל ב-2012 לגנוטיפ 1 בלבד ולדרגת פיברוזיס בינונית ומעלה (F2-4). טיפול זה היה מורכב ומסורבל, היה כרוך בתופעות לוואי קשות עוד יותר מהטיפול ב- IFN /RBV ושיעור ה-SVR היה מאכזב בטיפול ב-real life לעומת המחקרים הקליניים: 75%-52% בלבד. טיפול זה לא נתן מענה לאוכלוסיות רבות של חולים: חולים עם שחמת מתקדמת (decompensated cirrhosis), גנוטיפים אחרים מגנוטיפ 1, חולים במחלות נלוות מורכבות, מחלות אוטואימוניות, אי ספיקה כלייתית, חולים מבוגרים יחסית ועוד.
פריצת הדרך הגדולה בטיפול בהפטיטיס C
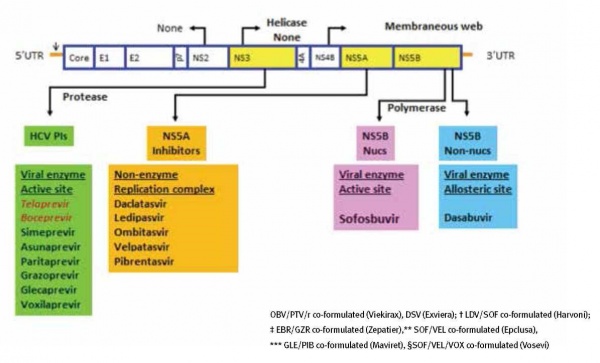
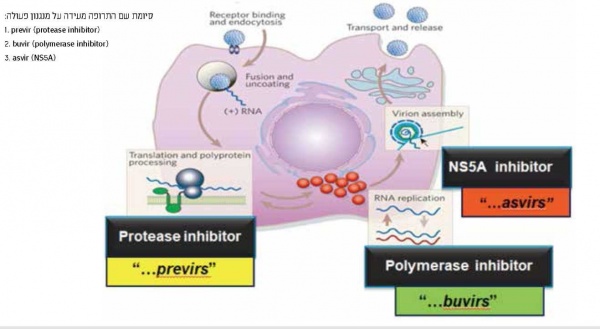
פריצת הדרך הגדולה בטיפול בהפטיטיס C, ייתכן שבין המשמעותיות ביותר ברפואה המודרנית ב-50 השנים האחרונות, חלה ב-2014 עת הופיע הטיפול הפומי ("נטול" IFN או interferon-free) המבוסס על שילוב של שתי תרופות או יותר ונמצא יעיל בגנוטיפים שונים. שינוי הגישה של טיפול שהיה למעשה immune-modulator, לטיפול הפועל ישירות כנגד מרכיבים שונים של מעגל החיים של הנגיף (direct antiviral agents או DAAs), הוא שהביא למהפכה בטיפול. התרופות השונות כוללות מעכבי פרוטיאז (protease inhibitor NS3/4A PI), מעכבי פולימראז מסוג nucleotide NS5B NUC-I) polymerase inhibitor), מעכבי פולימראז מסוג non-nucleotide NS5B polymerase inhibitor (non-NOC או NNI) ומעכבי NS5A-1) NS5A) הנחשב למרכיב חשוב ברפליקציה, בבנייה (assembly) ובשחרור של הנגיף (תמונה מסי 1 ו-2).
הטיפול ניתן רק בשילוב של שתי תרופות או יותר הפועלות במנגנונים שונים עם או בלי ריבוירין ולא כמונותרפיה. מטרת הטיפול הייתה להשיג יעילות בשיעור 100%, שהטיפול יהיה יעיל כנגד כל סוגי הגנוטיפים (pan-genotypic), שיתאים לכל אוכלוסיות החולים, שיהיה ללא תופעות לוואי משמעותיות ונסבל, שלא תתפתח עמידות (high barrier to resistance), שתהיה תגובה בין-תרופתית מינימלית (DDI או drug-drug interaction), משך הטיפול יהיה קצר ככל האפשר ובעיקר פשוט, על מנת להגביר את ההיענות ושיעור השימוש בתרופה (טבליה אחת המכילה תשלובת של שתיים או שלוש תרופות), להימנע ככל האפשר משימוש RBV-n בגלל תופעות הלוואי (אנמיה, תפרחת ושיעול) ומספר הטבליות היומי[1], [2], [3] ושמחיר הטיפול יהיה נמוך ככל האפשר.
האם ב-2017 נמצאת בידינו תרופת הפלא, אותה טבליה הניתנת לכל החולים, לכל סוגי הגנוטיפים, למשך 4 או 6 שבועות עם שיעור ריפוי של 100%: ה-"Perfectovir"? משנת 2014 אכן חלה התקדמות רבה בהשגת מטרות אלו עם הופעת הדור השני של התרופות אך עדיין קיימים יעדים שלא הושגו (unmet needs).
המצב בישראל
המצב בישראל ב-2017 לגבי נגישות ואפשרויות הטיפול טוב יחסית אך לא מושלם וזאת בעיקר בגלל מגבלות התקציב של סל הבריאות.
בשנים 2015–2017 הוכללו בסל התרופות הישראלי כל התרופות והתשלובות שאושרו על ידי ה-FDA וה-EMEA: Paritaprevir/ritonavir/ombitasvir ,(Viekirax) + dasabuvir (Exviera) Sofosbuvir (sovaldi), Daclatasvir Daklinsa), Sofosbuvir/Ledipasvir) Harvoni), (Grazoprevir/Elbasvir (Zepatier) ו- (Epclusa) Sofosbuvir/Velpatasvir.
אכן האפשרויות הטיפוליות הורחבו באופן משמעותי מ-2015 ועד 2017 והן כוללות טיפול בכל הגנוטיפים (גנוטיפ 1–4) בדרגת פיברוזיס מתקדמת (F3) או שחמת (F4) ובגנוטיפים 1 ו-4 גם לדרגת פיברוזיס בינונית (F2). הטיפול כולל גם חולים עם ביטויים חוץ-כבדיים של הזיהום ב-HCV (וסקוליטיס על רקע קריוגלובולינמיה, לימפומה של תאי B) וחולים לאחר השתלת כבד. חולים בדרגת פיברוזיס קלה (F0-1) עדיין לא נכללים כזכאים לקבלת הטיפול במסגרת הסל וחולים אלה מהווים כ-50% מהחולים המחכים לטיפול. ה-"Perfectovir" עדיין לא נמצאת ברשימת התשלובות הנ"ל, אולם בהחלט אנו מתקרבים לכך.
ברוב התשלובות היעילות מגיעה ל-100%-95%, משך הטיפול 12 שבועות, אין תופעות לוואי משמעותיות ורמת ה-DDI סבירה וניתנת לטיפול. תוצאות הטיפול ב-"Real Life" בישראל, כמו במדינות אחרות במחקרים רב מרכזיים שהוצגו, דומות לאלו שדווחו במחקרים קליניים הן לגבי היעילות והן לגבי הבטיחות[4], [5].
תשלובות שונות לאוכלוסיות חולים שונות
אולם, לא כל אוכלוסיות החולים זהות ויש צורך בניצול היתרונות ולהימנע מחסרונות התשלובות השונות באוכלוסיות השונות. לכל תשלובת יש "ייחוד" מסוים לגבי יעילות בסוג אוכלוסיית חולים מסוימת, לגבי משך הטיפול, הצורך ב-RBV, DDI ושיעור הופעת עמידות ולכן רצוי לשמור את כל האופציות הטיפוליות "קרוב לחזה". לדוגמה:
- קיים הבדל בין תת-זני ה- 1a HCV ו-1b (1b קל יותר לטיפול) מבחינת היעילות והופעת עמידות המחייב טיפול ארוך יותר ושילוב של RBV בחלק מהתשלובות.
- קיימת הוראת נגד לשימוש בתשלובות המכילות מעכבי פרוטיאזות בחולים עם שחמת לא מפוצה (decompensated cirrhosis).
- רק בתשלובות מסוימות ניתן לקצר את הטיפול ל-8 שבועות (בחולים שאינם צירוטיים ושלא קיבלו טיפול אנטי ויראלי קודם).
- בחולים עם אי ספיקה כלייתית מתקדמת ( mL/min/1.73m2 eGFR30) בטוח יותר לטפל רק בתשלובות מסוימות ולא באלו המכילות Sofosbuvir.
- בתשלובות מסוימות קיימת DDI רבה יותר מאשר אחרות בעיקר עם תרופות מסוג anti retroviral treatment) ART) לנשאי HIV ומעכבי calcineurin במושתלי כבד. קבוצות החולים שנשארו "אגוז קשה לפיצוח" הן של חולים עם decompensated cirrhosis, בעיקר אלה בדרגה מתקדמת Child-Pugh Class C, חולים שחמתיים שנכשלו בטיפול ב-IFN/RBV וחולים שנכשלו בטיפול ב-DAAs, בעיקר בטיפול שהכיל מעכבי NS5A. העמידות למרכיב זה בתשלובת היא בעייתית מאחר שה-Resistance Associated Substitutions (RASs) האחראים להיעדר תגובה לטיפול (בגלל relapse או breakthrough) שורדים שנים רבות ויהיה צורך בטיפול משולב (לעיתים off-label), ארוך יותר (24 שבועות) ומכיל ריבוירין על מנת להתגבר על העמידות. הטיפול הקרוב ביותר ל-"Perfectovir" יהיה הטיפול היעיל ביותר אבל גם הפשוט ביותר. בהנחה שיעילות ששיעורה נע בין 95% ל-100% הושגה, "הפשטת" הטיפול פירושה שהטיפול יהיה פשוט יותר הן למטפל: זמן טיפול קבוע בכל החולים ללא קשר לגנוטיפ, לעומס הנגיפי, לאוכלוסייה המטופלת, למחלות נלוות (co-morbidities) ול-DDI, והן למטופל: טבליה אחת ביום, זמן טיפול קצר ככל האפשר ללא תופעות לוואי. המושג "טיפול פשוט" מקביל ל-"one size fits all". האם אנו נמצאים כבר שם? אושרו על ידי ה- FDA וה--EMEA שתי תשלובות טיפוליות המשדרגות באופן משמעותי את היכולת הטיפולית בקבוצות חולים בעייתיות בהיותן pan-genotypic ובעלות פוטנציאל לפשט את הטיפול ולקצרו. שתי הטכנולוגיות החדשות הוגשו להכללה בסל התרופות של 2018.
טכנולוגיות חדשות
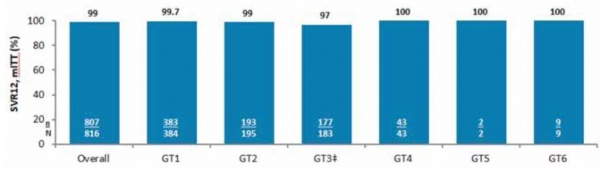
(Maviret) Glecaprevir/Pibrentasvir - התרופה הראשונה היא שילוב של שתי תרופות כלל-גנוטיפיות מהדור השני NS5A inhibitor Pibrentasvir ו-NS3/4A protease inhibitor Glecaprevir. התרופה המשולבת נקראת Maviret. התרופה ניתנת ב-3 טבליות פעם ביום ועוברת מטבוליזם בכבד. באנליזה של נתונים מקובצים ממחקרים בפזה 2 ו-3, ב-816 חולים מכל הגנוטיפים[4], [5], [6], [1], [2], [3] ללא שחמת נאיביים לטיפול או שנכשלו בטיפול קודם ב-IFN/RBV או Sofosbuvir שקיבלו 8 שבועות טיפול בלבד, שיעור השגת SVR היה מושלם 100%-99% (בגנוטיפ 3 כולם היו נאיביים, שיעור 97% SVR (177/183) (תמונה מסי 3)[6], [1]. בניתוח התוצאות לא היה הבדל בין הגזעים, ה-BMI, עומס נגיפי, גיל > 65 שנים או co-infection HIV/HCV.
High Rates of Efficacy with 8 Weeks of G/P in Treatment-naive and Experianced Adults with Chronic GT1-6 HCV Infection without Cirrhosis: An Integrated Analysis
Integrated efficacy analysis 'of 8 or 12 weeks' G/P treatment in non-cirrhotic patients with GT1-6 infection across seven phase 2 or 3 clinical trials
פרופיל הבטיחות היה מצוין עם שיעור נמוך של תופעות לוואי משמעותיות שנסבלו היטב (כאבי ראש, עייפות ושיעור נמוך של שלשול).
במחקר EXPIDITION-I טופלו בתרופה במשך 12 שבועות 146 חולים עם שחמת מפוצה (compensated) נאיביים או מנוסים בטיפול קודם בכל הגנוטיפים מלבד גנוטיפ 3. שיעור השגת SVR גם בחולים אלה היה מושלם (100%-99%) ורק בחולה אחד בלבד (גנוטיפ 1a) נצפתה הישנות. גם בקבוצת החולים השחמתיים פרופיל הבטיחות היה מצוין ללא תופעות לוואי שונות מהחולים ללא שחמת[2]. מאחר שגנוטיפ 3 הוא גנוטיפ בעייתי, ובעיקר בחולים השחמתיים, הופרדו חולים אלה ו"זכו" להתייחסות מיוחדת.
במחקר 3-ENDURANCE נמצא שטיפול של 8 שבועות בחולים עם גנוטיפ 3 נאיביים לטיפול קודם ושאינם שחמתיים הביא להשגת SVR ב-95% מהחולים (149/153) בדומה לאלה שטופלו במשך 12 שבועות או ב-Daclatasvir + Sofosbuvir ל-12 שבועות[3].
במחקר 3 SURVEYOR II Part נבדק טיפול ב-Maviret בחולים שחמתיים ו/או שקיבלו טיפול בעבר ב-IFN/RBV או Sofosbuvir ל-12 או 16 שבועות. בחולי גנוטיפ 3 צירוטיים ומנוסים בטיפול, שיעור ה-SVR היה גבוה, 95% אבל מספר החולים היה יחסית נמוך בזרוע זו (45/47) וקבוצה זו טופלה למשך 16 שבועות[7].
המחקר הנוסף שבחן הטיפול ב-Marivet בחולים עם אי ספיקה כלייתית מתקדמת (82% ,4-5 CKD stage מטופלי דיאליזה) היה ה-4-EXPIDITION שהראה SVR בשיעור גבוה 100% (102/102 חולים) עם פרופיל בטיחות מצוין[8] ומאיסוף כלל הנתונים ממחקרי פאזה 2 ו-3 של יותר מ-100 חולים עם אי ספיקה כלייתית כרונית (3–5 CKD). התוצאות דומות: 100%-95% בכל הגנוטיפים, בין אם היו שחמתיים או לא.
קבוצה בעייתית נוספת היא של חולים שנכשלו בטיפול ב-DAAs בעבר בעיקר בתשלובות שהכילו NS5A-inhibitors. במחקר Part 2 ,MAGELLAN נמצא שבחולים שבהם נמצאו RASs ב-NS5A (בעיקר (Y93H/N ו/ או ב-NS3/4A (PI) שיעור ה-SVR ירד פלאים ל-79% עד 88% בין אם הטיפול נמשך 12 או 16 שבועות[9]. שיעורי SVR ברמה כזו בהחלט אינם מספקים בקבוצת חולים זו, וזו אחת החולשות של התשלובת הנקראת Maviret.
לאור הנ"ל, ה- label האירופאי אינו ממליץ כלל על טיפול חוזר בתרופה בקבוצת נכשלי DAAs ואילו האירופאי מתווה הנחיה מסורבלת שאינה פשוטה כלל ועיקר. ביתר המקרים, ההתוויות פשוטות: בכל החולים הנאיביים לטיפול שאינם שחמתיים הטיפול יימשך 8 שבועות בכל הגנוטיפים ובשחמתיים 12 שבועות. בחולי גנוטיפ 3 שטופלו ב-IFN/RBV ו/או Sofosbuvir, הטיפול יימשך 16 שבועות בכולם.
מכאן שהשילוב Glecaprevir/pibrentasvir (Maviret) הוא כמעט ^"Perfectovir", למעט בחולי גנוטיפ 3 מנוסי Sofosbuvin IFN/RBV ולצורך טיפול חוזר בנכשלי DAAs.
Sofosbuvir/Velpatasvir/Voxilaprevir (Vosevi) - תרופה זו מורכבת מ-Non-NUC ,(SOF) NS5B polymerase inhibitor מ-NS5A (VEL) inhibitor, מעכב כלל גנוטיפי מהדור השני ומ-PI כלל גנוטיפי מהדור השני. תרופה זו היא למעשה תוספת של PI לתרופה המוכרת SOF/VEL) Epclusa). כל שלושת המעכבים נמצאים בטבליה אחת ניתנת פעם ביום.
במחקר 2 POLARIS (פאזה 3) נבדקה היעילות של הטיפול ב- 501 חולים מכל הגנוטיפים (1–6 genotype) כולל כ-20% שחמתיים למשך 8 שבועות כנגד Epclusa) SOF/VEL) ל-12 שבועות. בניתוח התוצאות של 3 POLARIS (110 חולים שחמתיים עם גנוטיפ 3) ו-POLARIS2, 611 חולים מכל הגנוטיפים, חלקם שחמתיים אולם נאיבים לטיפול ב-DAAs שטופלו בטבליה אחת למשך 8 שבועות, התוצאות היו מצוינות: SVR שהושג היה 94% (גנוטיפ 4) ו-98%-97% בגנוטיפ 1b, 2 ו-3. בגנוטיפ 1a רק 92% (אוכלוסייה אמריקאית, בהם RAS Q80K נפוץ ומקטין משמעותית ה-SVR). גם כאן פרופיל הבטיחות היה מצוין ולא נרשמו תופעות לוואי יוצאות דופן מהמוכרת בשימוש ב-DAAs [10] (תמונה 4).
לגבי גנוטיפ 3 הבעייתי, במחקר POLARIS 3 נבדק הטיפול ב-SOF/VEL/VOX ל-8 שבועות ב-110 חולי שחמת עם גנוטיפ 3 בלבד (35 טופלו בעבר ב-IFN/RBV) שמהווה קבוצה בעייתית ביותר. ה-SVR שהושג בקבוצה זו היה גבוה מזה שהושג אי פעם על ידי שילוב כלשהו וזאת בטבליה אחת ליום ללא ריבוירין: 96% (106/110). בניתוח התוצאות הסתבר ששיעור השגת SVR גבוה גם באלה שנכשלו בטיפול קודם ב-DAAs 97% (34/35). נראה שנמצא הפתרון לחולי גנוטיפ 3 צירוטיים ומנוסים, אם יאושר הטיפול בתשלובת זאת שהיא נוחה, פשוטה לשימוש ויעילה מאוד.
קבוצה נוספת שמהווה "אגוז קשה" היא קבוצת החולים שנכשלו בטיפול קודם ב-DAAs ובמיוחד במעכבי NS5A. מחקרי פאזה 3, 1 POLARIS ו-4 POLARIS מספקים מענה גם לקבוצה זאת. בשני המחקרים (סה"כ 745 חולים שנכשלו בטיפול ב-DAAS עם או בלי מעכבי NS5A) טופלו החולים בטבליה אחת ליום למשך 12 ימים. בקבוצה הבעייתית יותר (מנוסי NS5A-inhibitors) שיעור ה-SVR הכללי היה 99% (140/142) ובחולים שחמתיים 93% (113/121), שיעור שנחשב לגבוה מאוד בקבוצה זו. שיעור התגובה הגבוה היה זהה בכל הגנוטיפים ואפילו בגנוטיפ 3 הבעייתי 93% (52/56) - שיעורי הצלחה שלא הכרנו[11] (תמונה 4). החולשה המסוימת בתשלובת זו היא SVR נמוך יחסית בחולי גנוטיפ 1a, אבל כשנבדקו חולים ממדינות אירופה, שיעור ה-SVR עלה. חולי גנוטיפ 1a בישראל מהווים רק 20% בלבד מכלל חולי גנוטיפ 1 ונראה שבעיה זו זניחה.
לאור התוצאות המרשימות, labels של התרופה כפי שנרשם באירופה: vesovi בטבליה אחת ליום תינתן לכל החולים הנאיביים לטיפול ב-DAAs שאינם שחמתיים למשך 8 שבועות ואילו בשחמתיים ו/או באלה שנכשלו בעבר בטיפול ב-DAAs (בין אם שחמתיים אם לאו) הטיפול יימשך 12 שבועות. בארצות הברית, הוגשה התרופה לרישום רק לנכשלי DAAs. לא ניתן להשתמש באף אחת מן התרופות חדשות בחולים עם שחמת שאינה מפוצה (decompensated) בגלל המרכיב של מעכב הפרוטיאז בשתיהן.
סיכום
בפתח עומדות שתי טכנולוגיות שמקרבות אותנו ל-"Perfectovir" ומשדרגות את היעילות ופשטות הטיפול שהן מפתח להיענות גבוהה. רוב החולים, שאינם שחמתיים (F0-2) ונאיביים לטיפול, חולים שמהווים את מרבית אוכלוסיית הממתינים והחדשים, יוכלו ליהנות מ-8 שבועות טיפול בלבד בכל הגנוטיפים וללא קשר לעומס ויראלי. גם הקבוצות הבעייתיות (גנוטיפ 3, צירוטיים מנוסים ואלה שנכשלו בטיפול קודם) זוכות למענה של טיפול בן 12 שבועות.
החולים שהם HIV/HCV co-infected מטופלים כחולים עם HCV בלבד. בחולים עם שחמת שאינה מפוצה עדיין, קיימת אפשרות טיפול בתרופות שאינן מכילות PI (כמו Epclusa או Harvoni) עם או בלי ריבוירין. זמן ארוך מ-12 שבועות ו/או שימוש בריבוירין יישמר כנראה לתת קבוצות בעייתיות מאוד כמו decompensated cirrhosis וחולים עם הופעת עמידות קשה לטיפול. והחשוב מכל, למרות טכנולוגיות הטיפול שבידינו, לא נוכל למגר את המחלה בישראל אם לא נאבחן את 75% מהחולים שלא נבדקו מעולם ונמצאים בקבוצות סיכון שהוגדרו בישראל, ואם לא ננגיש את הטיפול לכל החולים, כולל במחלה קלה (F0-1) במסגרת סל הבריאות בשיעור שחייב לעלות על מספר החולים הנוספים מדי שנה.
ביבליוגרפיה
- ↑ 1.0 1.1 1.2 Glecaprevir and pibrentasvir yield high response rates in patients with HCV genotype 1-6 without cirrhosis. Kow PY, et al. J Hepatol. 2017 Aug;67(2):263-271. doi: 10.1016/j.jhep.2017.03.039. Epub 2017 Apr 13.
- ↑ 2.0 2.1 2.2 Glecaprevir plus pibrentasvir for chronic hepatitis C virus genotype 1, 2, 4, 5, or 6 infection in adults with compensated cirrhosis (EXPEDITION-1): a single-arm, open-label, multicentre phase 3 trial. Forns X, et al. Lancet Infect Dis. 2017 Aug 14. pii: S1473-3099(17)30496-6. doi: 10.1016/S1473-3099(17)30496-6. [Epub ahead of print].
- ↑ 3.0 3.1 3.2 Efficacy of G/P Compared to SOF + DCV in Treatment-Naive HCV GT3-Infected Patients without Cirrhosis: ENDURANCE-3. Foster GR, et al. J Hepatol 2017; 66(Suppl 1):S33.
- ↑ 4.0 4.1 The Real-World Israeli experience of treating chronic hepatitis C CHC), genotype 1 (GT1) patients with advanced fibrosis with paritaprevir/ritonavir/ombitasvir, dasabuvir with or without ribavirin (3D±R): a large multi-center cohort. Zuckerman E, et al. Hepatology 2016, 63 (suppl 1): 1003A.
- ↑ 5.0 5.1 The Real-World Israeli Experience of Treating Chronic Hepatitis C (CHC), Genotype 1 (GT1) and Genotype 4 (GT4) Patients with Advanced Fibrosis with Elbasvir\ Grazoprevir: A Large Multi-Center Cohort . Zuckerman E., et al. (AASLD Annual Meeting, Washington DC, October 20-24, 2017).
- ↑ 6.0 6.1 High rates of efficacy with 8 weeks of G/P in treatment-naive and experienced adults analysis, Puoti M, et al. J Hepatol 2017; 66(Suppl 1):S721.
- ↑ Efficacy of G/P for 12 or 16 Weeks in HCV GT3-Infected Patients with Prior Treatment Experience and/ or Cirrhosis: SURVEYOR-II, Part 3. Wyles DL, et al. Hepatology 2016; 64(Suppl 1):62A-63A.
- ↑ High SVR12 Rates with 12 Weeks G/P in GT1-6 Infected Patients with Severe Renal Impairment: EXPEDITION-4. Gane EJ, et al. Hepatology 2016; 64(Suppl 1):1125A (Oral presentation, LB-11
- ↑ Efficacy of G/P for 12 or 16 Weeks in Patients with HCV GT1 or 4 Infection and Prior DAA Treatment Failure: MAGELLAN-1, PART 2. Poordad F, et al. J Hepatol 2017; 66(Suppl 1):S83-84.
- ↑ Efficacy of 8 Weeks of Sofosbuvir, Velpatasvir, and Voxilaprevir in Patients With Chronic HCV Infection: 2 Phase 3 Randomized Trials.Jacobson I, et al. Gastroenterology 2017, doi: 10.1053/j. gastro.2017.03.047
- ↑ Sofosbuvir, Velpatasvir, and Voxilaprevir for Previously Treated HCV Infection. Bourliere M, et al. N Engl J Med 2017;376:2134-46
המידע שבדף זה נכתב על ידי פרופסור אלי צוקרמן, מנהל היחידה למחלות כבד, מחוז חיפה וגליל מערבי ומרכז רפואי כרמל, שירותי בריאות כללית, יו"ר החברה הישראלית לחקר הכבד


 כניסה
כניסה  עקבו אחרינו בפייסבוק
עקבו אחרינו בפייסבוק