הורמון אנטי דיורטי - Anti diuretic hormone
| מדריך בדיקות מעבדה | |
| הורמון אנטי-דיורטי | |
|---|---|
| Anti Diuretic Hormone | |
| שמות אחרים | varginine vasopressin או AVP, וכן ADH ,vasopressin ,argipressin |
| מעבדה | אנדוקרינולוגיה בדם |
| תחום | הערכת רמת ההורמון המווסת רמת מים בגוף |
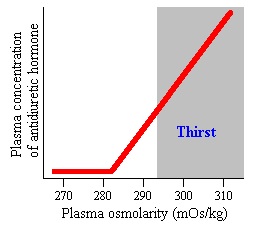
| טווח ערכים תקין | ערכי ADH בדם תלויים ברמת האוסמולליות שלו. וכך בדגימת דם עם אוסמולליות של 270-280 מיליאוסמול' לק"ג, רמת ADH נמוכה מ-1.5 פיקוגרם למ"ל; ברמת אוסמולליות של 285-290 מיליאוסמול' לק"ג, רמת ADH היא 1-5 פיקוגרם למ"ל; ברמת אוסמולליות של 295-300 מיליאוסמול' לק"ג, רמת ADH היא 4-12 פיקוגרם למ"ל. |
| יוצר הערך | פרופ' בן-עמי סלע |
מטרת הבדיקה
הבדיקה תידרש במצבי עודף נוזלים בגוף המתבטאים בבצקת, מצבי polyuria, היפונתרמיה ללא סיבה מובהקת, מצבי צמא משמעותיים שאינן ניתנים לשליטה. מתן ניכר של שתן מלווה בצמא כפייתי מחשיד לתרחיש של סוכרת תפלה (diabetes insipidus) בו מדידת ADH חיונית, לבדוק חסר אפשרי ב-ADH. בדיקת ADH תידרש בתרחיש כרונית של hypovolemia, או בחשש ל-SIADH או תסמונת ההפרשה הלא תואמת של הורמון ADH, בה יש הפרשת יתר של ADH, תסמונת שעלולה להתבטא בכאבי ראש, בחילות והקאות, בלבול, ובמקרים חמורים אף תרדמת ופרכוסים. בדיקת ADH תידרש במקרים של אוסמולליות נמוכה עיקשת בדם. עם זאת הדרישה למדידת רמת ADH בפלזמה פחתה באופן משמעותי בעשייה הרפואית, שכן ההערכה של התרחישים שלמעלה מבוססים בדרך כלל על הרקע הקליני ועל מבדקי מעבדה אחרים כמו אוסמולליות בדם ובשתן, כמו גם רמת אלקטרוליטים.
בסיס פיזיולוגי
מים מהווים כ-60% ממסת הגוף, אך למרות שינויים ניכרים בכמות המים שהגוף קולט מדי יום, רמת המים בגוף נותרת יציבה באופן מוקפד. הפיקוח והוויסות של רמת המים בגוף ברמת כלי הדם והכליות נעשית על ידי מספר הורמונים, ו-ADH ממלא כאן תפקיד מרכזי.
כאשר הגוף חש בירידה ברמת המים בדם (ובעליית ריכוז המלחים בו) מופרש ADH מבלוטת יותרת המוח (היפופיזה) לדם ומגיע לכליות, ובאמצעות הגברת הספיגה חוזרת של מים מהנפרון שבכליה אל הדם, מקטין ADH את כמות המים שיופרשו בשתן. ADH מבצע זאת על ידי גירוי תאים המקיפים את הצינור המאסף (Collecting duct), שבו מתבצע הסינון האחרון של השתן המופרש לפני הגעתו לשלפוחית השתן. ADH מגרה תאים אלו לייצר ולשחרר שלפוחיות המכילות חלבונים (aquaporins), ובמקרה זה-AQP-2. חלבונים אלו משמשים תעלות להולכת מים, בכך שהשלפוחיות מתמזגות עם קרום התא הפונה אל הצינור המאסף וריכוז תעלות המים שבקרום עולה משמעותית. בעקבות כך, מים יוצאים מהצינור המאסף אל תאים אלו ומשם בפעפוע אל מחזור הדם.
מבנה ADH
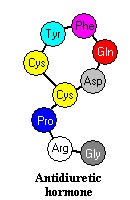
הגן המקודד ל-ADH ממוקם על כרומוזום 20, ויש לו 3 אקסונים שרק אחד מהם (אקסון A) כרוך לרצף תשע חומצות האמינו של הורמון זה: Cys-Tyr-Phe-Gln-Asn-Cys-Pro-Arg-Gly, כאשר 2 שיירי הציסטאין יוצרים קשר די-סולפידי ולולאה פנימית במבנה ADH (ראו תרשים).
בחזירים, אנו מוצאים גרסה של lysine vasopressin, בו שייר ליזין מופיע במקום ארגינין, והוא משמש לעתים בתרפיה בבני אדם.
סינתזה של ADH
ההורמון ADH מסונתז בהיפו-תאלאמוס תחת השפעה של המערכת הסימפתטית וה-locus ceruleus הממוקם ב-pons שבגזע המוח. שני סוגי תאי עצב ייעודיים מייצרים ADH:
- תאים parvo-cellular, הממוקמים בגרעין ה-para-ventricular בהיפו-תאלאמוס, כאשר תאים אלה משפיעים בעיקר על ההיפופיזה הקדמית, כאשר ADH המשתחרר שם מגרה את השחרור של ACTH.
- תאים magno-cellular, הממוקמים בגרעין ה-supra-optic בהיפו-תאלאמוס, שהאקסונים שלהם מפרישים ADH בהיפופיזה האחורית, אך גם משפיעים על ההיפופיזה הקדמית דרך המערכת הפורטלית. גופי הרינג שהם עיבוי של קצות אקסונים בחלק האחורי של ההיפופיזה, משמשים כמאגר זמני ל-ADH המגיע מההיפותלמוס דרך האקסונים, עד לשחרורו לזרם הדם. בתוך תאי העצב בהיפו-תאלאמוס ADH ארוז יחד עם חלבון נשא הקרוי neurophysin, ושני אלה משתחררים ביחד לדם עם הפרשת ADH.
סינתזת ADH מתחילה בתרגום mRNA לשלב מוקדם ולא פעיל של ההורמון הקדומני (pre-pro-hormone) המכיל 166 חומצות אמינו, בריבוזום של הגרעין הסופרה-אופטי. כאן מתרחש ביקוע הפפטיד "המסמן" כאשר הפפטיד הקדומני השלם עדיין קשור לריבוזום, ליצירת pro-hormone. לאחר מכן חלה גליקוזילציה של ב-Golgi והתכנסות לתוך גרנולות.
בקרת הפרשת ADH
הפרשת ADH מההיפופיזה הקדמית באה בתגובה לירידה בנפח הפלזמה, בתגובה להגברת האוסמולליות בפלזמה, ובתגובה ל-cholecystokinin או CCK המופרש במעי הדק: הפרשה בתגובה לנפח מופחת של פלזמה משופעלת על ידי קולטני-לחץ בורידים, בעורקים ובקארוטידים. הפרשת ADH בתגובה להגברת הלחץ האוסמוטי בפלזמה, נעשית בתיווכם של קולטנים אוסמוטיים בהיפו-תאלאמוס.
תאי העצב בגרעיני המוח הסופרה-אופטיים והפארא-ונטריקולארים המייצרים ADH, הם עצמם מהווים קולטנים אוסמוטיים (osmoreceptors), והם מקבלים איתותים מקולטנים אוסמוטיים נוספים מאזורים הסמוכים לקיר הקדמי של חדר המוח השלישי. אזורים אלה כוללים את organum vasculosum של ה-lamina terminalis, וכן מה-subfornical organ.
הקולטנים האוסמוטיים בהיפותאלאמוס חשים בשינויים בריכוז הנתרן בדם. אם ריכוז הנתרן גבוה, הקולטנים האוסמוטיים יפרישו ADH. ואילו כאשר ריכוז הנתרן בדם נמוך הם יפרישו מעט ADH אם בכלל.
האוסמו-רצפטורים מופעלים על ידי שינוי ברמת המים התוך תאית. המים חודרים לתאים ההיפו-תאלאמיים דרך תעלות מים, וחדירת המים מתבצעת על בסיס מפלי ריכוזים. במצבים של דהידרציה, יצאו מים מתוך התא המשמש כאוסמו-רצפטור אל התווך החוץ תאי, מה שיביא לצמצום נפח התא, להפעלת תעלות קטיוניות ולדה-פולריזציה בתא, שתעודד הפרשת ADH.
תרחיש של התייבשות שגורם ליציאת מים מתוך התא אל חוץ התא, מופעל בעיקר במצב של היפרנתרמיה, כאשר הקולטנים חשים בעודף של הנתרן וכתוצאה מכך מווסתים את הפרשת ADH. דהינו, הנתרן מהווה אוסמו-רגולאטור עיקרי אשר קובע את מידת ההפרשה של ADH. ווסת נוסף המשפיע על שחרור ADH הוא גלוקוז, בעיקר במצבי סוכרת לא מאוזנת: כאשר רמת גלוקוז עולה בדם, משתחרר אינסולין המחדיר הגלוקוז לתוך תאים, אך במצבי של סוכרת לא מאוזנת, המאופיינת ברמות גבוהות של סוכר כתוצאה ממחסור באינסולין או בעמידות להורמון זה, התא יאזן ריכוזי אוסמולליות על ידי הפרשת מים החוצה, וכך יקטן נפח התא והאוסמו-רצפטורים יביאו להפרשת ADH.
קולטנים ל-ADH
קיימים כמה קולטניםים לואזופרסין, עם מבנה של קולטני G protein, עם 7 לולאות טרנס-ממברנליות.
קולטן מסוג V1- קולטן זה נמצא על תאי שריר חלק בדופן כלי דם, בעיקר עורקים וגורם לכיווצם. לאחר היקשרות ADH לקולטן זה, מתבצע שפעול של פוספוליפאז C אשר מפרק PIP2 ליצירת אינוזיטול תלת זרחתי (IP3) ו-diacylglycerol או DAG. יצירת DAG משפעת את האנזים פרוטאין קינטזה C, שיכול אף הוא לתרום לכיווץ השריר החלק הוסקולארי דרך זרחון של חלבון, וכתוצאה מכך מגביר את לחץ הדם העורקי. כתוצאה מהגעתו של IP3 לרטיקולום הסארקופלזמי, משתחרר סידן, ומתרחש כיווץ. עם זאת, הריכוזים הפיזיולוגיים הנורמאליים של ADH, נמוכים מאלה בתחום הגורם לו להיות vasoactive. עם זאת, ניסויים הראו שבתרחיש של הלם היפו-וולמי חמור, כאשר שחרור ADH מאוד מוגבר, תורם הורמון זה באופן מפצה להגברה של התנגודת הוסקולארית הסיסטמית.
הפעלת הרצפטור ל-ADH בכליה מביאה גם לשחרור של פרוסטגלנדין ופרוסטציקלין. חומרים אלו מפריעים לפעילותו של ההורמון בכליה וגם לפעילותו בכיווץ כלי דם. כלומר, ההורמון מפעיל על ידי משוב שלילי חומרים אשר מעכבים את פעילותו. מעבר לפעולתו בכיווץ כלי דם, ידוע ש-ADH מעלה בנסיוב את רמות פקטור קרישה VIII, זאת כנראה על ידי גירוי של שחרור האחרון מתאי האנדותל, ובכך הוא מעודד צימות טסיות.
קולטן מסוג V2- קשור בהשפעה האנטי-דיורטית של ההורמון: ההורמון מגיע אל הכליה וגורם לחדירה של מים בחזרה אל הגוף דרך תעלות מים מסוג aqua-porin 2, במנגנון הבא: ההורמון מגיע מהדם, נקשר לקולטן מסוג V2 אשר נמצא בצד הבאזו-לטרלי של האבובית המאספת ( collecting duct). על ידי ההיקשרות לקולטן, ADH משפעל adenylate cyclase, הגורם ליצירת cAMP מ-ATP, מה שיביא בהמשך למודיפיקציה באנזים ה- protein kinase A. שינוי באנזים זה יביא לפוספורליציה של שלפוחיות (vesicles) המכילות aqua porin 2, הנמצאות בצד הלומנאלי (הפונה ל-lumen) ולא בצד הבאזולטרלי.
לכן מים חודרים דרכן לתוך התא, אך כדי לצאת ולחזור בחזרה לדם יש צורך בתעלות מסוג aqua porin 3 ו- 4. כאשר נפסקת פעולת ADH, תעלות אלו עוברות אנדוציטוזה לתוך התא. פעילות ADH גורמת לריכוזו של השתן, כדי לרכז את השתן יש צורך שהמדולה תהיה היפרטונית-מרוכזת. לעתים, במצבים של שתייה מוגזמת, המדולה אינה היפרטונית מספיק והיכולת התגובה של ADH נמוכה. במצבים של מתן משתנים כגון פוסיד, הרה-אבסורפציה קטנה ויש שיבוש ביכולת לרכז שתן.
יתרה מכך, ADH מגביר את החדירות של urea בצינורות המאספים, מה שמגביר הגברת הספיגה מחדש של urea במדולה של הכליה. urea אינו מהווה גירוי המעכב הפרשת ADH. תפקיד חשוב נוסף של ADH הוא בעידוד של ספיגה מחדש של נתרן בחלק העולה של לולאת Henle.
קולטן מסוג V3-נמצא בעיקר בהיפופיזה, והוא מצומד ל-G-protein ומגביר את רמת הסידן התוך תאי כאשר הוא משופעל. קולטן זה קשור לשחרור ACTH ופועל כנוירו-טרנמיטור או מתווך הקשור לתהליכי אגירת זיכרון, וויסות טמפרטורת הגוף.
תכשירים אנלוגים של ADH
חומרים אגוניסטים של ADH משמשים בתרחישים קליניים אחדים, כאשר האנלוג הסינתטי desmopressin נמצא בשימוש במצבים של הפרשה נמוכה של ההורמון, כמו גם כדי לשלוט על דימום (בצורות מסוימות של מחלת von Willebrand או בהמופיליה A מתונה). התכשיר terlipressin משמש לעתים כמכווץ כלי-דם. מאז שנות ה-70 יש שימוש באנלוגים של ADH במצבי של דליות בוושט (esophageal varices).
הסוגיה של טיפול ב-ADH בתרחיש של דום לב
הזרקת הוואזו-פרסוֹר אפינפרין בתרחיש חרום של דום לב וירידה פתאומית דרמטית בלחץ הדם, הוצעה עוד בראשית המאה הקודמת כטיפול חירום אפשרי. בשנות ה-60 התעורר נושא השימוש ב-vasopressors לטיפול בדום לב, בעקבות סדרת ניסויים בחתולים. רעיון טיפולי זה עלה שוב בתחילת שנות ה-90, כאשר נמצא שרמות ADH בדם עולות משמעותית לאחר טיפולי החייאה מוצלחים. ניסויים בחיות תמכו בשימוש ב-ADH או באפינפרין במצבי החייאה בדום-לב, תוך שהדגימו שיפור בלחץ זילוח כלילי כמו גם שיפור בהישרדות לטווח קצר כמו גם שיפור בממצאים הנוירולוגיים לאחר אירוע כזה.
למרות ש-ADH ואפינפרין שונים בפעולתם בכך של-ADH אין השפעה ישירה על התכווצות הלב, ל-ADH יש יתרון משוער על פני אפינפרין, בכך שהוא אינו מגביר את דרישת שריר הלב והמוח לאספקת חמצן. אך הערכה אחרונה זו שנויה במחלוקת, ולכן ה-AHA בהנחיותיו משנת 2010 ממליץ לשקול טיפול באפינפרין במצבי חירום של החייאה במבוגרים עם דום לב, ולא להשתמש ב-ADH למטרה זו.
פעילות ADH המופרש בתוך המוח
ADH מופרש לתוך המוח בתדירות צירקדיאנית, כאשר להורמון זה מיוחסת השפעה בתחום הזיכרון לטווח הקצר והארוך, רפלקסים מושהים וקליטת דמויות, אם כי מנגנונים פעילות זו אינם ברורים, ולכן השערות אלה עדיין אינן מבוססות. סביר ש-ADH פועל בתאום עם CRH או corticotropin-releasing hormone לגרום למודולציה של שחרור קורטיקו-סטרואידים מהאדרנל בתגובה למצבי עקה, בעיקר בתקופת הריון והנקה ביונקים. ניסויים בבעלי חיים מרמזים לתפקיד ADH במצבי אגרסיה כלפי זכרים אחרים, בקשרים בין-מיניים, מוטיבציה מינית, תחושת זוגיות, והתנהגות חברתית ככלל.
תרחישים קליניים
מצב של עלייה גבוהה מאוד של ADH בפלזמה נובע מהפרשה אקטופית של ADH מגידולים סרטניים שונים ברחבי הגוף.
מצב של רמת ADH מוגברת בפלזמה מתרחש נובע בתסמונת SIADH, בגידולים מוחיים, ב-acute intermittent porphyria, בתסמונת Guillain-Barre, במחלות אינפקטיביות של כלי הדם או המוח, דלקת ריאות, בשחפת ריאתית, במנינגיטיס שחפתית, בסיכרת תפלה נפרוגנית.
מצב של חסר בהפרשת ההורמון ADH בסוכרת תפלה מרכזית (central diabetes insipidus), בו יש הפרשה רבה מאוד של שתן, מופיעה היפר-נתרמיה, והחולה החש צימאון נמצא בסכנת התייבשות. הטיפול בתרחיש זה כצפוי הוא בהזרקה של ADH. ירידה ברמת ADH אופיינית לתרחיש של psychogenic polydipsia, וכן לתסמונת נפרוטית, ולנזק לבלוטת יותרת המוח.
עוד מצב בו יש ירידה ברמות ADH בגוף הוא אלכוהוליזם. אתנול מפחית את הפרשת ADH התלויה בסידן, על ידי חסימה של תעלות סידן המופעלות על ידי מתח חשמלי (voltage gated) בקצות העצבים הנוירו-היפופיזיאלים. הירידה בהפרשת ADH מביאה להגברת הפרשת מים בשתן, מה שמביא להתייבשות ולתחושת חמרמורת (hangover).
תסמונת ההפרשה-הלא-תואמת של הורמון ADH או SIADH מתאפיינת בהפרשת-יתר של ADH.
תסמונת זו יכולה להיגרם בתרחישים רבים כגון מחלה חדה וכרונית של מערכת העצבים, שבץ, זיהום על ידי מנינגוקוקוס, טראומה גופנית, עירור אדרנרגי או הפרשה אקטופית של ADH על ידי גידולים שונים (כגון גידולי ריאה מסוג קרצינומה קשקשית, small cell carcinoma). ניתוחי חזה גדולים עלולים לגרום גם הם לתרחיש של SIADH, וכן גם מחלות ריאה כגון אטלקטזיס, דלקת ריאות או קצרת.
חשד לתסמונת זו מתעורר בנבדקים בעלי היפונתרמיה עיקשת, שיכולה להיגרם מעודף של ההורמון ADH. האוסמולליות בפלזמה גדלה ורמות הנתרן נמוכות באופן יחסי. אצל מטופלים עם אוסמולליות שתן נמוכה פחות מהמקסימום, גם כן ניתן לחשוד כי הם סובלים מ-SIADH. באופן כללי, כאשר הפלזמה מהולה, הצפי הוא שהשתן יהיה מהול בהתאם, אולם מאחר שאצל חולים אלו יש עודף בהורמון ADH, השתן יהיה מרוכז מעט יותר. לאישוש האבחנה של SIADH, יש לשלול מצבים אחרים דוגמת מחלת כליות גם בה תיתכן פגיעה במנגנון ריכוז או מיהול השתן.
תכשירים ותרופות המשפיעות על רמת ADH בנסיוב
- מגבירים את רמת ההורמון: תכשירים אנטי-פסיכוטיים (דוגמת haloperidol ו-phenothiazines), ברביטורטים, carbamazepine ,chlorpropamide, ציספלטין, clofibrate ,cyclophosphamide ,furosemide (לעתים נדירות), משככי כאבים נרקוטיים כגון מורפין, thiazides, נוגדי דיכאון כפרוזאק וכן נוגדי-דיכאון טריציקליים דוגמת amitriptyline ו-desipramine, vidarabine, vinblastine, vincristine, tolbutamide, ניקוטין, היסטמין, ברומוקריפטין.
- מפחיתים רמת ההורמון: ליתיום קרבונאט, phenytoin, ethanol, סידן, demeclocycline.
- תרופות המסייעות להגברת ההשפעה של ADH: אספירין ותרופות נוגדות דלקת לא-סטרואידליות (NSAIDs) אחרות, acetaminophen, מתפורמין, תאופילין.
מבדק דיכוי ADH על ידי העמסת מים או Water loading ADH suppression test
מבדק זה יתבצע לסייע באבחון SIADH, בנבדקים עם רמות נתרן ואוסמולליות נמוכות בדם, אך עם רמת נתרן תקינה בשתן. נבדקים אלה אינם מייצרים כמות שתן כמצופה, והאוסמולליות בשתן שלהם גבוהה יחסית לזו שבדמם. רמת ADH בדם גבוהה מהנורמה.
מבחן עידוד ADH על ידי הצמאה - Water deprivation ADH stimulation test
מבדק זה נועד להבדיל בין 2 סוגים של סוכרת תפלה - diabetes insipidus:
- סוכרת תפלה מרכזית-מאופיינת על ידי ייצור נמוך של ADH ואי היכולת לרכז שתן הבאה לביטוי על ידי עליה באוסמולליות של השתן אחרי מתן ADH אך לא על ידי הצמאה או שלילת מים בלבד.
- סוכרת תפלה נפרוגנית-מאופיינת על ידי אטי היכול שת הכליות להגיב ל-ADH הבאה לביטוי בחוסר שינוי באוסמולליות של השתן לפני או אחרי מתן ADH.
הוראות לביצוע הבדיקה
לפני נטילת דם לצורך הבדיקה, יש לקחת בחשבון שמספר תכשירים ותרופות יכולים להשפיע בצורה ניכרת על תוצאת הבדיקה, באופן שיכול לחייב הפסקת נטילתם במידת האפשר. כך למשל צריכת אלכוהול, אינסולין, חומרים משתנים, וניקוטין תשפיע על תוצאות הבדיקה, בנוסף לתכשירים אחרים המפורטים למעלה. את הדם יש ליטול במבחנת ספירת-דם (EDTA, פקק סגלגל), כאשר יש להפריד בסרכוז במהירות האפשרית את הדם בצנטריפוגה מקוררת, ולהקפיא את הפלזמה באופן מיידי, אם הבדיקה לא מתבצעת בזמן אמת. יש לקחת בחשבון שהפרשת ADH מוגברת כאשר האדם במצב זקוף, וכן בשעות הלילה, או כאשר הוא נתון בכאבים, בעקה, או לאחר פעילות גופנית מאומצת. רמת ADH בדם פוחתת אם הנבדק נתון במצב שכיבה ממושך, או כאשר הוא סובל מיתר לחץ-דם.


 כניסה
כניסה  עקבו אחרינו בפייסבוק
עקבו אחרינו בפייסבוק