סרטן ריאה - טיפולים חדשים - טיפולים ביולוגיים וטיפולים אימונותרפיים - Lung cancer - immunotherapy
| סרטן הריאה - טיפול אימונולוגי | ||
|---|---|---|
| Lung cancer - immunotherapy | ||
| ||
| יוצר הערך | ד"ר מיה גוטפריד, ד"ר משה משאלי, ד"ר נטלי מימון רבינוביץ | |
לערכים נוספים הקשורים לנושא זה, ראו את דפי הפירושים: – סרטן ריאה , סל תרופות 2016
NSCLC (Non Small Cell Carcinoma) מהווה בעיית תחלואה עיקרית עולמית וגורם מוביל בתמותה מסרטן. ברוב החולים מאובחנת המחלה בשלב מפושט שאינו ניתן לכריתה בניתוח. במיעוט החולים, המחלה מאובחנת בשלבים מוקדמים ונתיחים, ורק כ-15 אחוזים מכלל חולי סרטן הריאות נרפאים. שני שלישים מהחולים מאובחנים עם מחלה מוקדית מתקדמת או עם גרורות, הפרוגנוזה (Prognosis) שלהם גרועה ושיעורי ההישרדות לחמש שנים הם נמוכים[1].
גורם הסיכון העיקרי לסרטן הריאה הוא עישון, אשר מעלה את הסיכון לכל סוגי סרטן הריאה. גורמים נוספים כוללים עישון סביל, חשיפה לגז Radon וכן חשיפה ל-Asbestos ולחומרי תעשייה שונים[2].
קיימים שלושה תת-סוגים עיקריים של סרטן ריאה מסוג NSCLC:
- Squamous cell carcinoma (סרטן תאי קשקש)
- Adenocarcinoma (סרטן מסוג אדנוקרצינומה)
- (Large cell (anaplastic carcinoma (סרטן מסוג תאים גדולים)
ישנה חשיבות בהפרדה בין הסוגים השונים, מאחר שזהו גורם חשוב בהחלטה על המשך בירור מולקולארי (Molecular) וטיפול מערכתי.
מטרות הטיפול בחולים בשלב מחלה מפושטת כוללות הקלה בתסמיני המחלה (שיעול, קוצר נשימה, כאבים וכדומה), שליטה בסרטן, הארכת הזמן עד התקדמות המחלה והארכת ההישרדות[3]. כימותרפיה (Chemotherapy) היא מבסיסי הטיפול המערכתי בחולים אלה ואנו עדים, לאחר שנות האלפיים, למחקרים קליניים רבים שמטרתם למצוא את השילובים היעילים ביותר. נמצא שמשלב של שתי תרופות כימותרפיות הכולל Platinum הביא לשיפור בתגובה לטיפול, בהישרדות ובאיכות החיים[4]. עם זאת, נמצא שאין יתרון לתרופה מסוימת במשלב עם Platinum, וכי כל המשלבים מביאים לזמן הישרדות זהה של 9–10 חודשים בלבד. משלב של יותר משתי תרופות נבדק במחקרים קליניים רבים, אולם לא הביא לשיפור בהישרדות אלא רק לעלייה ברעילות[5]. משלב המכיל Pemetrexed (Alimta) ו-Cisplatin הוא המועדף בסוג ההיסטולוגי (Histology) של NSCLC[6].
שיעורי הישרדות נמוכים של חולים עם מחלה גרורתית המטופלים בכימותרפיה, יחד עם הבנה טובה יותר של התהליכים המעורבים בהיווצרות שאתות של סרטן הריאה, מביאים למחקר ולפיתוח תרופות חדשות.
התרופות החדשות, לרוב עם רעילות נמוכה, משפרות בצורה משמעותית את הישרדות החולים. הבנת המנגנון החיסוני של הסביבה הגידולית ומנגנוני ההישרדות של הגידול אפשרה פיתוח תרופות חדשות. תרופות הפועלות במנגנון של חסימת 1-Anti PD-1) PD), מסלול המווסת את פעילות מערכת החיסון כנגד הגידול, מדגימות שיעורי תגובה גבוהים וממושכים.
תרופות אונקולוגיות מותאמות אישית מאפשרות טיפול אופטימלי בחולה בהתאם למאפיינים ייחודיים שלו ושל הגידול. רפואה מותאמת אישית חשובה ברפואה בכלל ובאונקולוגיה בפרט בגלל ההשפעה הישירה של בחירת הטיפול על הישרדות החולה והשונות הגדולה במאפייני המחלה והחולים.
Epidermal Growth Factor Receptor (EGFR)
בשאתות ריאה מסוג NSCLC קיימות מוטציות (Mutations) ספציפיות ב-Tyrosine kinase שב-EGFR (הנקרא גם HER1). הפעלת הקולטן ורצף הסיגנלים (Signals) בעקבותיו מעודדים שגשוג תאים. קולטנים עם מוטציה בתאים ממאירים מגיבים ביתר לגורמי גדילה באופן המגביר את ההתנהגות הממאירה של התא. קיימות מספר מוטציות כאשר שתיים מהן הן השכיחות ביותר ומאותרות בכ-90 אחוזים מהשאתות[6].
דור ראשון
Gefitinib ,Erlotinib
Gefitinib ו-Erlotinib הן תרופות פורצות דרך בטיפול הממוקד בסרטן הריאה. התרופות פועלות על ידי חסימה הפיכה, תוך תאית, של הקולטן על ידי עיכוב של ה-Tyrosine kinase [בחלק הפנימי של הקרום (Membrane)]. התוצאה היא בלימת הקולטן, בלימת מעבר אותות הגדילה התוך תאיים ומוות תאי מתוכנת (Apoptosis). התרופות פועלות כטיפול קו ראשון רק בחולים עם מוטציה ב-EGFR[7]. המוטציות שכיחות בעיקר בשאתות מסוג Adenocarcinoma, בנשים ובלא מעשנים[8]. במחקר שלב שלישי, שבו הושווה טיפול ב-Geftinib לעומת טיפול במשלב כימותרפיה [[[Carboplatin]] ו-Paclitaxel (Taxol)] במטופלים עם סרטן ריאה מפושט שלא טופלו לפני כן, הודגם יתרון הישרדותי לטיפול ב-Geftinib לעומת כימותרפיה בחולים עם מוטציה ב-EGFR. בחולים אלה, הזמן עד התקדמות המחלה (Progression Free Survival ,PFS) היה ארוך באופן משמעותי ושיעור התגובה לטיפול היה גבוה יותר. במטופלים ללא מוטציה ב-EGFR היה יתרון הישרדותי לקבוצה שטופלה בכימותרפיה[9].
דור שני
Afatinib
Afatinib היא מולקולה (Molecule) קטנה, המעכבת באופן בלתי הפיך את EGFR. התרופה נבדקה, במחקר בינלאומי שלב שלישי, מול טיפול כימי במשלב עם Pemetrexed (Alimta), ונמצא יתרון של כ-4 חודשים בזמן עד להתקדמות המחלה בטיפול ב-Afatinib[10]. כמו כן, Afatinib הראתה יתרון בהישרדות הכוללת של למעלה משנה לעומת משלב הטיפול הכימי Pemetrexed ו-Cisplatin, בחולים עם מוטציה ב-Axon19.
המגבלה העיקרית בטיפול במעכבי Tyrosine kinase, EGFR היא העמידות הנרכשת לטיפול, המתפתחת ברוב המקרים. הגורם העיקרי לעמידות הוא מוטציה נרכשת בשם T790M, המתרחשת בכמחצית מהחולים. שתי תרופות חדשות הדגימו, במחקר שלב 1, פעילות כנגד מוטציה זו. תרופות אלו שייכות לדור השלישי של מעכבי EGFR.
Vascular endothelial growth factor (VEGF) ו- Angiogenesis
אנגיוגנזה (Angiogenesis, יצירת כלי דם חדשים) היא תהליך המאפשר לתאים לקבל אספקת חמצן וחומרי מזון, ולפיכך חיוני לצמיחתם. בתאים סרטניים יש חשיבות לתהליך גם ביכולת שליחת גרורות לאיברים מרוחקים. תהליך זה משופעל בשאתות על ידי הפרשת החלבון VEGF. עיכוב התהליך מביא להפרעה ביצירת כלי דם חדשים עם פגיעה בגדילה, חדירה ופיזור של התאים הסרטניים[11].
Bevacizumab
Bevacizumab היא התרופה הראשונה שנכנסה לטיפול קליני הפועלת במנגנון של עיכוב אנגיוגנזה. זהו נוגדן חד שבטי (Monoclonal) הנקשר ספציפית ל-VEGF ומונע ממנו להיקשר לקולטנים על פני תאי האנדותל (Endothelium) ולשפעלם, וכך מעכב את תהליך האנגיוגנזה. בנוסף, התרופה משפרת את הגעת הכימותרפיה לשאת על ידי הפחתת החדירות הגבוהה המאפיינת את דופן כלי הדם שנוצרו בתהליך האנגיוגנזה. במחקר שלב שלישי, נבדקה יעילות ה-Bevacizumab במשלב עם כימותרפיה מקובלת של Carboplatin ו-Paclitaxel בקרב חולי סרטן ריאה עם גרורות, Non-squamous NSCLC, בקו טיפול ראשון. המחקר העלה כי הוספת התרופה לכימותרפיה הביאה להארכה מובהקת בהישרדות החציונית של החולים בהשוואה לכימותרפיה בלבד (12.3 לעומת 10.3 חודשים) ולשיפור המדדים[12].
Nintedanib
במחקר אקראי, שלב שלישי, השילוב של Nintedanib עם Docetaxel נמצא יעיל כטיפול קו שני לחולי NSCLC מתקדמים שטופלו לפני כן במשלב כימי מבוסס Platinum. היעילות נצפתה במיוחד בחולים עם Adenocarcioma. הזמן החציוני ללא התקדמות מחלה היה גבוה יותר בקבוצה שטופלה בשילוב, לעומת הקבוצה שטופלה ב-Docetaxel לבד (3.4 חודשים לעומת 2.7 חודשים בהתאמה). כמו כן, Nintedanib מוסיפה להישרדות הכוללת חודשיים, בחולים עם Adenocarcinoma, בהשוואה ל-Docetaxel לבד[13].
Ramucirumab
Ramucirumab היא תרופה נוספת הפועלת על ידי עיכוב אנגיוגנזה. במחקר אקראי, שלב שלישי, נמצא שהשילוב של Ramucirumab עם Docetaxel משפר שרידות בחולי NSCLC מתקדמים שקיבלו את הטיפול כקו שני[14].
EML4-ALK fusion protein
נמצאה התמרה (Transformation) גנטית חדשה אשר תוצאתה היא חיבור של שני גנים (Genes) - הגן ALK (Anaplastic Lymphoma Kinase) וה-EML4 (Echinoderm Microtubule associatedprotein-Like 4) ב-Chromosome p2[15]. החיבור מביא ליצירת חלבון עם פעילות סרטנית והפעלה בלתי תקינה של מסלולים תוך תאיים[16]. נכון להיום, FISH (Fluorescence In Situ Hybridization) היא בדיקת הבחירה של החיבור ALK-EML4. תוצאה חיובית (ALK חיובי) מוגדרת כאשר מוצאים את החיבור לפחות ב-15 אחוזים מהתאים[17]. פגם זה נמצא בעיקר בחולים לא מעשנים, בשאתות מסוג Adenocarcinoma (שכיחות של 2–5 אחוזים), בקבוצת גיל צעירה יחסית ובשאתות ללא מוטציה בגורם הגדילה EGFR[18].
Crizotinib
Crizotinib היא התרופה הראשונה מסוגה שאושרה לטיפול בחולים עם ALK חיובי. זוהי מולקולה קטנה ובררנית, הניטלת בדרך פומית ומעכבת תחרותית של ALK וקינאזות (Kinases) נוספות [כגון MET (Mesenchymal Epithelial Transition) ו-ROS]. התרופה מעכבת את שגשוג התא וכך גורמת ל-Apoptosis של התא הסרטני. במחקר שלב שלישי, בחולים עם ALK חיובי, נבדקה התרופה לעומת כימותרפיה כקו טיפול שני ונמצא שיפור משמעותי בזמן עד להתקדמות המחלה (מ-3 חודשים ל-7.7 חודשים). אולם, לא נמצא שיפור בהישרדות הכללית, קרוב לוודאי עקב מעבר של חולים מזרוע מחקר הכימותרפיה לזרוע ה-Crizotinib[19].
Ceritinib
Ceritinib היא תרופה שאושרה באפריל 2014 על ידי ה-FDA (Food and Drug Administration) כטיפול בחולים עם ALK חיובי לאחר כישלון טיפולי ב-Crizotinib.
Alectinib
בדומה ל-Ceritinib, מטרת ה-Alectinib לפעול באותם המקרים אשר מפתחים עמידות לאחר השימוש ב-Crizotinib. מחקר שלב ראשון שנערך בארצות הברית, על חולי NSCLC חיוביים ל-ALK ושטופלו לפני כן ב-Crizotinib, הראה שיעור תגובה של 54.5 אחוזים ל-Alectinib[20].
אימונותרפיה - תרופות המשפעלות את מערכת החיסון
משנות האלפיים חלה התקדמות משמעותית בתחום האימונותרפיה (Immunotherapy) בסרטן, שבין היתר מהווה בשורה לחולי סרטן הריאה המתקדם. מטרת הטיפולים האימוניים בסרטן היא לעורר את פעילות מערכת החיסון כנגד תאי הסרטן.
הבנת המנגנון החיסוני של הסביבה הגידולית ומנגנוני ההישרדות של הגידול אפשרה פיתוח תרופות חדשות. השינוי התפישתי שחל הוא הכרה והבנה של מסלולי הבקרה של התגובה החיסונית, ה-Immune checkpoints.
משפחת הנוגדנים מסוג ה-PD-1 וה-PD-L1
מספר תרופות בתת-קבוצה זאת נמצאות בשלבים מתקדמים של מחקר קליני. בהן 1-Anti PD (Programmed cell Death-1) (Pembrolizumab ו-Nivolumab) ו-Anti PD-L1 (Programmed Death-Ligand 1) (Atezolizumab).
1-Anti PD: מסלול 1-PD הוא אחד מנקודות הבקרה של התגובה החיסונית. 1-Anti PD הוא נוגדן חד שבטי שאושר במספר מדינות לשימוש ב-Melanoma גרורתית ובסרטן ריאות מסוג NSCLC. התרופות ממשפחת ה-1-Anti PD עובדות בצומת שבין הלימפוציט (Lymphocyte) המשופעל לתאי הגידול הסרטני, בסביבת הגידול. תאי הלימפוציטים מסוג-T מבטאים את הקולטן 1-PD, ואילו הליגנדים (Ligands, מולקולות הקישור) שלו, PDL-20 ,PD-L1 מבוטאים על ידי תאי הגידול. אינטראקציה (Interaction) בין הקולטן לליגנד מעכבת את פעילות הלימפוציט.
ניסויים פרה-קליניים (Preclinical) הראו כי חסימת הקישור בין 1-PD לאחד הליגנדים באמצעות נוגדנים חד שבטיים מובילה לשפעול של מערכת החיסון ולפעילות אנטי סרטנית.
מחקר רב מרכזי ובינלאומי (001 Keynote) שבחן את יעילות ובטיחות הטיפול ב-Pembrolizumab בחולי NSCLC הוצג בכנס ה-AACR (The American Association for Cancer Research) האחרון ופורסם במאמר ב-NEJM (New England Journal of Medicine) על ידי Garon וחבריו במאי 2015. 495 חולים השתתפו במחקר, מתוכם כ-20 אחוזים טופלו ב-Pembrolizumab כקו ראשון למחלה מתקדמת.
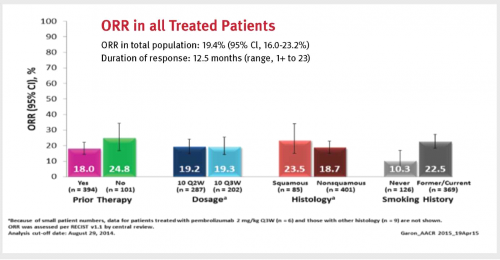
שיעור התגובה בכלל אוכלוסיית המחקר היה 19.4 אחוזים ומשך התגובה בחולים שהגיבו היה מעל שנה (12.5 חודשים). שיעור התגובה בחולים הנאיביים (101 מטופלים) עמד על 24.8 אחוזים (תמונה מספר 1)[21].
שימוש בביומרקרים (Biomarkers) לאפיון החולים והתאמת הטיפול מאפשרים טיפול ממוקד בחולים אשר להם סיכוי מרבי להגיב. בניסיון לחפש אחרי גורמים מנבאי תגובה לטיפול (Predictive factors) נבדק ביטוי הליגנד PD-L1 ברקמות הגידול של החולים.
במסגרת המחקר של Garon וחבריו דגימות הביופסיה (Biopsy) שנלקחו מהחולים עברו הערכה לסטטוס צביעה ל-PD-L1 באמצעות נוגדן הקרוי C322. ביטוי PD-L1 הוגדר חיובי אם נצבעו לפחות אחוז רחד מתאי הגידול. לאחר שנמצא קשר ראשוני בין ביטוי PD-L171 ליעילות של Pembrolizumab, אושר הקשר בצורה פרוספקטיבית (Prospective) במחקר[21].
ניתן להתרשם מגרף השרידות הכוללת (Overall Survival ,OS), המצורף (תמונה מספר 2), ששיעור גבוה מהחולים מפיקים תועלת ארוכת טווח מהטיפול, וכי התועלת משמעותית יותר באוכלוסייה לה צביעה חיובית לביומרקר.
תופעות הלוואי הנפוצות ביותר שנצפו במחקר של Garon כללו: תשישות, גרד וירידה בתיאבון[21]. כמו כן, נצפו תופעות לוואי אימוּניות (Immune adverse reactions), שלרוב ניתנו לשליטה טובה עם טיפול הולם. הטיפול ב-anti 1-PD הוא בעל פרופיל בטיחות סביר ואף משביע רצון בהשוואה לטיפולים הקיימים. חשיבות רבה יש למודעות, לזיהוי ולניהול נכון של תופעות הלוואי האימוּניות.
על סמך הנתונים שהתקבלו ממחקר Keynote 001; Pembrolizumab (Keytruda) קיבלה את אישור ה-FDA בתחילת חודש אוקטובר 2015 לחולי סרטן ריאה מתקדם מסוג NSCLC, אשר הגידול שלהם מבטא PD-L1 חיובי, כפי שנקבע בבדיקת ביומרקר מאושרת FDA, ואשר מחלתם מתקדמת במהלך או אחרי טיפול כימי מבוסס פלטינום. חולים עם מוטציה ב-EGFR או כאלו שהם ALK חיוביים יטופלו תחילה באחד מהטיפולים, מאושרי ה-FDA, המיועדים למוטציות אלו.
Pembrolizumab אושרה על ידי משרד הבריאות בארץ בספטמבר 2015 לשימוש בסרטן ריאה גרורתי מסוג NSCLC בחולים שמחלתם התקדמה תוך כדי או לאחר קו טיפול כימותרפי קודם מבוסס Platinum[22].
במהלך 2016 צפויים להתפרסם נתונים ראשוניים מתוך ה-010 Keynote שמטרתו להשוות את מדדי השרידות לאחר טיפול ב-Pembrolizumab לעומת טיפול ב-Docetaxet בחולי NSCLC שטופלו בעבר ויש להם ביטוי גבוה של PD-L1, ובנוסף, להעריך את בטיחות וסבילות התרופה.
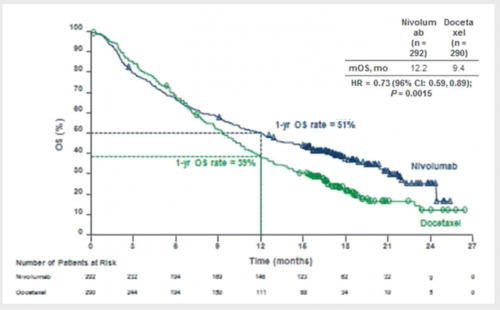
מחקר שלב שלישי, אקראי, אשר השווה טיפול ב-Nivolumab לעומת Docetaxel בחולים עם Nonsquamous NSCLC, לאחר שמחלתם התקדמה תוך כדי או אחרי טיפול כימי מבוסס פלטינום, הראה יתרון שרידותי ל-Nivolumab (שרידות כוללת חציונית 12.2 חודשים לעומת 9.4 חודשים בקבוצה שטופלה ב-Docetaxel). שרידות לאחר שנה בקבוצה שקיבלה Nivolumab עמדה על שיעור של 51 אחוזים בהשוואה ל-39 אחוזים בקבוצה שטופלה ב-Docetaxel. היתרון השרידותי אינו נצפה בחולים עם מוטציה ב-EGFR. שיעור התגובה, גם כן, היה גבוה באופן מובהק בחולים שקיבלו Nivolumab (19 אחוזים לעומת 12 אחוזים). לא נמצאו הבדלים מובהקים בין הקבוצות בזמן עד להתקדמות המחלה (PFS) (תמונה מספר 3)[23].
בניתוח התוצאות על פי אחוזי הצביעה של PD-L1 השרידות הכוללת החציונית, בחולים שטופלו ב-Nivolumab, הייתה 17.2, 18.2 ו-19.4 חודשים בחולים עם צביעה חיובית של אחוז אחד ומעלה, 5 אחוזים ומעלה ו-10 אחוזים ומעלה בהתאמה, בהשוואה ל-9, 8 ו-8 חודשים ל-Docetaxel[23].
השרידות הכוללת החציונית של חולים עם ביטוי PD-L1 נמוך מאחוז, נמוך מ-5 אחוזים ונמוך מ-10 אחוזים נמצאה זהה ל-Nivolumab (10.4-9.7 חודשים) ול-Docetaxel (10.3-10.1 חודשים)[23].
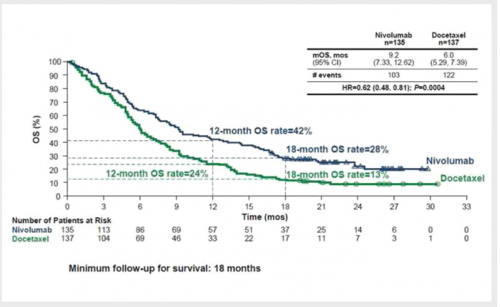
Nivolumab קיבלה את אישור ה-FDA בחודש מרץ 2015 לטיפול בחולי Squamouos NSCLC גרורתי, אשר מחלתם התקדמה תוך כדי או לאחר הטיפול הכימי. האישור התבסס על תוצאות מחקר בינלאומי, אקראי, אשר השווה טיפול ב-Nivolumab לעומת Docetaxel. התוצאות הראו יתרון ל-Nivolumab, אשר הציגה שיפור מובהק סטטיסטית בשרידות הכוללת (שרידות כוללת חציונית 9.2 חודשים לעומת 6 חודשים באלה שטופלו ב-Docetaxel) (תמונה מספר 4)[24].
Nivolumab (Opdivo) אושרה על ידי משרד הבריאות בארץ במרץ 2015 לשימוש כמונותרפיה (Monotherapy) בסרטן ריאה גרורתי מסוג NSCLC בחולים שמחלתם התקדמה לאחר קו טיפול כימותרפי קודם מבוסס Platinum[22].
ביבליוגרפיה
- ↑ Ferlay J, Shin HR, Bray F et al, Estimates of worldwide burden of cancer in 2008:GLOBOCAN 2008. Int J Cancer, 2010;127:2893-917.
- ↑ Hecht SS, Tobacco Smoke Carcinogens and Lung Cancer. Review. NCI J Natl Cancer Inst, 1999;91: 11941210.
- ↑ Chemotherapy in addition to supportive care improves survival in advanced non-small-cell lung cancer: a systematic review and meta-analysis of individual patient data from 16 randomized controlled trials. J Clin Oncol, 2008; 26:4617.
- ↑ Delbaldo C, Michiels S, Syz N et al, Benefits of adding a drug to a single-agent or a 2-agent chemotherapy regimen in advanced non-small-cell lung cancer: a meta-analysis. JAMA, 2004; 292:470.
- ↑ Schiller JH, Harrington D & Belani CP, Comparison of Four Chemotherapy Regimens for Advanced Non-Small- Cell Lung Cancer N Engl J Med. 2002; 346:92-98.
- ↑ 6.0 6.1 Li AR, Chitale D, Riely GJ et al, EGFR mutations in lung adenocarcinomas: clinical testing experience and relationship to EGFR gene copy number and immunohistochemical expression. J Mol Diagn,. 2008;10:242-8
- ↑ Lynch TJ, Bell DW, Sordella R et al, Activating mutations in the epidermal growth factor receptor underlying responsiveness of non-small-cell lung cancer to gefitinib. N Engl J Med, 2004;350:2129-39.
- ↑ Pao W, Miller V, Zakowski M et al, EGF receptor gene mutations are common in lung cancers from "neve rsmokers" and are associated with sensitivity of tumors to gefitinib and erlotinib. Proc Natl Acad Sci USA,. 2004;101:13306-11
- ↑ Mok T, Wu YP, Thongprasert S et al, Gefitinib or carboplatinpaclitaxel in pulmonary adenocarcinoma. N Engl J Med, 2009;361:1018-1020.
- ↑ Sequist LV, Yang JC, Yamamoto N, et al, Phase III study of afatinib or cisplatin plus pemetrexed in patients with metastatic lung adenocarcinoma with EGFR mutations. J Clin Oncol 31:3327-3334;2013.
- ↑ Aggarwal C, Somaiah N &Simon G, Antiangiogenic agents in the management of non-small cell lung cancer: where do we stand now and where are we headed? Cancer Biol Ther, 2012;13:247-63.
- ↑ Sandler A, Gray R &Perry MC, Paclitaxel-Carboplatin : Alone or with Bevacizumab for Non-Small-Cell Lung Cancer. N Engl J Med,. 2006;355:2542-50
- ↑ Martin R et al, Docetaxel plus nintedanib versus docetaxel plus placebo in patients with previously treated non-small-cell lung cancer (LUME-Lung 1): a phase 3, double-blind, randomised controlled trial. The Lancet, Vol 15, No. 2, p143-155, 2014.
- ↑ Garon EB et al, Ramucirumab plus docetaxel versus placebo plus docetaxel for second-line treatment of stage IV non-small-cell lung cancer after disease progression on platinum-based therapy (REVEL): a multicentre, double-blind, randomised phase 3 trial. The Lancet. Vol 384, No. 9944, p665-673, 2014.
- ↑ Soda M, Choi YL, Enomoto M et al, Identification of the : transforming EML4-ALKfusion gene innon-small-cell lung cancer. Nature, 2007; 448: 561-566.
- ↑ Kwak EL, Bang YJ &Camidge R, Anaplastic lymphoma kinase inhibition in non-smallcell lung cancer. N Engl J Med, 363: 1693-1703.
- ↑ Sholl LM, Weremowicz S, Gray SW et al, Combined use of ALK Immunohistochemistry and FISH for Optimal Detection of ALK-Rearranged Lung Adenocarcinomas. J Thoraci Oncol, 2013;8:322-328.
- ↑ Koh Y, Kim DW, K im TM et al, Clinicopathologic characteristics and outcomes of patients with anaplastic lymphoma kinase-positive advanced pulmonary adenocarcinoma: suggestion for an effective screening strategy for these tumors. J Thorac Oncol,. 2011;6:905 12
- ↑ Shaw AT, Kim DW, Nakagawa K et al, Crizotinib versus Chemotherapy in Advanced ALK-Positive Lung Cancer. N Engl J Med. 2013; 368:2385.
- ↑ Mark MA & Alice TS, ALK Inhibitors in Non-Small Cell Lung Cancer: Crizotinib and Beyond, Clin Adv Hematol Oncol. 2014 Jul; 12(7): 429^39.
- ↑ 21.0 21.1 21.2 Garon EB et al, Pembrolizumab for the Treatment of Non-Small-Cell Lung Cancer. N Engl J Med. 2015; 372:2018-2028.
- ↑ 22.0 22.1 מאגר התרופות של משרד הבריאות:https://www.old.health.gov.il/units/pharmacy/trufot/
- ↑ 23.0 23.1 23.2 Paz-Ares L et al, Phase III, randomized trial (CheckMate 057) of nivolumab (NIVO) versus docetaxel (DOC) in advanced non-squamous cell (non-SQ) non-small cell lung cancer (NSCLC). J Clin Oncol 33, 2015.
- ↑ Brahmer J et al, Nivolumab versus Docetaxel in Advanced Squamous-Cell Non-Small-Cell Lung Cancer. N Engl J Med 2015; 373:123-135.
קישורים חיצוניים
המידע שבדף זה נכתב על ידי ד"ר מיה גוטפריד, ד"ר משה משאלי, ד"ר נטלי מימון רבינוביץ - יחידת ריאות, המכון לאונקולוגיה, מרכז רפואי מאיר, כפר סבא


 כניסה
כניסה  עקבו אחרינו בפייסבוק
עקבו אחרינו בפייסבוק