אסתמה חמורה - טיפולים ביולוגים חדשים - Severe asthma - new biological therapy - 2021
הופניתם מהדף אסטמה אאוזינופילית חריפה, טיפולים ביולוגים חדשים - Acute eosinophilic asthma, new biological therapy - 2017 לדף הנוכחי.
| אסתמה חמורה - טיפולים ביולוגים חדשים 2021 | ||
|---|---|---|
| Severe asthma - new biological therapy - 2021 | ||
| ||
דוגמא לאאוזינופיל
| ||
| ICD-10 | Chapter J 46. | |
| ICD-9 | 493.01
, 493.91 |
|
| MeSH | D013224 | |
| יוצר הערך | ד"ר דניאל בן דיין הערך עודכן והורחב על ידי ד"ר אמיר בר- שי |
|
לערכים נוספים הקשורים לנושא זה, ראו את דף הפירושים – אסתמה#טיפול
אסתמה (Asthma) היא מחלה דלקתית כרונית של דרכי האוויר (הסימפונות) אשר מתפתחת עקב גורמים גנטיים וסביבתיים. היא מאופיינת באירועים חוזרים של תסמינים נשימתיים (כגון צפצופים, שיעול, קוצר נשימה, ליחה מרובה ולחץ בחזה) אשר משתנים בתדירות ובעוצמה לאורך זמן, וכן היא מאופיינת במגבלה משתנה בזרימת אוויר בבדיקת תפקודי ריאות. מאפיין חשוב נוסף של אסתמה הוא אירועים של התלקחויות חריפות. התלקחות חריפה מאופיינת בהחמרה חדה של הסימפטומים הנשימתיים וצורך בטיפול דחוף.
אסתמה היא מצב של רגישות יתר של הסימפונות אשר יכולה להופיע בכל גיל ולמעשה איננה חולפת, אם כי בהחלט יכולה להיות לא פעילה כלל למשך שנים רבות. הטיפול באסתמה מוכתב על פי שלושה מישורים: שליטה בתסמיני המחלה, קיומן של התלקחויות חריפות ומצב תפקודי הריאות בבדיקת ספירומטריה (Spirometry). מטרת הטיפול באסתמה היא שליטה בשלושת המישורים הללו, הואיל וחוסר איזון או העדר שליטה בכל אחד מהם מעיד על קיומה של דלקת בדרכי האוויר, אשר עלולה להוביל לנזקים בלתי הפיכים בסימפונות (Remodeling). טיפול נכון בדלקת בסימפונות מוביל לשליטה במחלה ומונע התפתחות פגיעה קבועה לדרכי האוויר. במרבית המקרים הדלקת בסימפונות היא דלקת מסוג 2 (Type 2 Inflammation), והתאים העיקריים הפעילים בדלקת זו הם האאוזינופילים (Eosinophils). שמות אחרים לדלקת בסימפונות הם דלקת אאוזינופילית או דלקת אלרגית. לרוב הסובלים מאסתמה דרגת המחלה היא קלה ובינונית והיא ניתנת לשליטה על ידי הטיפולים המקובלים במשאפים המכילים סטרואידים. חמישה עד עשרה אחוזים מחולי האסתמה סובלים מאסתמה חמורה (Severe Asthma), עד לתחילת המאה ה-21, לאסתמה חמורה לא היה מענה טיפולי מיטבי וחולים רבים סבלו מאסתמה חמורה שאינה בשליטה ( Severe Uncontrolled Asthma). לאסתמה שאיננה בשליטה יש השלכות אישיות, חברתיות וכלכליות קשות[1].
זיהוי מנגנונים ייחודיים לתהליך הדלקתי באסתמה ופיתוח תרופות ביולוגיות המותאמות לאטיולוגיה הדלקתית מגבירים את יכולת מתן המענה לחולים עם אסתמה חמורה, אשר היו נעדרי טיפול הולם. הטיפולים הביולוגיים באסתמה חמורה נמצאים בשגשוג, וממשיכים להיות במחקר ולהשתפר. חולים הסובלים מאסתמה חמורה שאינה בשליטה חווים היום שיפור ניכר באיכות החיים ובהפחתה משמעותית בהתלקחויות חדות, אישפוזים, ביקורים במיון ובמרפאות קהילה. על חולים הסובלים מאסטמה חמורה שאינה בשליטה להגיע לרופא המומחה באסתמה חמורה על מנת להתאים להם את הטיפול המתאים ביותר.
הגדרת אסתמה חמורה
אסתמה מוגדרת כמחלה חמורה כאשר נדרש טיפול של סטרואידים בשאיפה (Inhaled corticosteroids ,ICS) במינון גבוה ומרחיבי סמפונות ארוכי טווח על מנת להשיג שליטה במחלה, או לחלופין כאשר למרות טיפול זה אין שליטה במחלה[2]. לפני אבחנה סופית של אסתמה חמורה, ראוי לבדוק האם יש גורמים אשר ניתן לשנות ולשפר אשר עשויים להוביל לשליטה במחלה כגון: אי התמדה בטיפול, טכניקת לא נכונה בשימוש המשאפים, חשיפה לאלרגנים (Allergens), מחלות נלוות שאינן מטופלות [[[GERD|רפלוקס קיבתי ווישטי]] (GastroEsophageal Reflux, GERD), נזלת אחורית (Post-Nasal Drip, PND), או מיצוי לא מקסימלי של הטיפול הסטנדרטי[2][3].
על פי ההערכות, 10-5 אחוזים מתוך חולי האסתמה סובלים מאסתמה חמורה[1]. מתוכם, שיעור החולים שמחלתם איננה בשליטה הוא בין 30 ל-50 אחוזים במדינות שונות. בישראל שיעור חולי האסתמה החמורה נמצא 4.65 אחוזים מכלל חולי האסתמה, מתוכם 2/3 עם מחלה נשלטת ו-1/3 עם אסתמה שאיננה בשליטה[4]. אסתמה חמורה איננה מחלה אחידה וסמנים ביולוגיים (Biomarkers) שונים מסייעים לזיהוי הטיפול היעיל ביותר לכל מטופל. הסמנים הביולוגיים כוללים: אאוזינופילים בדם; ספירת אאוזינופילים בכיח; רמות IgE (Immunoglobulin E); תבחיני אלרגיה; רמת NO (Nitric oxide) באוויר ננשף (Fractional Exhaled NO ,FeNO); קיום מחלות נילוות (פוליפים אפיים, סינוסיטיס כרונית, Atopic Dermatitis)[3].
פתוגנזה של אסתמה חמורה
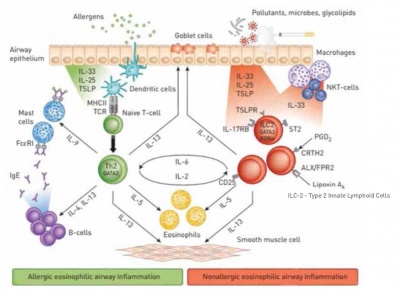
בשל העובדה שחולים הסובלים מאסתמה חמורה סובלים מאוד בתפקוד ברמה היומיומית, בשל תסמיני המחלה, סיבוכיה ותופעות הלוואי של התרופות אותן הם מקבלים, מנגנוני פעילות תאי מערכת החיסון בתהליך הפתוגני של אסתמה חמורה זכו להתעניינות רבה. הדלקת הנוצרת בסימפונות במחלת האסתמה מערבת תאים רבים וכן ציטוקינים (Cytokins) (מולקולות בעלות פעילות דלקתית, מתווכי דלקת) רבים. בין התאים הפעילים ביותר הוא האאוזינופיל, אך גם לתאי האפיתל של הסימפונות וכן לתאי Mast ולימפוציטים (Lymphocytes) תפקיד רב בתהליך המורכב המתרחש בסימפונות. מתווכי הדלקת הפעילים באסתמה הם TSLP (Thymic Stromal LymphoPoietin), IL-5 (InterLeukin), IL-4, IL-13, IgE, IL-33. מולקולות אלו מופרשות מלימפוציטים Th2 (T helper) או 2-Type 2 Innate Lymphoid Cells) ILC), מתאי האפיתל או מתאי Plasma, ומשפעלות את תאי מערכת החיסון, בעיקר אאוזינופילים, וגורמות לדלקת בסימפונות. דלקת ממושכת בסימפונות מובילה לרגישות יתר של דרכי האוויר, לנזק לתאי האפיתל העוטפים אותן ולשינוי מבני (Remodeling) שלהן[5].
דלקת אאוזינופילית של דרכי האוויר יכולה להיות קשורה הן לאסתמה אלרגית והן לאסתמה שאינה אלרגית. באסתמה אלרגית עם דלקת אאוזינופילית, האלרגנים הם שמובילים לשיעתוק ציטוקינים ולביטוי מוגבר של קולטנים כימוקינים בתאי Th2. כמו כן קיימת הפעלה של תאי Plasma לייצור והפרשה של נוגדני IgE אשר משפעלים תאי Mast המחמירים את התהליך הדלקתי. לעומת זאת, באסתמה אאוזינופילית שאינה אלרגית, מזהמים, חלקיקים נשאפים, חיידקים או גליקוליפידים (Glycolipids) משפעלים את האאוזינופילים דרך ציטוקינים אחרים דרך הפעלת תאי 2-ILC (תמונה 1). שפעול האאוזינופילים מוביל לתהליך דלקתי הרסני של המרכיבים השונים של הסימפונות וכולל נזק לתאי האפיתל, יצירת ריר מוגברת, הפעלת יתר של השריר החלק העוטף את הסימפונות, עיבוי השריר החלק של הסימפונות, התעבות והרחבה של שכבת המוקוזה והיצרות של החלל של דרכי האוויר (תמונה 2).
אסתמה אאוזינופילית מוגדרת כאשר יש עליה בכמות האאוזינופילים בכיח (מעל 3 אחוזים מכלל תאי הדלקת בכיח), ברם, ספירת התאים בכיח היא בדיקה לא שגרתית הדורשת מיומנות וציוד מיוחד. לכן, הבדיקה החלופית היא ספירת תאי האאוזינופילים בדם היקפי (Peripheral). בדיקה זו היא ספירת דם, בדיקה קלה, שגרתית וזמינה, אולם אינה ספציפית לאסתמה אאוזינופילית. אסתמה אאוזינופילית חמורה מוגדרת כאשר יש מעל 300 אאוזינופילים למיקרוליטר בספירת הדם של מטופל עם עדות קלינית ותפקודית של אסתמה חמורה[6]. אך קיימת קבוצה לא מבוטלת של חולים הסובלים מאסתמה חמורה אשר בספירת הדם שלהם רמת האאוזינופילים אינה גבוהה. בחולים אלו ייתכן ורמת האאוזינופילים בכיח תהיה גבוהה, או לחלופין שהתהליך הדלקתי בסימפונות שלהם חמור, מאופיין בדלקת מסוג 2, אך האאוזינופילים אינם השחקן היחיד או המוביל. כמו כן במקרים רבים ישנה חפיפה בין התהליכים השונים של הדלקת הסימפונית. הבנת התהליך הפתולוגי בדרכי האוויר הוא שיכול להוביל להתאמת הטיפול הביולוגי האופטימלי לסובלים מאסתמה חמורה.
התרופות הביולוגיות לטיפול באסתמה חמורה
רקע כללי לטיפולים ביולוגיים:
לאור העובדה שטיפול ביולוגי מותווה רק בחולים עם אסתמה חמורה שאיננה בשליטה, כל הטיפולים הביולוגיים ניתנים כתוספת לטיפול הסטנדרטי. הטיפולים ניתנים בהזרקה (תת עורית או תוך ורידית) ומחייבים מעקב של פולמונולוג (רופא ריאות) או רופא מומחה באלרגיה/אימונולוגיה.
Omalizumab
Omalizumab - נוגדן אנושי חד שבטי (Monoclonal antibody) (IgG) הוא הטיפול הביולוגי הראשון שאושר על ידי ה-FDA (Food and Drug Administration) לטיפול באסתמה חמורה. הנוגדן נקשר לנוגדן ה-IgE בדם המטופל ומונע את קישורו לקולטן שלו בתאי המטרה (תאי Mast). הטיפול מתאים לחולי אסתמה בעלי מרכיב אלרגי (הוכחה של אלרגיה בתבחיני עור או בבדיקות IgE ספציפי בדם) ורמת IgE מעל 30 בבדיקת דם. Omalizumab הוא בולם ניתן בהזרקה תת-עורית (Sub-Cutaneous, SC) במינון הנקבע בהתאם לרמת ה-IgE ומשקל המטופל. בשנת 2005 פורסם המחקר שהדגים את יעילות התרופה בחולי אסתמה קשה הסובלים מהתלקחויות חוזרות[7]. מחקר זה ומחקרים רבים אחריו הראו כי טיפול ב-Omalizumab הוביל להפחתה משמעותית בתדירות ההתלקחויות החריפות, הורדת תדירות האשפוזים בשל התקפי אסתמה, הורדת מינוני הסטרואידים הסיסטמיים (Systemic steroids) ושיפור בתפקודי הריאות. עוד נמצא כי האפקטיביות של הטיפול אינה תלויה ברמת האאוזינופילים בדם או ברמת ה-FeNO[8][9][10]
Mepolizumab
Mepolizumab - נוגדן אנושי חד שבטי (k־Ig1) כנגד IL-5 . זהו הטיפול הביולוגי הראשון שאושר על ידי ה-FDA לטיפול באסתמה אאוזינופילית חמורה, בתוספת טיפול סטנדרטי. Mepolizumab ניתן בהזרקה תת-עורית במינון של 100 מיליגרמים ללא קשר למשקל המטופל. הוא נקשר בספציפיות גבוהה ל־5־IL אנושי, וההיקשרות מונעת איתות ומביאה לירידה בייצור האאוזינופילים ומנטרלת את פעילותם ואת הישרדותם[11].
3 מחקרים מרכזיים מבוקרים כפולי סמיות בחנו את יעילות Mepolizimab אצל חולי אסתמה אאוזינופילים חמורה [SIRIUS (Steroid Reduction with Mepolizumab Study), MENSA (Mepolizumab as Adjunctive Therapy in Patients with Severe Asthma), DREAM (Dose Ranging Efficacy and Safety with Mepolizumab)] [12][13][14].
במחקרי MENSA ו-DREAM, מינון של 100 מיליגרמים תת-עורי כל 4 שבועות במשך כ-8 חודשים הביא לירידה משמעותית בתדירות החרפות בהשוואה לקבוצת ה-Placebo (הפחתה של 53 אחוזים, 0.001>P), לשיפור בתפקודי הריאות [FEV1 (Forced Expiratory Volume in one second) עלה ב־98 מילילטרים, 0.03 =P] ובאיכות החיים (0.001>P). נכללו מטופלים עם רמת אאוזינופילים בדם מעל 150 למיקרוליטר, אבל ניתוח הנתונים הראה שתוצאות הטובות ביותר הופיעו אצל מטופלים עם אאוזינופילים מעל 300 למיקרוליטר בדם ההיקפי[12][13].
מחקר ה-SIRIUS בחן את יעילות Mepolizumab בהפחתת צריכת סטרואידים סיסטמיים (OCS) במטופלי אסתמה אאוזינופילית קשה שנזקקו לטיפול כרוני ב-OCS. תוצאות המחקר הראה סיכוי גדול פי 2.39 לצמצום צריכת OCS בקבוצת ה-Mepolizumab בהשוואה לקבוצת ה-Placebo (0.008=P) . בנוסף לצמצום מינוני הסטרואידים הסיסטמיים, הושגה גם ירידה של 32 אחוזים בשיעור ההתלקחות השנתי בקבוצת ה-Mepolizumab בהשוואה ל-Placebo (0.04 = P)[14].
Reslizumab
Reslizumab - נוגדן אנושי חד שבטי בולם 5־IL, השני שאושר על ידי ה-FDA לטיפול באסתמה אאוזינופילית חמורה. Reslizumab נקשר לאזור המקביל לחומצות אמינו 89–92 על גבי 5-IL ובולם את השפעתו. הוא אושר במינון של 3 מיליגרמים לקילוגרם משקל גוף וניתן באופן תוך ורידי, בעירוי למשך 20–50 דקות, פעם ב-4 שבועות.
שני מחקרי רישום דומים ומקבילים בחנו את יעילות Reslizumab בחולים עם אסתמה אאוזינופילית חמורה שאינה בשליטה[15][16] למשתתפים במחקר הייתה לפחות ספירת דם אחת עם מספר אאוזינופילים מעל 400 מיקרוליטרים והם טופלו ב-ICS במינון בינוני/גבוה עם או בלי אמצעי שליטה נוסף. בשני המחקרים, הסיכוי להתלקחויות חדות הצטמצם בצורה משמעותית בקבוצה ה-Reslizumab לעומת קבוצת ה-Placebo: 50 אחוזי הפחתה בהתלקחויות במחקר הראשון (0.0001>P), ו-59 אחוזים במחקר השני (0.0001>P). בנוסף, בקרב החולים בקבוצת ה-Reslizumab נצפה שיפור מובהק בתפקודי ריאות (עלייה של 160 מיליליטרים ב-FEV1) ובמדדי איכות החיים. מכיוון ש-0.3 האחוז מהמשתתפים במחקרים פיתחו תגובה אנאפילקטית (Anaphylactic reaction), הוציא ה-FDA אזהרה והנחיה לפקח על החולים במסגרת רפואית אחרי עירוי התרופה[17]. לא היו תופעות לוואי משמעותיות אחרות.
Benralizumab
Benralizumab - נוגדן חד שבטי (IgG1kappa) הניתן בהזרקה תת-עורית כל 8 שבועות ואושר על ידי ה-FDA לטיפול באסתמה אאוזינופילית חמורה בסוף 2017. בניגוד לשני הנוגדנים הקודמים אשר נקשרים ישירות ל- IL-5, נוגדן זה נקשר לתת-יחידה α בקולטן ל־IL-5. קשירה זו מובילה לשני תהליכים שונים: האחד קישור לאאוזינופילים ובאזופילים (Basophils) הגורם לבלימת ייצור האאוזינופילים וניטרול פעילותם. השני הוא קישור באפיניות גבוהה לקולטנים המצויים בעיקר על גבי תאי הרג טבעי-NK (Natural Killer), היקשרות המביאה להיצמדות האאוזינופילים לתאי NK, ול-Apoptosis (מוות תאי) של האאוזינופילים בתהליך הנקרא Antibody dependent cell cytotoxicity ADCC[18].
Benralizumab ניתן במינון של 30 מיליגרמים במתן תת-עורי והוא נבחן בתדירות שונה בשני מחקרי רישום דומים (\[SIROCCO (Efficacy and safety of benralizumab for patients with severe asthma uncontrolled with high-dosage inhaled corticosteroids and long-acting β2-agonists) ו-CALIMA (Benralizumab, an anti-interleukin-5 receptor α monoclonal antibody, as add-on treatment for patients with severe, uncontrolled, eosinophilic asthma)][19][20]: תדירות של פעם ב־4 שבועות ותדירות של פעם ב־8 שבועות (כששלוש ההזרקות הראשונות של הטיפול הן בכל 4 שבועות) .
במחקר SIROCCO[19] נבדקו 1,205 חולים. המחקר הראה ירידת משמעותית בשיעור ההחרפות השנתי (45 אחוזים בקבוצת ה-Benralizumab בתדירות של אחת ל־4 שבועות ו-51 אחוזים בקבוצת מתן Benralizumab בתדירות של אחת ל-8 שבועות). כמו כן, הזמן עד להתלקחות החדה הראשונה היה ארוך יותר בשתי תדירויות בקבוצת הטיפול בהשוואה ל-Placebo. המחקר גם הראה שיפור משמעותי סטטיסטית ב-FEV1 של 159 מיליליטרים בקבוצת המטופלים שקיבלו Benralizumab כל 8 שבועות וב-106 מילילטרים בקבוצת המטופלים שקיבלו Benralizumab כל 4 שבועות. תסמיני האסתמה השתפרו רק בקבוצת מתן ה-Benralizumab כל 8 שבועות. התוצאות הטובות ביותר נצפו במטופלים עם רמת אאוזינופילים גבוהה מ-300 למיקרוליטר בספירת דם.
סיכום הממצאים משני המחקרים הללו הוכיח כי מתן Benralizumab בתדירות של 8 שבועות יעיל יותר מתדירות של 4 שבועות, ולכן הטיפול נרשם במינון של 30 מ"ג פעם ב-8 שבועות. לא נרשם שיעור תופעות לוואי שונה בקבוצת Benralizumab בהשוואה ל-Placebo.
מחקר ZONDA (Oral Glucocorticoid–Sparing Effect of Benralizumab in Severe Asthma)[21] בחן אפשרות צמצום OCS אצל הסובלים מאסתמה אאוזנופילית חמורה הזקוקים לשימוש כרוני ב-OCS. התוצאות הראו הורדה של 75 אחוזים במינון ה-OCS בהשוואה ל-Placebo שבו התאפשרה ירידה של 25 אחוזים בלבד (0.001>P). הסיכוי לצמצום מינון ה-OCS היה גדול פי 4.1 בקבוצות ה-Benralizumab בהשוואה ל-Placebo. במקביל לירידה במינוני ה-OCS, הייתה ירידה של 70 אחוזים בשיעור ההתלקחויות השנתי (0.001>P) וירידה של 93 אחוזים בשיעור הביקורים במיון. גם במחקר זה תדירות תופעות הלוואי הייתה דומה בקבוצות ה-Benralizumab וה-Placebo.
Dupilumab
Dupilumab (שם מסחרי: דופיקסנט - Dupixent) - נוגדן אנושי חד שבטי (Monoclonal antibody) הנקשר ופועל נגד תת-היחידה α של הקולטן לציטוקין IL-4 . בהיקשרותו לקולטן הוא מעכב את התקדמות התהליך הדלקתי התלוי ב-IL-4 ו- IL-13, ובכך מפחית משמעותית דלקת מסוג 2. זהו הטיפול הביולוגי הראשון שאושר על ידי ה-FDA לטיפול ב- Atopic Dermatitis, ואושר לראשונה לטיפול באסתמה חמורה המדגימה דלקת מסוג 2 ב-2018. Dupilumab ניתן בהזרקה תת-עורית במינון של 300 מיליגרמים פעם בשבועיים. בטיפול באסתמה חמורה קיימת מנת העמסה בטיפול הראשון של 600 מיליגרמים באופן חד פעמי. מינון זה ניתן ללא קשר למשקל המטופל או לרמת האאוינופילים בדם.
מחקר מבוקר כפול סמיות פאזה שלישית בחן את יעילות Dupilumab בחולי אסתמה בינונית עד חמורה נקרא מחקר ה-QUEST (Dupilumab Efficacy and Safety in Moderate-to-Severe Uncontrolled Asthma)[22]. במחקר בדקו שני מינונים שונים של Dupilumab, 200 מיליגרמים פעם בשבועיים ו-300 מיליגרמים פעם בשבועיים והוא נעשה על חולים הסובלים מאסתמה חמורה ללא הגבלה בספירת האאוזינופילים בדם. תוצאות המחקר היו טובות יותר במינון הגבוה ולכן זהו המינון שנרשם כמינון המומלץ בטיפול באסתמה חמורה שאינה בשליטה. במחקר זה נמצא כי טיפול ב-Dupilumab הפחית ב-46 אחוזים את שיעור ההתלקחויות החדות בהשוואה לקבוצת ה-Placebo (p<0.001) ושיפר ב-130 מיליליטרים את ה-FEV1 של המטופלים שקיבלו Dupilumab יחסית לקבוצת ה-Placebo (p<0.001).
הואיל וספירת האאוזינופילים לא הייתה בקריטריוני ההכללה במחקר, בתום המחקר בוצע ניתוח התוצאות על פי רמת האאוזינופילים של המטופלים שהשתתפו בו. המחקר הראה שהירידה המשמעותית ביותר בשיעור ההתלקחויות השנתי הייתה בחולים בהם רמת האאוזינופילים הייתה מעל 300 למיקרוליטר (67.4 אחוזים פחות התלקחויות בקבוצת ה- Dupilumab יחסית ל-Placebo, p<0.001), אך גם במטופלים שספירת האאוזינופילים שלהם הייתה בין 150 ל־300, נמצאה הפחתה ניכרת בתדירות ההתלקחויות (44.3 אחוזים הורדה בשיעור ההתלקחויות). עם זאת, בקבוצת המטופלים עם ספירת אאוזינופילים נמוכה מ־150 תאים למיקרוליטר, לא נמצא הבדל משמעותי בין קבוצת הטיפול ב-Dupilumab לבין קבוצת ה-Placebo. בניתוח התוצאות לפי רמת ה-FeNO של המטופלים, נמצא כי הירידה בשיעור ההתלקחויות הייתה משמעותית סטטיסטית בחולים להם רמת ה-FeNO הייתה מעל ppb 25 . מחקר ה-VENTURE (Evaluation of Dupilumab in Patients With Severe Steroid Dependent Asthma)[23] בדק את השפעת Dupilumab על הפחתת מינון ה-OCS בחולי אסתמה חמורה התלויים ב-OCS. המחקר הדגים ירידה של 70 אחוזים במינון ה-OCS בקבוצת ה-Dupilumab לעומת ירידה של 41.9 אחוזים בקבוצת הPlacebo (p<0.001). במקביל לירידה במינוני ה-OCS, נמצא כי שיעור ההתלקחויות השנתי בקבוצת ה-Dupilumab היה נמוך ב-59 אחוזים משיעור ההתלקחויות הקשות בקבוצת ה-Placebo (0.001>P), וכן כי ה-FEV1 היה גבוה יותר ב-220 מיליטרים בקבוצת ה-Dupilumab[23].
טבלה 1 - ריכוז טיפולים ביולוגיים לטיפול באסתמה חמורה
| Omalizumab | Mepolizumab | Reslizumab | Benralizumab | Dupilumab | |
|---|---|---|---|---|---|
| שם מסחרי | Xolair | Nucala | Cinqair | Fasenra | Dupixent |
| יצרן | Novartis | GSK | Teva | Asrtazeneca | Sanofi |
| מנגנון פעילות | Anti IgE | Anti IL-5 | Anti IL-5 | Anti IL-5Rα | Anti IL-4Rα |
| מינונים | בהתאם לרמת IgE ומשקל המטופל | 100 מיליגרמים | 3 מיליגרמים לקילוגרם | 30 מיליגרמים | 300 מיליגרמים |
| אופן הזרקה | תת-עורי | תת-עורי | תוך ורידי בעירוי למשך 20–50 דקות | תת-עורי | תת-עורי |
| תדירות הזרקה | אחת לשבועיים או אחת ל-4 שבועות, בהתאם למינון | 4 שבועות | 4 שבועות | 8 שבועות (ב־3 ההזרקות הראשונות כל 4 שבועות) | פעם בשבועיים (בטיפול הראשון מינון כפול) |
| גיל | 6 ומעלה | 12 ומעלה | 18 ומעלה | 18 ומעלה | 12 ומעלה |
ביבליוגרפיה
- ↑ 1.0 1.1 Chung, K. F et. al. "International ERS/ATS guidelines on definition, evaluation and treatment of severe asthma." Eur. Respir. J 2014 ;43(2): 343-373.
- ↑ 2.0 2.1 GINA. (2016). "Global Strategy for Asthma Management and Prevention 2016." www.ginasthma.org ;
- ↑ 3.0 3.1 Gauthier, M, et al Am J Respir Crit Care Med 2015;192 (6): 660-668.
- ↑ Versano S et al. Respir Med 2017:131-139
- ↑ Patterson, M. et al .J Asthma Allergy 2015; 8: 125-134 :
- ↑ Fowler S et al J All Clin Immunol 2015 822-824
- ↑ Allergy 2005:60:309-316
- ↑ Am J Respir Crit Care Med 2013 Apr 15;187(8):804-11
- ↑ Eur Respir J 2018; 51: 1702523
- ↑ J Asthma Allergy. 2018; 11: 53–61
- ↑ Hannah H et al: a US perspective Journal of Asthma and Allergy 2014:7 53-65
- ↑ 12.0 12.1 Pavord ID et al Lancet 2012 ;380, 9842:651-9
- ↑ 13.0 13.1 Ortega HG et al. NEJM 2014 371:1198-1207
- ↑ 14.0 14.1 Bel E, et al. NEJM 2014; 371: 1189-97.
- ↑ Bjermer L et al. Chest 2016;150:789-798
- ↑ Castro M et al. Lancet Respir Med. 2014 (11):879-890.
- ↑ Masselli DJ et al. Journal of Asthma and Allergy 2016:9 155-162
- ↑ Kolbeck R, et al. J Allergy Clin Immunol. 2010;125(1):1344-53
- ↑ 19.0 19.1 Bleeker ER et al. Lancet. 2016 Oct 29;388(10056):2115-2127
- ↑ FitzGerald JM et al. Lancet. 2016; 388:2128-2141
- ↑ Nair et al. NEJM. 2017 ;376(25):2448-2458
- ↑ N Engl J Med 2018;378:2486-96.
- ↑ 23.0 23.1 N Engl J Med 2018;378:2475-85
המידע שבדף זה נכתב על ידי
- ד"ר דניאל בן דיין, מנהלת מחלקת ריאות, מנהלת המרכז הארצי לשחפת, מומחית לרפואה פנימית וריאות מבוגרים, בית החולים שמואל הרופא
- ד"ר אמיר בר- שי, מומחה ברפואה פנימית ולמחלות ריאה, ראש מערך רפואת הריאות במרכז הרפואי האוניברסיטאי ברזילי


 כניסה
כניסה  עקבו אחרינו בפייסבוק
עקבו אחרינו בפייסבוק