אפילפסיה עמידה בפני טיפול תרופתי - טיפול ברדיוכירורגיה - Radiosurgery for drug-resistant epilepsy
לערכים נוספים הקשורים לנושא זה, ראו את דף הפירושים – אפילפסיה
אפילפסיה היא בין ההפרעות הנוירולוגיות הנפוצות ביותר ושכיחותה באוכלוסיה הכללית היא כ-1%. ב-65-70% מהחולים ניתן להגיע לשליטה מלאה בפרכוסים בעזרת טיפול תרופתי, אולם כשליש מהחולים עמידים לטיפול. ההגדרה של עמידות לטיפול נתונה במחלוקת, אך מקובל להגדירה ככישלון להגיע לשליטה בפרכוסים למרות טיפול מיטבי (בתרופה ההולמת את סוג הפרכוסים ובמינון מספק) בשתי תרופות. במצב זה, הסיכוי לעצור את הפרכוסים בעזרת תרופה נוספת הוא קלוש (סביב 5%).
הגישה הטיפולית בעלת הסיכוי הטוב ביותר לשליטה בפרכוסים באפילפסיה ממקור מוקדי (Focal epilepsy) הינה ניתוח לכריתה של המוקד האפילפטי. לשם כך יש לבצע הערכה בה, בשלב הראשון, מאתרים את המוקד האפילפטי בעזרת ההסתמנות הקלינית של ההתקפים, בדיקת רשמת מוח חשמלית (Electroencephalography ,EEG) להערכת הפעילות האינטראיקטלית (Interictal), וידאו EEG להדגמת פעילות איקטלית (Ictal), בדיקות הדמייה כגון תהודה מגנטית (Magnetic Resonance Imaging ,MRI) של המוח בשאלה של מום מבני המהווה את המוקד האפילפטוגני (Epileptogenic) ומיפויים שונים כגון בדיקת PET (Positron Emission Tomography) ו-SPECT (Single Photon Emission Computed Tomography). בשלב הבא מעריכים את הסיכון לחסרים נוירולוגים עקב הניתוח, כגון הפרעת שפה והפרעה משמעותית בזיכרון. הערכה זו מתבצעת בעזרת מבחנים קוגניטיביים, בדיקת תהודה מגנטית תפקודית (Functional MRI) ובדיקת Wada. אם החולה נמצא מתאים לניתוח הסיכוי להפוך חופשי מפרכוסים עומד על כ-60% [כ-60-70% בחולי אפילפסיה ממקור טמפורלי (Temporal) וכ-50% בחולי אפילפסיה ממקור פרונטלי (Frontal)]. הסיכונים בניתוח פתוח, בדומה לניתוחים נוירוכירורגים אחרים, כוללים דימום, זיהום, היווצרות קריש וחסרים נוירולוגים כגון פגיעה בשדה הראייה, הפרעות שפה, הפרעות זיכרון וחולשה מוטורית. הסיכון לחסר נוירולוגי קבוע משתנה ממרכז למרכז וממנתח למנתח ונע סביב 1-3%. ניתוח פתוח מלווה לרוב בכאבי ראש משמעותיים במשך מספר ימים לאחר הניתוח. תקופת ההחלמה באשפוז נמשכת 3-4 ימים ולאחר מכן ישנה תקופת התאוששות נוספת בבית.
אם ניתוח איננו אפשרי מסיבות שונות, הסיכוי להטיב את מצב החולה בצורה משמעותית נמוך והאפשרויות הטיפוליות הן ניתוח פליאטיבי לצמצום שכיחות ההתקפים וחומרתם (כגון Corpus callosotomy), השתלת קוצבים [גירוי מוחי עמוק (DBS, Deep Brain Stimulation), קוצב וגאלי (VNS, Vagus Nerve Stimulation)], דיאטה קטוגנית ותרופות ניסיוניות.
גישות זעיר פולשניות להסרת המוקד האפילפטי מאפשרות שליטה בהתקפים בדומה לתוצאות הניתוחיות בגישה הפתוחה מחד, אך לא כרוכות בסיכונים ותופעות הלוואי הנלוות לניתוח פתוח, מאידך. גישות אלו כוללות רדיו-כירורגיה, צריבה (בחום או בקור) של המוקד האפילפטי וכן הזלפה מקומית של תרופות אנטי אפילפטיות אל המוקד האפילפטי.
אופן הטיפול
טיפול ברדיו-כירורגיה עושה שימוש בקרינה מייננת המכוונת אל המטרה המבוקשת. מקור הקרינה המייננת שונה מטכניקה לטכניקה וממכשיר למכשיר:
- Proton beam accelerator - מקור הקרינה הוא מאיץ היוצר אלומת חלקיקים (לרוב פרוטונים אך לעיתים נויטרונים)
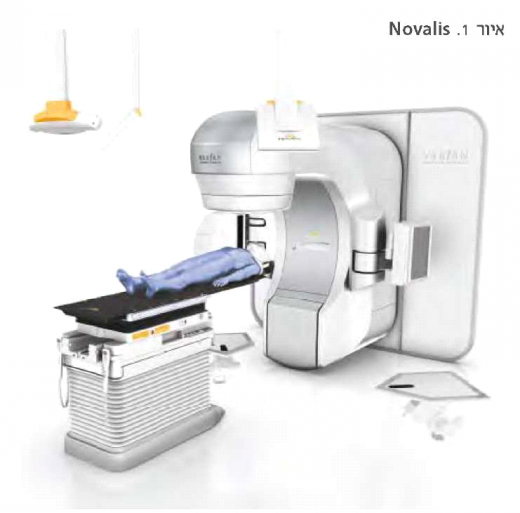
- Linear accelerator - מקור הקרינה הוא מאיץ קווי היוצר אלומת פוטונים. שיטה זו נפוצה יותר בשימוש הקליני. קיימים מכשירים שונים המבוססים על המאיץ הקווי כגון Cyber knife, Novalis ו-Gamma knife
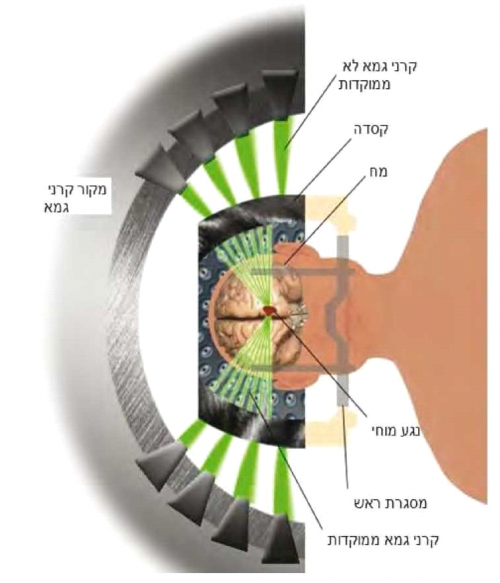
הקרינה המייננת פוגעת ב-DNA של התאים, גורמת לשבירה של קשרים כימיים במולקולה וליצירה של קשרים לא תקינים. בנוסף נוצרים רדיקלים חופשיים הפוגעים אף הם ב-DNA. שינויים אלה מובילים לפגיעה, לרוב בלתי הפיכה, ולמוות תאי (Apoptosis) או נמק (Necrosis) של התא. תאים מתחלקים רגישים יותר לנזקי הקרינה לעומת תאים ממוינים כמו תאי עצב. מחקרים שונים הדגימו כי קיים אפקט טיפולי נוסף של הקרינה על תאי העצב מעבר להרס התאים וזאת על ידי הפרעה לתפקוד התא והפרעה לתהליכים של הנצה (Sprouting) של תאי העצב המשחקים תפקיד מרכזי בתהליכי היצירה של המוקד האפילפטי. הקרינה ניתנת באלומות רבות מכיוונים שונים, המתמקדות על המטרה המיועדת להקרנה. בשל כך, מינון הקרינה שסופג האזור המיועד להקרנה גבוה בהרבה לעומת שאר רקמת המוח, הסופגת מינונים נמוכים יותר.
שימוש קליני
ההתוויות לשימוש ברדיו-כירורגיה הם:
- גידולים שפירים שאינם נגישים לכריתה ניתוחית כגון נוירומה אקוסטית (Acoustic neuroma) ומנינגיומה (Meningioma)
- גרורות
- מלפרמציות עורקיות-ורידיות (AVM, Arterio-Venous Malformation)
- הפרעות תפקודיות כגון הפרעות תנועה ונוירלגיה טריגמינלית (Trigeminal neuralgia)
במהלך השנים הצטברו עדויות רבות על ההשפעה האנטי אפילפטית של הטיפול הרדיו-כירורגי, כאשר האפילפסיה התפתחה בעקבות הנגע הראשוני שטופל ברדיו-כירורגיה לפי ההתוויה המקובלת. חולים עם מלפרמציות עורקיות-ורידיות שטופלו ברדיו-כירורגיה הדגימו ירידה של 50-80% בתדירות הפרכוסים[1]. חולים שטופלו בשל קברנומה (Cavernoma) הדגימו ירידה של 25-60% בפרכוסים[2] וחולים עם המרטומה היפופיזרית (Hypophysaire hamartoma) הדגימו 30% ירידה בתדירות הפרכוסים לאחר טיפול ברדיו-כירורגיה[3]. כל אלה הביאו לבדיקה של יעילות רדיו-כירורגיה בטיפול באפילפסיה.
Vejtech et al[4] אספו בעבודה רטרוספקטיבית 14 מקרים של חולי אפילפסיה ממקור טמפורלי על רקע טרשת מסיו-טמפורלית (MTS, Mesial Temporal Sclerosis) שטופלו ברדיו-כירורגיה עם תקופת מעקב של מעל 8 שנים. הקרינה כוונה אל האמיגדלה (Amygdala), ראש וגוף ההיפוקמפוס (Hippocampus) וכן אל החלק הקדמי של הגירוס הפרהיפוקמפלי (Pre-hippocampal gyrus). שישה מהחולים טופלו בקרינה בעוצמה של 18Gy (Grey), שני חולים בעוצמה של 20Gy ושישה טופלו בקרינה בעוצמה של 25Gy. שבעה מהחולים נזקקו לניתוח פתוח לאחר למעלה מ-3 שנים מהטיפול הרדיו-כירורגי (שלושה מהם טופלו בקרינה במינון גבוה). בחולים שלא עברו ניתוח חוזר לא הושגה שליטה בפרכוסים. ארבעה מתוך שבעת החולים שנותחו בשנית נהפכו לחופשיים מהתקפים. עבודה זו מדווחת על שיעור גבוה של סיבוכים לאחר טיפול ברדיו-כירורגיה. שלושה חולים נותרו עם חסר קבוע בשדה הראייה לאחר הטיפול, שני חולים עם חסר ברביע העליון (Quadranopsia) וחולה אחד עם חסר במחצית שדה הראייה (Hemianopsia). שני חולים פיתחו יתר לחץ תוך גולגולתי ושני חולים פיתחו פסיכוזה. בהשוואה של מינוני הקרינה נמצא כי חולים שטופלו במינון קרינה גבוה פיתחו תופעות לוואי בשיעור גבוה יותר וללא השפעה על תדירות הפרכוסים.
בעבודתם של Regis et al[5] התקבלו תוצאות טובות יותר. עבודה זו נעשתה באופן פרוספקטיבי בהשתתפות מספר מרכזים רפואיים ובה גויסו 20 חולי אפילפסיה עמידה לטיפול ממקור טמפורלי על רקע טרשת מסיו-טמפורלית. החולים טופלו ברדיו-כירורגיה במינון של 24Gy שכוונה אל האמיגדלה (Amigdalofugal complex), ראש ההיפוקמפוס וכן לחלק הקדמי של הגירוס הפרהיפוקמפלי, הקורטקס האנטורינלי (Entorhinal cortex) והחריץ הרינלי (Rhinal sulcus). לאחר הטיפול נשארו החולים במעקב במשך מעל לשנתיים. בביקור הראשון, שנערך חודש לאחר הניתוח, נצפתה ירידה בשכיחות הפרכוסים לעומת שכיחותם לפני הניתוח ואולם בביקור העוקב, חצי שנה לאחר הניתוח, נצפתה עלייה בשכיחות הפרכוסים לעומת הביקור הקודם (אך פחות משכיחותם לפני הטיפול). בהמשך המעקב נרשמה ירידה הדרגתית אך קבועה בשכיחות הפרכוסים ולאחר שנתיים של מעקב היו 65% מהחולים חופשיים מהתקפים. במבחנים הקוגניטיביים לא נראתה פגיעה בזיכרון. החולים דיווחו על שיפור במצבם המנטלי והתפקודי אך ללא שינוי במצבם הפיזי. מחצית מהחולים פיתחו הפרעות בשדה הראייה, עם חסר ברביע העליון של שדה הראייה בתשעה מהחולים וחסר במחצית שדה הראייה בחולה אחד. חולה אחד נפטר במהלך המעקב מהתקף לב שלא יוחס לטיפול הרדיו-כירורגי.
בעבודה נוספת של Barbaro et al[6] שבוצעה במתודולוגיה דומה (פרוספקטיבית, רב-מרכזית) התקבלו תוצאות דומות. למחקר זה גויסו 30 חולי אפילפסיה ממקור טמפורלי עם טרשת מסיו-טמפורלית עמידים לטיפול תרופתי. בדומה לעבודות קודמות, כוונה הקרינה אל האמיגדלה, החלק הקדמי של ההיפוקמפוס ואל הגירוס הפרהיפוקמפלי. בעבודה זו חולקו החולים באופן מקרי לשתי קבוצות. קבוצה אחת, בת 17 חולים, טופלה בקרינה במינון של 20Gy וקבוצה שנייה, בת 13 חולים, טופלה בקרינה במינון 24Gy. לאחר הטיפול היו החולים במעקב במשך מעל לשלוש שנים. גם בעבודה זו נראתה עלייה בפרכוסים המוקדיים הפשוטים (Simple partial seizures) בתקופה הראשונית של בין 5 ל-15 חודשים לאחר הטיפול, במקביל לירידה בפרכוסים חלקיים מורכבים (Complex partial seizures). לאחר תקופה זו נראתה ירידה משמעותית בשכיחות הפרכוסים בכלל החולים, אך בחולים שטופלו במינון הגבוה של הקרינה, הירידה הייתה משמעותית יותר. בתום המעקב, 67% מהחולים שטופלו בקרינה במינון הנמוך ו-77% מהחולים שטופלו במינון הגבוה של הקרינה הדגימו נסיגה מהפרכוסים (פחות מ-3 פרכוסים בשנה). ב-15% מהחולים הייתה פגיעה בזיכרון המילולי (Verbal memory).
העבודות שנעשו עד כה (נכון לשנת 2013) מציגות תוצאות סותרות ובאף אחת מהן לא בוצעה השוואה אל הניתוח הפתוח שהוא הטיפול המקובל (ה-Gold standard). בשל כך מתקיים בימים אלה ה-Rose study[7] (Radiosurgery or Open Surgery for Epilepsy). מחקר זה מתבצע במימון ה-NIH (National Institutes of Health) במספר רב של מרכזים בארה"ב, קנדה ובריטניה ונעשה באופן פרוספקטיבי וכפול סמיות (Double blind). אל המחקר יגויסו 234 חולים עם אפילפסיה ממקור טמפורלי על רקע טרשת מסיו-טמפורלית העמידה לטיפול תרופתי. החולים יחולקו לשתי קבוצות, האחת תטופל ברדיו-כירורגיה והשנייה תטופל בניתוח פתוח. תוצאות המחקר צפויות להתקבל באוגוסט 2016 ולאחר מכן ניתן יהיה להגדיר את תפקידה של הרדיו-כירורגיה בטיפול באפילפסיה עמידה.
ביבליוגרפיה
- ↑ Steiner L, Lindquist C, Adler JR, et al., J Neurosurg, 1992 ;77,1
- ↑ Kim W, Stramotas S, Choy W, et al., J Clin Neurosci, 2011;18,877
- ↑ Frazier JL, Goodwin CR, Ahn ES, et al., Childs Nerv Syst, 2009;25,423
- ↑ Vojtech Z, Vladyka V, Kalina M et al., Epilepsia, 2009;50,2061
- ↑ Regis J, Rey M, Bartolomei F et al., Epilepsia, 2004;45,504
- ↑ Barbaro NM, Quigg M, Broshek DK et al., Ann Neurol, 2009;65,167
- ↑ http://epilepsysurgery-rosetrial.com
קישורים חיצוניים
המידע שבדף זה נכתב על ידי
ד"ר שמואל אפל, המחלקה לנוירולוגיה, המרכז הרפואי ע"ש שיבא, תל השומר ובית הספר לרפואה ע"ש סאקלר, אוניברסיטת תל-אביב.
ד"ר אילן בלט, המחלקה לנוירולוגיה, המרכז הרפואי ע"ש שיבא, תל השומר ובית הספר לרפואה ע"ש סאקלר, אוניברסיטת תל-אביב.
ד"ר רוברטו שפיגלמן, המחלקה לנוירוכירורגיה, המרכז הרפואי ע"ש שיבא, תל השומר ובית הספר לרפואה ע"ש סאקלר, אוניברסיטת תל-אביב


 כניסה
כניסה  עקבו אחרינו בפייסבוק
עקבו אחרינו בפייסבוק