דלקת מפרקים ניוונית - טיפול בתוספי תזונה - Osteoarthritis - treatment with nutritional supplements
| טיפול בתוספי תזונה בדלקת מפרקים ניוונית | ||
|---|---|---|
| nutritional supplements as a treatment for osteoarthritis | ||
| יוצר הערך | ד"ר אמיר אורון, ד"ר רונן דבי, ד"ר יפתח בר, ד"ר נחום הלפרין, ד"ר גבריאל אגר 
|
|
לערכים נוספים הקשורים לנושא זה, ראו את דף הפירושים – אוסטאוארתריטיס
מבנהו הייחודי של הסחוס המפרקי (Articular cartilage) מאפשר לו לתפקד כמשטח בעל מקדם חיכוך נמוך, עם יכולת מצוינת לספיגה ופיזור של זעזועים ועמידות רבה בפני כוחות גזירה (Shear stresses). הסחוס המפרקי מורכב בעיקר מרקמת המשתית החוץ-תאית (Extracellular matrix) שבתוכה פזורים תאי סחוס. במפרק האנושי קיים איזון עדין בין כוחות הגורמים להרס הסחוס המפרקי לבין גורמי גדילה (Growth factors) הפועלים לשיקומו. הפגיעה בסחוס המפרקי יכולה להיות ממוקדת, או מפושטת - בדמות דלקת מפרקים ניוונית (Osteoarthritis). תרכובות המכילות Glucosamine ו-Chondroitin, הנמכרות כתוספי תזונה מגיני סחוס, הן חלק מאפשרויות הטיפול בדלקת מפרקים ניוונית, זוכות לתשומת לב ציבורית והיוו מוקד למחקרים שתוצאותיהם פורסמו לאחרונה. נראה, כי בטיפול בחולים הסובלים מדלקת מפרקים ניוונית, יש מקום לבצע ניסיון טיפולי בן שלושה חודשים לפחות בתוספי תזונה מגני סחוס המכילים Glucosamine ו- Chondroitin.
מבנה הסחוס המפרקי
מבנהו הייחודי של הסחוס המפרקי מאפשר לו לתפקד כמשטח בעל מקדם חיכוך נמוך, עם יכולת מצוינת לספיגה ופיזור של זעזועים ועמידות רבה בפני כוחות גזירה. במרבית המפרקים הסינוביאליים (Synovial joints) בגופנו מספק הסחוס תכונות ביומכניות אלו למשך שמונה עשורים ויותר. אף חומר סינתטי שנוסה עד היום, לא הצליח להחליף את המשטח המפרקי מכוסה הסחוס בצורה טובה. נסקור כאן את התובנות החדשות על מבנהו של הסחוס המפרקי, משמעותן הקלינית והטיפול בתוספי תזונה מגיני סחוס, כגון Glucosamine ו- Chondroitin.
הסחוס המפרקי מורכב בעיקר מרקמת המשתית החוץ-תאית שבתוכה פזורים תאי סחוס (כונדרוציטים). המרכיבים העיקריים של המשתית החוץ-תאית הם מים, פרוטאוגליקנים (Proteoglycans) ומולקולות קולגן. רכיבים אלו עם חלבונים וגליקופרוטאינים (Glycopeptides) נוספים מקנים לסחוס את תכונותיו הייחודיות.
האזורים השונים בסחוס
מבנהו ומרכיביו של הסחוס משתנים בהתאם לעומק: מהמשטח המפרקי ועד לעצם התת-סחוסית (Subchondral). ניתן לחלק את הסחוס לארבעה אזורים: האזור השטחי, האזור המרכזי או אזור המעבר, האזור העמוק והאזור של הסחוס המסויד (Calcified cartilage).
האזור השטחי הוא זה שיוצר את משטח ההחלקה בין שני חלקי המפרק. סיבי הקולגן מסודרים במקביל למשטח המפרקי ותאי סחוס מאורכים ופחוסים מסודרים אף הם במקביל למשטח זה. תכולת הפרוטאוגליקנים באזור זה היא הנמוכה ביותר, בעוד שתכולת המים היא הגבוהה ביותר. האזור המרכזי, או אזור המעבר, מכיל סיבי קולגן שפזורים בלא סידור מרחבי מוגדר ובתוכו נעוצים תאי סחוס בעלי מראה עגול. בעבר נטען כי אזור זה מאופיין במבנה מרחבי מוגדר של קשתות העולות אל פני הסחוס מעומק המשטח, אך טענה זאת הופרכה. האזור העמוק מאופיין בסיבי קולגן רחבים שמסודרים במאונך למשטח המפרקי. הוא מכיל את הריכוז הגדול ביותר של פרוטאוגליקנים ותכולת המים בו היא הנמוכה ביותר. באזור זה תאי הסחוס סגלגלים בצורתם ומסודרים בעמודות. האזור העמוק ביותר, זה של הסחוס המסויד, מהווה חיץ בין הסחוס ההיאליני (Hyaline cartilage) לבין העצם התת-סחוסית. הוא מאופיין בתאים קטנים הפזורים במשתית הזרועה במוקדי שקיעה של מלחי סידן. בצביעה היסטולוגית בהמטוקסילין ואאוזין (Haematoxylin and eosin staining) נראה קו תכול גלי הקרוי קו הגאות (Tidemark), המפריד בין האזור העמוק לזה של הסחוס המסויד.
מבנה המשתית הסחוסית
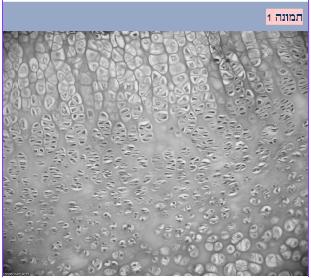
יצירת המשתית החוץ-תאית ותחזוקתה תלויים בתאי הסחוס. המשתית החוץ-תאית הסמוכה לתא הסחוס נקראת המשתית הפריצלולרית (Pericellular matrix). אזור זה מכיל כמעט אך ורק פרוטאוגליקנים ואינו מכיל סיבי קולגן. את אזור המשתית הפריצלולרית הצמודה לתאי הסחוס, מקיף אזור המשתית הטריטוריאלית (Territorial matrix). המשתית הטריטוריאלית מאופיינת בסיבי קולגן דקים שיוצרים רשת מקומית המבודדת מרשת סיבי הקולגן, המרכיבה את המשתית הבין-טריטוריאלית (Interterritorial matrix). המשתית הבין-טריטוריאלית היא חלק הארי של הסחוס המפרקי, והיא שמקנה לסחוס את תכונותיו. היא מכילה בתוכה סיבי קולגן, הפרושים ברשת סבוכה ועבה. בין סיבי הקולגן לכודות מולקולות של פרוטאוגליקנים, המקנים לסחוס את תכונותיו המיוחדות. תאי הסחוס פעילים מאוד מבחינה מטבולית ומגיבים למגוון רחב של גירויים סביבתיים. בתנאי עקה (Stress) תאי הסחוס עוברים לייצור מוגבר של מרכיבי הסחוס כדי לנסות ולמנוע או אף לתקן פגיעות במשתית הסחוס המפרקי. (תמונה 1).
רכיבי המשתית הסחוסית
משתית הסחוס המפרקי בנויה משני רכיבים עיקריים: מולקולות קולגן המהוות אבני בניין לסיבי הקולגן, המרכיבים יחדיו רשת סבוכה, ומולקולות של פרוטאוגליקנים הלכודים בינות לסיבי רשת הקולגן. קולגן מסוג II שיעורו כ-95% מסך הקולגן, אך המשתית הסחוסית מכילה גם קולגן מסוג 5, 6, 9, 10 ו-11. סיבי הקולגן מקנים למשתית הסחוסית את עמידותה בפני עומסים ישירים וכוחות גזירה. סיבי הקולגן בנויים משרשראות מסוג אלפא. שלוש שרשראות מסוג זה, המחוברות יחדיו במבנה של סליל משולש (Triple helix), מהוות מולקולת קולגן בודדת. סיב קולגן מורכב ממספר מולקולות קולגן הסדורות במבנה שלישוני שבו כל מולקולה מסודרת במרחב ברבע סיבוב לעומת קודמתה בסיב. בין סיבי הקולגן נוצרים קשרים קוולנטיים התורמים ליציבות המבנה המרחבי ומסייעים בקיבוע הפרוטאוגליקנים במרחב. הפרוטאוגליקנים הם חומרים המורכבים, כמשתמע משמם, מגרעין מרכזי הבנוי חלבון אשר אליו קשורות שרשרות מרובות סוכרים (גליקוזאמינוגליקנים). הגליקוזאמינוגליקנים מורכבים ממולקולות די-סכרידים (Disaccharide). יש חמישה סוגי גליקוזאמינוגליקנים: Chondroitin sulfate, Hyaluronan, Keratan sulfate, Heparan sulfate ו- Dermatan sulfate. ה- Chondroitin sulfate הוא הנפוץ ביותר מבין השלושה, ולו שני איזומרים - 4 ו-6 סולפט. היחס בין שני איזומרים אלו משתנה עם הגיל וכן במפרק הסובל משינויים דלקתיים.
פגיעות סחוס
הסחוס האנושי חשוף לפגיעה במשך כל חיינו, ועליו לעמוד בלחצים ובכוחות מגוונים. במפרק האנושי קיים איזון עדין בין כוחות הגורמים להרס הסחוס המפרקי, לבין גורמי גדילה הפועלים לשיקומו. גורמי הגדילה השכיחים הם: גורם גדילה דמוי אינסולין (Insulin-like growth factor), גורם גדילה המופק מטסיות (Platelet derived growth factor) וכן גורם גדילה ממיר בטא (Transforming growth factor beta). גורמי ההרס הטיפוסיים הם אינטרלוקינים, הנוצרים בסחוס המפרקי וברקמה הסינוביאלית העוטפת את המפרק, וכן הורמונים הפועלים בצורה מקומית בסחוס כמו פרוסטגלנדינים וחנקן חמצני (Nitric oxide).
להרס הסחוס הממוקד תהליך אופייני שבא לידי ביטוי הן בבדיקה הקלינית המבוצעת בארתרוסקופיה, והן בהביטנו אל הרקמה כיחידה היסטולוגית.
כדי להקל את הבנת התהליכים המתרחשים ברקמת הסחוס כאשר היא נפגעת, ניתן לדמות את רקמת הסחוס לספוג רחצה פשוט העטוף ברשת מתכת. הפרוטאוגליקנים המרכיבים את רקמת הסחוס הם היגרוסקופיים (Hygroscopic) מאוד (בעלי נטייה לספוח מים, כמו ספוג) בעוד סיבי הקולגן, המרכיבים את השלד של רקמת הסחוס, מונעים מהפרוטאוגליקנים למצות את פוטנציאל ספיחת המים שלהם, בדומה לרשת הברזל העוטפת את הספוג.
בשלב ראשון נהרס מערך סיבי הקולגן, המרכיב את רקמת הסחוס, וכך יכולים הפרוטאוגליקנים למצות את פוטנציאל ספיחת המים שלהם. בשלב זה הסחוס נראה שמור מבחינה ארתרוסקופית, אך הוא רך למגע. ייתכן שבשלב זה תהיה הרחבה פרדוקסלית של המרווח המפרקי בשל ספיחת המים על ידי הסחוס. השלב השני בהרס הסחוס המפרקי מוגדר כהופעת בקיעים במשטח הסחוסי. לסחוס אובדת בשלב זה חלק מיכולתו לעמוד בפני פגיעות מכניות וכוחות גזירה. בדומה לספוג שאינו מוגן עוד על ידי רשת המתכת העוטפת אותו, כך גם משתית הסחוס הפגועה, שמכילה פרוטאוגליקנים רוויים במולקולות מים, חשופה לכוחות הגורמים לאותם בקיעים במשטח הסחוסי (Fissuring).
השלב השלישי במהלך הרס הסחוס הוא כאשר הפגיעה במשתית הופכת קשה יותר והרקמה הופכת פריכה. בשלב זה מופיעים שרכי רקמת סחוס בארתרוסקופיה (Fraying). שלב זה ניתן לאבחון בקלות בארתרוסקופיה ויש לו מראה אופייני.
השלב הרביעי והאחרון במהלך הרס הסחוס הוא הרס מוחלט של רקמת הסחוס והופעת רקמת עצם חשופה (Eburnated bone). בשלב זה העצבים המצויים בעצם התת-סחוסית חשופים לכוחות המכניים הפועלים במפרק, ולעתים קרובות תנועת המפרק תלווה בכאב עז. ארבעת השלבים שתוארו לעיל, מאפיינים הן הרס סחוסי ממוקד והן הרס סחוסי מפושט בדמות דלקת מפרקים ניוונית, הגם שדלקת מפרקים ניוונית אינה מתאפיינת במעבר ברור בין השלבים.
דלקת המפרקים הניוונית היא מחלה האופיינית לגיל הזהב. הארכת תוחלת החיים הצפויה בעולם המערבי תביא לעלייה דרמטית בתחלואה בדלקת מפרקים ניוונית, ועד לשנת 2020 היא צפויה להיות המחלה הרביעית בחומרתה כגורם לנכות ולמוגבלות. הסימנים הרנטגניים האופייניים לדלקת מפרקים ניוונית הם היצרות המרווח המפרקי, דחיסות עצם תת-סחוסית, הופעת כיסיות (ציסטות) והימצאות בליטות גרמיות (אוסטאופיטים). אין התאמה בין הממצאים הרנטגניים לאלו הקליניים. עם התקדמות הגיל שכיחות הימצאות השינויים הרנטגניים עולה בהתמדה, ומעל גיל 65 אחוז האנשים שבהם מודגמים שינויים אלו יכול להגיע ליותר מ-85%, ובה בעת מופיעה התסמונת הקלינית באחוזים נמוכים יותר.
הטיפול בתוספי תזונה מגני סחוס
הטיפול בדלקת מפרקים ניוונית נחלק לטיפול שמרני וניתוחי. הטיפול השמרני נחלק אף הוא לטיפול שמטרתו למנוע את החמרת המחלה, ולטיפולים שנועדו לאפשר לחולים להתמודד עם תסמיניה (הסימפטומים) הקליניים של המחלה ביתר קלות. הטיפול המונע את החרפת המחלה ממוקד בשינוי אורחות החיים של הסובלים מדלקת הפרקים הניוונית וכולל ירידה במשקל, שימוש בהנעלה ובמדרסים מתאימים, היעזרות במחוכים ובמכשירי עזר, דוגמת מקל הליכה, פעילות גופנית מבוקרת ופיזיותרפיה. הטיפולים שנועדו לסייע לחולים להתמודד עם תסמיניה הקליניים של המחלה, הם תרופתיים בעיקר וכוללים תרופות נוגדות דלקת ומשככות כאב, הזרקות מקומיות של חומרים שונים, וכן מריחת משחות או שימוש באגדים (תחבושות) המכילים חומרים פעילים שונים.
טיפול בתרכובות המכילות Glucosamine ו- Chondroitin, זוכה לתשומת הלב הציבורית, ומהווה מוקד למחקרים שתוצאותיהם פורסמו לאחרונה. תרכובות המכילות Glucosamine ו- Chondroitin נמכרות כתוספי תזונה שלהם נודע תפקיד בטיפול בדלקת מפרקים ניוונית. תוספי תזונה אלו זכו לפרסום רב בקרב הציבור הרחב כאמצעי טיפול יעיל ובטוח לטיפול בתסמינים של דלקת מפרקים ניוונית.
מטה-אנליזה של מחקרים שבוצעו לצורך הערכת יעילות השימוש בתוספי תזונה אלו העידה על פוטנציאל טיפולי, אך העלתה את הצורך במחקרים גדולים ומבוקרים נוספים. מחקר ה-GAIT (Glucosamine/chondroitin arthritis intervention trial) בא לענות על שאלת יעילות הטיפול המשולב ב- Glucosamine ו- Chondroitin בכאבי ברכיים הנובעים מדלקת מפרקים ניוונית תוך שימוש בכלים מדעיים מקובלים והיצמדות לעקרונות ביצוע מחקר רב מרכזי, כפול-סמיות, מבוקר ואיכותי.
תוספי תזונה מגיני סחוס מוגדרים כחומרים שלהם תכונות התורמות להאטת תהליכי דלקת הפרקים הניוונית ולהאצת תהליכי השיקום של המשתית הסחוסית והנוזל הסינוביאלי. Glucosamine ו-Chondroitin הם למעשה אבני הבניין של הסחוס המפרקי (כמפורט לעיל), ואם נתייחס לדברים כפשוטם, נוכל לומר כי במצבי עקה יש מקום להעשיר את תאי הסחוס ה"סובלים" באבני בניין ככל שנוכל כדי שיוכלו להתמודד עם ה"משא" הכבד של גופנו. אך אין הדברים פשוטים כלל ועיקר, ול-Glucosamine ו-Chondroitin נודעות השפעות מעבר להיותם אבני בניין של המשתית הסחוסית בלבד.
Glucosamine
ה-Glucosamine מיוצר על ידי תאי הסחוס ממולקולות הגלוקוז, ומתן תוספת חיצונית שלו מהווה, כאמור, אבן בניין נוספת לסחוס הסובל, מבלי שיצטרך להשקיע אנרגייה ביצירת ה- Glucosamine מגלוקוז. עם זאת, ל- Glucosamine כמגן סחוס תפקיד נוסף לתפקידו המבני, ומספר עבודות הדגימו כי הוא מעודד יצירת פרוטאוגליקנים וקולגן על ידי תאי הסחוס וכן יכול לעודד פרוליפרציה של תאי הסחוס בתרביות תאים. Gouze וחב' הדגימו לאחרונה כי ל- Glucosamine יכולת אנטי-דלקתית משמעותית, ולתפישתם, יכולתו של ה- Glucosamine לגרום לעיכוב של פעילות האינטרלוקין 1-בטא כגורם דלקת, היא הסיבה העיקרית ליעילותו הקלינית.
Chondroitin
תרכובת זו היא הגליקוזאמינוגליקן הנפוץ ביותר בסחוס המפרקי. כגליקוזאמינוגליקן, חשיבותו נודעת בשל תפקידו המבני בייצוב הקשר עם רשת סיבי הקולגן שבה שזורים הפרוטיאוגליקנים. עם זאת, כתוסף תזונה מגן סחוס, יש לו גם תפקיד מטבולי. ה-Chondroitin הוא מעכב תחרותי לרבים מהאנזימים הקטבוליים שמפרקים את המשתית הסחוסית ואת הנוזל המפרקי בדלקת מפרקים ניוונית. כך, השימוש ב-Chondroitin יכול להשיב את שיווי המשקל בין תהליכי ההרס לבנייה בסחוס המפרקי. ל-Chondroitin ידועה גם השפעה אנטי-דלקתית, השפעה המעכבת מוות תאי והשפעה על שינויים מבניים בעצם התת-סחוסית. מחקרי מנגנון רבים מדגימים את האגבור (סינרגיזם) בשימוש בשילוב של Glucosamine ו-Chondroitin הן במבחנה (In vitro) והן בחיים (In vivo).
טיפול משולב ב-Glucosamine ו-Chondroitin
האמונה הרווחת בקרב ציבור הרופאים המטפלים בדלקת הפרקים הניוונית היא כי קיים חסר הן ב-Glucosamine והן ב-Chondroitin בנוזל המפרקי בחולים, חסר שלו ביסוס מדעי, וכי החסר המקומי במרכיבי המפתח הטבעיים המרכיבים את הסחוס האנושי ניתן לטיפול על ידי העשרת האספקה של חומרים אלו לגופנו על ידי תוספי תזונה. אמונה זאת מייחסת לתוספים אלו השפעה על תסמיני המחלה (כאב, נוקשות ותפקוד המפרק) וכן יכולת למנוע את התקדמות המחלה (למעשה, האטת תהליך ההתקדמות של דלקת הפרקים הניוונית). לשימוש בשני חומרים אלו יחדיו במינון מתאים נודעת השפעה אגבורית (סינרגיסטית) שבאה לידי ביטוי אף במחקר ה-GAIT.
Glucosamine ו-Chondroitin הם תוספי התזונה הנפוצים ביותר המשמשים כטיפול בדלקת מפרקים ניוונית. מחקר ה-GAIT בוצע מתוך מטרה להעריך את היעילות והבטיחות של השימוש בחומרים אלו במחלת מפרקים ניוונית של הברך, עקב תפוצתם הנרחבת. מחקר זה של Clegg וחב' תוכנן כמחקר רב מרכזי, כפול-סמיות. הן אינבו (Placebo) והן טיפול ב- Celecoxib שימשו כביקורת. במסגרת עבודה זאת שזכתה למימון ה-NIH (National institutes of health) האמריקאי, חולקו 1,583 חולים שסבלו ממחלת פרקים ניוונית תסמינית בברכיהם, לחמש קבוצות. גילם הממוצע של החולים היה 59 שנה ו-64% מתוכם היו נשים. קבוצה אחת טופלה ב-1,500 מ"ג Glucosamine מדי יום, שנייה ב-1,200 מ"ג Chondroitin sulfate מדי יום, שלישית בשני חומרים אלו גם יחד מדי יום, רביעית ב-200 מ“ג Celecoxib (נוגד דלקת לא סטרואידי (NSAID) מקבוצת ה-COX2) מדי יום וחמישית באינבו מדי יום. משך המעקב היה עשרים וארבעה שבועות ו- Acetaminophen עד 4,000 מ"ג מדי יום הוגדר כמשכך כאב לעת מצוא.
החולים השתייכו לשתי קבוצות: האחת (1,229 חולים) שבה נכללו אלו שסבלו מכאבי ברכיים שהוגדרו כקלים, והשנייה (354 חולים) שבה נכללו אלו שסבלו מכאבי ברכיים שהוגדרו כבינוניים עד קשים. מדד ההצלחה הראשי לטיפול היה ירידה בת 20% לפחות במידת הכאב לאחר עשרים וארבעה שבועות של טיפול. בהתייחס לכלל אוכלוסיית משתתפיו, תוצאות מחקר זה הצביעו על שיעור הצלחה של 60.1% לטיפול באינבו, ו-66.6% הצלחה לטיפול המשולב ב- Glucosamine ו- Chondroitin (ללא משמעות סטטיסטית, p=0.09). שיעורים נמוכים יותר ושאינם בעלי משמעות סטטיסטית נמצאו בטיפול בכל אחד ממרכיבים אלו בזכות עצמו. טיפול ממושך בן 24 שבועות הוביל לשיעורי הצלחה של 70.1% בטיפול ב- Celecoxib (מובהק סטטיסטית, p=0.008). בקרב החולים שסבלו מכאב ברכיים שהוגדר כבינוני עד קשה בתחילת המחקר, נמצא שיעור הצלחה גבוה באופן משמעותי לטיפול המשולב ב-Glucosamine ו-Chondroitin לעומת הטיפול באינבו - 79.2% לעומת 54.3% (p=0.002). מסקנת החוקרים הייתה כי הטיפול ב-Glucosamine וב-Chondroitin sulfate במשולב, או כל חומר בפני עצמו, לא הובילה לשיכוך כאב יעיל בכלל אוכלוסיית החולים, אך עם זאת, ייתכן כי טיפול משולב ב-Glucosamine ו-Chondroitin בקרב קבוצת החולים הסובלים מכאבי ברכיים המוגדרים כבינוניים עד קשים הוא יעיל. הביקורת העיקרית לגבי מחקר זה היא שיעור גבוה מהצפוי של יעילות האינבו במדד העיקרי (60.1%), שמקשה על הסקת מסקנות ברורות, והכללת מטופלים רבים (71%) בדרגה קלה של המחלה.
אחד המחקרים המרשימים ביותר, פורסם לאחרונה ע"י Kahan וחב' - מחקר STOPP (Osteoarthritis progression prevention). מחקר זה בדק את ההשפעה ארוכת הטווח של Chondroitin לעומת אינבו על שינויים רדיוגרפיים במפרק הברך ועל השינויים בתסמינים הנובעים מדלקת מפרקים ניוונית. במחקר השתתפו 622 מטופלים מאירופה ומארה“ב, בגילאים 80-40 הסובלים מדלקת מפרקים ניוונית. הקריטריונים להכללה כללו בין השאר מרווח מפרקי של 1 מ“מ לפחות בכניסה למחקר, ולפיכך המטופלים היו צפויים להיצרות משמעותית וניתנת למדידה. כמו כן, נבחרו רק מטופלים עם שינויים במשטח המדיאלי של מפרק הברך. התכנון הנכון וצמצום ההטרוגניות איפשרו אומדן הבדלים רדיולוגיים בתקופה המוגבלת של המחקר. התוצאות הראו שנטילת Chondroitin למשך שנתיים יכולה למנוע דגרדציה של מבנה המפרק אצל מטופלים עם דלקת מפרקים ניוונית של הברך. כמו כן, הודגם שיפור מהיר יותר בכאב בברך בקבוצת ה- Chondroitin בהשוואה לאינבו בין החודש הראשון לחודש התשיעי למחקר (p<0.01 על סמך מדדי VAS (Visual analogue scale) ו- WOMAC (Western ontario and mcmaster university index of osteoarthritis)).
סיכום הטיפול בתוספי תזונה בדלקת מפרקים ניוונית
מבנהו המרחבי המורכב של הסחוס ההיאליני ורכיביו השונים עושים אותו לבעל תכונות פיזיקליות ייחודיות כל כך. לפגיעות הסחוס הממוקמות והנרחבות במפרקים נודעת השפעה מכרעת על איכות החיים והתפקוד היום-יומי, ופתולוגיות אלו מלוות בעלות כלכלית משמעותית . מחקרים שפורסמו בשנים האחרונות מצאו כי לתוספי התזונה מגני הסחוס תפקיד חשוב בהקלת תסמיני דלקת הפרקים הניוונית. ממצאי מחקר ה-GAIT הראו כי בחולים הסובלים מכאבי ברכיים המוגדרים כבינוניים עד קשים הטיפול המשולב ב-Glucosamine ו-Chondroitin נמצא יעיל, אך בחולים שסבלו מכאבי ברכיים המוגדרים כקלים, ממצאי המחקר לא היו חד-משמעיים.
נראה כי בטיפול בחולים הסובלים מדלקת מפרקים ניוונית, יש מקום לבצע ניסיון טיפולי בן שלושה חודשים לפחות בתוספי תזונה מגני סחוס המשלבים Glucosamine (לפחות 1,500 מ"ג ליום) ו- Chondroitin (לפחות 1,200 מ"ג ליום). אם יש שיפור בתסמיני המחלה במשך תקופת הטיפול, יש מקום להמליץ על המשך הטיפול בחומרים אלו, אך אם לא נרשם שיפור, לא נראה כי יש מקום להמשיך בטיפול זה מעבר לשלושה חודשים. לסיכום, לאור הפוטנציאל הגלום בטיפול בתוספי התזונה מגיני הסחוס, תופעות הלוואי המועטות הכרוכות בשימוש בהם, והרצון למצות את כלל אמצעי הטיפול השמרניים בחולים אלו בטרם פונים לטיפול ניתוחי, מקומם של תוספי התזונה מגני הסחוס כאמצעי טיפולי מן השורה הראשונה נותר איתן.
ביבליוגרפיה
קישורים חיצוניים
המידע שבדף זה נכתב על ידי ד"ר אמיר אורון, ד"ר רונן דבי, ד"ר יפתח בר, ד"ר נחום הלפרין, ד"ר גבריאל אגר


 כניסה
כניסה  עקבו אחרינו בפייסבוק
עקבו אחרינו בפייסבוק