האינסולין טוג'או לטיפול בחולי סוכרת
ערך זה נמצא בבדיקה ועריכה על ידי מערכת ויקירפואה, וייתכן כי הוא לא ערוך ומוגה.
| טוג'או - אינסולין אולטרה-ארוך חדש ויעיל לחולי סוכרת מסוג 1 ו-2 | ||
|---|---|---|
| Toujeo | ||
| יוצר הערך | ד"ר רננה שור | |
ייצור אינסולין בלבלב חיוני לשמירה על רמות תקינות של סוכר בדם ועל ספיגתו וניצולו ברקמות שריר ושומן לאחר ארוחות, ובמקביל מווסת אינסולין את ייצור הסוכר על ידי הכבד בזמן צום (gluconeogenesis). באנשים בריאים, קיימת הפרשה בסיסית (בזאלית) של אינסולין מתאי הבטא בלבלב בזמן צום וכן עלייה חדה ברמות האינסולין המתרחשת לאחר הארוחות. בקרב חולי סוכרת, הפרשת האינסולין מהלבלב אינה מספקת בעקבות הרס של תאי בטא בלבלב (סוכרת מסוג 1) או בשל הידרדרות הדרגתית בתפקוד תאי הבטא על רקע של תנגודת לאינסולין (סוכרת מסוג 2). על כן, מטרת הטיפול בסוכרת היא לאזן את רמות הסוכר תוך צמצום תופעות הלוואי כמו סיכון להיפוגליקמיה.
מקומו של האינסולין הבזאלי בפרוטוקול הטיפולי הוא לספק את רמת האינסולין הבסיסית המופרשת מהלבלב בזמן צום. לרוב, הטיפול באינסולין באזלי ניתן בשילוב עם תרופות נוספות שמטרתן להפחית את רמות הסוכר לאחר הארוחות ו/או להגביר את הרגישות לאינסולין [1].
על פי ההנחיות הטיפוליות של המועצה הלאומית לסוכרת שהתפרסמו ב-2016 [2], הקו הראשון בטיפול בסוכרת היה ונותר שינוי באורח החיים בשילוב עם מטפורמין, וכאשר רמת ההמוגלובין המסוכרר גבוהה מ-7.5%, יש לשקול שילוב עם תרופות נוספות, וברמת המוגלובין מסוכרר מעל 9% או במטופל תסמיני, יש לשקול מתן אינסולין.
ע"פ ההנחיות, אינסולין בזאלי ניתן כקו טיפול שלישי לחולים שלא הצליחו להגיע ליעד המטרה בשילוב של מטפורמין ושתי תרופות נוספות [2].
אינסולין בזאלי בראי ההיסטוריה
אינסולין NPH נכנס לשימוש בשנת 1946 כאשר לרוב נדרש מתן דו יומי בגלל משך הפעולה הקצר שלו (עד 12 שעות). פרופיל הפעולה של NPH הראה פיק משמעותי כארבע שעות לאחר ההזרקה ועל כן שימוש בו היה כרוך בסיכון גבוה להיפוגליקמיה ובתנודות משמעותיות ברמות הסוכר לאורך היממה. בשנת 2000 נכנס לשימוש אינסולין לנטוס - אינסולין בזאלי ארוך פעולה שפרופיל הפעולה הפרמקולוגי שלו היה שטוח ביחס ל-NPH ובעל משך פעולה ארוך משמעותית (כ-24 שעות), דבר שאפשר את הזרקתו החד יומית. בהשוואה ל-NPH, לנטוס הפחית באופן משמעותי את שיעור ההיפוגליקמיות הליליות ובמשך כל היום, והדבר הפך אותו לאחת התרופות הנמכרות בכל הזמנים.
למרות יעילותה של לנטוס ואחר כך גם זו של לבמיר שנכנסה לשימוש כאינסולין בזאלי, עדיין מתקשים רבים ממטופלי הסוכרת להגיע לאיזון וליעד המטרה של ההמוגלובין המסוכרר ועדיין קיימים אירועי היפוגליקמיה הן לילית והן לאורך שעות היום. המטופלים נדרשים להקפיד על זמני הזרקה קבועים פחות או יותר וגם הגבלה זו גורמת הרבה פעמים לבעיות לוגיסטיות לא פשוטות למטופלים. כמענה לבעיות אלו נכנסו לאחרונה לשוק הדור הבא של האינסולינים הבזאליים האולטרא ארוכים: טרגלודק וטוג'או. בסקירה זו נרחיב את הדיבור על טוג'או.
יתרונותיו של האינסולין טוג'או
טוג'או (Toujeo) הוא אינסולין אולטרה-ארוך, המבוסס על פורמולציה של מולקולת הגלרג'ין. לטוג'או מספר יתרונות ביחס ללנטוס.
שיפור בתכונות הפרמקוקינטיות והפרמקודינמיות (PK/PD) של התרופה - בדומה ללנטוס, המגיע בפורמולציה בעלת PH חומצי, גם טוג'או יוצר משקע תת עורי במגע עם ה-PH הפיזיולוגי (PH 7.4). אולם, בניגוד ללנטוס, שטח הפנים של המשקע בטוג'או קטן בחצי, דבר המאפשר שחרור איטי יותר מן הצבר אל הדם.
הדבר אושר במחקרים פרמקוקינטים ופרמקודינמים (PK/PD) שהראו כי פרופיל הפעולה של טוג'או שטוח יותר בהשוואה ללנטוס, עם משך פעולה ארוך יותר שמכסה מעבר ל-24 שעות ומגיע עד 36 שעות פעילות. ממצאים אלה הובילו ליתרונות הקליניים והבטיחותיים של התרופה כפי שהודגמו במחקרי ה-EDITION. הללו בדקו מגוון אוכלוסיות: חולי סוכרת סוג 1 ו-2, מטופלים נאיביים לאינסולין והן כאלה שעברו מאינסולין בזאלי אחר ואף חולים יפנים.
היעילות והבטיחות של טוג'או בטיפול בסוכרת מסוג 2 - תכנית המחקר בסוכרת מסוג 2 כללה שלושה מחקרי phase-3 שהקיפה את מגוון החולים בסוכרת וביניהם חולים המטופלים בבזאל-בולוס (BB) (EDTION1) [2], חולים המטופלים באינסולין בזאלי בתוספת לתרופות פומיות (EDITION 2) [3], וכן חולים המטופלים בתרופות פומיות והיו נאיביים לאינסולין (EDITION 3) [4]. מחקר נוסף כלל חולים יפנים המטופלים בתרופות פומיות. בסך הכל השתתפו במחקרים 2,737 חולים בסוכרת מסוג 2 מעל גיל 18.
מחקר ה-EDITION1 כלל חולי סוכרת מסוג 2 המטופלים באינסולין בזאלי ואינסולין מהיר (BB) והראה יעילות דומה לטוג'או בהורדה של ההמוגלובין המסוכרר לאחר 6 חודשים. בנוסף, טוג'או הפחית את אחוז החולים שסבלו מהיפוגליקמיה (blood glucose≤70mg/dL) לילית (בין השעות 00:01-05:59 (ב-24% במהלך כל תקופת המחקר וב-28% במהלך תקופת הטיטרציה (8 השבועות הראשונים של המחקר).
מחקר ה-EDITION 2 כלל חולים המטופלים באינסולין בזאלי בנוסף לתרופות פומיות וגם במחקר זה התקבלה יעילות דומה בהורדה של ההמוגלובין המסוכרר לאחר 6 חודשים. בנוסף, טוג'או הפחית את אחוז החולים שסבלו מהיפוגליקמיה (blood glucose≤70mg/dL) לילית (בין השעות 00:01-05:59 ( ב-27% במהלך כל תקופת המחקר וב-46% במהלך תקופת הטיטרציה (8 השבועות הראשונים של המחקר). כמו כן, הקבוצה שטופלה בטוג'או עלתה פחות במשקל במהלך תקופת המחקר ביחס לקבוצה שטופלה בלנטוס (הפרש של 580 גרם בין שתי הקבוצות בתום חצי שנה של מחקר).
מחקר ה-EDITION3 כלל מטופלים נאיבים לאינסולין והראה יעילות דומה בהורדה של ההמוגלובין המסוכרר לאחר 6 חודשים. במחקר זה נצפתה מגמה שאינה מובהקת סטטיסטית להפחתה של 23% באחוז החולים שסבלו מהיפוגליקמיה (blood glucose≤70mg/dL) לילית (בין השעות 00:01-05:59).
בכל המחקרים שבדקו את היעילות והבטיחות של טוג'או בהשוואה ללנטוס התוצא העיקרי היה non-inferiority בירידה ברמות ההמוגלובין המסוכרר. בכל המחקרים הושג התוצא העיקרי והתקבלה ירידה דומה ברמות ההמוגלובין המסוכרר בהשוואה בין שתי זרועות הטיפול לאחר חצי שנה (ירידה של 1.02% במטה-אנליזה של מחקרי ה- N=2400 EDITION 1-3) [5]. בנוסף, שיעור החולים שהגיעו ליעד המוגלובין מסוכרר הנמוך מ-7% היה דומה בשתי הקבוצות (36.2% בקבוצת הטוג'או ו-35.5% בקבוצת הלנטוס).
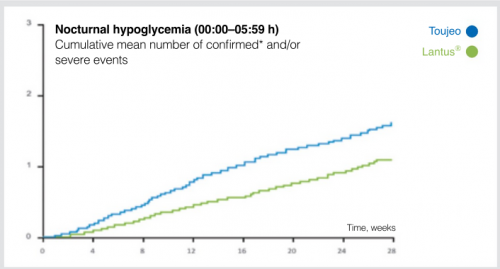
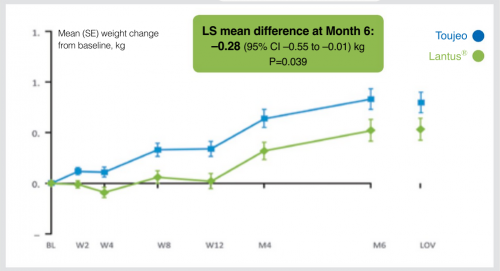
מספר אירועי ההיפוגליקמיה הליליים (≤70mg/dl) ירד ב-31% בקבוצת הטוג'או בהשוואה ללנטוס (תרשים מס' 1). כמו כן, מספר אירועי ההיפוגליקמיה במהלך כל היום ירד אף הוא ב-14%. ההבדל בהיפוגליקמיה לטובת הטוג'או בא לידי ביטוי כבר בתקופת הטיטרציה (8 השבועות הראשונים של המחקר) עובדה העשויה לסייע לחולים לבצע טיטרציה אופטימלית של מינון האינסולין מבלי לחשוש מאירועי היפוגליקמיה. בנוסף, נצפתה עלייה פחותה במשקל בקבוצת הטוג'או בהשוואה ללנטוס (-0.28kg).
גמישות בשעות ההזרקה – בתת מחקר של ה-EDITION1 ו-EDITION2 נבדקה האפשרות של מועד הזרקה גמיש (±3 שעות ממועד ההזרקה הקבוע). מן התוצאות עולה כי זמן הזרקה גמיש לא פגע באיזון הסוכר של החולים ולא העלה את אחוז החולים שסבלו מהיפוגליקמיה.
היעילות והבטיחות של טוג'או בטיפול בסוכרת מסוג 1 - היעילות והבטיחות של טוג'או נבדקה בשני מחקרים שכללו חולים בסוכרת מסוג 1 EDITION4,EDITION JP1 [5], [6]. בשני המחקרים טוג'או הפחית את רמות ההמוגלובין המסוכרר בדומה ללנטוס. ב-EDITION4 נצפתה מגמה של 10% ירידה באירועי ההיפוגליקמיה הלילית במשך כל תקופת המחקר (לא מובהקת סטטיסטית) וירידה מובהקת סטטיסטית של 31% בהיפוגליקמיה לילית במהלך תקופת הטיטרציה (8 השבועות הראשונים של המחקר). בנוסף, הקבוצה שטופלה בטוג'או עלתה פחות במשקל במשך תקופת המחקר (הפרש של 0.6 ק"ג בין שתי הקבוצות).
במחקר היפני, נצפתה ירידה של 34% באירועי היפוגליקמיה לילית במשך כל תקופת המחקר וירידה של 20% בהיפוגליקמיה במשך כל היום.
נפח הזרקה קטן יותר - מאחר שטוג'או מכיל ריכוז הגבוה פי שלושה מלנטוס (300 יחידות אינסולין למ"ל בהשוואה ל-100 יחידות למ"ל בלנטוס), נפח ההזרקה הנדרש עבור אותו מספר יחידות אינסולין נמוך בשני שלישים, דבר המקל על מטופלים רבים, ובין השאר, גם על אלה הנאלצים להזריק נפחים גדולים.
לסיכום, אינסולין בזאלי ארוך פעולה ממשיך להוות חלק מרכזי בפרוטוקול הטיפולי בסוכרת. טוג'או מהווה תוספת חדשה ומשופרת לארסנל הטיפולי וזאת בזכות תכונות פרמקולוגיות משופרות הכוללות: פרופיל פעולה שטוח יותר ומשך פעולה ארוך יותר בהשוואה ללנטוס. במחקרים הקליניים טוג'או הדגים ירידה בשיעור אירועי היפוגליקמיה לילית ובמשך כל היום ועלייה פחותה במשקל ביחס ללנטוס. אי לכך, שימוש בטוג'או יכול לסייע למגוון רחב של מטופלים חולי סוכרת סוג 1 וחולי סוכרת סוג 2.
ביבליוגרפיה
- Bolli GB et al. Diabetes Obes Metab 2015; 17: 386–394
- M. Matsuhisa et al. Diabetes, Obesity and Metabolism 18: 375–383, 2016
- ↑ P. D. Home Diabetes, Obesity and Metabolism 17: 1011–1020, 2015
- ↑ 2.0 2.1 2.2 Ofri Mosenson et al. Diabetes Care 2016;39(Suppl. 2):S146–S153
- ↑ Riddle MC et al. Diabetes Care 2014; 37:2755-2762
- ↑ Yki-Jarvinen H et al. Diabetes Care 2014; 37: 3235–3243
- ↑ 5.0 5.1 Robert Ritzel et al. Diabetes, Obesity and Metabolism 17: 859–867, 2015
- ↑ Philip D. Home et al. Diabetes Care 2015;38:2217–2225
קישורים חיצוניים
המידע שבדף זה נכתב על ידי ד"ר רננה שור - רופאה פנימית בכירה, המרכז הרפואי אסף הרופא, מרפאות סוכרת מכבי, צריפין, באר יעקב


 כניסה
כניסה  עקבו אחרינו בפייסבוק
עקבו אחרינו בפייסבוק