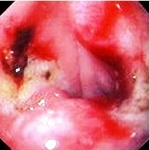
כיב התריסריון - Duodenal ulcer
הופניתם מהדף כיב התריסריון לדף הנוכחי.
עקרונות בכירורגיה
מאת ד"ר צבי קויפמן
| עקרונות בכירורגיה | ||
|---|---|---|
| ||
| שם המחבר | ד"ר צבי קויפמן | |
| שם הפרק | כירורגיה של הקיבה והתריסריון | |
כיב התריסריון מאופיין בנוכחות פצע כרוני ברירית התריסריון. המקום השכיח ביותר למציאת הכיבים העיכוליים (פפטיים) הוא בחלק הראשון של התריסריון (בצל התריסריון), בדופן הקדמית או האחורית שלו. מקומות פחות שכיחים למציאת הכיבים הללו הם ברירית שלאחר בצל התריסריון (פוסטבולברית), או נדיר - בחלק האחר של התריסריון. כיבים הממוקמים בשוער מתנהגים ככיבים פפטיים בתריסריון, ולכן נהוג להתייחס אליהם כאל כיבים פפטיים בתריסריון. בארה"ב מאובחנים כ-4 מיליון חולי כיב תריסריון חדשים בכל שנה. הערכה היא שכ-20 מיליון מאזרחי ארה"ב סובלים ממחלת הכיב.
כ-15%-5% מהאוכלוסייה העולמית סובלת מכיב פפטי. 20%-15% מהחולים יופיעו בפעם הראשונה עם סיבוכי הכיב, בלא עבר של מחלת כיב.
אפידמיולוגיה
כיב התריסריון שכיח יותר בגברים ובייחוד בבני 60-20. כ-15%-20% מהאוכלוסייה המערבית סובלת מכיב פפטי. ניכרת מגמת ירידה בשכיחותו של הופעת כיב התריסריון באוכלוסייה המערבית. מגמה זו החלה בשנות ה-60 ונמשכת עד היום. התרופות הנוגדות יצירת כיבים לא שינו את המהלך הטבעי של המחלה. מגמת הירידה בשכיחות בולטת יותר בקרב צעירים. השכיחות בנשים היא 0.25-0.14 ל-1,000 בשנה, ובגברים - 3-1.5 ל-1,000 בשנה. בשנים האחרונות מדווחים על עלייה בשכיחות הופעת כיבים בנשים. כחצי מיליון מקרים חדשים של כיב פפטי מתגלים באוכלוסייה הכללית בכל שנה בארה"ב.
אטיולוגיה
כיב התריסריון הוא מחלה ראשונית ברוב החולים, הקשור לנוכחות זיהום בחיידקי הליקובקטר פילורי והפרשת חומצה-פפסין. שכיחות יתר של הופעת כיב התריסריון משני מדווח בספרות במקרים הבאים:
- מחלות שונות כמו:

- מזון ועישון: אין קשר סטטיסטי ברור בין Caffeine לבין שכיחות הופעת הכיבים. לעומת זאת, בין עישון (השפעת הניקוטין) לבין נוכחות כיב התריסריון נמצא קשר. הפסקת עישון מסייעת בריפוי הכיב.
- תרופות: עם התרופות המוזכרות בספרות כמשפיעות על מהלך הכיב נמנים הסטרואידים, Acetylsalicylic Acid, Indomethacin, Phenylbutazone או נוגדי דלקת אחרים שאינם סטרואידים. תרופות אלה יכולות לפעול באחד המנגנונים הבאים:
- עלייה בחדירות (פרמאביליות) של רירית הקיבה
- שינויים בזרימת הדם ועיכוב הפרשת הריר בקיבה
- עיכוב יצירת פרוסטגלנדינים ודיכוי הפרשת הביקרבונט
- גורמים גנטיים - גורמים אטיולוגיים תורשתיים השכיחים בחולי כיב התריסריון:
- גסטרינומה - בתסמונת 1-MEN, המועברת בצורה אוטוזומלית דומיננטית
- עמילואידוזיס מסוג IV
- Tumor nystagmus ulcer syndrome
- ההבדלים בשכיחות בין גברים לנשים, בין שחורים ללבנים ובין אזורים שונים בעולם ובאותן ארצות, אף הם מעידים על סיבות תורשתיות.
- פפסינוגן T1 ברמה גבוהה.
- בהיפרפפסינוגנמיה ובהתרוקנות מהירה של הקיבה ניתן למצוא במחצית החולים עדות לתורשה אוטוזומלית דומיננטית.
- בעלי קבוצת דם O, שאינם מפרישים
- נוכחות נוגדנים ה-IgA המופרש בחולים עם כיב התריסריון, או נוגדנים המגרים להפרשת חומצה באחרים, גם הם מרמזים על כך, שלמחלה יש קשר לשינויים אימונולוגיים תורשתיים.
פתופיזיולוגיה
כיב התריסריון נוצר עקב חוסר איזון בין המערכת של חומצה ופפסין לבין מערכת ההגנה של הרירית. יש תחרות בין הפרשת החומצה והפפסין לבין מנגנוני ההגנה שיוצרת הרירית. כאשר החומצה והפפסין המציפים את התריסריון גוברים על מנגנון ההגנה של התריסריון, הם פוגעים ברירית וגורמים לכיב.
כמה עובדות מאפיינות את חולי כיב התריסריון:
- נוכחות מסיבית של חיידקי הליקובקטר פילורי הפוגעים בהגנה של הרירית
- ערכי BAO (Basal acid output) MAO (Maximal acid output) גבוהים מאשר בקבוצות בלא כיב. התחומים לגבי שתי קבוצות אלו הם רחבים, ולכן חופפים האחד את השני. אין התאמה בין רמת החומצה לבין משך הסבל, או שכיחות הסיבוכים ממחלת הכיב.
- מסת התאים הפריאטליים גדולה יותר, ולכן בתגובה לגירוי – כמות החומצה המופרשת גדולה. רגישות התאים הפריאטליים לגירוי סטנדרטי, ממושכת וחזקה יותר.
- העלייה בטונוס עצב התועה (הואגוס) היא ממצא שקשה למדוד אותו, אבל הוא קיים.
- בעקבות הרמות הגבוהות של החומצה סביר היה למצוא רמה נמוכה של גסטרין בדם. ואולם בחולים אלה רמת הגסטרין גבוהה יחסית, בלא קשר לרמה הגבוהה של החומצה בקיבה. הפרשת החומצה בתגובה למזון גבוהה או תקינה בנוכחות חומצה ברמה גבוהה בקיבה.
- באדם בריא ארוחה עשירה בחלבון מגבירה את הפרשת החומצה ב-40%-25%. בחולי כיב מצב זה בולט פחות.
- הכנסת סוכר מרוכז, שומנים וחומצה מעכבת את הפרשת החומצה באותה מידה בחולים ובבריאים.
- הפרשת הביקרבונט מהלבלב מופחתת. הפרשת הסקרטין בתריסריון - בתגובה לחומצה - פחותה, ולכן הפרשת הביקרבונט המנטרל את החומצה קטנה.
- יש הטוענים, שהפרעות במנגנונים של הסומטוסטטין, גלוקגון, VIP והורמונים ניורוקריניים, אנדוקריניים ופאראקריניים קשורים להופעת הכיבים.
- התרוקנות הקיבה מהירה יותר. ההתרוקנות מואטת בנוכחות שומן במזון, ואולם בנוכחות חומצה, שבמהלך תקין אמורה להאט את התרוקנות הקיבה, ההתרוקנות אינה מואטת.
- שחרור מוגבר של פפסינוגן ההופך לפפסין.
הזיהום החיידקי במחלת הכיב העיכולי
על הימצאות חיידקים ספירליים בקיבה דווח כבר לפני כחמישים שנה. ב-1940 מצאו Barron- Freedburg "ספירוכטות" בכ-37% מהקיבות שנכרתו בניתוח. ב-1975 דיווחו Colin Jones- Steer על נוכחות חיידקים גרם-שליליים על שטח פני אפיתל מערת השוער (האנטרום) בכ-80% מהלוקים בכיב קיבה (על כך זכו בפרס נובל ב-2005). ב-1983 זכה הנושא לתנופה של ממש כש-Marshall- Warren דיווחו על נוכחות חיידקים אלה של פני רירית האנטרום בחולים הלוקים בדלקת קיבה אנטרלית. מאז פורסמו עבודות רבות התומכות בממצא זה.
החיידק זוהה ואופיין, ונמצא כי מבחינה מורפולוגית הוא דומה ל-Campylobacter jejuni. בהמשך כינו אותו Campylobacter pylori וכיום Helicobacter pylori. זהו חיידק נייד, גרם-שלילי וספירלי, בעל שוטונים מרובים. הוא נבדל מזני הליקובקטר אחרים בחלבוני שטח הפנים שלו, בחומצות שומן שמרכיבות את דופן התא ובהרכב חומצות הגרעין שלו. החיידק צומח בצורה מיטבית באטמוספירה דלת חמצן, בטמפרטורה של כ-37 מ"צ. את החיידק אפשר לזהות במיקרוסקופ בעזרת צביעת כסף, או להצמיח אותו בתרבית. בשל יכולתו לפרק אוריאה, משמשת גם בדיקת פעילות אוראזה בהומוגנאט של ביופסיה ככלי אבחנתי סגולי. בחולים עם הליקובקטר ניתן למצוא כייל גבוה של נוגדנים נגד הליקובקטר מן הסוג IgA- IgG, הן בביופסיות והן בנסיוב ובמיץ הקיבה.
בבדיקה In vitro נמצא, שהליקובקטר רגיש לכמה תכשירים אנטיביוטיים, כולל Tetracycline, Erythromycin, Penicillin, Cefalotin ו-Metronidazole. החיידק אינו רגיש ל-Vancomycin, ל-Sulphamethoxazole ול-Trimethoprim. הוא רגיש גם לתרכובות Bismuth, אך לא לCimetidine, לCarbenoxolone ולSucralfate.
החיידק בודד מרירית הקיבה של כ-90% מהלוקים בדלקת קיבה אנטרלית, ורק לעתים רחוקות מרירית הקיבה של בני אדם בריאים. ההנחה היא, שהחיידק חודר מתחת לשכבת הריר המגנה על רירית הקיבה ומאפשר לחומצה, לפפסין ולגורמים מזיקים אחרים, לחדור בעקבותיו ולגרום לירידה בהפרשת הריר. בעקבות כך מופיעים דלקת קיבה וכיב קיבה. נמצא גם, שרירית האנטרום שיכולה להימצא בבצל התריסריון, יכולה להזדהם אף היא בהליקובקטר ולגרום באופן דומה לדואודניטיס ולכיב תריסריון. ואמנם, כבר ב-1964 תיארו James, ואחר כך גם Patrick וחבריו, נוכחות אפיתל קיבה בבצל התריסריון של חולי דואודניטיס וכיב תריסריון. ההנחה היתה, שבחולים אלה, אזור המעבר בין רירית הקיבה לרירית התריסריון נמצא בבצל התריסריון, ולא בשוער.
הימצאות הליקובקטר והשכיחות של התכייבות בקיבה ובתריסריון בחולים בדלקת קיבה אנטרלית ידועים כיום. ההליקובקטר נמצא בחולים הלוקים בדלקת קיבה (Gastritis) אנטרלית ראשונית. אין מוצאים אותו בדלקת קיבה אנטרלית משנית לסיבה ידועה, כגון מחלת קרוהן, דלקת קיבה ומעיים (Gastroenteritis) אאוזינופילית או דלקת קיבה משנית לתרופות. החיידק זוהה זה גם בשוליים של כיב התריסריון. בכ-90% מהלוקים בכיב תריסריון זוהה הליקובקטר בתאי אפיתל אנטרליים הסמוכים לכיב. כל החולים האלה לקו גם בדלקת קיבה. מטפלים אחרים מצאו אף הם הליקובקטר בתריסריון, אבל רק בסמיכות למטפלזיה קיבתית. בלט העדר הליקובקטר באפיתל בנוכחות מטפלזיה אינטסטינלית באנטרום.
גם אם ברור, כי החיידק אכן נמצא באנטרום של הלוקים בדלקת קיבה אנטרלית ובתריסריון שמכיל רירית אנטרלית, אין פירוש הדבר שהחיידק אכן גורם דלקת ונזק לתאים, וייתכן שהוא נוטה להתיישב בתאים שניזוקו על-ידי גורמים אחרים. ראיה התומכת בכך שההליקובקטר הוא אכן פתולוגי בעבור האדם מוצאים בעבודה נוספת , שבה מתנדב בלע כ-900 חיידקי הליקובקטר אחרי שקיבל טיפול ב-Cimetidine. ביופסיות שנלקחו חודש קודם לכן מרירית קיבתו היו תקינות. ביום השמיני לאחר בליעת ההליקובקטר לקה המתנדב בהקאות ובהמשך גם בכאב ראש. ביום העשירי נלקחו ביופסיות חוזרות שהדגימו הפעם דלקת קיבה חדה. בבדיקה מיקרוסקופית הודגמו חיידקי הליקובקטר, וביופסיות חוזרות מרירית הקיבה ביום ה-14 הצביעו על שיפור ניכר. מכאן שהליקובקטר אכן מסוגל לגרום לדלקת אנטרלית.
מקצת העבודות הראו, כי אפשר להמשיך ולבודד את ההליקובקטר בקיבה, גם לאחר ריפוי מלא של כיב. מכאן ניתן לשער, שהישרדות החיידק בקיבה היא האחראית לאופי החוזר ונשנה של מחלת הכיב העיכולי. אמנם Cimetidine, שבו טופלו חולים אלה, הביא לריפוי מהיר של הכיב, אך לא לריפוי דלקת הקיבה או להכחדת החיידק. בעקבות זאת, המשיך החיידק לפגוע ברירית הקיבה או התריסריון, וכך גרם להיווצרות כיב מחודשת. כמו-כן נמצא כי טיפול בכיב בעזרת תכשיר נוגד חיידקים, כגון Bismuth, או Bismuth בשילוב עם אנטיביוטיקה, הביא הן לריפוי הכיב והן לקצב חזרה נמוך מזה שהושג בעזרת טיפול ב-Cimetidine בלבד.
ברוב המקרים, נוכחות ההליקובקטר פילורי אינה גורמת לכל בעיה, אולם אצל חלק מבני האדם נוכחותו עשויה לגרום לדלקות וכיבים. צורת החיידק ואופן תנועתו מאפשרות לו לחדור את השכבה הרירית המגנה על דופן הקיבה ולהפכה לפגיעה להשפעת חומצות ואנזימים. החיידק עלול אף להיצמד אל תאי הקיבה, ובאופן זה להחליש עוד יותר את מנגנון ההגנה של הקיבה ולגרום לדלקת מקומית. בנוסף, מסיבות שאינן מובנות לחלוטין, מסוגל החיידק גם לגרום לקיבה לייצר חומצה נוספת. עודף חומציות זו עשויה לגרום לדלקת בחלק הראשון של התריסריון. כמה שבועות לאחר ההידבקות בהליקובקטר פילורי מפתחים מרבית האנשים דלקת בדופן הקיבה, אולם במרבית המקרים לא יופיעו כל בעיות או תסמינים בעקבות הזיהום. יתכן וההסבר להופעת תסמיני מחלה רק אצל חלק מהאוכלוסיה טמון בהבדלי תורשה ותנאים סביבתיים.
הראיות ההצטברו מהנתונים המורפולוגיים, הסרולוגיים והטיפוליים מעידות על כך, שהליקובקטר הוא הגורם לדלקת קיבה אנטרלית ולהתכייבות עיכולית, וזו האטיולוגיה העיקרית המקובלת כיום לכיב עיכולי.
הליקובקטר שכיח יותר בארצות מתפתחות בהשוואה למפותחות. שכיחותו עולה עם הגיל. בישראל נמצא שהליקובקטר שכיח ב-40% מגילאי 30-20 שנה, וב-80% מגילאי 80 שנה ומעלה. מקור הזיהום הוא בני אדם המהווים מאגר ומאכסן טבעי של ההליקובקטר. דרך ההדבקה המקובלת כיום היא פומית-פומית (Oro-oral) או פומית-צואתית (Oro-fecal). הדרך הראשונה היא השכיחה יותר. מאחר שבארצות מפותחות שיעור ההדבקה מחדש לאחר הכחדת ההליקובקטר, כחלק מהטיפול בחולי כיב, הוא נמוך יותר, אין הוריה לטיפול נוגד הליקובקטר בבני משפחה של חולה כיב.
אבחון
זיהום בהליקובקטר ניתן לאבחון בכמה שיטות:
- תבחין סרולוגי.
- תבחין נשימה עם שינן (אוריאה) מסומן.
- תבחין לנוכחות אוריאזה, המפרק שינן לאמוניה ולמים. בדגימת רירית הנלקחת בזמן האנדוסקופיה נבדקת נוכחות אוריאזה, המעביר את הסביבה החומצית לבסיסית בזמן הפעולה, ולכן משנה את הצבע במבחנה.
- תרבית רקמה.
- בדיקת PCR (Polymerase chain reaction) שהיא בדיקה ביולוגית מולקולרית.
טיפול בנוגדי דלקת
לטיפול בסטרואידים ובנוגדי דלקת שאינם סטרואידים מיוחסת שכיחות רבה יותר של כיבים בקיבה או בתריסריון וסיבוכיהם. נתונים אפידמיולוגיים הראו ששימוש בנוגדי דלקת, בעיקר בצורה מתמשכת, קשור לעלייה בשכיחות של כיב עיכולי וסיבוכיו. מעריכים שכ-1% מתושבי ארה"ב נוטלים יום-יום תכשירים אלה. כ-12%-30% מהמשתמשים בנוגדי דלקת ילקו בכיב קיבה, כ-19%-2% בכיב התריסריון וכ-2%-1% בסיבוכים של ממש. בארה"ב נרשמים בכל שנה כ-7,000 מקרי מוות עקב נזקים לדרכי העיכול הקשורים לשימוש בנוגדי דלקת.
הנזק לרירית הקיבה כולל דימומים בתת-אפיתל, ארוזיות וכיבים (תמונה 2.3). החשש ללקות בסיבוכים המסוכנים, כגון דימום או נקב בדופן הקיבה, גדול יותר בכיב מאשר בארוזיות או בדימומים בתת-אפיתל.
מנגנון הנזק של נוגדי הדלקת: הפרוסטגלנדינים השכיחים ברירית דרכי העיכול הם PGF2, PGE2 (Dinoprostone), PGI2 (Prostacyclin). פרוסטגלנדינים בריכוז גבוה מעכבים את הפרשת החומצה בקיבה על-ידי עיכוב יצירת אדנוזין חד-פוספאט ציקלי (cAMP - Cyclic adenosine monophosphate) תוך-תאי, ובריכוז נמוך יותר מגינים על רירית דרכי העיכול על-ידי גירוי להפרשת ריר וביקרבונט מתאי הציפוי של רירית המעי. כך משתפרת יכולת הרירית לאזן חומציות, מתחדשים תאי הציפוי של רירית דרכי העיכול ומשתפרת זרימת הדם לרירית. נוגדי הדלקת מעכבים את יצירת הפרוסטגלנדינים ברקמות הגוף על-ידי עיכוב האנזים ציקלואוקסיגנזה ובכך הם פוגעים במנגנון ההגנה של הרירית וגורמים לנטייה לדימום על-ידי אצטילציה של הטסיות ופגיעה ביכולת האגירה שלהן.
נוגדי הדלקת גורמים נזק לדרכי העיכול: בשלב ראשון על-ידי פגיעה ישירה בחדירות קרום התא של רירית הקיבה ועצירת יוני מימן בתוך האפיתל, ובשלב שני על-ידי כניסת יוני נתרן ואשלגן לתוך התאים ופליטת יוני מימן לקיבה, העלאת חומציות הקיבה ופגיעה ברירית.
טיפול בנוגדי דלקת גורם נזק לרירית הקיבה התלוי במינון. הנזק עלול לכלול דימום בתת-אפיתל, ארוזיות או כיבים. טיפול במינון גבוה של נוגד דלקת יגרום ליצירת נזק לרירית. טיפול מתמשך במינון נמוך גורם להסתגלות של הרירית ולהקטנת הנזק.
Misoprostol, שהוא חומר סינתטי דמוי פרוסטגלנדין E1, Sucralfate וחסמי H2 מגינים על רירית הקיבה מפני הנזק הנגרם לה בשימוש קצר מועד בנוגדי דלקת. Misoprostol הוא התכשיר היחיד שקיימת הוריה לטיפול בו למניעת כיב קיבה במשך הטיפול בנוגדי דלקת.
בשונה מהטיפול לטווח הקצר - הטיפול לטווח ארוך עלול לגרום לכיבים עמוקים, לדימום מדרכי העיכול, לנקב בקיבה ולמוות. ב-60% מהמטופלים סיבוך מסכן חיים של כיב הוא הביטוי הראשון של נזק בדרכי העיכול עקב נוגדי דלקת.
סיבוכים אלו מתאפיינים בשיעור הגבוה של תופעות לוואי והעדר מתאם בין תסמינים של דרכי העיכול העליונות לבין קיומם של כיבים באנדוסקופיה.
הדרך הטובה ביותר למניעת נזק לרירית דרכי העיכול היא להימנע מנטילת נוגדי דלקת.
נטילת חוסמי H2 יעילה במניעת כיב התריסריון, אך לא במניעת כיב קיבה. לעומת זאת, התכשיר היחיד המונע התפתחות כיב בקיבה ובתריסריון בחולים הנוטלים נוגדי דלקת הוא Misoprostol (שם מסחרי Cytotec). הדרך היעילה ביותר לרפא חולים שחלו בכיב תוך כדי טיפול בנוגדי דלקת, היא על-ידי הפסקת נוגדי הדלקת ומתן טיפול כמקובל בכיב עיכולי. בחולים שמהלך מחלתם הסתבך בכיב, תוך כדי טיפול בסטרואידים, יש לטפל בחוסמי H2. נתונים בספרות מראים שריפוי הכיב בעת ובעונה אחת עם מתן סטרואידים וחוסמי H2 יעיל באותה מידה כבחולים שאינם מטופלים בסטרואידים. באחרונה דווח בספרות הרפואית שטיפול נגד הליקובקטר פילורי לפני התחלת הטיפול בנוגדי דלקת, הוריד את שיעור הסיבוכים בקיבה ובמעי בשיעור ניכר.
ראו גם
- לנושא הקודם: כיב עיכולי (פפטי) - Peptic ulcer
- לנושא הבא: סיבוכים שכיחים לאחר ניתוחי כיב - Common postoperative complications of ulcer surgery
- לתוכן העניינים של הפרק
- לתוכן העניינים של הספר
- לפרק הקודם: כירורגיה של הצפק
- לפרק הבא: כירורגיה של המעי הדק
המידע שבדף זה נכתב על ידי ד"ר צבי קויפמן, מומחה בכירורגיה, מנהל היחידה לבריאות השד, מרכז רפואי מאיר, כפר סבא


 כניסה
כניסה  עקבו אחרינו בפייסבוק
עקבו אחרינו בפייסבוק