מחלת קושינג - טיפולים תרופתיים חדשים - 2012 - Cushing disease - new treatments
הופניתם מהדף מחלת קושינג - טיפולים תרופתיים חדשים - Cushing disease - new treatments לדף הנוכחי.
לערכים נוספים הקשורים לנושא זה, ראו את דף הפירושים – מחלת קושינג
מחלת קושינג נובעת מעודף הפרשת ACTH (AdrenoCorticoTropic Hormone) ו-Cortisol בשל Adenoma מפרישת ACTH ביותרת המוח. מחלה זו מלווה בתחלואה ותמותה גבוהות אם המחלה אינה מאובחנת נכון ומטופלת ביעילות. הטיפול המקובל כולל ניתוח להסרת ה-Adenoma, ובמקרים שאין ריפוי לאחר הניתוח – קרינה מכוונת ל-Adenoma ולעיתים רחוקות אף כריתה דו-צדדית של בלוטות יותרת הכליה. הוכנסו לשימוש כמה תרופות חדשות לטיפול ודיכוי הפרשה עודפת של Cortisol בחולים הסובלים ממחלת קושינג. נסקור כאן את האפשרויות הטיפוליות המכוונות לרמת יותרת המוח, יותרת הכליה והקולטן ל-Glucocorticoid.
הקדמה
תסמונת קושינג (עודף הפרשת Cortisol) נגרמת על ידי גידולים של בלוטת יותרת המוח (היפופיזה, Hypophysis), בלוטת יותרת הכליה (Adrenal) וגידולים אקטופיים (Ectopic) (לרוב גידולי ריאה כמו Carcinoid). התסמונת כרוכה בתחלואה ניכרת (סוכרת, יתר לחץ דם, עודף משקל, קרישיות יתר, Osteoporosis, נטייה לזיהומים, אבני כליה, דיכאון, חרדה ופסיכוזה), ותמותה מוגברת אם האבחון והטיפול מתעכבים. מחלת קושינג הנגרמת כתוצאה מ-Adenoma ביותרת המוח גורמת לכ-70 אחוזים מכלל מקרי התסמונת.
ניתוח (טרנס-ספנואידלי, Transsphenoidal) לכריתת Adenoma מפרישת ACTH ביותרת המוח וניתוח לפרוסקופי (Laparoscopic) להסרת גידול (Carcinoma ,Adenoma) מפריש Cortisol ביותרת הכליה הם הקו הראשון בטיפול בתסמונת קושינג. ניתוח טרנס-ספנואידלי משיג הפוגה בכ-60 אחוזים מחולי מחלת קושינג. לפי הצורך אפשר להציע היום לחולים עם מחלת קושינג פעילה לאחר ניתוח לא מוצלח גם קרינה לאוכף הטורקי או כריתה דו-צדדית של בלוטות האדרנל.
תרופות מכוונות לאדרנל - Steroidogenesis Inhibitors
קיימים טיפולים תרופתיים שעשויים לעזור לחלק מהחולים במחלת קושינג פעילה. אלה תרופות שפעילותן מתמקדת בדיכוי הייצור של Cortisol ביותרת הכליה באמצעות עיכוב אנזימים המעורבים בשלבי הייצור של ה-Cortisol. תרופות אלה אינן פועלות ישירות לדיכוי ה-Adenoma בהיפופיזה, והן לא אושרו לשימוש שכן אין מחקר גדול שהוכיח יעילותן, והשימוש בהן כרוך בהתפתחות תופעות לוואי במקרים מסוימים. שתי התרופות העיקריות מקבוצה זו הן Metyrapone ו-Ketoconazole. [1] [2], Metyrapone (במינון 250–500 מיליגרמים, שלוש פעמים ביום) נוטה לדכא גם את ייצור ה-Aldosterone ויכול לגרום להצטברות חומרים עם השפעה מינרלוקורטיקואידית (Mineralocorticoid) חלש ולפיכך לתופעות לוואי של עליית לחץ דם, בצקות ו-Hypokalemia. גם שיעור יתר הוא תופעת לוואי מוכרת, כמו גם פריחה, הפרעות במערכת העיכול ופגיעה בכבד. קטוקונזול (המשמש לטיפול בפטרת) במינון 200 מ"ג, 6-2 פעמים ביום יעיל גם כן בדיכוי הפרשת Cortisol במחלת קושינג. תופעות לוואי כוללות פגיעה בכבד, פריחה, Hypogonadism, Gynecomastia, ואף תת-פעילות של יותרת הכיליה, שמחייבות הפסקת הטיפול או הפחתת המינון. השימוש בסוג זה של תרופות מיועד לחולים עם הפרשת Cortisol גבוהה מאוד כהכנה לניתוח לכריתת ה-Adenoma, וזאת כדי להקטין הסיכון הניתוחי הכרוך ברמות גבוהות מאוד של Cortisol; בחולים לאחר ניתוח לא מוצלח; ובחולים הממתינים להשפעת הטיפולי (שלעיתים מושג לאחר שנה-שנתיים) של קרינה מכוונת ל-Adenoma באוכף הטורקי לדיכוי הפרשת ACTH ו-Cortisol. יש חולים המגיבים היטב לטיפול באחת משתי התרופות ללא תופעות לוואי, ומטופלים שנים ארוכות ובהצלחה, ללא איבוד ההשפעה המדכאה של התרופות על הפרשת ה-Cortisol. בחולים כאלה בטיפול תרופתי ממושך צריך לחזור על הדמיה של יותרת המוח כדי לשלול התפתחות מחלת Nelson (גדילה לא מבוקרת של אדנומת ACTH). תכשירים אלה אינם רשומים בישראל להתוויה של מחלת קושינג, ולכן השימוש בהם הוא off Label. תכשיר ה-Mitotane נמצא יעיל בדיכוי ארוך טווח של הפרשת Cortisol בחולים עם תסמונת קושינג תלוית ACTH, בשל האפקט האדרנוליטי החזק שלו, אך בשל תופעות לוואי שכיחות משמש בעיקר לטיפול בחולים עם Carcinoma של האדרנל.
אגוניסט לדופמין – Cabergoline – טיפול מכוון ל-Adenoma ביותרת המוח
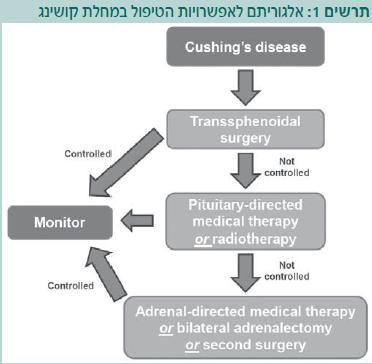
אגוניסטים (agonists) ל-Dopamine כמו Bromocriptine ו-Cabergoline (Dostinex) משמשים בהצלחה לטיפול באדנומות (Adenomas) מפרישות Prolactin הן בנשים והן בגברים. דיכוי הפרשת ה-Prolactin נעשה באמצעות התקשרות לקולטן D2 (Dopamine) הנמצא על גבי התאים מפרישי ה-Prolactin ומתבטא גם ב-75 אחוזים מהאדנומות מפרישות ה- ACTH בהיפופיזה[3]. וכן על ידי חשיפה של תאים מפרישי ACTH המבטאים רצפטור לדופמין לטיפול באגוניסטים לדופמין ודיכוי הפרשת ACTH מהתאים in vitro[3]. מתברר שטיפול של כמה חודשים ב-Cabergoline מסוגל לדכא הפרשת Cortisol בחולים עם מחלת קושינג באמצעות השפעה ישירה על תאי ה-Adenoma[4]. [5], אף שאחרי חודשי טיפול אחדים תיתכן דעיכה של השפעת לדיכוי הפרשת ה-Cortisol בחלק מהחולים, אחוז לא מבוטל של חולים עם מחלת קושינג (עד 40 אחוזים) יתמידו בדיכוי מלא או חלקי של הפרשת ה-Cortisol לתקופות ארוכות במסגרת טיפול ב-Cabergoline במינון של 1–7 מיליגרמים לשבוע. במקביל, בחלק מהחולים נוכל לצפות להצטמקות של ה-Adenoma, לירידת לחץ דם ולירידה ברמות הסוכר. טיפול תרופתי ב-Cabergoline יכול להינתן לחולים אחרי כישלון ניתוחי, אם ניתוח חוזר אינו בא החשבון, או כשלא מזהים Adenoma בהדמיה חוזרת של האוכף לאחר חזרת המחלה (תרשים 1).
אנטגוניסט לרצפטור לגלוקוקורטיקואיד Mifepristone
ה-Mifepristone פותח כ-Antagonist לקולטן ל-Progesterone ומשמש כתכשיר להפסקת היריון במקום גרידה כשנוטלים אותו יחד עם אנלוג לפרוסטגלנדין (Misoprostol, Prostaglandin analogue) ב-7 השבועות הראשונים להיריון. תכשיר זה הוא גם אנטגוניסט יעיל מאוד לקולטן לגלוקוקורטיקואיד ומשמש בהצלחה חלקית לטיפול בחולים עם הפרשה אקטופית (Ectopic) של ACTH ותסמונת קושינג[6]. כמו כן הוא נקשר לקולטן האנדרוגני (Androgenic). התכשיר ניתן למספר מוגבל של חולי Carcinoma של האדרנל, הפרשת ACTH אקטופית ומחלת קושינג. החולים נטלו את התרופה באופן אוראלי במינון התחלתי של 400-200 מיליגרמים ליום והמינון הוגדל ל-2–4 שבועות בהתאם ליעילות הקלינית ולסבילות. היעילות נקבעת רק לפי פרמטרים קליניים, כמו ירידת משקל, שיפור בסימנים בעור, לחץ דם וירידה ברמות הסוכר בחולים עם ערכי סוכר מוגברים[6]. כיוון שרמות ACTH ו-Cortisol עולות בחולים המטופלים באנטגוניסט, אי אפשר להשתמש בהן כמדד ליעילות התרופה. אי-ספיקה אדרנלית עם חולשה, הקאות ו-Hypoglycemia יכולה להתפתח כתוצאה ממינון יתר של התרופה. הטיפול באי ספיקת האדרנל הוא בעייתי וקשה, כיוון ש-Hydrocortisone אינו יעיל בנוכחות התרופה, ובלית ברירה יש להשתמש אז ב-Dexamethasone. Hypokalemia היא תופעת לוואי שכיחה מאוד (בשליש מחולי הקושינג שטופלו) כתוצאה מרמות Cortisol גבוהות ומעודף אפקט מינרלוקורטיקואידי, כיוון ש-Mifepristone אינו נקשר ואינו חוסם את הקולטן למינרלוקורטיקואיד. גם עליית לחץ דם נצפתה בכמה חולים שטופלו בתכשיר, כנראה כתוצאה מאותו מנגנון. הטיפול בתופעות אלה כולל תוספות אשלגן ומתן תכשיר נוגד Aldosterone (כמו Spironolactone). תופעת לוואי נוספת היא Hyperplasia של רירית הרחם בגלל ההשפעה המתמשך של העמידות ל-Progesterone. הניסיון בשימוש בתרופה מצומצם לא רק במספר החולים, אלא גם במשך הטיפול, משום שרוב המטופלים סבלו מ-Carcinoma של האדרנל עמידה לטיפול אחר[6].
באחרונה פורסמו תוצאות ראשוניות של טיפול ב-50 חולים בתסמונת קושינג עמידה לטיפול, שטופלו ב-Mifepristone בצורה מבוקרת במשך 24 שבועות. 43 מתוכם חולים במחלת קושינג לאחר כישלון הטיפולים המקובלים הקיימים[7]. המדדים למעקב כללו בין השאר ירידה בסוכר (מ-149 ל-110 מיליגרמים אחוז) וברמת ההמוגלובין המסוכרר (HbA1C, Hemoglobin A1C) בחולי סוכרת (מ-7.4 אחוזים ל-6.4 אחוזים), ירידת לחץ דם דיאסטולי (Diastolic) של מעל 5 ממ"כ (מילימטרים כספית) נצפתה ב-38 אחוזים מהחולים, ירידה ממוצעת של 5.7 קילוגרמים במשקל, שיפור במראה הקושינגואידי, שיפור בתנגודת ל-Insulin ובדיכאון. במקביל נצפתה עלייה משמעותית ברמות ACTH ו-Cortisol בדם, וכן Cortisol ברוק ובאיסוף שתן. 34 חולים השלימו את תקופת המחקר, ו-7 פרשו בשל תופעות לוואי.
Pasireotide - אנלוג חדש ל-Somatostatin עם אפיניות גבוהה לקולטן מספר 5
אנלוגים ל-Somatostatin (Octreotide, Lanreotide) משמשים שנים רבות לטיפול בחולים עם אקרומגליה (Acromegaly) פעילה, שניתוח לא הביא לדיכוי רמות ה-GH (Growth Hormone) וה-IGF-1 (Insulin-like growth factor 1) ולרמיסיה (Remission). אנלוגים אלה נקשרים באפיניות גבוהה במיוחד לקולטן מספר 2 ל-Somatostatin ולא הראו שום השפעה על דיכוי הפרשת ACTH ו-Cortisol בחולים במחלת קושינג. הושקעו מאמצים רבים לפתח תכשירים ביולוגיים חדשים עם יכולת להיקשר לקולטנים נוספים ל-Somatostatin מתוך חמשת הידועים. תכשיר חדש מקבוצת האנלוגים ל-Somatostatin, ה-Pasireotide שנקשר באפיניות טובה לקולטנים 1, 2, 3, ו-5 ל-Somatostatin, ובייחוד לקולטן 5 [8] נמצא בפיתוח וניסויים קליניים לכמה מחלות כולל מחלת קושינג, אקרומגליה וגידולים נוירואנדוקריניים (Neuroendocrine) כמו CArcinoid. תכשיר זה עשוי להיות אפקטיבי בחולים במחלת קושינג לאור העובדה שאדנומות ACTH מבטאות היטב קולטן מספר 5. [9] תכשיר זה נבדק במחקר שלב (Phase) 2, והראה השפעה יפה לאחר שבועיים של טיפול בחלק מהחולים לדיכוי הפרשת Cortisol בשתן (5 מתוך 29 חולים דיכאו את ה-Cortisol לנורמה)[10]. חברת Novartis השלימה מחקר בינלאומי, רב-מרכזי, בשלב 3 שבו טופלו 162 חולים במחלת קושינג (חולים לאחר כישלון ניתוחי או חולים נאיביים, Naive) בזריקות Pasireotide (מינון יומי של 2 זריקות של 1,200-600 מיקרוגרמים) במשך שנה. כ-20 אחוזים מהמטופלים השיגו הפוגה (Remission) לאחר 6 ו-12 חודשי טיפול, ורוב החולים דיכאו את הפרשת ה-Cortisol משמעותית אף על פי שלא השיגו הפוגה מלאה. סך הכול ירדה הפרשת ה-Cortisol הממוצעת בכלל החולים ב-50 אחוזים כבר אחרי חודש וחודשיים של טיפול פעיל. נוסף על כך, הייתה השפעה יפה על ירידת משקל ולחץ-דם במטופלים. למרות תופעות הלוואי השכיחות של Hyperglycemia, החמרה בסוכרת או הופעת סוכרת שנצפו בכשליש מהחולים, האפשרות לטיפול תרופתי בחולים עם מחלת קושינג פעילה ישירות באמצעות דיכוי הפרשת ACTH מה-Adenoma ביותרת המוח היא משהו חדשני. התרופה עומדת לפני אישור של רשות התרופות האירופית (בשם המסחרי Signifor), ותינתן לחולים עם מחלת קושינג בצורת שתי זריקות תת-עוריות ליום באופן קבוע, אם יראו תגובה טובה של דיכוי הפרשת ה-Cortisol בשתן. השימוש בתכשיר זה עשוי להיות יעיל יותר בשילוב עם מקצת התכשירים שפורטו קודם, כמו מתן משולב עם Cabergoline ו-Ketoconazole כפי שדווח בקבוצת חולים במחלת קושינג בהולנד ששילוב כזה דיכא הפרשת Cortisol לנורמה כמעט בכולם[11].
ביבליוגרפיה
- ↑ Biller BMK, Grossman AB, Stewart PM, Melmed S, Bertagna X, Bertherat J, Buchfelder M, Colao A, Hermus AR, Hofland LJ, Klibanski A, Lacroix A, Lindsay JR, Newell-Price J, Nieman LK, Petersenn S, Sonino N, Stalla GK, Swearingen B, Vance ML, Wass JA, Boscaro M Treatment of adrenocorticotropin-dependent Cushing's syndrome: a consensus statement. J Clin Endocrinol Metab 93:2454-2462, 2008.
- ↑ הערה2
- ↑ 3.0 3.1 Pivonello R, Ferone D, de Herder WW, Kros JM, De Caro ML, Arvigo M, Annunziato L, Lombardi G, Colao A, Hofland LJ, Lamberts SW. Dopamine receptor expression and function in corticotroph pituitary tumors. J Clin Endocrinol Metab 89:2452-2462, 2004.
- ↑ Pivonello R, De Martino MC, Cappabianca P, De Leo M, Faggiano A, Lombardi G, Hofland LJ, Lamberts SWJ, Colao A. The medical treatment of Cushing’s disease: effectiveness of chronic treatment with the dopamine agonist cabergoline in patients unsuccessfully treated by surgery. J Clin Endocrinol Metab 94: 223–230, 2009.
- ↑ Godbout A, Manavela M, Danilowicz K, Beauregard H, Bruno OD, Lacroix A. Cabergoline monotherapy in the long-term treatment of Cushing's disease. Eur J Endocrinol 163:709–716, 2010.
- ↑ 6.0 6.1 6.2 Castinetti F, Conte-Devolx B, Brue T. Medical treatment of Cushing's syndrome: glucocorticoid receptor antagonists and Mifepristone. Neuroendocrinology 92 (Suppl 1):125-130, 2010.
- ↑ Fleseriu, M, Biller, BM, Findling, JW, et al. Mifepristone, a glucocorticoid receptor antagonist, produces clinical and metabolic benefits in patients with refractory Cushing syndrome: results from the Study of the Efficacy and Safety of Mifepristone in the Treatment of Endogenous Cushing Syndrome (SEISMIC). Fleseriu, M, Biller, BM, Findling, JW, Molitch, ME, Schteingart, DE, Gross C. Endocr Rev, Vol. 32 (03_MeetingAbstracts): OR09-5, 2011.
- ↑ Bruns C, Lewis I, Briner U, Meno-Tetang G, Weckbecker G. SOM230: a novel somatostatin peptidomimetic with broad somatotropin release inhibiting factor (SRIF) receptor binding and a unique antisecretory profile. Eur J Endocrinol 146:707-716, 2002.
- ↑ Hofland LJ, Van Der Hoek J, Feelders R, et al. The multi-ligand somatostatin analogue SOM230 inhibits ACTH secretion by cultured human corticotroph adenomas via somatostatin receptor type 5. Eur J Endocrinol 152:645-654, 2005.
- ↑ Boscaro M, Ludlam WH, Atkinson B, et al. Treatment of pituitary dependent Cushing's disease with the multi-receptor ligand somatostatin analog pasireotide (SOM230): a multicenter, phase II trial. J Clin Endocrinol Metab 94:115-122, 2009.
- ↑ Feelders RA, de Bruin C, Pereira AM, et al. Pasireotide alone or with cabergoline and ketoconazole in Cushing's disease. N Engl J Med 362:1846-1848, 2010.
- Colao A, Petersenn S, Newell-Price J, et al. Pasireotide (SOM230) provides clinical benefit in patients with Cushing’s disease: Results from a large, 12-month, randomized-dose, double-blind, Phase III study. ENEA meeting, Liege, Belgium, 2010.
קישורים חיצוניים
- טיפולים תרופתיים חדשים במחלת קושינג, מדיקל מדיה
המידע שבדף זה נכתב על ידי פרופ' אילן שמעון ונערך ע"י פרופסור יונה גרינמן


 כניסה
כניסה  עקבו אחרינו בפייסבוק
עקבו אחרינו בפייסבוק