מעקב לאחר כריתת פוליפים במעי הגס
ערך זה נמצא בבדיקה ועריכה על ידי מערכת ויקירפואה, וייתכן כי הוא לא ערוך ומוגה.
| מעקב לאחר כריתת פוליפים במעי הגס | ||
|---|---|---|
| ' | ||
| יוצר הערך | ד"ר אמיר קליין | |
לערכים נוספים הקשורים לנושא זה, ראו את דפי הפירושים: – סרטן מעי גס וחלחולת, פוליפים
מבוא
סרטן המעי הגס הוא גורם משמעותי לתחלואה ותמותה בעולם המערבי[1]. קולונוסקופיה כבדיקת סריקה לגילוי מוקדם של סרטן המעי הגס, מפחיתה שכיחות של סרטן המעי הגס ותמותה ממחלה זו[2]. חשיבותה העיקרית של קולונוסקופיה, נובעת ככל הנראה מהיותה בדיקת סריקה יעילה, המאפשרת גילוי של סרטן בשלבים מוקדמים וגילוי והסרה של נגעים טרום סרטניים (פוליפים ניאופלסטים)[3][4].
נוסף על כך, קולונוסקופיה יכולה לשמש בדיקת מעקב המשפיעה על הורדת שכיחות סרטן המעי הגס והתמותה ממחלה זאת. נוכחות של פוליפים ניאופלסטים מסוג משונן (serrated) או אדנומה (adenoma) במעי הגס מהווה גורם סיכון להתפתחות של סרטן המעי הגס[5]. קיימת השערה שהכנסת מטופלים להם הוסר פוליפ ניאופלסטי לתוכנית מעקב, תסייע בגילוי מוקדם של נגעים נוספים ובמניעת סרטן. אולם, היעילות של מעקב עם קולונוסקופיה לאחר הסרת פוליפים במניעה של סרטן המעי הגס הודגמה רק בעבודות אפידמיולוגיות ולא במחקרים רנדומליים פרוספקטיביים. עבודות אלו הראו סיכון של פי 3–4 לסרטן המעי הגס בקרב אנשים שלא הוכנסו לתוכנית מעקב מסודרת לאחר כריתת פוליפים במעי הגס[6].
בגילאים 50–75 אנו מצפים למצוא פוליפים ניאופלסטים בכ-30% מהנבדקים. עם השימוש הגובר באנדוסקופים בעלי רזולוציה גבוהה (high definition) ניתן להגיע לאחוזי גילוי של עד 50% [7][8]. בדיקות קולונוסקופיה למעקב אחרי כריתת פוליפים מהוות כ-20% מסך נפח בדיקות הקולונוסקופיה[9]. לאור כך, שימוש לא מושכל בקולונוסקופיה למעקב אחרי כריתת פוליפים יגרום למעמסה קלינית וכלכלית כבדה על המטופל ועל מערכת הבריאות.
גורמי סיכון
הצטבר מידע לגבי מאפיינים של פוליפים המנבאים סיכון מוגבר להתפתחות של סרטן המעי הגס. נוכחות של פוליפ בגודל מעל 10 מ"מ, או פוליפ המכיל מרכיב ווילוזי (villous architecture), או נוכחות של דיספלזיה גבוהה (high grade dysplasia) מגדירים את הפוליפ כאדנומה מתקדמת (advanced adenoma)[10][11]. נגעים מסוג זה מתקדמים והופכים לגידול סרטני בקצב של כ-5% בשנה אם הם לא נכרתים[12]. גורמי הסיכון הללו גם מושפעים זה מזה. לדוגמה, אנו יודעים שככל שהפוליפ גדול יותר, כך הוא יכיל מרכיבים היסטולוגיים מתקדמים, כגון דיספלזיה בדרגה גבוהה או מרכיב ווילוזי באחוזים גבוהים יותר[13]. יתרה מכך, נוכחות של פוליפ בגודל של מעל 10 מ"מ (שנכרת) מנבאת סיכון מוגבר לפתח סרטן המעי הגס במועד מאוחר יותר[10]. גורם נוסף המשפיע בצורה משמעותית על הסיכון להתפתחות של סרטן המעי הגס הוא מספר האדנומות שהתגלו בבדיקה. ריבוי פוליפים, ובמיוחד ריבוי פוליפים מתקדמים, מנבאים התפתחות של פוליפים מתקדמים וסרטן המעי הגס במועד מאוחר יותר[10].
חשיבות המעקב
נבדקים שבגופם התגלה והוסר פוליפ במהלך קולונוסקופיה, נמצאים בסיכון להימצאות פוליפים בכלל ופוליפים מתקדמים בעתיד[5]. מלבד הנטייה האישית של הפרט לפתח פוליפים במעי הגס, הנובעת מגורמים גנטיים, סביבתיים או שילוב שלהם, קיימים גורמי סיכון הקשורים ישירות למגבלות בדיקת הקולונוסקופיה. הסרה לא שלמה של פוליפ במהלך קולונוסקופיה אינה נדירה, וככל הנראה תורמת באופן משמעותי להתפתחות של interval cancer. כריתה לא שלמה נמצאה ב-7% מהפוליפים בגודל 5–9 מ"מ, בעד 23% מהפוליפים בגודל 15–20 מ"מ, ובעד 47% מהמקרים של פוליפים משוננים גדולים[14]. interval cancer יכול להיגרם גם כתוצאה מהחמצה של פוליפים בזמן קולונוסקופיה. גם קולונוסקופיה טובה אינה מגלה 100% מהפוליפים. עבודות שונות הדגימו שיעורי החמצות (miss rates) של 12-6% עבור פוליפים בגודל מעל 10 מ"מ ועד 27% לפוליפים בגודל קטן מ-5 מ"מ[15][16]. קולונוסקופיה כבדיקת מעקב יכולה למתן סיכון זה, על ידי מציאת פוליפים שהוחמצו בבדיקה קודמת או כאלה שנכרתו בצורה לא מלאה בטרם עברו התמרה לסרטן פולשני.
המלצות
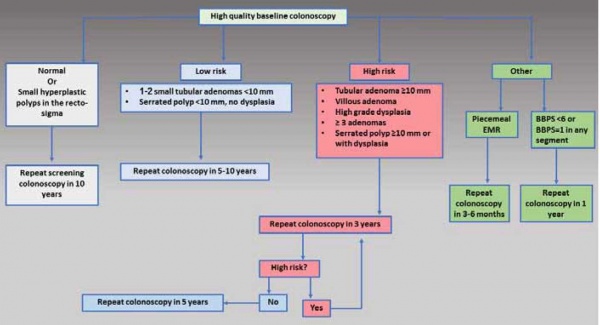
מספר איגודים מקצועיים ממליצים על מעקב עם קולונוסקופיה אחרי כריתת פוליפים במעי הגס. קיימת מידה מסוימת של חוסר אחידות בהגדרת קבוצות הסיכון ובהמלצות למעקב בין הקווים המנחים השונים, הנובעת בעיקר ממחסור בעבודות גדולות ואיכותיות בנושא. הקווים המנחים של כוח המשימה הרב-חברתי האמריקני (U.S. Multi-Society Task Force - MSTF) משנת 2012 ושל החברה האירופית לאנדוסקופיה של דרכי העיכול (European Society of Gastrointestinal Endoscopy - ESGE) משנת 2013, הם העדכניים ביותר, ושניהם מרוכזים סביב העיקרון של רמת סיכון נמוכה ורמת סיכון גבוהה לאדנומות עם אקסטרפולציה לפוליפים מסוג משונן (תרשים מס' 1)[17][18]. איכות העבודות עליהן נשענים כל הקווים המנחים אינה גבוהה, ורוב ההמלצות ניתנות כהמלצות חזקות עם איכות הוכחות בינונית עד נמוכה. לעומת זאת, בין כל הקווים המנחים קיים קונצנזוס המבוסס על הוכחות טובות, לכך שהתנאי הבסיסי לכל תוכנית מעקב מושתת על קולונוסקופיה ראשונה (בדיקת סריקה) איכותית עם הכנה טובה, הסרה של כל הפוליפים שמתגלים וריבוד (סטרטיפיקציה) של רמת הסיכון לנבדק הספציפי[19].
קולונוסקופיה ראשונה ללא אדנומות
נבדקים שעברו קולונוסקופיה איכותית בה לא נמצאו אדנומות כלל, או שנמצאו רק פוליפים היפרפלסטים באזור הרקטום והסיגמא, הם בקבוצת סיכון נמוכה ביותר. עבודות רבות הדגימו שפוליפים היפרפלסטים ברקטו-סיגמה אינם קשורים לסיכון מוגבר לפתח אדנומות מתקדמות או סרטן המעי הגס בעתיד[17]. לכן ההמלצה במקרים כאלו היא לבצע קולונוסקופיה מעקב כעבור עשר שנים בדומה לכלל האוכלוסייה.
קבוצת סיכון נמוך - low risk adenoma
קבוצת סיכון נמוכה מכילה נבדקים בעלי 1–2 אדנומות טובולריות קטנות מ-10 מ"מ. עבודות רטרוספקטיביות גדולות הדגימו שיעור דומה של סרטן מעי גס בין מטופלים מקבוצת סיכון זו שלא ביצעו מעקב לבין כלל האוכלוסייה. בנוסף, שכיחות של אדנומות מתקדמות במועד מאוחר יותר אינה מוגברת בקבוצה זו בהשוואה לנבדקים ללא אדנומות כלל בבדיקת הסקירה הראשונה, ולא קיים הבדל בשכיחות אדנומות מתקדמות במעקב של 3–5 שנים לעומת מעקב של 5–10 שנים. לאור כך, הקווים המנחים של ה-MSTF ממליצים על בדיקת מעקב אחרי 5–10 שנים, ואילו ה-ESGE ממליץ על בדיקת מעקב אחרי 10 שנים לקבוצה זו[17][18].
קבוצת סיכון גבוה - high risk adenoma / advanced adenoma
קבוצת סיכון זו מכילה נבדקים בעלי אדנומה טובולרית גדולה מ-10 מ"מ, אדנומה ווילוזית, אדנומה המכילה דיספלזיה בדרגה גבוהה או למעל משלוש אדנומות טובולריות. בקבוצה זו, עבודות אפידמיולוגיות גדולות הדגימו סיכון מוגבר פי 3–6 לחלות בסרטן המעי הגס ויעילות גבוהה של מעקב אנדוסקופי בהפחתת הסיכון לסרטן המעי הגס[6][20]. בנוסף, הסיכון לפתח אדנומות מתקדמות בעתיד מוגבר פי 5–7 בקבוצה זו בהשוואה לנבדקים ללא אדנומות בבדיקה הראשונה[18]. לאור כך, בקבוצה זו, מומלץ על בדיקת קולונוסקופיה למעקב כעבור שלוש שנים[17][18].
פוליפים מסוג משונן
פוליפים מסוג משונן נחשבים לנגעים טרום סרטניים מהם מתפתחים 30-20% ממקרי סרטן המעי הגס במנגנון מולקולרי של היפר-מטילציה המערב מוטציות 1-BRAF בשכיחות גבוהה ואי יציבות גנומית (microsatellite instability - MSI) בעד 50% מהמקרים[21]. פוליפים אלו שכיחים יותר בחלקו הימני של המעי הגס ויכולים גם להכיל אזורים עם דיספלזיה (דמוית אדנומה) המייצגים נגע מתקדם יותר פוליפים מסוג משונן, מיוצגים ביתר בקבוצה של interval cancer, ככל הנראה כתוצאה מהקושי בגילוי והסרה שלהם בזמן קולונוסקופיה. על בסיס הוכחות מעטות, פוליפ משונן קטן מ-10 מ"מ, שאינו מכיל דיספלזיה, מוגדר כסיכון נמוך וניתן להתייחס אליו בדומה לאדנומה בסיכון נמוך (low risk adenoma). לעומת זאת, פוליפ משונן בגודל של 10 מ"מ ומעלה או כזה המכיל דיספלזיה, מוגדר כקבוצת סיכון גבוהה ויש צורך להתייחס אליו כאל אדנומה בסיכון גבוה (high risk adenoma) מבחינת ההמלצות למעקב עם קולונוסקופיה[17][18].
מקרים מיוחדים
- נבדקים שנמצאו אצלם יותר מ-10 אדנומות בבדיקת סריקה של קולונוסקופיה, זקוקים לייעוץ גנטי בחשד לתסמונות של פוליפוזיס ובדיקת קולונוסקופיה למעקב בתוך פחות משלוש שנים
- נבדקים עם חשד לתסמונת פוליפוזיס משוננת (serrated polyposis syndrome) (נבדקים שלהם יותר מחמישה פוליפים מסוג זה פרוקסימלית לסיגמא, ששניים מהם גדולים מ-10 מ"מ, או נבדקים עם יותר מ-20 פוליפים מסוג זה בכל מיקום במעי הגס ובכל גודל), צריכים לקבל ייעוץ גנטי ולבצע מעקב שנתי עם קולונוסקופיה
- נבדקים שעוברים כריתה של פוליפ שטוח גדול מ-10 מ"מ במספר חתיכות (piecemeal), צריכים לבצע קולונוסקופיה להדגמת שלמות הכריתה בתוך שישה חודשים, לפני החלטה על פרוטוקול המעקב המתאים
סיכום
בעידן בו שיעורים הולכים וגדלים של האוכלוסייה מבצעים בדיקות סריקה לגילוי מוקדם של סרטן המעי הגס, קולונוסקופיות למעקב אחרי כריתת פוליפים יתפסו נפח הולך וגדל מסך הבדיקות המבוצעות, ויהוו נטל משמעותי על נבדקים ועל מערכת הבריאות. היעדר מחקרים פרוספקטיביים גדולים מקשה על מתן המלצות, אך נראה כי התועלת ארוכת הטווח מבדיקות קולונוסקופיה למעקב ברורה הרבה פחות מזו המופקת מבדיקת הקולונוסקופיה המשמשת לסריקה ראשונית. המידע שקיים ומשתקף בקווים המנחים של האגודות המקצועיות, מרמז שבדיקות קולונוסקופיה למעקב הן ככל הנראה משמעותיות בעיקר עבור אנשים בקבוצת הסיכון הגבוה.
ביבליוגרפיה
- ↑ Edwards BK, Noone AM, Mariotto AB, et al. Annual Report to the Nation on the status of cancer, 1975¬2010, featuring prevalence of comorbidity and impact on survival among persons with lung, colorectal, breast, or prostate cancer. Cancer. 2014 May 1;120(9):1290-314. Epub 2013 Dec 16.
- ↑ Zauber AG, Winawer SJ, O'Brien MJ, et al. Colonoscopic polypectomy and long-term prevention of colorectal-cancer deaths. N Engl J Med. 2012 Feb 23;366(8):687-96.
- ↑ Baxter NN, Goldwasser MA, Paszat LF, et al. Association of colonoscopy and death from colorectal cancer. Ann Intern Med. 2009 Jan 6;150(1):1-8. Epub 2008 Dec 15.
- ↑ Kahi CJ, Imperiale TF, Juliar BE, et al. Effect of screening colonoscopy on colorectal cancer incidence and mortality. Clin Gastroenterol Hepatol. 2009 Jul;7(7):770-5. Epub 2009 Jan 11.
- ↑ 5.0 5.1 Cottet V, Jooste V, Fournel I, et al. Long-term risk of colorectal cancer after adenoma removal: a population-based cohort study. Gut. 2012 Aug;61(8):1180-6. Epub 2011 Nov 22.
- ↑ 6.0 6.1 Brenner H, Chang-Claude J, Jansen L, et al. Role of colonoscopy and polyp characteristics in colorectal cancer after colonoscopic polyp detection: a population-based case-control study. Ann Intern Med. 2012 Aug 21;157(4):225-32.
- ↑ Regula J, Rupinski M, Kraszewska E, et al. Colonoscopy in colorectal-cancer screening for detection of advanced neoplasia. N Engl J Med. 2006 Nov 2;355(18):1863-72.
- ↑ Kahi CJ, Hewett DG, Norton DL, et al. Prevalence and variable detection of proximal colon serrated polyps during screening colonoscopy. Clin Gastroenterol Hepatol. 2011 Jan;9(1):42-6. Epub 2010 Oct 1.
- ↑ Lieberman DA, Holub J, Eisen G, et al. Utilization of colonoscopy in the United States: results from a national consortium. Gastrointest Endosc. 2005 Dec;62(6):875-83.
- ↑ 10.0 10.1 10.2 Winawer SJ, Zauber AG, O'Brien MJ, et al. Randomized comparison of surveillance intervals after colonoscopic removal of newly diagnosed adenomatous polyps. The National Polyp Study Workgroup. N Engl J Med. 1993 Apr 1;328(13):901-6.
- ↑ Brenner H, Hoffmeister M, Stegmaier C, et al. Risk of progression of advanced adenomas to colorectal cancer by age and sex: estimates based on 840,149 screening colonoscopies. Gut. 2007 Nov;56(11):1585-9. Epub 2007 Jun 25.
- ↑ Eide TJ. Risk of colorectal cancer in adenoma-bearing individuals within a deined population. Int J Cancer. 1986 Aug 15;38(2):173-6.
- ↑ Lieberman D, Moravec M, Holub J, et al. Polyp size and advanced histology in patients undergoing colonoscopy screening: implications for CT colonography. Gastroenterology. 2008 Oct;135(4):1100-5. Epub 2008 Jul 3.
- ↑ Pohl H, Srivastava A, Bensen SP, et al. Incomplete polyp resection during colonoscopy-results of the complete adenoma resection (CARE) study. Gastroenterology. 2013 Jan;144(1):74-80. Epub 2012 Sep 25.
- ↑ Rex DK, Cutler CS, Lemmel GT, et al. Colonoscopic miss rates of adenomas determined by back-to-back colonoscopies. Gastroenterology. 1997 Jan;112(1):24-8.
- ↑ Pickhardt PJ, Choi JR, Hwang I, et al. Computed tomographic virtual colonoscopy to screen for colorectal neoplasia in asymptomatic adults. N Engl J Med. 2003 Dec 4;349(23):2191-200. Epub 2003 Dec 1.
- ↑ 17.0 17.1 17.2 17.3 17.4 Lieberman DA, Rex DK, Winawer SJ, et al. Guidelines for colonoscopy surveillance after screening and polypectomy: a consensus update by the US Multi-Society Task Force on Colorectal Cancer. Gastroenterology. 2012 Sep;143(3):844-57. Epub 2012 Jul 3.
- ↑ 18.0 18.1 18.2 18.3 18.4 Hassan C, Quintero E, Dumonceau JM, et al. Post-polypectomy colonoscopy surveillance: European Society of Gastrointestinal Endoscopy (ESGE) Guideline. Endoscopy. 2013 Oct;45(10):842-51. Epub 2013 Sep 12.
- ↑ Ladabaum U, Schoen RE . Post-polypectomy surveillance that would please Goldilocks - not too much, not too little, but just right. Gastroenterology. 2016 Apr;150(4):791-6. Epub 2016 Feb 2.
- ↑ Atkin WS, Morson BC, Cuzick J. Long-term risk of colorectal cancer after excision of rectosigmoid adenomas. N Engl J Med. 1992 Mar 5;326(10):658-62.
- ↑ Legget B, Whitehall V. Role of serrated pathway in colorectal cancer pathogenesis. Gastroenterology. 2010 May;138(6):2088-100.
קישורים חיצוניים
- במה עמוד 33
המידע שבדף זה נכתב על ידי ד"ר אמיר קליין - מכון גסטרואנטרולוגיה, המרכז הרפואי רמב"ם; הפקולטה לרפואה ע"ש ברוס רפפורט, הטכניון, חיפה


 כניסה
כניסה  עקבו אחרינו בפייסבוק
עקבו אחרינו בפייסבוק