כולסטרול - Cholesterol
הופניתם מהדף Cholesterol לדף הנוכחי.
| מדריך בדיקות מעבדה | |
| כולסטרול | |
|---|---|
| Cholesterol | |
| מעבדה | כימיה בדם |
| תחום | משק השומנים בגוף |
| יחידות מדידה | מיליגרם לד"ל |
| טווח ערכים תקין | דם טבורי: זכרים - 44-103, נקבות - 50-108; גיל 0-4 שנים: (ז) - 114-203, (נ) - 112-200; גיל 5-9 שנים: (ז) - 121-202, (נ) - 126-205; גיל 10-14 שנים: (ז) - 119-202, (נ) - 124-201; גיל 15-19 שנים: (ז) - 113-197, (נ) - 119-200; גיל 20-24 שנים: (ז) - 124-218, (נ) - 122-216; גיל 25-29 שנים: (ז) - 133-244, (נ) - 128-222; גיל 30-34 שנים: (ז) - 138-254, (נ) - 130-230; גיל 35-39 שנה: (ז) - 146-270, (נ) - 140-242; גיל 40-44 שנים: (ז) - 151-268, (נ) - 147-252; גיל 45-49: (ז) - 158-276, (נ) - 152-265; גיל 50-54: (ז) - 158-277, (נ) - 262-285; גיל 55-59 שנים: (ז) - 156-276, (נ) - 172-300; גיל 60-64 שנים: (ז) - 159-276, (נ) - 172-297; גיל 65-69 שנים: (ז) - 158-274, (נ) - 171-303; גיל מעל 70 שנה: (ז) - 144-265, (נ) - 173-280. ערכי נורמה אלה מבוססים על ערכים ממוצעים של אוכלוסיה בריאה בארה"ב, והם גבוהים ב-2-6% מנתונים דומים של אוכלוסיות אירופיות, וגבוהים ב-10-15% מאוכלוסיות באסיה ואף יותר מכך באפריקה. הסיבה לערכים ממוצעים גבוהים יותר אלה נגזרת בעיקר מהרכב הדיאטה הצפון-אמריקנית העשירה יותר בשומנים. ערכי הנורמה באוכלוסיה אפרו-אמריקנית גבוהים בממוצע ב-10 מיליגרם לד"ל בהשוואה לאוכלוסיה הלבנה שם. |
| יוצר הערך | פרופ' בן-עמי סלע |
לערכים נוספים הקשורים לנושא זה, ראו את דף הפירושים – הפרעה בשומני הדם
מטרת הבדיקה
מדידת כולסטרול מתבצעת כחלק בלתי נפרד מפרופיל מלא של מדדים ביוכימיים בדם, שיכול להתבצע במסגרת בדיקות שגרה תקופתיות או במהלך אשפוז. בדרך כלל מתבצעת מדידת סך-כולסטרול, כחלק מפרופיל שומנים ביחד עם מדידת HDL וטריגליצרידים, כאשר רמת LDL נקבעת באופן חישובי מנתוני שלושת המדדים האחרים בעזרת נוסחת Friedewald. הערכת רמות כולסטרול, LDL, HDL וטריגליצרידים חיונית להערכת הסיכון לטרשת עורקים ומחלות קרדיו-וסקולאריות. מדדים אלה חיוניים גם להערכת מטבוליזם של השומנים בגוף, וכן לסיוע לאבחון מפגעים אחרים כגון מחלת כבד, תסמונת נפרוטית, דלקת הלבלב, או הפרעות בפעילות בלוטת התריס.
בסיס פיזיולוגי
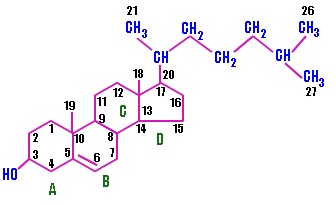
הנוסחה המולקולארית של כולסטרול היא C27H45OH ובהתאם משקלו המולקולארי הוא 386 דלטון. מולקולת כולסטרול מורכבת מ-3 מרכיבים: מבנה טבעתי המורכב מ-4 טבעות הידרוקרבוניות, זנב הידרוקרבוני על פחמן מספר 17, ושייר הידרוקסיל קוטבי על פחמן מספר 3 שמקנה לכולסטרול את הגדרתו כאלכוהול אך גם כסטרול. המבנה ה-4 טבעתי אופייני לכל ההורמונים הסטרואידים כגון טסטוסטרון ואסטרוגן, ואמנם כל הסטרואידים נוצרים מכולסטרול. שייר ה-OH של כולסטרול יכול ליצור קשרי מימן עם החמצן הקרבונילי של פוספוליפידים וספינגוליפידים בסביבתו הקרובה. כולסטרול הוא מוצק כעין דונג בטמפרטורת החדר, ונמס ב-150 מעלות. כולסטרול מסיס בכלורופורם, באתיל אתר או באלכוהול חם.
למרות השייר ההידרוקסיל הקוטבי, חלק הארי של מולקולת כולסטרול, הזנב ההידרוקרבוני והמבנה הטבעתי אינם קוטביים, לכן המולקולה בכללותה היא מסיסת שומן, ואינה מסוגלת להתמוסס בתווך מימי כמו פלזמת הדם, למרות שבהגדרה כהולסטרול היא מולקולה אמפיפאטית. זו גם הסיבה לכל שכולסטרול נע בדם כשהוא חלק מליפופרוטאינים דוגמת LDL ו-HDL.
ביוסינתזה של כולסטרול
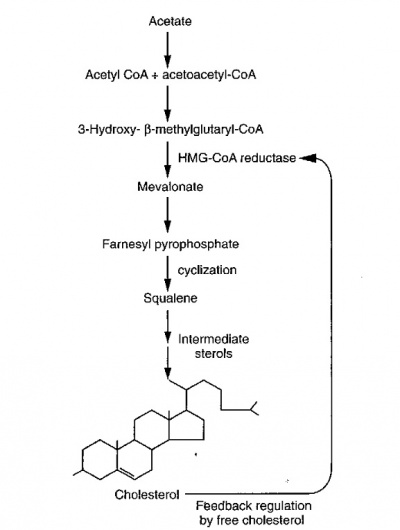
כ-20-25% מכלל הכולסטרול שהגוף מייצר מדי יום מיוצר בכבד, ורקמות אחרות בהן מיוצר כולסטרול הן בלוטות האדרנל, המעי, ואברי הרבייה. הסינתזה הנמשכת לאורך 37 שלבים, מתחילה ממולקולה אחת של אצטיל קואנזים A, המתקבלת מחמצון חלקי של גלוקוזה, וכן מפירוק של חומצות שומניות בתהליך חמצונן במיטוכונדריה. מולקולת acetyl-CoA אחת מגיבה עם מולקולת acetoacetyl-CoA, ליצירת 3-hydroxy-3-methylglutaryl CoA או HMG-CoA. המולקולה של HMG-CoA מחוזרת אז על ידי האנזים HMG-CoA reductase, ליצירה של mevalonate. במבוגרים, הכבד ודופן המעי מספקים למעלה מ-90% של הכולסטרול בפלזמה המגיע ממקורות אנדוגניים. יצירת כולסטרול בכבד, בניגוד לזו המתרחשת במעי, מעוכבת על ידי הכולסטרול המגיע מהמזון על ידי משוב שלילי. מדי יום הגוף מייצר באדם מבוגר במשקל 70 ק"ג 1 גרם כולסטרול, הן מיצור עצמי והן ממקורות המזון, כאשר קצב הייצור האנדוגני נקבע על ידי שלב אנזימטי זה שהוא בלתי הפיך ומעוכב על ידי סטאטינים. תכולת כולסטרול בגוף של אדם בוגר היא כ-35 גרם, כאשר רוב הכולסטרול מרוכז בממברנות תאי הגוף. צריכת הכולסטרול היומית במזון באוכלוסיה מערבית היא 200-300 מיליגרם.
קצב הפעולה של האנזים HMG-CoA reductase מווסת גם על ידי רמת כולסטרול בדם, וככל שזו גדלה, כך יורדת פעילות האנזים. בהמשך מסלול הסינתזה של כולסטרול, mevalonate מוסב על ידי דה-קרבוקסילציה ל-3-isopentenyl pyrophosphate על ידי 3 ריאקציות הדורשות ATP. שלוש מולקולות של isopentenyl pyrophosphate עוברות דחיסה ליצירת farnesyl pyrophosphate על ידי האנזים geranyl transferase. בשלב זה 2 מולקולות של farnesyl pyrophosphate נדחסות ברטיקולום האנדופלזמי על ידי האנזים squalene synthase ליצירה של squalene, והאנזים oxidosqualene cyclaseהופך squalene על ידי ציקלציה ל-lanosterol כאשר זה ברצף של 19 ריאקציות מורכבות הופך לכולסטרול. להלן תרשים של הריאקציות העיקריות במסלול יצירת כולסטרול.
הוויסות של ביוסיתזה של כולסטרול
ככל שקולטים מהמזון יותר כולסטרול, כך פוחתת יצירתו האנדוגנית, והיפוכו של דבר בקליטה זעומה של כולסטרול מהמזון. מנגנון הוויסות המרכזי הוא על ידי חישה של הכולסטרול התוך-תאי בתוך הרטיקולום האנדופלזמי על ידי החלבון SREBP הידוע כ- sterol regulatory element-binding protein 1 and 2. בנוכחות כולסטרול, SREBP נקשר ל-2 חלבונים נוספים, SCAP או SREBP-cleavage-activating protein וכן Insig1. כאשר רמת כולסטרול פוחתת, משתחרר Insig-1 מהקומפלקס SREBP-SCAP, מה שמאפשר לקומפלקס זה לנדוד ל-Golgi apparatus, שם מתפרק SREBP על ידי 2 האנזימים S1P ו-S2P (או site-1 and -2 protease) המשופעלים על ידי SCAP כאשר רמת כולסטרול נמוכה. חלבון SREBP המפורק נודד אז לגרעין התא ופועל שם כגורם שעתוק (transcription factor) על ידי שהוא נקשר ל-SRE או sterol regulatory element, המעודד שעתוק של 2 מרכיבים במכלול של הכולסטרול: הוא מעודד את יצירת הקולטן של LDL וכן את יצירת האנזים HMG-CoA reductase, וכך יצירה מוגברת של הקולטן ל-LDL מרחיקה חלקיקי LDL מהצירקולציה, בעוד האנזים מחיש יצירה אנדוגנית של כולסטרול.
אך מסתבר שיצירה אנדוגנית של כולסטרול יכולה להיחלש גם על ידי חישת רמת כולסטרול גבוהה בצירקולציה. האנזים HMG CoA reductase, מכיל חלק ציטופלזמטי האחראי לפעילות הקטליטית של האנזים, וגם חלק המקובע בממברנת התא, והאחרון משמש כחיישן האחראי לפירוק אנזים זה. כאשר רמות כולסטרול בדם גבוהות, מביאות לשינוי במצב האוליגומריזציה של החלק הממברנלי של האנזים האמור, מה שהופך את האנזים לחשוף יותר להרס בתוך ה-proteosome התאי.
תפקידיו הפיזיולוגיים של כולסטרול
אחד התפקידים המרכזיים של כולסטרול הוא בבניה של ממברנות תאים ובתמיכה בשלמותם, ובעיקר יש לכולסטרול תפקיד מרכזי בנזילות (fluidity) של ממברנות התאים, בטווח רחב של טמפרטורות פיזילוגיות. שייר ההידרוקסיל של הכולסטרול מגיב עם שיירים קוטביים של פוספוליפידים וספינגוליפידים בממברנה, כאשר החלקים ההידרופוביים של מולקולת כולסטרול (הגרעין הטבעתי הסטרואידי והזנב ההידרוקרבוני) מקובעים בשכבה השומנית של הממברנה לצד שרשראות לא-קוטביות של שומנים אחרים. על ידי התגובה עם הפוספוליפידים בממברנה, הכולסטרול מגדיל את קשיחותה ובכך מפחית את הנזילות שלה. לעומת זאת, המבנה ה-4 טבעתי של כולסטרול תורם להקטנת נזילות הממברנה, ומפחית את החדירות שלה לממסים ניטראליים במטענם החשמלי, כמו גם לפרוטונים או ליוני נתרן. למרות שרוב מכריע של כולסטרול נמצא בממברנה החיצונית של התא (plasma membrane), נמצא כמות קטנה שלו גם בממברנות של אברונים תוך-תאיים כמו מיטוכונדריה ורטיקולום אנדופלזמי.
בתוך ממברנת התא מתפקד כולסטרול גם לצורכי טרנספורט תוך-תאי, איתות בינתאי והעברת אותות עצביים. לאחרונה, הודגש תפקיד כולסטרול בתהליכי איתות תאי, על ידי סיוע ביצירת ערוצי מעבר שומניים (lipid rafts) בממברנת התא, המסייעים ביצירת הקשר בין קולטנים חלבוניים על פני התא עם מולקולות הנועדות להעביר איתות אל תוך התא (second messenger). בתאי עצב רבים, האקסון העטוף בשכבת מיאלין העשירה בכולסטרול, לצורך "בידוד חשמלי" של האקסונים באופן המסייע להעברת אות חשמלי לאורכם בדרכו לסינפסה.
בתוך התאים, כולסטרול משמש בתור precursor לכמה מסלולים ביוכימיים: בכבד, מוסב כולסטרול לחומצות מרה, הנאגרות בכיס המרה, ותפקידן להמסת שומנים במערכת העיכול ולסיוע לספיגתן במעי של מולקולות שומן כמו גם של הוויטמינים מסיסי שומן A, D, E ו-K. כולסטרול הוא גם פרקורסור חשוב בסינתזה של ויטמין D, והורמונים סטרואידים כקורטיזול ואלדוסטרון, כמו גם הורמוני מין כפרוגסטרון, אסטרוגנים וטסטוסטרון ונגזריהם.
טרנספורט של כולסטרול בפלזמה
כאמור, מתאפשרת תנועת כולסטרול בדם כחלק מקומפלקס עם ליפופרוטאינים בעלי מעטפה חיצונית אמפיפילית של חלבונים ופוספוליפידים, כאשר כולסטרול וטריגליצרידים נמצאים בליבת החלקיקים הללו. בדם קיימים מספר סוגים של ליפופרוטאינים נושאי-כולסטרול, ואלה בסדר צפיפות עולה הם כילומיקרונים, LDL, IDL, VLDL ו-HDL. ככל שהליפופרוטאין מכיל בהרכבו יותר שומן ופחות חלבון צפיפותו קטנה יותר. כולסטרול מופיע בחלקיקי ליפופרוטאינים אלה או ככולסטרול חופשי, או ככולסטרול-אסטר אליו מחוברת חומצת שומן. ההתקשרות של חלקיקי הליפופרוטאין לקולטנים על פני התאים אליהם מועבר כולסטרול, נעשית דרך אפו-ליפופרוטאינים, המשמשים כליגנדים להתקשרות לקולטנים שעל פני ממברנות תאי היעד.
כילומיקרונים, החלקיקים מובילי כולסטרול שצפיפותם נמוכה ביותר, מובילים שומנים הנספגים במעי לרקמת השריר ולרקמות נוספות הזקוקות לחומצות שומן ליצירת אנרגיה או לאגירת שומן. כולסטרול שאינו נצרך על ידי רקמת השריר, נותר בשאריות (remnants) של כילומיקרונים-עתירי כולסטרול הנקלטים בכבד. חלקיקי VLDL מיוצרים על ידי הכבד, ומכילים עודף טריגליצרידים וכולסטרול שאינם דרושים לכבד לצורך הסינתזה של חומצות מרה. בשעת המעבר בדם, נוצרים חלקיקי IDL (ליפופרוטאינים בעלי צפיפות ממוצעת) המכילים אחוז כולסטרול גבוה יותר. חלקיקי IDL יכולים בחלקם להיקלט על ידי קולטנים ל-LDL על פני תאי כבד, ואילו חלקם האחר ממשיך לאבד מולקולות טריגליצרידים בדם עד שהם הופכים לחלקיקי LDL, בהם ריכוז הכולסטרול הוא הגבוה ביותר.
אם כך, חלקיקי LDL הם הנשאים העיקריים של כולסטרול בדם, כאשר בכל חלקיק נמצאים כ-1,500 מולקולות כולסטרול-אסטר. מעטפת LDL מכילה רק מולקולה אחת של apolipoprotein B100, המזוהה על ידי קולטני LDL ברקמות ההיקפיות. כאשר הקומפלקס LDL-קולטן מוחדר לתא בתהליך אנדוציטוזה ליצירת חלקיק אנדוזום, המתאחה בהמשך עם ליזוזום אשר בתוכו עוברות מולקולות כולסטרול-אסטר הידרוליזה על ידי האנזים lysosomal acid lipase. הכולסטרול החופשי המשתחרר בתוך התא יכול לשמש לביו-סינתזה של ממברנת התא, או אם אין בו צורך הוא יכול לעבור שוב אסטריפיקציה ולהיות מאוחסן בתוך התא עד שיהיה בו צורך.
וויסות הסינתזה של הקולטנים ל-LDL נעשה על ידי SREBP, אותו חלבון רגולטורי המשמש לוויסות סינתזת כולסטרול בתגובה לרמתו בתאים. במצב של עודף כולסטרול בתא, נחסמת סינתזת הקולטנים ל-LDL, וכך נמנעת קליטת מולקולות LDL בתא, והיפוכו של דבר בחסר כולסטרול בתא. כאשר עודף מולקולות LDL שאינן יכולות להיקלט על ידי התאים נעות בזרם הדם, הן מתחמצנות ונקלטות על ידי מקרופאגים ההופכים לתאי קצף הנלכדים בדופן כלי הדם ותורמים לתהליך הופעת טרשת העורקים.
לעומת זאת, חלקיקיHDL משמשים להחזרת מולקולות כולסטרול בחזרה לכבד להפרשה מהגוף, או לרקמות אחרות בהן ישמש לסינתזה של הורמונים. נוכחות של כמות גדולה של חלקיקי HDL גדולים מזוהה עם שיפור מדדי בריאות כלי הדם. לעומתה, נוכחות של מספר קטן של חלקיקי HDL גדולים, כרוכה באופן בלתי-תלוי בהקדמות התהליך הטרשתי בעורקים.
מטבוליזם של כולסטרול
כולסטרול מתחמצן בכבד למגוון של חומצות מרה, שיכולות לעבור קוניוגציה עם מולקולות כגון גליצין, טאורין, סולפאט וחומצה גלוקורונית. תערובת של מלחי מרה שעברו קוניוגציה או כאלה שלא עברו קוניוגציה, יחד עם כולסטרול עצמו, מופרשים מהכבד לתוך המרה. בערך 95% מחומצות המרה נספגות מחדש מהמעי, והיתר מופרשות בצואה. ההפרשה והספיגה מחדש של חומצות מרה, יוצרות את הבסיס לצירקולציה האנטרו-הפאטית החיונית לעיכול וספיגה של שומנים מהמזון. בנסיבות מסוימות, לדוגמה כאשר ריכוזו של כולסטרול גדול יותר כמו בכיס המרה, הוא נוטה להתגבש ומהווה מרכיב עיקרי של רוב אבני כיס המרה, אם כי אבנים בהרכב של לציטין ובילירובין גם כן מופיעות בשכיחות נמוכה יותר. מדי יום בערך 1 גרם של כולסטרול שמקורו במזון, במרה, או בתאי מעי המתפרקים מגיע למעי הגס, שם הוא עובר מטבוליזם על ידי הפלורה של חיידקי המעי הגס. כאן מוסב כולסטרול בעיקר ל-coprostanol, שהוא סטרול שאינו נספג ומופרש בצואה.
הכולסטרול ברקמות הגוף נמצא בשווי משקל מתמיד עם הכולסטרול בפלזמה. בערך 55% מהכולסטרול המגיע מהמזון נספג במעי באופן תקין ונשמר בגוף, לעומת פחות מ-1 אחוז מהסטרולים האחרים במזון. למרות שרוב המאגר של כולסטרול מקורו בסינתזה de novo, מקורות דיאטתיים שלו הם בעלי תפקיד חשוב בשמירה על המאזן הכולל של כולסטרול בגוף. עודף כולסטרול בגוף הנובע מיצירה אנדוגנית שלו או מספיגה מהמזון, מופרש באופן בלעדי על ידי הכבד, או על ידי הפרשה ישירה של כולסטרול חופשי לתוך המרה, או על ידי הפיכתו לחומצות מרה, והפרשתו בצורה זו דרך המרה. הגוף מחדש מדי יום כ-2% מכלל מלאי הכולסטרול שלו, זאת כיוון שמדי יום 1-2 גרם של כולסטרול מופרשים בצואה.
כולסטרול מצוי כמרכיב בכל הסוגים של ליפופרוטאינים בפלזמה, אך 60% מסך כולסטרול בפלזמה נישא בחלקיקי LDL. כשני שליש מסך כולסטרול בפלזמה עובר אסטריפיקציה עם חומצות שומן ארוכות-שרשרת, כאשר באדם חומצה לינולאית היא חומצת השומן העיקרית הקשורה לכולסטרול. הידרוליזה של כולסטרול-אסטר מתבצעת בכבד, אם כי הסינתזה שלו מתבצעת בעיקר בפלזמה, על ידי טרנספר של שייר חומצת שומן מלציטין (lecithin) לכולסטרול חופשי על ידי האנזים LCAT או Lecithin:cholesterol acyltransferase. המצע הליפופרוטאיני המועדף על ידי LCAT הוא HDL, והכולסטרול-אסטר הנוצר ב-HDL מועבר בהמשך ל-LDL ול-VLDL, באופן חלקי בשחלוף עם טריגליצרידים.
אחד מתפקידי HDL הוא להעביר כולסטרול, בצורת כולסטרול-אסטר, מהרקמות לכבד במנגנון הבא: הכבד והמעיים מסנתזים apoA-I דל-שומן בדרך ליצירת חלקיק קדם-HDL דל-שומן. חלקיק אחרון זה מגיב עם ABCA1 או ATP-binding cassette transporter A1, הממוקם על פני מקרופאגים עורקיים, ומעביר כולסטרול חופשי לחלקיקי HDL דלי שומן. בשלב זה HDL-כולסטרול עובר אסטריפיקציה על ידי LCAT באופן המאפשר לחלקיק HDL לקלוט יותר כולסטרול חופשי. הכולסטרול-אסטר ב-HDL עובר טרנספר לחלקיקי LDL ו-VLDL, כאשר LDL מעביר לרקמות היקפיות כמו גם לכבד את תכולת הכולסטרול-אסטר, אלא שבכבד עובר כולסטרול-אסטר הידרוליזה ונכנס למאגר הכולסטרול החופשי בהפאטוציטים. ההשתחררות של כולסטרול חופשי מהכבד נעשית כפי שתואר למעלה על ידי המרה, או בהסבתו לחומצות מרה, או על ידי קליטתו המחודשת בחלקיקי VLDL.
מקורות כולסטרול במזון
בערך 98-99% מהשומן הנמצא במזון מורכב מטריגליצרידים, מתוכם 92-95% הם חומצות שומן והיתר הוא גליצרול. יתר מכסת 1-2% של השומן במזון מכילה כולסטרול, פוספוליפידים, דו-גליצרידים, חד-גליצרידים, ויטמינים מסיסי שומן, סטרואידים, terpenes ושומנים אחרים. רוב הטריגליצרידים מכילים ארבע או חמש חומצות שומן עיקריות, רוויות ובלתי רוויות. חלק קטן של חומר שאינו ניתן לעיכול בשומנים שבמזון מורכב מסטרולים, כהלים שומניים, פיגמנטים, הידרוקרבונים ואסטרים גליצרולים. רוב הסטרולים מורכבים מכולסטרול, אך הם תלויים בסוג הדיאטה, כאשר פיטוסטרולים המיוצרים בצמחים מהווים כצפוי מרכיב עיקרי בקליטת סטרולים באנשים בעלי דיאטה צמחונית או טבעונית.
כיוון שפיטוסטרולים המיוצרים בצמחים מתחרים עם כולסטרול מהחי על יכולת הספיגה מהמעי וכך הם יכולים להפחית פוטנציאלית את ספיגת כולסטרול לדם, יש המצדדים בצריכה של פריטי-מזון עתירי פיטוסטרול כגון תכשירים הידועים כ-nutraceuticals, שנמצאו במחקרים אחדים כבעלי יכולת להפחית רמת LDL בדם. יש המלצות עדכניות של ממסדים רפואיים כ-FDA, EFSA, ATP III ו-Health Canada, על צריכה יומית של פיטוסטרולים במינון של 1.6-3.0 גרם, כאשר מחקר עדכני מצביע על הפחתה של 8.8% ברמת LDL בצריכה יומית של 2.15 גרם פיטוסטרול. מנגד, יש המעלים ספקות לגבי היתרונות של דיאטה מועשרת בפיטוסטרולים. מקובל שכאשר תאי רירית המעי סופגים פיטוסרולים במקום כולסטרול, הם מפרישים מחדש את הפיטוסטרולים לצינור העיכול.
רוב הכולסטרול המגיע מהמזון עובר אסטריפיקציה, ומולקולות של כולסטרול-אסטר אינן נספגות היטב במעי. הגוף מפצה על ספיגת עודף כולסטרול בהפחתת הסינתזה העצמית שלו. מסיבות אלה צריכת כולסטרול מהמזון היא בעלת השפעה מוגבלת על הרמה הכללית של כולסטרול בגוף או על ריכוז כולסטרול בדם. הכבד מפריש כולסטרול בצורתו החופשית דרך המרה לצינור העיכול, ובערך 50% מהכולסטרול המופרש נספג מחדש במעי הדק וחוזר למחזור הדם. שומנים רוויים, חד בלתי רוויים ורב בלתי רוויים ידועים ככאלה המגבירים רמות HDL, בעוד ששומנים בלתי-רוויים מעלים רמות LDL בדם. שומני טרנס נמצאו מפחיתים רמת HDL, אך מעלים רמת LDL. ה-USDA ממליץ לאלה המבקשים להפחית רמת כולסטרול בדמם על ידי איזון דיאטתי, לצרוך מזון המכיל פחות מ-7% שומנים רוויים ופחות מ-200 מיליגרם כולסטרול ביום.
תכולת כולסטרול במזון: איגוד הלב האמריקני (AHA) ממליץ על צריכת כולסטרול יומית שאינה עולה על 300 מיליגרם. לאלה עם רמות LDL גבוהות, או כאלה הנוטלים תרופות להפחתת רמת כולסטרול, מומלץ על צריכה יומית של 200 מיליגרם כולסטרול במזון.
| סוג המזון מקור הכולסטרול | רמת כולסטרול במ"ג, לכל 100 גרם ממנת המזון האמור |
|---|---|
| חלמון ביצה בלתי מבושלת | 1234.9 |
| כבד תרנגולת (אפוי, מבושל) | 561.2 |
| ביצה שלימה (מבושלת, מטוגנת) | 456.5 |
| טפלי תרנגולת (giblets) מבושלים או מטוגנים | 442.1 |
| ביצה שלימה לא מבושלת | 424.0 |
| בשר בקר, מבושל או מטוגן | 381.2 |
| טפלי תרנגול הודו מבושלים או מטוגנים | 289.0 |
| סרטנים (משומרים) | 251.6 |
| חמאה | 246.0 |
| נקניק מבשר חזיר | 179.9 |
| סרטנים מבושלים או מטוגנים | 177.8 |
| כופתאות קמח תירס גס מטוגנות (Hush puppies) | 173.1 |
| עוגת הבית | 169.8 |
| בשר עגל בכל צורת הגשה | 134.1 |
| גבינת פילדלפיה (15% שומן) | 54.0 |
| גבינת קוטג' (9%) | 27.0 |
| שוקולד חלב | 14.0 |
| שוקולד מריר | 0.3 |
רמה רצויה של כולסטרול בדם ושיקולי ההערכה המעבדתית שלה
דו"ח המצוטט תדירות של "התכנית הלאומית לחינוך בנושא כולסטרול" (NCEP), ממליץ על רמת סך-כולסטרול שלא תעלה על 200 מיליגרם לד"ל, כאשר רמות כולסטרול בין 200-239 מיליגרם לד"ל מוגדרות כ"רמות גבוליות של סיכון גבוה", ואילו רמות כולסטרול מעל 240 מיליגרם לד"ל נכללות בהגדרה של "סיכון גבוה". גם ה-AHA שותף לתחומי רמות אלה של כולסטרול הנמדדות בצום. כיום, הדגש הוא על רמת LDL מתוך סך-כולסטרול שתהיה נמוכה מ-100 מיליגרם לד"ל, ולאחרונה יש אף המצדדים ביעד מטרה עליון ל-LDL של 70 מיליגרם לד"ל, לגבי אלה הנמצאים בסיכון גבוה למחלות קרדיו-וסקולאריות. יש המצדדים במדד יעד נוסף, והוא היחס בין סך-כולסטרול ל-HDL האמור להיות קטן בהרבה מיחס של 5:1 בגברים, וקטן מ-4.4:1 בנשים.
סך-כולסטרול מוגדר כסכום הריכוזים בדם של LDL, HDL ו-VLDL, כאשר בשגרת המעבדה נמדדים רק רמות סך-כולסטרול, HDL וטריגליצרידים, כאשר רמת VLDL מוערכת כרמת טריגליצרידים מחולקת ב-5, ורמת LDL מוערכת על פי נוסחת Friedwald:
Estimated LDL = [total cholesterol] − [total HDL] − [triglyceride]/5
מדידה ישיר של רמת LDL מבוצעת כאשר רמות טריגליצרדים נמצאות מעל 400 מיליגרם לד"ל, שכן אז הערכת רמות VLDL וממילא זו של LDL, אינה מדויקת. לנוסחת Friedwald יש מגבלות גם בנוכחות כילומיקרונים, וכן במטופלים עם dysbetalipoproteinemia (type III hyperlipoproteinemia), וכן אם לא חלפו 12 שעות מהארוחה האחרונה בגלל עליה של 20-30% ברמת טריגליצרידים, או תוך 24 שעות מצריכה ניכרת של אלכוהול.
מפגעים קליניים ותרחישים הקשורים לרמות מוגברות של כולסטרול
היפרליפופרוטאינמיה משפחתית או פוליגנית מסוג IIa ו-IIb , וכן מסוג I, IV ו-V, היפרליפידמיה משפחתית משולבת, familial dys-β-lipoproteinemia type III, היפר-α-ליפופרוטאינמיה, היפר-ליפופרוטאינמיה שניונית למחלה הפאטו-צלולרית, עימדון מרה (כולסטזיס) תוך וחוץ-כבדי, גלומרולו-נפריטיס, תסמונת נפרוטית, כשל כליות כרוני, מחלה ממאירה של בלוטות הלבלב והערמונית, היפו-תירואידיזם, צינית (gout), מחלת לב איסכמית, הריון, סוכרת מסוג 2, אלכוהוליזם, analbuminemia, dysgammaglobulinemia, מחלות אגירת גליקוגן מסוג I (מחלת von Gierke), מסוג III ו-IV, תסמונת Werner, אנורקסיה נרבוזה, היפר-קלצמיה אידיופתית, דיסגלובולינמיה כגון פארא-פרוטאינמיה או α-גלובולין מוגבר במחלת לופוס, תסמונת Cushing, השמנת יתר, עישון, מחלת לב כלילית, צמקת מרתית ראשונית, היפרכולסטרולמיה שניונית למחלת כבד חסימתית, familial defective apoB-100 היפרכולסטרולמיה פוליגנית (ספוראדית), פורפיריה סירוגית חריפה, חסר מבודד של הורמון גדילה (hGH). בחורף יש נטייה לעליה ברמת כולסטרול לעומת מדידת כולסטרול בקיץ, כאשר בגברים נרשמת עליה ממוצעת ב-2.2 מיליגרם לד"ל, ובקרב נשים ב-6.0 מיליגרם לד"ל.
מפגעים קליניים ותרחישים הקשורים לרמות מופחתות של כולסטרול
חוסר α-ליפופרוטאין (מחלת Tangier), היפו-β-ליפופרוטאינמיה או a-β-lipoproteinemia, נמק הפאטו-צלולרי, מחלה ממאירה של הכבד, מיאלומה, לויקמיה מיאלוציטית כרונית. מאקרוגלובולינמיה ע"ש Waldenstrom, היפר-תירואידיזם, מפגעי ספיגה של המעי, תת-תזונה, אנמיה מגלובלסטית, אנמיה סידרובלסטית, תאלאסמיה, פוליציטמיה וֶרָה, מיאלופיברוזיס, כוויות נרחבות, שטף דם מוחי, COPD, פיגור שכלי ותזונה לא מאוזנת, rheumatoid arthritis, מצבי דלקת כללית, intestinal lymphangiectasia. כמו כן מתקבלת תוצאת כולסטרול מופחתת בתקופת התאוששות מהתקף לב, איבוד משקל משמעותי באנשים כבדי משקל, בדיאטה דלת כולסטרול או עתירה בשומנים רב בלתי רוויים.
גורמי סיכון לרמה מוגברת של כולסטרול
- גנטיקה: גורמים תורשתיים הם כנראה בעלי ההשפעה המצטברת הניכרת ביותר על רמת כולסטרול בדם. כמחצית מכלל המקרים של היפר-כולסטרולמיה הם בעלי בסיס גנטי.
- גיל: בלידה רמת כולסטרול נעה סביב 65 מיליגרם לד"ל, והוא עולה בהדרגה עם הגיל בערך ב-1.5 מיליגרם לד"ל מדי שנה. גיל מעל 45 שנה בגברים ו-55 שנה בנשים נחשב כגורם סיכון לרמת כולסטרול מוגברת.
- מין: נשים בגיל שלפני חידלון הווסת, נוטות לרמות כולסטרול נמוכות מאלו של גברים באותו גיל, אם כי בגיל המעבר רמות הכולסטרול בנשים משתוות ואף עולות במקצת מעל רמות כולסטרול בגברים באותו גיל, בהם רמת כולסטרול מגיעה לטווח הערכים העליון בגיל 50-65 שנה.
- חוסר פעילות גופנית: משטר חיים פעיל מבחינת פעילות גופנית, משפיעים להפחתת רמת כולסטרול, ופעילות גופנית סדירה של 30 דקות לפחות מדי יום, כרוכה בהפחתת רמת כולסטרול בדם.
- עישון סיגריות: מקובל על בסיס מחקרים אפידמיולוגיים באוכלוסיות דולות, כמעלה רמת סך-כולסטרול.
- עודף משקל (obesity): מעלה רמת כולסטרול, והפחתת משקל מסייעת להפחתת רמת כולסטרול. המלצות עדכניות של NCEP ATP III מדגישות את הצורך להפחית עודף משקל, ולשמור על BMI שבין 23.0-27.0 לשמירה על רמה נאותה של כולסטרול. מדד אחד המקובל לשמירה על סף משקל גבוה הוא מדד היקף המותניים שלא יעלה על 102 ס"מ בגברים, או על 89 ס"מ בנשים.
- הורמונים: הורמון גדילה (GH), תירוקסין (T4) וגלוקגון מפחיתים רמת כולסטרול בדם, בעוד סטרואידים אנאבוליים ופרוגסטינים מעלים אותה. הפחתה ברמת אסטרוגנים בנשים מבוגרות כרוכה בעליה ברמת כולסטרול.
- דיאטה: שומנים רווים במזון מעלים רמת כולסטרול בדם, בעוד שומנים רב-בלתי רוויים מפחיתים את רמתו. גם שומני טרנס מעלים רמת כולסטרול, כמו גם פריטי מזון עתירים בכולסטרול המפורטים בטבלה. שמן דגים מפחית רמת טריגליצרידים וליפופרוטאין (a) יותר מאשר הוא מפחית רמת כולסטרול. ההמלצות העדכניות מדגישות שרמת שומנים רוויים לא תעלה על 7% מכלל הצריכה הקלורית, ושסך השומנים בדיאטה לא יעלה על 35% מכלל הקלוריות הנצרכות, עם צריכת כולסטרול יומית שלא תעלה על 200 מיליגרם. צריכת פירות וירקות שריכוז הסיבים בהם גבוה יחסית, טובה לשמירה על רמת כולסטרול נאותה.
- תכשירים ותרופות המעלים רמת כולסטרול כתוצאה מהשפעה פיזיולוגית
ACTH, מלחי מרה, amiodarone, אנדרוגנים, קטכולאמינים, גלוקו-קורטיקוסטרואידים, levodopa, ציקלוספורין, disulfiram, רטינואידים, carbamazepine, דיאטה עתירת כולסטרול או שומנים רוויים, phenothiazines, מעכבי פרוטאזות לטיפול ב-HIV, משתנים ממשפחת התיאזיד (השפעה קלה), isotretinoin ,ergocalciferol (במינונים גבוהים), micronazole ,etretinate, חומצב כנודאוקסי-כולית (chenodiol).
- תכשירים ותרופות המביאים לתוצאה מוגברת של כולסטרול כתוצאה מהשפעה אנליטית
חומצה אסקורבית (ויטמין C) בתלות שיטת הבדיקה, בילירובין מוגבר, β-hydroxysterols.
- תכשירים ותרופות המפחיתים רמת כולסטרול כתוצאה מהשפעה פיזיולוגית
asparaginase, חומצה אמינו סליצילית, carbutamide, תכשירים קושרי חומצות מרה כגון cholestyramine ו-colestipol, קלונידין, clomiphene, הפארין, doxazosin ,prazosin, אסטרוגנים, fenfluramine, תירוקסין, hydralazine, אינטרפרון, tacrolimus, נאומיצין, sitosterols, צריכה ממושכת של אלכוהול, סטאטינים, cyproterone acetate. נגזרות של פיבראט כגון clofibrate ו-gemfibrozil מעודדים פעילות האנזים lipoprotein lipase, מפחיתים הפרשת LDL והגברת יצירת קולטנים ל-LDL על ידי התקשרות ל-peroxisome proliferator- activated receptor α. ניאצין חוסם את פירוק השומנים מה שמביא להפחתת רמת חומצות שומן חופשיות בדם, ובהתאם מפחית הפרשת VLDL וכולסטרול מהכבד. ketoconazole (במינון גבוה), הלופרידול, כלורטטראציקלין, probucol. התכשיר ezetimibe מעכב ספיגת כולסטרול במעי, ואילו orlistat מונע ספיגת כולסטרול על ידי הפחתת הפרשת ליפאזה מהלבלב והמעי.
- תכשירים ותרופות המפחיתים רמת כולסטרול כתוצאה מהשפעה אנליטית
חומצה אסקורבית (ויטמין C) בתלות בשיטת הבדיקה, בילירובין (בתלות בשיטת הבדיקה).
רמת כולסטרול בנוזל השדרה (CSF): בדיקה המבוצעת לעתים נדירות כאשר הרמה התקינה היא מתחת ל-0.5 מיליגרם לד"ל. רמות מוגברות כולסטרול בנוזל השדרה יכולות להתקבל במקרים של דלקת קרום המוח, גידול או מורסה מוחית, בשטף דם מוחי, וגם בטרשת נפוצה, לעומת זאת, רמה נמוכה במיוחד של כולסטרול בנוזל השדרה מזוהה עם ניוון צרבאלי או קורטיקאלי.
הוראות לביצוע הבדיקה
מומלץ על ידי ה-AHA שגברים מעל גיל 25 שנה או נשים מעל גיל 35 שנה יבצעו מדידת כולסטרול אחת ל-5 שנים גם בבריאות מלאה, ותדירות הבדיקה תהיה תכופה יותר באלה עם גורמי סיכון משמעותיים למחלה קרדיו-וסקולארית, או באלה עם רקע משפחתי של מחלת לב או רמת שומנים גבוהה בדם. הבדיקה מתבצעת לאחר צום של 9-12 שעות, כאשר הדם נלקח במבחנה כימית (פקק אדום או צהוב) או במבחנת ספירת-דם (EDTA, פקק סגלגל) או במבחנת הפארין (פקק ירוק), אך לא במבחנה המכילה אוקסלאט, פלואוריד או ציטראט. הפרדת הנסיוב או הפלזמה מהכדוריות האדומות חייבת להתבצע לא יאוחר משעתיים מנטילת הדם, והדגימה יציבה 5-7 ימים בקירור, או שלושה חודשים בהקפאה במינוס 20 מעלות, או לזמן בלתי מוגבל בטמפרטורה של מינוס 70 מעלות. יש להימנע מהקפאות והפשרות חוזרות. בלקיחת הדם יש להימנע משימוש ארוך והדוק מדי בחוסם העורקים.
יש לפסול דגימת דם המוליטית באופן משמעותי, מחשש לתוצאה מוגברת כזובה של כולסטרול. בפלזמה (מבחנת EDTA) תוצאות כולסטרול מתקבלות נמוכות ב-3-6% מאלה המתקבלות בנסיוב (מבחנה כימית). יש להימנע משימוש בחומרי שימור בנסיוב כגון נתרן אזיד או thimerosal, שכן אלה נוטים להפחתה ברמת הכולסטרול הנמדד.
יש להימנע משמירת נוזל הבדיקה בטמפרטורת החדר, שכן במצב זה עלולים להשתנות היחסים בין כולסטרול חופשי לכולסטרול-אסטר, שבמצב נורמאלי הם 25-35% כולסטרול חופשי ו-65-75% כולסטרול אסטר, מסך הכולסטרול, כתוצאה מפעילות האנזים LCAT או lecithin-cholesterol acyltransferase. שיטות המדידה האנזימטיות של כולסטרול החליפו בשנים האחרונות של שיטת המדידה הכימית הקלאסית הידועה כשיטת Liebermann-Burchard. לשיטות האנזימטיות יש ספציפיות טובה יותר לכולסטרול, אם כי בשיטה בה נעשה שימוש בכולסטרול אוקסידאזה, האנזים הזה אינו מגיב עם3β-hydroxycholesterols כגון DHEA או pregnenolone, הנמצאים בדרך כלל בנסיוב אדם בכמויות נמוכות מאוד.


 כניסה
כניסה  עקבו אחרינו בפייסבוק
עקבו אחרינו בפייסבוק