נוהל לניסויים רפואיים בבני-אדם - הליך אישור בקשה חדשה לניסוי רפואי
|
| ||
|---|---|---|
| נוהל לניסויים רפואיים בבני-אדם - חוזר משרד הבריאות | ||

| ||
| תחום | מנהל רפואי | |
| מספר החוזר | נוהל מס' 14, עדכון 2016 כולל תיקון מיום 29/05/2017 | |
| סימוכין | נכתב בהתאם לתקנות בריאות העם (ניסויים רפואיים בבני אדם) התשמ"א 1980 | |
| קישור | באתר משרד הבריאות | |
| תאריך פרסום | 1 בפברואר 2016, תיקון מיום 29/05/2017 | |
לערכים נוספים הקשורים לנושא זה, ראו את דף הפירושים – זכויות החולה
ערך מורחב – נוהל לניסויים רפואיים בבני-אדם - הנוהל
הליך אישור בקשה חדשה מתבסס על תקנות בריאות העם, כמפורט:
החוקר הראשי יגיש את הבקשה לניסוי לוועדת הלסינקי של המוסד הרפואי.
הבקשה תיבדק לשלמותה על פי טופס 9.
ועדת הלסינקי תדון בכל בקשה, בין אם זו נדרשת לאישור משרד הבריאות ובין אם לא, ותקבע אם לאשר את הבקשה; לבקש תיקונים/השלמות או לדחותה.
יושב ראש הוועדה יחתום על טופס אישור ועדת הלסינקי (טופס 6 או טופס 16[1]) לאחר שהוועדה מאשרת את ביצוע הניסוי.
הוועדה יכולה לדרוש השלמות/התיקונים טרם אישורה הסופי של בקשה (אישור בהתניה). במקרה זה, על החוקר להעביר לוועדה את המסמכים המתוקנים בהתאם לכל הדרישות, בצירוף טופס 12. לאחר בדיקת ההשלמות/התיקונים, יו"ר הוועדה רשאי לחתום על טופס אישור ועדת הלסינקי (טופס 6).
כמו כן, הוועדה/יו"ר יסווגו את הבקשה כניסוי "מיוחד" או כניסוי "שאינו מיוחד", בהתאם לקריטריונים המפורטים בפרק 4. ניסויים "מיוחדים" יועברו לאישור מנהל המוסד הרפואי כמפורט בסעיף 5.1.
ניסויים "לא מיוחדים" יועברו לאישור משרד הבריאות, כמפורט בסעיף 5.2.
כל בקשה שקבלה אישור של ועדת הלסינקי: ניסויים מיוחדים וניסויים שהוחלט בישיבת הוועדה שאינם מיוחדים, תישלח במלואה, בגרסה מעודכנת המתאימה לתאריכים הכתובים בטופס 6 המצורף לבקשה, באופן מקוון למשרד הבריאות. עבור בקשות שסווגו כניסויים שאינם מיוחדים, בתכשירים או באמ"ר (אביזרים ומכשירים רפואיים), טופס 6 יועבר למשרד הבריאות מאוחר יותר, כמפורט בסעיף 5.2.1.
- כל החלטות הוועדה (אישורים ודחיות) חייבות להיות מנומקות ומתועדות בכתב בפרוטוקול הישיבה.
לאחר כל ישיבה של ועדת הלסינקי, מזכירות הוועדה תעביר למחלקה לניסויים קליניים במשרד הבריאות את פרוטוקול הדיון של הישיבה, כמפורט בפרק 17.
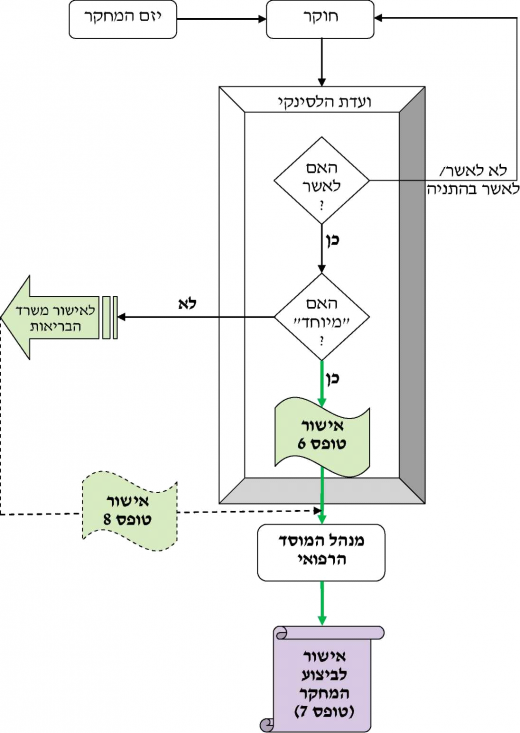
לסיכום, הליך כללי של טיפול בבקשות חדשות לניסויים רפואיים - במוסד הרפואי מתואר להלן באיור 2.
- הטיפול בבקשות חדשות לניסויים רפואיים מיוחדים - במוסד הרפואי
- ועדת הלסינקי תעביר לחוקרים הראשיים את החלטותיה לגבי הבקשות לניסויים רפואיים, אשר נדונה על ידה. אישורי ועדת הלסינקי של המוסד הרפואי (טופס 6) יועברו לחוקר הראשי עם עותק למנהל
- טרם אישור הניסוי על-ידי המנהל, ועדת הלסינקי תוודא: שהניסוי נרשם באתר ה-MOH, Ministry Of Health (כמפורט להלן בפרק 6); שההסכם החוזי לביצוע הניסוי בין היוזם למוסד הרפואי (כמפורט להלן בפרק 7) חתום על-ידי כל הנוגעים בדבר; שהביטוח מוסדר (תיקון מיום 29/05/2017)
- המנהל ינפיק אישור לניסוי רפואי לחוקר הראשי, ובו פירוט התנאים וההגבלות (טופס 7). העתק מאישור המנהל יועבר למנהל בית המרקחת במוסד הרפואי (על פי הצורך). החוקר יעביר עותק מהאישור ליזם הניסוי
- החוקר רשאי להתחיל בביצוע הניסוי הרפואי רק לאחר קבלת אישור זה.
- הטיפול בבקשות חדשות לניסויים רפואיים לא מיוחדים - במוסד הרפואי
- הליך מקביל :
עבור בקשות לניסויים קליניים בתכשירים ובאמ"ר - יו"ר הוועדה יקבע בתוך 48 שעות מקבלת הבקשה השלמה, אם יש צורך באישור נוסף של משרד הבריאות, על-פי הקריטריונים וההגדרות המפורטים בפרק 4. היזם יוכל לצרף את המלצתו/נימוקו לסיווג הבקשה כניסוי מיוחד/לא מיוחד. לאחר סיווג הבקשות כניסויים לא מיוחדים, אלו יועברו מיד, באופן מקוון, למשרד הבריאות. הדיון בבקשה בוועדת הלסינקי ובמשרד הבריאות יתנהל במקביל.
הודעה על סיווג הבקשה כ"לא מיוחד" תשלח לנציג היזם (פרטי התקשרות בטופס 1).
אם הוועדה מאשרת את הבקשה ללא הערות, יו"ר הוועדה יחתום על טופס אישור ועדת הלסינקי (טופס 6). טופס זה ישלח באופן מקוון וישלים את מסמכי הבקשה במשרד הבריאות.
אם הוועדה דרשה השלמות/תיקונים לבקשה, הודעה על כך תשלח לחוקר ולמשרד הבריאות.
אם משרד הבריאות דרש השלמות/תיקונים לבקשה, הודעה על כך תשלח לוועדת הלסינקי וליזם.
החוקר יעביר לוועדה את המסמכים המתוקנים בהתאם לכל הדרישות, בצירוף טופס שינויים (טופס 12). לאחר אישור ההשלמות/התיקונים, יו"ר הוועדה יחתום על טופס אישור ועדת הלסינקי (טופס 6). טופס 6 והמסמכים המתוקנים ישלחו באופן מקוון וישלימו את מסמכי הבקשה המקוונת במשרד הבריאות.
בנוסף, טופס 6 וכן המסמכים המתוקנים בגרסת "עקוב אחר שינויים" ישלחו בעותק מודפס למשרד הבריאות, להשלמת מסמכי הבקשה המודפסת - הממשק בין המערכת הממוחשבת של ועדת הלסינקי לבין זו של משרד הבריאות.
הממשק בין המערכת הממוחשבת של ועדת הלסינקי לבין זו של משרד הבריאות. עותק אלקטרוני של הבקשה יועבר מוועדות הלסינקי למשרד הבריאות.
במוסדות רפואיים המשתמשים במערכת "מטרות", הגשת הבקשה לוועדה מייצרת עותק אלקטרוני.
במוסדות האחרים, החוקר יגיש לוועדה עותק אלקטרוני המכיל את כל מסמכי הבקשה. עותק זה יכלול את טופס 1 כקובץ PDF חתום וקובץ doc) WORD שאינו חתום) לצורך הקלדה ידנית במשרד הבריאות.
לכל בקשה חדשה הנקלטת במשרד הבריאות יועבר בממשק היזון-חוזר אשר יעדכן את מספר הבקשה במשרד הבריאות ותאריך הקליטה.
רשימת המסמכים המפורטת של הבקשה (קיט מלא) מפורט בטבלה מסי 1.
העותק האלקטרוני יכיל קבצים בגודל עד 80 mega; בפורמטים מקובלים: doc, xIs, pdf, zip. קבצים מוצפנים לא יתקבלו.
העברת קובצי המידע והמסמכים מהמרכזים הרפואיים למשרד הבריאות תתבצע בצורה מאובטחת - אופן העברת הבקשות למשרד הבריאות:
בקשות הנדרשות לאישור משרד הבריאות, בין אם סווגו לדיון במקביל ובין אם סווגו כבקשות לא מיוחדות בדיון הוועדה (ניסויים בתרפיות מתקדמות, ניסויים גנטיים, ניסויים בהפריית אישה שלא כדרך הטבע וניסויים ללא מוצר מחקר) ישלחו גם בעותקים מודפסים, כמפורט להלן:- בקשות לניסויים רפואיים בתכשירים יועברו ליחידה לניסויים קליניים בתרופות באגף הרוקחות בעותק מודפס
- בקשות לניסויים רפואיים באמ"ר וכן בקשות לניסויים בתרפיות מתקדמות, יועברו ליחידה לניסויים קליניים באמ"ר באגף הרוקחות בחמישה עותקים מודפסים
- בקשות לניסויים הנדרשים לאישור הוועדה העליונה לניסויים רפואיים בבני-אדם יועברו למדען הראשי, לידי מרכז הוועדה העליונה, בשלושה עשר עותקים, מהם שלושה מודפסים. יתר העותקים יוגשו על גבי דיסקים
- כל יתר הבקשות לניסויים רפואיים - יועברו ליחידה לניסויים קליניים בתרופות באגף הרוקחות, בעותק אחד מודפס
- הליך מקביל :
- תפקידי היזם בהליך אישור בקשה חדשה לניסוי רפואי
- הגשת עותק אלקטרוני לחוקר
היזם יעביר לחוקר עותק אלקטרוני של הבקשה המלאה. טופס 1 יהיה בקובץ WORD. לאחר אישור הבקשה על-ידי הוועדה, העותק האלקטרוני, יועבר למשרד הבריאות בצורה מאובטחת, כמצוין לעיל בסעיף 5.2.2 - המלצה לסיווג הבקשה
בשלב הראשון בו מוגשים המסמכים ליו"ר ועדת הלסינקי לצורך סיווג הבקשה כניסוי מיוחד/לא מיוחד, היזם יוכל לצרף למסמכים את המלצתו/נימוקו הכתוב לסיווג הבקשה.
היזם יקבל הודעה על סיווג הבקשה ואופן המשך הטיפול בה באמצעות איש הקשר שפרטיו רשומים בטופס 1 - עדכון ועדות הלסינקי בניסוי רב-מרכזי
אם הבקשה סווגה כניסוי לא מיוחד במרכז הרפואי הראשון, באחריות היזם לעדכן את הוועדות (באמצעות החוקרים הראשיים) של כל שאר המרכזים הצפויים להשתתף בניסוי (בין אם כבר נקבע על ידם שמדובר בניסוי מיוחד ובין אם לא) כי הבקשה הועברה לטיפולו של משרד הבריאות ויש להמתין להחלטת המשרד - תיקונים למסמכי הבקשה בהליך מקביל
היזם יקבל הערות לתיקונים במסמכי הבקשה מוועדת הלסינקי ו/או ממשרד הבריאות ויבצע את התיקונים פעם אחת, תוך סימון בצבע/הדגשה שונה של השינויים שנדרשו מכל אחד מהגופים
- הגשת עותק אלקטרוני לחוקר
- הודעה על אישור משרד הבריאות בניסוי רב-מרכזי
לאחר שהבקשה אושרה על-ידי משרד הבריאות, נשלח האישור (טופס 8) ליו"ר ועדת הלסינקי של המרכז הרפואי הראשון וליזם. היזם יודיע לשאר המרכזים הרפואיים המתוכננים להשתתף בניסוי על אישור (לרבות תנאים והגבלות) של משרד הבריאות. אישור זה יצורף לבקשה שהוגשה/תוגש לוועדת הלסינקי המוסדית במרכזים הללו. קבלת טופס 8 תאפשר סיום הליך האישור במוסד הרפואי, לפי סעיפים 4.1.3 או 4.2.3.
הערה: היזם יקבל קוד ייחודי, שיאפשר לו לקבל מידע על סטאטוס הטיפול בבקשה - באמצעות המערכת הממוחשבת של משרד הבריאות - הטיפול בבקשות חדשות לניסויים רפואיים לא מיוחדים - במשרד הבריאות
- מסלולי הטיפול המפורטים מתייחסים לכל הבקשות הנדרשות לאישור משרד הבריאות
- מסלולי הטיפול
משרד הבריאות יבחן את הבקשה, ויחליט על מסלול הטיפול בה בהתאם לאחת מארבע האפשרויות הבאות:- הבקשה נדרשת לדיון בוועדה:
ההודעה תישלח לוועדת הלסינקי, לחוקר וליזם. בהודעה יפורטו המסמכים או הנתונים הנדרשים לצורך המשך הטיפול בבקשה.
הוועדות המרכזיות לניסויים רפואיים בתכשירים ובאמ"ר מתכנסות כל 6-4 שבועות; הוועדה המרכזית לניסויים רפואיים בתכשירים המכילים תאים ורקמות חיים ממקור הומני מתכנסת 4 פעמים בשנה;
הוועדה העליונה לניסויים גנטיים במשרד הבריאות מתכנסת כל 4 שבועות; הוועדה העליונה לטיפול גני מתכנסת 4 פעמים בשנה.
הוועדות דנות בבקשות שכל החומר הנדרש לגביהן התקבל במשרד הבריאות עד 2–3 שבועות (בהתאם לתדירות התכנסות הוועדה) לפני מועד הדיון.
באתר האינטרנט של המחלקה לניסויים קליניים מתפרסמת התוכנית השנתית של מועדי הישיבות.
לאחר הדיון בוועדה וקבלת המלצותיה והחלטותיה, משרד הבריאות ישלח את ההחלטה[2] ליו"ר ועדת הלסינקי (שיודיע לחוקר) וכן ליזם. החלטה תינתן תוך 60 ימים[3], מיום קבלת הבקשה - הבקשה נדרשת לדיון בוועדה ולחוות דעת מומחים:
קיימים מקרים בהם לאחר קבלת חוות דעת הבקשה מובאת לדיון בוועדה, או שלאחר דיון בוועדה נדרשת חוות דעת של מומחים נוספים עם/ללא דיון נוסף בוועדה.
לאחר הדיון בוועדה וקבלת המלצותיה והחלטותיה, משרד הבריאות ישלח את ההחלטה ליו"ר ועדת הלסינקי (שיודיע לחוקר) וכן ליזם. החלטה עשויה להתארך מעבר ל-60 ימים, מיום קבלת הבקשה - הבקשה נדרשת לחוות דעת מומחים בלבד:
ההודעה תישלח לוועדת הלסינקי, לחוקר וליזם. בהודעה יפורטו המסמכים או הנתונים הנדרשים לצורך המשך הטיפול בבקשה. המומחים מתבקשים להעביר את חוות הדעת בתוך 3–4 שבועות מיום קבלתם את הבקשה. ההחלטה תינתן תוך 45 ימים, מיום קבלת הבקשה - הבקשה אינה נדרשת לדיון בוועדה או לחוות דעת מומחים:
ההחלטה תישלח ליו"ר ועדת הלסינקי (שיודיע לחוקר) וכן ליזם. ההחלטה תינתן תוך 30 ימים, מיום קבלת הבקשה.
ניתן להגיש תיקונים והשלמות יותר מפעם אחת לצורך אישור הניסוי הרפואי.
לוח הזמנים להגשת תיקונים והשלמות הוא 6 חודשים מתאריך מכתב ההחלטה
- הבקשה נדרשת לדיון בוועדה:
- הנפקת אישור לניסוי שאינו מיוחד
בהתאם לתקנות בריאות העם, אישור משרד הבריאות (טופס 8) יינתן רק לאחר שהתקבל אישור ועדת הלסינקי (טופס 6) לבקשה.
בהגשה מקבילה:- אם ונדרשו השלמות/תיקונים לבקשה
- רק על-ידי ועדת הלסינקי:
היזם יעביר לוועדה (באמצעות החוקר) את המסמכים המתוקנים בהתאם לכל הדרישות. הוועדה תעביר למשרד הבריאות את המסמכים הללו יחד עם אישורה (טופס 6). אישור משרד הבריאות יינתן על גבי טופס 8 - רק על-ידי משרד הבריאות:
היזם יעביר במקביל את המסמכים המתוקנים לוועדת הלסינקי (באמצעות החוקר) ולמשרד הבריאות. אישור משרד הבריאות יינתן על גבי טופס 8 (טופס 6 נמצא כבר במשרד הבריאות) - הן על-ידי ועדת הלסינקי והן על-ידי משרד הבריאות:
היזם יעביר את המסמכים המתוקנים לוועדת הלסינקי (באמצעות החוקר). השינויים הנדרשים על-ידי ועדת הלסינקי יסומנו במסמכים באופן שונה מהשינויים הנדרשים על-ידי משרד הבריאות. ועדת הלסינקי תאשר את הניסוי ותעביר למשרד הבריאות את אישורה (טופס 6) יחד עם המסמכים המתוקנים, להשלמת הליך האישור במשרד הבריאות והוצאת טופס 8.
הערה: טופס 12 יישלח למשרד הבריאות יחד עם המסמכים המתוקנים רק במקרים בהם התיקונים נדרשו על ידי משרד הבריאות
- אם לא נדרשו השלמות/תיקונים לבקשה מוועדת הלסינקי וממשרד הבריאות, אישור משרד הבריאות (טופס 8) יינתן, כאמור, לאחר שיתקבל אישור ועדת הלסינקי (טופס 6).
האישור (טופס 8) יישלח ליו"ר ועדת הלסינקי, עם העתק למנהל המוסד הרפואי וליזם.
אישור של מנהל המוסד הרפואי (טופס 7) לניסוי לא מיוחד יונפק בהתאם להליך המפורט לעיל בסעיפים 5.1.2 ו- 5.1.3.
החוקר רשאי להתחיל בביצוע הניסוי הרפואי רק לאחר קבלת אישור המנהל.
לסיכום, הליך הטיפול בבקשות חדשות לניסויים רפואיים ”לא מיוחדים" בתהליך של הגשה מקבילה מתואר להלן באיור 3 - הטיפול בבקשות חדשות למחקרים שנערכים על-ידי משרד הבריאות:
חוקר שהוא עובד משרד הבריאות (למעט עובד בבית חולים ממשלתי), המתכנן לערוך מחקר יגיש את הבקשה בעותק אלקטרוני למזכירות הוועדה העליונה לניסויים רפואיים בבני-אדם, המשמשת כוועדת הלסינקי מוסדית עבור משרד הבריאות, לכל דבר ועניין, לרבות דיווחים והארכות תוקף אישור.
אישור ועדת הלסינקי העליונה (על גבי טופס 6) יועבר למנהל הכללי של משרד הבריאות או מי שהסמיכו לעניין זה. הלה ינפיק אישור למחקר ובו פירוט התנאים וההגבלות (על גבי טופס 7). העתק מאישור המנהל הכללי יועבר למחלקה לניסויים קליניים.
חוקר המבקש לבצע מחקר של משרד הבריאות באופן רב מרכזי במוסדות רפואיים נוספים, יציג למנהל המוסד הרפואי את אישור משרד הבריאות לביצוע המחקר (טופס 7), ויקבל את אישורו לביצוע המחקר במוסדו. מנהל המוסד הרפואי רשאי לקבוע הליך שונה לאישור המחקר במוסדו
- הטיפול בבקשות לניסויים רב-מרכזיים
- ניסוי רב-מרכזי נדון בוועדות הלסינקי במוסדות הרפואיים הצפויים להשתתף במחקר. סיווג הבקשה כניסוי מיוחד/לא מיוחד, נעשה בהתאם לקריטריונים המפורטים בפרק 4 ואינו קשור לכך שהניסוי רב-מרכזי
- המרכז הרפואי הראשון שסווג את הבקשה כניסוי שאינו מיוחד, יעביר למשרד הבריאות את הבקשה המלאה, בהתאם לסעיף 5.2 לעיל.
כל ועדה במרכז אחר שקבעה כי הבקשה נדרשת לאישור משרד הבריאות לא תשלח את הבקשה, אלא תדון בה כרגיל ותמתין להחלטת משרד הבריאות - אם ועדת הלסינקי בכל אחד מהמרכזים האחרים כבר דנה בבקשה והחליטה לאשרה כניסוי שאינו מיוחד, קבלת אישור משרד הבריאות מהיזם (כמצוין לעיל בסעיף 5.3.5) תאפשר את סיום הליך האישור במוסד הרפואי לפי סעיפים 4.1.3 או 4.2.3
- אם ועדה במרכז מסוים כבר אישרה את הבקשה כניסוי מיוחד וניתן אישור המנהל (טופס 7) לפני שניתן אישור משרד הבריאות, יש להשהות[4] את הליכי הניסוי עד לקבלת הודעה מהיזם על אישור משרד הבריאות
- טיפול בבקשות בהליך ייחודי
ניסויים בנושאים המפורט מטה, נדרשים לאישור משרד הבריאות בהליך ייחודי (בהתאם לחקיקה הקיימת ונוהלי משרד הבריאות):- ניסויים בהם נעשה שימוש בהיפנוזה נדרשים לאישור הוועדה המייעצת לפי חוק ההיפנוזה, תשמ״ד - 1984 וכן לאישור המנהל הכללי או לרופא שהסמיך לכך
- ניסויים בהם נעשה שימוש בקנביס נדרשים לאישור מקדים של היחידה לקנביס רפואי (יק"ר) להיתכנות הניסוי בטרם הגשת הבקשה. וכן לאישור המנהל הכללי או מי שהסמיכו ואישור היק"ר, לאחר שהבקשה אושרה בוועדת הלסינקי. זאת לפי נוהלים 105 ו-106 של אגף הרוקחות
- הליך האישור והנושאים המיוחדים שיכללו במסמכי הבקשה, מפורטים בנספח 9
הערות שוליים
- ↑ בפרק זה ובכל הנוהל, בכל מקום בו כתוב טופס 6 הכוונה גם לטופס 16 - במקרים הרלוונטיים. בכל מקום בו כתוב טופס 7 הכוונה גם לטופס 17 - במקרים הרלוונטיים
- ↑ החלטה היא אישור (approval) על גבי טופס 8, אישור בהתניה, או אי-אישור (reject) הבקשה.
- ↑ בכל מקרה שתדרשנה השלמות במהלך הטיפול בבקשה, זמן ההמתנה להשלמות אינו נכלל בחישוב זמן הטיפול.
- ↑ השהייה משמעותה הפסקת גיוס משתתפים חדשים, אולם משתתפים שהתחילו לקבל טיפול - הטיפול "משך בהתאם לפרוטוקול הניסוי.


 כניסה
כניסה  עקבו אחרינו בפייסבוק
עקבו אחרינו בפייסבוק