|
|
| (גרסת ביניים אחת של אותו משתמש אינה מוצגת) |
| שורה 85: |
שורה 85: |
| | ==תוצאות הבדיקה== | | ==תוצאות הבדיקה== |
| | בבלוטות לימפה, בשקדים ובטחול, צביעה ל-clusterin צובעת תאים דנדריטים פוליקולריים. תאי B, תאי T והיסטיוציטים אינם נצבעים. צביעה ל-clusterin מתקבלת לעיתים קרובות חיובית בתאים סרטניים של -large-cell lymphoma אנאפלסטית, אך הצביעה בדרך כלל שלילית בתאי Reed Sternberg בלימפומה קלאסית ע"ש Hodgkin (על פי Grogg וחב' ב-Am J Surg Pathol משנת 2004, Grogg וחב' ב-Modern Pathol משנת 2005, ו-Saffer וחב' ב-Modern Pathol משנת 2002). | | בבלוטות לימפה, בשקדים ובטחול, צביעה ל-clusterin צובעת תאים דנדריטים פוליקולריים. תאי B, תאי T והיסטיוציטים אינם נצבעים. צביעה ל-clusterin מתקבלת לעיתים קרובות חיובית בתאים סרטניים של -large-cell lymphoma אנאפלסטית, אך הצביעה בדרך כלל שלילית בתאי Reed Sternberg בלימפומה קלאסית ע"ש Hodgkin (על פי Grogg וחב' ב-Am J Surg Pathol משנת 2004, Grogg וחב' ב-Modern Pathol משנת 2005, ו-Saffer וחב' ב-Modern Pathol משנת 2002). |
| − |
| |
| − | {{בדיקת מעבדה
| |
| − | |שם עברי=קטכולאמינים
| |
| − | |שם לועזי=Catecholamines
| |
| − | |קיצור=
| |
| − | |תמונה=
| |
| − | |כיתוב תמונה=
| |
| − | |מעבדה=[[כימיה בדם]] ו[[כימיה בשתן]]
| |
| − | |תחום=
| |
| − | |יחידות מדידה=
| |
| − | |טווח ערכים תקין=
| |
| − | '''בדם''':{{ש}}אפינפרין בדם טבורי - 20-300 פיקוגרם למ"ל; ביילודים בשבוע החיים הראשון - 20-130 פיקוגרם למ"ל; בילדים בגיל 1-16 שנים - 20-115 פיקוגרם למ"ל. במבוגרים - אפינפרין (בשכיבה) - 20-110 פיקוגרם למ"ל, (בעמידה) - 20-140 פיקוגרם למ"ל.{{ש}}נוראפינפרין בדם טבורי - 700-1,600 פיקוגרם למ"ל; ביילודים בשבוע החיים הראשון - 200-420 פיקוגרם למ"ל; בילדים בגיל 1-16 שנים - 150-400 פיקוגרם למ"ל. במבוגרים - נוראפינפרין - (בשכיבה) - 70-750 פיקוגרם למ"ל, (בעמידה) - 200-1,700 פיקוגרם למ"ל.{{ש}}דופאמין בדם במבוגרים: (אין הבדל בין אם הדם נדגם בשכיבה או בעמידה) - פחות מ-30 פיקוגרם למ"ל; מטנפרין בדם (אין הבדל בין אם הדם נדגם בשכיבה או בעמידה) – פחות מ-100 פיקוגרם למ"ל. בדם,
| |
| − |
| |
| − | '''קטכולאמינים בשתן''' (מחושב בערכים של מיקרוגרם לאיסוף 24 שעות):{{ש}}אפינפרין - בתינוקות מתחת גיל שנה - 0-2.5; בגיל 1 שנה - 0.3.5; בגיל 2-3 שנה-0.6.0; מגיל 4-9 שנים - 0.2-10; בגיל 10-15 שנה - 0.2-20 במבוגרים מעל 15 שנה - פחות מ-20.{{ש}}נוראפינפרין - בתינוקות מתחת גיל שנה - 0-10; בגיל שנה - 1-17; בגיל 2-3 שנה - 4-29; בגיל 4-6 שנים - 8-45; בגיל 7-9 שנים - 13-65; מעל גיל 10 שנים - 15-80.{{ש}}דופאמין - בתינוקות מתחת גיל שנה - 0-85; בגיל שנה - 10-140; בגיל 2-3 שנים - 40-260 מעל גיל 4 שנים - 65-400.{{ש}}מטנפרין (במבוגרים) - 74-297; נור-מטנפרין (במבוגרים) - 105-354; (במבוגרים) VMA - פחות מ-9.
| |
| − |
| |
| − | '''קטכולאמינים בשתן''' (מחושב בערכים של מיקרוגרם לגרם קראטינין):{{ש}}אפינפרין - בתינוקות עד גיל שנה - 0-375; בגיל 1-4 שנים - 0-82; בגיל 4-10 שנה - 5-93; בגיל 10-18 שנה - 3-58; מעל גיל 18 שנה - 1-44.{{ש}}נוראפינפרין - בתינוקות עד גיל שנה - 25-310; בגיל 1-4 שנה - 25-290; בגיל 4-10 שנים - 27-108; בגיל 10-18 שנים - 4-105; מעל גיל 18 - 9-112.{{ש}}דופאמין - בתינוקות עד גיל שנה - 240-1,290; בגיל 1-4 שנה - 80-1,220; בגיל 4-10 שנים - 220-720; בגיל 10-18 שנים - 120-450; מעל גיל 18 שנה - 30-350.{{ש}}קטכולאמינים במי שפיר בעת הלידה (מחושב בערכים של מיקרוגרם למ"ל): אפינפרין - 0.34±1.11; נוראפינפרין - 2.84 ±0.81.{{ש}}סך רמת קטכולאמינים בשתן (מבוטאת בערכים של מיקרוגרם למטר בריבוע ל-24 שעות): בגיל 2-3 חודשים - 5-34; בגיל 4-11 חודשים - 8-51; בגיל 12-19 חודשים - 19-48; במבוגרים - מתחת ל-100.
| |
| − | |יוצר הערך=[[משתמש:בן עמי סלע|פרופ' בן-עמי סלע]]
| |
| − | |אחראי הערך=
| |
| − | }}
| |
| − | ==מטרת הבדיקה==
| |
| − |
| |
| − | איסוף שתן למדידת קטכולאמינים או מדידת רמתם בדם מתבצעת כדי לאבחן [[יתר לחץ-דם]] שמקורו בגידול של יותרת הכליה - [[פאוכרומוציטומה]] - המפריש קטכולאמינים או גידול כ[[נוירובלסטומה]]. כן נעשית בדיקה זו לניטור השפעת הטיפולים האלה במאובחנים עם גידולים אלה. בדיקה זו יכולה להידרש במקרה של מטופל עם לחץ-דם גבוה עם תסמינים של [[כאבי ראש]], הזעה מופרזת, סומק וקצב לב מוחש שאינו מגיב לטיפול הקונבנציונאלי. מקובל שאלה עם גידול כפאוכרומוציטומה עמידים לטיפולים התרופתיים המקובלים. בדיקת השתן מודדת את סך הקטכולאמינים שהופרשו משך 24 שעות, ובכך יתרונה על בדיקת הדם המשקפת את רמת הקטכולאמינים בנקודת זמן נתונה, ולדבר יש משמעות כיוון שרמת קטכואמינים מתנודדת באופן משמעותי במלך היממה, ולכן בדיקת השתן עשויה לגלות רמת יתר שתוחמץ במדידת קטכולאמינים בדם.
| |
| − |
| |
| − | ==בסיס פיזיולוגי==
| |
| − |
| |
| − | קטכולאמין- תרכובת המכילה קבוצת קטכול שהיא טבעת בנזן המכילה שני שיירי הידרוקסיל, שרשרת אתילית וכן מתמיר אמיני. הקטכולאמינים מתקבלים מחומצת האמינו טירוזין. חומרים אלו מסיסים במים ונקשרים לחלבונים שונים, ובאופן זה מועברים בזרם הדם בגוף. שלושת הקטכולאמינים העיקריים הם [[אפינפרין]], [[נוראפינפרין]] ו[[דופאמין]]. אפינפרין ונוראפינפרין משתחררים מליבת יותרת הכליה, והם בעלי תפקיד מכריע בוויסות תגובת "הילחם או ברח" (fight or flight) בגוף. המשקל המולקולארי של אפינפרין הוא 183.2, של נוראפינפרין – 169.2 ושל דופאמין – 153.2.
| |
| − |
| |
| − | ===יצירת קטכולאמינים===
| |
| − |
| |
| − | קטכולאמינים מיוצרים בעיקר בתאי הכרומפין של ליבת האדרנל (medulla) וכן בתאי כרומפין בבטן, בצוואר ובסיבים בתר-גנגליוניים של מערכת העצבים הסימפטתית. דופאמין, המשמש נוירוטרנסמיטור במערכת העצבים המרכזית, מיוצר בעיקר בתאי עצב בשני אזורים של גזע המוח: ב-Substania nigra, ובאזור הטגמנטלי הגחוני. גופי תאים באזור ה-Locus ceruleus מייצרים נוראפינפרין שהוא התוצר העיקרי המיוצר במערכת העצבים המרכזית, לעומת אפינפרין שהוא הקטכולאמין המרכזי המיוצר באדרנל.
| |
| − |
| |
| − | אפינפרין משתחרר מליבת האדרנל בשעת שפעול של עצבים סימפטתיים קדם-גנגליוניים המעצבבים את הרקמה הזו. שפעול זה מתרחש בעיתות עקה כמו פעילות גופנית מאומצת, כשל לב, עקה רגשית או התרגשות ו[[כאב]]. נוראפינפרין מהווה כ-20% מהקטכולאמינים המופרשים מליבת האדרנל. המקור העיקרי של נוראפינפרין בדם הוא זליגה מעצבים סימפטתיים המעצבבים כלי-דם. במצב תקין, רוב הנוראפינפרין המופרש בדרך זו , נקלט בחזרה על ידי העצבים שם הם עוברים מטבוליזם. יחד עם זאת, כמות קטנה של נוראפינפרין עוברת דיפוזיה לדם, ולעתים במצבים של שפעול מסיבי של עצבים סימפטתיים, כמות נוראפינפרין המגיעה לדם יכולה לעלות באופן דרמטי.
| |
| − |
| |
| − | אפינפרין בדם גורם להגברת קצב הלב (תוך התקשרות לקולטן האדרנרגי β1), לכיווץ רוב העורקים והוורידים (תוך התקשרות לקולטני α1 ו-α2), והרחבת כלי דם בשרירים ובכבד בריכוזי אפינפרין נמוכים (תוך התקשרות לקולטני β2), או הרחבת כלי הדם האחרונים בריכוזי אפינפרין גבוהים (תוך התקשרות לקולטני α1). סך התגובה הקרדיו-וסקולארית לריכוזים נמוכים עד בינוניים של אפינפרין, היא זו של הגברת תפוקת הלב והפניית תפוקה זו לצירקולציה של הדם ושל השרירים והכבד עם שינויים קלים בלבד של לחץ הדם העורקי הממוצע. למרות הגברת תפוקת הלב, אין שינוי משמעותי בלחץ הדם העורקי, שכן התנגודת הוסקולארית הסיסטמית פוחתת כתוצאה משפעול של קולטני β2 . בריכוזים גבוהים של אפינפרין בפלזמה, הוא מגביר את הלץ העורקי כתוצאה מהתקשרותו לקולטני α על פני דופן כלי הדם, המבטלת את ההשפעה מרחיבת כלי הדם של ההתקשרות של אפינפרין לקולטני β2.
| |
| − |
| |
| − | נוראפינפרין בדם גורם להגברת קצב הלב (אם כי באופן זמני) ולהגברת האינוטרופיה הקרדיאלית (בתיווך קולטני β1). ברוב העורקים והוורידים מתרחש תהליך כיווץ. סך התגובה הקרדיו-וסקולארית לנור-אפינפרין היא זו של הגברת תפוקת הלב, וכן הגברה של התנגודת הוסקולארית הסיסטמית, המביאה לעליה בלחץ הדם העורקי. למרות שקצב הלב נוטה בתחילה לעלות בהשפעת נור-אפינפרין, הוא יורד בהמשך על ידי שפעול של ברורצפטורים הממוקמים במקומות שונים בלב ובעורקים, וכן כתוצאה מתיווך וגאלי מואט קצב הלב.
| |
| − |
| |
| − | ===ביוסינתזה של קטכולאמינים===
| |
| − |
| |
| − | השלבים האנזימטיים לצירת קטכולאמינים נראים בתרשים.
| |
| − |
| |
| − |
| |
| − | [[קובץ:קטכולאמינים.jpg|מרכז]]
| |
| − |
| |
| − |
| |
| − | טירוזין מגיע הן מהמזון או על ידי הידרוקסילציה של פניל-אלנין על ידי האנזים פניל-אלנין הידרוקסילאזה. האנזים הראשון טירוזין הידרוקסילאזה (TH) קובע את קצב הביוסיתזה (rate-limiting enzyme), והוא באופיו oxidase המשתמש בחמצן מולקולארי ובטירוזין כסובטראטים וכן משתמש ב-Biopterin כקו-פקטור. אנזים זה מקטלז הוספה של שייר הידרוקסילי לעמדה meta בטבעת הבנזנית, ליצירת 3,4dihydroxyl-L-phenylalanine או L-DOPA. טירוזין הידרוקסילאזה יכול להוסיף שייר הידרוקסיל לפניל-אלנין, ההופך ל-L-DOPA, שזהו מסלול חלופי שעשוי להיות בעל משמעות בסובלים מ[[phenylketonuria|פניל-קטונוריה]], מפגע בו ירודה פעילות האנזים פניל-אלנין הידרוקסילאזה. TH הוא אנזים מסיס במים אלא שתגובה שלו עם מרכיבי ממברנת תאים כגון פוספאטידיל-סרין, או עם פוליאניונים דוגמה הפארין סולפאט, משנה את תכונותיו הקינטיות. אנלוגים של טירוזין דוגמת alpha-methyl-p-tyrosine {{כ}}{AMPT), מהווים מעכבים תחרותיים של האנזים TH.
| |
| − |
| |
| − | האנזים DOPA decarboxylase מקטלז הרחקת שייר הידרוקסיל מ-DOPA ליצירת דופאמין שהוא תוצר קצה עיקרי ב-CNS, בו הוא משמש כנוירוטרנסמיטור: אנזים זה זקוק ל[[ויטמין B6]] ([[פירידוקסין]]) כקו-פקטור, והוא יכול גם לעשות דקרבוקסילציה של חומצות אמינו ארומטיות כמו גם של 5-הידרוקסי-טריפטופן, הקודמן של [[סרוטונין]]. אנזים זה שכיח בנוירונים המכילים קטכולאמינים או כאלה המכילים סרוטונין, וכן ברקמות לא עצביות כמו כליות וכלי דם. בנוירונים מכילי-דופאמין אנזים זה היא האנזים הסופי במסלול זה, כאשר בנוירונים המסנתזים אפינפרין או נוראפינפרין, השלב האנזימטי הבא הוא זה של Dopamine β-hydroxylase. בדומה ל-TH מדובר באוקסידאזה המייצרת שייר הידרוקסילי על פני פחמן β בשרשרת הצדדית של דופאמין. במהלך ריאקציה זו, חומצה אסקורבית מחוזרת ל-Dihydroascorbate, באופן שמשמש מקור אלקטרונים. האנזים DBH מכיל נחושת דו-ערכית, המעורבת במעבר אלקטרונים במהלך הריאקציה, ובהתאם תכשירים הקושרים נחושת כגון Diethyldithiocarbamate, הם מעכבים יעילים של האנזים.
| |
| − |
| |
| − | בתאים המסנתזים אפינפרין השלב האחרון במסלול הקטכולאמינים מקוטלז על ידי האנזים phenylethanolamine N-methyltransferase{{כ}} (PNMT), אנזים הנמצא בקבוצה קטנה של נוירונים בגזע המוח, נוירונים המשתמשים באפינפרין כנוירוטרנסמיטור, אך בעיקר הוא פועל בתאי הליבה של האדרנל, בהם אפינפרין הוא ההורמון העיקרי. PNMT מעביר שייר מתיל מ- S-adenosylmethionine לחנקן של נוראפינפרין, תוך יצירת אמין שניוני. פעילות PNMT מווסתת על ידי [[קורטיקוסטרואידים]]. כדי שהאנזים PNMT יוכל לפעול על נוראפינפרין בציטוזול של התאים, הוא חייב לצאת מהגרגירים (granules) של תאי כרומפין. פעולה זו מתבצעת על ידי חלבון הטרנספורט VMAT 1 {{כ}}(Vesicular monoamine transporter 1), שתפקידו גם להחדיר אפינפרין שזה עתה סונתז מהציטוזול אל תוך גרגירי הכרומפין כהכנה לקראת שחרורם לדם.
| |
| − |
| |
| − | יצירת האנזים PNMT מושרה על ידי [[קורטיזול]], שריכוז גבוה שלו בתוך האדרנל נדרש ליצירת PNMT בליבת (medulla) האדרנל. מתן חיצוני של סטרואידים מדכא יצירת קורטיזול אנדוגני, ובכך פוחתת רמת הקורטיזול סביב ליבת האדרנל, ופוחתת יצירת אפינפרין. ההורמונים של הליבה באדרנל נאגרים תוך יצירת קומפלקס עם חלבונים כגון Chromogranin A , Dopamine-β-hydroxylase וכן עם ATP בתוך גרגירי תאי כרומפין. שחרור של קטכולאמינים מליבת האדרנל נעשה בתגובה למצב של תת לחץ-דם, [[היפוקסיה]], חשיפה לקור, מאמץ שרירים מוגבר וכן במצבי סערה רגשית. כל זמן שקטכולאמינים אגורים בגרגירי הכרומפין הם שומרים על יציבות, אך מרגע שהם משתחררים לדם יש להם זמן מחצית חיים קצר של מספר דקות, כיוון שהם עוברים פירוק מהיר על ידי שני אנזימים: א. Catechol-O-methyltransferase{{כ}} (COMT), שגורם מתילציה של קטכולאמינים; ב. Monoamine oxidase {{כ}}(MAO), הגורם לדה-אמינציה שלהם.
| |
| − |
| |
| − | רק מקטע קטן של קטכולאמינים (כ-2%) אינו עובר מטבוליזם ומופרש בשתן כקטכולאמינים חופשיים. האנזים COMT נמצא ברקמות רבות, בעיקר בכבד, כליות וכדוריות דם אדומות. אנזים זה עושה מתילציה של השייר ההידרוקסילי על C-3 של נוראפינפרין ואפינפרין, ליצירת Normethanephrin ו-Methanephrin, בהתאמה. בערך 20% מהקטכולאמינים מופרשים לשתן כמטנפרינים, ורוב הקטכולאמינים עוברים הסבה לחומצה וניליל-מנדלית (VMA) על ידי הפעולה המשותפת של COMT ו-MAO, כאשר האחרון הוא אנזים מאוד נפוץ ברקמות שונות. דופאמין הופך לחומצה הומו-ונילית (Homovanillic acid {{כ}}(HVA)); נוראפינפרין הופך ל-Normetanephrin ול-VMA, ואילו אפינפרין הופך ל-Metanephrin ול-VMA.
| |
| − |
| |
| − | כאמור, MAO הוא האנזים העיקרי האחראי לקטבוליזם של קטכולאמינים. מעכבי אנזים זה או תכשיר כ-Methaamphetamine נקשרים לאנזים ומונעים את פרוק הקטכולאמינים. זו גם הסיבה העיקרית מדוע השפעת אמפטמינים נמשכת זמן ממושך יותר מאשר זו של [[קוקאין]], או של סמים אחרים. [[אמפטמינים]] לא רק גורמים לשחרור דופאמין, אפינפרין ונור-אפינפרין לדם, אלא גם מדכאים את ספיגתם מחדש.
| |
| − |
| |
| − | ===תפקידי קטכולאמינים===
| |
| − |
| |
| − | שני הקטכולאמינים, נוראפינפרין ודופאמין, פועלים כנוירוטרנסמיטורים במערכת העצבים המרכזית, אך גם כהורמונים בדם. נוראפינפרין הוא גם נוירוטרנסמיטור של מערכת העצבים הסימפטתית, ולעומתו אפינפרין הוא הורמון המופרש בעיקר כתגובה למצבי עקה פיזית או נפשית. ההורמונים, נוראפינפרין ואפינפרין, מכינים את הגוף לתגובת "הילחם או ברח" כאשר גורמי דחק סביבתיים כמו גלי קול צורמים, הבהקי אור חזקים, או רמת לחץ דם נמוכה מגרים לתגובה זו. מספר פעולות הורמונאליות אופייניות של קטכולאמינים אלה כוללים קצב לב ולחץ דם מוגברים, כמו גם הגברת שחרור [[t:גלוקוז - Glucose|גלוקוז]] ממאגרי אנרגיה, והגדלת המוכנות של שרירי שלד, בין שאר הפעילויות של מערכת העצבים הסימפטתית.
| |
| − |
| |
| − | שני הקטכולאמינים, נוראפינפרין ואפינפרין, משפיעים על המערכת הוסקולארית , בעוד אפינפרין משפיע על תהליכים מטבוליים כמו זה של פחמימות. הפעילויות הביולוגיות של קטכולאמינים מתחילות על ידי האינטראקציה שלהם עם הקולטנים α ו-β אדרנרגיים. קולטנים אלה הם בעלי זיקות שונות לשני קטכולאמינים אלה, ולעתים בעלי פעילות פיזיולוגית הפוכה. נוראפינפרין מגיב בעיקר עם קוטלטנים α-אדרנרגיים, ואילו אפינפרין מגיב עם שני סוגי הקולטנים, α ו-β. גירוי הקולטנים מסוג α מביא לכיווץ כלי-דם, לירידה בהפרשת אינסולין, ל[[הזעת יתר]], לסמירת שיער, לעידוד גליקוגנוליזה בכבד ובתאי שריר השלד, מה שמביא להגדלת ריכוז [[t:גלוקוז - Glucose|גלוקוז]] בדם. גירוי הקולטנים מסוג β, לעומת זאת, מרחיב כלי דם, מגביר הפרשת [[אינסולין]], מקטין קצב פעימות הלב, מרפה שרירים חלקים במערכת העיכול, מרחיב דרכי ריאות על ידי הרפיית שרירים חלקים בסמפונות הריאה , מעודד שחרור ההורמון [[רנין]] המגביר ספיגה מחדש של נתרן מהכליות ומגביר ליפוליזה.
| |
| − |
| |
| − | ===מערכת הקולטנים לקטכולאמינים===
| |
| − |
| |
| − | הקולטנים האדרנרגיים מצומדים לחלבון G, משמשים להתקשרות של נוראפינפרין ואפינפרין , בעוד שדופאמין נקשר לקולטנים דופאמינרגיים. תאים רבים מבטאים את הקולטנים הללו, והקישור של אגוניסט לקולטנים אלו יביא לתגובה סימפתטית של מערכת העצבים , כמו לדוגמה התגברות קצב הלב, הרחבת אישונים. ישנן שתי קבוצות עיקריות של קולטנים אדרנרגיים: אלפא (α) ובתא (β). אפינפרין (אדרנלין) פועל הן על קולטנים מסוג אלפא (α) והן מסוג בתא (β), ובכך הוא מביא הן להתכווצות של כלי הדם והן להרחבתם, לאור פעולתם ההפוכה של שני תת-סוגי הקולטנים הללו. כאשר קיימות רמות גבוהות של אפינפרין בפלזמה, רבה יותר השפעתם של קולטנים מקבוצה α, ועל כן תתרחש התכווצות של כלי הדם. רמות נמוכות יותר בדם של אפינפרין, יביאו להשפעה גבוהה יותר של קולטנים מקבוצה β, ולהתרחבות של כלי דם.
| |
| − |
| |
| − | קולטנים אדרנרגיים אלפא כוללים קולטנים מסוג α1 ומסוג α2. הקולטן α1 פועל בהשפעת מתווכים שניוניים בתא, אינוזיטול טריפוספט (IP3) ודיאציל גליצרול (DAG), באופן בו חלה עלייה ברמות הסידן התוך-תאי החיוני לכיווץ של תאי שריר חלק, ועקב כך להתכווצות של כלי הדם, שכן כלי הדם עטופים בשכבת תאי שריר חלק. פעילות הקולטן α2 קשורה בהפחתת פעילות cAMP בתא, שתוצאתו אף היא התכווצות תאי שריר חלק. קולטני α1 כרוכים בכיווץ של כלי דם שונים בעור, במערכת העיכול, בכליה ובמוח, ברחם, בצינור הזרע, בשיער, בסוגר שלפוחית השתן, בסמפונוני הריאות ובגוף הריסני בעין. פעולות נוספות של קולטנים אלו כוללות גליקוגנוליזה, גלוקונאוגנזה, הפרשת זיעה וספיגה מחדש של נתרן באבובית הכליה. נוראפינפרין ואפינפרין מהווים אגוניסטים לקולטנים מקבוצה זו.
| |
| − |
| |
| − | קולטנים מסוג α2 פועלים באופן כללי על ידי הרפיית שריר הלב, פעולה מעורבת על כלי דם ושריר חלק ועיכוב הפרשת טרנסמיטורים עצביים במשוב שלילי. כך פוחת שחרור אינסולין לעומת הגברה של הפרשת גלוקגון מהלבלב; חל כיווץ סוגרים של מערכת העיכול; וכתוצאה ממשוב שלילי בסינפסות עצביות, פוחת שחרור נוראפנפרין במערכת העצבים המרכזית; יש עליה בצימות של טסיות. אפינפרין ונוראפינפרין מהווים אגוניסטים לקולטנים מקבוצה זו.
| |
| − |
| |
| − | קולטנים אדרנרגיים בתא כוללים את תת-הסוגים β1, β2 ו-β3, ושלושת תת-סוגים אלה פועלים במסלול של אדניליל ציקלאז, אגוניסט הנקשר לקולטנים אלו ומביא לעלייה בריכוז התוך-תאי של המתווך התאי שניוני cAMP. כך אחראים קולטנים אלו להתכווצות שריר הלב, הרפיה של שריר חלק, וגליקוגנוליזה. התרופה איזופרנלין היא אגוניסט סלקטיבי של קולטנים מקבוצה זו.
| |
| − |
| |
| − | קולטני β1 אחראים בעיקר על הגברת כיווץ שריר הלב ועלייה בתפוקת הלב, על ידי העלאת קצב הלב (אפקט כרונוטרופי חיובי), הגברת קצב ההולכה החשמלי, ועלייה בכיווץ. העלאת הפרשת רנין מתאים שליד הפקעיות (juxtaglomerular) בכליה. העלאת הפרשת ההורמון ghrelin בקיבה. אגוניסטים לקבוצה זו כוללים איזופרנלין, [[t:אדרנלין - Adrenaline|אדרנלין]] ונוראדרנלין והתרופה [[דובוטמין]]. אנטגוניסטים לקבוצה זו כוללים חוסמי בטא מסוג [[מטופרולול]] ו[[אטנולול]].
| |
| − |
| |
| − | קולטני β2 אחראים בעיקר להרפיה של שריר חלק שריר חלק בסימפונות הריאות ובמערכת העיכול; ליפוליזה בתאי שומן; פעולות אנאבוליות בתאי השריר; הרפיית שריר הרחם; הרפיה של שריר השלפוחית; הרחבת עורקים המזינים את שרירי השלד; גליקוגנוליזה וגלוקונאוגנזה; גירוי להפרשת אינסולין; עיבוי הפרשות של בלוטות רוק; מניעת שחרור [[היסטמין]] מתאי פיטום; עלייה בהפרשת רנין מהכליות. איזופרנלין, אפינפרין ונוראפינפרין, הם אגוניסטים של קבוצת קולטנים זו.
| |
| − |
| |
| − | כיוון שקטכולאמינים פועלים על הלב ועל כלי הדם על ידי פעולתם על קולטנים אדרנרגיים מסוג אלפא ובתא, ניתן לחסום את הפעילות הקרדיו-וסקולארית של קטכולאמינים על ידי תכשירים חוסמי α או β. חסימה של קולטני אלפא או של קולטני בתא בנפרד, תאפשר לקטכולאמינים להיקשר לסוג הקולטנים שלא נחסם, ולדוגמה כאשר נחסום רק את קולטני α, הפעלה של קולטני β2 תגרום לתגובה משמעותית של הפחתת לחץ-דם, כתוצאה מהרחבה סיסטמית של כלי-דם, זאת למרות עידוד פעולת הלב הנגרמת משפעולם של הקולטנים האדרנרגיים מסוג β1.
| |
| − |
| |
| − | לדופאמין חמישה קולטנים מטבוטרופיים והוא מעורב בתפקודי תנועה, קשב ולמידה. שלושת המערכות הדופמינרגיות החשובות במח הן: א. המערכת הניגרוסטריאטלית- מצויה בחומר השחור ושולחת אקסונים לנאוסטריאטום שבגנגליונים הבסיסיים - לגרעין הזנב ול-Putamen שחשיבותו בבקרת התנועה; ב. המערכת המזולימבית - מצויה בטגמנטום הגחוני ושולחת אקסונים שלהם לכמה חלקים במערכת הלימבית, - לגרעין האקומבנס, לאמגידלה ולהיפוקמפוס. גרעין האקומבנס ממלא תפקיד חשוב בהשפעות על כמה סוגי גירויים, כגון אלה של סמים אסורים; ג. המערכת המזו-קורטיקלית - מצויה בטגמנטום הגחוני ושולחת אקסונים לקורטקס הקדם-מצחי. למערכת זו השפעה מעוררת על הקורטקס והשפעתה על תפקודים כגון יצירת זיכרונות קצרי-טווח, ותכנון פיתרון בעיות.
| |
| − |
| |
| − | ===השפעת תרופות על סינפסות דופמינרגיות===
| |
| − |
| |
| − | # '''השפעה על ייצור דופאמין''': ל-L-Dopa השפעה אגוניסטית המגבירה ייצורו, ולעומתה האנטגוניסט AMPT משבש את פעילות האנזים טירוזין הדירוקסילז, שהופך את הטירוזין ל-L DOPA.
| |
| − | # '''השפעה על הקולטנים''': אפומורפין- בכמות קטנה בעל פעילות אנטגוניסטית בהיותו מגרה את אחד הקולטנים (D2) הקדם סינפטיים - אנטגוניסט. לעומת זאת בכמויות גדולות משמש תכשיר זה אגוניסט בגרותו את אחד הקולטנים (גם כן D2) הבתר סינפטיים. קוקאין אף הוא אגוניסט בהיותו מגרה קולטונים דופאמינרגיים בתר סינפטיים.
| |
| − | האנטגוניסטים לשימוש בחולי סכיזופרניה כלורופרומאזין - חוסם קולטנים D2, וקלוזאפין - חוסם קולטני D4.
| |
| − | # '''השפעה על השפעול מחדש והספיגה החוזרת''': האגוניסטים וריטלין אמפטאמין - מעכבים ספיגה חוזרת של הדופאמין. האגוניסט דפרניל - הורס את הפעילות של האנזים MAO B.
| |
| − |
| |
| − | תרופות, תכשירים ומצבים המעלים רמת קטכולאמינים בפלזמה באופן פיזיולוגי: [[t:Aminophylline|Aminophylline]] ,Ajmaline diazoxide, Ethanol, Caffeine, Ether, שאיפת Isoproterenol, מעכבי MAO, אמפטמינים, נוגדי דיכאון טריציקליים, תרופות להפחתת גודש באף כמו [[Phenylephrine]] או [[Pseudoephedrine]], [[ליתיום]], קוקאין, ניטרוגליצרין, [[פרופרנולול]], תאופילין, Phentolamine ,Tolcapone, תנוחה אנכית, [[פעילות גופנית]] מאומצת, עקה נפשית (stress).
| |
| − |
| |
| − | תרופות ותכשירים המעלים רמת קטכולאמינים בפלזמה בשל התערבות או הפרעה (interference) לעצם המדידה האנליטית: Phenothiazines, [[Levodopa|L-dopa]], Methyldopa.
| |
| − |
| |
| − | [[Clonidine] מפחית באופן פיזיולוגי את רמת קטכולאמינים בפלזמה.
| |
| − |
| |
| − | תרופות ותכשירים המעלים רמת קטכולאמינים בשתן באופן פיזיולוגי: קפאין, אפינפרין, אתנול, Isoproterenol ,{{כ}}[[Levodopa]], [[ניקוטין]], ניטרוגליצרין, Reserpine{{כ}} ,[[Theophylline]] {{כ}},[[Imipramine]].
| |
| − |
| |
| − | תכשירים המפריעים באופן אנליטי לבדיקת קטכולאמינים בשתן בבדיקה הפלואורסצנטית: [[אספירין]], כלורל הידראט, [[אריתרומיצין]], פורמאלדהיד שעלול להגיע מתרכובות של Methenamine, {{כ}}Isoproterenol{{כ}}, Labetanol, מתילדופה, [[ויטמין B3|ניאצין]] (במינונים גבוהים), [[Quinidine]]{{כ}}, [[Quinine]], [[ויטמין B2|ריבופלבין]], תה, טטרציקלינים, ויטמינים מקבוצת B, דופאמין ו-Deyydroxyphenylacetic acid. הפרעה אנליטית לשיטות מדידה כרומטוגרפיות או ספקטרופוטומטריות נגרמת על ידי Phenothiazines.
| |
| − |
| |
| − | תרופות המפחיתות באופן פיזיולוגי רמת קטכולאמינים בשתן: [[קלונידין]], Guanethidine{{כ}} ,ouabain ,{{כ}}Prozosin , {{כ}}Reserpine {{כ}},Bretylium, תכשירים רדיוגרפיים.
| |
| − |
| |
| − | ==פענוח תוצאות המעבדה==
| |
| − |
| |
| − | רמות גבוהות מהמקובל של קטכולאמינים ומטנפרינים בדם או בשתן וכן קטכולאמינים ו-VMA בשתן, יכולות להופיע במקרים של דאגנות חריפה או [[דיכאון]] ולחץ נפשי, פעילות גופנית מאומצת באופן חריג, מצבי עקה כ[[כוויות]], [[ספסיס]], ניתוח או פציעה טראומטית. גם עקה הנגרמת מחשיפה לצלילים בדציבלים גבוהים או צורמנים, חשיפה להבהקי אור חזקים או בירידה ניכרת ברמת סוכר בדם תביא לרמה מוגברת של קטכולאמינים. כן נמצא רמות מוגברות בפאוכרומוציטומה משפחתית (הכוללת [[von Hippel-Lindau syndrome|תסמונת von Hippel-Lindau]]{{כ}}, [[Paraganglioma]], ו-[[MEN 2|Multiple endocrine neoplasia II]]), [[נוירובלסטומה]] (אך ללא עליה באפינפרין), [[גנגליובלסטומה]], [[גנגליונוירומה]] (רמות גבוהות של דופאמין, נוראפינפרין והמטבוליטים שלהם), [[Shy-Drager syndrome|תסמונת Shy-Drager]]. רמת קטכולאמינים תתקבל גם בחסר האנזים MAO-A. בפאוכרומוציטומה רמת נוראפינפרין גבוהה מזו של אפינפרין בפלזמה.
| |
| − |
| |
| − | רמת קטכולאמינים תימצא מוגברת לאחר אוטם שריר לב, במצבי עקה, ב[[היפותירואידיזם]], ב[[DKA|חמצת סוכרתית]], במצבי דיכאון. רמות אפינפרין ונוראפינפרין מוגברות בפאזה הלוטאלית של המחזור, ופוחתות לרמה מינימאלית בפאזת הביוץ, כאשר שינויים דומים נרשמים ברמת VMA. מדידת קטכולאמינים חופשיים, מטנפרינים ו-VMA בשתן יכולה להיות שימושית באבחון של מחלת הליבה של האדרנל. אחוז ניכר של מטבוליטים של קטכולאמינים מופיע בשתן כנגזרות של סולפאט.
| |
| − |
| |
| − | רמות נמוכות מהמקובל של קטכולאמינים ניתן למצוא ב[[סוכרת]], ב[[מחלת פרקינסון]], ו[[Orthostatic hypotension|בתת-לחץ דם אורתוסטטי]].
| |
| − |
| |
| − | פענוח תוצאת בדיקת קטכולאמינים בשתן: בפאוכרומוציטומה ניתן למצוא בשתן רמת נוראפינפרין של 10,000 מיליגרם ליום, ורמת אפינפרין של 750 מיליגרם ליום. אם רמת האפינפרין גבוהה יותר מזו נוראפינפרין, ניתן להניח שמקור הגידול בליבת האדרנל או שמקורו ב-Organ of Zuckerkandl, שהוא גופיף כרומפין הנובע מהרכס העצבי הממוקם בהתפצלות של אבי העורקים במקור העורק המזנטרי התחתון. רמת קטכולאמינים בשתן בלילה נמוכה בהרבה מרמתם בשתן במשך שעות היום.
| |
| − |
| |
| − | כיוון שמבחן לרמת קטכולאמינים רגיש להשפעות "חיצוניות" רבות, עלולות להגביר את רמתם בעוד שמקרי פאוכרומוציטומה נדירים יחסית (בממוצע מקרה אחד לכל 200 מקרים של יתר לחץ-דם), יהיו מטבע הדברים יותר מקרים של תוצאות false positive מאשר מקרים אמיתיים של הגידול האמור. אם בנבדק סימפטומתי מוצאים רמה גבוהה של קטכולאמינים בדם או בשתן, יש צורך בברור מתקדם נוסף, שכן מחלה קשה ועקה נפשית יביאו לעליה זמנית משמעותית ברמות קטכולאמינים.
| |
| − |
| |
| − | מדידה בעת ובעונה אחת של HVA ו-VMA בשתן, יכולה לסייע לאבחון של גידולי הרכס העצבי (neural crest). מדידת מטנפרינים בשתן מומלצת לעתים קרובות כשיטת בדיקה מקדימה לפאוכרומוציטןמה עם דרגת רגישות אבחונית של 100%. מדידה של VMA ושל קטכולאמינים בשתן, יותר ספציפית אך פחות רגישה מאשר מדידת מטנפרינים לאבחון פאוכרומוציטומה. רמות מוגברות של דופאמין בשתן מאפיינות תרחיש של נוירובלסטומה. מדידה של מטנפרינים חופשיים בפלזמה, מומלצת כבדיקה מקדימה לפאוכרומוציטומה, שכן יש לה דרגות רגישות וספציפיות גבוהות. רוב המדידות המעבדתיות עוסקות רק בקטכולאמינים חופשיים, ומיעוטן מודדות לצד הקטכולאמינים החופשיים גם את אלה המצומדים. קטכולאמינים חופשיים משקפים טוב יותר את מסת הגידול הסרטני, מאשר הקטכולאמינים המצומדים.
| |
| − |
| |
| − | פאוכרומוציטומה אינה מייצרת בהכרח קטכואמינים בקצב קבוע. יחד עם זאת, אם לנבדק הייתה לאחרונה אפיזודה של [[יתר לחץ-דם]], רמת קטכולאמינים בדם ובשתן שלו יכולה להיות תקינה או קרוב לתקינה, גם אם אין ספק שהגידול אמנם קיים בו. כמות הקטכולאמינים המופרשים מהגידול, אינו בהכרח מתאים למסת הגידול. לסך רמת הקטכולאמינים המיוצרים יש נטייה לעלות, במקביל לעלייה בממדי הגידול.
| |
| − |
| |
| − | מבחן דיכוי על ידי קלונידין: מבדק זה יכול להתבצע כדי לברר האם לחץ דם מוגבר נובע מגידול באדרנל. במבחן זה נמדדת רמת קטכולאמינים בדם לפני ואחרי נטילת כמות קטנה של התכשיר קלונידין המשמש לטיפול בלחץ דם גבוה. אם אמנם קיים גידול, נטילת קלונידין לא תגרום לשינוי ברמת הקטכולאמינים הנמדדים. אם לעומת זאת לחץ הדם הגבוה נגרם כתוצאה מגורמים אחרים, קלונידין יגרום לרמת קטכולאמינים לרדת.
| |
| − |
| |
| − | ===מפגעים===
| |
| − |
| |
| − | רמות גבוהות במיוחד של קטכולאמינים יכולות להופיע במקרה של טראומה במערכת העצבים המרכזית כתוצאה מגירוי או נזק לגרעינים בגזע המוח, בעיקר אלה המשפיעים על מערכת העצבים הסימפטתית. ברפואת חירום התרחשות כזו מוכרת כ-catecholamine dump. מפגעים ספציפיים כקשורים לקטכולאמינים כוללים נוירובלסטומה, פאוכרומוציטומה, כמודקטומה, תסמונת פאראגנגליומה משפחתית, חסר האנזים Dopamine-β-hydroxylase וחסר של Tetrahydrobiopterin{{כ}} (THB). בנוירובלסטומה שמקורה מהרכס העצבי של מערכת העצבים הסימפטתית יש ייצור מוגבר של קטכולאמינים.
| |
| − |
| |
| − | בפאוכרומוציטומה יש הפרשה מסיבית של קטכולאמינים, אך כאן יש רמה מוגברת של נוארפינפרין בהשוואה לאפינפרין. ב-Chemodectoma, הידוע גם כ-Nonchromaffin paraganglioma, שהוא בדרך כלל גידול שפיר (ולעתים ממאיר) נדיר של מערכת הכמו-רצפטורים, שיכול להופיע בבטן, בקנה הנשימה או באזור הראש והצוואר, יש רמה מוגברת של קטכולאמינים. גידול שצמיחתו איטית באזור הראש והצוואר ידוע כ-Familial paraganglioma syndrome מפריש אף הוא קטכולאמינים לדם.
| |
| − |
| |
| − | מחלת פרקינסון נוצרת כתוצאה מהתנוונות הנוירונים הדופאמינרגיים המצויים בחומר השחור, שבמע` הניגרו-סטריאטלית. חולי פרקינסון מקבלים את התרופה L-Dopa, הקודמן של דופאמין, שאיננו יכול לעבור את מחסום הדם-מח. תרופה זו עוברת מחסום זה, מוכנסת לנוירונים הדופאמינרגיים בתהליך של קליטה חוזרת והופכת לדופאמין. וכך חולי פרקינסון מוגברת הפרשתו של הדופמין מהנוירונים הדופמינרגיים שעדיין נותרו.
| |
| − |
| |
| − | ==הוראות לביצוע הבדיקה==
| |
| − | הנבדק צריך להיות במצב שכיבה ורגיעה למשך 30 דקות. יש להימנע מנטילת הדגימות כאשר טמפרטורת הגוף נמוכה במיוחד (כגון לאחר שהייה בחוץ ביום חורפי מה שעלול להעלות רמת קטכולאמינים בשתן. יש לשתות באופן סדיר נוזלים 24 שעות לפני הבדיקה למנוע דהידרציה. יש להימנע מנטילת תרופות ללחץ-דם 48 שעות לפני הבדיקה, כמו גם תרופות לאלרגיה, או תכשירים להרזיה או להצטננות. כן יש להימנע מנטילת אספירין, ניטרוגליצרין, תאופילין, טטרציקלין, הדם צריך להילקח במבחנת הפארין (פקק ירוק) או במבחנת ספירת דם (EDTA, פקק סגלגל), ולהיות מקורר מייד לאחר נטילתו. לאחר סרכוז הדגימה בצנטריפוגה מקוררת ויש להקפיא את הפלזמה מייד (רצוי בטמפ. של מינוס 70 מעלות), אם המדידה לא מתבצעת מייד. יש הממליצים להוסיף Metabisulfite או גלותתיון לגדימת הפלזמה כדי למנוע את חמצון הקטכולאמינים. הדגימה יציבה למשך 8 חודשים בהקפאה עמוקה.
| |
| − |
| |
| − | לגבי מדידת קטכולאמינים בשתן, יש לעשות איסוף שתן של 24 שעות בכלי פלסטיק המכיל 20 מיליליטר של תמיסת 6M של חומצת מלח (HCl), כאשר המיכל נשמר בקירור במשך 24 שעות האיסוף. באיסוף שתן של ילדים בהם נפח השתן אינו עולה על 400 מיליליטר ב-24 שעות, מומלץ להוסיף מראש למיכל האיסוף 4 מ"ל של חומצה גפריתית בריכוז 5M. אין להשתמש להחמצה בחומצה בורית. בסוף האיסוף ה-pH של השתן אמור להיות נמוך מ-3.0.
| |
| − |
| |
| − | כיוון שתוצאות מדידת קטכולאמינים יכולות להיות מושפעות ממספר תרופות או פריטי מזון נצרך, כמו גם מדרגת הפעילות הגופנית או מעקה נפשית, יש להתחשב בכל אלה לפני מתן דגימת דם או שתן. יש על כן להימנע ב-24 עד 48 שעות לפני מתן הדגימה מצריכת משקאות המכילים קפאין כמו תה, קקאו וקפה, או מאכלים עשירים באמינים כמו בננות, אגוזי מלך, אבוקדו, פול, וכן גבינה, בירה ויין אדום. יש להימנע כמו כן מאכילת שוקולד, לימון, וכן וניל או Licorice. יש להימנע כמו כן מפעילות גופנית בעצימות גבוהה, ועד כמה שאפשר להיות רגועים ולהימנע מעקה נפשית ומ[[עישון]]. יש להימנע מהפשרה והקפאה נוספת של הפלזמה.
| |
| | | | |
| | ==ראו גם== | | ==ראו גם== |
| | *[[מדריך בדיקות מעבדה|חזרה לדף מדריך בדיקות מעבדה]] | | *[[מדריך בדיקות מעבדה|חזרה לדף מדריך בדיקות מעבדה]] |
| | * [[סמנים סרטניים|בדיקות מעבדה - סמנים סרטניים]] | | * [[סמנים סרטניים|בדיקות מעבדה - סמנים סרטניים]] |
| | + | |
| | | | |
| | {{ייחוס בן עמי}} | | {{ייחוס בן עמי}} |
| | | | |
| − | [[קטגוריה:בדיקות מעבדה: כימיה בשתן]]
| |
| | [[קטגוריה:בדיקות מעבדה - סמנים סרטניים]] | | [[קטגוריה:בדיקות מעבדה - סמנים סרטניים]] |
| מדריך בדיקות מעבדה
|
| קלאסטרין
|
| Clusterin
|
| שמות אחרים
|
CLU, ApoJ או apolipoprotein J; testosterone-repressed prostate message 2 (או TRPM-2); complement lysis inhibitor (או CLI), secreted glycoprotein gp80; complement-associated protein SP-40, AAG4, KUB1, sulfated glycoprotein-2 ,SGP2 NA1/NA2.
|
|
|
|
|
| מעבדה
|
פתולוגיה ברקמה
|
|
|
|
| תחום
|
חלבון רב-תכליתי בסוגי סרטן ובמחלות נוירו-דגנרטיביות.
|
|
|
|
|
|
| יוצר הערך
|
פרופ' בן-עמי סלע
|
המבנה של clusterin
Clusterin הוא גליקו-חלבון הטרודימרי עתיר חומצה סיאלית כאשר כל מולקולה של clusterin מכילה 28 שיירים של חומצה סיאלית. המשקל המולקולרי של clusterin הוא 75–80 אלף דלטון, והוא מורכב מ-2 שרשרות פפטידיות (שרשרת α ושרשרת β) לא זהות הקשורות ביניהן על ידי 5 קשרים די-סולפידיים. בבני אדם, clusterin מקודד על ידי הגן CLU הממוקם על כרומוזום 8 בעמדה 18p21-p12, גן המכיל 9 אקסונים ומבטא שלושה איזופורמים שעברו splicing באקסון 1 (על פי Koltai ב-Onco Targets Ther משנת 2014). האיזופורמים ממוקמים באזורי-תא שונים: אחד מהם ממוקם בגרעין התא, איזופורם אחר ממוקם בציטופלזמה, והאיזופורם השלישי מופרש מהתא (Lin וחב' ב-J Hepatol משנת 2014). לאיזופורמים אלה תפקידים מנוגדים: האיזופורם בגרעין נקשר לחלבון Ku70 ועל ידי כך משחרר את BAX ומשרה בתאים אפופטוזיס (Sansanwal וחב' ב-J Am Soc Nephrol משנת 2015), בעוד שהאיזופורמים הציטופלזמטי והמופרש הם בעלי השפעה מעכבת אפופטוזיס. האיזופורם בגרעין מקודד לחלבון בעל משקל מולקולרי של 49KDa, בעוד שהאיזופורם המופרש שהוא האיזופורם העיקרי מקודד לחלבון בעל המשקל המולקולרי של KDa75-80 לאחר בשלותו (גליקוזילציה, הפרשה ודימריזציה). חלבון clusterin הבשל מכיל 449 חומצות אמינו. הגן CLU מבוטא חזק בכבד, במוח, בשחלות ובאשכים, ומבוטא בעוצמה מופחתת יותר בריאות, בלב, בשד ובטחול (Aronow וחב' ב-Proc Natl Acad Sci USA משנת 1993). ל-clusterin של אדם יש הומולוגיה של 75% עם זה של עכבר, והומולוגיה של 77% עם clusterin של חולדה.
Clusterin מסונתז כפוליפפטיד המכיל 427 חומצות אמינו, העובר ברטיקולום האנדופלזמטי ביקוע פרוטאוליטי בין Arg205 ו-Ser-206, ליצירת 2 תת-יחידות הנותרות קשורות ביניהן על ידי קשרים דיסולפידיים לקבלת הטרודימר. צורת הקודמן או ה-pre-clusterin, היא בעלת משקל מולקולרי של 69 קילו-דלטון, בעוד שמולקולת clusterin הבשלה שעברה גליקוזילציה היא בעלת משקל מולקולרי של 75–80 קילו-דלטון, והיא מכונה secretory clusterin או sClu. המבנה של clusterin מנבא שהוא מכיל סלילונים אמפיפתיים, העשויים לסייע לקשר שלו עם חלקיקי HDL. ה-clusterin הגרעיני (או nClusterin) מתורגם תחילה כקודמן של חלבון non-glycosylated, המכונה pnCLU והוא בעל משקל מולקולרי של 49 קילו-דלטון, שעובר טרנסלוקציה לגרעין. יש ראיה לכך שקיימות שתי מולקולות clusterin גרעיני שונות. בעלות משקלים מולקולריים של 50 קילו-דלטון ו-60 קילו-דלטון, בערך (Pajak וחב' ב-J Cereb Blood Flow Metab משנת 2007), שיכולות להיווצר על ידי תרגום המתחיל או ב-ATG הנמצא על אקסון 3, או על אקסון 1, בהתאמה.
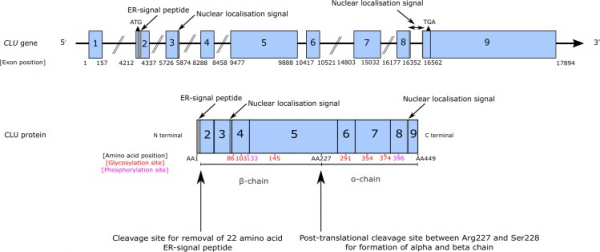
תרשים סכמטי של מבנה הגן CLU והחלבון cluserin
תפקודו של clusterin
החלבון clusterin התגלה לראשונה בנוזל האשכים של עגל, בו הוא הראה נטייה של הצמדות (clustering) עם תאי Sertoli ועם אריתרוציטים ומכאן נגזר שמו (Fritz וחב' ב-Reprod Biol משנת 1983). CLU הוא חבר במשפחת חלבוני heat shock, ולכן הוא מוגדר chaperone מולקולרי. שלא בדומה לרוב חלבוני chaperone האחרים, המסייעים לחלבונים תוך-תאיים, CLU הוא chaperone ב-Golgi, המסייע להתקפלות של חלבונים מופרשים באופן שאינו תלוי ב-ATP. הגן CLU משומר מאוד בין species שונים, והחלבון clusterin נפוץ מאוד ברקמות ואיברים שונים, בהם הוא משתתף בתהליכים כמו טרנספורט של ליפידים, תהליכי recycling של ממברנות, ספיחה בינתאית, אפופטוזיס, ותמס תאים בתיווך המשלים.
ביטוי-יתר של של האיזופורם המופרש של CLU מגן על התא מפני אפופטוזיס המושרה על ידי כימותרפיה, הקרנות, או חסר של אנדרוגן/אסטרוגן. Clusterin מעודד הישרדות התא במספר דרכים: על ידי העיכוב של BAX על ממברנת המיטוכודריון, על ידי השפעול של המסלול phosphatidylinositol 3-kinase/protein kinase B, מודולציה על ידי איתות של ERK או extracellular signal–regulated kinase ושל ביטוי האנזים matrix-metallopeptidase-9, סיוע לתהליך ה-angiogenesis, ומעורבות במסלול של NF-κB. כמו כן, clusterin מאפשר את השפעול של p53, באופן המשנה את היחס בין הפעילות המקדמת אפופטוזיס לבין הפעילות האנטי-אפופטוטית של חברי משפחת Bcl-2, דהיינו ריסון פעילות clusterin מאפשר את השפעול של p53, מה שגורם לשיבוש הפעילות המיטוכונדריאלית ולמות התא.
חלבון זה כרוך בפינוי של פסולת תאית ובאפופטוזיס (Jones ו-Jomary ב-Int J Biochem Cell Biol משנת 2002). שלושת האיזופורמים של clusterin כרוכים כאמור באופן דיפרנציאלי בתהליכים מקדמי-אפופטוזיס או בתהליכים מנוגדי-אפופטוזיס. בתור שכזה, clusterin קשור למחלות רבות בהן מתרחשים עקה חמצונית, כולל מחלות נוירו-דגנרטיביות, מחלות דלקתיות, סרטן והזדקנות (Koltai ב-OncoTargets and Therapy משנת 2014, ו-Sansanwal וחב' ב-J Am Soc Nephrol משנת 2015, וכן Lin וחב' ב-J Hepatol משנת 2014).
הפונקציות של clusterin אינן ברורות בשלמותן. חילוקי הדעות באשר לתפקודי חלבון זה, נובעים בעיקר מאי ההבנה של שניים מתוך שלושת האיזופורמים של חלבון זה בעלי פעילות סותרת במידה מסוימת. מספר תפקודים כוללים השתתפות באפופטוזיס על ידי יצירת קומפלקס עם Ku70 autoantigen המסייעת לאפופטוזיס, ומאידך גיסא הפרעה לשפעול של Bax המונע אפופטוזיס Yang) וחב' ב-Proc Natl Acad Sci USA משנת 2000, Leskov וחב' ב J Biol Chem משנת 2003, Zhang וחב' ב Nat Cell Biol משנת 2005, ו-Zhang וחב' בBJU Int משנת 2006).
החלבון clusterin נכרך גם תהליך הספרמטוגנזה (Roberts וחב' ב Endocrinology משנת 1991), בטרנספורט של ליפידים על ידי יצירת קומפלקס עם apolipoprotein A-1 בפלזמה (Jenne וחב' בJ Biol Chem משנת 1991, ו Calero-וחב' ב Biochem J משנת 1999, ו Gelissen -וחב' ב Biochem J משנת 1998). כמו כן נכרך clusterin בהתמיינות (דיפרנציאציה) של תאי אפיתל French) וחב' ב J Cell Biol-משנת 1993, Schedin וחב' ב J Mammary Gland Biol Neoplasia משנת 2000, ו- Kim וחב' ב-Diabetes Res Clin Pract משנת 2007), בשפעול המשלים ( Kirszbaum וחב' ב FEBS Lett משנת 1992) ובאיתות של TGF-β דרך Smad2/Smad3 על פי Lee וחב' ב-Biochem Biophys Res Commun משנת 2008).
משמעות קלינית של clusterin
Clusterin יכול לעודד תהליכים טומורוגניים על ידי סיוע להתקשרות בין BAX ו-CLU70, ועל ידי כך למנוע את ההתקשרות של BAX לממברנה החיצונית של המיטוכונדריה המעודדת מות תאים. בקרצינומה של תאי Clear בכליה, פועל clusterin לוויסות האיתות של ERK 1/2, ושל ביטוי של האנזים MMP-9 לעודד נדידת תאים סרטניים, את חדירתם לרקמות בריאות, ואת יצירת גרורות. בסרטן אפיתליאלי של השחלות, נמצא ש-clusterin מעודד אנגיוגניות ועמידות לכימותרפיה. מסלולים אחרים בהם clusterin משתתף על מנת להפחית אפופטוזיס בתאים סרטניים כוללים את מסלולי P13/AKT/mTOR ו-NF-κB. בניגוד לסוגי סרטן אחרים בהם רמות clusterin מוגברות על מנת להגביר את הישרדות התאים הסרטניים, ב-testicular seminoma רמות clusterin נמוכות יותר, מה שמאפשר רגישות מוגברת לטיפול כימותרפי. אכן, עיכוב clusterin מביא להגברת היעילות של תכשירים כימותרפיים, ולדוגמה custirsen, שהוא antisense oligonucleotide החוסם את ה-mRNA של clusterin, מעודד את הפעילות המעכבת של heat-shock protein 90, על ידי דיכוי תגובת heat-shock בסרטן ערמונית העמיד לסירוס.
כפי שמסתבר מתפקידי המפתח של clusterin בתהליך הסרטני, חלבון זה עשוי להיות גם יעד תרפויטי לעיכוב שגשוג הגידול הסרטני ולמניעת עמידות הסרטן לכימותרפיה. נמצא ש-clusterin מעורב גם במחלות מידבקות כגון הפטיטיס C. נראה ש-clusterin מושרה על ידי העקה של הידבקות בנגיף Hep C שפוגעת בוויסות של גלוקוזה. נראה ש-clusterin מסייע להתגבשות הנגיף על ידי ייצוב יחידות NS5A והליבה (core) של הנגיף. הביטוי של clusterin בכליות משחק תפקיד במחלות כליה, כגון nephropathic cystinosis, המהווה סיבה עיקרית לתסמונת Fanconi. בנוסף למחלות שהוזכרו, clusterin נכרך גם עם מצבים נוספים הנגרמים מנזק חמצוני, כולל הזדקנות, גלומרולו-נפריטיס, טרשת עורקים ואוטם שריר הלב.
מלבד תפקידו החשוב של clustertin באפופטוזיס, יש לו פעילויות נוספות הקשורות להתנהגות תאי הסרטן. לדוגמה, ב-clear cell renal carcinoma, מווסת clusterin פעילות אגרסיבית על ידי מודולציה חוץ-תאית של איתות הקינאזה ERK1/2, וביטוי של MMP-9 (על פי Wang וחב' ב-Urol Int משנת 2013). על ידי ביטול פעילות של sClusterin נמצא כושר נדידה מופחת של התאים, כושר מופחת של יכולת פלישה in vitro, כמו גם פוטנציאל גרורתי מופחת של התאים הסרטניים. ביטוי-יתר של clusterin בסרטן אפיתליאלי של השחלות, עם יכולת אנגיוגנית מוגברת, במה שיכול להתפרש כתפקיד של clusterin כאונקוגן בביולוגיה של סרטן השחלות. בנוסף, sClusterin מגביר את העמידות של תאי סרטן השחלות לכימותרפיה. כמו כן, clusterin מווסת את הפעילות של NF-κB (על פי Essabbani ב-J Biol Chem משנת 2010). רמות מוגברות של clusterin בשתן התגלו במצבים של נזק לאבוביות הקריבניות והרחיקניות בכליה, אך לא במצבים של נזק גלומרולרי.
Clusterin וסרטן השד
הביטוי של clusterin נמצא במתאם עם התפתחות סרטן השד (Redondo וחב' ב-Am J Pathol משנת 2000, ו-Krueger וחב' ב- Neoplasma משנת 2007). בסרטן השד, הרלוונטיות של clusterin דומה לזו שבסרטן הערמונית: Wang וחב' הראו ב-J Chemother משנת 2012, ש-sClusterin מקנה לתאי סרטן שד עמידות לאפופטוזיס המושרה על ידי TNF-α, דרך שפעול של NF-κB וביטוי-יתר של Bcl-2. מחקר שבחן את ההשפעה של עיכוב Bcl-2 על ידי siRNA על נדידת תאי שד סרטניים, חודרנותם לרקמות בריאות, ויכולת שגשוגם in vivo ו-in vitro, נקט בטרנספקציה של תאי שד סרטניים מסוג MDA-MB-231 עם pSuper-siRNA/sCLU (על פי Niu וחב' ב-Arch Biochim Biophys משנת 2012). תוצאות ניסוי זה הראו שהשקטת sClusterin עיכבה באופן משמעותי את השגשוג של תאי MDA-MB-231. כמו כן הופחתו יכולות הנדידה והחודרנות של תאים אלה, ועלתה הפעילות האפופטוטית של תאים אלה שעיכבה את גידול התאים, ופחתה יכולתם לשלוח גרורות לריאות.
תאי סרטן שד triple negative (בו התאים הסרטניים של הגידול אינם מבטאים קולטנים לאסטרוגן ולפרוגסטרון וכן אינם מבטאים כמות מוגברת של החלבון HER2, כאשר כ-10-20% מכלל מקרי סרטן השד הם שליליים לשלושת הסמנים) מכילים sClusterin באחוז גבוה הרבה יותר בהשוואה לתאי סרטן שד שאינם triple negative. אכן התאים האחרונים אגרסיביים יותר מתאי סרטן שד שאינם triple negative. חלק מהחוקרים סבורים ש-sClusterin כרוך בתהליך של triple negativity של תאי סרטן שד (Zhang וחב' ב-Cancer Biol Ther משנת 2012).
Clusterin וסרטן המעי הגס והחלחולת
עיכוב של clusterin ושל thrombospondin-1, מבטל את הזרחון על ידיp38 mitogen-activated protein kinase ואת פעילות MMP-9. Clusterin ו- thrombospondin-1 המופרש מטסיות-דם, מעודדים את ויסות האיתות של MMP-9 בתהליך הגרורתי של סרטן המעי הגס דרך מסלול המווסת על ידי p38 mitogen-activated protein kinase. ממצאים אלה רלוונטיים לפיתוח של תכשירים טיפוליים המפחיתים את הגרורתיות של אדנו-קרצינומה של המעי הגס (Radziwon-Balicka וחב' ב- Carcinogenesis משנת 2013). במעי הגס, ביטוי-יתר של s-clusterin נמצא רק בציטופלזמה של גידולים מאוד גרורתיים. הרמה המוגברת של האיזופורם המופרש, וההיעלמות של האיזופורם הגרעיני, נכרכים באופן ישיר עם הישרדות גדולה יותר, אגרסיביות מוגברת ופוטנציאל גרורתי גבוה יותר (Pucci וחב' ב-Oncogene משנת 2004). רמות מוגברות של clusterin נמצאו בציטופלזמה של תאי סרטן המעי הגס והחלחולת (Xie וחב' ב-World J Gastroenterol משנת 2005), ורמות clusterin מוגברות נכרכו עם פרוגנוזה גרועה באלה עם סרטן המעי הגס stage II (Kevans וחב' ב- Cancer Epidemiol Biomarkers Prev משנת 2009, ו-Kruger וחב' ב-Neoplasma משנת 2007). רמות clusterin מוגברות נמצאו גם בצואה של חולים סרטן המעי הגס (Pucci וחב' ב- Am J Gastroenterol משנת 2009).
Clusterin וסרטן הערמונית
מספר מחקרים מצאו רמות נמוכות של clusterin בסרטן הערמונית (Bettuzzi וחב' ב-Oncogene משנת 2000, Scaltriti וחב' ב-Int J Cancer משנת 2004 ו-Rauhalta וחב' ב-Int J Cancer משנת 2008). לעומת זאת, ישנם גם דיווחים על רמת clusterin מוגברת בסרטן הערמונית, במיוחד לאחר טיפול אבלציה להפחתת רמת האנדרוגן (July וחב' ב-The Prostate משנת 2002). הבדל זה מוסבר על ידי מדידה של איזופורמים שונים של clusterin: רמת האיזופורם המעודד אפופטוזיס nCLU יורדת, לעומת האיזופורם האנטי-אפופטוטי sCLU שרמתו עולה, אכן, תרפיה של antisense oligonucleotide כנגד clusterin נבחנת בניסויים קליניים, בעיקר כדי למנוע עמידות לטיפולים כימיים (Sowery וחב' ב-BJU Int משנת 2008, ו-Zelinski וחב' ב-Cancer J משנת 2003). clusterin משמש בטיפולים משולבים עם tocetaxel בסרטן ערמונית מתקדם, העמיד לסירוס (Higano ב-Oncol Targets Therapy משנת 2013). נתונים המאששים תפקיד מדכא של clusterin כוללים דיווחים על בקרה אפיגנטית של ביטוי clusterin בשורות תאי סרטן הערמונית. פותח זן טרנסגני של עכבר knockout הידוע כ-TRAMP/cluCO שאינו מייצר clusterin ומפתח סרטן ערמונית פחות ממוין ויותר גרורתי (Bettuzzi וחב' ב-Oncogene משנת 2009). על פי Rauhalta וחב' ב-Int J Cancer משנת 2008, רמת clusterin נמצאת תחת ויסות באופן אפיגנטי בסרטן הערמונית.
בתאי סרטן הערמונית נתגלתה היכולת של sClusterin לווסת את ה-ubiquitination ואת קצב הפירוק של COMM domain-containing protein 1. (על פי Zoubeidi וחב' ב-Mol Cancer Res משנת 2010). בהתאם, פגיעה ב-sClusterin מייצבת את COMM domain-containing protein 1, מנטרלת את NF-κB בציטופלזמה, ומפחיתה את השעתוק של רבים מהגנים המווסתים על ידי גנים. הביטוי של clusterin נמצא תחת בקרה גנטית ואפיגנטית, כאשר האחרונה מושפעת ממתילציה של ה-promoter שלה (Serrano וחב' ב-Tumor Biol משנת 2009).
Clusterin וסרטן השחלות
ביטוי מוגבר של clusterin כרוך בהתנהגות ביולוגית אגרסיבית והישרדות נמוכה בסרטן השחלות (Yang וחב' ב- Int J Gynecol Cancer משנת 2009, ו-Wei וחב' ב-Int J Cancer משנת 2009). מתילציה של ה-promoter בגן CLU מופיעה בתדירויות נמוכות בגידולים של תאי אפיתל בשחלות, והיא כרוכה באופן משמעותי בביטוי גני נמוך יותר של clusterin (Yang וחב' ב- Arch Gynecol Obstet משנת 2013). נמצא שבתאי גרנולוזה בשחלות של אדם ושל חולדה יש השרייה של אפופטוזיס על ידי cAMP במנגנונים בלתי מזוהים. ההשפעה האפופטוטית של cAMP מלווה על ידי הגברה של ביטוי של p53 ושל Bax. לא התגלה שום שינוי ברמת החלבון Bcl-2 בתאי גרנולוזה מטופלים ב-cAMP, מה שמצביע על כך ש-cAMP עשוי לשפעל אפופטוזיס על ידי שינוי היחס בין death promoter genes לבין death repressor genes דרך שינוי היחס בין ביטוי p53 לבין ביטוי Bax. כיוון ש-cAMP נמצא גם מעכב את ביטוי הגן CLU, נראה שיש לחלבון זה תפקיד באפופטוזיס המושרה על ידי cAMP בתאי גרנולוזה (Zwain ו-Amato ב- Endocr Res משנת 2001). טיפול של תאי גרנולוזה עם antisense oligonucleotide המכוון נגדclusterin גרם להגברת אפופטוזיס, מה שמרמז שחסר ב-clusterin יכול לגרום לאפופטוזיס בשחלות ולאטריזיה פוליקולרית (Zwain ו-Amato ב-Cell Res Exp משנת 2000). על פי Fu וחב' ב-Mol Med Rep משנת 2013, ביטוי יתר של clusterin מעודד אנגיוגניות דרך VEGF בסרטן שחלות ראשוני וממילא מגביר את האגרסיביות של סרטן זה.
Clusterin וסרטן הפנקריאס
השרייה של clusterin מלווה תהליכי רגנרציה בפנקריאס של חולדות לאחר כריתה חלקית של הבלוטה (Lee וחב' ב- Dev Dyn משנת 2011). בעכברי knockout שאינם מייצרים clusterin, כריתת הבלוטה גורמת ליצירה מעטה של אוניות הבלוטה, ובעיקר הרגנרציה של תאי β הייתה מועטה יחסית והייתה כרוכה בהיפר-גליקמיה. תאי צנרירי הבלוטה (duct cells) שמקורם מעכברי knockout שהוסרה בהם בלוטת הלבלב החסרים clusterin היו לקויים ביצירת תאי β במערכת in vitro, ויצירה זו שוחזרה על ידי הוספה של clusterin אקסוגני. נראה אם כן ש-clusterin הוא גורם חשוב בביולוגיה של הפנקריאס (Xie וחב' ב-Cancer משנת 2005). טרנספקציה של ה-cDNA של clusterin לתוך תאי duct פנקראטיים בתרבית, הביאה להגברה פי-2.5 בשגשוג תאים, ובהתמרה המושרית של תאי duct בלתי-ממויינים לתאים ממוינים המבטאים cytokeratin. בסרטן הפנקריאס, הביטוי של clusterin כרוך בהישרדות ארוכה יותר (Xie וחב' ב-Pancreas משנת 2002).
Clusterin ו-hepatocarcinoma
קרצינומה של תאי כבד היא אחד מסוגי הסרטן השכיחים והאגרסיביים ביותר, עם פרוגנוזה גרועה של פחות מ-5% למשך 5 שנים. רמות גבוהות של sClusterin נכרכות בממאירויות מוגברות כולל סרטן הכבד. נמצא ש-clusterin מבוטא ביתר ברקמת סרטן כבד גרורתי בהשוואה לסרטן כבד לא-גרורתי (Lau וחב' ב-Oncogene משנת 2006), ומגביר על ידי כך פי-2 את כושר הנדידה של גידול זה in vitro. דווח ש-clusterin משחק תפקיד חשוב בגרורתיות של hepatocarcinoma על ידי הגברת הביטוי של MMP-2 הפחתת הביטוי של E-cadherin (Chen וחב' ב- Int J Mol Sci משנת 2012). נמצא שביטוי יתר של sClusterin תורם לעמידות הסרטן לטיפול ב-oxaliplatin על ידי שפעול מסלול AKT (Xiu וחב' ב-Cancer Sci משנת 2013).
Clusterin וסרטן ריאות
Yan וחב' הציעו ב-Hepatogastroenterology משנת 2013 ש-sClusterin משחק תפקיד חיובי בשגשוג של תאי NSCLC, שעשוי להיות מתווך על ידי מסלול האיתות של PI3K/AKT, והדגימו שהשתקת הגן sCLU המפריע לפעילות RNA, היא אסטרטגיה טיפולית במקרי NSCLC כיוון שהיא פוגעת בשגשוג התאים הסרטניים, חוסמת את מסלול PI3K/AKT, ומשרה אופטוזיס. אף על פי שהביטוי של clusterin נכרך עם ממאירויות שונות באדם, המנגנונים דרכם clusterin מעודד התפשטות וממאירות של סרטן ריאות לא בהירים דיים (Panico וחב' ב-Adv Cancer Res משנת 2009). Chou וחב' דיווחו ב-Signal Cell משנת 2009 ש-clusterin מווסת את מעבר התאים הסרטניים האפיתליאליים לסטאטוס מזנכימלי, ולהתנהגות אגרסיבית של תאי אדנו-קרצינומה של הריאות על ידי מודולציה של איתות ERK וביטוי של Slug/E-cadherin. בשורות תאי small cell lung cancer, נמצא ש-oblimersen, שהוא antisense Bcl-2 oligodeoxynucleotide, מגביר את התגובה של תאים אלה להקרנות. מנגנון הפעולה של oblimersen דומה לזה שלcustirsen בכך שגם הוא מגביר אפופטוזיס.
יש מספר ראיות לכך שעיכוב sClusterin בשלבים מאוחרים של סרטן ריאות יכול להיות טיפול תועלתי, בעוד שבשלבים מוקדמים של המחלה, התוצאות עלולות להיות הפוכות. בניסוי in vitro, השתקת clusterin על ידי antisense oligonucleotides ו-siRNA כנגד mRNA של clusterin שנמצא ברמה גבוהה בשורות תאים מסרטן ריאות, הביא להגברת רגישותם לכימותרפיה ולהקרנות והפחית את הפוטנציאל הגרורתי שלהם. In vivo, מחקר של Panico שבחן את התפקיד הפרוגנוסטי של clusterin ב-NSCLC, מצא שחולים חיוביים ל-clusterin היו בעלי הישרדות טובה יותר מאשר חולי סרטן ריאות זה ללא clusterin. ממצאים אלה נמצאים בסתירה לתוצאות המעודדות של הניסוי in vitro. על בסיס ממצאים אלה מציע Panico שבסרטן ריאה בשלביו המוקדמים, clusterin עשוי להוות סמן חיובי התואם הישרדות טובה יותר.
Clusterin ומלנומה
Hoeller וחב' דיווחו ב-J Invest Dermatol משנת 2005 שבדגימות של מלנומה, הביטוי של clusterin היה נמוך ב-nevi אך גבוה במלנומה ראשונית ובגרורות של מלנומה. Clusterin היה גם מאוד בולט בשורות תאי מלנומה בתרבית, אך היה מבוטא בקושי במלנוציטים בתרבית. על מנת לפרש את התפקיד של clusterin בעמידות של מלנומה לתרופות, נוסו גישות של הגברת הביטוי של clusterin על ידי החדרת פלסמיד לתאים, או החלשת ביטויו על ידי טיפול בתכשירי antisense. נמצא שביטוי יתר של החלבון האמור הביא להגברת העמידות של מלנומה לתרופות, ולהישרדות גבוהה יותר של התאים הסרטניים, ולעומת זאת החלשת הביטוי של clusterin על ידי antisense oligonucleotides המכוונים כנגד mRNA של החלבון, הביאה להחלשת התנגודת של תאי מלנומה לתרופות. Shannan וחב' הראו ב-Anticancer Res משנת 2006, ביטוי מוגבר של clusterin בתאי מלנומה ראשוניים ובתאים גרורתיים של סרטן זה, אך ביטוי מאוד מוחלש בתאי nevus או מלנוציטיים.
הקשר קליני של clusterin למחלת אלצהיימר
שני מחקרים בלתי-תלויים במסגרת genome-wide association studies מצאו קשר סטטיסטי בין SNP בגן ל-clusterin לבין הסיכון ללקות באלצהיימר (להלן (AD. מחקרים בהמשך הראו שמאובחנים עם אלצהיימר, מכילים בדמם רמות גבוהות יותר של clusterin, וכן שיש מתאם בין רמות אלה לבין דעיכה קוגניטיבית מהירה יותר בקרב חולי אלצהיימר, (Lambert וחב' ב-Nat Genet משנת 2009, ו-Harold וחב' באותו כתב עת מאותה שנה, Schrijvers וחב' ב-JAMA משנת 2011), אך עם זאת לא נמצא שרמות clusterin עשויות לנבא את הופעת אלצהיימר (Nuutinen וחב' ב-Brain Res Rev משנת 2009). בנוסף לאלצהיימר, clusterin מעורב גם במחלות נוירו-דגנרטיביות אחרות כמו במחלת Huntington. הסברה היא ש-clusterin מווסת את היצירה וההרחקה של amyloid. רמות מוגברות של clusterin התגלו במוחות ובנוזל השדרה של חולי AD. קבוצתה של Breteler בחנה במסגרת מחקר Rotterdam מדגם של 60 חולי AD שנבדקו לרמת clusterin בדמם, ומדגם נוסף של 156 משתתפים שנתגלו כחולי AD במעקב ממוצע של 7.2 שנים. מחקר זה מצא שההסתברות תחלואה ב-AD שיש ל-clusterin גוברת במתאם טוב עם רמת clusterin בדם. לאחר התאמה לגיל, מגדר, רמת השכלה, סטאטוס apoE, סוכרת, עישון, יתר לחץ-דם ומחלת לב, הסיכון ללקות ב-AD גדל ב-63% ברמות גבוהות של clusterin (Lambert וחב' ב-Nature Genet משנת 2009). בחולי AD רמות מוגברות של clusterin נמצאו כרוכות במחלה חמורה יותר, כפי שנקבע על ידי הדעיכה בתוצאת Mini-Mental State Examination. השערה עדכנית היא שיש ל-clusterin יכולת לקשור פפטידים של Aβ ובכך משפיעה על האגרגציה של העמילואיד, על השקיעה המוחית של העמילואיד ועל כושר הפינוי שלו מהמוח, אם כי מנגנונים אלה צריכים עדיין להיחקר.
תכשירים פרמצבטיים בהֶקשר של clusterin
חברת OncoGeneX Pharmaceutical פיתחה את התכשיר custirsen (או OGX-011 במקור), שהוא antisense oligonucleotide מהדור השני, שתוכנן לחסום את ה-mRNA של sClusterin, כדי להפחית את יצירת החלבון האמור ולשפר ממצאים קליניים בתרחיש של סרטן מתקדם של הערמונית העמיד לסירוס. יש ראיות לכך ש-custirsen עשוי להיות יעיל גם בסוגי סרטן נוספים כמו סרטן שד, סרטן שחלות, סרטן ריאות (Laskin וחב' ב-J thorac Oncol משנת 2012), ו-clear cell renal carcinoma.
מה היו הסיבות לפיתוח custirsen ? יכולת תכשיר זה להיקשר לאקסון 1 של sClusterin mRNA וחסימת התרגום שלו. אכן, פיתוח תכשיר זה התקדם על בסיס הממצאים הבאים:
- תאי renal carcinoma המבטאים ביתר את sClusterin נעשים עמידים יותר לאפופטוזיס (Miyake וחב' ב-Mol Urol משנת 2001)
- אוליגונוקלאוטידים המתכווננים כנגד sClusterin מגבירים את רגישות תאי סרטן הערמונית לטיפולי הקרנות (Zellweger וחב' ב-Clin Cancer Res משנת 2002)
- אוליגונוקלאוטידים המכוונים כנגד sClusterin מגבירים את רגישות התאים לתכשירים כימותרפיים (Gleave וחב' ב-Urology משנת 2001)
הניסוי המכונן של Miyake וחב' שהתפרסם ב-J Urol בשנת 2002, בו החדירו חוקרים אלה את הגן CLU לתאי renal cell carcinoma ועודדו בכך את הפוטנציאל הגרורתי של תאים אלה, הביא להפנמת הגישה של הצורך להפחית את הביטוי או את הפעילות של clusterin בתאים הסרטניים. Custirsen נמצא מגביר את הציטו-טוקסיות כאשר הוא משולב עם docetaxel בתאי קרצינומה של הערמונית, או עם sorafenib ב-clear cell renal carcinoma (על פי Kusuda וחב' ב-Br J cancer משנת 2012), עם cisplatin ב-clear cell renal carcinoma, או עם gemcitabine ותרכובות platin בתאי סרטן ריאות. Clusterin נמצא ראוי להוות יעד טיפולי בסרטן לא רק בגלל הפעילות האנטי-אפופטוטית שלו לאחר טיפול כימותרפי, אלא גם בגלל פעילויות מעודדות ממאירות שהוא עלול לייצר, כגון שפעול של המסלול P13K/AKT, הגברת הריכוז של vascular endothelial growth factor, איתות על ידי ERK1/2, ביטוי-יתר של MMP-9 ווויסות NF-κB. עיכוב של clusterin על ידי שימוש ב-custirsen מעודד פעילות של מעכב של heat-shock protein 90 על ידי דיכוי תגובת heat-shock בתאי סרטן ערמונית עמידים לסירוס. הבחירה במסלול האפופטוזיס כיעד של תכשירים טיפוליים, מסמלת בהחלט גישה חדשה בפיתוח המואץ של תכשירים דוגמת oblimersen (שהוא antisense oligonucleotide החוסם את Bcl-2) על פי Loriot וחב' ב-Anticancer Res משנת 2010, ו-Advani וחב' ב-Expert Opin Drug Metab Toxicol משנת 2011). תכשירים חדשים נוספים הם apatorsen (או OGX-427) שהוא antisense oligonucleotide המכוון כנגד heat-shock protein 27 הנבחן בטיפול משולב עם gemcitabine ו-cisplatin בסרטן מתקדם של שלפוחית השתן (Ischia וחב' ב-Nature Rev Urol משנת 2012).
הוראות לביצוע הבדיקה
הבדיקה מתבצעת על ידי צביעה אימונו-היסטוכימית של ביופסיה או של רקמה שהתקבלה בצורה אחרת, כאשר חיתוך במיקרוטום צריך להיות מכוון לפרוסות בעובי של 4 מיקרון. יתקבלו במעבדה הפתולוגית בלוקים שעברו פיקסציה בפורמלין, ותהליך של embedding בפרפין. יש לדחות דגימות של רקמה קפואה או רטובה, משטחים ציטולוגיים, רקמה שלא עברה קיבוע בפורמלין, או שלא עברה embedding בפרפין. לא יתקבלו non-charged slides, או probeOn slides. עדיף שהדגימות תגענה למעבדה בטמפרטורת החדר, אך גם דגימות בקירור תתקבלנה.
תוצאות הבדיקה
בבלוטות לימפה, בשקדים ובטחול, צביעה ל-clusterin צובעת תאים דנדריטים פוליקולריים. תאי B, תאי T והיסטיוציטים אינם נצבעים. צביעה ל-clusterin מתקבלת לעיתים קרובות חיובית בתאים סרטניים של -large-cell lymphoma אנאפלסטית, אך הצביעה בדרך כלל שלילית בתאי Reed Sternberg בלימפומה קלאסית ע"ש Hodgkin (על פי Grogg וחב' ב-Am J Surg Pathol משנת 2004, Grogg וחב' ב-Modern Pathol משנת 2005, ו-Saffer וחב' ב-Modern Pathol משנת 2002).
ראו גם


 כניסה
כניסה  עקבו אחרינו בפייסבוק
עקבו אחרינו בפייסבוק 
