המדריך לטיפול בסוכרת - התסמונת המטבולית וטרום סוכרת
המדריך לטיפול בסוכרת
מאת המועצה הלאומית לסוכרת, משרד הבריאות. עורכים מדעיים: ד"ר עופרי מוסנזון, פרופ׳ איתמר רז
ערך זה נמצא בבדיקה ועריכה על ידי מערכת ויקירפואה, וייתכן כי הוא לא ערוך ומוגה.
לערכים נוספים הקשורים לנושא זה, ראו את דפי הפירושים: – תסמונת מטבולית, סוכרת
תסמונת מטבולית המאופיינת על ידי השמנה, היפרגליקמיה, היפרליפידמיה ויתר לחץ דם מהווה גורם סיכון משמעותי להתפתחות סוכרת מסוג 2, סיבוכים קרדיווסקולרים ותמותה[1][2][3].
על פי ההגדרות המקובלות ניתן לסווג אדם כסובל מתסמונת מטבולית כאשר מתקיימים לפחות 3 מהתנאים הבאים[4]:
- סוכר בצום מעל 100 מיליגרם /ר"ל או נטילת טיפול תרופתי לסוכרת
- השמנה בטנית המוגדרת כהיקף מותנים מעל 88 סנטימטר בנשים או מעל 102 סנטימטר בגברים
- רמות טריגליצרידים מעל 150 מיליגרם /דציליטר או טיפול תרופתי הניטל להורדת רמות טריגליצרידים
- רמות HDL נמוכות מ-40 מיליגרם /דציליטר בגבר ונמוכות מ-50 מיליגרם /דציליטר באישה
- לחץ דם גבוה מ-130/85 או נטילת טיפול להורדת לחץ דם
על פי הגדרות אלה, השמנה מאופיינת כעלייה בהיקף מותניים ולא ב-BMI וזאת עקב העובדה שעלייה בהיקף המותניים קשורה באופן הדוק יותר מ-BMI לסיכון בהתפתחות סוכרת מסוג 2 וסיבוכים קרדיווסקולרים[5][6][7]. כפי שניתן לראות בהגדרות, ה-BMI אינו מהווה קריטריון להגדרת תסמונת מטבולית למרות היותו גורם סיכון מובהק לסיבוכים קרדיווסקולרים, כיוון שמטרת ההגדרה של התסמונת המטבולית היא לאתר גורמי סיכון נוספים מעבר ל-LDL.
תהליכים פיזיולוגיים שונים משפיעים ומזרזים התפתחות של תסמונת מטבולית: אורח חיים, גנטיקה, גיל, השמנה, תנגודת לאינסולין ועוד. מתוך הידע הנצבר, נראה כי התנגודת לאינסולין מהווה את הגורם המכריע והמקשר בהתפתחות התסמונת המטבולית[8]. תנגודת לאינסולין נגרמת, בין השאר, עקב עלייה בחומצות שומן חופשיות (FFA) אשר משפעלות מסלולים דלקתיים, הפרשה של ציטוקינים[9][10], פגיעה במיטוכונדריה התאית ועלייה ביצירה של רדיקלים חופשיים[11].
לאור הקשר ההדוק שבין התסמונת המטבולית לבין תחלואה בסוכרת, סיבוכים קרדיווסקולרים ותמותה כללית, ישנה חשיבות קלינית בזיהוי חולים אלה והתערבות טיפולית הכוללת שינוי אורח חיים, פעילות גופנית, הורדת לחץ דם וכולסטרול.
טרום סוכרת
טרום סוכרת היא מצב מטבולי מורכב אשר השלכותיו משמעותיות הרבה מעבר להפרעה במטבוליזם הסוכר. על פי ה-ADA, טרום סוכרת מוגדרת כאחד מהבאים (Diagnosis and classification of diabetes, ADA):
- רמות גלוקח בצום- (125-100 - impaired fasting glucose (IFG מיליגרם /דציליטר
- HbAlc- 6.4 אחוזים-5.7 אחוזים
רמות גלוקוז שעתיים לאחר העמסת גלוקוז (75 מיליגרם )-140-199 -(impaired glucose tolerance (IGT מיליגרם /דציליטר.
החשיבות בהגדרה זו נובעת ישירות מהעובדה שמטופלים עם טרום סוכרת נמצאים בסיכון גבוה מאוד, פי 3–10 לפתח סוכרת. ה-ADA מעריך כי כ-70 אחוזים מהאנשים עם טרום סוכרת יפתחו סוכרת במהלך חייהם. כמו כן, טרום סוכרת מהווה גורם סיכון לסיבוכים מיקרו ומאקרווסקולריים וכן כבד שומני, תסמונת דום נשימתי בשינה ועוד[12]. ביכולתנו כמטפלים לעכב ואף למנוע את התקדמות המחלה על ידי עידוד המטופל לשינוי אורח חיים והתאמת טיפול תרופתי.
מצב של טרום סוכרת מהווה, כאמור, גורם סיכון מג'ורי להתפתחות סוכרת אשר גובר עוד יותר בהינתן גורמי סיכון נוספים כגון היסטוריה משפחתית, סוכרת בהיריון, השמנה, תסמונת מטבולית. מספר עבודות ניסו לפתח סמנים ואלגוריתמים אשר יחזו את הסיכון של האדם לעבור מטרום סוכרת לסוכרת, אולם טרם נעשה בהם שימוש קליני רחב[13][14] ה-Centers for Disease Control and Prevention) CDC) פיתח שאלון קצר למבוגרים אסימפטומטיים אשר מעריך את הסיכון שלהם לפתח טרום סוכרת:
- האם נולד לך ילד במשקל העולה על 4 ק"ג
- האם יש לך אחים/יות עם סוכרת?
- האם הוריך סבלו/ים ממחלת הסוכרת?
- האם ה-BMI שלך מעל 27
- האם אתה פעיל גופנית בצורה יומיומית?
- האם גילך 64-45?
- האם גילך מעל 65?
כל שאלה מקבלת ניקוד ואם התוצאה עולה על 9 נקודות, הסיכון של המטופל לפתח טרום סוכרת גבוה[15].
מחלת הסוכרת מהווה מגפה עולמית וההיארעות של טרום סוכרת עולה מאוד הן בארצות המפותחות והן בארצות המתפתחות. ה-CDC מדווח כי בארצות הברית חיים כ-84 מיליון בני אדם הסובלים מטרום סוכרת וכי 9 מתוך 10 אנשים עם טרום סוכרת כלל לא מודעים למצבם (https://www.cdc.gov/diabetes/pdfs).
ה-IDF) international Diabetes Federation) העריך שכ-352 מיליון בני אדם בעולם נמצאים במצב של טרום סוכרת נכון ל-2017 ומהווים כ-7.3 אחוזים מהאוכלוסייה המבוגרת העולמית. מספר זה צפוי לעלות ל-כ-587 מיליון בני אדם, כ-8.3 אחוזים מהאוכלוסייה המבוגרת בשנת 2045[16]. העובדה שאחוזים גבוהים מאלה המוגדרים כטרום סוכרתיים יוגדרו כחולי סוכרת מדי שנה היא בלתי נתפסת, ומדאיגה מאוד את הקהילה הרפואית העולמית.
על פי הערכת הרשם הלאומי לסוכרת, נכון לשנת 2015, כ-6.7 אחוזים מאוכלוסיית ישראל חולים במחלת הסוכרת. בגילאי 65 ומעלה מדובר באחד מתוך כל שלושה ישראלים (סוכרת בישראל, תמונת מצב. המדריך לטיפול בסוכרת 2019.
רמות גלוקוז מוגברות בחולים הטרום סוכרתיים נובעות מהשילוב בין תנגודת השריר והכבד לפעולתו של האינסולין (insulin resistance, IR) לבין הירידה ביכולת של תאי הבטא בלבלב להפריש אינסולין בתגובה לגלוקוז. גורמי סיכון להתפתחות IR הן כל הסיבות שצוינו לעיל: השמנה, בעיקר בטנית, חומצות שומן חופשיות בפלזמה (FFA) ועוד. אחד המחקרים (The Whitehall study) הראה כי תופעת התנגודת לאינסולין מתחילה כ-13 שנה טרם האבחנה של הסוכרת וכי רמות גלוקוז קרובות לנורמה בשנים אלה נובעת עקב עלייה בייצור והפרשת האינסולין על ידי תאי הבטא. בסופו של דבר המעבר מ-IR בלבד לסוכרת נובע מכישלון של תאי הבטא להפריש מספיק אינסולין על מנת להתגבר על ה-IR. כאן, למעשה, מתבטאת השונות הגנטית בין בני האדם. חולים עם נטייה גנטית לפתח סוכרת יחוו כישלון של תאי הבטא להפריש כמות נאותה של אינסולין ויפתחו היפרגליקמיה ואילו תאי הבטא של אנשים ללא נטייה לפתח סוכרת ימשיכו להפריש רמות מספקות של אינסולין על מנת להתגבר על ה-IR. מה, אם כן, גורם לכשל של תאי הבטא? שאלה זו נחקרה רבות מאוד בעשורים האחרונים. הסברה משלבת בין הטוקסיות של רקמת השומן (lipotoxicity), הטוקסיות של רמות גלוקוז גבוהות (glucotoxicity), הפעלה של תהליכי דלקת והמנגנונים המפצים בתוך תאי הבטא, אשר גורמים מחד להפרשת יתר של אינסולין ומאידך לפגיעה בתהליכים תוך תאיים אשר עלולים לגרום למות התא.
למרות כל הנאמר, לא כל הטרום סוכרתיים יפתחו בסופו של דבר סוכרת. לכן יש להעריך כל טרום סוכרתי על פי גורמי הסיכון האישיים שלו לפתח סוכרת. מאמר מציע אלגוריתם לחשב את הסיכון של הטרום סוכרתי לפתח סוכרת[17].
המצב הטרום סוכרתי נמצא באסוציאציה לעלייה בסיכון להתפתחות סיבוכים מיקרווסקולרים ומאקרווסקולרים. בין השאר נמצא כי ישנה עלייה בסיכון לנפרופתיה אשר מתבטאת במיקרואלבומינוריה[18], נוירופתיה אוטונומית וסנסורימוטורית[19][20] ורטינופתיה[21]. מבחינה מאקרווסקולרית, טרום סוכרת מהווה גורם סיכון להתקפי לב, שבץ מוחי ותמותה כללית כתוצאה מאירועים קריווסקולרים[18]. לדוגמה, מחקר ה-EPIC-Norfolk הראה כי כל עלייה של 1% ב-HbAic, על אף היותו ברמות ה"נורמה", מעלה את הסיכון לתמותה קרדיווסקולרית תוך 10 שנים.
עם זאת, המצב הטרום סוכרתי הוא, פעמים רבות, מופע קליני אחד מתוך גורמי סיכון רבים כגון השמנה, לחץ דם לא מאוזן, שומני דם גבוהים ולא מאוזנים או תסמונת מטבולית מלאה, אשר כל אחד מהם מהווה גורם סיכון לסיבוכים המוזכרים מעלה. לכן, קשה לעיתים להפריד בין ההשפעה של טרום סוכרת per se על סיבוכים מיקרו ומאקרווסקולרים לבין שילוב הגורמים שיחד מהווים זרז להתפתחות סיבוכים אלה.
מניעת התפתחות סוכרת באנשים הסובלים מטרום סוכרת
לאחר דיון על המצב המוגדר כטרום סוכרת נבחן אפשרויות להתערבות וטיפול. כפי שהוצג, טרום סוכרת מהווה גורם סיכון ברור לסוכרת ועלולה להוות, בנוסף, גורם סיכון לסיבוכים מיקרו ומאקרווסקולרים. לעומת זאת, מדובר במצב התחלתי ואסימפטומטי אשר יכול להימשך שנים רבות. על מנת לבחון בצורה נכונה התערבויות טיפול חייבים קודם להגדיר את מטרות הטיפול. כמו כן, בכל טיפול מסוים יש לשקול יעילות מול בטיחות המטופל. באופן מיטבי, אמור כל טיפול לטרום סוכרת לפעול במספר מישורים:
- דחיית/מניעת הופעת סוכרת
- שמירת תפקוד תאי הבטא
- מניעת סיבוכים מיקרווסקולריים
- מניעת סיבוכים מאקרווסקולריים (תחלואה קרדיווסקולרית)
המציאות רחוקה מכך. מחקרים רבים הציגו התערבויות מגוונות במטופלים עם טרום סוכרת אשר הצליחו לדחות את הופעת הסוכרת בצורה יעילה, אך קשה יותר להדגים שטיפולים אלו אכן מגנים על תפקוד תאי בטא ומונעים סיבוכים וסקולריים.
שינוי באורח החיים
מחקרים רבים מוכיחים ששינויים באורח החיים דוחים/מונעים את הופעת מחלת הסוכרת. שינויים אלו כוללים ירידה במשקל, שינוי מרכיבי התפריט ופעילות גופנית קבועה. חלק מהמחקרים בדקו כל מרכיב בנפרד, אך ההשפעה החזקה ביותר הייתה בשילוב ביניהם.
במחקר ה-Finish Diabetes Prevention study, החלה קבוצת גברים עם השמנה ו-IGT תוכנית לירידה במשקל ופעילות גופנית קבועה, מול קבוצת ביקורת[22]. לאחר שנתיים הייתה ירידת ממוצעת של 3.5 קילוגרם (לעומת 0.8 קילוגרם בביקורת), ולאחר 4 שנים הדגימה קבוצת ההתערבות שכיחות סוכרת של 11 אחוזים (לעומת 23 אחוזים בביקורת). גם לאחר הפסקת המחקר נמשכה ההשפעה המיטיבה של התוכנית. שבע שנים לאחר סיום המחקר עמדה שכיחות הסוכרת על 23 אחוזים, לעומת 38 אחוזים בקבוצת הביקורת.
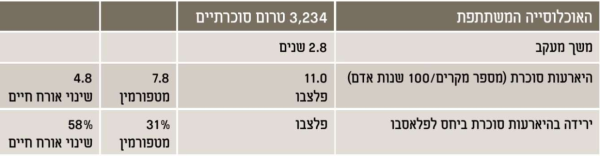
מחקר נוסף -Diabetes Prevention Program, בדק את השפעת השינויים באורח החיים על הופעת סוכרת[23]. במחקר זה, חולקו גברים ונשים בעלי השמנה וטרום סוכרת ל-3 קבוצות: שינויים אינטנסיביים באורח החיים (ירידת משקל ופעילות גופנית), מתן מטפורמין יחד עם מידע על דיאטה/פעילות גופנית, ופלצבו יחד עם מידע על דיאטה/פעילות גופנית[23]. התוצאות היו מרשימות וברורות כל כך, שוועדת בטיחות הפסיקה את המחקר שנה לפני הסיום המתוכנן. לאחר 3 שנים הייתה הופעת הסוכרת שונה באופן מובהק בין זרועות המחקר: 14 אחוזים (שינוי אינטנסיבי באורח חיים), 22 אחוזים (מטפורמין), ו-29 אחוזים (פלצבו). שינוי באורח החיים הוריד את שכיחות הסוכרת ב-58 אחוזים ללא קשר למין, גיל או מוצא אתני. כל משתתף בקבוצה זו הוריד בממוצע 7 אחוזים ממשקלו בשנה הראשונה ולרוב נשמר משקל זה במשך שנות המחקר. למעשה, המרכיב בתוכנית שניבא בצורה החזקה ביותר את היכולת למנוע סוכרת, היה ירידה במשקל. כל ירידה של 1 קילוגרם במשקל הפחיתה את הסיכון לסוכרת ב-16 אחוזים. גם במחקר זה, התועלת של ההתערבות התמידה למשך שנים לאחר סיום המחקר. ראשית, 85 אחוזים מהמשתתפים בחרו מרצונם להמשיך מעקב בקבוצת תמיכה. שנית, כעבור 10 שנים מסיום המחקר, שכיחות הסוכרת בקבוצת ההתערבות הופחתה ב-34 אחוזים לעומת קבוצת הפלצבו.
לאחר הצגת חשיבות אורח החיים הבריא לצורך מניעת סוכרת, נבחן סוגי תפריט ספציפיים. המאכלים המסייעים במניעת סוכרת כוללים חיטה מלאה, ירקות, פירות ושומנים בלתי רוויים וכן הימנעות משומן טראנס, שומן מן החי ופחמימות פשוטות. מספר מחקרים מציינים באופן מיוחד את תפריט הדיאטה הים תיכונית, אשר מפחית את הסיכון לפתח סוכרת. במחקר מסוים, הפחית תפריט ים תיכוני מועשר בשמן זית את השכיחות לסוכרת ב-40 אחוזים, לעומת קבוצת הביקורת. לא היה שוני בשתי הקבוצות במשקל או בהיקף הפעילות הגופנית[24].
הדיאטה הקטוגנית (דיאטה דלת פחמימות) הפכה לפופולרית מאוד בקרב הקהל הרחב. מספר מחקרים נעשו בשאלה האם דיאטה קטוגנית תשפר באופן משמעותי את האיזון המטבולי בטרום סוכרת וסוכרת והראו שיפור משמעותי ברמות ההמוגלובין המסוכרר וכן בירידה במשקל[25][26]. עם זאת, טרם נעשו מחקרים רנדומאליים מבוקרים גדולים על השפעת התזונה הקטוגנית לאורך שנים וכן לא ברור מהו הסיכון לקטואצידוזיס בחולי סוכרת מסוג 1 או אנשים התלויים באינסולין על דיאטה זו. כמו כן, הנושא פרוץ מבחינת כמות הפחמימות הנצרכת המומלצת ובצורך לעקוב אחר קטונים בדם.
על אף כל הנאמר, מתגבשת ההבנה כי תזונה "נכונה" צריכה להיות מותאמת אישית לכל בן אדם ואין מסגרת אחת הנכונה לכולם.
לסיכום: שינויים משולבים באורח החיים (כולל ירידה במשקל, שינוי מרכיבי התפריט וביצוע פעילות גופנית קבועה), עוזרים בצורה יעילה להפחית במשקל ולצמצם את הסיכון לפתח סוכרת. בשני המחקרים הגדולים שהוצגו לעיל, השינויים הללו נשמרים למשך שנים לאחר סיום המחקר. ממצאים אלו מזכירים את תופעת ה"הזיכרון המטבולי" (Metabolic memory) אשר הודגמה במחקרי מעקב של ה-DCCT ו-UKPDS. על פי הנתונים הללו, חשוב לאתר מטופלים בסיכון גבוה לסוכרת בשלבים מוקדמים של חייהם, על מנת להמליץ עבורם על שינוי מהותי והוליסטי באורח החיים, לפני הופעת הסוכרת. שינויים אלו יטיבו עם המטופלים בהווה ובעתיד. היות שאין מדובר בהתערבות ניתוחית או תרופתית, הסיכון למטופל הוא מינימלי ולכן הרווח גובר מאוד על ההפסד.
טיפולים תרופתיים
תרופות רבות נבדקו ונמצאו יעילות במניעת התפתחות סוכרת[27][28]. חלקן נחקרו בשילוב עם שינויים באורח חיים וחלקן בטיפולים תרופתיים בלבד. רוב המחקרים בחנו תכשירים מורידי סוכר (Glucose lowering agents) מקבוצות שונות כגון מטפורמין, אקרבוז, פיוגליטזון, אינסולין-גלרג'ין וגלימפיריד, אך ישנם מחקרים אשר בדקו גם תרופות מקבוצות אחרות כגון אורליסטט, וולסרטן ורמיפריל. היות שחלק גדול מהתרופות הללו הם תכשירים מורידי סוכר, ייתכן והם ממסכים את הופעות הסוכרת אך אינם מונעים אותה. כמו כן, בניגוד לשינוי באורח החיים, מדובר בתרופות עם סיכונים ותופעות לוואי.
מטפורמין נמצא יעיל בהורדת הסיכון לפתח סוכרת, במחקרים רבים. לעומת זאת, הוא פחות יעיל משינויים באורח החיים. הוא מיטיב במיוחד עם מטופלים צעירים שמנים ונשים עם סוכרת הריונית בעבר. מעבר להורדת ערכי הסוכר, הוא משפר במעט את BMM ופרופיל השומנים.
נעשו מחקרים על אגוניסטים של 1-GLP ובהם לירגלוטייד אשר במינונים של 3-1.8 מיליגרם ליום במטופלים עם השמנת ייתר הורידו שכיחות של סוכרת ב-84 אחוזים עד 96 אחוזים במעקב של שנה[29] וב-52 אחוזים במעקב של שנתיים[30]. מחקרים רבים שהוזכרו לעיל הצליחו להדגים ירידה משמעותית בשכיחות סוכרת עם נטילת תרופות. במיוחד פיוגליטזון, אורליסטט, וולסרטן ורמיפריל. למרות זאת, התכשירים הללו אינם בשימוש שגרתי למטרה זו, עקב תופעות לוואי רבות. בהמשך נציג את המלצת ה-ADA לגבי טיפול תרופתי בטרום־סוכרת.
ניתוחים בריאטריים
ניתוחים בריאטריים מפחיתים משקל באופן משמעותי ובמקביל משפרים את איזון הסוכר אך המידע המחקרי למניעת סוכרת במטופלים לאחר ניתוחים בריאטריים הוא דל ביותר. במחקר Swedish obese Subject Trial נבדקו מטופלים 15 שנים לאחר הניתוח[31]. רק 7 אחוזים מהם פיתחו סוכרת, לעומת 28 אחוזים בקבוצת הביקורת. במחקר זה לא התייחסו למצב הסוכר (prediabetes, normoglycemia) לפני הניתוח. כמו כן, היו פגמים רבים באיכות המחקר. נראה שהניתוח הבריאטרי משפר את האיזון הגליקמי הרבה לפני שמתקיימת הירידה במשקל ולכן המחשבה היא שישנו שינוי הורמונאלי משמעותי לאחר ניתוחים אלה והשינויים הללו הם האחראים לירידה החדה ברמות הסוכר.
אנו זקוקים למחקרים נוספים לצורך בחינת כוחו של הניתוח למנוע סוכרת. בנוסף, אנו זקוקים למחקרים לגבי ההתערבויות האחרות במערכת העיכול כגון הכנסת בלון לקיבה, שהן פחות אינווזיביות מהניתוחים הבריאטריים אולם התועלת שלהן במניעת סוכרת לא נחקרה.
התערבות ניתוחית אכן יכולה למנוע סוכרת אך מדובר בתהליך קיצוני לצורך טיפול בטרום סוכרת בלבד. נכון למועד כתיבת מסמך זה, הניתוחים הללו הם לאוכלוסיית מטופלים עם השמנה משמעותית בשילוב מחלות נלוות.
שמירת תפקוד תאי בטא ומניעת סיבוכים וסקולריים ומטבוליים
ידוע שמטופלים עם טרום סוכרת כבר סובלים בשלב זה מפגיעה מסוימת בתפקוד תאי הבטא. כמו כן, הם בעלי סיכון לפתח סיבוכים מיקרווסקולרים (רטינופתיה, אלבומינוריה, נוירופתיה) וקרדיווסקולרים, עוד לפני התפתחות הסוכרת. לכן, ראוי לבחון את היכולת של הטיפולים שהוצגו לעיל (שינוי אורח חיים וטיפולים תרופתיים) לשמר את תאי הבטא ולמנוע סיבוכים. אין מחקרים אשר מצליחים להדגים תוצאות מובהקות אלו. קלינאים רבים מסיקים מהמידע אשר מוכר לנו ממטופלים עם סוכרת. לדוגמה, איזון הסוכרת מונע סיבוכים מיקרווסקלריים ולכן הגיוני לטעון שמניעת מעבר מטרום סוכרת לסוכרת ימנע גם סיבוכים דומים[32]. אשר בדק את יעילות הפיוגליטזון במניעת אירועים קרדיווסקולרים (AMI, CVA, מוות) במטופלים לאחר CVA\TIA עם תנגודת לאינסולין (אך ללא סוכרת). בקבוצת הטיפול, נצפתה ירידת בשיעור ה-CVA וה-AM1 לעומת קבוצת הביקורת (11.8 אחוזים לעומת 9.0 אחוזים). כאן בדקו מטופלים עם תנגודת לאינסולין על פי HOMA-IR INDEX ולא טרום סוכרת.
מחקר אחר על פיוגליטזון בחולי טרום סוכרת הסובלים מכבד השומני (מוכח בביופסית כבד) הראה שטיפול בפיוגליטזון במשך 36 חודשים גרם לירידה משמעותית מאוד בסטאטוזיס הכבדי וכן גרם לנסיגה של המחלה ב-51 אחוזים מהמטופלים. עם זאת, טיפול זה גרם לעלייה במשקל בחולים אלה[33].
לסיכום: חשוב לבחון באופן מחקרי פרוספקטיבי את ההשפעה של טיפול בטרום סוכרת במניעת סיבוכים וסקולרים ובשימור תפקוד תאי בטא.
התוכנית הלאומית למניעת סוכרת בישראל
מדינת ישראל הכירה בעובדה שמחלת הסוכרת מהווה עומס כבד על מערכת הבריאות בבתי החולים ובקהילה. בכדי להתמודד טוב יותר עם המחלה וסיבוכיה הוקם גוף בלתי תלוי, "המועצה הלאומית לסוכרת", אשר מטרתו לבחון ולייעץ למשרד הבריאות בנושאים כגון הגברת המודעות למחלה, חומרתה, הצורך במניעתה והתמודדות עם סיבוכיה. מטרה נוספת היא ליצור מסד נתונים לאומי בתחום הסוכרת על סוגיה השונים, תחלואה, גורמי סיכון ומניעה.
המועצה הלאומית לסוכרת שותפה לתוכנית למניעת סוכרת דרך ניסיון חלוצי המשתמש באיגרות חוב חברתיות לגיוס כספים לשם הפרויקט. מטרת המחקר הייתה לגייס כ-2,250 איש עם טרום סוכרת מתקדמת ולבדוק את השפעת אורח החיים והפעילות הגופנית על מניעת התפתחות סוכרת באוכלוסייה זו.
קיים קושי רב בגיוס מטופלים עם טרום סוכרת וסוכרת לשינוי אורח חיים וכן קיימת נשירה משמעותית במהלך המחקר. דבר זה מתבטא באופן בולט בעבודתה של פרופ׳ רונית אנדוולט וחבריה, במחקרים נוספים בעולם[34][35] וכן במעורבות נרחבת של המועצה למניעת סוכרת בעיר נצרת שבה, למרות מאמצים ניכרים והשקעת כסף רבה, נענו רק 13 אחוזים מהאנשים בסיכון לקריאה לקחת חלק בסדנאות לשינוי אורח חיים. לאור נתונים אלה, המסקנה של המועצה הלאומית הייתה שקשה מאוד למנוע התפתחות סוכרת על ידי סדנאות לאורח חיים בריא בלבד. היות שכך, משנה המועצה כיוון ומתחילה להתרכז במטופלים בסיכון גבוה להתפתחות סוכרת אשר מוגדרים כבעלי רמות סוכר בצום מעל 110 מיליגרם אחוז בלפחות שתי בדיקות אקראיות במשך שנתיים ו-HbAic מעל 6. כיוון שרוב קופות החולים מבצעות בדיקות אלה בכל מקרה במרבית האוכלוסייה המבוגרת בישראל, קל יחסית לזהות את המטופלים בסיכון גבוה ולתכנן דרכי מניעה יעילות. לחלופין, בעולם מקובל להשתמש בשאלוני סקירה ואחד השאלונים הנפוצים ביותר הוא Finish diabetes risk scored, אולם נראה כי Risk scored בישראל שונה ולכן קשה להתבסס על שאלון זה לאיתור חולים בסיכון גבוה בישראל. נעשה מחקר בראשות ד"ר עופרה קלטר המנסה לבנות שאלון שיתאים לאוכלוסייה הישראלית (Personal communication), אולם כיוון ששאלון זה עדיין אינו מתוקף, טרם נעשה בו שימוש קליני.
על סמך הנתונים לגבי יעילות מטפורמין באוכלוסיות מסוימות (ראו את החלק על טיפולים תרופתיים), ממליצה המועצה הלאומית על מתן מטפורמין במניעה לחולים בסיכון גבוה (על פי הנתונים המפורטים מעלה) אשר עונים על אחד הקריטריונים:
- גיל מתחת ל-70
- BMI>30
- נשים עם היסטוריה של סוכרת היריון בעברן
סיכום
טיפול בטרום סוכרת מונע התפתחות סוכרת. ניתן למנוע סוכרת על ידי שינוי באורח חיים ובטיפולים תרופתיים. טרם הוצגה באופן מובהק היכולת למנוע סיבוכים וסקולריים והחמרת תפקוד תאי בטא. חשוב לפתח מחקר מכוון אשר בודק את השפעת הטיפול בטרום סוכרת בפרמטרים הללו - ממצאים חדשים בתחום זה עשויים לשנות את הצורה בה אנו מטפלים בטרום סוכרת. האיגוד האמריקאי ADAהערה|שם=הערה37|(2019) 3. Prevention or delay of type 2 diabetes: Standards of medical care in diabetesd2019. Diabetes Care. https://doi. org/W.2337/dc19-S003.}} ממליץ על שינוי באורח החיים אצל כל מטופל עם טרום סוכרת. השינוי כולל הפחתת משקל במטופלים עם השמנת יתר של כ-7 אחוזים, פעילות גופנית קבועה (30 דקות ליום, 150 דקות לשבוע) והפסקת עישון. כמו כן חשוב להעריך ולאזן גורמי סיכון קרווסקולריים נוספים כגון יתר לחץ דם ודיסליפידמיה. ניתן לשקול תוספת תרופתית במטפורמין במטופלים עם הסיכון הגבוה ביותר לפתח סוכרת, במיוחד מטופלים עם אפיונים מיוחדים (גיל פחות מ-60, BMI מעל 35, נשים שסבלו מסוכרת הריונית בעבר). שימוש ארוך טווח במטפורמין עלול לגרום לחסר של B12 וכדאי לעשות סקירה של רמות B12 במיוחד במטופלים עם אנמיה או/ו נוירופתיה. לגבי תרופות אחרות כגון אגוניסטים ל-1-GLP ואקרבה, תרופות אלה אינן מאושרות על ידי ה-FDA לטיפול בטרום סוכרת אולם יש לשקול את יעילותן במניעת סוכרת כנגד הפרופיל הבטיחותי שלהן.
לסיכום: עלינו לאתר את המטופלים עם טרום סוכרת מוקדם ככל הניתן. אנו מחויבים לכרות איתם ברית ארוכת שנים. המטופלים חייבים להבין שהם מצויים בסיכון מוגבר לפתח מחלות רבות (סוכרת, לחץ דם, דיסליפדמיה, סיבוכים וסקולרים) והדבר מחייב אותם לבצע מעקב קליני ומעבדתי קבוע. כמו כן, נדרש מהם לפתח הרגלים בריאים הכוללים ירידה במשקל ופעילות גופנית קבועה. במקרים מסוימים ניתן לשקול גם מתן מטפורמין.
הדבר החשוב ביותר הוא ביקור קבוע של המטופלים במרפאה שלנו, היות שמדובר במאבק כרוני ולא במחלה חולפת. בכל ביקור עלינו לבחון אותם, להעריך, להמליץ, לעודד ולחייך - כך גוברים הסיכויים שיישמו את המלצותינו ויגיעו אלינו לביקור נוסף.
חשוב לזכור - התסמונת המטבולית וטרום סוכרת
- קיים קשר הדוק בין התסמונת המטבולית לבין תחלואה בסוכרת, סיבוכים קרדיווסקולרים ותמותה כללית
- מטופלים המוגדרים כ"טרום סוכותיים" נמצאים במצב ביניים ובעלי סיכון גבוה מאוד להתפתחות סוכרת והתפתחות סיבוכים קרדיווסקולרים
- כ-318 מיליון בני אדם בעולם נמצאים במצב של טרום סוכרת. מספר זה צפוי לעלות לכ-482 מיליון בני אדם בשנת 2040
- מספו התערבויות הוכחו כיעילות למניעת התפתחות סוכרת בחולים טרום סוכרתיים - שינוי אורח חיים, טיפול תרופתי וניתוחים בריאטריים
- מטפורמין נמצא יעיל בהורדת הסיכון לפתח סוכרת בעיקר באוכלוסיות מסוימות
- יש לשקול טיפול במטפורמין כמניעה של סוכרת מסוג 2 במטופלים עם טרום סוכרת ובמיוחד במטופלים בעלי אפיונים מסוימים - BMI מעל 35, גיל פחות מ-60, נשים שסבלו מסוכרת הריונית בעבר ומטופלים עם HbAic אשר ממשיך לעלות, למרות השינוי באורח החיים
ביבליוגרפיה
- ↑ Pajunen P, Harkanen T, Jula A, et al (2010) The metabolic syndrome as a predictor of incident diabetes and cardiovascular events in the health 2000 Study. Diabetes Metab. https://doi.Org/W.l016/j.diabet.2010.04.003
- ↑ Mottillo S, Filion KB, Genest J, et al (2010) The metabolic syndrome and cardiovascular risk: A systematic review and me- ta-analysis. J. Am. Coll. Cardiol.
- ↑ Ford ES (2005) Risks for all-cause mortality, cardiovascular disease, and diabetes associated with the metabolic syndrome: A summary of the evidence. Diabetes Care
- ↑ Alberti KGMM, Eckel RH, Grundy SM, et al (2009) Harmonizing the metabolic syndrome: A joint interim statement of the international diabetes federation task force on epidemiology and prevention; National heart, lung, and blood institute; Ameri- can heart association; World heart federation; International. Circulation
- ↑ Ohlson LO, Larsson B, Svardsudd K, et al (1985) The influence of body fat distribution on the incidence of diabetes mellitus. 13.5 Years of follow-up of the participants in the study of men born in 1913. Diabetes, https://doi.org/l0.2337/diab.34.10.1055
- ↑ Alberti KGMM, Zimmet P, Shaw J (2005) The metabolic syndrome - A new worldwide definition. Lancet
- ↑ Yusuf S, Hawken S, Ounpuu S, et al (2005) Obesity and the risk of myocardial infarction in 27 000 participants from 52 coun- tries: A case-control study. Lancet. https://doi.org/10.1016/S0140-6736(05)67663-5
- ↑ De Groot L, Chrousos G, Dungan K, et al (2000) Comprehensive Free Online Endocrinology Book
- ↑ Weisberg SP, McCann D, Desai M, et al (2003) Obesity is associated with macrophage accumulation in adipose tissue. J Clin Invest, https://d0i.0rg/10.1172/JCI200319246
- ↑ Jialal I, Huet BA, Kaur H, et al (2012) Increased toll-like receptor activity in patients with metabolic syndrome. Diabetes Care. https://doi.org/! 0.2337/dd 1 -2375
- ↑ Hojlund K, Mogensen M, Sahlin K, Beck-Nielsen H (2008) Mitochondrial Dysfunction in Type 2 Diabetes and Obesity. Endo- crinol. Metab. Clin. North Am.
- ↑ Wilson ML (2017) Prediabetes: Beyond the Borderline. Nurs. Clin. North Am.
- ↑ Edwards CM, Cusi K (2016) Prediabetes: A Worldwide Epidemic. Endocrinol. Metab. Clin. North Am.
- ↑ Buijsse B, Simmons RK, Griffin SJ, Schulze MB (2011) Risk assessment tools for identifying individuals at risk of developing type 2 diabetes. Epidemiol Rev. https://doi.org/10.1093/epirev/mxq019
- ↑ ML W (2017) Prediabetes: Beyond the Borderline. Nurs Clin North Am 665-677
- ↑ IDF https://diabetesatlas.org/IDF_Diabetes_Atlas_8e_interactive_EN/
- ↑ Yokota N, Miyakoshi T, Sato Y, et al (2017) Predictive models for conversion of prediabetes to diabetes. J Diabetes Complica- tions. https://d0i.0rg/10.1016/j.jdiacomp.2017.01.005
- ↑ 18.0 18.1 Bahar A, Makhlough A, Yousefi A, et al (2013) Correlation between prediabetes conditions and microalbuminuria. Nephrou- rol Mon. https://doi.org/10.58l2/numonthly.7646
- ↑ Tesfaye S, Boulton AJM, Dyck PJ, et al (2010) Diabetic neuropathies: Update on definitions, diagnostic criteria, estimation of severity, and treatments. In: Diabetes Care
- ↑ Papanas N, Vinik Al, Ziegler D (2011) Neuropathy in prediabetes: Does the clock start ticking early? Nat. Rev. Endocrinol.
- ↑ Nathan DM, Chew E, Christophi CA, et al (2007) The prevalence of retinopathy in impaired glucose tolerance and recent-on- set diabetes in the diabetes prevention program. Diabet Med. https://doi.Org/10.H11/j.l464-5491.2007.02043.x
- ↑ E. S, M. L, Y. C, et al (2014) Diabetes mellitus, prediabetes, and incidence of subclinical myocardial damage. Circulation. https://doi.org/10.1161/CIRCULATIONAHA.114.010815
- ↑ 23.0 23.1 Knowler WC, Barrett-Connor E, Fowler SE, et al (2002) Reduction in the Incidence of Type 2 Diabetes with Lifestyle Interven- tion or Metformin - NEJMoa012512. N Engl J Med. https://doi.org/10.1056/NEJMoa012512
- ↑ Salas-Salvado J, Bullo M, Babio N, et al (2011) Reduction in the Incidence of Type 2 Diabetes with the Mediterranean Diet. Diabetes Care. https://doi.org/10.2337/dcW-1288.
- ↑ Saslow LR, Kim S, Daubenmier JJ, et al (2014) A randomized pilot trial of a moderate carbohydrate diet compared to a very low carbohydrate diet in overweight or obese individuals with type 2 diabetes mellitus or prediabetes. PL0S One. https://doi. org/10.1371/journal.pone.0091027
- ↑ Saslow LR, Mason AE, Kim S, et al (2017) An online intervention comparing a very low-carbohydrate ketogenic diet and life- style recommendations versus a plate method diet in overweight individuals with type 2 diabetes: A randomized controlled trial. J Med Internet Res. https://doi.org/10.2196/jmir.5806
- ↑ Stevens JW, Khunti K, Harvey R, et al (2015) Preventing the progression to Type 2 diabetes mellitus in adults at high risk: A systematic review and network meta-analysis of lifestyle, pharmacological and surgical interventions. Diabetes Res. Clin. Pract.
- ↑ Gillies CL, Abrams KR, Lambert PC, et al (2007) Pharmacological and lifestyle interventions to prevent or delay type 2 diabe- tes in people with impaired glucose tolerance: Systematic review and meta-analysis. Br. Med. J.
- ↑ Astrup A, Rossner S, Van Gaal L, et al (2009) Effects of liraglutide in the treatment of obesity: a randomised, double-blind, placebo-controlled study. Lancet. https://doi.org/10.1016/S0140-6736(09)61375-1
- ↑ Astrup A, Carraro R, Finer N, et al (2012) Safety, tolerability and sustained weight loss over 2 years with the once-daily human GLP-1 analog, liraglutide. Int J Obes, https://doi.org/10.1038/ijo.2011.158
- ↑ Naslund I, Carlsson B, Bouchard C, et al (2012) Bariatric Surgery and Prevention of Type 2 Diabetes in Swedish Obese Sub- jects. N Engl J Med. https://doi.org/10.1056/nejmoa1112082
- ↑ Phillips LS, Ratner RE, Buse JB, Kahn SE (2014) We can change the natural history of type 2 diabetes. Diabetes Care
- ↑ Cusi K, Orsak B, Bril F, et al (2016) Long-term pioglitazone treatment for patients with nonalcoholic steatohepatitis and prediabetes or type 2 diabetes mellitus a randomized trial. Ann Intern Med. https://doi.org/10.7326/M15-l774
- ↑ Sawamoto R, Nozaki T, Furukawa T, et al (2016) Predictors of dropout by female obese patients treated with a group cogni- tive behavioral therapy to promote weight loss. Obes Facts, https://doi.org/! 0.1159/000442761
- ↑ Endevelt R, Peled R, Azrad A, et al (2015) Diabetes prevention program in a Mediterranean environment: Individual or group therapy? An effectiveness evaluation. Prim Care Diabetes. https://doi.Org/10.10l6/j.pcd.2014.07.005
המידע שבדף זה נכתב על ידי
- ד"ר גניה אהרון־חננאל - מומחית לרפואה פנימית, המכון האנדוקריני במרכז הרפואי על שם שיבא, תל השומר ו-DMC
- פרופסור איתמר רז, יושב ראש המועצה הלאומית לסוכרת
- ד"ר יוני שפירא, מומחה ברפואה פנימית ואנדוקרינולוגיה, המרכז הרפואי תל-אביב ומכבי שירותי בריאות


 כניסה
כניסה  עקבו אחרינו בפייסבוק
עקבו אחרינו בפייסבוק