גורם וון וילברנד - Von Willebrand factor
| מדריך בדיקות מעבדה | |
| גורם וון-וילברנד | |
|---|---|
| von Willebrand factor | |
| שמות אחרים | Ristocetin cofactor; vWF |
| |
| מעבדה | תפקודי קרישה בדם |
| תחום | בירור אפשרות של מחלת וון-וילברנד בתרחישי דמם קשים |
| טווח ערכים תקין | ערכי vWF משתנים בהתאם לקבוצת הדם: בסוג דם O ערכי vWF הם- 50-150 יח' לד"ל, בעוד שבקבוצות דם אחרות רמת VWE גבוהה יותר, 90-200 יח' לד"ל. בדרך כלל מדווחות התוצאות כאחוז של רמה צפויה של VWF בפלזמה תקינה: רמה תקינה-50-150%; בצורה מתונה של מחלת vW נמצא-20-40%; צורה חמורה יותר של המחלה-פחות מ-10%. |
| יוצר הערך | פרופ' בן-עמי סלע |
לערכים נוספים הקשורים לנושא זה, ראו את דף הפירושים – תפקודי קרישה
מטרת הבדיקה
מדידת vWF מסייעת לאבחנה מבדלת בין המופיליה לבין מחלת vW. כיוון שתסמיני מחלת vW יכולים להתבטא בדימומים תכופים מהאף, לאחר טיפולי שיניים, מחזורים חודשיים עם איבוד דם מסיבי, או תינוקות עם דימום לא שגרתי לאחר ברית מילה, תידרש מדידת vWF בתרחישים אלה. בדיקת vWF מתבצעת יחד עם מבחני מעבדה אחרים המיועדים לבחון את תפקודי הקרישה כמו מבחני זמן קרישה, PT ו-aPTT, רמת factor VIII המשפיעה באופן ישיר על רמת VWF, וכן פעילות קו-פקטור Ristocetin.
בסיס פיזיולוגי
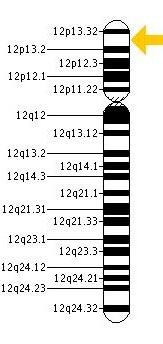
גורם vW הוא גליקופרוטאין המקודד על ידי גן הממוקם על הזרוע הקצרה של כרומוזום 12 (ראו תמונה), כאשר יחידת הבסיס (מונומר) היא של חלבון במשקל מולקולארי של 250,000 דלטון. כל מונומר כזה מורכב מ-2,050 חומצות אמינו. המולקולה השלמה מורכבת מ-80 עד 200 מונומרים הקשורים ביניהם בקשרים דיסולפידיים בין 2 שיירי ציסטאין, ויכולה להגיע בהתאם לגודל של עד 20 מיליון דלטון. רק מולקולות vWF המורכבות ממולטימרים גדולים פונקציונליות בנושא הקרישה. גורם וון-ויליברנד מיוצר ע"י גופיפי Weibel-Palade בתאי האנדותל וע"י מגה-קריוציטים (הקודמנים של טסיות הדם), וכן ברקמת החיבור התת-אנדותליאלית. ניסויים עדכניים מצביעים על כך שעיקר ה-vWF מגיע מתאי אנדותל, בעוד שיש ספק לגבי המשמעות הפיזיולוגית של vWF הגיע ממגה-קריוציטים.
לכל מונומר יש אתרי קישור של גורם קרישה VIII, וכן אתרי קישור לגליקופרוטאין GPIb של טסיות הדם, וכן אתרי קישור ל-GPIIb/IIIa, להפארין ולקולאגן, לפי הפרוט הבא: מקטע D’/D3 נקשר לפקטור VIII; מקטע A1 נקשר להפארין, לקולטן GPIb שעל פני הטסיות, וכנראה גם לקולאגן; מקטע A3 נקשר לקולאגן; מקטע C1 נקשר למולקולת אינטגרין αIIbβ3 בהיותה משופעלת; "קשר ציסטאין" בקצה ה-C טרמינאלי של vWF משותף ל-vWF ולגורמי הגדילה PDGF ו-TGFβ, כמו גם ל-βHCG.
התהליך הקטבולי של vWF מושפע על ידי האנזים ADAMTS-13 ממשפחת המטאלו-פרוטאזות, המבקע את vWF בין טירוזין בעמדה 842 לבין מתיונין בעמדה 843 הממוקמים ב-A2 domain. ביקוע זה מפרק את המולטימרים הגדולים ליחידות קטנות יותר, המתפרקות על ידי פעילות של פפטידאזות בדם. כיוון שהיחידות הגדולות הן הפעילות בצימות טסיות הדם, כישלון לבקע ולפרק יחידות גדולות אלו, יעודד כמובן תהליך פקקתי. אכן, המטופלים עם חסר באנזים ADAMTS-13 מוגברת הסכנה להופעת קרישי דם. הופעת TTP כרוכה לעתים בחסר מולד של ADAMTS-13 או בנוגדנים עצמיים כנד אנזים זה, מה שמדגיש את משמעות ביקוע vWF על ידי האנזים ADAMTS-13.
רקע היסטורי
המחלה נקראת ע"ש אריק וון-ויליברנד שהיה הראשון לזהות את המפגע. רופא פיני זה אבחן בשנת 1924 ילדה בת 5 מאיי Åland בין שוודיה לפינלנד ובדיעבד ב-66 מבני משפחתה ודווח ב-1926 על מחלת דמם שלא תוארה קודם לכן, מתאפיינת בנטייה לדמם עורי ומרקמות ריריות כמו מהאף והחניכיים, ובדימום ווסתיח מוגבר (menorrhagia), שהייתה שונה מהמופיליה קלאסית. בניגוד להמופיליה דימומים לתוך מפרקים (השכיחים מאוד בחולי המופיליה) נדירים יחסית בחולי וון-ויליברנד ומתרחשים רק בסוגי המחלה החמורים יותר (מחלה מסוג 3). הוא זיהה את ההורשה האוטוזומאלית של המפגע בבני משפחה זו בניגוד לתאחיזה בכרומוזום-X בהמופיליה, זיהה בהם זמן קרישה תקין (בניגוד לחולי המופיליה), לעומת זמן דימום ממושך מתנוך האוזן (שיטת Duke). וון וילברנד זיהה מייד שכיחות גדולה יותר של תסמיני הדימום בילדים ובנשים בגיל הפוריות, אבחן שהדימום בלט ברקמות חיפוי ריריות, וכן מצא שעירוי דם היה יעיל לא רק לתקן את האנמיה המתהווה אלא גם לשלוט על הדימום.
בשנות ה-50 התחוור שגורם הקרישה האנטי-המופילי (Factor VIII) החסר בדמם של חולי המופיליה חסר גם בדמם של חולי וון-וילברנד, ושניתן היה לתקן את זמן הדימום הממושך ואת החסר של פקטור VIII על ידי הוספת מקטע Cohn-I-0 של הפלזמה. עובדה זו והעובדה שבאותו הזמן הסיבה למחלה לא הייתה ידועה, גרמו לחוקרים לחשוד שמקור הבעיה הינו כלי הדם עצמם, לכן כונה המצב "המופיליה של כלי דם". מאוחר יותר נמצא שפלסמה מחולי המופיליה מסוגלת לשפר את מצבם של אנשים הסובלים ממחלת וון-ויליברנד אך ההיפך אינו נכון. מכאן היה ברור שמדובר בשתי בעיות שונות למרות שבשתיהן ניתן למצוא חסר דומה של מרכיב כלשהוא בדם. בשנות ה-70 נוקה vWF. הבעיה המדויקת נתגלתה מאוחר יותר כאשר זוהה הפקטור הבעייתי הגורם למחלה שזכה לשם ה"פקטור ע"ש וון-וילברנד". בשנות ה-80 נעשתה ההבחנה המולקולארית בין המופיליה A לבין מחלת vW, כאשר התברר שהגן לפקטור VIII על כרומוזום 10 תקין בחולי vW, כאשר הפגמים הם בגן ל-vWF על כרומוזום 12.
פעילותו הביולוגית של vWF
התפקיד העיקרי של vWF הוא הקישור לפקטור VIII, שהוא קו-פקטור לפקטור IXa, אשר בעזרת סידן ופוספוליפידים יוצר קומפלקס ההופך את פקטור X לצורתו האקטיבית – פקטור Xa. פקטור VIII הוא גליקופרוטאין המשוחרר לדם מתאי האנדותל. במחזור הדם, פקטור VIII ו-vWF הנקשר אליו יוצרים מבנה יציב, אך שפעול על ידי תרומבין גורמת לדיסוציאציה של הקומפלקס, כאשר פקטור VIII המשתחרר מתאחיזת vWF משמש קו-פקטור לפקטור IXa, כדי לשפעל את פקטור X. בכך תורם vWF להמוסטאזיס.
חשיבות הקישור של vWF לפקטור VIII היא בהגנה שהוא מקנה לגורם הקרישה אליו הוא נקשר שעובר בדם פירוק פרוטאוליטי מהיר כאשר אינו קשור ל-vWF. בנוסף, vWF נקשר לקולאגן כאשר זה נחשף בשכבת האנדותל כתוצאה מנזק שנגרם לכלי הדם. כמו כן, vWF נקשר ל-GPIb על פני טסיות כאשר זה יוצר קומפלקס עם GPIX ו-GPV. קשר זה נוצר בעיקר בתנאי עקת גזירה גבוהה (shear stress) האופיינית לכלי-דם קטנים.
טסיות הדם מאתחלות את תהליך קרישת הדם במסלול הרגיל, כאשר מופרש החלבון vWF בין האנדותל לדופן החיצוני של כלי הדם, שכבה מופרדת מזרם הדם התקין. פגיעה בכלי דם חושפת את ה-vWF לדם באופן המגייס נוגדנים, קולאגן וגורמי קרישה נוספים. טסיות הדם נצמדות לקולאגן, עוברות שפעול: באמצעות vWF הנקשר לקולטנים על פני הטסיות, יש שחרור של תוכן הטסיות וחומרים כגון ADP ו- סרוטונין, מה שמגביר את יכולת ההיצמדות של פיברינוגן באיזור הפגוע.
תפקיד vWF ביצירת הקריש
הקישור לטסיות דורש שפעול ראשוני של vWF כדי שיביא לשינוי מבני של החלבון באופן שמקטע A1 יוכל להיקשר לקומפלקס GPIb-IX-V על פני טסיות הדם. קישור זה מתרחש גם על טסיות בלתי משופעלות. השפעול של vWF על ידי התקשרותו למבנים הנחשפים לאחר נזק אנדותליאלי או תחת עקת גזירה גבוהה בעורקיקים קטנים או בעורקים טרשתיים. בנוסף, קישור של vWF ל-GPIb של הטסיות מייצר תת חלקיקים הנגזרים מהטסיות, המחישים עוד יותר את תהליכי יצירת הקריש הדם.
קולטן טסיות נוסף המשמש את vWF הוא GPIIb/IIIa, אך זה אינו קושר vWF אלא אם כן הטסיות משופעלות, כולל השפעול של הקומפלקס GPIb-IX-V. האינטראקציה של vWF עם הקולטן GPIIb/IIIa כמו גם למולקולות משופעלות שלintegrin , תורמת לספיחה הסופית והבלתי הפיכה של הטסיות לתת-אנדותל, ומשחקת תפקיד עיקרי בצימות של הטסיות, במיוחד תחת מצבי עקת גזירה גבוהים. בנוסף, vWF נקשר למספר סוגי קולאגן, ובעיקר לקולאגן type IV, ברקמת החיבור התת-אנדותליאלית. הקישור לקולאגן מביא לשינוי קונפורמציה באזור של פני vWF הקושר פקטור VIII, מה שמחליש את זיקת vWF לגורם קרישה זה. וכך פקטור VIII המשתחרר מתאחיזת vWF יכול לסייע באופן מקומי ליצירת קריש הפיברין, ולדבר יש חשיבות מיוחדת כאשר יש "פציעה" של כלי הדם וחשיפה של השכבות התת-אנדותליאליות כפי שקורה ב-ACS.
ללא vWF, תקופת מחצית החיים של פקטור VIII הייתה מתקצרת בדם פי-10 עד פי-20, כתוצאה מפעילות פרוטאוליטית שהייתה גורמת לאינאקטיבציה של פקטור VIII על ידי protein C והקו-פקטור שלו, protein S. כאמור, vWF יכול לקשור פקטור VIII רק לאחר שהאחרון עבר ביקוע על ידי תרומבין. החשיבות הקלינית של פקטור VIII ביצירת תרומבין, מודגמת יפה על ידי העובדה שחסר פקטור VIII גורם לתופעות הקליניות של המופיליה מסוג A. פקטור VIII נמצא בחסר במחלת vW, כאשר רמות נמוכות שלו מביאות לכשל ביצירת קריש פיברין.
שכיחות
המחלה ע"ש וון-וילברנד על סוגיה השונים נפוצה מאוד באוכלוסיה והיא למעשה מחלת הקרישה התורשתית הנפוצה ביותר באוכלוסיה. מחקרים שונים הצביעו על שכיחות של 1-1.5% חולים באוכלוסיות השונות. המחלה מופיעה באחוזים דומים בנשים ובגברים. למרות זאת שכיחות המקרים הדורשים טיפול משמעותי עקב דימום הינו נמוך יותר ומוערך במקרה בודד לכל 10.000 איש באוכלוסיה. המחלה שכיחה ומשמעותית יותר באלה עם סוג דם O.
תורשה
התורשה ברוב המקרים אוטוזומלית דומיננטית, באופן שמחלת vW תתבטא גם עם גן פגום אחד. בחלק מהמקרים עוברת מחלה זו בהורשה "אוטוזומלית רצסיבית", כאשר 2 גנים פגומים נדרשים להתבטאות המצב.
סוג 1: זהו הסוג הנפוץ ביותר ואחראי על 60-80% מכלל המקרים של מחלת VW. סוג זה מאופיין בירידה בכמות VWF בדם (10-45% מהכמות הנורמאלית) אם כי נשמרות פעילויותיו הביולוגיות. זמן הדימום מוארך. בדיקת תפקודי הקרישה יכולה להיות תקינה או להצביע על PTT מוארך. רמת factor VIII בדם יכולה להיות תקינה או מופחתת מעט. מדובר בהפרעת קרישה קלה יחסית, כאשר הדימומים לרוב אינם משמעותיים. ברוב המקרים המחלה אינה מאובחנת לאורך החיים, ועשויה להתגלות מדמם בעקבות ניתוחים, או טיפולי שיניים, או מתרחישי ווסת קיצונית. סוג זה עובר בהורשה אוטוזומלית-דומיננטית.
סוג 2: מהווה כ-20-30% מכלל מקרי מחלת vW ומתחלק ל-4 תת-סוגים (2A, 2B, 2M, 2N). מתאפיין בפגיעה שהיא גם כמותית אך גם בפגיעה בחלק מתפקודיו הביולוגים של הפקטור.
סוג 2A: בסוג זה קיימים המולטימרים הקטנים של vWF, וחסרים המולטימרים בגדלים הבינוניים והגדולים. כמות של הפקטור בדם קטנה ביחס לנורמה וקיימת פגיעה משמעותית בפעילותו הביולוגית. זמן הדימום ארוך באופן בינוני (ארוך יותר מאשר בסוג 1 אך פחות ארוך מאשר בסוג 3). תפקודי הקרישה יהיו תקינים או מעט מוארכים ורמת factor VIII יכולה להיות תקינה. הורשת הפגם אוטוזומלית דומיננטית. בסוג זה יש פעילות נמוכה במיוחד קו-פקטור ristocetin בהשוואה לאנטיגן vW.
סוג 2B: המוטציה בתת-סוג זה גורמת לתפקוד פעיל במיוחד של תת-היחידות הבסיסיות, המתבטא בזיקת-יתר של VWF לטסיות והוא נקשר אליהן ספונטאנית אף ללא סיבה מיוחדת או פגיעה בכלי-הדם. כך נצמדות טסיות ביניהן, וצברי הטסיות המתהווים יחד עם המולטימרים הגדולים של VWF מורחקים ממחזור הדם, באופן שיכול להתבטא בתרומבוציטופניה מתונה, אם כי רמת factor VIII מראה רק חסר קל או שהיא אפילו נורמאלית. בסוג זה יש נטייה לדמם. מעניין שתרחישים המעלים את רמת VWF בדם (כגון עקה, אירוע דלקתי חריף, הריון), מחמירים את הדמם כתוצאה מירידה נוספת ברמת הטסיות. רמת VWF נמוכה מהצפוי, וזמן הדימום מוארך בדומה לזה שמוצאים בסוג 1. מדידת תפקודי הקרישה (PTT) תהיה נורמאלית או מוארכת. במטופלים עם סוג 2B לא ניתן לטפל ב-Desmopressin במקרי דמם, שכן הוא יכול לגרום לצימות לא רצוי של טסיות. צורת התורשה היא אוטוזומלית דומיננטית.
סוג 2M: רמות vWF בסוג זה תקינות, כאשר הפגיעה היא איכותית הגורמת לו לחוסר יכולת להתקשר ולקשור טסיות. אין כל בעיה אחרת בפקטור והוא עדיין יכול לשמש כנשא לפקטור הקרישה VIII. חוסר היכולת לקשור טסיות מונע יצירת פקקת יעילה ולכן זמן הדימום יהיה מוארך בצורה בינונית אך תפקודי הקרישה יהיו תקינים לחלוטין. רמת factor VIII תקינה אך הפעילות הביולוגית של החלבון פגועה משמעותית, עם פעילות נמוכה של קופקטור Ristocetin. מצב זה דומה מאוד לזה של הסוג 2A אך ההבדל הוא בכך שבסוג 2M אין חסר במולטימרים הגדולים של vWF, ואף ניתן למצוא מולטימרים גדולים במיוחד.
סוג 2N (ידוע גם כ-Normandy): בצורה זו הפגיעה היא ביכולת הקשירה של vWF ל-factor VIII. ולמעשה מתקבלת כאן מצב זהה לזה של המופיליה אך לא עקב הפגם הגנטי הרגיל המוביל להמופיליה. יש לחשוד בסוג 2N כאשר הממצאים הקליניים מזכירים המופיליה A, אך ההורשה אוטוזומאלית רצסיבית ולא X-linked. כאשר פקטור VIII אינו קשור ל-vWF הוא מפונה במהירות מהדם ומתפרק ורמתו נמוכה מאוד ואינה מאפשרת קרישת דם תקינה ואמנם בסוג זה זמן הדימום תקין, אך תפקודי הקרישה לקויים. רמת פקטור VIII תהיה נמוכה מאוד בעוד רמת VWF נמוכה רק מעט, עם כל המולטימרים מופיעים בדם כרגיל. בדיקת פעילותו הביולוגית תימצא תקינה או נמוכה מעט מהצפוי.
סוג 3: הצורה החמורה ביותר של המחלה ונטייה לדימומים קשים כולל דימומים תוך-גולגולתיים. הוא נובע מקיומם של שני גנים פגועים בהורשה אוטוזומלית רצסיבית, ולכן יש צורך בשני הורים נשאים. הגנים יכולים להיות בעלי אותה הפגיעה (הומוזיגוטיות) או שני גנים הפגועים באופן שונה (compound heterozygous). בחולים אילו למעשה לא ניתן לזהות את הפקטור כלל בדם ולכן הם גם סובלים מחוסר משמעותי של פקטור הקרישה VIII. בחולים אילו ניתן לזהות דימומים למפרקים (hemarthroses) כמו שמוצאים במקרי המופיליה מתונים). שכיחות סוג זה הינה 1 לחצי מליון איש באוכלוסיה. בדיקה המעבדה ל-PTT תהיה מאוד מוארכת כמו גם הבדיקה לזמן דימום. לא ניתן למצוא בדם את vWF.
פסאודו-וון-וילברנד (או platelet type): זהו למעשה תרחיש המועבר בהורשה אוטוזומלית-דומיננטית המקביל לזה המופיע בסוג 2B של מחלת vW, שאינו נגרם עקב ליקוי ב-vWF אלא ממוטציות “gain of function" בקולטנים על פני הטסיות. באופן ספציפי המוטציה ממוקדת בשרשרת אלפא של הקולטן הגליקופרוטאיני GPIb. גליקופרוטאין זה מהווה חלק מהקומפלקס הגדול יותר GPIb/V/IX היוצר את הקולטן ל-vWF על פני טסיות. כתוצאה ממוטציות אלה יש עודף קשירה בין vWF לטסיות אך במקרה זה זיקת היתר מגיעה דווקא מצד הטסיות גם כש"אין סיבה לכך". מצב זה גורם לכך שטסיות הקשורות לפקטור מתפנות מהדם וניתן לראות ירידה ברמתן, וכן יש ירידה ניכרת של מולטימרים גדולים של vWF. בנוסף יש גם ירידה בפעילות קו-פקטור ristocetin.
מחלת וון-וילברנד נרכשת (acquired VWD): תרחיש הנגרם מפגיעה בייצור vWF או בהרחקתו מהדם באופן שניוני. לעיתים הירידה ברמת vWF מופיעה זמן ניכר טרם הופעת תסמיני המחלה עצמה ולכן במקרים אלה קיים קושי להבדיל בין מצב מולד לנרכש. מחלת vW נרכשת תוארה גם במקרים של Wilms tumor, תת-תריסיות או בדיספלזיות מזנכימליות. מחלת VW נרכשת מופיעה במטופלים עם נוגדנים עצמיים כנגד vWF, באופן שהקומפלקס הנוצר עם WF מורחק במהירות מהצירקולציה. סיבה נוספת למחלה נרכשת של VW היא תרומבוציטופניה , בה יש הפחתה של vWF בדם מעצם ספיחתו למספר הגדול של טסיות הדם. גם המטופלים עם היצרות (stenosis) של אבי העורקים, הגורמת לדימום בדרכי המעי (תסמונת Heyde).
DDAVP – או Desmopressin הוא נגזר סינתטי של ואזופרסין, שהרכבו 1-Desamino-8-D-arginine vasopressin. התכשיר המשווק כ- Desmopressin acetate או Stimate, פועל על ידי העלאת רמת vWF בדם על ידי שהוא משרה שחרור של vWF האגור בגופיפי Weibel-Palade בתאי האנדותל. בדרך כלל אלה המאובחנים עם מחלת vW אינם נזקקים לטיפול סדיר, למרות היותם בסכנה מתמדת לדימומים. תכשיר זה ניתן להינתן בעירוי ישיר לדם, או בשאיפה לאף, כאשר באיש בריא תוך 60 דקות נמדדת עליה של פי-3 ברמת פקטור VIII. יחד עם זאת, יעילות תכשיר זה מופגנת בטיפול בסוגים 1, 2A ו-2M, אך אינו יעיל בסוג 2N. גם נשים עם דימום ניכר בעת המחזור או עם משכי מחזור ארוכים מהמקובל, או אלו הנוטלות גלולות למניעת הריון, או אלה המיועדים לניתוח עשויים להיעזר בתכשיר זה.
משמעות vWF במצבים פתולוגיים
חסר מולד של vWF יביא לתופעות דימום אופייניות, בצורת דימום מהאף, מהחניכים, ווסת מרובת דם ודימום ממערכת העיכול. רוב המקרים של מחלת vW הם תורשתיים, אך מצבים אנומליים יכולים להיות נרכשים: לדוגמה, היצרות אבי העורקים יכולה להיות קשורה למחלת vW מסוג 2A, תוך גרימת דימום במערכת העיכול, האופייני לתסמונת Heyde. בפורפורה תרומבוטית טרומבוציטופנית (TTP) וכן ב-תסמונת המוליטית-אורמית (HUS), יש חסר של ADAMTS-13 או עיכוב שלו על ידי נוגדנים עצמיים, מה שמביא לשבירה מופחתת של המולטימרים הגדולים של vWF, ולמצב של Microangiopathic hemolytic anemia, עם משקעי פיברין וטסיות דם בכלי דם קטנים, ולנמק בקפילארות. רמות גבוהות יותר של vWF שכיחות יותר בין אנשים שחוו בפעם הראשונה שבץ מוחי כתוצאה מקרישיות-יתר.
קישור vWF לקומפלקס של שלושת הגליקופרוטאינים על פני טסיות מחיש את שפעול תאים אלה ואת הצימות שלהם עם מרכיבים אחרים כמו קולאגן באזור הפגוע והחשוף של כלי הדם. מצב זה מאיץ את יצירת קריש הדם ועצירת שטף הדם. כאשר vWF פעיל, הוא נמצא בצורתו הפרוסה או הבלתי מקופלת, באופן שחושף את האזורים על פני vWF הנקשרים אל הקולטנים המתאימים על פני הטסיות. יחד עם זאת, הצורה הפרוסה של חלבון זה, חושפת אתרי ביקוע לאנזים ADAMTS-13 המבקע את vWF למקטעים קצרים שמוגבלת יכולתם להיקשר לקולטני הטסיות.
יצירת vWF אנדותליאלי יכולה להתרחש על ידי מספר גירויים בגוף אך גם במערכות in-vitro, כגון היפוקסיה, ציטוקינים דלקתיים, תרומבין, האנזים Elastase המופרש מלויקוציטים, פעילות גופנית נמרצת, אנדו-טוקסינים של חיידקים, אדרנלין, חסימה בהפרשת NO, ובעיקר מעולת ההורמון Vasopressin. אכן, אלה עם מחלת vW מטופלים ביעילות עם Desmopressin האנלוג המבני של Vasopressin, כדי להעלות את רמת vWF. התת-אנדותל התקין מכיל כמויות משתנות של vWF, בהתאם למיקומו האנטומי.
גורמים המשפיעים על רמת פקטור ע"ש וון-ויליברנד
רמתו של vWF בדם ומשתנה בתנאים מסוימים, שכן הוא נחשב אחד מ"חלבוני העקה" (acute phase). רמת vWF עולה בדם בזמן הריון פי 2-3 מהערכים התקינים. סיבות נוספות המעלות רמת vWF בדם הן מחלת כבד קשה או יתר פעילות של בלוטת התריס. מסיבות אילו תיתכן לעיתים החמצה של דימום חריג בזמן הריונות לידות וניתוחים דחופים, בהם רמת vWF גבוהה כחלבון "עקה", וניתן יהיה לאבחן מחלת חסר vWF במצבי דימום המתרחשים בעת "רגיעה". כפי שצויין רמת vWF נמוכה יחסית באנשים בעלי סוג דם O, ולעומת זאת באלה עם סוג דם AB נמצא רמת vWF הגבוהה ביותר, בממוצע. במקרים של תוצאת vWF גבולית עם רמה גבוהה משמעותית של CRP תיתכן מחלת vW.
אבחון מחלת vW וממצאי המעבדה
בחשד למפגע הקשור ל-vWF הפלזמה תיבדק באופן איכותי וכמותי לאפשרות של חסר בגורם זה. ניתן למדוד רמת vWF הן באופן ישיר, ואת תפקודו של vWF ניתן להעריך במבחן הקישור ל-GPIb, במבחן הקישור לקולאגן, או במבחן RIPA או ristocetin induced platelet agglutination או ב- RiCof אוcofactor ristocetin activity. גם רמת פקטור VIII נמדדות, אם כי תוצאה תקינה של רמת פקטור VIII אינה מחלת vW, בעיקר מסוג 2, כאשר האחרונה יכולה להתגלות רק על ידי מדידת האינטראקציה של טסיות עם שכבת התת-אנדותל תחת זרימת דם (PAF), בדיקה מורכבת שאינה מתבצעת בשגרת רוב המעבדות הקליניות. מבחן צימות טסיות יכול להראות תגובה בלתי נורמאלית ל-Ristocetin, לעומת תגובה תקינה לאגוניסטים אחרים שנבדקו. סוג 2N יכול להיות מאובחן רק על ידי ביצוע מבדק של "קשירת פקטור VIII". ממצאי המעבדה של מחלת vW: זמן פרותרומבין נורמאלי; זמן טרומבופלסטין חלקי (aPTT) מוארך; זמן דימום מוארך; ספירת טסיות דם בלתי מושפעת.
הוראות לביצוע הבדיקה
יש ליטול דם במבחנת ציטראט (פקק תכול), ולאחר סרכוז יש להעביר למבחנת פלסטיק, ואם הבדיקה לא נעשית מיד, יש להקפיא את הפלזמה. אין לקבל פלזמה המוליטית, פלזמה קרושה חלקית, או דגימה שהתקבלה במעבדה מעל 4 שעות מנטילת הדם.
ראו גם
המידע שבדף זה נכתב על ידי פרופ' בן-עמי סלע, המכון לכימיה פתולוגית, מרכז רפואי שיבא, תל-שומר;
החוג לגנטיקה מולקולארית וביוכימיה, פקולטה לרפואה, אוניברסיטת תל-אביב (יוצר הערך)


 כניסה
כניסה  עקבו אחרינו בפייסבוק
עקבו אחרינו בפייסבוק