גמילה מעישון, תרופות בסל 2018 ויעילות הטיפול בליווי רופא המשפחה - Smoking cessation, the family doctors’ beneficial role
לערכים נוספים הקשורים לנושא זה, ראו את דף הפירושים – עישון
כ־19 אחוזים ממקרי התמותה בישראל כל שנה נגרמים כתוצאה ישירה מנזקי עישון (עישון ישיר וכפוי יחד) - כ־8,000 מקרי מוות כל שנה[1]. גם בעולם, עישון הוא גורם הסיכון המשמעותי ביותר לתחלואה ולתמותה, עם כ־7 מיליון מקרי תמותה כל שנה כתוצאה ישירה מגורם זה[2]. מעשן מאבד בממוצע בין 10–12 שנים מתוחלת החיים שלו כתוצאה ישירה מהעישון[3], וכ־50–66 אחוזים מהמעשנים ימותו בטרם עת עקב העישון[4][5], הפעולה הרפואית היעילה ביותר שניתן להציע עבור אדם מעשן, זו שתשפר את איכות חייו ותאריך אותם, היא גמילה מעישון.
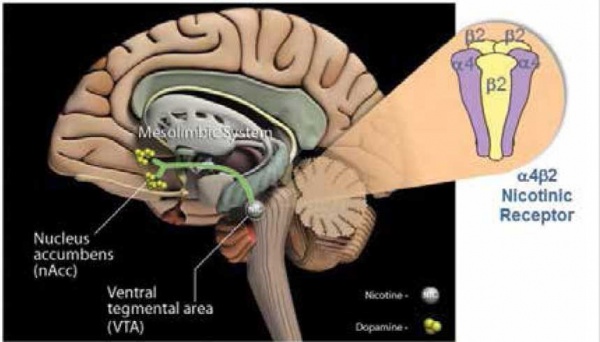
פעמים רבות נהוג להתייחס לעישון בנשימה אחת יחד עם גורמי סיכון אחרים הנובעים מאורח חיים כגון השמנה, חוסר פעילות גופנית, יושבנות, מתח נפשי ועוד. אכן, שינוי באורח החיים הכולל אחד מגורמי הסיכון שלעיל, כולל עישון, דורש שינוי התנהגותי, שינוי הרגלים ותהליך למידה של הרגלים חדשים. עם זאת, בשונה משאר גורמי סיכון אלה, לעישון יש מרכיב חזק מאוד של התמכרות גופנית (תמונה מספר 1).
ניקוטין, החומר העיקרי הגורם להתמכרות, נספג ביעילות רבה ומגיע למוח בתוך כעשר שניות מלקיחת השאיפה. מהירות ההגעה של ניקוטין למוח היא אחד מהמרכיבים העיקריים הגורמים להתמכרות לניקוטין. עם הגעת הניקוטין למוח, הוא נקשר לקולטן (Receptor) ספציפי במערכת ה-Mesolimbic (מזו-לימבית) ומוביל להפרשת דופמין. שחרור הדופמין במערכת המזו־לימבית הוא שגורם לתחושת הרוגע והסיפוק מהסיגריה אצל המעשן[6]. כאשר רמות הניקוטין (ואיתן רמות הדופמין) יורדות, מתחילה תסמונת גמילה גופנית שיכולה לכלול עצבנות, חוסר ריכוז, השתוקקות לסיגריה, רעד בידיים, עלייה בתיאבון, נדודי שינה ועוד[6].
הטיפול במעשן מחייב טיפול משולב גם בהתמכרות הגופנית וגם בהתמכרות ההתנהגותית.
סקירת Cochrane שכללה 52 מחקרים ויותר מ־19,000 משתתפים, מראה כי טיפול משולב הכולל ליווי התנהגותי וטיפול תרופתי הוא הטיפול היעיל ביותר לגמילה מעישון, המעלה את הסיכוי להיגמל פי 1.83 בהשוואה לטיפול רגיל (RR (Relative Risk) 1.83, CI (Confidence Interval) 95% 1.98-1.68)[7].
החל משנת 2010, זכאי כל אזרח בישראל, כחלק מסל השירותים הרפואיים, לטיפול משולב זה - ליווי התנהגותי חינם (הניתן באמצעות סדנה קבוצתית בקופות החולים השונות) בשילוב עם טיפול תרופתי מסובסד[8]. הליווי ההתנהגותי הניתן הוא אינטנסיבי וכולל שמונה מפגשים קבוצתיים של כשעה וחצי־שעתיים למפגש. בשנת 2016, 26,944 מעשנים השתתפו בסדנאות לגמילה מעישון בארבע קופות החולים יחד, המהווים כ־2.2 אחוזים מסך המעשנים בישראל[8]. שיעור זה נותר ללא שינוי כאשר המשמעות היא שמרבית המעשנים בישראל אינם נעזרים בשיטה זו, למרות יעילותה הגבוהה ביותר.
בנוסף לכך, מחקרים הוכיחו כי מרבית המעשנים לשעבר נגמלו לבד, ללא כל עזרה התנהגותית או תרופתית. שיעור ההצלחה של גמילה עצמית הוא הנמוך ביותר (כ־5 אחוזים) אך עדיין מהווה את צורת הגמילה המועדפת ביותר על המעשנים[9][10][11], יתרה מכך, כ־50 אחוזים מניסיונות הגמילה הם ספונטניים (ללא תכנון מראש) ושיעור ההצלחה של ניסיונות אלה אינו נופל משיעור ההצלחה של הניסיונות המתוכננים[12].
בניגוד לשאר העולם, שיעורי העישון בישראל לא השכילו לרדת ואף נצפתה מגמת עלייה קלה כאשר 22.5 אחוזים מבני 18 ומעלה מעשנים בישראל[8].
כחלק מתוכנית כוללנית להורדת שיעורי העישון בישראל (שנדרשת לכלול גם העלאת מיסים, הגבלות על פרסום ושיווק, הגבלות על מכירה והגבלות על מקומות מותרים לעישון), נדרש גם לפעול להגברת ההשתתפות בתוכניות גמילה מעישון. ברמת האוכלוסייה בישראל, על מנת להעלות את שיעורי הגמילה מעישון, לא מספיק להסתכל רק על יעילות השיטה המוצעת, אלא נדרש להתייחס גם לשיעור השימוש בפועל: Efficacy = Effectiveness X Reach; תועלת = יעילות X שימוש בפועל. לכן אף על פי שבישראל מוצעת השיטה היעילה ביותר לגמילה מעישון, השימוש בפועל בשיטה זו אינו נרחב והפוטנציאל להרחבת שיעורי הגמילה עדיין גבוה.
מרבית המחקרים שבדקו את יעילות הטיפול התרופתי לגמילה מעישון שילבו את הטיפול התרופתי עם קבלת ליווי התנהגותי קצר מועד על ידי רופא המשפחה או איש צוות רפואי אחר. בסקירת Cochrane האחרונה שפורסמה על יעילות הטיפול התרופתי Varenicline בגמילה מעישון נכללו 39 מחקרים מבוקרים רנדומליים כפולי סמיות. מתוך אלה, ב־25 מהמחקרים המטופלים קיבלו ייעוץ שהוגדר כייעוץ קצר מועד בלבד, פחות מעשר דקות, על ידי רופא המשפחה או איש צוות אחר במספר מועט של מפגשים שנפרסו לכל אורך הטיפול התרופתי. מצב זה מדמה טיפול שגרתי במעקב וליווי של רופא המשפחה במרפאה בקהילה, ולא את הייעוץ האינטנסיבי הניתן כעת בישראל במסגרת קבוצתית. סקירה זו מצאה כי הטיפול התרופתי ב-Varenicline מעלה את סיכוי הגמילה פי 2.24 בהשוואה לאינבו (27 מחקרים, 12,625 משתתפים, (RR 2.24 2.06–2.43 95% CI)[13]. סקירות Cochrane נפרדות על יעילות של תחליפי ניקוטין[14] ו-Bupropion[15] מצאו אף הן כי תרופות אלו יעילות ללא תלות בליווי התנהגותי.
הוכח כי המלצה מרופא על גמילה מעישון, מעלה פי 1.66 את הסיכוי שמעשן יבצע ניסיון גמילה מעישון (RR 1.66, 1.42–1.94 95% CI)[16]. בנוסף לכך, כפי שתואר לעיל, לטיפול התרופתי יש יעילות גבוהה יותר מאינבו, גם כאשר הוא ניתן בליווי קצר מועד של רופא המשפחה בלבד (פחות מעשר דקות למפגש, מספר מפגשים מועט)[13].
במצב הקיים בישראל, על מנת ליהנות מהטיפול התרופתי בסבסוד, מטופל נדרש להירשם ולחכות לפתיחת סדנה קבוצתית. מצב זה מפלה לרעה אוכלוסיות בפריפריה, עולים חדשים ואוכלוסיות שאין להן מענה ספיצפי כגון נשים בהיריון ומטופלים המתמודדים עם מחלות נפש. כיוון שסדנה קבוצתית נפתחת רק כאשר מספר מינימלי של אנשים נרשם אליה, מטבע הדברים קשה יותר לפתוח סדנה באזורים מרוחקים ו/או בשפה אחרת. מכאן, שהמצב הקיים תורם, שלא במתכוון, להגדלת הפערים החברתיים ואינו נותן מענה טוב מספיק דווקא לאוכלוסיות החלשות הזקוקות לכך.
ישראל היא אחת המדינות הבודדות בעולם המתנות בפועל את קבלת התרופה בסבסוד בהשתתפות חובה בליווי התנהגותי. פתיחת האפשרות למטופלים לקבלת ליווי התנהגותי קצר על ידי רופא המשפחה, בשילוב הטיפול התרופתי, תאפשר הנגשה של הטיפול לגמילה מעישון לשיעור גבוה יותר של מטופלים, ובפועל עשויה להוביל לעלייה בשיעורי הגמילה בישראל.
ביבליוגרפיה
- ↑ Ginsberg, G.M.; Geva, H. The burden of smoking in israel-attributable mortality and costs (2014). Isr J Health Policy Res 2014, 3, 28.
- ↑ Abajobir, A.A.; Abate, K.H.; Abbafati, C.; Abbas, K.M.; Abd-Allah, F.; Abdulle, A.M.; Abera, S.F.; Aboyans, V.; Abu-Raddad, L.J.; Abu-Rmeileh, N.M.E., et al. Global, regional, and national comparative risk assessment of 84 behavioural, environmental and occupational, and metabolic risks or clusters of risks, 1990–2016: A systematic analysis for the global burden of disease study 2016. The Lancet 390, 1345-1422.
- ↑ Jha, P.; Ramasundarahettige, C.; Landsman, V.; Rostron, B.; Thun, M.; Anderson, R.N.; McAfee, T.; Peto, R. 21st- century hazards of smoking and benefits of cessation in the united states. N Engl J Med 2013, 368, 341-350.
- ↑ Banks, E.; Joshy, G.; Weber, M.F.; Liu, B.; Grenfell, R.; Egger, S.; Paige, E.; Lopez, A.D.; Sitas, F.; Beral, V. Tobacco smoking and all-cause mortality in a large australian cohort study: Findings from a mature epidemic with current low smoking prevalence. BMC Medicine 2015, 13, 1-10.
- ↑ Gellert, C.; Schottker, B.; Brenner, H. Smoking and all-cause mortality in older people: Systematic review and meta-analysis. Arch Intern Med 2012, 172, 837-844.
- ↑ 6.0 6.1 Benowitz, N.L. Nicotine addiction. N Engl J Med 2010, 362, 2295-2303.
- ↑ Stead, L.F.; Koilpillai, P.; Fanshawe, T.R.; Lancaster, T. Combined pharmacotherapy and behavioural interventions for smoking cessation. Cochrane Database of Systematic Reviews 2016.
- ↑ 8.0 8.1 8.2 דוח שר הבריאות על העישון בישראל 2016, המחלקה לחינוך וקידום בריאות, משרד הבריאות, מאי 2017
- ↑ Fiore MC (Chair, G.P. Treating tobacco use and dependence: 2008 update. Services., U.S.D.o.H.a.H.; Service, P.H., Eds. 2008.
- ↑ Zhu, S.; Melcer, T.; Sun, J.; Rosbrook, B.; Pierce, J.P. Smoking cessation with and without assistance: A population-based analysis. Am J Prev Med 2000, 18, 305-311.
- ↑ Cokkinides, V.E.; Ward, E.; Jemal, A.; Thun, M.J. Under-use of smoking-cessation treatments: Results from the national health interview survey, 2000. Am J Prev Med 2005, 28, 119-122.
- ↑ Larabie, L.C. To what extent do smokers plan quit attempts? Tob Control 2005, 14, 425-428.
- ↑ 13.0 13.1 Cahill, K.; Lindson-Hawley, N.; Thomas, K.H.; Fanshawe, T.R.; Lancaster, T. Nicotine receptor partial agonists for smoking cessation. Cochrane Database Syst Rev 2016, Cd006103.
- ↑ Stead, L.F.; Perera, R.; Bullen, C.; Mant, D.; Hartmann- Boyce, J.; Cahill, K.; Lancaster, T. Nicotine replacement therapy for smoking cessation. Cochrane Database Syst Rev 2012, 11, CD000146.
- ↑ Hughes, J.R.; Stead, L.F.; Hartmann-Boyce, J.; Cahill, K.; Lancaster, T. Antidepressants for smoking cessation. Cochrane Database Syst Rev 2014, CD000031.
- ↑ Stead, L.F.; Buitrago, D.; Preciado, N.; Sanchez, G.; Hartmann-Boyce, J.; Lancaster, T. Physician advice for smoking cessation. Cochrane Database Syst Rev 2013, CD000165.
המידע שבדף זה נכתב על ידי ד"ר יעל בר זאב, מנהלת המרכז למניעה ולגמילה מעישון, החטיבה לבריאות בקהילה, הפקולטה למדעי הבריאות, אוניברסיטת בן-גוריון בנגב, יו"ר החברה הרפואית למניעה ולגמילה מעישון בישראל.


 כניסה
כניסה  עקבו אחרינו בפייסבוק
עקבו אחרינו בפייסבוק