גנטיקה בסרטן השד - היבטים כירורגיים - Genetics of breast cancer - surgical aspects
עקרונות בכירורגיה
מאת ד"ר צבי קויפמן
| עקרונות בכירורגיה | ||
|---|---|---|
| ||
| שם המחבר | ד"ר צבי קויפמן | |
| שם הפרק | כירורגיה של השד | |
לערכים נוספים הקשורים לנושא זה, ראו את דפי הפירושים: – נטיה גנטית לסרטן השד והשחלות, סרטן השד
מבחינה אטיולוגית ניתן לסווג את סרטן השד לקבוצות הבאות:
- סרטן שד ספורדי (Sporadic) - כאשר לחולה אין סיפור משפחתי כלשהו בשני הדורות האחרונים, הן מצד האם והן מצד האב.
- סרטן שד משפחתי (Familial) - כאשר לחולה יש קרוב/ת משפחה מדרגה ראשונה או שנייה הלוקה בסרטן השד.
- סרטן שד תורשתי (Hereditary) - באם מתקיים אחד מהמקרים הבאים:
- כאשר לחולה יש קרובים נוספים מדרגה ראשונה או שנייה (לפחות 4), הלוקים בסרטן השד או בסרטן במקום אחר בגוף.
- כאשר לחולה יש קרובי משפחה מדרגה ראשונה או שנייה המופיעים בגיל צעיר (45) עם ריבוי של שאתות בשני השדיים.
- כאשר לחולה יש קרובי משפחה מדרגה ראשונה או שנייה, בעלי תבנית המתאימה לתורשה אוטוזומלית דומיננטית.
- נשאות גנטית של אחת המוטציות המוכרות.
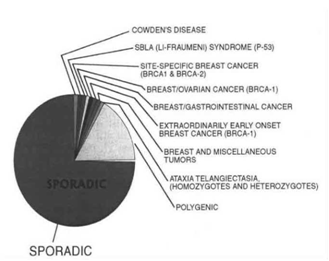
השיעורים של כל אחד מהמרכיבים הללו בתחלואה בסרטן השד מתוארת בתרשים 8.12 המונה גם את המחלות הגנטיות שבהם יש שכיחות יתר של סרטן שד.
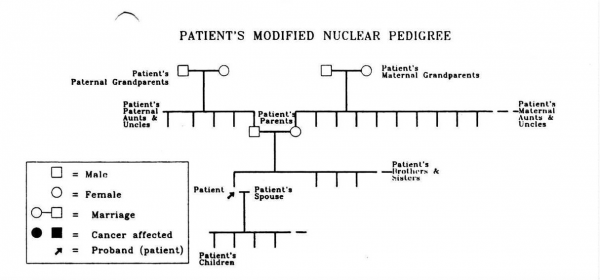
הבסיס לקביעת סרטן השד התורשתי היה בעבר העץ המשפחתי של קרובי משפחה מדרגה ראשונה ושנייה (תרשים 7.12).
אם נמצאו מספר קרובי משפחה שלקו במחלה, סרטן השד של החולה היה מוגדר כסרטן שד תורשתי. בסקר שנערך ב-76 בתי חולים בארה"ב נמצא שרק 4 ניהלו רישום טוב של העץ המשפחתי. כיום סרטן השד התורשתי מוסבר על-ידי גנים שהורשתם היא אוטוזומלית שולטנית (דומיננטית) ונבדלים ביניהם בשכיחותם ובחדירותם.
הגנים
10% עד 15% מקרב חולות סרטן השד הן בעלות רקע תורשתי. הסיכון לחלות בסרטן שד גדול פי 2.5 כאשר במשפחה אם או אחות חולה, וגדול פי 1.5, כאשר במשפחה סבתא או דודה חולה. הסיכון גבוה פי 14 בנשים שאימן ואחותן חולות בסרטן השד. מספר מחלות גנטיות קשורות להופעת יתר של סרטן השד (גרף 8.12).
לאחרונה התגלו שני הגנים העיקריים המעורבים בהתהוות סרטן השד. גנים אלה נקראים BRCA1 ו-BRCA2 . מניחים שפגמים ב-BRCA1 אחראים לכ-45% ממקרי סרטן השד התורשתי. במשפחות שבהן יש חולות בסרטן שד ושחלות עולה אחוז הנשאות לכ-90%. שיעור הסיכון של נשים בעלות פגם גנטי לחלות במחלה הוא כ-25% עד גיל 40, כ-40% עד גיל 50, וכ-57% עד 70% עד גיל 70. שיעור הסיכון ללקות במחלה של נשים ללא פגם גנטי הוא 1.5% עד גיל 50, ו-5% עד גיל 70.
איתור הגן BRCA1
במהלך 30 השנים האחרונות התמקד המחקר בחיפוש אחר גנים הגורמים לסרטן השד בתוך משפחות מרובות חולים הלוקים בסרטן השד. בדיקה של מאות סמנים גנטיים הצביעה על אזור פוטנציאלי בזרוע הארוכה של כרומוזום 17. באוקטובר 1990 מופה הגן, ונמצא קשר בין הגן המועמד שנקרא BRCA1 לבין סמן גנטי (D17S74) העובר בתורשה בחולות סרטן השד והשחלה. בתוך האזור שנסרק היו כ-1,000 גנים מועמדים, שמתוכם היה צריך לבודד את הגן הגורם לסרטן השד. חוקרים בעולם התאגדו לעבודה משותפת לשיבוט הגן. האסטרטגיה היתה אחידה. נעשה שימוש באנליזות של תאחיזה כדי לצמצם את האזור על פני הזרוע הארוכה של כרומוזום 17. בעבודה התמקדו בבדיקת התורשה של סמנים גנטיים במשפחות מרובות חולים הלוקים בסרטן השד. ככל שהמחקר התקדם, הצטמצם יותר ויותר האזור, וגנים מועמדים נסרקו כדי למצוא פגמים חוזרים ונשנים במשפחות של חולים. מציאת קשר בין פגמים בגן לבין המחלה חיזקה באופן ברור את מעורבותו של BRCA1 בהתהוות סרטן השד. על מנת לחזק את הממצא לפיו BRCA1 מעורב בהתהוות המחלה, נסרקו 214 משפחות של חולות סרטן השד, ו-57 משפחות של חולות הלוקות בסרטן שד או שחלות. נמצאה תאחיזה לסמני הגן ב-45% מהמשפחות עם סרטן השד, וב-90% מהמשפחות של חולות בסרטן השד ובסרטן השחלה. באוקטובר 1994 שובט הגן BRCA1. ה-BRCA1 הוא גן גדול, בעל 22 אקסונים מקודדים המייצר חלבון בעל 1863 חומצות אמיניות.
עד כה נמצאו כ-100 מוטציות. 22 מוטציות מוקמו באקסון מספר 11 , ממצא המוסבר בעובדה, שכ-60% מ-BRCA1 מקודדים באקסון זה. ב-BRCA1 אופיינו 3 מוטציות שכיחות: פגם 5382ins C בקודון 1756, אקסון מספר 20; פגם 185del AG בקודון 23, אקסון מספר 2; ופגם 4184del T בקודון 1355, אקסון מספר 11. שכיחות גבוהה של פגמים אלה מעידה על קיומם מזה זמן רב.
פגם חסר של אדנוזין גואנין בעמדה 185 (185delAG)
לאחרונה, התגלה ש-185delAG הוא פגם שכיח בקרב יהודיות אשכנזיות החולות בסרטן השד. במטרה לאפיין את הפגמים ב-BRCA1 הגורמים לסרטן שד בגיל צעיר, השוו בין חולות יהודיות אשכנזיות לבין חולות שאינן יהודיות. הממצאים הראו ש-21% מהנשים היהודיות האשכנזיות בעלות המוטציה חלו בסרטן השד עד גיל 40. הסיכון לחלות בסרטן השד בגיל צעיר גבוה פי 27 בנשים הנושאות את המוטציה, מאשר בקרב נשים שאינן נושאות פגם זה. בסקר של 858 יהודים אשכנזים בריאים (נשים וגברים) נמצא כי 0.9% מהם נשאו את המוטציה. ובסקר נוסף של 3000 יהודים אשכנזים בריאים נמצא כי 1.09% מהם נשאו את המוטציה.
פגם הוספה של ציטוזין בעמדה 5382 (5382insC)
פגם זה הוא הפגם הגנטי השכיח ביותר בנשים החולות בסרטן השד באוכלוסייה הלא יהודית. הוא קיים בשיעור גבוה יחסית גם בקרב חולות יהודיות אשכנזיות. במדגם שכלל 3000 דגימות של אשכנזים בריאים נמצא כי 0.13% נשאו את המוטציה. פגם זה ראוי לציון, כיוון שנשים הנושאות את המוטציות לקו בסרטן שד דו-צדדי, והשאת השנייה אובחנה במהלך חמש השנים הראשונות לאחר אבחון השאת הראשונה. קיים סיכון גבוה יותר לחלות גם בסרטן השחלה.
גנוטיפ ופנוטיפ
עדיין לא נמצא קשר ברור בין פגמים מסוימים ב- BRCA1 לבין הביטוי הקליני. מניחים שמוטציות באזור 5 מגבירות את הסיכון להתהוות סרטן השחלה.
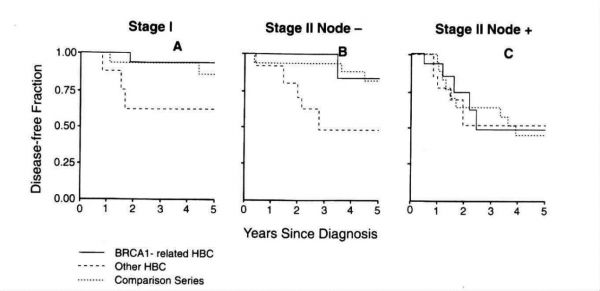
נמצא שההישרדות של נשים החולות בסרטן השחלה ובעלות מוטציה ב- BRCA1 שונה או אף גבוהה יותר מזו של נשים ללא פגם גנטי מוכח (גרף 12.4).
BRCA2
ה-BRCA2 הוא גן נוסף אשר תואר במשפחות שבהן האילן המשפחתי הצביע על קשר תורשתי ברור והן היו שליליות ל-BRCA1. הגן תואר ב-1995 כגן גדול המכיל 11,385 בסיסים ו-26 אקסונים מקודדים. עד כה אובחנו כ-20 מוטציות, רובן בעלות חלבון קצר עקב חסר של 6-1 בסיסים. 90%-80% מהנושאים מוטציות ב-BRCA2 ילקו במחלה עד גיל 80. כיום, ידועות שתי מוטציות ב-BRCA2 הקשורות במוצא אתני. המוטציה האיסלנדית באקסון 9, אותה נושאים מחצית הגברים מאיסלנד שאובחנו כחולים בסרטן השד, והמוטציה היהודית אשכנזית 6174delT. במדגם שכלל 3085 דגימות מיהודים אשכנזים בריאים נמצאו 1.52% של נשאי מוטציה זו.
כ-90% ממקרי סרטן השד התורשתי הם תוצאה של מוטציות ב-BRCA1 וב-BRCA2. כ-30% ממקרי סרטן השד בגיל צעיר בנשים יהודיות אשכנזיות הם תוצאה של שתי מוטציות: ה-del AG185 ב- BRCA1 וה-del T6174 ב- BRCA2. ה- delAG185 היא המוטציה השכיחה ביותר בקרב נשים חולות ממוצא אשכנזי יהודי, למרות שה-6l74delT שכיחה כמעט פי שניים בכלל האוכלוסייה האשכנזית, לפיכך 6174delT כנראה פחות חודרנית. BRCA1 דומה במבנה ל-BRCA2. שניהם גנים גדולים, בשניהם אקסון 11 גדול, והם עשירים בתבניות AT. שניהם משפיעים על התהוות סרטן בגיל צעיר. במשפחות של נשאי מוטציות ב-BRCA2 וב- BRCA1 יש דפוסי תחלואה שונים וידועות הנטיות הבאות: ה-BRCA1 קשור כנראה להתהוות סרטן השד וסרטן השחלה והסיכון של גברים נשאים לחלות בסרטן הערמונית והכרכשת גבוה פי ארבעה מזה של האוכלוסייה הבריאה. ה-BRCA2 מעורב בהתהוות סרטן השד גם בגברים, בסרטן המעי ובסרטן הלבלב, אך פחות מעורב בהתהוות סרטן השחלות. כמו-כן קיימים גנים אחרים, שפגמים בהם מעורבים בהתהוות סרטן השד, כמו p53, הגן לאטקסיה טלנגיאקטזיה (Ataxia talangiectasia) BRCA3 והקולטן לאנדרוגנים בסרטן השד בגברים.
נשאיות של גנים אלה ייפתחו גם שאתות באיברים אחרים. סרטן המעי הגס שכיח פי 6 בחולות אלה. שכיחות סרטן הערמונית (פרוסטטה) אצל גברים נשאים גבוהה פי שמונה מזו שקיימת בגברים לא נשאים. התמותה מסרטן המעי הגס בקרב נשאים גבוהה פי 1.5 מזו של האוכלוסייה הכללית וגבוהה פי 1.4 מהתמותה של החולים בסרטן הקיבה.
יעוץ גנטי
על מנת לגלות את הנשאיות של גנים אלו יש לבצע סיקור אוכלוסייה. נשאלת השאלה מי היא אוכלוסיית היעד. בהתאם להמלצה של ה-CGSC (Cancer genetic studies consulation) יש לסקור רק את אוכלוסיית החולות עם סיפור המתאים לסרטן שד משפחתי, נשים שבמשפחתן יש נשאיות של הגנים ונשים הלוקות בסרטן השד או בסרטן השחלה שחלו בגיל צעיר.
מה ניתן להמליץ לנשים שהן נשאיות של הגנים לסרטן השד? ההמלצות של ה- CGSC וה-NCI הן: אחרי גיל 25 שנה יש לבצע בדיקה קלינית כל חצי שנה עד שנה. בגילאי 35-25 שנה יש לבצע ממוגרפיה מדי שנה. יש לבצע את הממוגרפיה במקום קבוע ולהשוות צילומים. על הנבדקות לדעת שכיום אין מידע המוכיח שהממוגרפיה אכן יעילה בגיל זה, וכי הקרנת השד בגיל זה מגבירה את הסיכון ללקות במחלה.
בנוסף, מכיוון שקיים סיכון יתר ללקות בסוגי סרטן אחרים, יש להתייחס גם אליהם. יש להפנות את הנשים בגילאי 35-25 שנה לבדיקת על-שמע נרתיקית (Transvaginal ultrasound) מדי שנה. יש לזכור כי ב-3% מהנשים ניתן יהיה למצוא ממצאים בשחלות, כאשר 90% מהם ממצאים שפירים. אפשר להוסיף גם בדיקת 125-CA המעלה את סגוליות בדיקת האולטרה-סאונד. בדיקת דם סמוי בצואה בשילוב עם סיגמואידיסקופיה מקטינים את התמותה מסרטן הכרכשת. יש להמליץ על ביצוע בדיקה של דם סמוי פעם בשנה ושל סיגמואידוסקופיה פעם ב-5-3 שנים.
יש להעביר אינפורמציה לנשים ביחס לכירורגיה מונעת. כריתת שד דו-צדדית היא אחת הדרכים למנוע סרטן שד בנשאיות. את הכריתה יש לבצע בגיל מוקדם, 40-35 שנה. יש לזכור שכריתת שד ושחזור אינם מורידים לחלוטין את הסיכון לסרטן שד אלא מקטינים אותו. כיום אין שום מידע מדעי היכול להוכיח שאכן פעולה כזו מאריכה חיים בהשוואה לחולות שעברו כריתה כאשר המחלה רק נתגלתה. כריתה מונעת של שחלות יש לבצע במקביל עד גיל 35. יש להסביר לחולות שאין מדובר במניעה מוחלטת של המחלה, ודווח כבר בעבר על חולות בעלות פיזור גרורתי צפקי לאחר כריתה מונעת של השחלות. לא הוכח ששינויים בהרגלי החיים כמו תזונה וכו' משנים את מהלך המחלה. קרוב לוודאי, שבעתיד, מתן Tamoxifen במסגרת מניעה תרופתית (Chemoprevention) יוכל לסייע בהקטנת התחלואה בקבוצות בעלות סיכון גבוה ללקות בסרטן השד.
ראו גם
- לנושא הקודם: גלולות למניעת היריון וסרטן השד - Breast cancer and oral contraceptives
- לנושא הבא: שחזור השד - היבטים כירורגיים - Breast reconstruction - surgical aspects
- לתוכן העניינים של הפרק
- לתוכן העניינים של הספר
- לפרק הקודם: כירורגיה של הטחול
- לפרק הבא: בקעים
המידע שבדף זה נכתב על ידי ד"ר צבי קויפמן, מומחה בכירורגיה, מנהל היחידה לבריאות השד, מרכז רפואי מאיר, כפר סבא


 כניסה
כניסה  עקבו אחרינו בפייסבוק
עקבו אחרינו בפייסבוק