דלקת מפרקים שגרונתית - טיפולים חדשים - New therapies for rheumatoid arthritis
| דלקת מפרקים שגרונתית - טיפולים חדשים | ||
|---|---|---|
| New therapies for rheumatoid arthritis | ||
| שמות נוספים | חידושים בטיפול בדלקת מפרקים שיגרונית | |
| יוצר הערך | פרופ׳ מחמוד אבו-שקרה |
|
לערכים נוספים הקשורים לנושא זה, ראו את דף הפירושים – דלקת מפרקים
דלקת מפרקים שגרונתית (Rheumatoid arthritis) היא מחלה אוטואימונית (Autoimmune disease) דלקתית, כרונית ורב מערכתית, אשר הגורם לה אינו ידוע. המחלה מתאפיינת בדלקת ממושכת ושגשוגית של הרקמה הסינוביאלית (Synovial tissue) ומעורבות דלקתית של איברים שונים. ללא טיפול, המחלה עלולה לגרום למוגבלות ולנכות תפקודית. על כן יש צורך באבחון מהיר ובטיפול מוקדם, אשר עשוי למנוע סבל ולמנוע את סיבוכי המחלה.
הקו הטיפולי הראשון בדלקת מפרקים שגרונתית מבוסס על קבוצת תכשירי DMARDs (Disease Modifying Anti-Rheumatic Drugs). מלבדם, נפוץ השימוש בטיפולים ביולוגיים שונים. מתחילת שנות האלפיים פותחו טיפולים חדשים עבור דלקת מפרקים שגרונתית, אשר עשויים להיות יעילים אף יותר מהטיפולים השגרתיים.
אפידמיולוגיה
דלקת מפרקים שגרונתית נחשבת למחלת המפרקים הדלקתית השכיחה ביותר, כאשר 1-0.5 אחוזים מהאוכלוסייה הבוגרת לוקים בה. המחלה מאובחנת בדרך כלל בטווח גילאי 60-40 שנים, ושכיחותה בקרב נשים גבוהה פי שניים עד שלושה בהשוואה לגברים.
אטיולוגיה
בדומה למחלות אוטואימוניות אחרות, למרות שהגורם המשרה את המחלה אינו ידוע, קיימת חשיבות לגורמים סביבתיים, חיסוניים, הורמונאליים ותורשתיים להתפתחות המחלה ולקביעת חומרתה.
בתחילת שנות ה-70 תואר הקשר התורשתי בין דלקת מפרקים שגרונתית ו-4DR-HLA. תפקיד מערכת ה-HLA הוא זיהוי אנטיגנים (Antigens) שונים והצגתם לתאים לימפוציטים (Lymphocytes) מסוג T. מערכת HLA מקודדת על ידי הגן 1DRB-HLA. לגן זה יש יותר מ-20 אללים (Alleles) שונים. אצל מרבית האוכלוסייה הלבנה קיימים שני האללים הקשורים בהתפתחות המחלה, והם 0401*1DRB ו-404*1DRB. האלל 404/0401*1DRB מתאפיין במחלה בעלת מהלך קשה המלווה בעיוותי מפרקים ושחיקת המפרקים.
מאז שנת 2007 פורסמו מספר עבודות המצביעות על פולימורפיזם (Polymorphism) של גנים שונים הקשור בהתפתחות המחלה.
עישון הוא גורם הסיכון הסביבתי המובהק ביותר הקשור בהתפתחות המחלה.
פתוגנזה
דלקת מפרקים שגרונתית היא מחלה דלקתית המתאפיינת בשפעול מספר רב של תאים דלקתיים.
שפעול של לימפוציטים מסוג T ומאקרופאגים (Macrophages) על ידי אנטיגן לא ידוע מלווה ביצור ציטוקינים שונים, כולל אינטרלוקין (Interleukin) 1, אינטרלוקין 6, TNF-alpha וציטוקינים רבים אחרים. לחלק מציטוקינים אלו קיימת פעילות המגבירה את הפעילות הדלקתית וחלקם מדכאים פעילות דלקתית. בסופו של התהליך, קיימת פעילות יתר של ציטוקינים המגבירים פעילות דלקתית. ציטוקינים אלו גורמים לגיוס תאים דלקתיים שונים, שגשוג של תאי הרקמה הסינוביאלית, יצירת נוגדנים, יצירת רקמת הפאנוס (Pannus) האופיינית לדלקת מפרקים שגרונתית ושחרור אנזימים שונים הגורמים להרס ואיבוד רקמת הסחוס.
בנוסף, ללימפוציטים מסוג B (B lymphocytes) יש חשיבות פתוגנית עיקרית, בתפקודם כתאים מציגים אנטיגנים המשפעלים לימפוציטים מסוג T. כמו כן, ברקמה הסינוביאלית בחולי דלקת מפרקים שגרונתית ישנה הסננה של תאי פלזמה המפרישים Rheumatoid Factor (RF). רמה גבוהה של RF קשורה עם מחלה קשה ופעילה, מעורבות חוץ מפרקית ותמותה גבוהה.
RF אינו רגיש לאבחנה של דלקת מפרקים שגרונתית. הוא מופיע בקרב 70-50 אחוז מהחולים בלבד, ובנוסף איננו ייחודי למחלה זו. ניתן למצוא אותו במחלות רקמת חיבור שונות, זיהומים כרוניים כמו זיהום עם נגיף דלקת כבד C (Hepatitis C), גיל מבוגר וממאירות[1].
Anti-Citrullinated Peptide Antibody (ACPA) הוא נוגדן עצמי נוסף שהתגלה בנסיוב של חולי דלקת מפרקים שגרונתית. הנוגדן מכוון נגד מקטע אנטיגני המכיל את החומצה האמינית ציטרולין (Citrulline). חומצה זו היא נגזרת של החומצה ארגינין (Arginine) לאחר שפעול של האנזים Peptidyle arginine deaminase.
קליניקה
דלקת מפרקים שגרונתית היא מחלה רב מערכתית עם מעורבות הקשורה במפרקים. בחלק מהחולים מופיעים ביטויים דלקתיים חוץ מפרקיים. בנוסף, המחלה קשורה עם תחלואה נלווית, הכוללת שכיחות גבוהה של זיהומים, ממאירות לימפופרוליפרטיבית (Lymphoproliferative) וטרשת עורקים מואצת.
המחלה מערבת את מפרקי כפות הידיים והרגליים, ובהעדר מעורבות מפרקים אלו יש לשקול אבחנה אחרת. המעורבות המפרקית מתאפיינת על יד דלקת סימטרית של מפרקי Proximal interphalangeal, מפרקי Metacarpophalangeal, שורשי כפות ידיים, מרפקים, ירכיים, כתפיים, קרסוליים וכפות רגליים. אופי כאב המפרקים הוא דלקתי ומתאפיין בנפיחות, כאב ונוקשות במנוחה והקלה לאחר הפעלת המפרק. בהעדר אבחון וטיפול מוקדם, חלק משמעותי מהחולים מפתח עיוותים אופייניים הגורמים למגבלות ונכות. עיוותים אלו גורמים לאבוד המבנה והתפקוד התקין של המפרק כתוצאה מהרס רקמת הסחוס, שחיקה של עצמות, פגיעה במיתרים וגידים ודלדול רקמת השרירים.
התופעות חוץ מפרקיות מתחלקות לשתי קבוצות עיקריות:
- תופעות משניות לשקיעת מכלולים חיסוניים (Immune complexes) ברקמות וכלי דם: כגון דלקת קרום הריאה (Pleuritis) והלב (Pericarditis), כיבים עוריים, קשריות שגרונתיות (Rheumatoid nodule) ודלקת של כלי דם (Vasculitis).
- תופעות משניות להסננה ניכרת של הרקמות על ידי תאי דלקת: כגון Felty's syndrome, תסמונת שיוגרן (Sjögren's syndrome), הגדלת קשריות לימפה (Lymphadenopathy) והגדלת טחול (Splenomegaly).
אבחנה
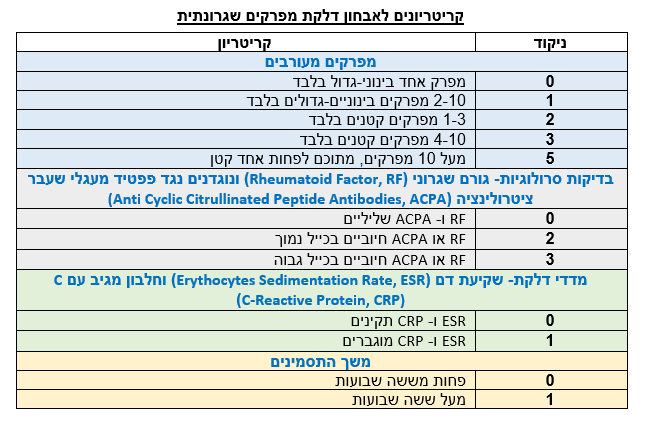
האבחנה של דלקת מפרקים שגרונתית היא בעיקר קלינית ומבוססת על נוכחות דלקת מפרקים בעלת מאפיינים דלקתיים ובהעדר הסבר אחר לדלקת המפרק. בשנת 2010 פורסמו מדדים חדשים לאבחון המחלה. מדדים אלה התבססו על עבודה משותפת של האיגוד האמריקאי למחלות פרקים (American college of rheumatology) והאיגוד האירופאי נגד מחלות פרקים (European league against rheumatism). על פי מדדים אלו, האבחנה נקבעת על פי צבירת שש מתוך עשר נקודות אפשריות בארבעה מדורים שונים.
נוגדני ACPA הם ייחודים ביותר לאבחון דלקת מפרקים שגרונתית עם סגוליות של 100-98 אחוז ורגישות של 80-60 אחוז. הנוגדן נמצא אצל 35% מחולי דלקת מפרקים שגרונתית ללא RF.
בחולים עם דלקת מפרקים בשלב מוקדם (עד שלושה חודשים מהופעת תסמינים) וללא אבחנה ברורה, לנוכחות ACPA קיימת סגוליות של 96% לאבחון דלקת מפרקים שגרונתית, לעומת 91% ל-RF מסוג אימונוגלובולין M (IgM, Immunoglobulin M). הערך המנבא החיובי (Positive predictive value) של ACPA הוא 91%. בנוסף, לנוגדנים אלו יש ערך מנבא של 91% לפתח שחיקה (Erosion) בעצם שנתיים לאחר האבחנה[2].
טיפול
מטרת הטיפול התרופתי בדלקת מפרקים שגרונתית היא הפחתת כאב ונפיחות, שיפור התפקוד, מניעת הופעת עיוותים והרס מפרקים ושיפור איכות החיים של החולים.
בחולים עם דלקת מפרקים שגרונתית יש שכיחות גבוהה של תחלואת לב וכלי דם, זיהומים חיידקיים ונגיפיים וסיכון מוגבר לפתח מחלות לימפופרוליפרטיביות. טיפול בגורמי סיכון לטרשת, מתן חיסונים מקיפים וסקירה לממאירות מהווים חלק מהטיפול והמעקב השוטף בחולים.
הקו הראשון של טיפול בדלקת מפרקים שגרונתית מבוסס על קבוצת DMARDs. תכשירים אלו מהווים את הקו הטיפולי העיקרי. לאחר קביעת האבחנה, כל חולה עם דלקת מפרקים שגרונתית חייב לקבל לפחות תכשיר אחד מקבוצה זו. ברוב המרכזים בעולם מקובל לשלב 3-2 תכשירים מסוג DMARDs בזמן קביעת האבחנה, ואילו חלק מהמרכזים מעדיפים להתחיל בתרופה אחת ולהוסיף תכשיר נוסף רק במידה ויש העדר תגובה נאותה. שילוב של Methotrexate או Salazopyrin (Sulfasalazine) ותכשירים נוגדי-מלריה (Antimalarial medication) הוא שילוב מקובל מאוד, המשתווה ביעילותו לטיפול ביולוגי[3].
ב-70-60 אחוז מהחולים מלווה טיפול ב-DMARDs בהפוגה או פעילות נמוכה של המחלה.
מתחילת שנות האלפיים יצאו חלק מהתכשירים השייכים לקבוצת ה-DMARDs משימוש, ובמקביל התווספו תכשירים אחרים. Methotrexate נחשב עדיין לטיפול הבחירה. התכשיר יעיל ולאחר שבועיים של טיפול מתקבלת תגובה המתבטאת בירידה במספר המפרקים המודלקים, בעוצמת הכאב ובשיפור ברמה התפקודית. Methotrexate ניתן במנה שבועית המחולקת לאורך 24 שעות או בהזרקה תת עורית פעם בשבוע, במינון של 25-15 מיליגרמים (מ"ג) לשבוע.
Arava (Leflunomide) הוא תכשיר נוסף מקבוצת ה-DMARDs עם מנגנון פעולה דומה ל-Methotrexate. הוא מעכב יצור פירימידין (Pyrimidine) על ידי עיכוב פעילות האנזים Dihydroorotate dehydrogenase. כ-50% מהחולים המטופלים בתרופה מגיבים לטיפול בהתאם למדד המקובל. תופעת הלוואי העיקרית, בדומה ל-Methotrexate, היא פגיעה בתפקודי כבד ובנוסף התרופה טרטוגנית (Teratogenic) במידה ניכרת[4].
טיפול ביולוגי
בהעדר תגובה נאותה לטיפול בתכשירי DMARDs, טיפול הבחירה הבא הוא טיפול ביולוגי.
הטיפולים הביולוגיים הוכנסו לשימוש רחב באמצע שנות ה-90 של המאה ה-20 והם מבוססים על איתור תא, קולטן או ציטוקין בעלי חשיבות עליונה בפתוגנזה של המחלה, ופיתוח נוגדן או קולטן שמטרתו לנטרל את פעילותם.
הטיפול הביולוגי הוא ייחודי ומכוון כנגד מתווך יחיד. הטיפולים הביולוגיים הזמינים בארץ ובעולם מתחלקים לשלוש קבוצות עיקריות: טיפול נגד ציטוקינים, טיפול נגד תהליך השפעול המשותף (Co-stimulation) וטיפול נגד לימפוציטים מסוג B.
טיפול נגד ציטוקינים
הקבוצה הראשונה של טיפולים ביולוגיים כוונה נגד הציטוקין alpha-TNF.
בנסיוב ובנוזל הסינוביאלי של חולי דלקת מפרקים שגרונתית ישנה רמה גבוהה של alpha-TNF המיוצר על ידי לימפוציטים מסוג T המסננים את הממברנה הסינוביאלית. פעילות זו נחשבת כהתרחשות מרכזית הגורמת לדלקת כרונית במחלה.
טיפול ביולוגי נגד הציטוקין אינטלוקין 6 מהווה אבן דרך עיקרית בטיפול בדלקת מפרקים שגרונתית. הטיפול שווק בתחילה כתכשיר הניתן דרך הווריד בתדירות של פעם בחודש, אך לאחר מכן שונה כך שניתן לתת טיפול בתכשיר גם בצורת מתן תת-עורי. יתרונו העיקרי של תכשיר זה הוא בכך שהוא ניתן כטיפול יחיד ללא צורך בטיפול נוסף מקבוצת DMARDs[5].
טיפול נגד תהליך השפעול המשותף
תהליך ההצגה של אנטיגן פתוגני על ידי התאים המאקרופאגים, המשמשים כתאים מציגי אנטיגן (Antigen presenting cells), ללימפוציטים מסוג T, קשור ביחסי הגומלין בין שני סוגי התאים בתהליך הנקרא "השפעול המשותף".
מנגנון הפעולה של Orencia (Abatacept) קשור בעיכוב קשירת 80CD הנמצא על פני מאקרופאגים למולקולת 28CD על פני לימפוציטים מסוג T. התכשיר נמצא יעיל עבור טיפול בדלקת מפרקים שגרונתית. הוא ניתן במתן תוך ורידי וגם תת עורי. יעילותו נבדקה מול Humira (Adalimumab) ונמצאה דומה[6].
טיפול נגד לימפוציטים מסוג B
קבוצה נוספת של טיפולים מכוונת כנגד 20CD הנמצא על פני לימפוציטים מסוג B. טיפול זה נחשב לקו אחרון של טיפול כיוון שהוא מכוון נגד תאים ומלווה בדיכוי של לימפוציטים מסוג B.
| מינון | צורת מתן | אתר פעילות | מבנה עיקרי | שם התכשיר |
|---|---|---|---|---|
| 3 מ"ג/ק"ג | דרך הוריד בשבוע 0, 2, 6 וכל 8 שבועות אתרי זה | TNF | נונדן אנושי-כימירי igGl | Infliximab |
| 25 מ"ג פעמיים בשבוע | הורקה תת עורית | TNF | חלבון שנוצר מחיבור של lg אינושי לבין שרשרת P75 של הקולטן ל TNF (P75-Fc IgG) | Enbrel (Etanercept) |
| 40 מ"ג כל שבועיים | הזרקה תת עורית | TNF | נוגדן חד שבטי lgG1 | Humira |
| 50 מ"ג כל חודש | הזרקה תת עורית | TNF | נוגדן חד שבטי אנושי lgG1k | Simponi (Golimumab) |
| 400 מ"ג בשבוע 0, 2, 4 ואתרי זה 200 מ"ג כל שבוע | הזרקה | TNF | Fab' fragment אנושי קשור ל- polyethylene glycol | Cimzia (Certolizumab pegol) |
| 8-4 מ"ג/ק"ג 162 מ"ג כל שבועיים | הזרקה פעם בחודש הזרקת תת-עורית | קולטן של IL-6 | נוגדן חד שבטי אנושי lgG1 | Actemra (Tocilizumab) |
| 1000-500 מ"ג כל עירוי
|
עירוי לתוך הוריד, ימים 29,15,1 וכל 28 יום לאחר מכן מתן תת עורי | מניעת קשירת CD80 (מקרופאנים) ו-CD28 (תאי T) | Fusion protein הכולל CTLA4 ו-FcIgG | Orencia |
| שני טיפולים במיגון של 1000 מ"ג ביום 15-11 | דרך הוריד | CD20 (B תאי) | נוגדן כימירי | Mabthera (Rituximab) |
טיפול מהדור החדש
דור חדש של טיפולים עבור דלקת מפרקים שגרונתית מכוון לעכב פעילות תוך תאית המתרחשת בעקבות קשירתם של ציטוקינים לקולטנים על פני ממברנת התאים.
מנגנון הפעולה
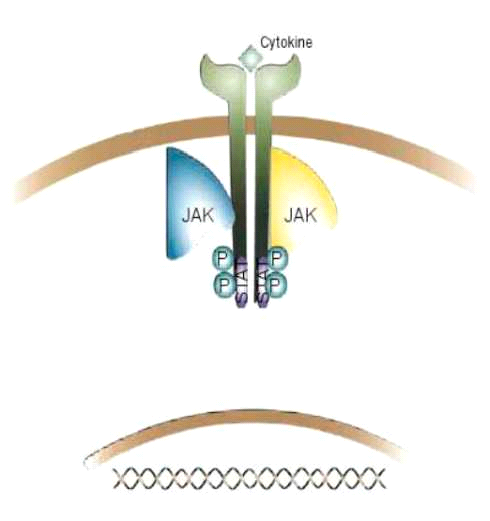
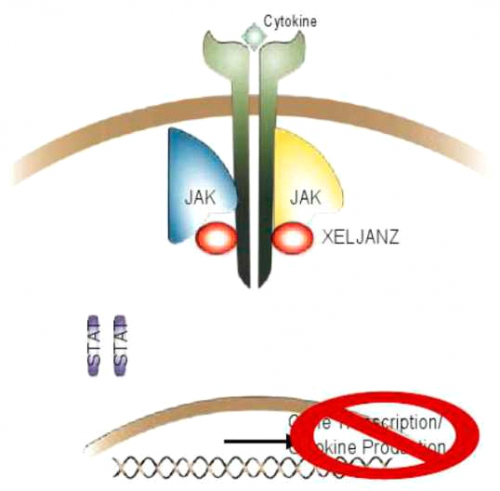
כאשר ציטוקין נקשר לקולטן שלו על פני ממברנת התא הוא גורם לשרשרת פעולות אנזימטיות תוך-תאיות, אשר מעבירות אותות לתוך גרעין התא. אותות אלו גורמים לשפעול DNA בתוך הגרעין. התוצאה של פעילות זו תהיה ייצור ציטוקינים או מתווכי דלקת אחרים המגבירים את שרשרת הפעילות הדלקתית.
אחד המנגנונים התוך-תאיים אשר נבדק בהרחבה וכנגדו פותחו טיפולים הוא מנגנון הקשור באנזים המזרחן שיירי טירוזין (Tyrosine kinase). אנזים זה פועל על ידי זירחון של אנזימים וחלבונים אחרים.
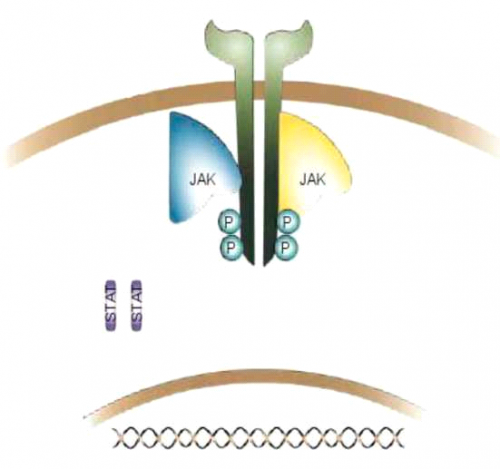
מערכת האנזימים המזרחנים JAK (Janus Kinases) נחקרה בצורה רחבה. מערכת זו כוללת ארבעה אנזימים (4-1JAK). בדרך כלל קשורים שני זוגות של אנזימי JAK לקולטן של הציטוקין ומהווים חלק ממנו.
מספר רב של ציטוקנים פועלים דרך מערכת JAK, ביניהם אינטרלוקינים 2,4,6,7,9,12,15,21 ו-23, ואינטרפרון אלפא (Interferon alfa), בטא (Interferon Beta) וגמא (Interferon gamma).
בעקבות קשירה של ציטוקין לקולטן מתרחשת שרשרת של תגובות תוך תאיות לפי הסדר הבא[7][8]:
- שינוי במבנה התוך תאי של הקולטן (Receptor polymerization)
- שינוי במבנה JAK ושפעולו (זירחון עצמי של האנזים)
- זירחון של הקולטן בחלקו התוך-תאי ויצירת אתר קשירה לחלבון המתמיר אותות ומשפעל שעתוק (STAT, Signal Transducer and Activator of Transcription)
- קשירת של חלבון STAT לקולטן
- זירחון של STAT
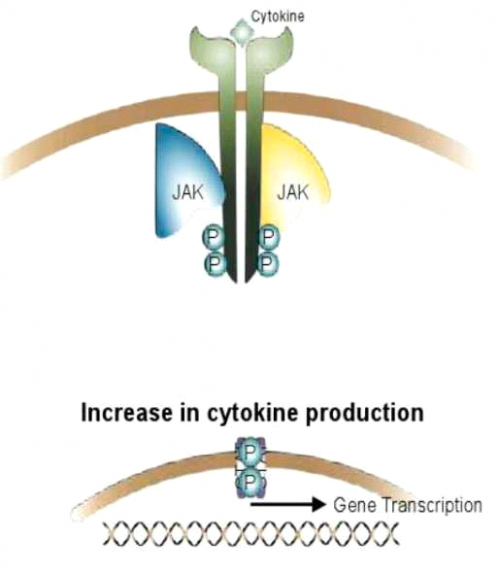
- שחרור STAT מהקשר שלו לקולטן ונדידתו לתוך הגרעין
- הפעלת DNA וייצור ציטוקינים אחרים - שעתוק גנומי (Gene transcription)
מעכבי האנזים JAK הם הדור החדיש ביותר של הטיפול בדלקת מפרקים שגרונתית. הם אינם נחשבים כטיפולים ביולוגיים כיוון שאינם מנטרלים תא או ציטוקין ייחודי. מחקרים הראו שיש להם פעילות דמוית DMARDs, היות והם משנים את מהלך המחלה. לכן הם מהווים קבוצה חדשה של תכשירים לטיפול בדלקת מפרקים שגרונתית.
Xeljanz (Tofacitinib) שייכת לדור חדש של תכשירים לטיפול בדלקת מפרקים שגרונתית. התכשיר נבדק בחולים עם דלקת מפרקים שגרונתית בשלבים שונים של המחלה ובכל המחקרים נמצא יותר יעיל בהשוואה לקבוצה ההשוואה. התרופות משתייכת לקבוצת המולקולות הקטנות (Small molecules).
Xeljanz הוא מעכב הפיך ייחודי, בררני ותחרותי של JAK, אשר נחקר בצורה רחבה ואף נרשם לטיפול בעולם ובארץ. התכשיר פותח נגד 3JAK אבל נמצא שפועל גם נגד 1JAK ו-2JAK. עיכוב הפעילות של 1JAK ו-3JAK היא הרבה יותר גבוהה מזו של 2JAK. התכשיר נקשר לאתר קושר ATP על פני JAK ועל ידי כך מונע זירחון עצמי של JAK לאחר קשירת ציטוקינים שונים לקולטן שלהם על פני ממברנת התא.
כתוצאה מעיכוב זה, JAK לא משופעל, ובעקבות כך לא מתרחש שפעול של STAT, לא מתרחשת העברת אותות לתוך הגרעין והתהליך הדלקתי לא מתקדם. מנגנון זה גורם לעיכוב פעילות ציטוקינים שונים ובעיקר אינטרלוקינים 6,7,15 ו-21 ואינטרפרון אלפא ובטא.
הטיפול ניתן בצורה פומית. התרופה נספגת מהר (תוך כ-30 דקות) עם זמינות ביולוגית (Bioavailability) של 74%. היא מופרשת תוך 3.2 שעות דרך הכבד (70%) ודרך הכליה (30%).
Xeljanz נמצא יעיל כטיפול בדלקת מפרקים שגרונתית עם טווח בטיחות מקובל. בנוסף להיותו תכשיר פומי, הוא פועל בצורה מהירה. במרבית החולים פעילות קלינית נצפית תוך שבועיים מתחילת הטיפול. התכשיר נבדק בשני מינונים שונים, חמישה ועשרה מ"ג, וניתן פעמיים ביום. שני המינונים מקובלים לשימוש קליני.
יעילות הטיפול
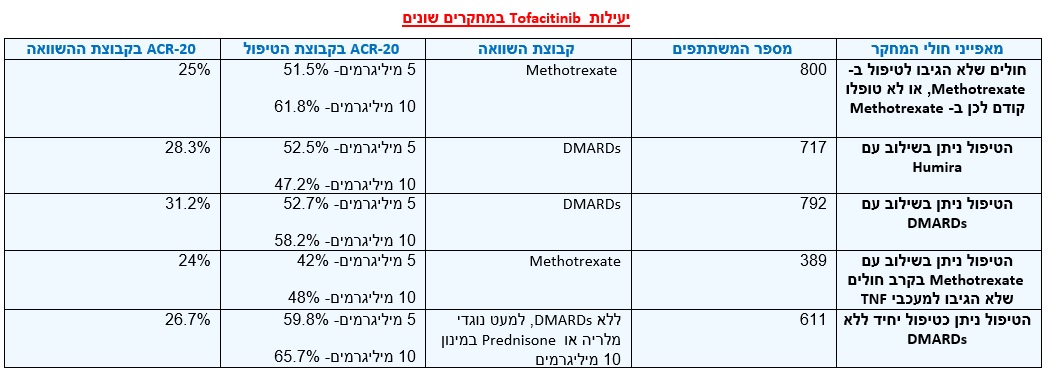
יעילות Xeljanz נבדקה בקבוצות שונות של חולים עם דלקת מפרקים שגרונתית פעילה בחומרה בינונית עד קשה. המחקרים כללו חולים שלא הגיבו לטיפול ב-Methotrexate וחולים לאחר כישלון טיפול במעכבי TNF. הפרוטוקול הטיפולי נבדק בשילוב עם Methotrexate או DMARDs אחרים (בהשוואה לחולים אשר טופלו ב-DMARDs בלבד), או במקביל לטיפול ב-Humira בהשוואה לאינבו (Placebo). כמו כן, נבדקה יעילותו כטיפול יחיד. לא בוצעו מחקרים שהשוו יעילות תכשירים אלו בהשוואה לכל הטיפולים הביולוגיים הנמצאים בשימוש רחב.
היעילות נבדקה בעזרת מדדים מקובלים להערכת תגובה קלינית, שכללו את אחוז החולים שהשיגו 20% שיפור במספר מפרקים נפוחים ביחד עם מספר מפרקים רגישים ושלושה מתוך חמישה משתנים נוספים הכוללים שקיעת דם (ESR) או CRP (C-Reactive Protein), הערכה כללית של פעילות המחלה על ידי הראומטולוג והחולה, הערכה כללית של חומרת כאב המפרקים על ידי המטופל והערכה כללית של מוגבלות על ידי החולה. מדדים אלו מכונים "תגובת 20 של הקבוצה האמריקאית למחלות פרקים" (The American College of Rheumatology 20 Response ,20-ACR).
מדד נוסף שנבדק הוא אחוז החולים שמחלתם נכנסה להפוגה מלאה או הפכה למחלה עם פעילות נמוכה. תוצא זה נבדק בעזרת "מדד פעילות המחלה 28" (28 Disease Activity Score ,28-DAS) המבוסס על הערכת 28 מפרקים, ESR או CRP והערכה כללית של פעילות המחלה על ידי החולה. ערך מתחת ל-2.6 נחשב להפוגה, ואילו ערך הנמוך מ-3.2 מעיד על פעילות נמוכה[9],[10],[11],[12],[13].
בטיחות הטיפול
מתאר הבטיחות של התרופה דומה למדווח בשאר הטיפולים הביולוגיים. תופעות הלוואי השכיחות אשר דווחו במטופלי Xeljanz כוללות כאב בטן, שלשול, כאב ראש וזיהומים של דרכי הנשימה העליונות. ב-4% מהחולים שהשתתפו במחקרים הופסק הטיפול עקב תופעות לוואי. זיהומים קשים המצריכים אשפוז וטיפול אנטיביוטי עוקף מערכת עיכול נצפו בכ-1% מהחולים. מדובר בעיקר בזיהומי דרכי נשימה וזיהומי רקמות רכות. כמו כן, דווח על מטופלים אשר אובחנו עם שחפת (Tuberculosis).
בנוסף, תוארה עלייה של 14-12 אחוז ברמת הכולסטרול מסוג LDL ועלייה דומה ברמת הכולסטרול מסוג HDL.
ההשפעה על ספירת הדם התבטאה בירידה בספירת נויטרופילים (Neutrophils) ולימפוציטים. ממוצע הירידה בספירה נויטרופילים היה כ-800 נויטרופלים בקרב החולים שטופלו במינון של חמישה מ"ג ו-1,300 בקרב חולים שטופלו בעשרה מ"ג פעמיים ביום. לא נצפתה נויטרופניה (Neutropenia) קשה.
פרוגנוזה
למחלה יש השפעה על אורך החיים ואיכותם, כמו גם על תפקוד החולים. עבודות מתחילת שנות ה-90 דווחו שהמחלה מקצרת את משך החיים ב-18-3 שנים. בנוסף, לאחר 10 ו-20 שנות מחלה, 50 ו-90 אחוזים מהחולים, בהתאמה, מאבדים לחלוטין את כושר העבודה ומפתחים מוגבלות ונכות משמעותיות.
ביבליוגרפיה
- ↑ MCLNNES IB, SCHETT G. THE PATHOGENESIS OF RHEUMATOID ARTHRITIS. NEJM. 2011:365:2205-19.
- ↑ WHITING PF, SMIDT N, STERNE JA, ET I. SYSTEMATIC REVIEW: ACCURACY OF ANTL-CITRUL-LINATED PEPTIDE ANTIBODIES FOR DIAGNOSING RHEUMATOID ARTHRITIS. ANN INTERN MED. 2010;152:456-64.
- ↑ O'Dell JR, MikulsTR, Taylor TH, eta i. Therapies for active rheumatoid arthritis after methotrexate failure. N Engl J Med. 2013;369:307-18
- ↑ SMOLEN JS, KALDEN JR, SCOTT DL, ET AL. EFFICACY AND SAFETY OF LEFLUNOMIDE COMPARED WITH PLACEBO AND SULPHASALAZINE IN ACTIVE RHEUMATOID ARTHRITIS: A DOUBLE-BLIND, RANDOMISED, MULTICENTRE TRIAL. EUROPEAN LEFLUNOMIDE STUDY GROUP. LANCET. 1999;353:259-66
- ↑ Burmester GR, Rubbert-Roth A, Cantagrel A, et al. A randomised, double-blind, parallel-group study of the safety and efficacy of subcutaneous Tocilizumab versus intravenous Tocilizumab in combination with traditional disease-modifying antirheumatic drjgs in patients with moderate to severe rheumatoid arthritis. Ann Rheum Dis2013 Sep 12. [Epub ahead of print]
- ↑ SCHIFF M, WEINBLATT ME, VALENTE R, ET AL. HEAD-TO-HEAD COMPARISON OF SUBCUTANEOUS Abatacept VERSUS Adalimumab FOR RHEUMATOID ARTHRITIS: TWO-YEAR EFFICACY AND SAFETY FINDINGS FROM AMPLE TRIAL. ANN RHEUM DIS. 2013 AUG 20.
- ↑ O'SHEAJJ, PLENGER. JAK AND STAT SIGNALING MOLECULES IN IMMUNOREGULATION AND IMMUNE-MEDIATED DISEASE. IMMUNITY. 2012:36:542-550.
- ↑ JIANG J, GHORESCHI K, DEFLORIAN F, ETAL. EXAMINING THE CHIRALITY, CONFORMATION AND SELECTIVE KINASE INHIBITION OF 3-((3R4׳R)-4-METHYL3־-(METHYL(7H-PYRROLO[2,3-D] PYRIMIDIN-4-YL)AMINO)PIPERIDIN-1־YL)3־-OXOPROPANENITRILE(CP690,550־
- ↑ Ghoreschi K, Laurence A, O'SheaJJ. Janus kinases in immune cell signaling. Im¬munol Rev. 2009:228:273-287.
- ↑ Van der Heijde D, Tanaka y, Fleischmann R, et al. Tofacitinib (CP-690,550) in pa-tientswith rheumatoid arthritis receiving methotrexate: twelve-month data from a twenty-four-month phase III randomized radiographic study. Arthritis Rheum. 2013 65:559-70
- ↑ KremerJ, Li ZG, Hall S, Fleischmann R, etal. Tofacitinib in combination with non-biologic disease-modifying antirheumatic drugs in patients with active rheumatoid arthritis: a randomized trial. Ann Intern Med. 2013 Aug 20:159:253-61
- ↑ Burmester GR, Blanco R, Charles-Schoeman C, et al Tofacitinib (CP-690,550) in combination with methotrexate in patients with active rheumatoid arthritis with an inadequate response to tumour necrosis factor inhibitors: a randomised phase 3 trial. Lancet. 2013;381:451-60
- ↑ Fleischmann R, Kremer J, Cush J, etal. Placebo-controlled trial of tofacitinib monotherapy in rheumatoid arthritis. N Engl J Med. 2012 ;367:495-507
קישורים חיצוניים
- חידושים בטיפול בדלקת מפרקים שיגרונית, TheMEDICAL
המידע שבדף זה נכתב על ידי פרופ׳ מחמוד אבו-שקרה, מנהל היחידה לראומטולוניה ומחלקה לרפואה פנימית ד, המרכז הרפואי אוניברסיטאי םורוקה, באר שבע


 כניסה
כניסה  עקבו אחרינו בפייסבוק
עקבו אחרינו בפייסבוק