הורמון גדילה - Growth hormone
| מדריך בדיקות מעבדה | |
| הורמון גדילה | |
|---|---|
| Growth hormone | |
| שמות אחרים | GH, סומטוטרופין |
| מעבדה | אנדוקרינולוגיה בדם |
| תחום | הערכת התפקוד של הורמון הקשור לשגשוג, גדילה, ומסת העצם |
| יחידות מדידה | ננוגרם למ"ל |
| טווח ערכים תקין | דם טבורי: 8-41; יום ראשון לחיים - 5-53; שבוע ראשון - 5-27; עד גיל 7 שנים - 1-13.6; גיל 7-11 שנה - 1-16.4; גיל 11-15 שנה - 1-14.4; גיל 15-19 שנה - 1-13.4; גברים - 1-9 נשים - 1-16. בנוזל מי שפיר: בשבוע ה-20 להריון - 10; בשבוע ה-40 להריון - 30. |
| יוצר הערך | פרופ' בן-עמי סלע |
מטרת הבדיקה
מדידת GH תידרש בתרחישים החשודים בילדים לענקות (gigantism) או ל-acromegaly במבוגרים. מדידת GH שנעשית לעתים במקביל לקביעת רמת IGF-1, מטרתה לנטר מצבים חוזרים של אי סדירות הורמון גדילה לאחר טיפול. הערכה פיזיולוגית משמעותית יותר של חסר או עודף בהורמון גדילה מושגת במבחני עידוד או דיכוי של יצירת GH. כיוון ש-IGF-1 משקף חסר או עודף של GH, וכיון שרמת IGF-1 יציבה לאורך שעות היום, היא יכולה לשמש לסיוע בהערכת רמת GH.
לקריאת מדרכים בנושא בעיות גדילה
בסיס פיזיולוגי
GH הוא הורמון פפטידי חד-שרשרתי בן 191 חומצות אמינו המעודד צמיחה, התרבות תאים והתחדשותם. הוא מהווה למעשה מיטוגן לסוגי תאים אחדים. הוא מיוצר, נאגר ומופרש מתאים סומטו-טרופיים בצידי החלק הקדמי של בלוטת יותרת המוח (היפופיזה). הגנים לשני האיזופורמים של הורמון הגדילה, GH1 (סומטוטרופין) ו-GH2, ממוקמים באיזור q22-24 של כרומוזום 17. גנים אלה קשורים לגנים המקודדים ל-placental lactogen, ויחד עם פרולקטין, שלושת הורמונים אלה הם מהווים קבוצת הורמונים עם פעילות מעוודדת צמיחה או עם פעילות לקטוגנית.
האיזופורם העיקרי של GH כאמור מכיל 191 חומצות אמינו ומשקלו המולקולארי 22,124 דלטון, והוא מכיל שייר סוכרי. מבנה ההורמון מכיל 4 גדילים המאפשרים קישור לקולטן של ההורמון. בהיפופיזה נמצאים מספר איזופורמים של GH וכולם מופרשים לדם. בין השאר קיים וריאנט בעל משקל מולקולארי של כ-20 אלף דלטון, המהווה כ-10% מכלל ההורמון המופרש לדם, וכן קיים וריאנט עם מ.מ. של 23,500 דלטון, שריכוזו בדם גבוה יותר לאחר פעילות גופנית מאומצת. כל הוריאנטים הללו קשורים באופן חלקי בדם לחלבון GHBP או Growth hormone binding protein.
הורמון הגדילה מופרש מהחלק הקדמי של בלוטת יותרת המוח (היפופיזה) ומווסת את צמיחת העצמות והשרירים. רמת ההורמון אינה אחידה במשך כל החיים ותקופות של צמיחה כמו גיל ההתבגרות מאופיינות ברמה גבוהה יחסית. רמה נמוכה של ההורמון מגיל צעיר עלולה לגרום לננסות, ואילו רמה גבוהה-לענקות. רמה גבוהה בגיל מבוגר גורמת לאקרומגליה (acromegaly), מחלה המתאפיינת בגדילה לא פרופורציונית של חלק מאברי הגוף.
וויסות הפרשת GH
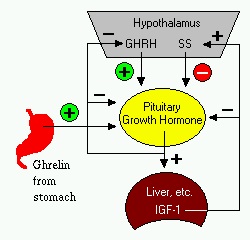
הפרשת GH מבלוטת יותרת המוח, מבוקרת על ידי גרעינים בהיפותלמוס המפרישים לתוך וריד השער של ההיפופיזה פפטידים כגון growth hormone releasing-hormone או GHRH הידוע גם כ-somatocrinin, אך גם growth hormone inhibiting-hormone או GHIH הידוע גם כ-somatostatin. הפרשת GH על ידי ההיפופיזה נקבעת בעיקר על ידי האיזון בין 2 פפטידים אלה, כאשר הם כשלעצמם מושפעים מגורמים פיזיולוגיים רבים (פעילות גופנית, תזונה, עקה, שינה) או מעכבים כגון חומצות שומן חופשיות.
התאים הסומטו-טרופיים בהיפופיזה מסנתזים ומפרישים GH במתכונת פעימתית (pulsatile), החל מגיל 4 שבועות למעשה בתגובה לגירויים מההיפותלמוס. בתינוקות עד גיל 4 שבועות יצירת GH עולה בתגובה להיפוגליקמיה ולעקה פיזית. ההפרשה הניכרת ביותר של GH מתרחשת כשעה לאחר תחילת שינה, עם רמות הורמון בפלזמה בין 13-72 ננוגרם למ"ל. הרמות GH בשעות היום שונות משמעותי בין בני-אדם. תשעים וחמישה אחוז מהפרשת GH מתרחשת בשלבי השינה הראשונית המוגדרים כ-NREM. גלי הפרשת ההורמון בשעות היום מתרחשים תוך פרקי-זמן של 3-5 שעות, כאשר בפרקי זמן אלה רמת ההורמון בפלזמה היא בין 5-45 ננוגרם למ"ל. בין שיאי הפרשת GH, הרמה הבסיסית של ההורמון בדם נמוכה יחסית, בדרך כלל פחות מ-5 ננוגרם למ"ל ברוב שעות היממה. הפרשת GH מושפעת מהגיל והמין, כאשר בשנות הנעורים מדי יום מופרשים כ-700 מיקרוגרם הורמון, בעוד שמבוגרים בריאים מפרישים מדי יום כ-400 מיקרוגרם. בתרחישים של acromegaly או של ענקות, המתכונת הפעימתית של הפרשת GH נעלמת.
בשעות היום רמות GH בדם מושפעות מאכילה, כאשר פחמימות מדכאות רמת GH בעוד תזונה עתירת חלבון מגבירה הפרשת GH. מכאן שקביעה נקודתית של רמת ההורמון בדם היא בדרך כלל בעלת משמעות מוגבלת. דרך נוספת להערכה של אפשרות של הפרשה מוגברת של ההורמון מההיפופיזה במטופל החשוד ל-acromegaly, היא על ידי מדידה של IGF-1, שכן רמות גורם זה המסונתז בכבד המשמש כמתווך של פעילות GH, מוגברות בתרחיש זה ומדידת IGF-1 עשויה לסייע באבחון מקרים גבוליים, כמו גם לעזור בניטור תוצאות הטיפול באלה עם acromegaly.
ההשפעה הפיזיולוגית של GH
ניתן לתאר באופן כללי את פעילותו של GH בגוף כאנבולית, כאשר הגברת הגובה בגיל הילדות היא אולי המוכרת ביותר. צמיחה לגובה מעוּדדת על ידי 2 מנגנונים:
- כיוון שהורמונים פפטידיים אינם מסיסים בשומן, הם אינם יכולים לחדור דרך ה-lipid bilayer של ממברנות התאים, לכן GH משפיע על ידי קישור לקולטנים על פני תאי היעד. קישור כזה משפעל את המסלול התוך תאי של PAPK/ERK, דרכו מעודד GH חלוקה והתרבות של התאים יוצרי הסחוס, כונדרוציטים. תאי שומן לדוגמה, אדיפוציטים, מכילים על פני התא קולטנים ל-GH, דרכם מעודד הורמון זה את תאי השומן לפרק טריגליצרידים ולדכא את יכולת תאים אלה לקלוט שומנים מהדם. הורמון הגדילה מעודד באופן ישיר קליטה של חומצות אמיניות לתאים לבניה של חלבונים. כן גם ישירה השפעת GH על מטבוליזם של פחמימות.
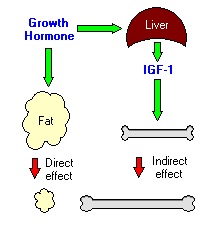
- הורמון הגדילה גם מעודד דרך מסלול האיתות JAK-STAT את יצירת IGF-1 או insulin-like growth factor-1 (שהיה מכונה בעבר somatomedin C), הורמון האנלוגי בפעילותו ל-proinsulin. איבר היעד העיקרי של GH לפעילות זו הוא הכבד, שבו אמנם עיקר היצירה של IGF-1, כאשר להורמון זה יש פעילויות במגוון רחב של רקמות. GH גם משרה את יצירת הקולטן של IGF-1 הידוע כ-insulin-like growh factor binding protein 3 או IGFBP3. ניתן לקבוע שרוב הפעילויות הבלתי-ישירות של GH בגוף, נעשות באופן עקיף על ידי IGF-1.
אם כן, IGF-1 משמש כתווך המוציא לפועל את השפעות GH באופן בלתי ישיר כגון המרצת התרבות כונדרוציטים, המתפתחים לבסוף לתאי עצם. ל-IGF-1 תפקיד מפתח בצמיחת שרירים על ידי עידוד התרבות תאים מיובלסטים.
הורמון הגדילה יכול להיחשב הורמון הפועל על רקמות רחוקות (אנדוקריני) אך הוא גם יכול להיווצר באותן רקמות ולהשפיע באופן מקומי-פאראקריני, בין השאר הוא בעל השפעה מעודדת על התאים יוצרי העצם-אוסטיאובלסטים ועל התאים יוצרי הסחוס-כונדרוציטים. השפעות GH על התאים יוצרי העצם והסחוס נעשית בתיווך IGF-1. גם השפעת הורמון הגדילה על קליטת חומצות אמינו וסינתזת חלבונים כמו גם הפחתת תהליכי חמצון חלבונים בשריר וברקמות אחרות נעשית בתיווך IGF-1.
בנוסף להשפעתו בעידוד הצמיחה בגיל הצעיר, יש ל-GH השפעות נלוות נוספות בגוף: GH מגביר את אצירת סידן באופן שמחזק ומגביר את תהליך המינרליזציה של העצם; מגביר בתיווך IGF-1 את מסת השריר על ידי הגדלת החלק המתכווץ שלו (מה שידוע כ-sarcomere hypertrophy); מעודד פירוק שומנים-ליפוליזה; מגביר סינתזת חלבונים; מעודד צמיחה וגדילה של כל איברי הגוף הפנימיים פרט למוח; מעודד את מערכת החיסון; תורם לאחזקת ותפקודם של איי בלוטת הלבלב; מפחית קליטת גלוקוזה על ידי הכבד אך מעודד את תהליך gluconeogenesis בכבד; משחק תפקיד ב-homeostasis. ההפרשה המרבית של GH ו-IGF-1 חלה בשנות הבשלות המינית ואכן באותם שנים תורמים השניים לצבירת ושמירת מסת העצם, במעבר לשנות הבגרות. חסר ב-GH כרוך בירידה במינרליזציה של העצם וצפיפותה (BMD).
GH הוא אחד מסדרת הורמונים התורמים לשמירת רמה נאותה של גלוקוזה בדם. נהוג להתייחס להורמון הגדילה כבעל פעילות anti-insulin כיוון שהוא מדכא את היכולת של אינסולין לעודד קליטת גלוקוזה ברקמות היקפיות, וכן בהיותו מעודד סינתזת גלוקוזה בכבד, ופירוק גליקוגן לגלוקוזה, וכתוצאה מכל אלה מעלה רמת גלוקוזה בדם. באופן מעט פרדוקסאלי מתן הורמון גדילה דווקא מעודד הפרשת אינסולין, מה שמוביל להיפר-אינסולינמיה.
משמעות קלינית
עודף GH: המחלה השכיחה ביותר הקשורה ליצור עודף של GH היא גידול סרטני של תאי ה-somatotroph בקדמת ההיפופיזה. גידולים אלה שכיחים יחסית אם כי הם פחות שכיחים מהגידולים המייצרים פרולקטין. אדנומות של תאים אלה המופיעות בדרך כלל בעשור החיים החמישי, שפירות באופיין וגדלות באופן איטי, ומייצרות בהדרגה כמויות הולכות וגדלות של GH. עודף מתמשך ברמת GH גורם להתעבות עצמות הלסת, ואצבעות הידיים והרגליים, נפיחות ברקמות רכות, ואף נטייה למחלת לב. כאשר ההתייחסות אל השינויים המורפולוגיים הללו היא כאל acromegaly. סיבוכים מתלווים לתסמונת זו הם הזעת יתר, לחץ מוגבר על העצבים הבא לביטוי בתסמונת המנהרה הקרפלית, חולשת שרירים, רמה מוגברת של החלבון נשא הורמוני המין SHBG, עמידות לאינסולין, או אפילו צורה נדירה של סוכרת type 2 וירידה בתפקוד המיני. נדיר ביותר שאדנומות אלה מופיעות בגיל הילדות, אך כאשר מתרחש אירוע כזה, עודף GH גורם לגדילה מוגזמת, שמתייחסים אלה באופן מסורתי כאל ענקוּת היפופיזאלית. עודף GH וכן IGF-1 יכולים לגרום למספר ליקויים מטבוליים כולל היפרגליקמיה. בענקוּת, רמות IGF-1 גבוהות יותר מאלה של GH עצמו.
בדרך כלל נוקטים בגישה ניתוחית להסרת גידולי היפופיזה אלה, אך יש גם הנוקטים בגישה של הקרנות ממוקדות, או שימוש באנטגוניסט של GH כגון pegvisomant הגורם לכיווץ הגידול או לחסום פעילותו. תכשירים אחרים המשמשים לחסום את GH הם האגוניסט של סומטוסטאטין-octerotide, או האגוניסט של דופאמין-bromocriptine, שכן סומטוסטאטין וכן דופאמין יכולים לעכב שחרור GH מושרה על ידי GHRG מההיפופיזה הקדמית.
חסר GH: ההשפעות של חסר בהורמון גדילה משתנות בהתאם לגיל בו החל חסר זה להתבטא. בילדים, פיגור בשגשוג וגובה נמוך הם התסמינים העיקריים של חסר GH, אם כי ייתכנו גם עיוותים מורפולוגיים מולדים. כן עלול להיגרם פיגור בבשלות המינית.
שימוש בהורמון גדילה למטרת שיפור ביצועים אתלטיים או בגישה של anti-aging
בתפקידו כתכשיר בעל פעילות אנבולית, נעשה החל משנות -60 שימוש בהורמון גדילה על ידי מתחרים במקצועות ספורט שונים, שכמובן נאסר על ידי איגודי ספורט בארה"ב ובאירופה. אלא שקושי לגלות נטילת HGH בבדיקות שתן כמקובל עד תחילת שנות ה-2000, מנע אכיפת איסור שימוש זה. החל משנת 2003 ניתן בבדיקות דם להבדיל בין הורמון גדילה אנדוגני לבין תכשיר סינתטי.
ספורטאים בענפי ספורט שונים ניסו טיפול ב-GH לשפר ביצועיהם האתלטיים, אך מחקרים לא הצליחו להוכיח שאכן טיפולים אלה בגברים שיפרו את הישגיהם על המסלול. מחקר מאנשי הרפואה של אוניברסיטת Stanford, שהתפרסם ב-2007 הראה אמנם שמתן GH למטופלים קשישים אך בריאים הגדיל את מסת השרירים ב-2 ק"ג בערך, והפחית את מצבורי השומן בגוף באותו סדר גודל. מחקר זה לא בחן את השפעת הטיפול על צפיפות העצם, רמת כולסטרול, צריכת חמצן מרבית, או כל גורם אחר שיוכל להעיד על שיפור היכולת הגופנית (fitness). לא ברור אם כן, מהי השפעת טיפול זה ברמת עוצמת שרירי הגוף, ומשמעותה התחרותית. יש הסבורים שהשפעת GH היא בהגדלת יכולת השריר לאגור מים מה שמגדיל את משקלו, אך לא בהכרח את מסת השריר.
כיוון שרמות HGH באופן טבעי פוחתות בגיל המתקדם, יש העוסקים בתחום ה-anti-aging שהעריכו שמתן הורמון גדילה עשוי להאט את הידלדלות השרירים, ושיפור החזות הקוסמטית. ההשערה שמא מתן הורמון גדילה לקשישים להגביר חיוניותם לא הוכחה במחקרים קליניים, וה-FDA אינו מאשר טיפולים ב-HG להאטת תהליך ההזדקנות. טענות ש-GH עשוי לשמש להאטת ההזדקנות, המושמעות על ידי הארגון השנוי במחלוקת American Academy of Anti-Aging Medicine, התבססו על מחקר בהיקף מצומצם שהתפרסם ב-NEJM בשנות ה-90, בו טופלו 12 גברים מעל גיל 60 ב-GH. בהשוואה למספר דומה של גברים מטופלי אינבו, נמצאה לכאורה עליה בצפיפות העצם וב"מסה הרזה של הגוף", אך גם בעלי המקר לא טענו בשל המדגם הזעיר שניתן להסיק ממנו ש-GH אמנם גרם לשינויים הנצפים.
פיתוח GH כתרופה
המדען המזוהה ביותר עם זיהוי GH (בשנת 1966), ניקוי ההורמון ולאחר מכן ביצוע הסינתזה של GH בשנת 1970, היה הביוכימאי הסיני Choh Hao Li מ-UCLA. חברת Genentech הייתה הראשונה להכין הורמון גדילה ריקומביננטי לטיפול בבני-אדם בשנת 1981, כאשר קודם לכן נהגו למצות הורמון זה למטרות רפואיות מהיפופיזות שנלקחו מגופות, אך גישה אחרונה זו הופסקה לאחר עדות למספר מקרים מאמצע שנות ה-80 בהם התגלתה מחלת יעקב-קרוצפלד במספר מטופלים שקבלו GH מגופות 15 שנים קודם לכן. כמו כן ניסו חוקרים ממונטריאול עוד בסוף שנות ה-50 להפיק את ההורמון מקופי Rhesus macaque. אך בשנת 1985 הוחל בארה"ב שימוש תקני ב-HGH שסונתז במעבדה, ואושר על ידי ה-FDA לטיפול בילדים קטני קומה מסיבה לא ידועה, או בילדים עם תסמונות Turner או Prader-Willi, באלה עם חסר בהורמון וכן במבוגרים עם תסמונת המעי הדק הקצר, או באלה עם חסר הורמון במקרים נדירים של גידול בהיפופיזה, או בתרחיש של דלדול שרירים בחולי איידס.
נכון לשנת 2005, GH רקומביננטי נמכר בשמות מותג שונים, כגון Nutropin של Genetech, וכן Humatrope של Lilly, כאשר Pfizer משווקת את Genotropin, חברת Novo יצאה עם Norditropin ואילו Merck Serono עומדים מאחורי Saizen. בשנת 2006 אישר ה-FDA גרסה רקומביננטית של HGH בשם המותג Omnitrope של חברת Sandoz.
שימושי off-label של GH
במרוצת השנים נעשו ב-GH שימושים בתרחישים קליניים שונים, שאינם משיקים לטיפול העיקרי המקובל של טיפול בילדים עם פיגור התפתחותי בגובהם. כך לדוגמה יש דיווחים על שימוש ניסויי לטיפול בטרשת נפוצה, להגברת הפחתת משקל במצבי obesity, לטיפול ב-fibromyalgia, באי-ספיקת לב, במחלת קרוהן בקוליטיס כיבית, כמו גם במצבי כוויות. כמו כן נעשה שימוש ב-GH במטופלים עם תסמונת המעי הקצר, כדי להפחית את הדרישה להזנת TPN תוך-ורידית.
שימוש בחקלאות
בארה"ב חוקי לטפל בפרות מפיקות חלב בהורמון גדילה ממקור בקר, אך אין הרשאה לטפל בהורמון זה בפרות שמגדלים לשחיטה כמקור לבשר. שימוש נוסף של הורמון גדילה הגידול חקלאי של בעלי חיים, הוא טיפול של חזירים צעירים עם GH ממקור חזיר, כאשר טיפול זה נמצא כמעודד באופן משמעותי שגשוג רקמה שריר, והפחתת רקמה שומנית בחזירים.
בחינת סטיות ברמת GH
כיוון שלא פשוט להסיק מסקנה קלינית מבדיקה בודדת אקראית של רמת הורמון הצמיחה, שמשתנה כאמור לאורך היממה ועקב מצבים שונים, נהוג לבצע בדיקה לאחר גירוי ההיפופיזה להפריש את ההורמון או דיכוי יכולת ההפרשה שלה. מטופלים עם acromegaly לדוגמה מגיבים באופן פחות מהמקובל להעמסת גלוקוזה. מטופלים עם גידולים בהיפופיזה לעתים קרובות מפרישים GH בתגובה לטיפול ב-TRH או ב-GnRH (הידוע גם כ-LHRH).
אי עליה ברמת GH תבחין האתגר של אינסולין שידוע כ-insulin challenge test וגם כ-insulin tolerance test, הוא המבחן השכיח ביותר לאבחון חסר של GH במבוגרים וגם בילדים קטנים. בבדיקה של מבוגרים מזריקים 0.1 יחידות אינסולין לק"ג משקל, כאשר יעד רמת גלוקוזה אליו מנסים להגיע הוא פחות מ-50 מיליגרם לד"ל. בנבדקים עם יצירה תקינה של GH, תתקבל עליה מהירה בריכוזי GH. בילדים הנבדקים משתמשים בלעתים קרובות שילוב של היפוגליקמיה מושרה על ידי אינסולין וכן מתן L-dopa שפעולתו במערכת העצבים המרכזית להשרות שחרור GH מההיפופיזה.
אינסולין בדרך כלל מוזרק ראשון, ודגימות דם נלקחות בפרקי זמן של 30 דקות למשך 90 דקות להערכת רמת GH. לאחר מכן ניתן תכשיר L-dopa וגם כאן נדגם דם כל 30 דקות למשך 120 דקות. יש לשים לב שהעקה הנגרמת בעקבות נטילת הדם במזרק מהווריד, תיתכן עליה קלה ברמת GH בנקודת זמן הבסיס של תבחיני העמסה אלה. הזמינות הנוכחית של גורם ההפרשה GH-RH מאפשרת הערכה טובה יותר במטופלים עם חסר חד של הורמון הגדילה: מתן GH-RH ומדידת GH שימושיים לגלוי צמיחה מואטת ממקור של ההיפותלמוס. הזרקת אינסולין אמורה להעלות רמת GH מעל 3 ננוגרם למ"ל, כאשר אי-עליה ברמת GH מעידה על חסר בהפרשה של ההורמון.
התבחין המקובל לאבחון הפרשה נמוכה של ההורמון כסיבה לננסות בילדים או לאבחון הפרעה בפעילות בלוטת יותרת המוח הוא תבחין אינסולין (insulin tolerance test): מזריקים 1 יחידת אינסולין, ורמת הורמון הגדילה צריכה לעלות מעל 3ng/ml. חוסר עלייה ברמת ההורמון מציין חוסר הפרשה של ההורמון.
תבחין אחר שהוא פחות מקובל בישראל הוא תבחין ארגינין (arginine test): מזריקים ארגינין ובודקים את העלייה ברמת הורמון הגדילה. ניתן לתת עירוי של ארגינין, או שילוב של עירוי ארגינין ו-GH-RH על פי העדפת הרופא. דגימת דם ראשונה נלקחת בין השעות 0600 ו-0800 להערכת רמת הבסיס של GH. לאחר מכן ניתן עירוי ורידי של ארגינין הנמשך 30 דקות ולאחריו נלקחות 4 דגימות דם בהפרשים של 30 דקות, או לחילופין ניתן עירוי תוך ורידי של GH-RH גם כן למשל 30 דקות, ולאחריו נדגם הדם 4 פעמים בהפרשים של 30 דקות. לצורך תבחין העמסה זה צריך להיות בצום של 10-12 שעות, וכן להגביל פעילות גופנית. יש להימנע משך יום מנטילת תרופות המשפיעות על רמת GH, ויש להיות במנוחה מוחלטת למשך 90 דקות לפני התחלת המבדק.
מבדק אחר על פי אותו עיקרון הוא במתן פומי של clonidine שאף הוא מעודד בדומה לארגינין הפרשת GH מההיפופיזה. מדידת דיכוי GH במתן פומי של גלוקוזה משמשת לאבחון יצירת יתר של GH.
בחינת עודף GH על ידי מבחן דיכוי באמצעות מתן פומי של גלוקוזה (GH suppression test)
התבחין האמין ביותר לאבחון acromegaly מעודף GH במבוגרים, או ענקוּת (gigantism) בילדים, או באלה עם רמה גבוהה של IGF-1, היא על ידי glucose tolerance test. אחרי שתייה של מנת גלוקוזה של 75 גרם, רמת GH צפויה ליפול משמעותית לפחות מ-1 ננוגרם למ"ל תוך שעתיים לאחר קליטת הסוכר. רוב המטופלים עם ייצור עודף של GH יראו רמות GH בנסיוב הגבוהות מ-2 ננוגרם למ"ל לאחר העמסת גלוקוזה.
גורמים המגבירים הפרשת GH
GHRH הפועל על ידי קישור לקולטן של GH, וכן ההורמון ghrelin המופרש מהקיבה מעודד הפרשת GH על ידי קישור לקולטנים של GH בתאים הסומטוטרופיים הידועים כ-secretagogue receptors או GHSR. גם הורמוני מין כאסטרוגנים מעודדים הפרשת GH וכן אנדרוגנים בתקופת הבשלות המינית, המופרשים מהאשכים או מקליפת האדרנל בנקבה. גם קלונידין ו-L-DOPA מגבירים הפרשת GH על ידי שהם מעודדים הפרשת GHRH. היפוגליקמיה מגבירה הפרשת GH בעיכוב שחרור סומטוסטטין. שינה עמוקה, צום ממושך, או פעילות גופנית בעצימות גבוהה מעודדים אף הפרשת GH.
גורמים המעכבים הפרשת GH
GHIH או somatostatin המופרש מהגרעין הפּרי-ונטריקולארי בהיפותלמוס אך גם מהלבלב; גם רמות מוגברות של GH עצמו וכן של IGF-1 בצירקולציה יפעלו במשוב שלילי על ההיפותלמוס וההיפופיזה להפחתת רמת GH; היפרגליקמיה. מצבי השמנת-יתר (obesity) מפחיתים את הפרשת GH, וכן משתבשת בהשמנת-יתר תגובת GH לאינסולין, לארגינין, לשינה או לפעילות גופנית. סיבות נוספות לירידה ברמת GH בפלזמה כוללות גידולים בהיפופיזה או בהיפותלמוס, הקרנות של המוח לטיפול בגידולים אלה, טראומה כתוצאה מפגיעת חבלה מוחית קשה. לעתים עלולה תת-פעילות מולדת להתרחש עקב גידול מסוג craniopharyngioma הלוחץ על ההיפותלמוס או על בלוטת ההיפופיזה וגורם לחסר הורמונאלי זה או אחר.
תרחישים בהם רמת GH בדם מוגברת: ענקוּת ממקור היפופיזאלי, שאת בהיפופיזה, אקרומגליה (עם רמות GH עד 400 ננוגרם למ"ל), ננסות ע"ש Laron (בגין פגם בקולטן ל-GH), במצבי הפרשה אקטופית של GH כגון הממאירויות של הקיבה והריאות), עמידות ל-GH, בתת-תזונה, כשל כליות, צמקת הכבד (cirrhosis), עקה נפשית או גופנית, פעילות גופנית מאומצת, צום ממושך או במצב של anorexia nervosa, שינה עמוקה.
- תרחישים בהם רמת GH בדם מופחתת
hypopituitarism, ננסות ממקור היפופיזאלי, פעילות יתר אדרנו-קורטיקאלית.
אינטראקציות עם תרופות
- תרופות המשפיעות להעלאת רמת GH בדם
חוסמי בטא (atenolol ,metoprolol ,propanolol), ארגינין, היסטמין, אמפטמינים, bromocriptine (בתלות במינון, השפעה חולפת), קורטיקו-טרופינים, אסטרוגנים כגון גלולות למניעת הריון, גלוקגון, אינסולין, דופאמין, levodopa ו-methyldopa, קלונידין (השפעה חולפת), baclofen ,metoclopramide ,methylphenidate ,nalorphine ,guanfacine (השפעה חולפת), metyrapone (במינונים של מעל 6 גרם), עירוי תוך ורידי של ניאצין (בצורת חומצה ניקוטינית או ויטמין B3) וכן vasopressin ו-oxprenolol.
- תרופות המשפיעות להורדת רמת GH בדם
bromocriptine (בתלות במינון, במקרים של acromegaly), קורטיקו-סטרואידים, dihydrotestosterone, גלוקוזה, enothiazines ,pirenzepine ,probucol ,octreotide.
- רמת GH בנוזל מי-שפיר
העלייה ההדרגתית של רמת GH בנוזל מי השפיר במהלך הריון, תואמת היטב את העלייה במסת ההיפופיזה במוחו של העובר ובהתאם תואם את העלייה בריכוז GH בפלזמה שלו, וכן נמצא בניגוד לחוסר השינוי ברמת GH בפלזמה של האם במהלך ההיריון. אמנם, התרחיש הקליני היחיד בו יש דיכוי ברמת GH במי השפיר הוא במקרין הנדירים של עוברים הלוקים ב-anencephaly.
הוראות לביצוע הבדיקה
יש להשתמש במבחנה כימית (פקק אדום או צהוב) ולסרכז בקירור. הנבדק חייב להיות בצום של 8 שעות, ובמנוחה מוחלטת של לפחות 30 דקות לפני נטילת הדם. יש להימנע מעקה נפשית. פלזמה במבחנת ספירת דם (EDTA, פקק סגלגל) נותנת תוצאות נמוכות בשיטות מדידה אחדות. הדגימה יציבה 8 שעות בקירור, ולזמן ארוך יותר בהקפאה. יש לקחת בחשבון שביצוע מדידת GH תוך שבוע לאחר ביצוע radioactive scan יכולה להביא לתוצאה נמוכה כזובה בשיטות מדידה מסוימות.
המידע שבדף זה נכתב על ידי פרופ' בן-עמי סלע, המכון לכימיה פתולוגית, מרכז רפואי שיבא, תל-שומר;
החוג לגנטיקה מולקולארית וביוכימיה, פקולטה לרפואה, אוניברסיטת תל-אביב (יוצר הערך)


 כניסה
כניסה  עקבו אחרינו בפייסבוק
עקבו אחרינו בפייסבוק