הנחיות לטיפול תזונתי בחולי מחלות מעי דלקתיות - התמיכה והטיפול בתוספי תזונה במחלות מעי דלקתיות
הנחיות לטיפול תזונתי בחולי מחלות מעי דלקתיות - נייר עמדה
מאת עמותת עתיד - עמותת הדיאטנים והתזונאים בישראל
|
| |
|---|---|
| הנחיות לטיפול תזונתי בחולי מחלות מעי דלקתיות | |
| |
| האיגוד המפרסם | פורום גסטרו - עמותת עתיד – עמותת הדיאטנים והתזונאים בישראל |
| קישור | באתר העמותה |
| תאריך פרסום | דצמבר 2018 |
| יוצר הערך | וועדת היגוי המסמך |
| ניירות עמדה מתפרסמים ככלי עזר לרופא/ה ואינם באים במקום שיקול דעתו/ה בכל מצב נתון. כל הכתוב בלשון זכר מתייחס לשני המגדרים. | |
לערכים נוספים הקשורים לנושא זה, ראו את דפי הפירושים: – מחלות מעי דלקתיות, תזונה
כללי
למטופלים עם מחלת מעי דלקתית בשלבי המחלה השונים כמו גם בתקופות החיים השונות, קיימים מצבים הדורשים הערכה קלינית וטיפולית לגבי הצורך בטיפול בתוספי תזונה הן כחלק מהתזונה היומית והן כחלק ממצב המחלה והטיפול בה.
חולים במחלות מעי דלקתיות נמצאים בסיכון לחסרים תזונתיים. קיימת שכיחות גבוהה יותר של חסרים של מיקרונוטריאנטים לעומת מאקרונוטריאנטים[1].
כיוון שמחלות אלו מערבות את מערכת העיכול האחראית על עיכול וספיגת המזון, נפוצים מצבי חסר המאפיינים בעיקר מחלת קרוהן, בשל תת-ספיגה, תת-תזונה, אובדן משקל, עליה בדרישות הגוף לנוטריינטים, ובנוסף ישנה אנורקסיה משנית למחלה הגורמת לירידה בצריכת מזון[2][3][4].
היעד הטיפולי בסוגיית התוספים: הגעה/השלמה לרמות תקינות של רכיבים חסרים. יעד זה יכול להיות מושג עבור מרבית רכיבי התזונה והוא בעל השפעה מדידה ומשמעותי תעל בריאות ותפקוד המטופל.
תפקידו של הצוות המטפל: לאתר ולנטר באופן שגרתי הן במצב של מחלה פעילה והן במצב של מחלה לא פעילה אחר חסרים באמצעים השונים (הערכה/אנמנזה תזונתית, בדיקות דם).
הטיפול בתוספים: יש להשלים חסרים באמצעות תזונה ותוספים מתאימים. באם אין אפשרות להשיג צריכה מספקת באמצעות התזונה בלבד, תוסף פומי הוא קו ראשון ופשוט ביותר לתיקון חסרים תזונתיים או באם יש צורך תיסוף אחר (תוך שרירי/תוך ורידי) .
טבלה 4: חסרים תזונתיים שכיחים בחולים עם מחלות מעי דלקתיות
| רכיב תזונה | אוכלוסיות בסיכון | מדד לאבחון |
|---|---|---|
| ויטמין B12 |
|
רמות B12 בפלזמה |
| חומצה פולית |
|
רמות חומצה פולית בפלזמה |
| סידן, |
|
אנמנזה תזונתית (יומית, שבועית, תדירות)
בדיקת צפיפות עצם (DEXA) רמות ויטמין D בפלזמה: |
| אבץ |
|
אין מדד מקובל לאבחון סטטוס של אבץ (רמות אבץ בסרום אינן מדד רגיש)
רמות נמוכות בסרום יכולות להעיד על דלקת וכמו כן מושפע מהיפואלבומינמיה |
| ברזל | UC (Ulcerative Colitis)
שכיחות רבה יותר של אובדנים |
רמות ברזל, פריטין, טרנספרין, יחד עם רמות המוגלובין |
תיסוף במולטיויטמין + מולטימינרל
ממחקרים עולה כי רוב החולים במחלות מעי דלקתיות לא מגיעים ל-(DRI (Dietary Reference Intakes. מחקר חתך בילדים ובני נוער עם מחלות מעי דלקתיות הראה צריכה נמוכה באופן מובהק יחסית ל-(RDA (Recommended Dietary Allowances של סידן (49 אחוזים), ויטמין E (57 אחוזים), מגנזיום (76 אחוזים) ויטמין A (72 אחוזים). הצריכה נמצאה נמוכה גם בהשוואה לצריכה בקרב ילדים בריאים.
במחקר השתתפו גם ילדים שהוזנו בלעדית בפורמולות להזנה אנטרלית (EEN, Exclusive Enteral Nutrition) ונטלו תוספים של מיקרונוטריאנטים. בילדים אלו נצפתה צריכה גבוה של מיקרונוטריאנטים, ברזל וויטמינים מסיסי מים, בהשוואה לילדים ללא IBD (Inflammatory Bowel Disease)[5][6].
מחקר נוסף שבדק צריכת מיקרונוטריאנטים[7] מצא כי בקרב אוכלוסייה של מטופלים בוגרים היה מספר גבוה של אילו שלא הגיעו להמלצה לצריכה יומית מומלצת (RDA), של ויטמין E (62.8 אחוזים), ויטמין D (36.2 אחוזים), סידן (22.9 אחוזים), חומצה פולית (19.1 אחוזים), ברזל (13.3 אחוזים) וויטמין C (10.5 אחוזים). מחקר זה לא כלל משתתפים שהוזנו ב-EEN ואת אלה שנטלו תוספי תזונה.
ניתן להסיק שהצריכה התזונתית של חולים במחלות מעי דלקתיות איננה מספקת את ההמלצה היומית של מיקרונוטריאנטים. מחקרים אלה לא התמקדו בסוגיית הספיגה ולא לקחו בחשבון שגם בצריכה המספקת של המיקרונוטריאנטים עלול להיווצר מחסור בהם עקב ספיגה לא מספקת. מחקרים נוספים הצביעו על רמות נמוכות של ויטמין K המקושרות לחומרת המחלה, ויטמין A בעת האבחון אצל הילדים, ותיאמין[8].
ההמלצה על מולטיויטמין וחינוך המטופל לנטילתם חשובה, כיוון שנמצאה השפעה חיובית לידע בנושא תפקיד המיקרונוטריאנטים על היענות המטופל ונטילת התוסף[9].
- המלצות הוועדה
| המלצה | חוזק ההמלצה | רמת הוכחה |
|---|---|---|
| מומלץ תוסף של 1 כדור/יום קומפלקס מולטיויטמין+מולטימינרל במינון של DRI, עקב אי הגעה לצריכה התואמת קצובה יומית מומלצת למעט במקרים של הזנה בלעדית בפורמולה להזנה אנטרלית | I | B |
| לא ניתן להמליץ על תיסוף במולטיויטמין ומינרל בחולים המקבלים הזנה אנטרלית בלעדית | III | C |
ברזל
בחסר ברזל קיימת המלצה לכלל האוכלוסייה לתיסוף פומי של 60–120 מיליגרם ברזל/יום[10]. דיאטנית לא תמליץ על תוסף ברזל במינון כזה, היות שהוא עולה על ה-UL (Upper Limit) לצריכת ברזל שעומד עד 45 מיליגרם/יום, ולכן מהווה מינון פרמקולוגי עליו ימליץ רופא. לתיסוף פומי מספר חסרונות, במיוחד עבור חולי IBD. תגובות דלקתיות במעי מפחיתות את ספיגת הברזל, ולכן היעילות של התוסף הפומי נמוכה. הברזל שלא נספג מגביר את העקה החמצונית במעי וכך עלול להחמיר את מצב הדלקת. בנוסף, במודלים של חיות נמצא כי תיסוף פומי אינטנסיבי משנה את הרכב חיידקי המעי ואף מגביר קרצינוגנזה[11]. מכאן, שאצל מטופלים עם מחלה פעילה, העדיפות תהיה להזרקת ברזל תוך ורידית. הניסיון של תיקון רמות הברזל באמצעות הזרקה תוך ורידית גבר, עם זאת קיימת אוכלוסייה שרגישה לצורה זאת של מתן הברזל. שימוש בתכשירים חדישים להזרקת הברזל מפחית את הסיכון לתופעת הרגישות[12].
התיסוף הפומי נשאר פתרון לשיקול דעתם של המומחים במקרים של רמת המוגלובין מעל 10 גרם/דציליטר אך פחות מהערכים התקינים או במקרה של רגישות להזרקות[10].
- המלצות הוועדה
| המלצה | חוזק ההמלצה | רמת הוכחה |
|---|---|---|
| מומלץ תוסף ברזל אם קיים חסר | I | A |
| מומלץ מתן ברזל תוך ורידי אם קיימת רמת המוגלובין נמוכה (המוגלובין מתחת ל-10 גרם/דציליטר) במקרים בהם יש חוסר סבילות/רגישות לתוספים פומיים. על ההזרקה ממליץ הרופא המטפל |
I | B |
מומלץ תוסף ברזל פומי ב-2 מקרים:
במקרה זה מי שימליץ על התיסוף יהיה הרופא המטפל עקב המינונים הגבוהים |
I | A |
אבץ
אבץ מהווה קו-פקטור לאנזימים ומייצב את המבנה של חלבונים רבים האחראיים על שעתוק גנים. בחינת סטטוס של אבץ על ידי בדיקת דם תלויה במצב אכילה/צום, מקצבים יומיים, דלקות, היריון, שימוש בגלולות למניעת היריון ועוד[13]. עקב קשיים אלה הדיווח על מחסור באבץ בקרב חולי CD (Crohn's Disease) אינו חד משמעי. מחקרים הראו כי בחולי קרוהן בהפוגה שכיחות רמת אבץ נמוכה (פחות מ-20 מיקרוגרם/ליטר) עומדת על 65 אחוזים[7][13]. מחקר נוסף מצביע על 20.5 אחוזים מהמטופלים, בזמן שבמחלה פעילה דווח על מחסור גבוה יותר[14]. במחקר שעקב 5 שנים אחר ילדים עם מחלת קרוהן שנטלו מולטיויטמין נמצא שהתוסף לא סייע במניעת מחסור באבץ בקרב 37 אחוזים מהילדים, ו-15 אחוזים מהילדים פיתחו מחסור שלא נצפה בתחילת המחקר[15].
אם מתגלות רמות נמוכות של האבץ בפלזמה או סימנים קליניים המצביעים על המחסור, בחולי קרוהן ניתן לתסף באחת הצורות הבאות[13]:
- 310-155 מיליגרם/יום של אבץ גלוקונט (תואם 20–40 מיליגרם אבץ אלמנטלי)
- 176 מיליגרם אבץ סולפט (40 מיליגרם אבץ אלמנטלי) פעם ביום
- 220 מיליגרם/יום אבץ סולפט (50 מיליגרם אבץ אלמנטלי) במנות מחולקות לאורך היום
חשוב ביותר כי התיסוף באבץ יתבצע תוך מעקב, מאחר שמינון יתר עלול לפגוע בספיגה ומטבוליזם של ברזל ונחושת וייתכן גם של סידן.
- המלצות הוועדה
| המלצה | חוזק ההמלצה | רמת הוכחה |
|---|---|---|
| מומלץ תוסף אבץ במינון של 20–40 מיליגרם אבץ אלמנטלי/יום בחולי קרוהן אם נצפית רמה נמוכה של האבץ בפלזמה.
יש לבצע מעקב למניעת אנמיה. |
I | A |
ויטמין D וסידן
ויטמין D: בחולים עם מחלות מעי דלקתיות נצפה מתאם בין רמות ויטמין D וחומרת מחלת המעי[16]. מכאן הועלתה ההשערה כי תיסוף של ויטמין D עשוי לשפר את המצב הקליני של המטופלים. ויטמין D הוא מרכיב חשוב בפעילות מערכת החיסון ובעל השפעה אנטידלקתית[17][18]. מחקרו של Jorgensen[19] הצביע על מגמה של ירידה במספר ההתלקחויות אצל החולים שטופלו בוויטמין D לעומת אלה שטופלו בפלצבו במשך 12 חודשים (13 אחוזים מהמטופלים בקבוצת הטיפול לעומת 23 אחוזים בקבוצת הפלצבו 0.06=p). עם זאת, אף מחקר קליני מבוקר ואקראי לא הציג תוצאה בעלת מובהקות סטטיסטית המראה שתיסוף בוויטמין D אכן משפר את המצב הקליני, משפיע על משך ההתקף או מאריך את תקופת ההפוגה של המטופלים.
על סמך האמור לעיל, אצל חולי מחלת מעי דלקתית מומלץ להקפיד על רמת ויטמין D תקינה בדם, התואמת את הרמה של האוכלוסייה הבריאה, והן לתקנה באמצעות תיסוף ויטמין D אם קיים מחסור עד להגעה לערכים התקינים.
סידן: צריכה מספקת של סידן חשובה למינרליזציה של העצם ושמירה על בריאותה. אף על פי שאין המלצה להימנע מצריכת מוצרי חלב, חלק ניכר מהמטופלים מגביל את צריכתם מסיבות שונות הכוללות חשש מאי סבילות ללקטוז[20][21]. בהתאם לאנמנזה התזונתית, לעיתים קרובות עולה צורך בתיסוף הסידן על מנת להשלים את הפער בין ההמלצה לצריכה הקיימת.
סוגיות הקשורות לוויטמין D וסידן אצל חולים המטופלים בגלוקוקורטיקואידים: גלוקוקורטיקואידים הם גורם סיכון עצמאי לאוסטאופורוזיס[22][23]. Glucocorticoid-Induced Osteoporosis) GIO) הוא אוסטאופורוזיס משני הנפוץ ביותר[24]. תכשירים סטרואידיים גורמים לעליה בסיכון לשברים שהיא תלוית מינון, כאשר סיכון זה עולה בצורה מרבית תוך 3–6 חודשים לאחר תחילת התרפיה[23]. אף על פי שתוצאות המחקרים חלוקות לגבי יכולתו של התיסוף המשותף בוויטמין D וסידן להגן בפני שברים, שני המיקרונוטריינטים אכן חשובים במניעת איבוד מסת העצם וכך הגנה על בריאותה[22] .
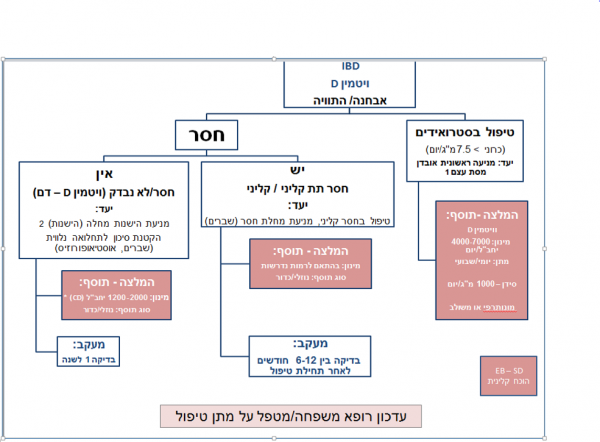
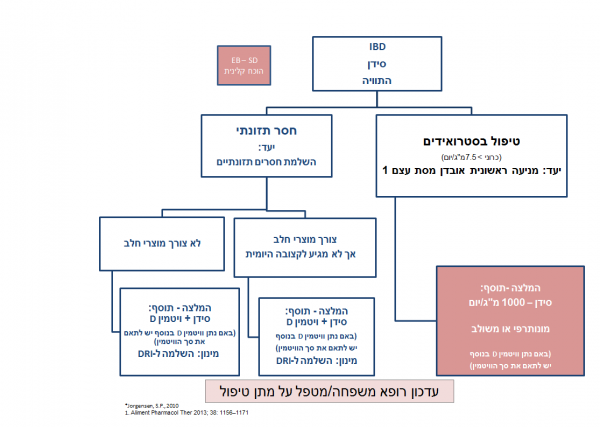
- להלן אלגוריתמים טיפוליים המוצעים על ידי צוות הוועדה לתיסוף ויטמין D וסידן
- ויטמין D–אלגוריתם טיפולי
- חסר בצריכה התזונתית
- חסר תת-קליני/קליני – רמות בדם
- תחלואה: אוסטיאופניה/אוסטיאופורוזיס (מניעה/טיפול)
- טיפול בסטרואידים
- הישנות מחלה – מניעה
- סידן –אלגוריתם טיפולי
התוויות לטיפול:[19]
- צריכה תזונתית לא מספקת
- טיפול בסטרואידים
- תחלואה: אוסטיאופניה/אוסטיאופורוזיס (מניעה/טיפול)
- המלצות הוועדה
| המלצה | חוזק ההמלצה | רמת הוכחה |
|---|---|---|
| מומלץ לנטר שנתית רמות ויטמין D | I | B |
| מומלץ להקפיד על רמת ויטמין D תקינה בדם - Sufficiency - מעל 30 ננוגרם/מיליליטר, ואם קיים מחסור לתסף עד הגעה לערכים התקינים | I | A |
| מומלץ להשלים לצריכת סידן על פי המלצות באמצעות תיסוף את ההפרש בין ההמלצה היומית לצריכה בפועל, בהתבסס על האנמנזה התזונתית.
בהחלטה על ההשלמה, יש לקחת בחשבון את כמות הסידן בקומפלקס מולטיויטמין/מולטימינרל במזון הרפואי – אם ניתן |
B | |
| מומלץ לתסף בסידן+ויטמין D מטופלים אשר נוטלים סטרואידים לתקופה ממושכת (מעל 6 שבועות) (*) | I | A |
(*) להסבר על הסיבות לתיסוף בשימוש בסטרואידים ראו טבלה מספר 4 בסעיף "חסרים תזונתיים שכיחים בחולים עם מחלות מעי דלקתיות"
ויטמין B12
ככלל, רוב המחקרים לא מצביעים על שיעור גבוה של מטופלים המפתחים חסר בוויטמין B12. נמצא שבקרב חולי קרוהן שיעור זה גבוה יותר מאשר בקרב חולי UC. נמצא גם שכריתת אילאום באורך פחות מאשר 20 סנטימטר לא מעלה סיכון לחסר בוויטמין[25].
עם זאת, כאשר בוצעו מדידות סדרתיות אצל המטופלים עם Restorative proctocolectomy שרובם עברו עקב UC[26], נמצא כי רמות הוויטמין B12 יורדות עם הזמן, גם אם לא חוצות את הגבול התחתון של הנורמה. אצל 25 אחוזים מהמטופלים אכן נצפתה רמה נמוכה מהתקינה, כאשר הגבול התחתון של הנורמה במחקר זה נחשב ל-188 פיקוגרם/מיליליטר. מעניין שכשבוצעו מבחני ספיגה (מבחן שילינג) אצל מטופלים אלה, נמצא כי אצל הרוב המוחלט מהמטופלים עם חסר בוויטמין B12, הספיגה הייתה תקינה והם לא הציגו סימני גדילת יתר של חיידקי המעי (Bacterial overgrowth). מכאן, המנגנון המדויק להיווצרות המחסור אינו ברור[26]. ערכי הנורמה לוויטמין B12 שונים ממחקר למחקר, כאשר רוב המחקרים מסתמכים על הגבול התחתון של 140–188 פיקוגרם/מיליליטר ובחלק מהם לוקחים בחשבון גם עליה באחד המרקרים המצביעים על המחסור בוויטמין (חומצה מתילמלונית או הומוציסטאין).
למרות ראיות לשיעור נמוך לחסר בוויטמין B12 אצל חולי IBD, מומלץ לבצע בדיקות תקופתיות של הוויטמין לאיתור חסר בעיקר בחולים במחלת קרוהן של מעי דק סופי וחולים שעברו כריתת איליום סופי. מומלץ מתן של ויטמין B12 בזריקות IM (Intra-Muscular) אם נמצא חסר אצל מטופלים לאחר כריתת אילאום באורך מעל 20 סנטימטר ועמידים לטיפול פומי. יש צורך בהפניה לרופא.
המלצות הוועדה:
| המלצה | חוזק ההמלצה | רמת הוכחה |
|---|---|---|
| מומלץ לנטר שנתית רמות B12 | I | B |
| מומלץ תוסף ויטמין B12 תת-לשוני במינון של 1,000 מיקרוגרם ליממה במקרה ויש חסר בוויטמין, ולמניעה וטיפול במחסור אצל המטופלים שעברו כריתת אילאום | I | B |
| מומלץ מתן IM של ויטמין B12 אם קיים מחסור שאינו ניתן לתיקון על ידי תוסף תת-לשוני. נדרשת הפניית הרופא המטפל | I | B |
חומצה פולית
חולים במחלות מעי דלקתיות נמצאים בסיכון לחסר חומצה פולית, כאשר חולים במחלת קרוהן נמצאים בסיכון גבוה יותר מחולים בקוליטיס כיבית. הסיבה למחסור בפולאט בחולים במחלות מעי דלקתיות נובעת בין היתר מצריכה נמוכה, אובדן במעי ותת ספיגה הנובעת מתחרות עם Sulfasalazine או Methotrexate[8].
במטא-אנליזה משנת 2017[27] שכללה 10 מחקרי מקרה-ביקורת ועוקבה ו-4,517 משתתפים, דווח אפקט מגן של התיסוף בחומצה הפולית בפני סרטן המעי הגס אצל חולים במחלות מעי דלקתיות (HR=0.58, 95% CI 0.37-0.80). המינונים שדווחו במחקרים שנכללו במטא-אנליזה היו לא אחידים (0.4 או 1 מיליגרם/יום), כאשר חלק מהמחקרים התייחסו לעצם התיסוף ולא למינון המדויק. מינון של 0.4 מיליגרם/יום נכלל בהרכב של מולטיוויטמינים רבים, ואם כך העניין, אין צורך בתיסוף נוסף אלא אם מתגלה מחסור בפולאט בבדיקות תקופתיות. את בדיקת הדם עבור פולאט מומלץ לבצע על בסיס שנתי.
- המלצות הוועדה
| המלצה | חוזק ההמלצה | רמת הוכחה |
|---|---|---|
| מומלץ לנטר שנתית רמות חומצה פולית | I | B |
| מומלץ ליטול תוסף חומצה פולית במינון של 5 מיליגרם יום לפני ויום לאחר טיפול ב-Methotrexate (לפי הוראת רופא - לוודא ביצוע) | I | A |
| מומלץ תיסוף במסגרת המולטיויטמין/מולטימינרל והן
מומלץ תוסף חומצה פולית אם קיים מחסור |
I | A |
פרוביוטיקה ופרהביוטיקה
פרוביוטיקה מוגדרת על פי ארגון הבריאות העולמי כ"מיקרואורגניזמים חיים, להם השפעה מיטיבה על המאחסן כאשר ניתנים בכמויות מתאימות". תוספת של חיידקים בעלי תכונות מיטיבות על תפקוד המעי נמצאה יעילה במצבים רבים, כולל קוליטיס כיבית ופאוצ'יטיס.
מחקרים הראו יעילות של /VSL#3 ויומיקס, תערובת פרוביוטית המכילה 8 זני חיידקים (מגיעה באבקה ודורשת קירור), בשמירה על הפוגה בחולים עם קוליטיס כיבית. מטא-אנליזה שפורסמה בשנת 2014 וכללה 5 מחקרים ו-441 משתתפים, סוכם כי /VSL#3 ויוומיקס שיפר תסמינים קליניים והעלה שיעורי הפוגה אצל מטופלים שמקבלים טיפולים ב-5-ASA (5-Amino Salicylic Acid) או אימונומודולטורים[28].
מטא-אנליזה נוספת מאותה שנה[29] בניתוח של תתי קבוצות של מחלת מעי דלקתית שונות הראתה שרק VSL#3 שיפרה את הכניסה להפוגה לעומת פלצבו. בנוסף, היה לה אפקט מגן מהתקפים של פאוצ'יטיס.
זנים בודדים של פרוביוטיקה, כגון E.coli Nissle 1917 או B. longum נוסו ונמצאו יעילים בקוליטיס כיבית, אך מטא-אנליזות לא הצליחו להראות את האפקט שלהם לעומת הפלצבו. בנוגע לזנים הבודדים, יש צורך במחקרים נוספים עם מתודולוגיה חזקה ומספר משתתפים גדול יותר[30]. זני פרוביוטיקה אלה אינם זמינים בישראל.
פרהביוטיקה היא רכיב מזון, בדרך כלל פחמימות שאינן נעכלות, אשר באופן סלקטיבי משפרים גדילה ופעילות של הפרוביוטיקה. צריכת פרהביוטיקה עם פרוביוטיקה יחד מוגדרת כסינביוטיקה. בנוגע לתפקידה של הפרהביוטיקה והסינביוטיקה ב-IBD, פורסמו מחקרים עם ממצאים סותרים. מחקרים אלה בחנו את ההשפעה של Germinated Barley Foodstuff) GBF), FOS ואינולין המועשר באוליגופרוקטוז. המחקרים שבדקו את הפרהביוטיקה והסינביוטיקה הראו הטרוגניות גבוהה מבחינת המבנה והגודל שלהם. חלקם מראים שיפור וחלקם הרעה במצבם של המשתתפים. לא קיימת המלצה לתיסוף בפרהביוטיקה[31].
| המלצה | חוזק ההמלצה | רמת הוכחה |
|---|---|---|
| רצוי לשקול תוסף חיידקים פרוביוטיים מסוג VSL#3/ויוומיקס בחולים עם קוליטיס כיבית בדרגת מחלה קלה-בינונית | IIa | A |
| מומלץ לתסף בחיידקים פרוביוטיים VSL#3/ויוומיקס, 2 מנות ביממה לחולים עם קוליטיס כיבית שעברו IPAA (Ileal Pouch-Anal Anastomosis), לצורך מניעת פאוצ'יטיס | I | A |
| לא ניתן להמליץ על תוסף רכיבים פרהביוטיים בחולי מחלת מעי דלקתית שכן לא הוכחה יעילות של רכיבים פרהביוטיים ב-IBD | III | B |
שמן דגים
שמן דגים מכיל כמות גדולה של חומצות שומן אומגה-3 ארוכות שרשרת, כאשר החשובות ביניהן הן EPA ו-DHA. לחומצות שומן אלה מעורבות בתפקוד תקין של מערכת החיסון ובפעילות נוגדת דלקת. תוצאות המחקרים לגבי השפעתן של EPA ו-DHA במחלות מעי דלקתיות הן סותרות.
מחלת קרוהן: במטא-אנליזה של Cochrane משנת 2014 [32] לא נמצאה יעילות של חומצות שומן אומגה-3 בהארכת הפוגה של חולים במחלת קרוהן. כאשר נכללו המחקרים של EPIC (מחקרים שבחנו אוכלוסייה גדולה של חולי קרוהן), לא נמצאה השפעה גם בהשראת הפוגה.
באחת ממטא-אנליזות[33] שכללה 4 מחקרים, נמצאה השפעה חיובית על הארכת הפוגה רק של שמן דגים בקפסולת Enteric coated ולא במעטפת ג'לטין סטנדרטית. אנליזה של תת-קבוצה של קפסולות ה-Enteric הראתה ירידה בסיכון להתלקחות (RR=0.49, 95%CI 0.35-0.69). עם זאת, מספר המשתתפים במחקרים אלה היה קטן יחסית (166 משתתפים ב-3 מחקרים).
קוליטיס כיבית: אף על פי שמחקרים קטנים מצביעים על שיפור במדדים קליניים, אנדוסקופיים והיסטולוגיים לאחר תיסוף שמן דגים להשראת הפוגה, במטא-אנליזה בתיסוף שמן דגים לעומת הפלצבו, לא נמצא יתרון ואף נמצאה החמרה של תופעות במערכת העיכול העליונה ושלשולים[34].
- המלצות הוועדה
| המלצה | חוזק ההמלצה | רמת הוכחה |
|---|---|---|
| אין להמליץ על תוסף שמן דגים לחולים עם קוליטיס כיבית להשראת הפוגה | III | A |
| אין להמליץ על תוסף של שמן דגים לחולים במחלת קרוהן להארכת הפוגה ולהשראתה | III | A |
כורכומין
כורכומין הוא רכיב של שורש הצמח Curcuma longa אשר משמש כתבלין וצמח מרפא ברפואה האיורוודית והסינית. לכורכומין השפעה נוגדת דלקת, כאשר המסלול הנלמד ביותר הוא דיכוי של הגורם NFkB[35]. פורסמו שני מחקרים קליניים מבוקרים לגבי השפעתו החיובית של כורכומין על חולים עם קוליטיס כיבית.
המחקר הראשון[36] בוצע בחולים עם קוליטיס כיבית בהפוגה הנוטלים Sulfasalazine או Mesalamine. המשתתפים קיבלו 2 גרם כורכומין/יום במשך 6 חודשים (מספר המשתתפים עמד על 43 בקבוצת הכורכומין ו-39 בקבוצת הפלצבו). שיעור המשתתפים שהתלקחו בתקופת המחקר עמד על 4.44 אחוזים בקבוצת הכורכומין ו-15.15 אחוזים בקבוצת הפלצבו.
במחקר נוסף של קבוצה ישראלית[37] נכללו 50 חולים בקוליטיס כיבית בהתלקחות בדרגה קלה-בינונית שלא הגיבו לטיפול במינון מרבי של 5-ASA. המשתתפים חולקו לקבוצת הכורכומין (3 גרם/יום) ופלצבו תוך המשך נטילת 5-ASA. הטיפול ניתן למשך חודש, תקופה בה 53 אחוזים מהמשתתפים בקבוצת הכורכומין נכנסו להפוגה לעומת אף מטופל בקבוצת הפלצבו.
תופעות לוואי שנמצאו במחקרים אלו כללו רגישות במערכת העיכול ועליה במספר היציאות ובחילה, אך הן היו זמניות וחלפו.
- המלצות הוועדה
| המלצה | חוזק ההמלצה | רמת הוכחה |
|---|---|---|
| רצוי לשקול תוסף כורכומין במינון של 2–4 גרם/יום בחולי UC הנוטלים תכשירים מסוג 5-ASA (כגון Sulfasalazine או Mesalamine) הן להשראת הפוגה והן לשמירה על הפוגה | IIa | B |
צמחי מרפא
קיימת גישה טיפולית המשלבת שימוש בצמחי מרפא שונים. נכון לכתיבת נייר עמדה זה ולאחר בחינת המחקרים אשר חקרו השפעות של צמחים אלה על מחלות מעי דלקתיות, ניתן להסיק כי חסרים מחקרים בבני אדם מבוססים במידה מספקת, ולכן לא ניתן לצאת בהמלצות לגבי צמחי מרפא.
ביבליוגרפיה
- ↑ Graham, T.O. and H.M. Kandil, Nutritional factors in inflammatory bowel disease. Gastroenterol Clin North Am, 2002. 31(1): p. 203-18.
- ↑ Brown, A.C., S.D. Rampertab, and G.E. Mullin, Existing dietary guidelines for Crohn's disease and ulcerative colitis. Expert Rev Gastroenterol Hepatol, 2011. 5(3): p. 411-25.
- ↑ Halmos, E.P. and P.R. Gibson, Dietary management of IBD--insights and advice. Nat Rev Gastroenterol Hepatol, 2015. 12(3): p. 133-46.
- ↑ Van Gossum, A., et al., ESPEN Guidelines on Parenteral Nutrition: gastroenterology. Clin Nutr, 2009. 28(4): p. 415-27.
- ↑ Hartman, C., R. Eliakim, and R. Shamir, Nutritional status and nutritional therapy in inflammatory bowel diseases. World J Gastroenterol, 2009. 15(21): p. 2570-8.
- ↑ Hartman, C., et al., Food Intake Adequacy in Children and Adolescents With Inflammatory Bowel Disease. J Pediatr Gastroenterol Nutr, 2016. 63(4): p. 437-44.
- ↑ 7.0 7.1 7 Vagianos, K., et al., Nutrition assessment of patients with inflammatory bowel disease. JPEN J Parenter Enteral Nutr, 2007. 31(4): p. 311-9.
- ↑ 8.0 8.1 Weisshof, R. and I. Chermesh, Micronutrient deficiencies in inflammatory bowel disease. Curr Opin Clin Nutr Metab Care, 2015. 18(6): p. 576-81.
- ↑ Greenley, R.N., et al., Vitamin and mineral supplement adherence in pediatric inflammatory bowel disease. J Pediatr Psychol, 2013. 38(8): p. 883-92.
- ↑ 10.0 10.1 Guagnozzi, D. and A.J. Lucendo, Anemia in inflammatory bowel disease: a neglected issue with relevant effects. World J Gastroenterol, 2014. 20(13): p. 3542-51.
- ↑ Kulnigg, S. and C. Gasche, Systematic review: managing anaemia in Crohn's disease. Aliment Pharmacol Ther, 2006. 24(11-12): p. 1507-23.
- ↑ Auerbach, M. and I. Macdougall, The available intravenous iron formulations: History, efficacy, and toxicology. Hemodial Int, 2017. 21Suppl 1: p. S83-S92.
- ↑ 13.0 13.1 13.2 Kruis, W. and G. Phuong Nguyen, Iron Deficiency, Zinc, Magnesium, Vitamin Deficiencies in Crohn's Disease: Substitute or Not? Dig Dis, 2016. 34(1-2): p. 105-11.
- ↑ Filippi, J., et al., Nutritional deficiencies in patients with Crohn's disease in remission. Inflamm Bowel Dis, 2006. 12(3): p. 185-91.
- ↑ Santucci, N.R., et al., Vitamin and zinc status pretreatment and posttreatment in patients with inflammatory bowel disease. J Pediatr Gastroenterol Nutr, 2014. 59(4): p. 455-7.
- ↑ Garg, M., et al., Association of circulating vitamin D concentrations with intestinal but not systemic inflammation in inflammatory bowel disease. Inflamm Bowel Dis, 2013. 19(12): p. 2634-43.
- ↑ Ardesia, M., G. Ferlazzo, and W. Fries, Vitamin D and inflammatory bowel disease. Biomed Res Int, 2015. 2015: p. 470805.
- ↑ Narula, N. and J.K. Marshall, Management of inflammatory bowel disease with vitamin D: beyond bone health. J Crohns Colitis, 2012. 6(4): p. 397-404.
- ↑ 19.0 19.1 19.2 Jorgensen, S.P., et al., Clinical trial: vitamin D3 treatment in Crohn's disease - a randomized double-blind placebo-controlled study. Aliment Pharmacol Ther, 2010. 32(3): p. 377-83.
- ↑ Munns, C.F., et al., Global Consensus Recommendations on Prevention and Management of Nutritional Rickets. J Clin Endocrinol Metab, 2016. 101(2): p. 394-415.
- ↑ Wagner, C.L., et al., Prevention of rickets and vitamin D deficiency in infants, children, and adolescents. Pediatrics, 2008. 122(5): p. 1142-52.
- ↑ 22.0 22.1 22.2 Fraser, L.A. and J.D. Adachi, Glucocorticoid-induced osteoporosis: treatment update and review. Ther Adv Musculoskelet Dis, 2009. 1(2): p. 71-85.
- ↑ 23.0 23.1 van Staa, T.P., H.G. Leufkens, and C. Cooper, The epidemiology of corticosteroid-induced osteoporosis: a meta-analysis. Osteoporos Int, 2002. 13(10): p. 777-87.
- ↑ Mazziotti, G., et al., Glucocorticoid-induced osteoporosis: an update. Trends Endocrinol Metab, 2006. 17(4): p. 144-9.
- ↑ Battat, R., et al., Vitamin B12 deficiency in inflammatory bowel disease: prevalence, risk factors, evaluation, and management. Inflamm Bowel Dis, 2014. 20(6): p. 1120-8.
- ↑ 26.0 26.1 Coull, D.B., et al., Vitamin B12 deficiency following restorative proctocolectomy. Colorectal Dis, 2007. 9(6): p. 562-6.
- ↑ Burr, N.E., M.A. Hull, and V. Subramanian, Folic Acid Supplementation MayReduce Colorectal Cancer Risk in Patients With Inflammatory Bowel Disease: A Systematic Review and Meta-Analysis. J Clin Gastroenterol, 2017. 51(3): p. 247-253.
- ↑ Mardini, H.E. and A.Y. Grigorian, Probiotic mix VSL#3 is effective adjunctive therapy formild to moderately active ulcerative colitis: a meta-analysis. Inflamm Bowel Dis, 2014. 20(9): p. 1562-7.
- ↑ Shen, J., Z.X. Zuo, and A.P. Mao, Effect of probiotics on inducing remission and maintaining therapy in ulcerative colitis, Crohn's disease, andpouchitis: meta-analysis of randomized controlled trials. Inflamm Bowel Dis, 2014. 20(1): p. 21-35.
- ↑ Jonkers, D., et al., Probiotics in the management of inflammatory bowel disease: a systematic review of intervention studies in adult patients. Drugs, 2012. 72(6): p. 803-23.
- ↑ Matijasic, M., et al., Modulating Composition and Metabolic Activity of the Gut Microbiota in IDB Patients. Int J Mol Sci, 2016. 17(4).
- ↑ Lev-Tzion, R., et al., Omega 3 fatty acids (fish oil) for maintenance of remission inCrohn's disease. Cochrane Database Syst Rev, 2014(2): p. CD006320.
- ↑ Turner, D., et al., Omega 3 fatty acids (fish oil) for maintenance of remission in Crohn's disease. Cochrane Database Syst Rev, 2007(2): p. CD006320.
- ↑ Turner, D., et al., Maintenance of remission in inflammatory bowel disease using omega-3 fatty acids (fish oil): a systematic review and meta-analyses. Inflamm Bowel Dis, 2011. 17(1): p. 336-45.
- ↑ Singh, S. and B.B. Aggarwal, Activation of transcription factor NF-kappa B is suppressed by curcumin (diferuloylmethane) [corrected]. J Biol Chem, 1995. 270(42): p. 24995-5000.
- ↑ Hanai, H., et al., Curcumin maintenance therapy for ulcerative colitis: randomized, multicenter, double-blind, placebo-controlled trial. Clin Gastroenterol Hepatol, 2006. 4(12): p. 1502-6.
- ↑ Lang, A., et al., Curcumin in Combination With Mesalamine Induces Remission in Patients With Mild-to-Moderate Ulcerative Colitis in a Randomized Controlled Trial. Clin Gastroenterol Hepatol, 2015. 13(8): p. 1444-9 e1.


 כניסה
כניסה  עקבו אחרינו בפייסבוק
עקבו אחרינו בפייסבוק