הרחבה טרום-לידתית של אגן הכליה - Prenatal hydronephrosis
| הרחבה טרום-לידתית של אגן הכליה | ||
|---|---|---|
| Prenatal hydronephrosis | ||
| שמות נוספים | הידרוקן הכליה, מיימת הכליה | |
| יוצר הערך | ד"ר לימור פרידנזון-צוק, רועי נדלר, גלית פומרנץ, ד"ר מאיר פומרנץ, פרופ' אבישלום פומרנץ
|
|
לבדיקת העל-קול העוברי (Prenatal ultrasound) יש חשיבות רבה לבריאות האם והעובר. בדיקות אלו גורמות לעומס כלכלי לא מבוטל על מערכת הבריאות, אך הן בעלות חשיבות רפואית בטיפול באם ובעובר במהלך ההיריון ולאחר הלידה.
האיגוד הקנדי לגינקולוגיה ולהיריון ממליץ על בדיקת סקר במהלך ההיריון בשבועות 16-20 לכל הנשים. זמינות השימוש בעל-קול משפרת את היכולת לאבחן ולטפל בעוברים וביילודים הסובלים ממומים מולדים בדרכי השתן. הידרוקן (Hydronephrosis) הוא הרחבה של אגן הכליה והגביעים (Calices). למרות פרסום מאמרים רבים בנושא, אין תמימות דעים לגבי צורת המעקב המומלצת או משכו.
חשוב להכיר את הגורמים השכיחים להרחבת אגן כליה עוברי, לדעת להצביע על הקשר בין הרחבת אגני כליה לתסמונות גנטיות שונות ולהכיר המלצות על דרך הניהול של המקרה במהלך ההיריון כדי להציע נוהל מעקב וטיפול לאחר הלידה.
אפידמיולוגיה
רוב ההפרעות בדרכי השתן מתגלות בעל-קול שגרתי (סקירת מערכות) המבוצע בשבועות 16-20 להיריון. מתוך מומים מולדים אלו הרחבת אגני הכליה היא השכיחה ביותר ושיעורה כ-50% מהמומים המולדים בדרכי השתן. שכיחות הרחבת אגן כליה כפי שמאובחנת בעל-קול עוברי היא 0.59-3% (2,1).
אטיולוגיה
ניתן לחלק את הרחבות אגן הכליה לשתי קבוצות עיקריות: הרחבה מבודדת או הרחבה בנוכחות תסמונת גנטית.
הרחבה מבודדת
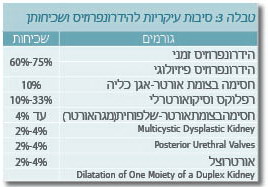
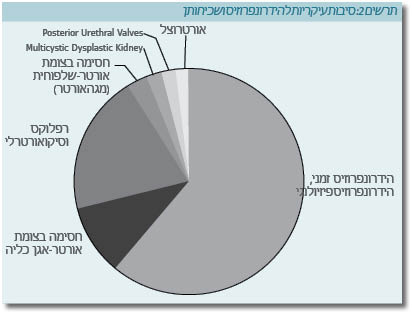
הגורמים השכיחים ביותר להרחבה מבודדת קלה הם הרחבת אגן כליה זמנית או פיזיולוגית (Physiologic). סיבות נוספות הגורמות להרחבה של דרכי השתן הן: חסימות של דרכי השתן ממוצא אגן הכליה ועד לקצה השופכה והחזר שלפוחית-שופכן (VUR, Vesicoureteral Reflux). מעבר לכך, כליה רב כיסתתית דיספלסטית (MCDK, Multicystic Dysplastic Kidney) יכולה לתת תמונה הדומה להרחבה של אגני הכליה (2,1). הסיבות ושכיחותן מסוכמות בטבלה 3 ובתרשים 2.
הגורמים להרחבה טרום-לידתית של אגן הכליה:
- הרחבת אגן כליה זמנית ופיזיולוגית - חולף עצמונית בדרך כלל בשליש השלישי או בילדות המוקדמת. לרוב היילודים יהיה על-קול תקין לאחר הלידה, ללא צורך בהמשך טיפול אנטיביוטי או בירור נוסף
- הרחבת אגן כליה טרום-לידתי מסיבה עלומה (Idiopathic) - אינו קשור במומים כלייתיים. הוא מופיע בשיעורים שונים עד מחצית מהמקרים. הוא בעל פרוגנוזה טובה. הרחבת אגן הכליה אינה קשה, לרוב אינה מערבת את הגביעים, ורקמת-התווך (Parenchyma) הכלייתית תקינה. ברוב המקרים ההרחבה של אגן הכליה תיסוג במהלך השנים הראשונות לחיים (2)
- חסימה בצומת שופכן-אגן כליה (UPJ, Ureteropelvic Junction) - זו החסימה השכיחה ביותר, מאחר שהיא מופיעה בגובה הפיצול הראשון של ניצן השופכן. לרוב החסימה אינה מלאה והיא כוללת היצרות פנימית ולאחריה כיפוף (2). היא מופיעה בעיקר בבנים (יחס 3:1 לעומת בנות). גם בהיעדר אבחנה תוך-רחמית של הפגם, תיתכן תקופה א-תסמינית ארוכה.
בחסימה חד-צדדית של מוצא הכליה יהיו האגן והגביעים מורחבים, ללא הרחבה של השופכנים. מוצא השלפוחית, גודלה ודופנה ייראו תקינים. במצבים חמורים ניתן יהיה לראות מבנה כיסתתי גדול, המורכב מהאגן ומהגביעים והוא עטוף ברקמת-תווך דקה או ללא רקמת-תווך כלל. לא ניתן לצפות בשופכן מתחת לגובה חסימה. בחסימה בצומת שופכן-אגן כליה חד-צדדית, הכליה שאינה פגועה והשלפוחית מתפקדות היטב בדרך כלל ומייצרות כמות תקינה של מי שפיר.
הורמוני האם מרפים שריר חלק גם בעובר, לכן תיתכן החמרה במצב החסימה לאחר הלידה. ברוב המקרים החסימה א-סימטרית. ב-10-30% מהמקרים יש פגיעה דו-צדדית בדרגות שונות. כמו כן, ייתכן מצב של חסימה בכליה אחת ואי-היווצרות של הכליה השנייה. באופן פרדוקסלי (Paradoxical), ב-25% מהמקרים יהיה ריבוי מי שפיר. בחסימה חמורה ניתן לראות הצטברות נוזל סביב הכליה, אורינומה (Urinoma), בשל קרע במערכת המאספת
- החזר שלפוחית-שופכן - לא ניתן לבצע אבחנה סופית של ההחזר בעל-קול טרום-לידתי. עם זאת, הרחבה לא קבועה של אגני כליה במהלך ההיריון או נוכחות של הידרוקן השופכן (Hydroureter) תומכים באבחנה של החזר שלפוחית-שופכן. החזר שלפוחית-שופכן קיים בשכיחות של עד 38% מהילדים, שסבלו מהרחבת שופכנים בתקופה הטרום-לידתית. ניתן לאבחן החזר שופכן ב-42% מהילדים עם הרחבת אגני כליה בתקופה הטרום לידתית וב-25% מהיילודים עם הרחבת אגני כליה טרום-לידתית ועל-קול כליות תקין בתקופה הטרום-לידתית.
Tibballs מדווח על החזר דרגה III-V ב-25% מהיילודים, שלהם הייתה הרחבה של דרכי השתן במהלך ההיריון, ועל-קול תקין בתקופה הטרום-לידתית. השכיחות של החזר בדרגה גבוהה הייתה גבוהה יותר בבנים מאשר בבנות. על-קול לאחר הלידה יכול להיות תקין לחלוטין או להדגים ממצאים לא טיפוסיים (כגון: עיבוי דופן שופכן ואגן הכליה, הרחבת שופכן וגביעים, התקה של זרם השופכן בשלפוחית או הרחבה לסירוגין של המערכת המאספת). בדיקת הבחירה לאבחון החזר הינה ציסטואורתרוגרמה (VCUG, Voiding Cystourethrogram). 56% מההרחבות חולפות תוך שנתיים (2,1)
- חסימה בצומת שופכן-שלפוחית - ניתן לחלקה לשני מצבים:
- בנוכחות מערכת מאספת כפולה - מצב זה שיעורו כ-4% מכלל ההפרעות בדרכי השתן, והוא נגרם מחוסר איחוי של ניצן השופכן. נזק בחלקו העליון של ניצן השופכן יגרום לחסימה ולעתים ליצירת אורטרוצלה (Ureterocele), בליטה של השופכן לתוך שלפוחית השתן. נזק בחלקו התחתון של הניצן יגרום להחזר שלפוחית-שופכן. האבחנה התוך-רחמית לא פשוטה, אך מאפשרת מתן אנטיביוטיקה מונעת ליילוד למניעת זיהום עד התיקון הניתוחי
- שופכן ענק (Megaureter) ראשוני - הרחבת שופכן [מעל 7 מילימטר (מ"מ)] סימטרית (Symmetric) בנוכחות שלפוחית תקינה, ללא החזר. החסימה היא תפקודית ומתאפיינת בהרחבת שופכן, שאינה מתאימה למידת הרחבת אגן הכליה. בדיקת הבחירה היא מיפוי, אך יש צורך בציסטואורתרוגרמה לשלילת החזר. לרוב מדובר במצב שפיר, שאינו פוגע בתפקוד הכליות והוא חולף או מתייצב עצמונית, ללא צורך בניתוח. יש צורך בטיפול אנטיביוטי מונע בשל אחוז הזיהומים הגבוה (2)
- כליה רב כיסתתית דיספלסטית - אינה סיבה להרחבת אגן כליה אלא מום כלייתי, היכול להידמות לכך. הפרעה זו נגרמת, ככל הנראה, מניוון ניצן השוכן בחלקו העליון, שאינו מאפשר ליחידת הכליה (Nephron) להיווצר מהבלסטמה המזונפרית (Mesonephric blastema). הצינורות המאספים מתרחבים למבנים כיסתתיים, בגדלים שונים, בסדר אקראי וללא קשר ביניהם. בין הכיסתות ניתן לראות איים קטנים המהווים את השארית של רקמת-התווך. מאחר שרק לעתים נדירות הפגיעה ביחידות הכליה מוחלטת, נוצר שתן בכמות מזערית, אך מבחינה מעשית מדובר בחוסר תפקוד כלייתי. הכיסתות יכולות לגדול או להיספג, נפח הכליה בתחילה יגדל, אך בהמשך ייתכן שהכליה תעבור לייפת (Fibrosis) והתכנסות. העובר יכול להמשיך לחיות במצב של כליה אחת מתפקדת. במקרים אלו כמות מי השפיר תקינה. בפחות מ-10% מהעוברים תופיע פגיעה גם בכליה השנייה. פגיעה קשה דו-צדדית עם מיעוט מי שפיר ניתנת לגילוי כבר בשבוע 12 להיריון
- שסתום שופכה אחורי (PUV, Posterior Urethral Valve) - גורמת להרחבה חד-צדדית או דו-צדדית. שסתום שופכה אחורי היא האבחנה החשובה מבין הגורמים להרחבה טרום-לידתית של דרכי השתן בעובר זכר והיא דורשת התערבות ניתוחית לאחר הלידה. במקרים נבחרים התערבות ניתוחית באה בחשבון גם במהלך ההיריון. הממצאים בעל-קול טרום-לידתי כוללים הרחבה דו-צדדית של אגני הכליות, עיבוי דופן השלפוחית והרחבה אחורית של השופכה. במקרים הקשים ניתן לראות שינויים ברקמת-התווך של הכליות (כליות דיספלסטיות), מיעוט מי שפיר ונוכחות של אורינומה ומיימת בעובר. כשקיימים הסימנים האופייניים, האבחנה המבדלת כוללת תסמונת חסר שרירי הבטן (Prune belly syndrome) עם או בלי איטמות (Atresia) שופכה, החזר שופכן דרגה V ומומים נוספים באברי מין.
הרגישות והסגוליות באבחון של שסתום שופכה אחורי בעל-קול טרום-לידתי השתפרו והן טובות יותר ממה שדווח בעבר. החסימה תלווה ברוב המקרים בשלפוחית מורחבת בעלת דופן מעובה (במצב תקין עובי דופן השלפוחית הוא עד 2 מ"מ, בשסתום שופכה אחורי עובי הדופן מגיע ל-10 מ"מ ומעלה) עם סימן "חור מפתח" (Key hole) - הרחבה אחורית של השופכה, והרחבה של השופכנים. שלפוחית חסומה יכולה למלא את כל האגן ואף יותר ממנו. בפחות משליש המקרים ההרחבה של אגן הכליה היא חד-צדדית. בבנות עם חסימה במוצא השלפוחית יש לחשוד באיטמות של שופכה עם תסמונת נסיגת עצם-הזנב (Caudal regression syndrome) או בלעדיה. בדיקת הבחירה לאבחון שסתום שופכה אחורי היא ציסטואורתרוגרמה. במחצית מהמקרים יהיה מיעוט מי שפיר ובכ-40% תהיה הרחבה של אגני הכליות. עלייה בלחץ בתוך המערכת המאספת עלול לגרום לנזק ולחוסר התפתחות תקינה של הכליות. הפגיעה הכלייתית יכולה להתבטא במיעוט מי שפיר. במקרים קשים ייתכן קרע עצמוני במערכת השתן והתפתחות אורינומה
הרחבה של המערכת המאספת ותסמונות גנטיות (Aneuploidy)
הרחבת אגן כליה מבודדת נצפית בכ-0.7% מהעוברים בשבועות 16-26 להיריון (13). ממצא זה יכול להיות ממצא בודד ב-2% מכלל העוברים שסובלים מתסמונת דאון (14). זאת אף שההסתברות לתסמונת דאון אינה מוגברת בעוברים עם הרחבת אגן כליה כממצא בודד (14).
קליניקה
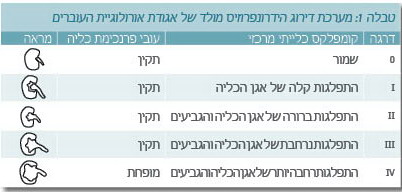
קיימות מספר שיטות סיווג הרחבת אגן הכליה. אגודת אורולוגיית העוברים (Society of fetal urology) פיתחה שיטה לדירוג ההרחבה המתבססת על מראה רקמת-התווך של הכליה, מערכת הגביעים ואגן הכליה בחתך אורכי של הכליה בעל-קול (טבלה 1) (1).
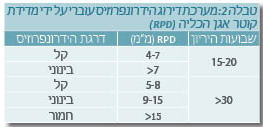
שיטה אחרת מבוססת על מדידת קוטר מירבי קדמי-אחורי של אגן הכליה (RPD, Renal Pelvic Diameter) (טבלה 2). קיימת מחלוקת לגבי קוטר הסף הנחשב לא תקין בעובר, מכיוון שייתכנו שינויים עם שבועות ההיריון, כתלות במצב המיום (Hydration) של האם ואף במהלך בדיקה בודדת כתלות במצב מילוי שלפוחית השתן (2,1). רוב הרופאים מחשיבים קוטר אגן כליה > 6 מ"מ כסמן להרחבת אגן הכליה, המצריך מעקב לאחר הלידה (1).
שיטה נוספת המדרגת הרחבת אגן כליה היא השיטה על שם Onen, המבוססת אף היא על המראה בעל-קול של אגן הכליה, הגביעים ורקמת-התווך (תרשים 1). יתרונה של שיטה זו הוא בהיותה קלה יותר למעקב (3).
שיטת אגודת אורולוגיית העוברים היא המקובלת לשימוש בצפון אמריקה ובישראל, ואילו השיטה המבוססת על מדידת קוטר אגן כליה מירבי שכיחה יותר בשאר העולם (4).
מומים בדרכי השתן המתבטאים במיעוט מי שפיר עלולים להתבטא בתקופה לאחר הלידה ובהמשך החיים כזיהומים חוזרים בדרכי השתן, אי ספיקת כליות ומחלת ריאה כרונית.
אבחנה
הרחבה של המערכת המאספת ואגן הכליה (Pyelectasis) העובריים מוגדרת כמום לידתי. במהלך ההיריון ניתן להעריך את הרחבת אגן הכליה העוברי באמצעות מדידת קוטר מירבי של אגן הכליה. הרחבה קלה של אגן הכליה מתבטאת בעל-קול כאזור היפואקוגני (Hypoechogenic) במבנה עגול או אליפטי (Ellipse) באזור אגן הכליה בקוטר 5-10 מ"מ. קוטר קטן מ-5 מ"מ נחשב כתקין ואינו דורש דיווח. הרחבת אגן הכליה לקוטר גדול מ-10 מ"מ לפני הלידה מוגדרת כהרחבת אגן טרום-לידתי ומצריכה מעקב. כל עובר עם הרחבה של קוטר אגן הכליה מעל 5 מ"מ נדרש למעקב טרום-לידתי. לעוברים עם הרחבה מעל 10 מ"מ מומלץ לבצע על-קול ביקורת בשליש השלישי להיריון.
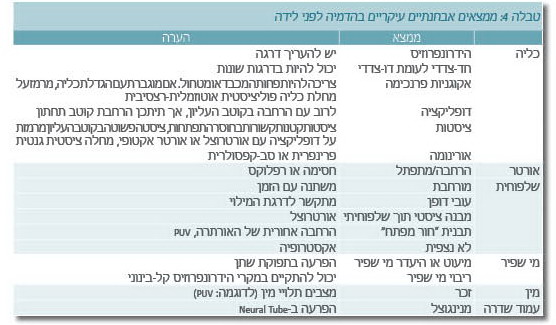
הממצאים העיקריים הניתנים לאבחנה בהדמיה טרום-לידתית מצוינים בטבלה 4. בהתאם למדדים הלו תתבצע ההחלטה לגבי המשך הטיפול - החל במעקב על-קול במהלך ההיריון ו/או לאחר הלידה, דרך התערבות במהלך ההיריון (הכנסת נקז בין שלפוחית השתן של העובר לשק מי השפיר) או לאחריו ועד לסיום מוקדם של ההיריון (4).
במחקר שבוצע על ידי Brunisholz וחברים נמצא, שמומים בשלפוחית השתן והשופכה אובחנו בגיל היריון צעיר יחסית (21.8 שבועות). מומים קריבניים (Proximal) יותר אובחנו בשבוע 27 לערך. מכאן מודגשת חשיבות ביצוע על-קול בשליש שני ושלישי (5). יתר על כן, במטה-אנליזה (Meta-analysis), שבוצעה על ידי Lee וחברים נמצא שיכולת הניבוי לתוצא לאחר הלידה של על-קול טרום-לידה שבוצע בשליש שלישי, הייתה טובה מזו של על-קול שבוצע בשליש שני. עם זאת, בשל חוסר האחידות בדיווח ובנהלים טרום-לידתיים, המחברים התקשו לקבוע אם תזמון העל-קול הטרום-לידתי או אם קיום מעקב על-קול סדרתי בזמן ההיריון השפיעו על התוצא או סיפקו מידע מנבא נוסף (6).
הערכה טרום-לידתית של הרחבת אגן הכליה כוללת מספר מדדים עיקריים:
- מעורבות חד-צדדית לעומת מעורבות דו-צדדית - ברוב המקרים הרחבת אגן כליה היא חד-צדדית. נדיר שמקרים אלו מצריכים התערבות במהלך ההיריון, לנוכח קיום כליה נגדית תקינה המונעת התפתחות של מיעוט מי שפיר. כמו כן, לא הוכח שהתערבות במקרים אלו משפרת את התוצאה (4). הרחבת אגן כליה דו-צדדית מתרחשת ב-17-34% מהמקרים. התערבות נדרשת ברוב המקרים שבהם קיימת חסימה במוצא השלפוחית. הסיבות השכיחות ביותר לחסימה במוצא השלפוחית הן שסתום שופכה אחורי ואיטמות שופכה, אך תועדו גם אורתרוצל חוסם ומקרים של סעיף בשופכה. מקרים אלו מסכנים את חיי העובר ומצריכים מעקב טרום-לידתי הדוק להערכת תפקוד הכליות וכמות מי השפיר (4)
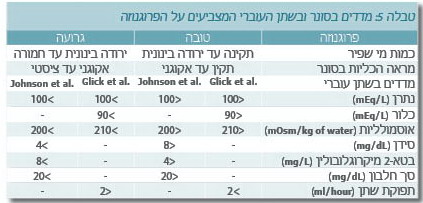
- כמות מי השפיר (תקינה, מיעוט מי שפיר או ריבוי מי שפיר) - כמות מי השפיר היא סמן גס המעיד על התפקוד הכלייתי (טבלה 5). כמות מי שפיר תקינה מעידה על תפקוד כלייתי סביר ומנבאת תפקוד ריאתי תקין לאחר הלידה. מיעוט מי שפיר, לדוגמה, יביא את הבודק לחפש מומים כלייתיים ובדרכי השתן
- חוסר התפתחות כליה בעל-קול (אי היווצרות הכליה)
- הערכת תפקודי כליות עובר לפי מדדים ביוכימיים
- מומים מולדים נלווים והערכת הסיכון למומים כרומוזומליים (Chromosomal)
סמן אחר לתפקוד הכלייתי הוא הגבול קליפה-ליבה (Cortico-medullar) בכליות. היעלמות גבול זה מעידה על ירידה בתפקוד הכליה. נוסף על כך, ממצאים של כליה בעלת אקוגניות (Echogenicity) גבוהה או כיסתות של קליפת הכליה תומכים בהתפתחות לא תקינה של הכליה (2,1).
כאשר קיים מיעוט מי שפיר קיצוני בשלבים הראשונים של ההיריון, נשקפת סכנה לתפקוד הריאתי לאחר הלידה. התערבות טרום-לידתית תישקל במקרים שבהם ניתן לשמר את הכליות. לקיחת דגימת שתן משלפוחית העובר לבדיקת נוכחות חלבונים בשתן [אלבומין ובתא-2-מיקרוגלובולין (β-2 Microglobulin)], אלקטרוליטים (נתרן וכלור) ובדיקת יכולת הריכוז של השתן [אוסמולליות (Osmolality)] עוזרת בקבלת החלטה זו. רמות נמוכות של חלבונים בשתן ותיעוד תפקוד תקין של האבובית (Tubule), המתבטא ברמת נתרן בשתן נמוכה מ-100 מילימול/ליטר, רמת כלור נמוכה מ-90 מילימול/ליטר ואוסמולליות נמוכה מ-210 מיליאוסמולר/ליטר מרמזים כולם על תפקוד כלייתי טוב (1).
- מומים נלווים להרחבת אגן כליה
אף שהרחבת אגן כליה בעובר הוא לרוב זמני ושפיר, יש צורך לחפש בעל-קול מומים נוספים פרט למומים במערכת השתן. במהלך סקירת מערכות בשבועות 16-20 להיריון יש לבחון נוכחות סמנים רכים (Soft markers), כגון הפרעות במבנה המוח העוברי, הפרעות באורך העצמות, חיך שסוע, הפרעות לבביות ועוד. מציאת סמנים, בפרט מסוג גדול (Major), מעלה את הסיכון למציאת מומים גנטיים, אולם היעדרם אינו מלמד על ירידה בסיכון העובר לקיום מחלות גנטיות. יש לשים לב להטעיה חיובית או שלילית שיכולה להשפיע על ניהול הממצאים ומעקב ההיריון (13-10).
ניתן להעריך את הסיכון לתסמונת דאון בעזרת התבחין המשולש, המומלץ לכל אישה בהיריון. התבחין בודק שלושה סמנים בדם האם: חלבון עוברי (α-FP, Alpha Fetoprotein), הורמון אסטריול והורמון בטא גונדוטרופין אנושי (β-HCG, Beta Human Chorionic Gonadotropin), הורמון שמקורו בשליה. בדיקה זו היא בדיקת סקר ואינה מאפשרת אבחנה של תסמונת דאון. היא מעריכה את הסיכון לעובר ללקות בתסמונת זו או במומים במערכת העצבים המרכזית. רמה גבוהה של החלבון העוברי מחשידה למום במערכת העצבים המרכזית. התבחין המשולש מזהה רק כ-60 אחוזים מהמקרים של תסמונת דאון. תוספת סמן רביעי, אינהיבין A (Inhibin A), מעלה בכחמישה אחוזים את הרגישות של הבדיקה לאבחנת תסמונת דאון. קיימות בדיקות נוספות המאפשרות אבחון מוקדם של תסמונת דאון, כגון: שקיפות עורפית וסמנים בסקירת מערכות. כאשר קיימת הרחבה של אגן כליה בעובר, נוכחות של סמנים רכים נוספים בעל-קול טרום לידתי, גיל אם מעל 35 שנים או תוצאת תבחין משולש המעידה על חשד לבעיה כרומוזומלית, כל אלה מחייבים הפניה לייעוץ גנטי. ללא נוכחות גורמי סיכון אלו, הסיכון לתסמונת דאון בנוכחות הרחבת אגן כליה קלה נשאר נמוך ואינו מצדיק המשך בירור גנטי (15).
הרחבת אגן כליה יכול ללוות תסמונות VACTREL (Vertebral anomalies, Anal atresia, Cardiovascular anomalies, Tracheoesophageal fistula, Renal and/or Radial anomalies, Limb defects).
סיכום ההמלצות לבירור מומים נלווים:
- בדיקת כליות העובר היא חלק מבדיקת הסריקה של העובר בשבועות 16-20 להיריון. אם אובחנה הרחבה של אגן הכליה, יש לבצע מדידה קדמית-אחורית של קוטר אגן הכליה בחתך רוחבי (III-B)
- עוברים עם הרחבת אגן כליה של 5 מ"מ ומעלה צריכים לעבור על-קול כליות בתקופה הטרום-לידתית. לעוברים עם הרחבה גדולה מ-10 מ"מ מומלץ על-קול טרום-לידתי בשליש השלישי (II-2A)
- הרחבה קלה בודדת של אגן הכליה אינה דורשת בירור קריוטיפ (Karyotype) (II-2E)
- הפניה לבירור גנטי מומלצת בהרחבת אגן כליה אם יש ממצא פתולוגי נוסף בסקירת העל-קול הטרום-לידתי או במקרים שבהם יש לאם סיכון מוגבר להפרעות כרומוזומליות בעובר, כמו גיל מבוגר של האם או תבחין משולש לא תקין (II-2A)
טיפול
התערבות במהלך ההריון: צנתר תוך רחמי
יש לחשוד בשסתום שופכה אחורי בכל זכר עם תמונה אופיינית המתבטאת בעל-קול בהרחבת אגני כליה דו-צדדית או חד-צדדית, שלפוחית שתן בעלת דופן מעובה עם סימן "חור מפתח" (בשל הרחבה אחורית של השופכה). במקרי שסתום שופכה אחורי, שבהם הוכח קיום של תפקוד כלייתי ניתן לשפר את הפרוגנוזה על ידי ניקוז השתן מהשלפוחית לשק מי השפיר על ידי נקז. ניתן לבצע אנדוסקופיה (Endoscopy) תוך-רחמית להסרת (Ablation) השסתומים במקרים נבחרים בלבד (2). אף שהוכח שיפור של תמונת האלקטרוליטים בשתן, תמונה זו אינה יכולה להעיד תמיד על התפקוד הכלייתי העתידי וב-43% מהמקרים התערבויות תוך-רחמיות גרמו לתמותת העובר (7). סקירה אחרת דיווחה שהכנסת צנתר תוך-רחמי שיפרה את התפקוד הריאתי, אך לא את תפקוד הכליה או השלפוחית (8). ניתוח תוצאות מחמש סדרות גדולות על ידי Coplen מגלה שרידות כוללת של 47% בעוברים שבהם הוכנס צנתר בצורה מוצלחת. סיבת המוות השכיחה הייתה חוסר התפתחות ריאתית (9).
מעקב לאחר הלידה
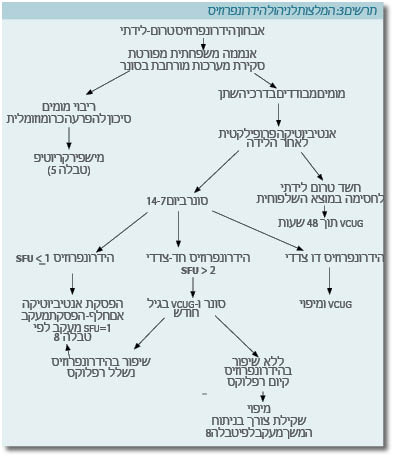
לאחר הלידה, הגישה הטיפולית להרחבת אגן הכליה תלויה בחומרתה בעל-קול, מעורבות חד-צדדית או דו-צדדית, תפקוד הכליות על פי מיפוי וקיום תסמינים. בביצוע סקירת ספרות הודגם כי למרות מאמרים רבים בנושא, לא קיימת תמימות דעים בנוגע לצורת המעקב המומלצת או משכה. תרשים 3 מסכם את ההמלצות מאחד המאמרים למעקב לאחר הלידה.
ברוב המקרים הרחבת אגן כליה טרום-לידתי הוא מצב שפיר וחולף עצמונית ללא פגיעה בתפקוד הכלייתי (3). יתרה מכך, בכ-21-28% מהמקרים שבהם מאובחנת הרחבת אגן כליה לפני הלידה, על-קול לאחר הלידה אינו מדגים הרחבת אגן (4). המחברים השונים מסכימים כי יש צורך בביצוע הדמיה לאחר הלידה הכוללת על-קול ובחלק מהמקרים ציסטוגרפיה (Cystography). במקרים מיוחדים יש צורך גם בביצוע מיפוי או תהודה מגנטית (MRI, Magnetic Resonance Imaging).
בימים הראשונים לאחר הלידה ליילוד תפוקת שתן נמוכה שעלולה ליצור תת-הערכה של חומרת הרחבת אגן הכליה (2,1). אף על פי כן, בסקירה שערכו Yiee ו-Wilcox, הכותבים מציעים שביצוע על-קול בגיל 24-48 שעות הוא מספק. המלצה זו מוסברת בכך שאף שתיתכן החמרה בהרחבת האגן הכלייתי בעל-קול עוקב בגיל 7-10 ימים, ילדים שנזקקו בהמשך לטיפול ניתוחי הדגימו ממצאים בעל-קול בגיל 48 שעות, כך שהחשיבות הקלינית של ממצאי העל-קול בגיל 10 ימים אינה ברורה (4). מחקר אחר השווה על-קול שבוצע ביום 6 לאחר הלידה לעל-קול שבוצע בשבוע 6 לאחר הלידה, ב-100 תינוקות שנמצאו כסובלים מהרחבת אגן כליה בעל-קול טרום-לידתי. במחקר נמצא שעל-קול, שמבוצע ביום 6 לאחר הלידה, אינו רגיש מספיק לשלילת חסימה (16). למרות זאת, רוב המחברים מעדיפים לבצע את העל-קול הבתר-לידתי סביב יום 7-10 לאחר הלידה (3-1).
מומלץ על טיפול אנטיביוטי מונע, בדרך כלל בצפלוספורינים (Cephalosporins) מדור ראשון או ב-Amoxicillin (במינון 10 מיליגרם/קילוגרם/יום) עד לשלילת פתולוגיה משמעותית בדרכי השתן המחייבת טיפול מונע באופן רציף (2,1). אין להשתמש ב-Resprim (TMP-SMX, Trimethoprim/Sulfamethoxazole) ביילודים בגלל השפעתו על משק הבילירובין (1).
יש לבצע ציסטואורתרוגרפיה ב-48 השעות לאחר הלידה ולפני השחרור מבית החולים, בכל יילוד החשוד כסובל מחסימה במוצא השלפוחית (לדוגמה, בשל שסתום שופכה אחורי) לפי על-קול (2,1).
ברוב המקרים שבהם מאובחנת הרחבת אגן כליה חד-צדדית, כמות מי השפיר תקינה וליילוד תפקוד ריאתי תקין.
- במקרים שבהם מאובחנת הרחבת אגן חד-צדדי דרגה I לפי אגודת אורולוגיית העוברים, על-קול תקופתי הוא כל המעקב הנדרש (טבלה 6). רובם המוחלט של המטופלים בקבוצה זו לא יזדקקו לטיפול נוסף (1)
- במקרים שבהם מאובחנת הרחבת אגן כליה חד-צדדית דרגה II-IV לפי אגודת אורולוגיית העוברים, יש צורך בביצוע ציסטואורתרוגרפיה לשלילת החזר. בהיעדר החזר יש לשלול חסימה בדרכי השתן על ידי מיפוי כליות. החזר יודגם בגיל חודש בכשליש מהחולים (1). קיימים חילוקי דעות לגבי ביצוע ציסטואורתרוגרפיה באופן שגרתי. מחקר שבוצע על ידי Ismaili, בחן באופן פרוספקטיבי (Prospective) 264 תינוקות שאובחנו כסובלים מהרחבה טרום-לידתית של אגן הכליה. במחקר זה בתינוקות, שבהם שתי בדיקות על-קול לאחר הלידה היו תקינות, ציסטואורתרוגרפיה הראתה פתולוגיה רק ב-6.7% מהמקרים (17). לעומת זאת, מצאו Aksu וחברים שב-51 מתוך 156 יילודים (33%) שאובחנו לפני לידתם כסובלים מהרחבת אגן הכליה, היה על-קול תקין לאחר 48 שעות. 23 מתוכם (15%) אובחנו כסובלים מהפרעה במערכת השתן בהמשך, בנוכחות על-קול תקין בגיל שבוע. 10 ילדים מתוך ה-23 הדגימו החזר בדרגות שונות או חסימה בצומת שופן-אגן כליה בציסטואורתרוגרפיה או בפיאלוגרפיה תוך-ורידית (IVP, Intravenous Pyelography) בגיל חודש (18). מחקרים רבים שנכללו במטה-אנליזה של Lee וחברים הדגימו שעל-קול תקין לאחר הלידה אינו סמן מהימן לשלילת החזר (6). לנוכח ריבוי המקרים של החזר המתגלים בגיל חודש בנוכחות שתי בדיקות על-קול תקינות, יש לשקול המשך בירור עם ציסטואורתרוגרפיה בגיל חודש ליילודים עם הרחבת אגן בדרגות גבוהות
- התוויות אפשריות נוספות לביצוע ציסטואורתרוגרפיה כוללות:
- הרחבת אגן כליה דו-צדדית
- חשד לחסימה במוצא השלפוחית
- הרחבה של השופכנים
- הרחבת אגן כליה שהולכת ומחמירה
- מערכת מאספת כפולה
- אורטרוצלה
- אקוגניות כלייתית לא תקינה או שלפוחית לא תקינה או בעלת דופן מעובה (4,1)
בדיקת הבחירה להערכת התפקוד הכלייתי ומערכת השתן היא מיפוי המבוצע בגיל 4-6 שבועות. החומר הרדיואקטיבי המועדף הוא MAG3 (99m Technetium Mercaptoacetyl-Triglycine) בשל הקליטה הראשונית הגבוהה שלו בכליה. לחילופין ניתן להשתמש ב-DTPA (99m Technetium Diethyl Triamine Pentaacetic Acid). אם לא נצפית גריפה של החומר בעשרים הדקות הראשונות לאחר ההזרקה, יש להוסיף משתן [על פי רוב Furosemide]. מערכות שתן שאינן חסומות יתנקזו לרוב לאחר שימוש במשתן (2). Kass וחברים הציעו את זמן מחצית החיים של הסמן הרדיואקטיבי כמדד להערכת החסימה. זמן מחצית חיים של פחות מ-10 דקות מצביע על מערכת לא חסומה, זמן מחצית חיים יותר מ-20 דקות מצביע על חסימה ולא ברורה לחלוטין המשמעות של זמן מחצית חיים בין 10 ל-20 דקות (19). למרות האמור, תוצאות המיפוי וזמן מחצית החיים של החומר הרדיואקטיבי תלויים בטכניקת ביצוע הבדיקה, במצב המיום של המטופל, בתפקוד ובאנטומיה הכלייתית. לדוגמה, כליה מורחבת, שאינה מתפקדת היטב, יכולה לתת תמונה של ניקוז פגום, אף שאינה חסומה. תפקוד מבדיל (Differential) מתחת ל-40% או לחילופין פער גדול מ-5% בבדיקות עוקבות במיפוי DTPA או MAG3 הם התוויה לתיקון ניתוחי (2,1). אף שבדיקת המיפוי נחשבת כבדיקה לא פולשנית, יש לזכור כי הבדיקה מצריכה עירוי, צנתור של השלפוחית אם ההרחבה משנית להחזר שופכן וחוסר תזוזת היילוד למשך שעה.
- תהודה מגנטית של מערכת השתן
חוקרים מסוימים נעזרים בתהודה מגנטית של מערכת השתן (MRI-Urography). זו אפשרות חלופית ביילודים עם הרחבת אגן כליה חמורה ותפקוד כלייתי לקוי. חתכי T2 יכולים להעריך הרחבת אגן כליה ולמקם את החסימה. הערכת הפגם התפקודי ועובי רקמת-תווך הכליה מתבצעת בחתכי T1. החיסרון בבדיקה זו הוא צורך בהרדמת הילד לשם ביצוע הבדיקה (1).
טיפול ניתוחי
המלצה על טיפול ניתוחי קיימת במקרים הבאים:
- הרחבת אגן כליה מלווה בשינויים ברקמת-התווך
- החמרה בדרגת הרחבת אגן הכליה בשתי בדיקות על-קול עוקבות
- ירידה בתפקוד כלייתי מבדיל (מתחת ל-40%)
- הידרדרות גדולה מ-5% בתפקוד כלייתי מבדיל
- הרחבת אגן כליה חד-צדדית גדולה (מעל 50 מ"מ)
- הרחבת אגן כליה משמעותית בנוכחות כליה בודדת
- הרחבת אגן כליה דו-צדדית משמעותית (מעל 30 מ"מ)
- נוכחות תסמינים (זיהום מלווה חום, כאב בשל חסימה) (3-1)
בהיעדר אחידות בין המוסדות השונים באשר לנהלים הטיפוליים, קיים פער בשיעור החולים המטופלים ניתוחית. על פי נהלים מסוימים, מומלץ על מעקב בכל החולים בשלב ראשון, ואילו בנהלים אחרים מומלץ על טיפול ניתוחי כבר בשלבים מוקדמים בחלק מהחולים (3).
מחקרים רבים השוו חולים עם אבחנה של הרחבת אגן כליה בדרגות III-IV, שחולקו אקראית לקבוצה שטופלה ניתוחית לעומת קבוצה שטופלה במעקב בלבד. אף על פי שלא נצפו הבדלים משמעותיים בתוצא, כ-25% מהמשתתפים שלא נותחו, נזקקו לתיקון ניתוחי בשנים הראשונות לחיים, על פי רוב בשל החמרה בהרחבת אגן הכליה, ירידה בתפקוד הכליה הנגדית, זיהומים בדרכי השתן או הופעת כאב (2,1).
Chertin וחברים מצאו, שהרחבת אגן כליה דרגה III-IV לפי אגודת אורולוגיית העוברים, מהווה מנבא משמעותי בלתי תלוי לצורך בטיפול ניתוחי. אף שבעבודה זו אין המלצה גורפת לטיפול ניתוחי בדרגות חומרה אלו, הכותבים מציינים כי יש מקום לשקול ביצוע ניתוח כדי לחסוך מעקב ארוך ויקר שבסופו של דבר יוביל לניתוח (21).
ההמלצות למשך המעקב בחולים שאינם מיועדים לניתוח ובחולים לאחר ניתוח שנויות במחלוקת. מחקרו של Onen מתייחס לתקופה גורלית בילדים הסובלים מהרחבת אגן כליה. בתקופה זו (עד גיל 3 שנים) צפויה להתבטא החסימה (3). ילדים שבהם הרחבת האגן הכלייתי השתפרה או חלפה במהלך השנים הראשונות לחיים, לרוב לא יחזרו לסבול מתסמיני הרחבת אגן כליה בהמשך (22,3). כמו כן, בחולים אשר הדגימו ניקוז טוב ושיפור בהרחבת אגן כליה בבדיקות לאחר ניתוח, הישנות חסימה או הידרדרות בתפקוד הכלייתי אינם שכיחים (21,3).
מומלץ לחזור על על-קול חודש לאחר הניתוח, שבו יש לצפות לשיפור קל או להיעדר החמרה. יש לבצע מעקב במיפוי ובעל-קול למשך 3 שנים. שיפור במיפוי נצפה תוך 3 חודשים ממועד הניתוח ובדרך כלל קודם לשיפור שיופיע בעל-קול (3).
הנחיות מפתח
- ביצוע על-קול בשליש שלישי מעלה את הסיכוי לגילוי מומים במערכת השתן
- אם נמצא מום במערכת השתן, יש לשלול מומים במערכות נוספות (לב, חוליות ועוד)
- הרחבת אגן כליה טרום-לידה אינה בהכרח מצביעה על חסימה בדרכי השתן. יש צורך בהדמיה נוספת להכרעה בשאלה זו
- התערבות טרום-לידתית בהרחבת אגן כליה נדרשת במקרים מועטים. גם במקרים שנבחרו בקפידה, ההתערבות שנויה במחלוקת
- אם עולה חשד טרום-לידתי לחסימה במוצא השלפוחית, יש לבצע על-קול וציסטואורתרוגרפיה תוך 48 שעות מהלידה וטרם השחרור מבית החולים
- הדמיה לאחר הלידה צריכה לכלול על-קול (עדיף בימים 7-14 לאחר הלידה) וציסתואורתרוגרפיה בסביבות גיל חודש (לשלילת החזר). במקרי הרחבת אגן כליה משמעותית (דירוג אגודת אורלוגים עובריים > II) או דו-צדדית יש להשלים בירור על ידי מיפוי
- מומלץ לתת טיפול אנטיביוטי מונע (טיפול מונע בדור ראשון של צפלוספורינים או ב-Amoxicillin פומי 10 מיליגרם/קילוגרם/יום) מיד לאחר הלידה ולהמשיך עד לשלילת החזר או פתולוגיה חסימתית אחרת המחייבת טיפול מונע
- קיים קשר חיובי בין דרגת הרחבת אגן הכליה לבין שכיחות פתולוגיה נוספת במערכת השתן. קשר זה לא הוכח עבור החזר
- התוויות לטיפול ניתוחי בהרחבת אגן הכליה כוללות: ירידה בתפקוד מבדיל (מתחת ל-40%), ירידה של יותר מ-5% בתפקוד הכלייתי הבסיסי, החמרה בהרחבת אגן הכליה, הרחבת אגן כליה חמורה (>50 מ"מ), זיהום עם חום או היענות הורים נמוכה למעקב ולטיפול
פרוגנוזה
כרבע מהמקרים שאובחנו לפני הלידה, יחלפו ולא יופיעו בסונר לאחר הלידה. רוב הרחבות אגן הכליה שממשיכות להתבטא גם לאחר הלידה, הן שפירות וחולפות עצמונית, ללא השפעה על התפקוד הכלייתי. קיים יחס הפוך בין דרגת הרחבת אגן הכליה לסיכוי להחלמה עצמונית: רוב המטופלים הסובלים מהרחבת אגן בדרגות I-II ישתפרו' ואילו מחצית בלבד בדרגות III-IV יעשו כן. כ-25% מהמטופלים עם הרחבת אגן משמעותית (קוטר קדמי-אחורי של אגן הכליה >3 ס"מ) יגיעו לתיקון ניתוחי, בסופו של דבר.
מטה-אנליזה שפורסמה על ידי Sidhu וחברים הדגימה שמתוך המטופלים הסובלים מהרחבה של אגן הכליה בדרגה I או II לפי אגודת אורלוגיית העוברים, 98% ישתפרו או יתייצבו ואילו 51% בלבד מהסובלים מהרחבת אגן בדרגות III ו-IV יעשו כן (20). מחקרם של Aksu וחברים מצא יחס הפוך בין דרגת הרחבת האגן לסיכוי להחלמה עצמונית. המחקר הדגים קשר חיובי בין דרגת ההרחבת אגן הכליה לסבירות לניתוח (18).
יילודים בעלי הרחבת אגן כליה טרום-לידתית (בכל דרגה) נמצאים בסיכון מוגבר לנוכחות מומים נוספים במערכת השתן בהשוואה לאוכלוסייה הכללית. במטה-אנליזה של Lee וחברים, נמצא קשר חיובי בין חומרת ההרחבת אגן הכליה ובין השכיחות של פתולוגיה נוספת במערכת השתן. שכיחות פתולוגיה נוספת הייתה 11.9% עבור הרחבת אגן כליה בדרגה קלה, 45.1% עבור הרחבה אגן כליה בדרגה בינונית ו-88.3% עבור הרחבת אגן כליה בדרגה חמורה. לא נמצא קשר בין דרגת הרחבת אגן הכליה לשכיחות החזר. עם זאת, במספר מחקרים קטנים הודגם סיכון מוגבר להחזר ביילודים שבהם נמצא הרחבת אגן כליה בעל-קול טרום-לידתי. מטופלים אלו היו בעלי מהלך שפיר יותר עם החלמה עצמונית באחוזים גבוהים יותר ביחס להחזר שנמצא לאחר מחלת חום (6).
ככל שהרחבת אגן הכליה משמעותית יותר, כך עולה הסיכוי למציאת פתולוגיה נוספת, מחד גיסא, ולצורך בטיפול ניתוחי, מאידך גיסא. יש צורך במעקב סדיר אחר מטופלים אלו כדי למנוע התפתחות פגיעה כלייתית בהמשך. התקווה היא שמחקרים עתידיים ייאפשרו אפיון טוב יותר של אוכלוסיית המטופלים, כך שמעטים יזדקקו למעקב ארוך ומרובה בדיקות.
דגלים אדומים
ביבליוגרפיה
- Belarmino JM, Kogan BA. Management of neonatal hydronephrosis. Early Hum Dev 2006;82(1):9-14
- Hassib N, Iradj A. Antenatal hydronephrosis. J Arab Neonatal Forum 2006;3:33-39
- Onen A. Treatment and outcome of prenatally detected newborn hydronephrosis. J Pediatr Urol 2007;3(6):469-476
- Yiee J, Wilcox D. Management of fetal hydronephrosis. Pediatr Nephrol 2008;23:347-353
- Brunisholz Y, et al. Prenatal diagnosis of urinary malformations: results in a series of 93 consecutive cases. Swiss Med Wkly 2001;131:95-98
- Lee RS, Cendron M, Kinnamon DD, et al. Antenetal hydronephrosis as a predictor of postnatal outcome: a meta-analysis. Pediatrics 2006;118(2):586-593
- Holmes N, Harrison MR, Baskin LS. Fetal surgery for posterior urethral valves: long term postnatal outcomes. Pediatrics 2001;108 (1):E7
- McLorie G, et al. Outcome analysis of vesicoamniotic shunting in a comprehensive population. J Urol 2001;166:1036-1040
- Coplen D. Prenatal intervention for hydronephrosis. J Urol 1997;157:2270-2277
- Langer B, Simeoni U, Montoya Y, et al. Antenataldiagnosis of upper urinary tract dilation by ultrasonography. Fetal Diagn Ther 1996;11:191-198
- Wilson RD, Lynch S, Lessoway VA. Fetal pyelectasis: comparison of postnatal renal pathology with unilateral and bilateral pyelectasis. Prenat Diagn 1997;17:451-455
- Devore GR. Trisomy 21: 91% detection rate using second-trimester ultrasound markers. Ultrasound Obstet Gynecol 2000;16:133-141
- Chudleigh PM, Chitty LS, Pembrey M, et al. The association of aneuploidy and mild fetal pyelectasis in an unselected population: the result of a multicenter study. Ultrasound Obstet Gynecol 2001;17:197-202
- Smith-Bindman R, Hosmer W, Feldstein VA, et al. Second-trimester ultrasound to detect fetuses with Down syndrome. A meta-analysis. JAMA 2001;285:1044-1055
- Aviram R, Pomeranz A, Sharony R, et al. The increase of renal pelvis dilatation in the fetus and its significance. Ultrasound Obstet Gynecol 2000;16:60-62
- Clautice-Engle T, Anderson NG, Allan RB, et al. Diagnosis of obstructive hydronephrosis in infants: comparison sonograms preformed 6 days and 6 weeks after birth. AJR 1995;164:953-967
- Ismaili K, Avni FE, Hall M. Brussels Free University Perinatal Nephrology (BFUPN) study group, Results of systematic voiding cystourethrography in infants with antenatally diagnosed renal pelvis dilatation. J Pediatr 2002;141:21-24
- Aksu N, et al. Postnatal management of infants with antenatally detected hydronephrosis. Pediatr Nephrol 2005;20:1253-1259
- Kass EJ, Majd M, Belman AB. Comparison of the diuretic renogram and the pressure perfusion study in children. J Urol 1985;134:92-96
- Sidhu G, Beyene J, Rosenblum ND. Pediatr Nephrol 2006;21:218-224
- Chertin B, et al. Conservative treatment of reteropelvic junction obstruction in children with antenatal diagnosis of hydronephrosis: lessons learned after 16 years of follow-up. Eur Urol 2006;49:734-739
- Ulman I, Jayanthi VR, Koff SA. The long term follow up of newborns with severe unilateral hydronephrosis initially treated non-operatively. J Urol 2000;164:1101-1105
קישורים חיצוניים
- הגישה להרחבה טרום-לידתית של אגן הכליה, מדיקל מדיה
המידע שבדף זה נכתב על ידי ד"ר לימור פרידנזון-צוק, רועי נדלר, גלית פומרנץ, ד"ר מאיר פומרנץ, פרופ' אבישלום פומרנץ; היחידה למחלות כליה ויתר לחץ דם בילדים ומחלקת נשים, מרכז רפואי מאיר, כפר סבא


 כניסה
כניסה  עקבו אחרינו בפייסבוק
עקבו אחרינו בפייסבוק