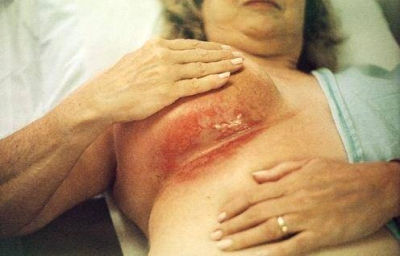
טיפול קרינתי בסרטן השד - Radiation therapy for breast cancer
עקרונות בכירורגיה
מאת ד"ר צבי קויפמן
| עקרונות בכירורגיה | ||
|---|---|---|
| ||
| שם המחבר | ד"ר צבי קויפמן | |
| שם הפרק | כירורגיה של השד | |
לערכים נוספים הקשורים לנושא זה, ראו את דפי הפירושים: – סרטן השד, טיפול בקרינה
טיפול בקרינה בסרטן השד תואר לראשונה כבר בראשית המאה העשרים, מאז הלך והתפתח הטיפול הקרינתי בסרטן השד. כיום, הוא ניתן על-ידי מכשור מתוחכם ולאחר תכנון באמצעות מערכת מחשוב מתקדמת. הגישה הטיפולית בסרטן השד הראשוני כוללת השגת בקרה מקומית באמצעות כריתת השד כולו או חלקו בשילוב טיפול קרינתי משלים, וטיפול מערכתי בגרורות זעירות באמצעות כימותרפיה או תרופות אנטי-הורמונליות.
שיעורי ההישנות המקומיות בחולות שעברו כריתה משמרת שד שלא עברו טיפול קרינתי הוא 25%-30% לעשר שנים, לעומת 41%-7% בחולות שקיבלו קרינה בעבודות מבוקרות. במספר עבודות אותרו גורמי סיכון להישנות מקומית של המחלה: גיל מתחת ל-35, שולי כריתה נגועים, חדירת תאי גידול לכלי דם ולימפה (Lymphovascular invasion, LVI) וריבוי מוקדים של שאת תוך צינורית (DCIS). הקרינה המקובלת ניתנת במינון של 5000-4500 cGy, במקטעים יומיים של 2-1.8 Gy, חמישה ימים בשבוע במשך חמישה שבועות. קודם למתן הקרינה תעבור החולה סימולציה ממוחשבת המאפשרת מתן קרינה ממוקדת לשד עם חשיפה מקטנית (מינימלית) של הריאות והלב. הקרינה ניתנת לשד באמצעות שתי אלומות פוטונים משיקות, המופקות במאיץ קווי באנרגיה 4-6 MV. לאחר הקרנת כל השד, מקובל לתת תוספת קרינה בשדה קטן למיטת השאת (Boost). נושא מתן Boosts שנוי במחלוקת. בעבודה מבוקרת של קבוצת ה-EORTC האירופית שכללה מעל 5000 חולות נמצא כי היה יתרון במתן קרינה למיטת השאת בעיקר בחולות צעירות מגיל 40 בהן נצפתה הפחתה בהישנות המקומית מ- 20% לכ-10% . בחולות שגילן מעל 50 מתן Boosts הפחית את שיעורי החזרה המקומית מ-1.5% ל-3% - שינוי מזערי. את ה-Boosts ניתן לתת על ידי קרן אלקטרונים או באמצעות ברכיתרפיה.
במספר מרכזים בעולם הצטבר ניסיון רב במתן טיפול מקומי למיטת השאת על ידי החדרת "מחטים רדיואקטיביות" למיטת השאת - High dose rate brachytherapy. טיפול זה יכול להינתן באופן אמבולטורי והוא עדיף על קרינת אלקטרונים בחולות עם שד גדול ושאת הממוקמת בעומק השד, עקב מגבלות בכושר החדירה של הקרינה ובגלל מנות הקרינה הגבוהות יחסית המתקבלות בעור.
שיטת טיפול אחרת בקרינה היא קרינה תוך ניתוחית חד פעמית, במנת קרינה גבוהה. בשיטה זו מקרינים רק את מיטת הגידול וסביבתו בזמן הניתוח. לאחר כריתת השאת, החולה בעודה רדומה מקבלת קרינה ממוקדת לתוך מיטת השאת על-ידי אלקטרודה המותאמת לגודל החלל שיצרה הלמפקטומיה. הפצע נסגר זמנית מעל האלקטרודה, הקרינה ניתנת ולאחר סיום הטיפול הקרינתי הפצע נסגר סופית. שיטה אחרת למתן קרינה מקומית היא הכנסה של צנתר מיוחד עם בלון בקצהו המותאם לגודל חלל הלמפקטומיה. הצנתר מוכנס דרך פתח נפרד בעור, כאשר העור מעל הבלון נסגר בשיטה המקובלת. לאחר כשבועיים מהניתוח, הצנתר מחובר למכשיר הקרינה והחולה מקבלת במשך שבוע ימים פעמים ביום את כל מנת הקרינה הנדרשת. בתום הקרינה הצנתר נשלף. הבסיס לגישה זו, של מתן קרינה למיטת השאת ולסביבתה הקרובה, מבוסס על התצפית שרוב החזרות המקומיות מתרחשות בסביבת הלמפקטומיה.
לטיפול הקרינתי יש תופעות לוואי וסיבוכים מאוחרים (תמונה 60.12). הסיבוכים המאוחרים כוללים: בצקת של היד, הפרעות בתפקוד הכתף, פגיעה במקלעת העצבים הברכיאלית, שברים בצלעות, דלקת ריאות קרינתית, מחלת לב איסכמית, קיפוח קוסמטי והופעת שאתות ממאירות מושרות קרינה.
קיימת שאלה לגבי התזמון המיטבי של הטיפול הקרינתי והטיפול הכימי. באופן תיאורטי, ככל שרב הזמן החולף בין הניתוח לתחילת הטיפול בהקרנות כך עלולה לגדול הסכנה להישנות מקומית. באותה מידה, דחיית הטיפול הכימי עד לסיום ההקרנות עלולה להקטין את יעילותו של טיפול זה במניעת גרורות מערכתיות. מכיוון שגרורות מערכתיות הן מסכנות חיים ופחות מחלה מקומית, נוהגים כיום לתת קודם טיפול כימי ולאחר מכן קרינה.
הקרינה גורעת בהתייחס לתוצאות הקוסמטיות. לא תמיד קל להפריד בין פגיעה קוסמטית שמקורה בניתוח לבין פגיעה שמקורה בקרינה.
שיעור ההישנות המקומית לאחר כריתה משמרת שד עקב שאת ממארת תוך צינורית (DCIS) היא 20%-10%, ומרבית ההישנויות מתפתחות לא לפני שנה וחצי ממועד הניתוח. כמחצית מהשאתות הנשנות הן בצורת סרטן חודרני. שתי קבוצות מחקר, v-NSABP האמריקאית ו-EORTC האירופאית, השוו קבוצה שנבחרה באופן אקראי ושעברה כריתה משמרת שד עם קרינה לקבוצה דומה ללא קרינה. הם דווחו על הישנות מקומית בשיעור של 72% בקבוצה ללא קרינה במעקב של שמונה שנים, לעומת 12% בחולות שהוקרנו. נמצאו מספר גורמי סיכון להישנות השאת התוך צינורית: גודל השאת, דרגת ההתמיינות, נמק תוך צינורי ורוחב השוליים. יש הטוענים שבגידולים קטנים בדרגת התמיינות טובה עם שוליים של 1 ס"מ לפחות ניתן להימנע מקרינה.
הטיפול הקרינתי לאחר כריתת שד הפך למקובל בתנאים מסויימים עם פרסומם של שני מחקרים מבוקרים - האחד מדנמרק והשני מקנדה. בשני מחקרים אלה דווח על הקטנה משמעותית בהישנות המקומית בחולות שהוקרנו לעומת חולות שלא הוקרנו וסיכויי ההישרדות גדלו בכ-10% לעשר שנים. תוצאות אלה מובהקות בחולות עם ארבע ויותר בלוטות נגועות בבית השחי, או כאשר קוטר השאת עולה על 5 ס"מ. חולות אלה מקבלות קרינה באמצעות אלומות פוטונים משיקות במנה של 50 GY ב-25 מקטעים יומיים לבית החזה ובית השחי. בחולות עם ארבע בלוטות נגועות ויותר, מוסיפים קרינה לבלוטות העל-בריחיות ולפסגת בית השחי. הקרנת שרשרת בלוטות הלימפה של ה-Internal mammary שנויה במחלוקת. מחקרים שונים מדווחים על תוצאות שונות הנעות מיעילות הטיפול ועד חוסר יתרון לקבוצה המטופלת.
ראו גם
- לנושא הקודם: שאתות ממאירות לא פולשניות - (Non-invasive breast cancer - (LCIS ,DCIS
- לנושא הבא: הטיפול הכימי וההורמונלי בסרטן השד - Chemotherapy and hormonal therapy for breast cancer
- לתוכן העניינים של הפרק
- לתוכן העניינים של הספר
- לפרק הקודם: כירורגיה של הטחול
- לפרק הבא: בקעים
המידע שבדף זה נכתב על ידי ד"ר צבי קויפמן, מומחה בכירורגיה, מנהל היחידה לבריאות השד, מרכז רפואי מאיר, כפר סבא


 כניסה
כניסה  עקבו אחרינו בפייסבוק
עקבו אחרינו בפייסבוק