טיפול קרינתי משלים בסרטן השד - Adjuvant radiotherapy for breast cancer
| טיפול קרינתי משלים בסרטן השד | ||
|---|---|---|
| Adjuvant radiotherapy for breast cancer | ||
| 250px | ||
| יוצר הערך | ד"ר מירב עקיבא-בן דוד | |
לערכים נוספים הקשורים לנושא זה, ראו את דפי הפירושים: – סרטן השד, טיפול בקרינה
קרינה משלימה לשד מהווה גורם משמעותי בתהליך הריפוי בקרב נשים שחלו בסרטן השד. על פי נתונים סטטיסטיים, מתן הקרינה מפחית את הסיכון לחזרת המחלה - בין אם מדובר במחלה מקומית או במחלה מרוחקת - ואף מפחית את התמותה מסרטן שד.
שינויים רבים חלו בתחום הקרינה לשד - עדכון מרבית המאיצים הקוויים בישראל, שינויים בפרוטוקולים הקרינתיים ובמשך זמן מתן הקרינה, חידושים לגבי שדות הקרינה וכן פרסום מחקרים המתייחסים לצורך בקרינה לבלוטות לימפה בשרשרת האינטרנל-ממרית (IMNs, Internal Mammary Nodes).
תהליך מתן הקרינה ותכנונו מתחיל בביצוע בדיקת CT (Computed Tomography) במטרה לראות את האנטומיה של המטופלת, את האיברים השונים ומיקומם כמו הלב, הריאות וכדומה, בהתאמה לשד המטופל. לכל מטופלת מתוכננת תכנית קרינה אישית, המותאמת למחלתה, לממדי גופה ולמצבה הכללי. הטיפול הקרינתי בחדר הטיפולים קצר ונמשך מספר דקות בלבד. במהלך הקרינה המטופלת אינה חשה בדבר. לאחר הטיפול היא יכולה לנהוג ברכב, ולחזור לשגרת חייה. היא אינה מעבירה קרינה לסובבים אותה, ויכולה לשהות במחיצת מבוגרים וילדים קטנים. קרינה לשד ניתנת מדי יום, למספר שבועות. תופעות הלוואי הנפוצות לאחר קרינה הן עייפות ואודם על פני שדות הטיפול.
הודות להתקדמות המדע, ניתן לרפא את מרבית הנשים שלקו בסרטן השד. מסיבה זו נדרשת התייחסות מיוחדת לתופעות הלוואי לטווח ארוך, הנגרמות ממתן הקרינה ועלולות לפגוע באיברים חיוניים, בהם הלב. בשיטות הקרינה הנהוגות, הלב נחסם משדה הקרינה ואינו מקבל קרינה ישירה במהלך הטיפול. משום כך, הסיכון ללקות במחלת לב (כלילית או אי ספיקת לב) כתוצאה מהקרינה נמוך ביותר. לעיתים, יש לנקוט בטכניקות מתקדמות כדי להגן על הלב.
קרינה לאחר ניתוח משמר שד
מתן קרינה משלימה (Adjuvant) לטיפול בסרטן שד מקומי-אזורי (Local-Locally Advanced) לאחר ניתוח משמר שד (Lumpectomy) מפחית את שיעורי החזרה המקומית ומשפר את הישרדות החולה. המטופלות מופנות לאחד ממרכזי הקרינה במכונים האונקולוגיים ברחבי הארץ ומקבלות (בדרך כלל) פרוטוקול קרינה הנמשך 6-7 שבועות.
בתחילת המאה ה-21 פורסמו מחקרים נרחבים המשווים פרוטוקול טיפולי ארוך של חמישה שבועות מול פרוטוקול טיפולי מקוצר של שלושה שבועות, אצל נשים עם ממאירות שד בשלב מוקדם. מחקרים אלה נערכו בקנדה ובאנגליה, ובמהלכם נערך מעקב אחר המטופלות במשך עשר שנים. המחקרים מראים שאין הבדל באחוזי החזרה המקומית של המחלה בהשוואה בין שתי צורות הטיפול. במעקב שנמשך עשר שנים בקרב כ-4,400 נשים, אחוזי החזרה המקומית אחרי קרינה היו בודדים, ונעו בטווח שבין 4.3% ל-8.8% בלבד. תוצאה זו הייתה נכונה לגידולים בכל סטטוס הורמונלי, בכל הגילאים ולכל דרגה (Grade). יתרה מזאת, נמצא כי אין הבדל בתוצאה הקוסמטית בין השיטות לאורך זמן[1].
שיטת הטיפול הקצר נהוגה במספר מכונים בישראל וניתנת כאשר מדובר בקרינה לשד אחד בלבד, ללא מתן קרינה לאזורי הניקוז הלימפטי: Supraclavicular ו-Axila. נראה כי לאור השיפור בשיטות הקרינה והחישוב התלת מימדי, מתן קרינה מקוצרת אינו גורם לתופעות לוואי חריפות (Acute) קשות יותר מאלו הנגרמות על ידי הפרוטוקול הרגיל, ונשמרת צורת השד, כפי שנצפה לאחר מעקב של עשר שנים.
לשיטה זו מספר יתרונות: לנשים המקבלות טיפול מקוצר, נחסכים לפחות שבועיים של טיפול קרינתי הכרוכים בהגעה יומית לבית חולים, כמו גם שיפור משמעותי באיכות חייהן, עם שמירה על תוצאות אונקולוגיות מעולות. רבים מבתי החולים בישראל עברו לטיפול בשיטה מקוצרת לפיה מקבלת המטופלת 15 או 16 פרקציות קרינה לכל השד בגידולים ממוקמים, שאינם כוללים טיפול קרינתי לאזורי הניקוז הלימפטי. מתן פרקציות גבוהות (כמו בטיפול הקרינתי המקוצר - 2.67Gy בכל פרקציה) לאזורי הניקוז הלימפטי כוללים גם מתן קרינה לכלי דם גדולים כמו העורק התת בריחי (Subclavian) ועורק התרדמה (Carotid). במצבים אלה מתעורר החשש ממתן קרינה במנות גבוהות לכלי דם חשובים, לאור המידע שהתקבל ממעקב ארוך טווח על מטופלים שקבלו קרינה למחלת הודג'קין (Hodgkin) (לאזורים צוואריים לדוגמה) עם פגיעה באדוונטיציה (Adventitia) לאורך שנים.
קרינה לשד שמאל
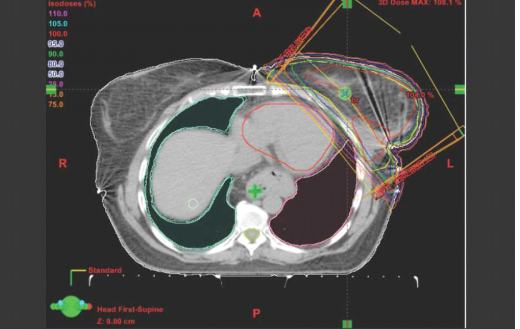
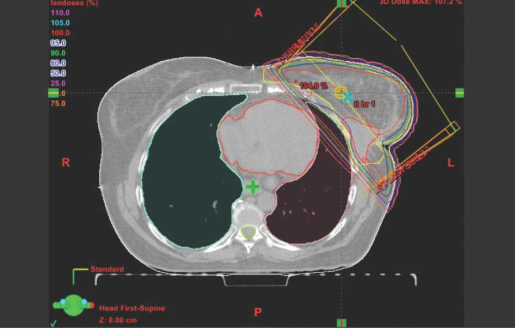
ניתן לרפא חלק ניכר מהנשים שלקו בסרטן שד, מבלי לפגוע בלב כתוצאה מהקרינה. עם זאת, לעיתים, כתוצאה מהתלות באנטומיה (תמונה מספר 1). היות שהלב נמצא במיקום קדמי (Anterior), מתן קרינה לשד ולמיקום הגידול המקורי מבלי להקרין חלק מהלב הוא בלתי אפשרי. במקרים כאלה יש לנסות לדחוק את הלב אחורנית (Posterior) ולהרחיקו מדופן בית החזה באמצעות נשימה עמוקה, שיכולה להזיזו משדה הטיפול למרחק של סנטימטר (ס"מ) וחצי לאחור, ולהוות חייץ המגן עליו (תמונה מספר 2).
הבעיה נעוצה בכך שאף מטופלת אינה יכולה לעצור את נשימתה לדקה - הזמן הנדרש למתן שדה קרינה. מסיבה זו יש לסנכרן בין מתן הקרינה במאיץ הקווי לבין נשימותיה של המטופלת, ולתת את הקרינה עצמה רק בפאזת השאיפה (Inspirium) העמוקה. מערכת כזו, המסנכרנת בין תנועות הנשימה לקרינה עצמה, נמצאת כיום (נכון לשנת 2015) במספר בתי חולים בארץ ואין ספק כי השימוש בה משפר את האפשרות לתת לחולות טיפול מיטבי ללא פגיעה בלב. מערכת זו נקראת RPM (Real time Position Management) והיא אחראית על מתן הקרינה בזמן השאיפה בלבד, כדי לוודא מיקום מרוחק של הלב מאזור הקרינה. המטופלת נדרשת לשתף פעולה, להבין את הנדרש ממנה ולנשום לפי הוראות המחשב, כדי שניתן יהיה להקרין את האזור בפאזת הנשימה הבטוחה.
במרכז רפואי ע"ש חיים שיבא, תל השומר, טופלו עד שנת 2015, 230 נשים בטכניקה זו בהצלחה. מתוך 260 נשים שביצעו בדיקת CT במטרה לבדוק אם ניתן לטפל בהן בשיטת RPM, ל-25 מהן לא נמצא יתרון בביצוע הטיפול הקרינתי בשאיפה [קרום הלב (Pericard) צמוד לדופן בית החזה הקדמי], וחמש נשים לא הצליחו לשתף פעולה ולבצע את הוראות הנשימה בתזמון הנדרש.
עם זאת, במחקר שנערך בשיבא, בהשוואה בין תכניות טיפול עם ובלי RPM, נמצא הבדל ברור ומובהק סטטיסטית לטובת שיטת RPM, לפיה רוב נפח השדיים עובר הקרנה מבלי לוותר על חלקו המדיאלי, בשל מיקום הלב. כמו כן, נמצא שיפור חד-משמעי בנפח הלב שקיבל קרינה מועטה בלבד, בשתי הטכניקות[2].
קרינה חלקית לשד - APBI - Accelerated Partial Breast Irradiation
ערך מורחב – טיפול קרינתי מואץ וממוזער בסרטן השד - Accelerated partial breast irradiation
במקרים בהם אובחנה ממאירות בשד ובבדיקת ה-Axila אין עדות להמצאות מחלה בבלוטות אקסילריות, נפח הקרינה המיועד למטופלת כולל את השד בלבד. רוב החזרות המקומיות (מעל 90%) נצפות בצמידות לאזור הכריתה המשמרת שד המקורית. בהקשר לכך עולות מספר שאלות: האם ניתן לחסוך קרינה לכל השד ולהתמקד רק במתן קרינה חלקית לאזור הגידול בלבד (Partial breast irradiation), האם ניתן, למשל, לקצר את משך הקרינה בצורה משמעותית ל-10 פרקציות שיינתנו פעמיים ביום, לשבוע אחד, או לחילופין לתת פרקציה בודדת במהלך הניתוח? המשמעות של טיפול זה, הנו מתן קרינה במנות גדולות ובזמן קצר, בטכניקה המכונה APBI (Accelerated Partial Breast Irradiation).
בכל המחקרים הרנדומליים הנרחבים המודרניים, בהם נדונה הסוגיה העוסקת בקרינה חלקית לשד, הוגדרו קריטריונים המתייחסים לאוכלוסיית היעד דהיינו, למי אפשר לתת קרינה לנפח חלקי של השד. בקבוצה זו נכללו נשים לאחר סיום הווסת (Postmenopausal), שהגידול שלהן הוסר בגבולות שליליים, גידול בודד שגודלו 2-3 ס"מ, ללא פלישה לכלי דם. לכל מחקר כזה היו קריטריונים משלו, כאשר קבוצת המחקר כללה נשים שהסיכון שלהן לחזרה מקומית היה קטן א-פריורית, לדוגמה ברצפטורים חיוביים לאסטרוגן, HER2 שלילי וכדומה.
בעשור האחרון נבדקו שיטות רבות לקרינה חלקית לשד, ובהן קרינה חיצונית, קרינה תוך ניתוחית וברכיתרפיה (Brachytherapy) לתוך רקמת השד לאחר הניתוח.
קרינה חיצונית
קרינה המתבצעת במאיץ הקווי, ניתנת בשכיבה על הגב או על הבטן. קרינה זו ניתנת מספר שבועות לאחר הניתוח, ולאחר תשובה פתולוגית סופית. פרוטוקול הטיפול הוא 3.8Gy לפרקציה, למנה סופית של 38Gy. היתרון של טיפול זה הוא בכך שאינו פולשני ומתבצע רק לאחר שכל המידע לגבי המשך הטיפול הסיסטמי והמקומי התקבל, כמו למשל החלטה על מתן כימותרפיה, הצורך בניתוח חוזר בשל שוליים קרובים או בבתירת בלוטות לימפה אקסילריות.
קרינה בשיטת הברכיתרפיה
קרינה בשיטת הברכיתרפיה מתחלקת למספר שיטות:
קרינה באמצעות ברכיתרפיה תוך רקמתית (Interstitial) (HDR, High Dose Rate): קרינה מסוג זה ניתנת בהרדמה, מספר שבועות לאחר הניתוח ולאחר שהפצע החלים. הקרינה מתבצעת באמצעות החדרת קטטרים חלולים אל מיטת הגידול, כאשר תכנון הטיפול נעשה באמצעות CT על ידי רופא מקרין. אל הקטטרים מוכנס מקור רדיואקטיבי פעיל, לזמן שנקבע בתכנון הקרינה (דקות). קרינה זו מחייבת מכשיר טעינה מרחוק של המקור הרדיואקטיבי (Afterloading). הטיפול ניתן פעמיים ביום, והקטטרים נשארים בשד המטופלת למשך חמישה עד שישה ימים. אין צורך באשפוז במהלך הטיפול.
קרינה באמצעות בלון הניתן לניפוח בתוך מיטת הגידול: קרינה זו ניתנת לאחר שכל המידע מהניתוח מתקבל. הקרינה מתבצעת בהרדמה מקומית בה מתבצע חתך של כ-0.5 ס"מ בעור השד, ודרכו מוחדר קטטר דמוי קטטר פולי (Intracavitary balloon) למיטת הניתוח, ומנופח בהתאמה לגודל החלל הקיים (ניתן אפילו לשאוב את ה-Seroma). בתוך המתקן קיימים מספר קטטרים דקים וחלולים, לתוכם מוחדר מקור רדיואקטיבי המקרין את רדיוס הרקמה סביב הבלון. קרינה זו מחייבת מכשיר טעינה מרחוק של המקור הרדיואקטיבי (Afterloading). הטיפול ניתן פעמיים ביום, בהפרש של שש שעות לפחות, במהלך 5-7 ימים, ללא צורך באשפוז במהלך הטיפול.
קרינה תוך ניתוחית למיטת הגידול, טרם סגירת הניתוח המשמר: אם נמצא לפני הניתוח כי הן מאפייני הגידול והן המטופלת מתאימים לטיפול באמצעות APBI, אפשר לתת טיפול קרינתי תוך-ניתוחי (בהסכמת המטופלת). מיד עם סיום הניתוח המשמר שד יישלח הפרפראט לצילום ולהערכה פתולוגית של שולי הגידול בצביעה מיידית, כדי לוודא שהשולים נקיים מגידול (אופציונלי). אם השוליים נקיים, תינתן קרינה תוך-ניתוחית, במהלך ההרדמה הכללית של המטופלת. הקרינה תינתן בחדר הניתוח בקרינת אלקטרונים עם מכשיר קרינה ייעודי (לדוגמה: Intrabeam) - במנה המומלצת של 18-21Gy בפרקציה בודדת. הפעולה תתבצע בנוכחות האונקולוג המקרין, הפיזיקאי והצוות המנתח. בבדיקה דפיניטיבית לאחר שיקוע פרפין, במקרים בהם שולי הניתוח יימצאו חיוביים או קרובים, או שתמצאנה בלוטות חיוביות במהלך הניתוח, הקרינה התוך ניתוחית לא תספיק, והמטופלת תקבל טיפול קרינתי משלים לכל השד ולאזורי הניקוז הלימפטיים לפי הצורך.
מחקרים רבים בעולם מדווחים על התוצאות בשיטות שונות של APBI עבור אוכלוסייה המוגדרת מראש כבעלת סיכון נמוך לחזרה מקומית. המחקרים הראו כי, כצפוי, הקרינה החלקית שוות ערך לקרינה לכל השד.
ישנה תקווה כי בעתיד הקרוב הקרינה המואצת לחלק מהשד תהיה חלק מהטיפול בנשים לאחר אבחנה של ממאירות שד מוקדמת. טיפול זה מאפשר לנשים אלו חזרה מהירה לשגרה, חוסך נסיעות מרובות והפסד ימי עבודה ומוריד את עלות הטיפול הכוללת למשק. למרות המחקרים המראים על יתרונות השיטה, קיימים חילוקי דעות לגבי יעילותה[3].
קרינה לאחר שחזור שד
ההתלבטות אם לבצע שחזור שד מיידי, או להמתין עד לסיום ההקרנות, עולה לעיתים תכופות. בנוסף, קיימות התלבטויות הקשורות לסוג השחזור: מותחן, שתל או רקמה אוטולוגית.
יש מקרים בהם מוסכם מראש כי אין לבצע שחזור מיידי, למשל בגידולים דלקתיים של השד או אם יש פלישה לעור או לדופן בית החזה. גם במקרים של סרקומה (Sarcoma) יש לשקול היטב את השחזור, מכיוון שמנת הקרינה המיועדת למטופלת גדולה יותר מהקרינה לאחר השחזור בעקבות קרצינומה (Carcinoma).
הנזק שעלול להיגרם לשתל לאחר הקרינה כולל התקשות הצלקת העוטפת את המשתל והתכווצות של הקופסית (Capsular contracture).
בספרות המקצועית מצוין כי התקשות בדרגה חמורה מופיעה באחוז גבוה מן המקרים, אם כי המחקרים שדנו בכך התבצעו בזמנים בהם הניתוחים ושיטות הקרינה היו בטכניקות שונות מהמקובל כיום. בנוסף, התנגדות רבת שנים של המקרינים לשחזור מיידי, נבעה מכך ששתל הסיליקון העגול שהיה נהוג, חסם את היכולת לתת מנה מלאה לחלק המדיאלי של רקמת השד הנותרת, ולשרשרת הבלוטות האינטרנל-ממרית.
כשם שהפלסטיקה התקדמה, כך התקדמו טכניקות נוספות, כמו הקרינה: יש יכולת לוודא מהי מנת הקרינה הניתנת לכל נקודה במרחב השד (והשחזור), ולהימנע מאזורים "חמים" יתר על המידה, שעלולים להגביר את תופעות הלוואי.
במחקר מעקב שבוצע בשיבא, שהשווה בין נשים שעברו שחזור שד עם שתל סיליקון ויריעת ADM, מול נשים שעברו שחזור ללא ADM, אחוז הסיבוכים החמורים של התכווצות הקופסית, היה נמוך, ועמד על 11% בלבד.
מרבית הרופאים הפלסטיקאים משתמשים בשתל בעל מבנה אנטומי המתרומם בהדרגה בחלקו המדיאלי של בית החזה ויוצר מראה הולם יותר של שד, ואף מאפשר למקרין לתכנן את שדה הקרינה באופן כזה שהן הבלוטות והן החלק המדיאלי של רקמת השד הנותרת, יקבלו את מנת הקרינה הנדרשת. טכניקות של RPM עוזרות למתכנן הקרינה לחשוף את הבלוטות לשדה הקרינה, ללא פגיעה מיותרת בשתל או בלב.
לעיתים, בשל אנטומיה מסוימת או חסר בעור, מוכנס במהלך ניתוח השחזור מותחן במקום שתל קבוע. הניפוח ההדרגתי (מדי מספר שבועות) מותח את העור ויוצר כיס אליו יוכנס שתל הסיליקון הסופי בהמשך. בחלק מהמקרים מוכנס שתל שחלקו סיליקון קבוע, וחלקו מותחן. במצב זה יש צורך להשלים את ניפוח המותחן לפני ביצוע הסימולציה לתכנון הקרינה, שכן כל שינוי בנפח השד המשוחזר יצריך סימולציה חדשה. בנוסף, ניסיון לניפוח יתר לפני ההקרנה יגרום לעור להיות דק יותר, וחשוף לתופעות לוואי של הקרינה, עד כדי פריצת השתל דרכו. מסיבה זו יש להקפיד ולבדוק לפני הקרינה שהעור אינו מתוח, ולעיתים אף צריך לבצע דה-אינפלציה של המותחן טרם הסימולציה.
במטרה למקסם את התוצאה הקוסמטית של שחזור השד לאחר הקרינה, כדאי להשתמש במידת האפשר בשתל אנטומי, וביריעת ADM, ולהימנע מניפוח יתר של המותחן לפני הקרינה. כדאי להתייעץ עם רופא קרינה לפני ההחלטה על השחזור המתאים.
ביבליוגרפיה
- ↑ Haviland JS,Owen JR,Dewar JA,et, et al. The UK standardisation of breast radiotherapy (START) trials of radiotherapy hypofractionation for treatment of early breast cancer: 10-year follow-up results of two randomised controlled trials. Lancet Oncol. 2013 Oct:14(11):1086-94.
- ↑ Kaplinsky A, Pyatigorskaya V, Gelernter I, Granot H, Ben-Ayun M, Alezra D, Symon Z, Ben-David M. Inspiration gating - Improving left breast coverage for patients with anterior heart position: the RPM advantage. Paper presented at: 33rd ESTRO Annual Conference; 2014 Apr 4-8; Vienna, Austria [Abstract no. E33-1659].
- ↑ Kaidar-Person O, et al. Is current evidence about intraoperative partial breast irradiation sufficient for broad implementation in clinical practice? Eur J Surg Oncol. 2014 Jul;40(7);791-3; Epub 2014 Mar 27(14):368-370.
קישורים חיצוניים
המידע שבדף זה נכתב על ידי ד"ר מירב עקיבא-בן דוד - מנהלת תחום הקרינה לשד, מרכז רפואי ע"ש שיבא תל השומר, רמת גן


 כניסה
כניסה  עקבו אחרינו בפייסבוק
עקבו אחרינו בפייסבוק