ניתוחים לפרוסקופיים באורולוגיית ילדים - Laparoscopic surgery in pediatric urology
| ניתוחים לפרוסקופיים באורולוגיית ילדים | ||
|---|---|---|
| Laparoscopic surgery in pediatric urology | ||
| יוצר הערך | ד"ר עמוס נאמן
|
|
לערכים נוספים הקשורים לנושא זה, ראו את דף הפירושים – אנדוסקופיה
ניתוחים לפרוסקופיים בילדים תופסים מקום מכובד בכירורגיה המודרנית. ניתוחים מסוימים, כגון כריתת כליה, תיקון היצרות מעבר אגן כליה שופכן (UPJ Plasty - Plasty of the pyelo-ureteral junction) וניתוח בטני חוקר (אקספלורציה בטנית) לאיתור אשכים טמירים, הפכו כבר לתקן הזהב (Gold standard)[1].
אימוץ הגישה הלפרוסקופית בילדים היא איטית יחסית לאימוץ גישה זו במבוגרים. ניתוחים מסוימים הנחשבים לתקן הזהב במבוגרים, עדיין מבוצעים בחלק מהמקומות בגישה פתוחה באוכלוסיית הילדים.
מספר מחקרים הראו יתרון מסוים לניתוחים לפרוסקופיים לעומת אותם ניתוחים בגישה פתוחה. מגוון הניתוחים הלפרוסקופיים בילדים הולך וגדל בד-בבד עם מזעור הציוד הלפרוסקופי ורכישת ניסיון כירורגי בניתוחים אלו.
היתרונות הפוטנציאליים שהגישה הלפרוסקופית מאפשרת - תוצאות קוסמטיות טובות יותר, זמן אשפוז קצר יותר והפחתה בצורך במשככי כאבים לאחר הניתוח - מצדיקים את המאמץ להמשיך לבצע ניתוחים אלו למרות זמן הניתוח הארוך יותר ועקומת הלמידה האיטית כדי שבעתיד ניתן יהיה לאפשר לילדים לעבור ניתוחים לפרוסקופיים.
התוויות אפשריות
מאז הצגת הניתוחים הלפרוסקופיים הראשונים באורולוגיית ילדים, היכולת לבצע ניתוחים אלו הלכה והשתפרה בהתמדה. במקביל לשיפור זה התרחבו ההתוויות האפשריות. כבר בשנת 1976 בוצע הניתוח הלפרוסקופי הראשון לאיתור אשך טמיר תוך-בטני[2]. כריתת כליה דווחה לראשונה בשנת 1992, ותיקון היצרות מעבר אגן כליה שופכן בשנת 1993[3]. בשנים האחרונות יש מספר לא מבוטל של דיווחים על ניתוחים מורכבים לשחזור דרכי שתן[4].
ניתוחים לפרוסקופיים לאיתור אשך טמיר וכריתת כליה נחשבים לתקן הזהב ברוב בתי החולים, אך ניתוחים מורכבים יותר, כגון כריתת כליה חלקית ופיילופלסטיה (Pyeloplasty) לפרוסקופית עדיין אינם מבוצעים באופן שגרתי.
אשך טמיר
שיעור אשך טמיר בילדים שנולדו במועד הוא כ-1%, מתוכם ל-20% אשך שאינו נמוש. ידוע שלהדמיות שונות יש ערך מוסף נמוך לאיתור האשך, ולכן במקרים שבהם האשך לא נמוש הפעולה הבאה היא בדיקה בהרדמה וניתוח לפרוסקופי חוקר (תרשים 1).
במהלך ביצוע ניתוח לפרוסקופי חוקר ייתכנו מספר מצבים:
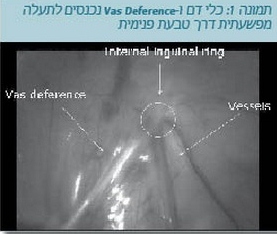
- זיהוי כלי דם וצינור זרע (Vas deferens) המסתיימים פרוקסימלית לטבעת הפנימית: במקרה זה האבחנה היא אשך שנעלם (Vanishing testis), ככל הנראה משני לאירוע וסקולרי סביב-הלידה (Perinatal), ובשלב זה מסתיימת הפעולה.
- זיהוי כלי דם וצינור זרע הנכנסים לתעלה המפשעתית: במקרה זה מבצעים ניתוח חוקר פתוח של המפשעה לאיתור האשך (תמונה 1).
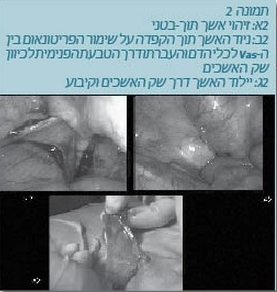
- זיהוי אשך תוך-בטני: במקרים אלו הכירורג יחליט איזו גישה ניתוחית עדיפה. האופציות העומדות בפניו הן:
- במקרה שהאשך קרוב לטבעת הפנימית לרוב הגישה המועדפת היא ניוד האשך וקיבוע האשך בשק האשכים (תמונה 2).
- במקרים בהם המנתח סובר כי לא יוכל לבצע פעולה זו עקב מרחק גדול (יותר מ-3 ס"מ בין האשך לטבעת הפנימית) תתבצע פרוצדורה על שם Fowler-Stephens, כלומר: חיתוך כלי הדם המספקים את האשך. גישה זו מתבססת על העובדה שהאשך מקבל אספקת דם מכלי דם שמקורם בצינור הזרע ובמשך הזמן מפתחים אספקת דם ממקורות אחרים (Collateral blood supply). ניתן לבצע פעולה זו:
- בשלב אחד (One stage Fowler-Stephens), כלומר: באותה פעולה לקבע את האשך בשק האשכים.
- בשני שלבים (Two stage Fowler-Stephens): בשלב ראשון חיתוך כלי הדם, ובשלב השני, חצי שנה לאחר מכן, כניסה נוספת עם הורדת האשך וקיבועו בשק האשכים.
- אם האשך אינו נראה תקין (קטן ואטרופי) מתבקשת פעולת כריתת האשך.
במחקר שכלל 364 ילדים עם אשך לא נמוש שעברו לפרוסקופיה חוקרת:
- ב-34% נמצאו אשכים תוך-בטניים. מתוכם, 60% הוגדרו כנמוכים ועברו ניוד וקיבוע ו-40% נחשבו לגבוהים ועברו Fowler-Stephens בשני שלבים.
- ב-43% מהמקרים נמצאו כלי דם וצינור זרע שחודרים את הטבעת הפנימית. מקרים אלו עברו ניתוח מפשעתי חוקר וב-23% נמצא אשך נעלם[5].
Docimo השווה את הגישות הלפרוסקופיות השונות והראה אחוזי הצלחה בגישות השונות[6]:
- ניוד וקיבוע האשך - 89%
- Fowler-Stephans חד-שלבי - 76%
- Fowler-Stephans דו-שלבי - 77%
Baker פרסם את אחוז האטרופיה של האשך בניתוחים השונים[7]:
- ניוד ראשוני של האשך וקיבוע בשק האשכים – 2.2%
- Fowler-Stephans חד-שלבי - 22%
- Fowler-Stephans דו-שלבי - 10%
דליות האשך (Varicocele)
קיימות מספר גישות כירורגיות לתיקון דליות האשך. ניתן לחלק את הגישות הכירורגיות השונות לשתי קבוצות עיקריות:
- קשירה גבוהה של ורידי האשך (High ligation of spermatic veins): גישה בטנית טרנספריטונלית או רטרופריטונלית. תוארו מספר טכניקות כירורגיות שונות לגישה זו:
- Palomo - קשירת עורק ווריד האשך ביחד
- Modified Palomo - שימור העורק
- כריתת דליות האשך עם שימור הלימפה (Lymphatic sparing laparoscopic varicocelectomy): קשירת ורידי האשך עם העורק ושימור כלי הלימפה
פורסמו מספר רב של מאמרים המתארים טכניקות אלו בגישה הלפרוסקופית ובגישה הפתוחה.
- קשירה נמוכה של ורידי האשך (Low ligation of spermatic vein): זיהוי ורידי האשך דיסטלית לטבעת החיצונית וקשירת הורידים תוך שימור העורק וכלי הלימפה. גישה זו מחייבת שימוש בהגדלה - בין אם מדובר במשקפיים טלסקופיות (לופות) המגדילות פי 2.5 ובין אם מדובר בהגדלה משמעותית יותר בעזרת מיקרוסקופ.
הדיון לגבי השיטה המועדפת לא יורחב להלן.
שיעור השכיחות של דליות האשך באוכלוסיות ילדים ומתבגרים הוא 10-15%. עדיין לא ברור מי מהילדים עם דליות האשך יסבול מבעית פוריות הקשורה לדליות האשך בהמשך החיים.
האינדיקציות לביצוע ניתוח לתיקון דליות האשך בילדים ומתבגרים הן:
- תת-גדילה (היפוטרופיה) של האשך (יש המשתמשים בערך של הפרש בנפח האשכים גדול מ-10% כאינדיקציה לניתוח)
- דליות אשך דו-צדדיות
- כאבים המשויכים לדליות האשך
- דרגת דליות האשך לכשעצמה אינו מהווה אינדיקציה לביצוע ניתוח
- בקבוצת הילדים לא ניתן לבצע ספירת זרע, ורק במקרים סלקטיביים במתבגרים מעל גיל 18 משתמשים בספירת זרע כגורם בקבלת החלטה לגבי הניתוח.
ניתוחים לפרוסקופיים לתיקון דליות האשך הוכחו כבטוחים ויעילים עם תוצאות דומות לגישה הפתוחה.
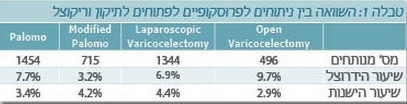
מאמר שפורסם ב-2009[8], בו נסקרה הספרות המקצועית העוסקת בתיקון דליות האשך בילדים ומתבגרים, השוותה מאמרים הנוגעים לניתוח פתוח (496 מנותחים) ולניתוח לפרוסקופי (1,344 מנותחים) (טבלה 1).
ההחלטה איזו גישה עדיפה אינה חד-משמעית, ומבוססת על ניסיון המנתח והעדפת ההורים.
נראה כי בניתוחים בשיטת Palomo, בין שהם מבוצעים בגישה לפרוסקופית ובין שבגישה פתוחה, שיעור הסיבוך של היווצרות מיימת אשכים (Hydrocele) גבוה יחסית (עד 30% בסדרות שונות), ולכן רצוי לבצע ניתוח סלקטיבי יותר שבו משמרים את כלי הלימפה.
במקרים הנדירים יותר בהם מדובר בניתוח דו צדדי לתיקון דליות האשך, יש העדפה מסוימת לגישה הלפרוסקופית על פני גישה מפשעתית דו-צדדית[9].
כריתת כליה
כריתת כליה לפרוסקופית במבוגרים לכליות לא מתפקדות וסרטן כליה הפכו לתקן הזהב.
האינדיקציה הנפוצה ביותר לכריתת כליה בילדים היא כליה לא מתפקדת משנית לחסימה מכנית, החזר שלפוחית-שופכן (Vesicoureteral reflux) או שופכן אקטופי (Ectopic ureter).
מספר רב של מחקרים השוו בין הגישה הפתוחה לגישה הלפרוסקופית. מחקרים אלו הראו שכריתת כליה בגישה לפרוסקופית היא בטוחה, יעילה ובעלת אחוז נמוך של מעבר לניתוח פתוח.
היתרונות הפוטנציאליים של הגישה הלפרוסקופית:
- שיפור קוסמטי בצלקות ניתוחיות
- הגדלה אופטית של השדה הניתוחי
- זמן אשפוז קצר יותר
- החלמה מהירה יותר (לכן ההורים חוזרים מהר יותר לעבודה)
- צורך מופחת במשככי כאבים לאחר הניתוח
החסרונות הפוטנציאליים של הגישה הלפרוסקופית:
- זמן ניתוח ממושך יותר
- עקומת למידה ממושכת יותר
- שיעור סיבוכים גבוה יותר (בעיקר בהתחלת עקומת הלמידה)
משך הניתוח משתפר בצורה משמעותית ככל שניסיון המנתח גדל. מספר מחקרים הראו כי אין הבדל משמעותי במשך הניתוח בילדים שעברו ניתוח לפרוסקופי לעומת אלו שעברו ניתוח פתוח[10][11].
Valla פרסם 100 מקרים ראשונים של כריתת כליה, בהם דווחו 4 סיבוכים מינוריים ללא צורך במתן דם וללא מעבר לניתוח פתוח, עם משך ניתוח ממוצע של 85 דקות[12].
גישה רטרופריטוניאלית (Retroperitoneal) מול גישה טרנספריטוניאלית (Transperitoneal)
יש שתי גישות בסיסיות לכריתת כליה: טרנספריטוניאלית (Transperitoneal) ורטרופריטוניאלית (Retroperitoneal). לכל אחת מגישות אלו יתרונות וחסרונות.
לגישה הרטרופריטוניאלית יתרון אפשרי בכך שאין חדירה לקרום הצפק (פריטונאום), ולכן שיעור נמוך של הידבקויות וחסימת מעיים בעתיד. יתרון זה לא הוכח עדיין באופן חד-משמעי.
הגישה הטרנספריטוניאלית מאפשרת שדה ניתוחי רחב יותר, עובדה חשובה יותר בילדים קטנים. לגישה הפתוחה יתרון בכך שלפי פרסומים שונים זמן הניתוח קצר יותר.
במאמר שפורסם לאחרונה וביצע סקירת ספרות נרחבת המשווה את שתי הגישות השונות בניתוחי כריתת כליה, צוטטו 51 מאמרים שכללו 689 פרוצדורות מתוכן 401 רטרופריטוניאלית ו-288 טרנספריטוניאלית. לא נראה הבדל סטטיסטי משמעותי בין שתי הקבוצות. פגיעה בכלי דם תוארה בשני מקרים בגישה הרטרופריטוניאלית ו-0 בגישה הטרנספריטוניאלית, ופגיעה במעי הדק תוארה בשני מקרים בגישה הרטרופרוטנאילית לעומת מקרה אחד בגישה הטרנספריטוניאלית. זמן הניתוח בגישה הטרנספריטוניאלית מעט ארוך יותר מהגישה הרטרופריטוניאלית (451 דקות לעומת 129 דקות)[13].
כריתה חלקית של כליה
ניתוח זה הוא אתגר כירורגי גדול יותר מאשר כריתת כליה פשוטה. האינדיקציה לכריתת כליה חלקית בילדים היא לרוב כריתת קוטב עליון או תחתון שאינם מתפקדים, והם חלק ממערכת מאספת כפולה.
כאשר מדובר בקוטב עליון, בדרך כלל מדובר בשופכן חסום ומורחב לכל אורכו, ויש צורך בכריתת השופכן עד לשלפוחית השתן. תוארו מקרים שבהם בזמן הניתוח לכריתת קוטב עליון נכרת השופכן המנקז את הקוטב התחתון. כדי לצמצם סיבוך זה יש מנתחים המכניסים תומכן לשופכן של הקוטב התחתון ובכך מקטינים את הסיכונים לפגיעה בשופכן.
ממצא נוסף שאופייני לכריתת קוטב עליון של מערכת מאספת כפולה הוא הצטברות נוזל מעל הקוטב התחתון. לאחר שנשללת דליפה מהקוטב התחתון מדובר בתהליך ללא משמעות קלינית. אם הנוזל ינוקז, לרוב תהיה חזרה - ככל הנראה עקב נפרונים שאריים (Residual nephrons). לפיכך, לרוב אין אינדיקציה לניקוז במקרים אלו.
סדרה אחת שתיארה 54 ניתוחים לפרוסקופיים של כריתת קוטב עליון של מערכת מאספת כפולה, הראתה שב-30% נוצרה ציסטה מעל לקוטב התחתון. במאמר זה השתמשו ב-Endoloop לכריתת הקוטב העליון, והמסקנה הייתה שנשארו חלקי גביע (Calyx) ב-Loop ואלו יצרו את המבנים הציסטיים[14].
האינדיקציה לכריתת קוטב תחתון נדירה יותר, בדרך כלל מדובר בחוסר תפקוד משני להחזר מאסיבי לקוטב התחתון. גם כאן יש לכרות את השופכן דיסטלית ככל שניתן, מבלי לפגוע באספקת הדם של השופכן התקין ולקשור את השופכן כדי למנוע החזר של שתן לחלל הבטן.
כריתת כליה חלקית תוארה הן בגישה טרנספריטוניאלית והן בגישה רטרופריטוניאלית. יש חשיבות רבה לזיהוי כלי הדם המספקים את הקוטב שמתכוונים לכרות. מספר מחקרים הראו כי באחוז מסוים יש קיפוח וסקולרי באספקת הדם לקוטב התקין עקב עווית (ספאזם) של כלי הדם או קשירתו בשוגג.
אטרופיה של הקוטב הנותר הוא סיבוך מוכר ומשמעותי. לאחר סגירת כלי הדם מתקבל לרוב קו הפרדה (Demarcation line) בין הקטבים, דבר המסייע בביצוע כריתת הקוטב החולה מבלי לפגוע או לפתוח מערכת מאספת של הקוטב השני.
Lee השווה 28 ילדים שעברו ניתוח לכריתת כליה חלקית בגישה לפרוסקופית לעומת אלו שעברו את הניתוח בגישה הפתוחה. זמני הניתוח לא היו שונים, בשני המקרים 194 דקות בממוצע, מנותחי הקבוצה הלפרוסקופית שהו באשפוז רק 1.7 ימים לעומת 4.7 ימים של הקבוצה הפתוחה, כמו כן מנותחי הקבוצה הלפרוסקופית נזקקו לפחות משככי כאבים - 0.44 מ"ג/ק"ג לעומת 1.53 מ"ג/ק"ג[15].
Chertin וחבריו הראו תוצאות דומות והדגימו יתרון משמעותי סטטיסטי לקבוצה הלפרוסקופית לעומת הקבוצה הפתוחה במדדים של זמן אשפוז וצורך במשככי כאבים לאחר הניתוח. לא היה הבדל משמעותי מבחינת משך הניתוח בין שתי הקבוצות[16].
גישה נוספת להתמודד עם הפרעות בניקוז של שופכן אקטופי המנקז קוטב עליון של מערכת מאספת כפולה, או שופכן עם החזר מאסיבי המנקז קוטב תחתון, היא השקה של השופכן הפתולוגי לשופכן הבריא (Ipsilateral uretero-ureterostomy). טכניקה זו תוארה גם בגישה הלפרוסקופית[17].
פיאלופלסטיה לפרוסקופית (Laparoscopic pyeloplasty)
פיאלופלסטיה לפרוסקופית תוארה לראשונה במבוגרים בשנת 1993[18] ובילדים תוארה לראשונה על ידי Peters בשנת 1995[19].
ביצוע פיאלופלסטיה לפרוסקופית תואר בגישה הטרנספריטוניאלית, רטרופריטוניאלית, ובעזרת רובוט. למעשה, הניתוח הלפרוסקופי מחקה את הניתוח הפתוח. הגישה הנפוצה כיום בשימוש היא Anderson-Hynes Pyeloplasty. ניתוח זה לא זכה לפופולריות בכל המרכזים בשל הקושי הטכני, במיוחד בביצוע ההשקה, עקב הצורך לביצוע תפירה בחלל קטן. דרך אחת להתגבר על קושי זה היא השימוש המודרני ברובוטים.
במחקר השוואתי בין פיאלופלסטיה פתוחה לפיאלופלסטיה לפרוסקופית רטרופריטוניאלית הודגם יתרון לגישה הלפרוסקופית במשך האשפוז (2.4 ימים לעומת 5 ימים) והפחתה בשימוש במשככי כאבים לאחר הניתוח. החיסרון בגישת הפיאלופלסטיה הלפרוסקופית התבטא בזמן ניתוח ארוך יותר - 219 דקות לעומת הניתוח הפתוח 96 דקות [20].
מחקר נוסף שהשווה את הניתוח הפתוח לפיאלופלסטיה לפרוסקופית הראה כי לגישת הפיאלופלסטיה הלפרוסקופית יש יתרון משמעותי סטטיסטית במספר פרמטרים[21]:
- איבוד דם (10 מ"ל לעומת 150 מ"ל בגישה הפתוחה)
- שימוש במשככי כאבים
- אשפוז קצר יותר
- חתך קטן יותר (3.5 ס"מ בגישה הלפרוסקופית לעומת 21 ס"מ בגישה הפתוחה)
- זמן ניתוח קצר יותר בגישה הלפרוסקופית - 80 דקות לעומת 120 דקות בגישה הפתוחה
הוכח כי ניתן לבצע ניתוחים אלו בכל קבוצת גיל - גם בילדים שמשקלם פחות מ-6 ק"ג[22].
תיקון החזר שלפוחית-שופכן (Vesicoureteral reflux)
תוארו מספר גישות לביצוע ניתוח לטיפול בהחזר שלפוחית שופכן בשיטה לפרוסקופית.
השיטה הראשונה שתוארה הייתה בגישה טרנספריטוניאלית חוץ-שלפוחיתית (בדומה לשיטה שתוארה על ידי Lich-Gregoire). בטכניקה זו יוצרים תעלה בין שריר שלפוחית השתן לרירית, ותופרים את השריר מעל השופכן כך שנוצרת תעלה ארוכה תוך-שלפוחיתית[23]. אומנם דווחו אחוזי הצלחה גבוהים בשיטה זו, אך עקב הקושי הטכני בביצוע פעולה זו ומשכה היא לא זכתה לפופולריות רבה.
שיטה נוספת שאחד התומכים הנלהבים שלה הוא CK Yeung היא בעצם חיקוי ניתוח ראימפלנטציה (Reimplantation) על שם Cohen בגישה לפרוסקופית תוך-שלפוחיתית (Vesicoscopic procedure). עקרונות גישה זו הם כניסה לשלפוחית השתן, ניפוח השלפוחית על ידי פחמן דו-חמצני וביצוע ראימפלנטציה.
נקודות טכניות חשובות בשיטה זו הן קיבוע של המחדרים (Trocars) לשלפוחית כדי שהגז לא ידלוף מהשלפוחית, והשארת צנתר (קתטר) ונקז (דריין) עד שהשלפוחית נאטמת - כ-3 ימים. במקרים בהם יש צורך לבצע Tailoring, יש לתת את השופכן המורחב דרך אחד החורים ולבצע את פעולת חיתוך ותפירת השופכן בשיטה ידנית.
ניתוחים לפרוסקופיים רקונסטרוקטיביים (Reconstructive) של דרכי השתן
ילדים הסובלים מהפרעות נוירולוגיות המשפיעות על שלפוחית השתן ודרכי העיכול נזקקים לעתים לניתוחים שנועדו לשפר את איכות החיים, העצמאות והשליטה בסוגרים. ניתוחים אלו, כגון אוגמנטציה של שלפוחית השתן, תעלות לצנרור השלפוחית (Mitrofanoff) או צנרור של מעי (Malone antegrade continent enema) מבוצעים באופן היסטורי בגישה פתוחה. בשלב הראשון מבוצע ניוד של מעי וניתוק של מקטע מעי (תוספתן, מעי דק, מעי גס או קיבה) ובשלב שני חיבור בין המקטע שנקצר לשלפוחית או מעי מצד אחד ולעור מצד שני.
מכיוון שניתוחים מסוג זה נחשבים למורכבים מאוד מבחינה כירורגית וביצוע ההשקה דורש מיומנות רבה, תוארו בתחילה ניתוחים שבהם החלק הראשון של ניוד המעי בוצע בגישה לפרוסקופית והחלק השני של ההשקה בוצע בגישה פתוחה (Laparoscopic assisted)[4][24].
אף על פי שתוארו מקרים שבהם בוצעה Augmentation cystoplasty בגישה לפרוסקופית בלבד[25], המחברים בעצמם טענו כי גישה זו עדיין שמורה למקרים מסוימים בלבד בידיים של מנתחים מנוסים. לא הודגם יתרון ברור על הגישה הפתוחה במקרים מורכבים אלו.
יתרונות הניתוח הלפרוסקופי
יתרונות פוטנציאליים לגישה לפרוסקופית הם:
- זמן אשפוז קצר יותר
- תוצאות קוסמטיות טובות יותר
- הגדלה אופטית של השדה הניתוחי ודיוק בתפירה
- צורך מופחת בשימוש בתרופות נגד כאבים לאחר הניתוח
עם זאת, עדיין אין עדות משכנעת לכך שלגישה הלפרוסקופית יש יתרונות משמעותיים, לדוגמה: היתרון הקוסמטי בניתוחים לפרוסקופיים הנחשב בעיני רבים כיתרון משמעותי, נתפס על ידי אחרים כיתרון קטן בלבד לעומת חתך גבי (Dorsal lumbotomy).
משך אשפוז
אחד היתרונות הידועים של ניתוחים לפרוסקופיים הינו משך החלמה מהיר ואשפוז קצר יחסית. החולים מחלימים מהר והצורך במשככי כאבים פוחת. משך האשפוז הקצר מוזיל את העלויות של ההליך הלפרוסקופי כמפורט להלן.
שימוש במשככי כאבים
אחד היתרונות של ניתוחים לפרוסקופיים הוא צורך מופחת במשככי כאבים לאחר הניתוח. למרות מספר פרסומים המראים יתרון לגישה הלפרוסקופית יש גם סדרות המראות כי אין הבדל משמעותי בין שתי הקבוצות.
קיים חוסר אחידות בהתוויות למתן משככי כאבים ואופן הערכת כאב. ילדים בגילאים השונים מגיבים שונה לכאב. הילדים הקטנים אינם מבטאים באופן מילולי את מכאוביהם, ולכן קיימות מספר שיטות להערכת כאב בגילאים הצעירים. אחד מהם הוא ה-FLACC (Face, legs, activity, cry and consolability) שנועד להערכת כאב בילדים בגילאים של חודשיים עד שלוש שנים[26]. עם זאת, בסדרות שונות ובפרסומים שונים משתמשים בכלים אחרים להעריך את מידת הכאב, ולכן אין אחידות מובהקת בעניין זה.
זמן הניתוח
אף שמספר רב של מחקרים הראה כי משך הניתוח בגישה לפרוסקופית הוא ארוך משמעותית לעומת הגישה הפתוחה, מחקרים רבים אחרים הראו כי אין הבדל משמעותי.
זמן הניתוח מוגדר באופן שונה במחקרים השונים, ולכן לא תמיד ניתן להשוות בין המחקרים. יש מחקרים המתייחסים לזמן הניתוח כזמן שעובר מהכנסת המחדר הראשון עד לסיום תפירת העור, ויש כאלו שמחשיבים זמן ניתוח כביצוע ציסטוסקופיה (Cystoscopy) והכנסת תומכן (סטנט). ניתן להכליל ולומר כי זמן הניתוח תלוי גם במיומנות המנתח, וקיימת עקומת למידה שבסופה זמן הניתוח בגישה הלפרוסקופית דומה לזמן ניתוח בגישה פתוחה.
שיקולים בהרדמה
ילדים קטנים ותינוקות נוטים לאבד חום באופן משמעותי יותר מאשר ילדים גדולים יותר או ילדים המנותחים בגישה פתוחה. שימוש באוויר חם לאינסופלציה (Insufflation) וחימום חדר הניתוח יכולים להפחית תופעה זו.
שינויים המודינמיים ונשימתיים נגרמים עקב הזרמה של פחמן דו-חמצני ולחץ שנוצר עקב ניפוח הבטן. במקרים שבהם הלחץ התוך-בטני עולה, יש ירידה בהחזר הוורידי ותנודות בלחץ הדם ובדופק. תיתכן גם עלייה בפחמן הדו חמצני בסוף נשיפה (End tidal CO2) עקב ספיגה של פחמן דו חמצני והגבלה בהתפשטות הריאתית. שמירה על לחצי אינסופלציה של 8-10 מ"מ לרוב תמנע תופעות אלו.
הלחמי וחב'[27] הראו כי גם בגישה הרטרופריטוניאלית והטרנספריטוניאלית יש עלייה בקצב נשימה, בלחץ השיא בדרכי האוויר (Peak airway pressure) ובפחמן הדו חמצני בסוף נשיפה, אך שינוי מינימלי בדופק ובריויון החמצן (סטורציה).
עלויות
קיים חוסר אחידות בנושא עלויות ההליך. יש סדרות המראות כי ניתוחים לפרוסקופיים יקרים יותר ויש כאלו שמראים שאין הבדל. שימוש חוזר במכשירים מוזיל את עלות הניתוח, קיצור משך הפעולה ומשך האשפוז מוזיל אף הוא את עלות הניתוח.
סיבוכים
שיעור הסיבוכים בסדרות גדולות של מבוגרים שעברו ניתוחים לפרוסקופיים עומד על 12-14%. במאמר שכלל 5,400 הליכים לפרוסקופיים בילדים, שבוצעו על ידי 153 מנתחים, שיעור הסיבוכים עמד על 5.4%. רוב הסיבוכים היו קלים, ורק 0.4% נזקקו לתיקון ניתוחי[28].
מאמר אחר שכלל 701 מקרים, רובם ניתוחים קטנים (אשך טמיר, דליות האשך), הראה שיעור סיבוכים של 2.7%[29].
סדרה שכללה 806 ניתוחים לפרוסקופיים הראתה שיעור סיבוכים של 2% (1.6% קשורים לשלב הכניסה לחלל הבטן). נראה כי הגישה הפתוחה לחלל הבטן היא בעלת שיעור סיבוכים נמוך במעט (אך לא משמעותי סטטיסטית) מאשר כניסה על ידי מחט Veress. מנתחים שביצעו יותר מ-12 ניתוחים לפרוסקופיים בשנה הם בעלי שיעור סיבוך נמוך יותר[30].
Peters הראה כי שיעור הסיבוכים יורד באופן משמעותי ככל שהמנתח מנוסה יותר. למנתח עם פחות מ-20 ניתוחים, כאשר הוא מבצע באופן עצמאי ללא הדרכה, שיעור הסיבוכים הוא 8.3% - לעומת מנתח עם יותר מ-100 פעולות, עבורו שיעור הסיבוכים הוא 2.8%.
תסחיף פחמן דו-חמצני
תסחיף פחמן דו-חמצני הוא סיבוך אופייני לאוורת צפק (Pneumoperitoneum): כניסה של גז לוורידים, בדרך כלל באזור שבו יש פגיעה בווריד. הגז גורם לחסימת מוצא החדר הימני ומחזור ריאתי המתבטא בירידה בריוויון החמצן וירידה בפחמן הדו חמצני בסוף נשיפה. הטיפול כולל השכבה על צד שמאל ושאיבה של האוויר דרך צנתר מרכזי (Central line).
המרה לניתוח פתוח (Conversion)
המעבר לניתוח פתוח יכול להיות ממספר סיבות:
- סיבוך משמעותי, כמו פגיעה בכלי דם, הדורש תיקון בגישה פתוחה
- חוסר התקדמות של הניתוח
- קושי טכני בביצוע השקות
שיעור המעבר לניתוח פתוח הוא 0-30% בסדרות השונות.
דימום
לפי רוב הפרסומים, שיעור הדימום בניתוחים לפרוסקופיים אינו גבוה יותר מהגישה הפתוחה ואף נמוך יותר. הגדלה וראות משופרת מאפשרים שליטה טובה בדימומים משמעותיים בזמן הניתוח הלפרוסקופי. סקירת חלל הבטן לאחר ריקון הבטן מפחמן דו-חמצני היא חלק מהטכניקה הניתוחית הטובה המוכוונת לאיתור דימומים.
פגיעה באיברים תוך-בטנים בזמן הכנסת המחדרים (טרוקרים)
חלק גדול מהסיבוכים המתוארים בספרות הם פגיעה באיברי הבטן בזמן הכנסת המחדרים. קיימות גישות שונות להכנסת מחדרים:
- שימוש במחט Veress
- כניסה עם Visual obturator
- כניסה בגישה פתוחה (Bailez ,Hasson)
ביבליוגרפיה
- Peters CA. Laparoscopy in pediatric urology. Curr Opin Urol 2004:14(2);67-73
- ↑ El-Ghoneimi A, et al. Retroperitoneal laparoscopic nephrectomy in children: At last the gold standard? J Pediatr Urol 2006;2(4):357-363
- ↑ Cortesi N, et al. Diagnosis of bilateral abdominal cryptorchidism by laparoscopy. Endoscopy 1976;8(1)::33-34
- ↑ Kavoussi LR, Peters CA. Laparoscopic pyeloplasty. J Urol 1993;150(6):1891-1894
- ↑ 4.0 4.1 Chung SY, Meldrum K, Docimo SG. Laparoscopic assisted reconstructive surgery: a 7-year experience. J Urol 2004;171(1):372-375
- ↑ Papparella A, et al. Laparoscopic management of nonpalpable testes: a multicenter study of the Italian Society of Video Surgery in Infancy. J Pediatr Surg 2005;40(4):696-700
- ↑ Docimo SG, et al. Laparoscopic orchiopexy for the high palpable undescended testis: preliminary experience. J Urol 1995;154(4):1513-1515
- ↑ Baker LA, et al. A multi-institutional analysis of laparoscopic orchidopexy. BJU Int 2001;87(6):484-489
- ↑ Barroso U, et al. Surgical treatment of varicocele in children with open and laparoscopic Palomo technique: a systematic review of the literature. J Urol 2009;181(6):2724-2728
- ↑ Glassberg KI, et al. Laparoscopic lymphatic sparing varicocelectomy in adolescents. J Urol 2008;180(1):326-330;Discussion 330-331
- ↑ Hamilton BD, et al. Comparison of laparoscopic versus open nephrectomy in the pediatric population. J Urol 2000;163(3):937-939
- ↑ El-Ghoneimi A, et al. Laparoscopic retroperitoneal nephrectomy in high risk children. J Urol 2000;164(3 Pt 2):1076-1079
- ↑ Steyaert H, Valla JS. Minimally invasive urologic surgery in children: an overview of what can be done. Eur J Pediatr Surg 2005;(5):307-313
- ↑ Kim C, McKay K, Docimo SG. Laparoscopic nephrectomy in children: systematic review of transperitoneal and retroperitoneal approaches. Urology 2009;73(2):280-284
- ↑ Mushtaq I, Haleblian G. Laparoscopic heminephrectomy in infants and children: First 54 cases. J Pediatr Urol 2007;3(2):100-103
- ↑ Lee RS, et al. Pediatric retroperitoneal laparoscopic partial nephrectomy: comparison with an age matched cohort of open surgery. J Urol 2005;174(2):708-711;Discussion 712
- ↑ Chertin B, et al. Pediatric transperitoneal laparoscopic partial nephrectomy: comparison with an age-matched group undergoing open surgery. Pediatr Surg Int 2007;23(12):1233-1236
- ↑ Gonzalez R, Piaggio L. Initial experience with laparoscopic ipsilateral ureteroureterostomy in infants and children for duplication anomalies of the urinary tract. J Urol 2007;177(6):2315-2318
- ↑ Schuessler WW, et al. Laparoscopic dismembered pyeloplasty. J Urol 1993;150(6):1795-1799
- ↑ Peters CA, Schlussel RN, Retik AB. Pediatric laparoscopic dismembered pyeloplasty. J Urol 1995;153(6):1962-1965
- ↑ Bonnard A, et al. Retroperitoneal laparoscopic versus open pyeloplasty in children. J Urol 2005;173(5):1710-1713;Discussion 1713
- ↑ Zhang X, et al. Retrospective comparison of retroperitoneal laparoscopic versus open dismembered pyeloplasty for ureteropelvic junction obstruction. J Urol 2006;176(3):1077-1080
- ↑ Neheman A, et al. Laparoscopic urinary tract surgery in infants weighing 6 kg or less: perioperative considerations and comparison to open surgery. J Urol 2008;179(4):1534-1538
- ↑ Lakshmanan Y, Fung LC. Laparoscopic extravesicular ureteral reimplantation for vesicoureteral reflux: recent technical advances. J Endourol 2000;14(7):589-593;Discussion 593-594
- ↑ el-Feel A, et al. Laparoscopic augmentation ileocystoplasty: results and outcome. Eur Urol 2009;55(3):721-727
- ↑ Lorenzo AJ, Cerveira J, Farhat WA. Pediatric laparoscopic ileal cystoplasty: complete intracorporeal surgical technique. Urology 2007;69(5):977-981
- ↑ Merkel SI, et al. The FLACC: a behavioral scale for scoring postoperative pain in young children. Pediatr Nurs 1997: 23(3)::293-297
- ↑ Halachmi S, et al. Hemodynamic and respiratory effect of pediatric urological laparoscopic surgery: a retrospective study. J Urol 2003;170(4 Pt 2):1651-1654;Discussion 1654
- ↑ Peters CA. Complications in pediatric urological laparoscopy: results of a survey. J Urol 1996;155(3):1070-1073
- ↑ Esposito C, et al. Complications of pediatric urological laparoscopy: mistakes and risks. J Urol 2003;169(4):1490-1492;Discussion 1492
- ↑ Passerotti CC, et al. Patterns and predictors of laparoscopic complications in pediatric urology: the role of ongoing surgical volume and access techniques. J Urol 2008;180(2):681-685
קישורים חיצוניים
- ניתוחים לפרוסקופיים באורולוגיית ילדים, מדיקל מדיה
המידע שבדף זה נכתב על ידי ד"ר עמוס נאמן, המחלקה האורולוגית, מרכז רפואי מאיר, כפר סבא


 כניסה
כניסה  עקבו אחרינו בפייסבוק
עקבו אחרינו בפייסבוק