סרטן השד - טיפול משלים - Breast cancer - adjuvant therapy
| סרטן השד - טיפול משלים | ||
|---|---|---|
| breast cancer - adjuvant therapy | ||

| ||
| ICD-10 | Chapter C 50. | |
| ICD-9 | 174
-175 |
|
| MeSH | D001943 | |
| יוצר הערך | ד"ר הדסה גולדברג | |
לערכים נוספים הקשורים לנושא זה, ראו את דף הפירושים – סרטן השד
טיפול משלים לסרטן השד הוא טיפול הניתן לאחר ניתוח להסרת הגידול, והוא כולל טיפול כימותרפי, טיפול הורמונלי וטיפול ביולוגי המכוון כנגד הקולטן HER2. תרומת הטיפול התרופתי המשלים לסיכויי ההישרדות עבור נשים אלו, הוכחה במחקרים מבוקרים רבים, והפכה לחלק בלתי נפרד מהטיפול בממאירות זו[1][2]. בשני העשורים האחרונים נצפתה ירידה מתמדת בתמותה מסרטן השד, על אף שהיארעות המחלה לא פחתה במשך תקופה זו[3]; ניתן ליחס מגמה זו במידה רבה, להוספת טיפול משלים תרופתי לנשים שאובחנו עם סרטן שד מוקדם.
בשנים האחרונות מודגש הצורך ביישום אמצעים שונים, ביניהם שיטות גנומיות, לסיוע בהתאמה של הטיפול המיטבי עבור כל מטופלת. אמצעים אלה נועדו למנוע מתן טיפול שתרומתו להישרדות קטנה ואינה מצדיקה את הרעילות הכרוכה בו. פריצת דרך זו בגישה הטיפולית בסרטן שד מוקדם, מתבססת על ההבנה כי לא מדובר במחלה אחת, אלא במספר תתי-סוגים ביולוגיים הנבדלים זה מזה בפתוגנזה, בביטוי הפתולוגי והקליני, בסיכויי ההחלמה ובסיכוי לתגובה לטיפולים השונים[4][5]. ההחלטה על טיב הטיפול המשלים לכל מטופלת מתבססת על שלב המחלה בעת האבחון ועל מאפייניה הביולוגיים, ובראשם נוכחות הקולטנים לאסטרוגן (ER ,Estrogen Receptor) ולפרוגסטרון (PR ,Progesterone Receptor). בנוסף יש לבחון האם הקולטן HER2 מבוטא בעודף בתאי הגידול[6].
הצורך בטיפול משלים כל-גופי בסרטן השד
כבר בשלהי שנות השישים של המאה הקודמת נודע כי סיכויי ההחלמה של אישה שאובחנה עם סרטן שד מוקדם, תלויים בעיקר בסיכון לפיזור גרורתי מרוחק. השגת שליטה מקומית בשד עצמו תורמת אך מעט לסיכויי ההחלמה. המסקנות שנגזרו מהבנה זו הן כי אין די בניתוח להסרת הגידול מהשד ומבית השחי, וכי יש להוסיף טיפול כל-גופי, אשר עשוי להפחית את הסיכון להתפתחות גרורות מרוחקות בהמשך. ההגדרה של סרטן שד מוקדם כוללת את כל השלבים בהם המחלה מוגבלת לשד ו/או לבלוטות הלימפה האזוריות, והיא תקפה כל עוד אין עדות לפיזור גרורתי מרוחק. נשים שאובחנו עם סרטן שד מוקדם נבדלות זו מזו הן בשלב המחלה בעת האבחון, והן בביולוגיה הראשונית של הגידול. שני מדדים אלו מכתיבים במידה רבה את מהלך המחלה ואת סיכויי ההישרדות. חלק מהחולות מחלימות באמצעות הטיפול המקומי בלבד הכולל ניתוח והקרנות; אצל חולות אחרות נמצאות גרורות מיקרוסקופיות באיברים מרוחקים בעת אבחון מחלתן, והן זקוקות לטיפול תרופתי משלים, אשר עשוי לשפר את סיכוייהן לשרוד. ההחלטה על טיפול משלים כל-גופי חייבת להתבסס על שני גורמים: הגורם הראשון הנו הערכת מידת הסיכון להישנות מחלתה של המטופלת, והגורם השני מתבסס על חיזוי הרגישות של הגידול לטיפול שניתן כנגדו ומידת התרומה של טיפול זה לסיכויי ההישרדות. בנוסף, יש להביא בחשבון את תופעות הלוואי של הטיפול, את הגיל הביולוגי של המטופלת, את מצבה הבריאותי הכללי (כולל מחלות רקע) וכן את העדפותיה האישיות.
חלק נכבד מהידע שנצבר לגבי הטיפולים המשלימים, מתבסס על מטא-אנליזה של ה-EBCTCG (Early Breast Cancer Trialists' Collaborative Group). פרויקט זה, המנוהל על ידי חוקרים ברחבי העולם, החל ב-1985, ומתעדכן כל חמש שנים. הוא מקיף כיום כ-100,000 מטופלות שהשתתפו ב-123 מחקרים אקראיים מבוקרים, בהם נבחנו היבטים שונים בטיפול המשלים בסרטן השד[1][2].
תת-הסוגים הביולוגיים בסרטן השד
כאמור, סרטן השד איננו מחלה אחת, אלא אוסף של תתי-סוגים ביולוגיים הנבדלים זה מזה בפתוגנזה, בביטוי הפתולוגי והקליני, בסיכויי ההחלמה ובסיכוי לתגובה לטיפולים השונים. באמצעות שיטות שונות מתחום מערך ה-DNA (Gene microarray), המתבססות על השוואת רמות הביטוי של גנים שונים בתאי הגידול, הוכח כי ניתן לחלק את כלל הגידולים הממאירים של השד לארבע תת-קבוצות עיקריות, הנבדלות זו מזו במידת הביטוי של גנים רבים:
- Luminal A
- Luminal B
- HER2 positive
- Basal-like
כמחצית מהגידולים בקבוצת ה-HER2 positive מבטאים גם תכונות של קבוצת ה-Luminal B, ובכללן ביטוי הקולטנים להורמוני המין[4][5].
בפרקטיקה היומיומית נקבעת תת הקבוצה של הגידול על פי מדדים פתולוגיים, הכוללים את הביטוי של הקולטנים להורמוני המין ER ו-PR, רמת הביטוי של הקולטן HER2, מדד השגשוג Ki67 ודרגת ההתמיינות של הגידול. השימוש במדדים פתולוגיים אלו כחלופה לבדיקת מערך DNA נעשית מתוך ידיעה כי החפיפה אינה מלאה. הקביעה לאיזו תת-קבוצה משתייך הגידול הפרטני, מסייעת בבחירת הטיפול (טבלה 1). פריצת הדרך המשמעותית ביותר בשנים האחרונות, בתחום זה, כרוכה בפיתוח אמצעים המאפשרים הבחנה טובה יותר בין תת הקבוצות השונות של סרטן השד. באמצעות שימוש מושכל בשיטות של ביולוגיה מולקולרית, ניתן להיטיב לאפיין את הגידול הפרטני ובהתאם לכך לבחור את הטיפול המיטבי לכל מטופלת[7][8].
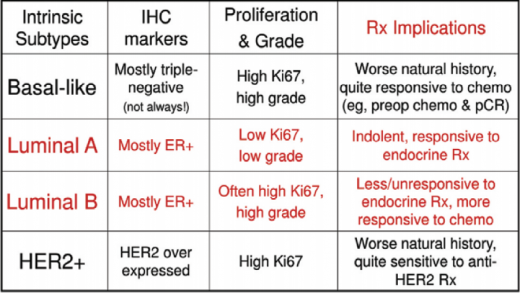
קביעת אופי הטיפול בהתאם לסוג הגידול
מהפרסום האחרון של EBCTCG משנת 2012, עולה כי היתרון היחסי בהישרדות כתוצאה ממתן כימותרפיה דומה בכל תת הקבוצות של סרטן השד, ללא תלות בגיל המטופלת, שלב המחלה, דרגת ההתמיינות או מידת הביטוי של הורמוני המין בתאי הגידול. עם זאת, התרומה האבסולוטית של הטיפול הכימותרפי המשלים עבור המטופלת הפרטנית, תלויה בסיכויי ההישרדות הבסיסיים טרם הטיפול, ואלו נקבעים על פי הביולוגיה של הגידול ומסת הגידול בשד ובבלוטות הלימפה האזוריות. לכן, על פי ההמלצות הבינלאומיות, יש לבסס את ההחלטה לגבי מתן טיפול כימותרפי על פי תת-הסוג הביולוגי של הגידול ושלב המחלה. בנוסף, ניתן לעשות שימוש מושכל במבחנים גנומיים כגון Oncotype Dx או Mammaprint[7][8] כאשר ההתוויה למתן טיפול כימותרפי אינה חד-משמעית (לדוגמה, בגידול מסוג Luminal B ללא מעורבות משמעותית של בלוטות הלימפה האזוריות). שיטות אלו מסייעות בקביעת הסיכון הראשוני לחזרת המחלה במטופלת הפרטנית ומנבאות את התרומה להישרדות כתוצאה ממתן טיפול כימותרפי משלים.
במצבים בהם הגידול הוא מסוג Luminal A, ניתן להסתפק בטיפול הורמונלי ללא צורך במתן כימותרפיה, אלא אם קיימת מעורבות משמעותית של בלוטות הלימפה. בגידול מסוג Luminal B המבטא גם HER2 בעודף, מומלץ טיפול משולב בכימותרפיה, טיפול הורמונלי ומתן Trastuzumab. בתת-הקבוצה בה נכללות נשים עם גידולים ממאירים מסוג HER2 positive שאינם מבטאים ER/PR, ניתן טיפול משולב בכימותרפיה וב-Trastuzumab[9][10][11]. גידולים מסוג Basal-like, הקרויים גם Triple Negative, נחשבים לאלימים ביותר (למעט תת-סוגים היסטולוגיים המאופיינים במהלך לא אלים) והם יטופלו לרוב בכימותרפיה, אלא אם קיימת התווית נגד לכך.
סוגי הטיפול המשלים בסרטן השד
ראו גם – הטיפול הכימי וההורמונלי בסרטן השד
טיפול הורמונלי משלים
במקרים בהם הגידול מבטא קולטנים להורמוני המין, בין אם הגידול הינו מסוג Luminal A או Luminal B, מומלץ מתן טיפול הורמונלי משלים, בלא תלות בשאלה האם ניתן למטופלת גם טיפול כימותרפי, או טיפול ביולוגי אחר[2]. ממחקר ATLAS שנמשך שנים רבות ותוצאותיו פורסמו בשנת 2013, עולה כי במטופלות עם סיכון מוגבר להישנות המחלה, יש יתרון משמעותי במתן Tamoxifen לעשר שנים, לעומת חמש שנים, כפי שהיה מקובל בעבר[12].
טיב התכשירים ההורמונליים הניתנים, מותנה בעיקר ברמת התפקוד השחלתי של המטופלת. כאשר מדובר באשה אצלה עדיין קיימת פעילות שחלתית, טיפול הבחירה הוא מתן Tamoxifen למשך 10-5 שנים. אם המטופלת נכנסת לגיל המעבר במהלך טיפול זה, מתן תרופה מסוג Letrozole (תכשיר מקבוצת מעכבי ארומטאז) לחמש שנים נוספות עשוי לתרום משמעותית לסיכויי ההישרדות. דיכוי הפעילות השחלתית, באמצעים תרופתיים או ניתוחיים, לא הוכחה כתורמת להישרדות, בהתווספה לטיפול ב-Tamoxifen. עם זאת, מספר עבודות הדגימו כי בנשים צעירות עם גידול המבטא קולטנים להורמוני המין, מתן משלב של Tamoxifen ודיכוי שחלתי, יעיל באותה מידה כמו התשלובת הכימותרפית CMF. לאור זאת, ניתן להשתמש במשלב הורמונלי זה כחלופה לטיפול הכימותרפי במצבים המתאימים לכך.
במטופלות לאחר חדילת אורח (Menopause), מומלץ לשלב תכשירים מקבוצת מעכבי ארומטאז (Letrozole, Exemestane, Anastrozole), במהלך הטיפול ההורמונלי. ממחקרים שונים עולה כי הוספת תכשירים אלה מאריכה את ההישרדות ללא מחלה, אך אינה תורמת משמעותית להישרדות הכללית של המטופלות. את התכשירים הללו ניתן לשלב לאחר תקופה של שנתיים וחצי או לאחר חמש שנים של מתן Tamoxifen. לחלופין, ניתן לתת מעכב ארומטאז כטיפול ראשוני למשך חמש שנים[13]. לפני ההחלטה על בחירת המשלב ההורמונלי יש להביא בחשבון את הרעילות הנלווית לכל אחד מהתכשירים ואת העדפותיה של המטופלת.
טיפול כימותרפי משלים
לטיפול הכימותרפי המשלים קיימת השפעה מיטיבה כלשהי עבור כל מטופלת שעברה הסרת גידול ממאיר של השד[1]. עם זאת, יש לזכור כי טיפול זה כרוך בתופעות לוואי בלתי מבוטלות, ובהן רעילות לבבית ממתן אנתרציקלינים, העלולה לסכן את חיי המטופלת בשיעור של כ-0.3%. כמו כן תיתכן פגיעה עצבית תחושתית היקפית ממתן טקסנים, ועלייה של פי 2.5 בסיכון לחלות בלוקמיה חריפה. זאת מלבד רעילות חריפה כגון התקרחות, בחילות והקאות, רעילות ללשד העצם ועוד, המשפיעה על איכות חיי המטופלת במהלך חודשי הטיפול. בשנים האחרונות חל אמנם שיפור משמעותי בטיפול התומך, המאפשר מתן תרופות כימותרפיות במינונים ראויים, אך אין בכך כדי להסיר לחלוטין את הקושי הכרוך בטיפול זה. מסיבה זו מן הראוי לבחור במתן טיפול כימותרפי משלים רק למטופלות שעבורן מתן טיפול כזה יפחית באופן משמעותי את הסיכון למות מהמחלה ולהימנע ממתן טיפול שתרומתו להישרדות קטנה ואינה מצדיקה את הרעילות הכרוכה בו.
מתן טיפול כימותרפי מומלץ במרבית הגידולים מסוג Triple Negative, בכל הגידולים המבטאים HER2 בעודף, וכן בגידולים מסוג Luminal עם סיכון גבוה להישנות. תרומת הטיפול הכימותרפי משמעותית יותר בגידולים שהם ER/PR שליליים. התכשירים הכימותרפיים שבשימוש כוללים אנתרציקלינים ו/או טקסנים. על פי תוצאות מחקר EBCTCG, מתן משלבים שהכילו תכשירים משתי קבוצות אלו, הביא להפחתה של 36% בתמותה מסרטן לעומת מטופלות שלא קיבלו כימותרפיה כלל. ההפחתה בתמותה נצפית גם לאחר חמש שנים. לתוספת של טקסנים לטיפול הכימותרפי תרומה מועטה, אך אמיתית, להישרדות חולות עם בלוטות נגועות. לגידולים בעלי קוטר גדול, ההחלטה על מתן טיפול כימותרפי נקבעת כתלות בביולוגיה של הגידול, ובהם ראוי לעשות שימוש מושכל בשיטות גנומיות.
תשלובת שאינה מכילה אנתרציקלינים, כגון Taxotere בשילוב עם Cytoxan, אפשרית כחלופה במצבים נבחרים. הטיפול הכימותרפי נמשך בין שמונה לעשרים וארבעה שבועות, בתלות בתשלובת שנבחרה. מתן טיפול במינון צפוף (Dose dense) מקובל כיום וניתן בשילוב תמיכה של גורם צמיחה מסוג GCSF (Granulocyte Colony-Stimulating Factor), במטרה למנוע התפתחות נויטרופניה. מתכונת זו משפרת את תרומת הטיפול בעיקר בגידולים שאינם מבטאים ER ו-PR[14].
טיפול המכוון כנגד הקולטן הממברנלי HER2
טיפול מכוון מטרה ב-Trastuzumab ניתן במשולב עם טיפול כימותרפי ומיועד עבור גידולים המבטאים HER2 בעודף, כתוצאה מהגברת ביטוי של הגן המקודד לקולטן זה. מאז 2005 פורסמו מספר מחקרים שכללו מטופלות רבות, אשר הוכיחו את ההשפעה המיטיבה של Trastuzumab על קבוצת חולות זו[9][10][11]. בעדכון של מחקרים אלו שפורסם לאחרונה, נראה כי השפעה זו אינה דועכת ונותרת בעינה גם לאחר חציון של שמונה שנות מעקב. תרומתו היחסית של Trastuzumab להישרדות דומה בכל תת-הקבוצות של המטופלות, ללא תלות בגיל המטופלת, במידת הביטוי של הקולטנים להורמוני המין, בגודל הגידול, בדרגת ההתמיינות שלו או במעורבות בלוטות הלימפה האזוריות. במתן טיפול זה הסיכון היחסי להישנות פוחת ב-40% והסיכון לתמותה מהמחלה פוחת ב-37%, בהשוואה למתן טיפול כימותרפי בלבד. מומלץ לתת Trastuzumab במשך שנה, מכיוון שלא נמצא יתרון במתן התרופה למשך שנתיים, וגם מתן התכשיר לחצי שנה בלבד לא צלח[15]. מתן תרופה זו בשילוב עם כימותרפיה, הפך לטיפול הבחירה עבור כל הנשים שאובחנו עם סרטן שד פולשני המבטא HER2 בעודף. בשלב מחלה מוקדם, ללא מעורבות בלוטות בית השחי, ניתן ככל הנראה, להסתפק בטקסנים כבסיס הכימותרפי בטיפול, ואין הכרח במתן אנתרציקלינים.
בדומה לפריצת הדרך הקשורה בזיהוי HER2 כאתר מטרה לטיפול משלים, נבחנים כיום אתרים נוספים בחולות עם סרטן שד גרורתי. התכשירים שיעילותם תוכח במסגרת זו עשויים להיבדק בהמשך גם עבור נשים עם סרטן שד מוקדם כטיפול משלים, או כטיפול קדם ניתוחי.
טיפול המותאם אישית לחולה
כפי שתואר עד כה, ER, PR, ו-HER2 משמשים כגורמי חיזוי לבחירת טיפול הורמונלי מכוון מטרה, או כנגד הקולטן HER2 בהתאמה. ההחלטה לגבי מתן טיפול כימותרפי משלים נעשית באופן מסורתי על בסיס הערכת הסיכון להישנות סרטן השד על פי גורמים פרוגנוסטיים שונים ובהם גיל החולה, גודל הגידול, מספר בלוטות הלימפה האזוריות הנגועות, דרגת ההתמיינות, מדד השגשוג Ki67, לצד רמות PR ו-ER וביטוי יתר של הקולטן HER2 בתאי הגידול. בהתאם לכך, נקבע הצורך במתן טיפול משלים לסוגיו, תוך התייחסות למצבה הכללי של המטופלת ולהעדפותיה. לצורך שקלול מידת הסיכון להישנות המחלה ולתמותה ממנה עבור המטופלת הפרטנית, ניתן להיעזר בתוכנות מחשב שיועדו לכך דוגמת ה-!Adjuvant[6].
תוכנה זו, המצויה באינטרנט, מחשבת גם את התרומה המוחלטת של הטיפול הכימותרפי וההורמונלי להישרדות עבור המטופלת, על פי נתוני מחלתה. כאשר קיים ספק באשר לצורך במתן טיפול כימותרפי משלים, ניתן ליישם שיטות גנומיות המשפרות את היכולת לברור באילו מקרים ניתן לוותר על טיפול זה, כיוון שתרומתו תהיה זניחה. שיטות אלו, המתבססות על טכנולוגיות חדשניות שונות, בוחנות את טביעת האצבעות המולקולרית של הגידול, דהיינו, באיזו מידה הגידול הנבדק מבטא סדרת גנים נבחרים בצורה חריגה, לעומת רקמת שד נורמלית. בהתאם לתוצאה המתקבלת ניתן להעריך את סיכויי ההישרדות של המטופלת ולנבא את מידת התרומה של טיפול כימותרפי לסיכויים אלה. מספר טכנולוגיות כאלו מצויות כיום בשימוש ובהן PAM50, MammaPrint ו-Oncotype DX[7][8]. פיתוח שיטות אלו התבסס על שימוש במידע רטרוספקטיבי ועל כן יש להתייחס לתוצאותיהן בזהירות הראויה. מספר מחקרים בוחנים כיום שיטות אלו באופן פרוספקטיבי (MINDACT, TAILORx, RxPONDER). פרסום ממצאי מחקרים אלו בעתיד יאפשר שימוש מדויק יותר בכלים חשובים אלו.
ביבליוגרפיה
- ↑ 1.0 1.1 1.2 Early Breast Cancer Trialists' Collaborative Group (EBCTCG), Peto R, Davies C, Godwin J, Gray R, Pan HC, Clarke M, Cutter D, Darby S, McGale P, Taylor C, Wang YC, Bergh J, Di Leo A, Albain K, Swain S, Piccart M, Pritchard K. Comparisons between different polychemotherapy regimens for early breast cancer: meta-analyses of long-term outcome among 100,000 women in 123 randomised trials. Lancet. 2012;379(9814):432.
- ↑ 2.0 2.1 2.2 Early Breast Cancer Trialists' Collaborative Group (EBCTCG), Davies C, Godwin J, Gray R, Clarke M, Cutter D, Darby S, McGale P, Pan HC, Taylor C, Wang YC, Dowsett M, Ingle J, Peto R. Relevance of breast cancer hormone receptors and other factors to the efficacy of adjuvant tamoxifen: patient-level meta-analysis of randomised trials. Lancet. 2011 ;378(9793)771
- ↑ Berry DA, Cronin KA, Plevritis SK, Fryback DG, Clarke L, Zelen M, Mandelblatt JS, Yakovlev AY, Habbema JD, Feuer EJ, Cancer Intervention and Surveillance Modeling Network (CISNET) Collaborators. Effect of screening and adjuvant therapy on mortality from breast cancer. N Engl J Med. 2005:353(17): 1784.
- ↑ 4.0 4.1 4.2 Perou CM, Sorlie T, Eisen MB, van de Rijn M, Jeffrey SS, Rees CA, Pollack JR, Ross DT, Johnsen H, Akslen LA, Fluge O, Pergamenschikov A, Williams C, Zhu SX, L0nning PE, B0rresen-Dale AL, Brown PO, Botstein D. Molecular portraits of human breast tumours. Nature. 2000;406(6797):747.
- ↑ 5.0 5.1 Comprehensive molecular portraits of human breast tumours. Cancer Genome Atlas Network. Nature. 2012:490(7418):61.
- ↑ 6.0 6.1 Adjuvant! Breast Cancer Help Files, www.adjuvantonline.com/index.jsp (Accessed on October 14, 2011).
- ↑ 7.0 7.1 7.2 Paik S, Shak S, Tang G, Kim C, Baker J, Cronin M, Baehner FL, Walker MG, Watson D, Park T, Hiller W, Fisher ER, Wickerham DL, Bryant J, Wolmark N. A multigene assay to predict recurrence of tamoxifen-treated, node-negative breast cancer. N Engl J Med. 2004;351(27):2817.
- ↑ 8.0 8.1 8.2 van 't Veer LJ, Dai H, van de Vijver MJ, He YD, Hart AA, Mao M, Peterse HL, van der Kooy K, Marton MJ, Witteveen AT, Schreiber GJ, Kerkhoven RM, Roberts C, Linsley PS, Bernards R, Friend SH. Gene expression profiling predicts clinical outcome of breast cancer. Nature. 2002:41 5(6871):530.
- ↑ 9.0 9.1 Romond EH, Perez EA, Bryant J, Suman VJ, Geyer CE Jr, Davidson NE, Tan-Chiu E, Martino S, Paik S, Kaufman PA, Swain SM, PisanskyTM, Fehrenbacher L, Kutteh LA, Vogel VG, Visscher DW, Yothers G, Jenkins RB, Brown AM, Dakhil SR, Mamounas EP, Lingle WL, Klein PM, Ingle JN, Wolmark N. Trastuzumab plus adjuvant chemotherapy for operable HER2-positive breast cancer. N Engl J Med. 2005;353(16):1673.
- ↑ 10.0 10.1 Piccart-Gebhart MJ, Procter M, Leyland-Jones B, Goldhirsch A, Untch M, Smith I, Gianni L, Baselga J, Bell R, Jackisch C, Cameron D, Dowsett M, Barrios CH, Steger G, Huang CS, Andersson M, Inbar M, Lichinitser M, Lang I, Nitz U, Iwata H, Thomssen C, Lohrisch C, SuterTM, Ruschoff J, Suto T, Greatorex V, Ward C, Straehle C, McFadden E, Dolci MS, Gelber RD, Herceptin Adjuvant (HERA) Trial Study Team. Trastuzumab after adjuvant chemotherapy in HER2-positive breast cancer. N Engl J Med. 2005;353(16):1659.
- ↑ 11.0 11.1 Slamon D, Eiermann W, Robert N, Pienkowski T, Martin M, Press M, Mackey J, Glaspy J, Chan A, Pawlicki M, Pinter T, Valero V, Liu MC, Sauter G, von Minckwitz G, Visco F, Bee V, Buyse M, Bendahmane B, Tabah-Fisch I, Lindsay MA, Riva A, Crown J, Breast Cancer International Research Group Adjuvant trastuzumab in HER2-positive breast cancer. N Engl J Med. 2011 ;365(14): 1273.
- ↑ Davies C, Pan H, Godwin J, Gray R, Arriagada R, Raina V, Abraham M, Medeiros Alencar VH, Badran A, Bonfill X, Bradbury J, Clarke M, Collins R, Davis SR, Delmestri A, Forbes JF, Haddad P, Hou MF, Inbar M, Khaled H, Kielanowska J, Kwan WH, Mathew BS, Mittra I, Muller B, Nicolucci A, Peralta O, Pernas F, Petruzelka L, Pienkowski T, Radhika R, Rajan B, Rubach MT, Tort S, Urrutia G, Valentini M, Wang Y, Peto R, Adjuvant Tamoxifen: Longer Against Shorter (ATLAS) Collaborative Group. Long-term effects of continuing adjuvant tamoxifen to 10 years versus stopping at 5 years after diagnosis of oestrogen receptor-positive breast cancer: ATLAS, a randomised trial. Lancet, 2013;381(9869):805.
- ↑ BIG 1-98 Collaborative Group, Mouridsen H, Giobbie-Hurder A, Goldhirsch A, Thurlimann B, Paridaens R, Smith I, Mauriac L, Forbes JF, Price KN, Regan MM, Gelber RD, Coates AS. Letrozole therapy alone or in sequence with tamoxifen in women with breast cancer. N Engl J Med. 2009:361 (8):766.
- ↑ Bonilla L, Ben-Aharon I, Vidal L, Gafter-Gvili A, Leibovici L, Stemmer SM. Dose-dense chemotherapy in nonmetastatic breast cancer: a systematic review and meta-analysis of randomized controlled trials. J Natl Cancer Inst. 2010 Dec; 102(24): 1845-54. Epub 2010 Nov 23.
- ↑ Pivot X, Romieu G, Debled M, Pierga JY, Kerbrat P, BachelotT, Lortholary A, EspieM, Fumoleau P, Serin D, Jacquin JP, Jouannaud C, Rios M, Abadie-Lacourtoisie S, Tubiana-Mathieu N, Cany L, Catala S, Khayat D, Pauportel, Kramar A, PHARE trial investigators. 6 months versus 12 months of adjuvant trastuzumab for patients with HER2-positive early breast cancer (PHARE): a randomised phase 3 trial. Lancet Oncol. 2013;14(8):741
קישורים חיצוניים
המידע שבדף זה נכתב על ידי ד"ר הדסה גולדברג - מנהלת המכון האונקולוגי, המרכז הרפואי לגליל, נהריה


 כניסה
כניסה  עקבו אחרינו בפייסבוק
עקבו אחרינו בפייסבוק