פרפור פרוזדורים - טיפול בדרונדרון - Atrial fibrillation - treatment with Dronedarone
| פרפור פרוזדורים - טיפול בדרונדרון | ||
|---|---|---|
| Atrial fibrillation - treatment with Dronedarone | ||
| יוצר הערך | ד"ר גיא עמית
|
|
לערכים נוספים הקשורים לנושא זה, ראו את דף הפירושים – פרפור פרוזדורים
פרפור פרוזדורים הוא הפרעת הקצב השכיחה ביותר, והיא נושאת בחובה תחלואה ותמותה משמעותיות[1]. למרות מחקרים רבים בתחום, שלושת עקרונות הטיפול בפרפור פרוזדורים - שליטה במקצב (Rhythm control), בקצב (Rate control) וטיפול נגד קרישה - אינם מיושמים בצורה אחידה. נדבך נוסף במורכבות הטיפול הוא שלכל חולה נגזרת תבנית טיפול אינדיווידואלית לפי צרכיו.
שליטה במקצב פירושה ניסיון לשמר מקצב סינוס ולמנוע הופעת פרפור פרוזדורים המבוצעת על ידי תרופות נגד הפרעות קצב או על ידי צריבה מילעורית (Percutaneous) או כירורגית. אף על פי שתרופות נגד הפרעות קצב נמצאות בשימוש שנים רבות, העדויות לתרומתן המיטיבה על תחלואה ותמותה היו עד כה דלות מאוד[2]. נוסף על כך, רוב התרופות נושאות בחובן סיכון של תופעות לוואי שלעתים מאפיל על התועלת נוגדת הפרפור שבהן.
לאחרונה, בעקבות שורת מחקרים קליניים, אושר השימוש בתרופה חדשה, Multaq (Dronedarone), כטיפול נגד הפרעות קצב בפרפור פרוזדורים. להלן עיקרי העדויות העולים מן המחקרים המדוברים, ומשנית לכך ההתוויות העדכניות לשימוש בתרופה.
פרמקוקינטיקה ופרמקודינמיקה
התרופה דומה מבחינת המבנה המולקולרי ל-Amiodarone, אולם אין בה מולקולות יוד[3]. על פי הסיווג המקובל לתרופות נגד הפרעות קצב, ובהתאם למנגנון פעילותה על מספר תעלות, היא משויכת לקבוצה III[4]. קלינית, התרופה מאטה את קצב הסינוס, מאריכה את מרווח AH (AH Interval) והתקופות הרפרקטוריות של של הקשרית העלייתית חדרית (Atrioventricular node) והחדרים[5]. נוסף על כך, היא מעכבת בתא-אדרנרגית (Beta-adrenergic blocking agent).
במודלים של חיות מנעה Multaq מאוץ חדרים (Ventricular tachycardia) ופרפור חדרים (Ventricular fibrillation) בזמן איסכמיה חדה[6]. כמו כן, הודגם כי למרות הארכת מה של פוטנציאל הפעולה, שמתבטאת בהארכת מרווח QT באלקטרוקרדיוגרם (ECG - Electrocardiogram), המאפשרת את ההשפעה נוגדת פרפור הפרוזדורים, אין התרופה גורמת לדפולריזציות (Depolarizations) מאוחרות, ולכן אינה מעודדת הפרעות קצב (אינה פרו-אריתמית)[7].
התרופה נספגת היטב ונקשרת לחלבוני הדם. במתן של פעמיים ליום היא מגיעה לרמות יציבות בדם אחרי 4-8 ימים. בכבד היא עוברת פירוק על ידי האנזים CYP3A4, אולם גם המטבוליט הינו פעיל.
התרופה מופרשת ברובה דרך דרכי העיכול, וזמן מחצית החיים לפינויה מהגוף הוא 20-40 שעות. בשל היותה מפורקת בכבד יש לה מספר אינטראקציות עם תרופות, כגון:
התרופה מעלה את רמת הקראטינין בדם, אולם לא משפיעה על תפקוד הכליות והסינון הפקעתי (Glomerular filtration)[4].
יעילות
שמירת מקצב סינוס
במחקר ה-DAFNE (Dronedarone Atrial FibrillatioN study after Electrical cardioversion) נבדקו מינונים שונים של Multaq לשמירת מקצב הסינוס לאחר היפוך קצב חשמלי בכ-200 חולים.
החולים חולקו לקבוצות מינון יומי: 800 מ"ג, 1,200 מ"ג או 1,600 מ"ג, הניתנים כשני חצאי המינון ביום (בכל הקבוצות) או אינבו (Placebo).
המעקב אחר החולים נעשה בעזרת ניטור טרנס-טלפוני. נבדק הזמן בין תחילת הטיפול עד לאירוע ראשון בן 10 דקות לפחות של פרפור פרוזדורים. חציון זמן זה היה חמישה ימים בקבוצת האינבו לעומת 60 יום בקבוצת מינון ה-800 מ"ג ביום. בחצי שנה, 10% ו-35% שמרו על מקצב סינוס בקבוצות האינבו וה-Multaq 800 מ"ג, בהתאמה. לא נמצאו הבדלים בין קבוצות המינון האחרות לאינבו, אולם היו יותר הפסקות בתרופה בשל תופעות לוואי ככל שהמינון היומי היה גבוה יותר.
לנוכח זאת, המינון שהשיג יעילות מרבית וכמות מועטה ביותר של תופעות לוואי נקבע כ-400 מ"ג פעמיים ביום (800 מ"ג ליום), והוא המינון היחיד שנבחן לאחר מכן בכל המחקרים הבאים.
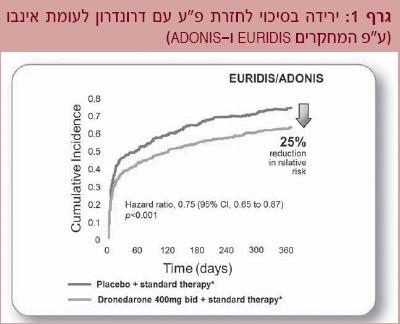
שני מחקרים נוספים - מחקר ה-ADONIS, שהוא מחקר אמריקאי-אוסטרלי-אפריקאי, ומחקר ה-EURIDIS האירופאי, בדקו את הטיפול ב-Multaq לשמירה על מקצב סינוס בפרפור ורפרוף פרוזדורים.
המחקרים הכלילו חולים שעברו לפחות תקרית אחת של פרפור פרוזדורים בשלושת החודשים לפני גיוסם למחקר, ושבעת הגיוס היו במקצב סינוס[8]. החולים עברו חלוקה אקראית (רנדומיזציה) ל-Multaq 400 מ"ג פעמיים ביום לעומת אינבו; זאת כתוספת לחוסמי בטא, חוסמי סידן או Digoxin. טיפול אחר נגד הפרעות קצב לא ניתן. הוצאו מן המחקר חולים עם הפרעות הולכה וברדיקרדיה, אי ספיקת לב משמעותית ואי ספיקת כליות.
התוצא העיקרי, בדומה למחקר הקודם, היה הזמן מהגיוס ועד חזרת פרפור פרוזדורים בן 10 דקות לפחות. שני המחקרים פורסמו כמאמר אחד ואף התוצאות הוצגו בנפרד ומאוחדות. חציון הזמן עד לחזרת פרפור פרוזדורים היה ארוך משמעותית בקבוצת ה-Multaq מול האינבו (116 לעומת 53 יום) (גרף 1).
בדומה, אחוז החולים בהם חזר פרפור הפרוזדורים בשנה אחת היה נמוך משמעותית בקבוצת התרופה (64% לעומת 75%, p<0.01). כלומר, אף שהזמן עד להופעת פרפור פרוזדורים התארך ולמרות אחוז נמוך יותר של חזרת הפרפור בקבוצת ה-Multaq, רוב החולים חוו פרפור פרוזדורים חוזר תוך שנה.
נוסף על כך, היות והחולים שידרו רק פרפור פרוזדורים שגרם לתסמינים, ייתכן שהוחמצו אירועי פרפור פרוזדורים "שקטים" כך שאחוז החזרה אף גבוה יותר. כמו כן, אין מידע לגבי האורך והכמות של האירועים שחוו הנבדקים.
עם זאת, החזרה הראשונה של פרפור פרוזדורים הייתה בקצב לב איטי יותר באופן משמעותי בקבוצת ה-Multaq (חציון קצב הלב בעת הפרפור: 103 פעימות לדקה עם Multaq מול 117 פעימות לדקה עם אינבו). נוסף על כך, אנליזה פוסט-הוק (Post-hoc) מצאה הפחתה בשיעור התוצא המשולב של אשפוז או מוות בקבוצת הטיפול, תוצאה שהביאה למחקרים נוספים בהמשך.
האטת קצב הלב
כאמור, במחקרים הקודמים בחולים שטופלו ב-Multaq ושהייתה אצלם חזרה של פרפור פרוזדורים, הקצב החדרי היה איטי יותר לעומת חולים שטופלו באינבו. מחקר ה-ERATO (The Efficacy and safety of Dronedarone for the cOntrol of ventricular rate during atrial fibrillation) גייס 174 חולים עם פרפור פרוזדורים קבוע, תסמיני, וקצב חדרי מהיר מ-80 פעימות לדקה ל-Multaq לעומת אינבו. זאת, כתוספת לטיפול התרופתי הרגיל שלהם שכלל חוסמי בטא (בכ-50%), Digoxin או חוסמי סידן (בכ-50%).
כעבור 14 יום מתחילת הטיפול היה קצב הלב בקבוצת ה-Multaq נמוך בממוצע ב-11 פעימות לדקה (באנליזת הולטר 24 שעות) מקבוצת האינבו (p<0.01). האטת קצב הלב הייתה משמעותית יותר בחולים שקיבלו חוסמי בטא ולא חוסמי סידן. האטת קצב הלב עם Multaq נצפתה הן במנוחה והן לאחר מאמץ בהשוואה לתחילת המחקר. גם כעבור 4 חודשים הייתה ירידה משמעותית בקצב הלב הממוצע ב-24 שעות בקבוצת ה-Multaq לעומת האינבו ללא קשר לטיפול התרופתי הנוסף.
חשוב לציין לגבי מחקר זה, שקצב הלב הממוצע בזמן תחילת המחקר לא היה מהיר מאוד (85, 90 פעימות לדקה בקבוצות ה-Multaq והאינבו, בהתאמה) וכלל לא ברור מהו קצב הלב המיטבי במנוחה בפרפור פרוזדורים קבוע. עם זאת, נתונים אלו והנתונים מהמחקרים הללו מראים כי לתרופה השפעה מיטיבה על קצב הלב בזמן פרפור עליות, קרוב לוודאי בשל השפעתה על ההולכה בקשרית העלייתית-חדרית.
הפחתת תחלואה ותמותה ממחלות לב וכלי דם
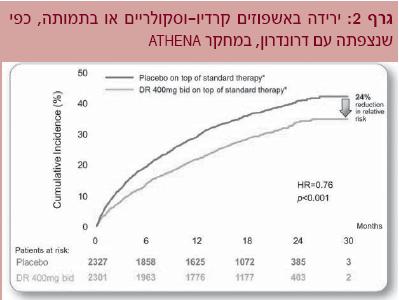
מטרתו של מחקר ה-ATHENA[10] הייתה לבדוק אם יש לתרופה השפעה מגינה מפני תמותה ואשפוזים בשל מחלות לב וכלי דם.
גויסו 4,544 חולים עם פרפור או רפרוף עליות התקפי ואשר היו מבוגרים מגיל 70 או שנוסף על הפרעת הקצב היו להם אחד או יותר ממאפייני סיכון גבוה שכללו:
- יתר לחץ דם
- סוכרת
- אירוע מוחי בעבר
- ירידה בתפקוד הלב - אחוז ההזרקה של חדר שמאל נמוך מ-40% (Left ventricular ejection fraction ≤40%)
החולים חולקו לקבוצת Multaq (400 מ"ג פעמיים ביום) או אינבו. חציון המעקב היה 21 חודשים, ורוב החולים נטלו גם טיפול מקובל בחוסמי בטא, מעכבי האנזים הממיר אנגיוטנסין (Angiotensin-converting-enzyme inhibitors) או חוסמי הקולטן לאנגיוטנסין (Angiotensin receptor blockers). נמצא שהתוצא הראשוני של תמותה או אשפוז בשל מחלות לב וכלי דם היה נמוך ב-24% בקבוצת ה-Multaq (רווח בר סמך (CI - Confidence interval) 95%, 0.69-0.84, יחס הסיכון (HR - Hazard ratio) 0.76) (גרף 2).
כמו כן, נצפתה ירידה בתמותה ממחלות לב וכלי דם (ב-29%, p=0.03) ובתמותה מהפרעות קצב (ב-45%, p<0.01). באנליזה מאוחרת נצפתה גם ירידה בכמות האירועים המוחיים.
מחקר זה הוא חדשני מבחינת העובדה שנעשה בו שימוש בתרופה נגד הפרעות קצב לצורך הפחתת תמותה ותחלואה ללא התחשבות בחזרת הפרעות הקצב, והוא אף הדגים את יעילותה. מצד אחד, זהו חוזקו הגדול של מחקר זה. לאף תרופה נגד הפרעות קצב עד כה אין יכולת מוכחת להפחית תמותה או אשפוזים בשל מחלות לב וכלי דם. מצד שני, השימוש העיקרי בתרופה הוא לצורך הפחתת כמות אירועי פרפור פרוזדורים, שיפור איכות החיים והורדת התחלואה הנלווית, כגון אירועים מוחיים, ומבחינה זו התקבלה תשובה חלקית בלבד.
התוויות נגד
מחקר ה-ANDROMEDA בדק אם Multaq יכולה להפחית את קצב האשפוזים בשל אי ספיקת הלב כמו גם תמותה משנית להפרעות קצב. למחקר גויסו חולים שאושפזו בשל החמרת אי ספיקת הלב - דרגה III או IV בסולם NYHA (New York Heart Association) - ותפקוד ירוד של חדר שמאל, עם אחוז הזרקה נמוך מ-35% (Left ventricular ejection fraction ≤35%). לכ-40% הייתה גם היסטוריה של פרפור פרוזדורים.
המחקר הופסק מוקדם בשל תמותת יתר בזרוע ה-Multaq לעומת זרוע האינבו (HR=2.13, 95% CI, 1.07–4.25). במעקב של 6 חודשים נוספים לא היה כבר הבדל בתמותה, אולם בעקבות מחקר זה הומלץ לא לטפל בתרופה בחולים עם אי ספיקת לב משמעותית המוגדרת כדרגה IV בסולם ה-NYHA, או כדרגה III או II שעברו אפיזודה של החמרה לאחרונה.
התרופה אסורה לשימוש בחולים עם אי ספיקת לב קשה, דרגה III או IV.
תופעות לוואי
פרופיל תופעות הלוואי של התרופה הוא טוב בהרבה מ-Amiodarone, והיא אינה מעודדת הפרעות קצב כמו תרופות אחרות לפרפור פרוזדורים. תופעות הלוואי השכיחות יותר הן בעיקר קלות וכוללות, אולם לא מוגבלות, לכאבי בטן, בחילות, פריחה וגרד. אולם, במסגרת מעקב אחרי התרופה, פרסם ארגון התרופות והמזון האמריקאי חשד לנזק כבדי עם התרופה שהוא אומנם נדיר, אבל בעקבותיו מומלץ מעקב אחרי תסמינים המחשידים לפגיעה כבדית, וכן לעקוב אחרי תפקודי הכבד, במיוחד במחצית השנה הראשונה לטיפול[11].
ההמלצות בארץ כרגע הן לעקוב אחר תפקודי כבד כל חודש ב-6 חודשים ראשונים, ולאחר מכן כל 3 חודשים, ולהפסיק את הטיפול אם קיימת עלייה של יותר מ-3 פעמים ערך הבסיס.
מחקר ה-DIONYSOS[9] השווה באופן מבוקר וכפול-סמיות (Controlled double blind study) Multaq (400 מ"ג פעמיים ביום) עם Amiodarone (600 מ"ג ליום לחודש ואחר כך 200 מ"ג ליום) למשך 6 חודשים לפחות, ב-504 חולים עם פרפור פרוזדורים. לחולים שלא הפכו למקצב סינוס עם תחילת תרופת המחקר, בוצע היפוך קצב חשמלי.
תוצא המחקר העיקרי, חזרה של פרפור פרוזדורים, חוסר יכולת להפוך למקצב סינוס או הפסקת תרופת המחקר בשנה אחת, היה גבוה יותר בקבוצת ה-Multaq (75%) לעומת ה-Amiodarone (60%) (p<0.01). חזרת פרפור פרוזדורים בלבד נרשמה ב-63% ממטופלי ה-Multaq ו-42% מטופלי ה-Amiodarone. תופעות לוואי נרשמו ב-39% ממטופלי ה-Multaq לעומת 44% ממטופלי ה-Amiodarone (p=0.13).
עם זאת, היו פחות תופעות לוואי הקשורות לבלוטת התריס, העור, העיניים ומערכת העצבים, כמו גם פחות הארכות מקטע QTc מעל 500 מ"ש ופחות עלייה בערכי ערך הקרישה המנורמל (INR - international normalized ratio) מעל לערך הטיפולי עם ה-Multaq. כלומר, ה-Multaq היה פחות יעיל מ-Amiodarone, אולם פרופיל תופעות הלוואי שלו היה טוב יותר.
זמינות בארץ
התרופה מאושרת לשימוש על ידי משרד הבריאות להורדת תחלואה ממחלות לב וכלי דם ולהורדת קצב הלב בחולים עם פרפור או רפרוף עליות, אשר נמצאים בקצב סינוס או לפני היפוך קצב, והינם בעלי גורמי סיכון נוספים, כגון:
- גיל >70 שנה
- סוכרת
- יתר לחץ דם
- אירוע מוחי
- הגדלת עליות הלב
- ירידה בתפקוד הסיסטולי (LVEF <40%)
התרופה אף מאושרת בסל הבריאות לחולים עם התוויות נגד ל-Amiodarone או שפיתחו תופעת לוואי לתרופה זו.
ביבליוגרפיה
- Benjamin EJ, Wolf PA, D’Agostino RB, et al. Impact of atrial fibrillation on the risk of death: the Framingham Heart Study. Circulation 1998;98(10):946–952
- Corley SD, Epstein AE, DiMarco JP, et al. Relationships between sinus rhythm, treatment, and survival in the Atrial Fibrillation Follow-Up Investigation of Rhythm Management (AFFIRM) Study. Circulation 2004;109(12):1509–1513
- Kathofer, et al. Cardiovasc Drug Rev 2005;23(3):217-230
- Briefing Information for the Mar 18, 2009 Meeting of the Cardiovascular and Renal Drugs Advisory Committee 2009; Availablefrom:
- Manning A, Thisse V, Hodeige D, et al. SR 33589, a new amiodarone-like antiarrhythmic agent: electrophysiological effects in anesthetized dogs. J Cardiovasc Pharmacol 1995;25(2):252–261
- Manning AS, Bruyninckx C, Ramboux J, et al. SR 33589, a new amiodarone-like agent: Effect on ischemia- and reperfusion-induced arrhythmias in anesthetized rats. J Cardiovasc Pharmacol 1995;26(3):453–461
- Varro A, et al. Brit J Pharmacol 2001;133:625-634
- Singh BN, Connolly SJ, Crijns HJ, et al. Dronedarone for maintenance of sinus rhythm in atrial fibrillation or flutter. NEJM 2007;357(10):987–999
- Le Heuzey JY, De Ferrari GM, Radzik D, et al. A short-term, randomized, double-blind, parallel-group study to evaluate the efficacy and safety of Dronedarone versus amiodarone in patients with persistent atrial fibrillation: the DIONYSOS study. J CardiovascElectrophysiol 2010;21(6):597-605. Epub 2010
- Hohnloser SH, Crijns HJ, van Eickels M, et al. Effect of Dronedarone on
cardiovascular events in atrial fibrillation. NEJM 2009;360(7):668–678
קישורים חיצוניים
המידע שבדף זה נכתב על ידי ד"ר גיא עמית, מנהל היחידה לטיפול בהפרעות קצב הלב (אלקטרופיזיולוגיה), המערך הקרדיולוגי, המרכז הרפואי האוניברסיטאי סורוקה, באר שבע


 כניסה
כניסה  עקבו אחרינו בפייסבוק
עקבו אחרינו בפייסבוק