קלאסטרין - Clusterin
| מדריך בדיקות מעבדה | |
| קלאסטרין | |
|---|---|
| Clusterin | |
| שמות אחרים | CLU, ApoJ או apolipoprotein J; testosterone-repressed prostate message 2 (או TRPM-2); complement lysis inhibitor (או CLI), secreted glycoprotein gp80; complement-associated protein SP-40, AAG4, KUB1, sulfated glycoprotein-2 ,SGP2 NA1/NA2. |
| מעבדה | פתולוגיה ברקמה |
| תחום | חלבון רב-תכליתי בסוגי סרטן ובמחלות נוירו-דגנרטיביות. |
| יוצר הערך | פרופ' בן-עמי סלע |
המבנה של clusterin
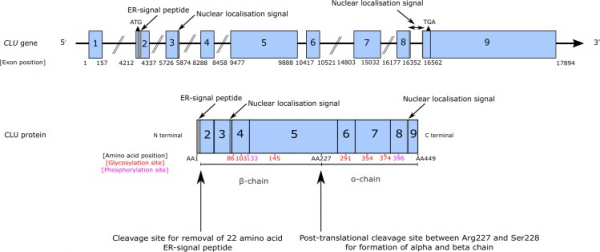
Clusterin הוא גליקו-חלבון הטרודימרי עתיר חומצה סיאלית כאשר כל מולקולה של clusterin מכילה 28 שיירים של חומצה סיאלית. המשקל המולקולרי של clusterin הוא 75–80 אלף דלטון, והוא מורכב מ-2 שרשרות פפטידיות (שרשרת α ושרשרת β) לא זהות הקשורות ביניהן על ידי 5 קשרים די-סולפידיים. בבני אדם, clusterin מקודד על ידי הגן CLU הממוקם על כרומוזום 8 בעמדה 18p21-p12, גן המכיל 9 אקסונים ומבטא שלושה איזופורמים שעברו splicing באקסון 1 (על פי Koltai ב-Onco Targets Ther משנת 2014). האיזופורמים ממוקמים באזורי-תא שונים: אחד מהם ממוקם בגרעין התא, איזופורם אחר ממוקם בציטופלזמה, והאיזופורם השלישי מופרש מהתא (Lin וחב' ב-J Hepatol משנת 2014). לאיזופורמים אלה תפקידים מנוגדים: האיזופורם בגרעין נקשר לחלבון Ku70 ועל ידי כך משחרר את BAX ומשרה בתאים אפופטוזיס (Sansanwal וחב' ב-J Am Soc Nephrol משנת 2015), בעוד שהאיזופורמים הציטופלזמטי והמופרש הם בעלי השפעה מעכבת אפופטוזיס. האיזופורם בגרעין מקודד לחלבון בעל משקל מולקולרי של 49KDa, בעוד שהאיזופורם המופרש שהוא האיזופורם העיקרי מקודד לחלבון בעל המשקל המולקולרי של KDa75-80 לאחר בשלותו (גליקוזילציה, הפרשה ודימריזציה). חלבון clusterin הבשל מכיל 449 חומצות אמינו. הגן CLU מבוטא חזק בכבד, במוח, בשחלות ובאשכים, ומבוטא בעוצמה מופחתת יותר בריאות, בלב, בשד ובטחול (Aronow וחב' ב-Proc Natl Acad Sci USA משנת 1993). ל-clusterin של אדם יש הומולוגיה של 75% עם זה של עכבר, והומולוגיה של 77% עם clusterin של חולדה.
Clusterin מסונתז כפוליפפטיד המכיל 427 חומצות אמינו, העובר ברטיקולום האנדופלזמטי ביקוע פרוטאוליטי בין Arg205 ו-Ser-206, ליצירת 2 תת-יחידות הנותרות קשורות ביניהן על ידי קשרים דיסולפידיים לקבלת הטרודימר. צורת הקודמן או ה-pre-clusterin, היא בעלת משקל מולקולרי של 69 קילו-דלטון, בעוד שמולקולת clusterin הבשלה שעברה גליקוזילציה היא בעלת משקל מולקולרי של 75–80 קילו-דלטון, והיא מכונה secretory clusterin או sClu. המבנה של clusterin מנבא שהוא מכיל סלילונים אמפיפתיים, העשויים לסייע לקשר שלו עם חלקיקי HDL. ה-clusterin הגרעיני (או nClusterin) מתורגם תחילה כקודמן של חלבון non-glycosylated, המכונה pnCLU והוא בעל משקל מולקולרי של 49 קילו-דלטון, שעובר טרנסלוקציה לגרעין. יש ראיה לכך שקיימות שתי מולקולות clusterin גרעיני שונות. בעלות משקלים מולקולריים של 50 קילו-דלטון ו-60 קילו-דלטון, בערך (Pajak וחב' ב-J Cereb Blood Flow Metab משנת 2007), שיכולות להיווצר על ידי תרגום המתחיל או ב-ATG הנמצא על אקסון 3, או על אקסון 1, בהתאמה.
תפקודו של clusterin
החלבון clusterin התגלה לראשונה בנוזל האשכים של עגל, בו הוא הראה נטייה של הצמדות (clustering) עם תאי Sertoli ועם אריתרוציטים ומכאן נגזר שמו (Fritz וחב' ב-Reprod Biol משנת 1983). CLU הוא חבר במשפחת חלבוני heat shock, ולכן הוא מוגדר chaperone מולקולרי. שלא בדומה לרוב חלבוני chaperone האחרים, המסייעים לחלבונים תוך-תאיים, CLU הוא chaperone ב-Golgi, המסייע להתקפלות של חלבונים מופרשים באופן שאינו תלוי ב-ATP. הגן CLU משומר מאוד בין species שונים, והחלבון clusterin נפוץ מאוד ברקמות ואיברים שונים, בהם הוא משתתף בתהליכים כמו טרנספורט של ליפידים, תהליכי recycling של ממברנות, ספיחה בינתאית, אפופטוזיס, ותמס תאים בתיווך המשלים.
ביטוי-יתר של של האיזופורם המופרש של CLU מגן על התא מפני אפופטוזיס המושרה על ידי כימותרפיה, הקרנות, או חסר של אנדרוגן/אסטרוגן. Clusterin מעודד הישרדות התא במספר דרכים: על ידי העיכוב של BAX על ממברנת המיטוכודריון, על ידי השפעול של המסלול phosphatidylinositol 3-kinase/protein kinase B, מודולציה על ידי איתות של ERK או extracellular signal–regulated kinase ושל ביטוי האנזים matrix-metallopeptidase-9, סיוע לתהליך ה-angiogenesis, ומעורבות במסלול של NF-κB. כמו כן, clusterin מאפשר את השפעול של p53, באופן המשנה את היחס בין הפעילות המקדמת אפופטוזיס לבין הפעילות האנטי-אפופטוטית של חברי משפחת Bcl-2, דהיינו ריסון פעילות clusterin מאפשר את השפעול של p53, מה שגורם לשיבוש הפעילות המיטוכונדריאלית ולמות התא.
חלבון זה כרוך בפינוי של פסולת תאית ובאפופטוזיס (Jones ו-Jomary ב-Int J Biochem Cell Biol משנת 2002). שלושת האיזופורמים של clusterin כרוכים כאמור באופן דיפרנציאלי בתהליכים מקדמי-אפופטוזיס או בתהליכים מנוגדי-אפופטוזיס. בתור שכזה, clusterin קשור למחלות רבות בהן מתרחשים עקה חמצונית, כולל מחלות נוירו-דגנרטיביות, מחלות דלקתיות, סרטן והזדקנות (Koltai ב-OncoTargets and Therapy משנת 2014, ו-Sansanwal וחב' ב-J Am Soc Nephrol משנת 2015, וכן Lin וחב' ב-J Hepatol משנת 2014).
הפונקציות של clusterin אינן ברורות בשלמותן. חילוקי הדעות באשר לתפקודי חלבון זה, נובעים בעיקר מאי ההבנה של שניים מתוך שלושת האיזופורמים של חלבון זה בעלי פעילות סותרת במידה מסוימת. מספר תפקודים כוללים השתתפות באפופטוזיס על ידי יצירת קומפלקס עם Ku70 autoantigen המסייעת לאפופטוזיס, ומאידך גיסא הפרעה לשפעול של Bax המונע אפופטוזיס Yang) וחב' ב-Proc Natl Acad Sci USA משנת 2000, Leskov וחב' ב J Biol Chem משנת 2003, Zhang וחב' ב Nat Cell Biol משנת 2005, ו-Zhang וחב' בBJU Int משנת 2006).
החלבון clusterin נכרך גם תהליך הספרמטוגנזה (Roberts וחב' ב Endocrinology משנת 1991), בטרנספורט של ליפידים על ידי יצירת קומפלקס עם apolipoprotein A-1 בפלזמה (Jenne וחב' בJ Biol Chem משנת 1991, ו Calero-וחב' ב Biochem J משנת 1999, ו Gelissen -וחב' ב Biochem J משנת 1998). כמו כן נכרך clusterin בהתמיינות (דיפרנציאציה) של תאי אפיתל French) וחב' ב J Cell Biol-משנת 1993, Schedin וחב' ב J Mammary Gland Biol Neoplasia משנת 2000, ו- Kim וחב' ב-Diabetes Res Clin Pract משנת 2007), בשפעול המשלים ( Kirszbaum וחב' ב FEBS Lett משנת 1992) ובאיתות של TGF-β דרך Smad2/Smad3 על פי Lee וחב' ב-Biochem Biophys Res Commun משנת 2008).
משמעות קלינית של clusterin
Clusterin יכול לעודד תהליכים טומורוגניים על ידי סיוע להתקשרות בין BAX ו-CLU70, ועל ידי כך למנוע את ההתקשרות של BAX לממברנה החיצונית של המיטוכונדריה המעודדת מות תאים. בקרצינומה של תאי Clear בכליה, פועל clusterin לוויסות האיתות של ERK 1/2, ושל ביטוי של האנזים MMP-9 לעודד נדידת תאים סרטניים, את חדירתם לרקמות בריאות, ואת יצירת גרורות. בסרטן אפיתליאלי של השחלות, נמצא ש-clusterin מעודד אנגיוגניות ועמידות לכימותרפיה. מסלולים אחרים בהם clusterin משתתף על מנת להפחית אפופטוזיס בתאים סרטניים כוללים את מסלולי P13/AKT/mTOR ו-NF-κB. בניגוד לסוגי סרטן אחרים בהם רמות clusterin מוגברות על מנת להגביר את הישרדות התאים הסרטניים, ב-testicular seminoma רמות clusterin נמוכות יותר, מה שמאפשר רגישות מוגברת לטיפול כימותרפי. אכן, עיכוב clusterin מביא להגברת היעילות של תכשירים כימותרפיים, ולדוגמה custirsen, שהוא antisense oligonucleotide החוסם את ה-mRNA של clusterin, מעודד את הפעילות המעכבת של heat-shock protein 90, על ידי דיכוי תגובת heat-shock בסרטן ערמונית העמיד לסירוס.
כפי שמסתבר מתפקידי המפתח של clusterin בתהליך הסרטני, חלבון זה עשוי להיות גם יעד תרפויטי לעיכוב שגשוג הגידול הסרטני ולמניעת עמידות הסרטן לכימותרפיה. נמצא ש-clusterin מעורב גם במחלות מידבקות כגון הפטיטיס C. נראה ש-clusterin מושרה על ידי העקה של הידבקות בנגיף Hep C שפוגעת בוויסות של גלוקוזה. נראה ש-clusterin מסייע להתגבשות הנגיף על ידי ייצוב יחידות NS5A והליבה (core) של הנגיף. הביטוי של clusterin בכליות משחק תפקיד במחלות כליה, כגון nephropathic cystinosis, המהווה סיבה עיקרית לתסמונת Fanconi. בנוסף למחלות שהוזכרו, clusterin נכרך גם עם מצבים נוספים הנגרמים מנזק חמצוני, כולל הזדקנות, גלומרולו-נפריטיס, טרשת עורקים ואוטם שריר הלב.
מלבד תפקידו החשוב של clustertin באפופטוזיס, יש לו פעילויות נוספות הקשורות להתנהגות תאי הסרטן. לדוגמה, ב-clear cell renal carcinoma, מווסת clusterin פעילות אגרסיבית על ידי מודולציה חוץ-תאית של איתות הקינאזה ERK1/2, וביטוי של MMP-9 (על פי Wang וחב' ב-Urol Int משנת 2013). על ידי ביטול פעילות של sClusterin נמצא כושר נדידה מופחת של התאים, כושר מופחת של יכולת פלישה in vitro, כמו גם פוטנציאל גרורתי מופחת של התאים הסרטניים. ביטוי-יתר של clusterin בסרטן אפיתליאלי של השחלות, עם יכולת אנגיוגנית מוגברת, במה שיכול להתפרש כתפקיד של clusterin כאונקוגן בביולוגיה של סרטן השחלות. בנוסף, sClusterin מגביר את העמידות של תאי סרטן השחלות לכימותרפיה. כמו כן, clusterin מווסת את הפעילות של NF-κB (על פי Essabbani ב-J Biol Chem משנת 2010). רמות מוגברות של clusterin בשתן התגלו במצבים של נזק לאבוביות הקריבניות והרחיקניות בכליה, אך לא במצבים של נזק גלומרולרי.
Clusterin וסרטן השד
הביטוי של clusterin נמצא במתאם עם התפתחות סרטן השד (Redondo וחב' ב-Am J Pathol משנת 2000, ו-Krueger וחב' ב- Neoplasma משנת 2007). בסרטן השד, הרלוונטיות של clusterin דומה לזו שבסרטן הערמונית: Wang וחב' הראו ב-J Chemother משנת 2012, ש-sClusterin מקנה לתאי סרטן שד עמידות לאפופטוזיס המושרה על ידי TNF-α, דרך שפעול של NF-κB וביטוי-יתר של Bcl-2. מחקר שבחן את ההשפעה של עיכוב Bcl-2 על ידי siRNA על נדידת תאי שד סרטניים, חודרנותם לרקמות בריאות, ויכולת שגשוגם in vivo ו-in vitro, נקט בטרנספקציה של תאי שד סרטניים מסוג MDA-MB-231 עם pSuper-siRNA/sCLU (על פי Niu וחב' ב-Arch Biochim Biophys משנת 2012). תוצאות ניסוי זה הראו שהשקטת sClusterin עיכבה באופן משמעותי את השגשוג של תאי MDA-MB-231. כמו כן הופחתו יכולות הנדידה והחודרנות של תאים אלה, ועלתה הפעילות האפופטוטית של תאים אלה שעיכבה את גידול התאים, ופחתה יכולתם לשלוח גרורות לריאות.
תאי סרטן שד triple negative (בו התאים הסרטניים של הגידול אינם מבטאים קולטנים לאסטרוגן ולפרוגסטרון וכן אינם מבטאים כמות מוגברת של החלבון HER2, כאשר כ-10-20% מכלל מקרי סרטן השד הם שליליים לשלושת הסמנים) מכילים sClusterin באחוז גבוה הרבה יותר בהשוואה לתאי סרטן שד שאינם triple negative. אכן התאים האחרונים אגרסיביים יותר מתאי סרטן שד שאינם triple negative. חלק מהחוקרים סבורים ש-sClusterin כרוך בתהליך של triple negativity של תאי סרטן שד (Zhang וחב' ב-Cancer Biol Ther משנת 2012).
Clusterin וסרטן המעי הגס והחלחולת
עיכוב של clusterin ושל thrombospondin-1, מבטל את הזרחון על ידיp38 mitogen-activated protein kinase ואת פעילות MMP-9. Clusterin ו- thrombospondin-1 המופרש מטסיות-דם, מעודדים את ויסות האיתות של MMP-9 בתהליך הגרורתי של סרטן המעי הגס דרך מסלול המווסת על ידי p38 mitogen-activated protein kinase. ממצאים אלה רלוונטיים לפיתוח של תכשירים טיפוליים המפחיתים את הגרורתיות של אדנו-קרצינומה של המעי הגס (Radziwon-Balicka וחב' ב- Carcinogenesis משנת 2013). במעי הגס, ביטוי-יתר של s-clusterin נמצא רק בציטופלזמה של גידולים מאוד גרורתיים. הרמה המוגברת של האיזופורם המופרש, וההיעלמות של האיזופורם הגרעיני, נכרכים באופן ישיר עם הישרדות גדולה יותר, אגרסיביות מוגברת ופוטנציאל גרורתי גבוה יותר (Pucci וחב' ב-Oncogene משנת 2004). רמות מוגברות של clusterin נמצאו בציטופלזמה של תאי סרטן המעי הגס והחלחולת (Xie וחב' ב-World J Gastroenterol משנת 2005), ורמות clusterin מוגברות נכרכו עם פרוגנוזה גרועה באלה עם סרטן המעי הגס stage II (Kevans וחב' ב- Cancer Epidemiol Biomarkers Prev משנת 2009, ו-Kruger וחב' ב-Neoplasma משנת 2007). רמות clusterin מוגברות נמצאו גם בצואה של חולים סרטן המעי הגס (Pucci וחב' ב- Am J Gastroenterol משנת 2009).
Clusterin וסרטן הערמונית
מספר מחקרים מצאו רמות נמוכות של clusterin בסרטן הערמונית (Bettuzzi וחב' ב-Oncogene משנת 2000, Scaltriti וחב' ב-Int J Cancer משנת 2004 ו-Rauhalta וחב' ב-Int J Cancer משנת 2008). לעומת זאת, ישנם גם דיווחים על רמת clusterin מוגברת בסרטן הערמונית, במיוחד לאחר טיפול אבלציה להפחתת רמת האנדרוגן (July וחב' ב-The Prostate משנת 2002). הבדל זה מוסבר על ידי מדידה של איזופורמים שונים של clusterin: רמת האיזופורם המעודד אפופטוזיס nCLU יורדת, לעומת האיזופורם האנטי-אפופטוטי sCLU שרמתו עולה, אכן, תרפיה של antisense oligonucleotide כנגד clusterin נבחנת בניסויים קליניים, בעיקר כדי למנוע עמידות לטיפולים כימיים (Sowery וחב' ב-BJU Int משנת 2008, ו-Zelinski וחב' ב-Cancer J משנת 2003). clusterin משמש בטיפולים משולבים עם tocetaxel בסרטן ערמונית מתקדם, העמיד לסירוס (Higano ב-Oncol Targets Therapy משנת 2013). נתונים המאששים תפקיד מדכא של clusterin כוללים דיווחים על בקרה אפיגנטית של ביטוי clusterin בשורות תאי סרטן הערמונית. פותח זן טרנסגני של עכבר knockout הידוע כ-TRAMP/cluCO שאינו מייצר clusterin ומפתח סרטן ערמונית פחות ממוין ויותר גרורתי (Bettuzzi וחב' ב-Oncogene משנת 2009). על פי Rauhalta וחב' ב-Int J Cancer משנת 2008, רמת clusterin נמצאת תחת ויסות באופן אפיגנטי בסרטן הערמונית.
בתאי סרטן הערמונית נתגלתה היכולת של sClusterin לווסת את ה-ubiquitination ואת קצב הפירוק של COMM domain-containing protein 1. (על פי Zoubeidi וחב' ב-Mol Cancer Res משנת 2010). בהתאם, פגיעה ב-sClusterin מייצבת את COMM domain-containing protein 1, מנטרלת את NF-κB בציטופלזמה, ומפחיתה את השעתוק של רבים מהגנים המווסתים על ידי גנים. הביטוי של clusterin נמצא תחת בקרה גנטית ואפיגנטית, כאשר האחרונה מושפעת ממתילציה של ה-promoter שלה (Serrano וחב' ב-Tumor Biol משנת 2009).
Clusterin וסרטן השחלות
ביטוי מוגבר של clusterin כרוך בהתנהגות ביולוגית אגרסיבית והישרדות נמוכה בסרטן השחלות (Yang וחב' ב- Int J Gynecol Cancer משנת 2009, ו-Wei וחב' ב-Int J Cancer משנת 2009). מתילציה של ה-promoter בגן CLU מופיעה בתדירויות נמוכות בגידולים של תאי אפיתל בשחלות, והיא כרוכה באופן משמעותי בביטוי גני נמוך יותר של clusterin (Yang וחב' ב- Arch Gynecol Obstet משנת 2013). נמצא שבתאי גרנולוזה בשחלות של אדם ושל חולדה יש השרייה של אפופטוזיס על ידי cAMP במנגנונים בלתי מזוהים. ההשפעה האפופטוטית של cAMP מלווה על ידי הגברה של ביטוי של p53 ושל Bax. לא התגלה שום שינוי ברמת החלבון Bcl-2 בתאי גרנולוזה מטופלים ב-cAMP, מה שמצביע על כך ש-cAMP עשוי לשפעל אפופטוזיס על ידי שינוי היחס בין death promoter genes לבין death repressor genes דרך שינוי היחס בין ביטוי p53 לבין ביטוי Bax. כיוון ש-cAMP נמצא גם מעכב את ביטוי הגן CLU, נראה שיש לחלבון זה תפקיד באפופטוזיס המושרה על ידי cAMP בתאי גרנולוזה (Zwain ו-Amato ב- Endocr Res משנת 2001). טיפול של תאי גרנולוזה עם antisense oligonucleotide המכוון נגדclusterin גרם להגברת אפופטוזיס, מה שמרמז שחסר ב-clusterin יכול לגרום לאפופטוזיס בשחלות ולאטריזיה פוליקולרית (Zwain ו-Amato ב-Cell Res Exp משנת 2000). על פי Fu וחב' ב-Mol Med Rep משנת 2013, ביטוי יתר של clusterin מעודד אנגיוגניות דרך VEGF בסרטן שחלות ראשוני וממילא מגביר את האגרסיביות של סרטן זה.
Clusterin וסרטן הפנקריאס
השרייה של clusterin מלווה תהליכי רגנרציה בפנקריאס של חולדות לאחר כריתה חלקית של הבלוטה (Lee וחב' ב- Dev Dyn משנת 2011). בעכברי knockout שאינם מייצרים clusterin, כריתת הבלוטה גורמת ליצירה מעטה של אוניות הבלוטה, ובעיקר הרגנרציה של תאי β הייתה מועטה יחסית והייתה כרוכה בהיפר-גליקמיה. תאי צנרירי הבלוטה (duct cells) שמקורם מעכברי knockout שהוסרה בהם בלוטת הלבלב החסרים clusterin היו לקויים ביצירת תאי β במערכת in vitro, ויצירה זו שוחזרה על ידי הוספה של clusterin אקסוגני. נראה אם כן ש-clusterin הוא גורם חשוב בביולוגיה של הפנקריאס (Xie וחב' ב-Cancer משנת 2005). טרנספקציה של ה-cDNA של clusterin לתוך תאי duct פנקראטיים בתרבית, הביאה להגברה פי-2.5 בשגשוג תאים, ובהתמרה המושרית של תאי duct בלתי-ממויינים לתאים ממוינים המבטאים cytokeratin. בסרטן הפנקריאס, הביטוי של clusterin כרוך בהישרדות ארוכה יותר (Xie וחב' ב-Pancreas משנת 2002).
Clusterin ו-hepatocarcinoma
קרצינומה של תאי כבד היא אחד מסוגי הסרטן השכיחים והאגרסיביים ביותר, עם פרוגנוזה גרועה של פחות מ-5% למשך 5 שנים. רמות גבוהות של sClusterin נכרכות בממאירויות מוגברות כולל סרטן הכבד. נמצא ש-clusterin מבוטא ביתר ברקמת סרטן כבד גרורתי בהשוואה לסרטן כבד לא-גרורתי (Lau וחב' ב-Oncogene משנת 2006), ומגביר על ידי כך פי-2 את כושר הנדידה של גידול זה in vitro. דווח ש-clusterin משחק תפקיד חשוב בגרורתיות של hepatocarcinoma על ידי הגברת הביטוי של MMP-2 הפחתת הביטוי של E-cadherin (Chen וחב' ב- Int J Mol Sci משנת 2012). נמצא שביטוי יתר של sClusterin תורם לעמידות הסרטן לטיפול ב-oxaliplatin על ידי שפעול מסלול AKT (Xiu וחב' ב-Cancer Sci משנת 2013).
Clusterin וסרטן ריאות
Yan וחב' הציעו ב-Hepatogastroenterology משנת 2013 ש-sClusterin משחק תפקיד חיובי בשגשוג של תאי NSCLC, שעשוי להיות מתווך על ידי מסלול האיתות של PI3K/AKT, והדגימו שהשתקת הגן sCLU המפריע לפעילות RNA, היא אסטרטגיה טיפולית במקרי NSCLC כיוון שהיא פוגעת בשגשוג התאים הסרטניים, חוסמת את מסלול PI3K/AKT, ומשרה אופטוזיס. אף על פי שהביטוי של clusterin נכרך עם ממאירויות שונות באדם, המנגנונים דרכם clusterin מעודד התפשטות וממאירות של סרטן ריאות לא בהירים דיים (Panico וחב' ב-Adv Cancer Res משנת 2009). Chou וחב' דיווחו ב-Signal Cell משנת 2009 ש-clusterin מווסת את מעבר התאים הסרטניים האפיתליאליים לסטאטוס מזנכימלי, ולהתנהגות אגרסיבית של תאי אדנו-קרצינומה של הריאות על ידי מודולציה של איתות ERK וביטוי של Slug/E-cadherin. בשורות תאי small cell lung cancer, נמצא ש-oblimersen, שהוא antisense Bcl-2 oligodeoxynucleotide, מגביר את התגובה של תאים אלה להקרנות. מנגנון הפעולה של oblimersen דומה לזה שלcustirsen בכך שגם הוא מגביר אפופטוזיס.
יש מספר ראיות לכך שעיכוב sClusterin בשלבים מאוחרים של סרטן ריאות יכול להיות טיפול תועלתי, בעוד שבשלבים מוקדמים של המחלה, התוצאות עלולות להיות הפוכות. בניסוי in vitro, השתקת clusterin על ידי antisense oligonucleotides ו-siRNA כנגד mRNA של clusterin שנמצא ברמה גבוהה בשורות תאים מסרטן ריאות, הביא להגברת רגישותם לכימותרפיה ולהקרנות והפחית את הפוטנציאל הגרורתי שלהם. In vivo, מחקר של Panico שבחן את התפקיד הפרוגנוסטי של clusterin ב-NSCLC, מצא שחולים חיוביים ל-clusterin היו בעלי הישרדות טובה יותר מאשר חולי סרטן ריאות זה ללא clusterin. ממצאים אלה נמצאים בסתירה לתוצאות המעודדות של הניסוי in vitro. על בסיס ממצאים אלה מציע Panico שבסרטן ריאה בשלביו המוקדמים, clusterin עשוי להוות סמן חיובי התואם הישרדות טובה יותר.
Clusterin ומלנומה
Hoeller וחב' דיווחו ב-J Invest Dermatol משנת 2005 שבדגימות של מלנומה, הביטוי של clusterin היה נמוך ב-nevi אך גבוה במלנומה ראשונית ובגרורות של מלנומה. Clusterin היה גם מאוד בולט בשורות תאי מלנומה בתרבית, אך היה מבוטא בקושי במלנוציטים בתרבית. על מנת לפרש את התפקיד של clusterin בעמידות של מלנומה לתרופות, נוסו גישות של הגברת הביטוי של clusterin על ידי החדרת פלסמיד לתאים, או החלשת ביטויו על ידי טיפול בתכשירי antisense. נמצא שביטוי יתר של החלבון האמור הביא להגברת העמידות של מלנומה לתרופות, ולהישרדות גבוהה יותר של התאים הסרטניים, ולעומת זאת החלשת הביטוי של clusterin על ידי antisense oligonucleotides המכוונים כנגד mRNA של החלבון, הביאה להחלשת התנגודת של תאי מלנומה לתרופות. Shannan וחב' הראו ב-Anticancer Res משנת 2006, ביטוי מוגבר של clusterin בתאי מלנומה ראשוניים ובתאים גרורתיים של סרטן זה, אך ביטוי מאוד מוחלש בתאי nevus או מלנוציטיים.
הקשר קליני של clusterin למחלת אלצהיימר
שני מחקרים בלתי-תלויים במסגרת genome-wide association studies מצאו קשר סטטיסטי בין SNP בגן ל-clusterin לבין הסיכון ללקות באלצהיימר (להלן (AD. מחקרים בהמשך הראו שמאובחנים עם אלצהיימר, מכילים בדמם רמות גבוהות יותר של clusterin, וכן שיש מתאם בין רמות אלה לבין דעיכה קוגניטיבית מהירה יותר בקרב חולי אלצהיימר, (Lambert וחב' ב-Nat Genet משנת 2009, ו-Harold וחב' באותו כתב עת מאותה שנה, Schrijvers וחב' ב-JAMA משנת 2011), אך עם זאת לא נמצא שרמות clusterin עשויות לנבא את הופעת אלצהיימר (Nuutinen וחב' ב-Brain Res Rev משנת 2009). בנוסף לאלצהיימר, clusterin מעורב גם במחלות נוירו-דגנרטיביות אחרות כמו במחלת Huntington. הסברה היא ש-clusterin מווסת את היצירה וההרחקה של amyloid. רמות מוגברות של clusterin התגלו במוחות ובנוזל השדרה של חולי AD. קבוצתה של Breteler בחנה במסגרת מחקר Rotterdam מדגם של 60 חולי AD שנבדקו לרמת clusterin בדמם, ומדגם נוסף של 156 משתתפים שנתגלו כחולי AD במעקב ממוצע של 7.2 שנים. מחקר זה מצא שההסתברות תחלואה ב-AD שיש ל-clusterin גוברת במתאם טוב עם רמת clusterin בדם. לאחר התאמה לגיל, מגדר, רמת השכלה, סטאטוס apoE, סוכרת, עישון, יתר לחץ-דם ומחלת לב, הסיכון ללקות ב-AD גדל ב-63% ברמות גבוהות של clusterin (Lambert וחב' ב-Nature Genet משנת 2009). בחולי AD רמות מוגברות של clusterin נמצאו כרוכות במחלה חמורה יותר, כפי שנקבע על ידי הדעיכה בתוצאת Mini-Mental State Examination. השערה עדכנית היא שיש ל-clusterin יכולת לקשור פפטידים של Aβ ובכך משפיעה על האגרגציה של העמילואיד, על השקיעה המוחית של העמילואיד ועל כושר הפינוי שלו מהמוח, אם כי מנגנונים אלה צריכים עדיין להיחקר.
תכשירים פרמצבטיים בהֶקשר של clusterin
חברת OncoGeneX Pharmaceutical פיתחה את התכשיר custirsen (או OGX-011 במקור), שהוא antisense oligonucleotide מהדור השני, שתוכנן לחסום את ה-mRNA של sClusterin, כדי להפחית את יצירת החלבון האמור ולשפר ממצאים קליניים בתרחיש של סרטן מתקדם של הערמונית העמיד לסירוס. יש ראיות לכך ש-custirsen עשוי להיות יעיל גם בסוגי סרטן נוספים כמו סרטן שד, סרטן שחלות, סרטן ריאות (Laskin וחב' ב-J thorac Oncol משנת 2012), ו-clear cell renal carcinoma.
מה היו הסיבות לפיתוח custirsen ? יכולת תכשיר זה להיקשר לאקסון 1 של sClusterin mRNA וחסימת התרגום שלו. אכן, פיתוח תכשיר זה התקדם על בסיס הממצאים הבאים:
- תאי renal carcinoma המבטאים ביתר את sClusterin נעשים עמידים יותר לאפופטוזיס (Miyake וחב' ב-Mol Urol משנת 2001)
- אוליגונוקלאוטידים המתכווננים כנגד sClusterin מגבירים את רגישות תאי סרטן הערמונית לטיפולי הקרנות (Zellweger וחב' ב-Clin Cancer Res משנת 2002)
- אוליגונוקלאוטידים המכוונים כנגד sClusterin מגבירים את רגישות התאים לתכשירים כימותרפיים (Gleave וחב' ב-Urology משנת 2001)
הניסוי המכונן של Miyake וחב' שהתפרסם ב-J Urol בשנת 2002, בו החדירו חוקרים אלה את הגן CLU לתאי renal cell carcinoma ועודדו בכך את הפוטנציאל הגרורתי של תאים אלה, הביא להפנמת הגישה של הצורך להפחית את הביטוי או את הפעילות של clusterin בתאים הסרטניים. Custirsen נמצא מגביר את הציטו-טוקסיות כאשר הוא משולב עם docetaxel בתאי קרצינומה של הערמונית, או עם sorafenib ב-clear cell renal carcinoma (על פי Kusuda וחב' ב-Br J cancer משנת 2012), עם cisplatin ב-clear cell renal carcinoma, או עם gemcitabine ותרכובות platin בתאי סרטן ריאות. Clusterin נמצא ראוי להוות יעד טיפולי בסרטן לא רק בגלל הפעילות האנטי-אפופטוטית שלו לאחר טיפול כימותרפי, אלא גם בגלל פעילויות מעודדות ממאירות שהוא עלול לייצר, כגון שפעול של המסלול P13K/AKT, הגברת הריכוז של vascular endothelial growth factor, איתות על ידי ERK1/2, ביטוי-יתר של MMP-9 ווויסות NF-κB. עיכוב של clusterin על ידי שימוש ב-custirsen מעודד פעילות של מעכב של heat-shock protein 90 על ידי דיכוי תגובת heat-shock בתאי סרטן ערמונית עמידים לסירוס. הבחירה במסלול האפופטוזיס כיעד של תכשירים טיפוליים, מסמלת בהחלט גישה חדשה בפיתוח המואץ של תכשירים דוגמת oblimersen (שהוא antisense oligonucleotide החוסם את Bcl-2) על פי Loriot וחב' ב-Anticancer Res משנת 2010, ו-Advani וחב' ב-Expert Opin Drug Metab Toxicol משנת 2011). תכשירים חדשים נוספים הם apatorsen (או OGX-427) שהוא antisense oligonucleotide המכוון כנגד heat-shock protein 27 הנבחן בטיפול משולב עם gemcitabine ו-cisplatin בסרטן מתקדם של שלפוחית השתן (Ischia וחב' ב-Nature Rev Urol משנת 2012).
הוראות לביצוע הבדיקה
הבדיקה מתבצעת על ידי צביעה אימונו-היסטוכימית של ביופסיה או של רקמה שהתקבלה בצורה אחרת, כאשר חיתוך במיקרוטום צריך להיות מכוון לפרוסות בעובי של 4 מיקרון. יתקבלו במעבדה הפתולוגית בלוקים שעברו פיקסציה בפורמלין, ותהליך של embedding בפרפין. יש לדחות דגימות של רקמה קפואה או רטובה, משטחים ציטולוגיים, רקמה שלא עברה קיבוע בפורמלין, או שלא עברה embedding בפרפין. לא יתקבלו non-charged slides, או probeOn slides. עדיף שהדגימות תגענה למעבדה בטמפרטורת החדר, אך גם דגימות בקירור תתקבלנה.
תוצאות הבדיקה
בבלוטות לימפה, בשקדים ובטחול, צביעה ל-clusterin צובעת תאים דנדריטים פוליקולריים. תאי B, תאי T והיסטיוציטים אינם נצבעים. צביעה ל-clusterin מתקבלת לעיתים קרובות חיובית בתאים סרטניים של -large-cell lymphoma אנאפלסטית, אך הצביעה בדרך כלל שלילית בתאי Reed Sternberg בלימפומה קלאסית ע"ש Hodgkin (על פי Grogg וחב' ב-Am J Surg Pathol משנת 2004, Grogg וחב' ב-Modern Pathol משנת 2005, ו-Saffer וחב' ב-Modern Pathol משנת 2002).
ראו גם
המידע שבדף זה נכתב על ידי פרופ' בן-עמי סלע, המכון לכימיה פתולוגית, מרכז רפואי שיבא, תל-שומר;
החוג לגנטיקה מולקולארית וביוכימיה, פקולטה לרפואה, אוניברסיטת תל-אביב (יוצר הערך)


 כניסה
כניסה  עקבו אחרינו בפייסבוק
עקבו אחרינו בפייסבוק