תנגודת לאינסולין - Insulin resistance
| תנגודת לאינסולין | ||
|---|---|---|
| Insulin resistance | ||

| ||
| יוצר הערך | פרופ’ מוחמד עבדולגני
|
|
לערכים נוספים הקשורים לנושא זה, ראו את דף הפירושים – סוכרת
כשמתפתחת תנגודת לאינסולין נפגמת יכולת האינסולין לדכא שחרור חומצות שומן מרקמת השומן, ולהוריד את רמת הסוכר בדם. ישנם גורמים שונים המביאים להתפתחות תנגודת לאינסולין, ולהתפתחותה יש תוצאות מטבוליות והשלכות קליניות. התנגודת ניתנת לאבחון, והטיפול בה שמרני ולעיתים גם תרופתי.
מבוא - פעולת האינסולין
אינסולין הוא ההורמון ההבנייתי (אנאבולי) העיקרי בגוף. לאינסולין יש מספר רב של פעולות מטבוליות הכוללות עיכוב פירוק חלבון בשריר, עיכוב פירוק ושחרור חומצות שומן מרקמת שומן והורדת רמת הסוכר בדם. נוסף על כך, אינסולין פועל גם כפקטור גדילה עם תפקיד חשוב בגדילה והתמיינות של תאים. הפרעה בפעולה התקינה של האינסולין בשלב העוברי גורמת להפרעות בהתפתחות התקינה של העובר ובפיגור בגדילה לאחר הלידה.
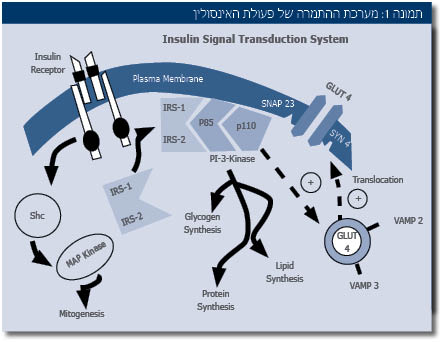
כל הפעולות הנ"ל של אינסולין מתווכות על ידי קולטן ספציפי הנמצא על פני התאים. התקשרות האינסולין לקולטן שלו מפעילה מערכת התמרה (Signal transduction) מורכבת (תמונה 1), שמתווכת בין פעולות האינסולין המטבוליות להשפעתו על גדילה ועל התפתחות תאים.
מערכת ההתמרה המופעלת על ידי התקשרות האינסולין לקולטן שלו, מורכבת משתי זרועות: הזרוע הראשונה כוללת את החלבונים IRS-IP3K-Akt, והיא שממשיכה את הפעילות המטבולית של ההורמון. זרוע נוספת - Sch-MAPK - ממשיכה את השפעת האינסולין על גדילה והתפתחות של תאים.
כשמתפתחת תנגודת לאינסולין, חלה הפרעה בזרוע המטבולית IRS-IP3K-Akt שפוגמת בהשפעות המטבוליות של האינסולין, וכתוצאה מכך נפגמת יכולתו לדכא שחרור חומצות שומן מרקמת השומן, ולהוריד את רמת הסוכר בדם. פעילות זרוע ההתמרה השנייה - Sch-MAPK - אינה מושפעת מהתפתחות תנגודת לאינסולין, והיא ממשיכה לפעול כרגיל.
אפידמיולוגיה
אטיולוגיה
תנגודת לאינסולין נובעת מהפרעה בהפעלת הזרוע המטבולית של מערכת ההתמרה של הקולטן לאינסולין. עלייה בתנגודת לאינסולין אופיינית לכל החולים הסובלים מסוכרת מסוג 2. תנגודת גבוהה לאינסולין מתלווה גם לעלייה במשקל ולעלייה בגיל. גורמים גנטיים תורמים גם הם להתפתחות התנגודת לאינסולין אם כי זהות הגנים הגורמים לכך עדיין אינה ידועה. דוגמה לחשיבות התרומה הגנטית להתפתחות התנגודת לאינסולין אפשר למצוא בעבודות שמדדו את התנגודת לאינסולין אצל צאצאים רזים צעירים ובריאים להורים סוכרתיים, שאף אצלם נמצאה תנגודת גבוהה לאינסולין בדומה להוריהם הסוכרתיים.
נוסף על חשיבות הרקע הגנטי בהתפתחות התנגודת לאינסולין, קיימת תרומה נוספת חשובה מאוד לסביבה ובעיקר לאורח החיים. עלייה במשקל וירידה בפעילות הגופנית הם שני הגורמים החשובים ביותר שתורמים להתפתחות תנגודת לאינסולין. כשקיים מאזן קלורי חיובי בגוף עודף הקלוריות נאגר בצורת שומן בתוך רקמת השומן. לרקמת השומן יש קיבולת מסוימת לאגירת שומנים. אם הגוף נמצא במאזן קלורי חיובי מתמיד (בשל אכילת יתר או ירידה בפעילות הגופנית), רקמת השומן מתמלאת, ועודף השומנים נשפך לזרם הדם ומשם נקלט על ידי הרקמות הרכות (שריר, כבד, עורקים) ומתחיל להצטבר בתוכם. תהליך צבירת השומן ברקמות הרכות מפעיל שורה של אנזימים תוך-תאיים שגורמים להפרעה במערכת ההתמרה המטבולית של האינסולין וגורמת להתפתחות תנגודת לפעולות המטבוליות של האינסולין. לכן, עודף משקל הוא מרכיב חשוב בהתפתחות תסמונת התנגודת לאינסולין או התסמונת המטבולית והוא אחד הקריטריונים לאבחונה.
קליניקה
בשל התפתחות תנגודת לאינסולין מתפתחות ההפרעות המטבוליות הבאות:
- חלה עלייה בשחרור חומצות שומן מרקמת שומן שגורמת לעלייה בריכוז חומצות שומן חופשיות בדם (טבלה 1).
- עלייה ביצירת סוכר בכבד וירידה בקליטת סוכר בשריר שגורמת לעלייה ברמת הסוכר בדם. העלייה ברמת הסוכר בדם מגרה את הפרשת האינסולין מהלבלב ומביאה לעלייה בריכוז האינסולין הבסיסי בדם.
- עודף חומצות שומן בדם נקלט על ידי הכבד, ובנוכחות ריכוז גבוה של סוכר ואינסולין בדם מהווים תנאים שמגבירים את ייצור השומנים (בצורה של טריגליצרידים) על ידי הכבד. חלק משומנים אלה נאגרים בתוך תאי הכבד ומביאים להתפתחות מצב הידוע בשם כבד שומני, החלק האחר של הטריגליצרידים מופרש לזרם הדם בצורת VLDL, שמהווה אמצעי הובלה לטריגליצרידים הנאגרים ברקמת השומן. לכן, עלייה ברמת טריגליצרידים בדם היא ההפרעה הראשונה במטבוליזם השומנים הנגרמת ע"י התפתחות תנגודת לאינסולין. בשל עליית ריכוז הטריגליצרידים בדם (VLDL) חלה עלייה בשחלוף השומנים בין VLDL ל-HDL ו-LDL, וכתוצאה מכך להקטנה בגודל החלקיקים של LDL ו-HDL. הקטנת גודל החלקיקים של HDL מביאה להאצת פינויים מזרם הדם ולירידה ברמת HDL. לכן, תנגודת לאינסולין מלווה ברמה גבוהה של טריגליצרידים בדם עם רמה נמוכה של HDL וירידה בגודל החלקיקים של LDL. הפרעה משולשת זו בשומני הדם היא אופיינית למצב של תנגודת גבוהה לאינסולין, וכל שלושת המרכיבים שלה הם גורמי סיכון עיקריים להתפתחות טרשת עורקים.
4. הפעלת הקולטנים לאינסולין בתאי אנדותל כלי הדם מגבירה את ייצור החנקן חמצני (NO) שמרחיב את כלי דם. לכן, התפתחות תנגודת לאינסולין מלווה בירידה ביצור NO בכלי הדם ובעלייה ברמת התכווצות כלי הדם. כיווץ היתר של כלי הדם תורם להתפתחות יתר לחץ דם, לכן הביטוי הקליני של תנגודת גבוהה לאינסולין כולל הפרעה במטבוליזם הסוכרים, מלווה ברמות גבוהות של אינסולין בדם, הפרעה בשומני הדם, כבד שומני ויתר לחץ דם, צירוף הידוע בשם תסמונת התנגודת הגבוהה לאינסולין או התסמונת המטבולית.
התפתחות סוכרת וטרשת עורקים
כפי שהוסבר לעיל, התנגודת לאינסולין גורמת לעלייה ברמת סוכר בדם שביטויה הפרעה ברמת הסוכר בדם לאחר צום לילה (IFG; Impaired fasting glucose) או הפרעה ברמת הסוכר בדם אחרי ארוחה (IGT; Impaired glucose tolerance). העלייה ברמת הסוכר בדם מגרה הפרשת יתר של אינסולין מתאי β של הלבלב, שמתבטאת בעלייה ברמת אינסולין בצום, או בתגובה מוגברת בהפרשת אינסולין אחרי ארוחה או בעקבות העמסת סוכר. ניתן לראות בעליית רמות האינסולין בצום במצב של תנגודת לאינסולין תגובת נגד של הגוף כדי למתן את העלייה ברמת הסוכר בדם ולמנוע התפתחות סוכרת. ולכן, רמות אינסולין גבוהות בדם בצום או אחרי ארוחה הן המדד הקליני הקל והרגיש ביותר לקיום תנגודת לאינסולין. מצד שני, רמות נמוכות של אינסולין בצום (במקביל לרמות תקינות של סוכר) הן סימן לרגישות גבוהה לאינסולין (ולא להפרעה בתפקוד הלבלב), ומעידה על סיכון מטבולי נמוך. אי לכך, רמות גבוהות של אינסולין הן מרכיב נוסף שמלווה את תסמונת התנגודת לאינסולין או התסמונת המטבולית. ככל שהתנגודת לאינסולין קשה או ממושכת יותר, ובעיקר באנשים עם נטייה גנטית לפתח סוכרת (כמו ילדים להורים סוכרתיים), הלבלב אינו מסוגל לעמוד "זמן ממושך" בעומס הפרשת יתר של אינסולין, ומתחיל להראות "סימני עייפות" (Beta cell failure). בשל התפתחות תשישות לבלבית כמות האינסולין שהלבלב מפריש אינה מספקת כדי להתגבר על התנגודת לאינסולין ועל שמירה על רמות סוכר תקינות בדם, ומתחילה עלייה הדרגתית ברמת הסוכר הן בצום והן לאחר ארוחות: מצב של הפרעה בסבילות לגלוקוז (IGT) והפרעה בריכוז הסוכר בצום (IFG). כשרמת הסוכר בדם בצום גדולה מ- 126 מ"ג/ד"ל ההפרעה מוגדרת כסוכרת. התנגודת לאינסולין היא גורם הסיכון החזק ביותר המנבא התפתחות סוכרת והתפתחות ההפרעות המטבוליות שמלוות את התנגודת לאינסולין: הפרעה במטבוליזם השומנים, הפרעה במטבוליזם הפחמימות, יתר לחץ דם והשמנה.
ההפרעות המטבוליות הן הגורמות לטרשת עורקים. כפי שהוסבר לעיל (תמונה 1) ההתפתחות של התנגודת לאינסולין מתרחשת רק בזרוע המטבולית ואינה מתרחשת בזרוע השנייה (Sch-MAPK). לכן, התפתחות תנגודת לאינסולין בכלי הדם עם עלייה ברמות אינסולין בדם מביאה להפעלת יתר של הזרוע השנייה של מנגנון ההתמרה של האינסולין (Sch-MAPK) וזאת מביאה להתרבות ולתגובת יתר של שריר חלק בדופן כלי הדם. התגברות השגשוג (פרוליפרציה) של שריר חלק בדופן כלי הדם בנוכחות ההפרעות המטבוליות המלוות את התנגודת לאינסולין גורמת להאצה ניכרת של תהליך טרשת העורקים ולהתפתחות מחלת לב איסכמית, ולכן חולים עם תנגודת גבוהה לאינסולין נמצאים בסיכון גבוה להתפתחות מחלת לב וכלי דם. עבודות אפידמיולוגיות רבות הראו שתנגודת מוגברת לאינסולין או עלייה ברמות אינסולין בדם הן גורם מנבא חזק ובלתי תלוי להתפתחות מחלת לב וכלי דם. תנגודת גבוהה לאינסולין היא גורם סיכון חזק לא רק להתפתחות סוכרת אלא גם למחלת לב וכלי דם.
אבחנה
חשוב לאתר אנשים עם תנגודת גבוהה לאינסולין ולטפל בהם כדי להפחית את הסיכון שלהם לפתח סוכרת ומחלות לב וכלי דם, שלהן שיעורי תחלואה ותמותה גבוהים. עבודות קליניות רבות הראו כי הורדת תנגודת לאינסולין אצל חולים עם תנגודת גבוהה לאינסולין מפחית באופן ניכר את הסיכון להתפתחות סוכרת ואת גורמי הסיכון למחלת לב וכלי דם. רמה גבוהה של אינסולין בדם היא סמן רגיש לקיום תנגודת לאינסולין. תנגודת לאינסולין ורמות האינסולין בדם הם משתנים רציפים, ולא קיימת רמת סף של אבחנת תנגודת לאינסולין. רמות אינסולין בדם מעבר ל- 60 pmol/L, הן רמות שנחשבות לגבוהות, וכשקיימות הפרעות מטבוליות המלוות רמת אינסולין גבוהה (לדוגמה, הפרעה בשומני הדם) הדבר מעיד על קיום תנגודת משמעותית לאינסולין, ומחייב התחלת תוכנית התערבות כדי להוריד את התנגודת לאינסולין.
מאחר שתנגודת לאינסולין מלווה בד"כ בעלייה במשקל, מומלץ לבדוק רמות אינסולין וסוכר בצום ופרופיל שומנים אצל כל האנשים הסובלים מעודף משקל וגם בצאצאים להורים סוכרתיים.
טיפול
הורדת משקל והגברת הפעילות הגופנית הם טיפול הבחירה אצל אנשים עם תנגודת גבוהה לאינסולין. ירידה קלה של 5%-3% במשקל הגוף עם הגברת פעילות גופנית של 45-30 דקות ליום 5 פעמים בשבוע מביא להורדת התנגודת לאינסולין והורדת ההיארעות של סוכרת ב- 60% והורדת השכיחות של גורמי הסיכון למחלת לב וכלי דם. בחולים שקיימת אצלם הפרעה במטבוליזם הסוכר וגילם מתחת ל- 65 או בעלי מדד מסת הגוף (BMI; Body mass index) >35 או המוגלובין מסוכרר (HbA1C) >6% הומלץ על ידי ארגון הסוכרת האמריקאי (ADA) להתחיל טיפול ב- Metformin נוסף על הורדה במשקל והגברת הפעילות הגופנית.
העלייה הניכרת בשכיחות השמנה אצל ילדים ומתבגרים מחייבת תשומת לב מיוחדת בקבוצות גיל אלה. בגלל הגיל הצעיר, ילדים ומתבגרים שלהם תנגודת גבוהה לאינסולין מפרישים כמויות עצומות של אינסולין שמונעת עלייה משמעותית של רמות סוכר בדם, למרות קיום תנגודת קשה לאינסולין. בגלל תוחלת החיים הארוכה של ילדים, קיום תנגודת קשה לאינסולין (גם ללא הפרעות ברמות הסוכר) בנוכחות כל גורמי הסיכון למחלות לב וכלי דם הנלווים אליה יביא להתפתחות מחלת לב וכלי דם בגיל צעיר יחסית (עשור רביעי וחמישי של החיים במקום בעשור השישי והשביעי), ולכן חשוב להתערב ולעקוב אחר ילדים אלה כדי להקטין את התנגודת לאינסולין. ניתן גם להשתמש ברמות אינסולין בצום כמדד להפחתת התנגודת לאינסולין במעקב אחרי התקדמות הטיפול. שינוי באורח חיים וטיפולים תרופתיים (Metformin ותרופות מקבוצת ה- Thiazolidinediones) שניהם הוכחו כיעילים בטיפול בחולים עם תנגודת לאינסולין.
פרוגנוזה
דגלים אדומים
1. Which metabolic of the following metabolic abnormalities is not part of the insulin resistance (metablic) syndrome:
a. Impaird fasting glucose and/or impaired glucose tolerance
b. Increased levels of triglycerides
c. Increased level of LDL
d. Hypertension
2. Which of the following treatments does not reduce the future risk for type 2 diabetes in subjects with increased insulin resistance?
a. Weight loss and exercise
b. Metformin
c. Thiazolidenedions
d. Insulin
ביבליוגרפיה
- Saltiel AR, Kahn CR. Insulin signalling and the regulation of glucose and lipid metabolism. Nature 2001;414:799-806
- Cusi K, Maezono K, Osman A, et al. Insulin resistance differentially affects the PI 3-kinase- and MAP kinase-mediated signaling in human muscle. J Clin Invest 2000;105:311-320
- Reaven GM. Insulin resistance: the link between obesity and cardiovascular disease. Endocrinol Metab Clin North Am 2008;37:581-601
- Lettner A, Roden M. Ectopic fat and insulin resistance. Curr Diab Rep 2008;8:185-191
- Abdul-Ghani MA, DeFronzo RA. Mitochondrial dysfunction, insulin resistance, and type 2 diabetes mellitus. Curr Diab Rep 2008;8:173-178
- Kraegen EW, Cooney GJ. Free fatty acids and skeletal muscle insulin resistance. Curr Opin Lipidol 2008;19:235-241
- Abdul-Ghani MA, Tripathy D, DeFronzo RA. Contributions of beta-cell dysfunction and insulin resistance to the pathogenesis of impaired glucose tolerance and impaired fasting glucose. Diabetes Care 2006;29:1130-1139
- Bays H, Mandarino L, DeFronzo RA. Role of the adipocyte, free fatty acids, and ectopic fat in pathogenesis of type 2 diabetes mellitus: peroxisomal proliferator-activated receptor agonists provide a rational therapeutic approach. J Clin Endocrinol Metab 2004;89:463-478
- Artz E, Freemark M. The pathogenesis of insulin resistance in children: metabolic complications and the roles of diet, exercise and pharmacotherapy in the prevention of type 2 diabetes. Pediatr Endocrinol Rev 2004;1:296-309
- Crandall JP, Knowler WC, Kahn SE, et al. Diabetes Prevention Program Research Group. The prevention of type 2 diabetes. Nat Clin Pract Endocrinol Metab 2008;4:382-393
- Phelan S, Wadden TA, Berkowitz RI, et al. Impact of weight loss on the metabolic syndrome. Int J Obes 2007;31:1442-1448
- Nathan DM, Davidson MB, DeFronzo RA, et al. American Diabetes Association. Impaired fasting glucose and impaired glucose tolerance: implications for care. Diabetes Care 2007;30:753-759
קישורים חיצוניים
- תנגודת לאינסולין, גורמים, ביטוי קליני וטיפול, מדיקל מדיה
המידע שבדף זה נכתב על ידי פרופ’ מוחמד עבדולגני, Division of Diabetes, University of Texas Health Science Center at San Antonio


 כניסה
כניסה  עקבו אחרינו בפייסבוק
עקבו אחרינו בפייסבוק