Napsin A
| מדריך בדיקות מעבדה | |
| Napsin A | |
|---|---|
| |
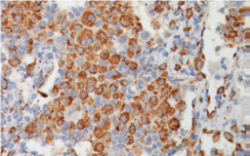
אנוקרצינומה של הריאה בצביעת Napsin A
| |
| מעבדה | פתולוגיה ברקמת ביופסיה |
| תחום | אבחנה מבדלת בין אדנו-קרצינומה ראשונית ריאתית לבין סוגי סרטן ריאות אחרים. |
| יוצר הערך | פרופ' בן-עמי סלע |
לערכים נוספים הקשורים לנושא זה, ראו את דף הפירושים – סרטן ריאות
בסיס פיזיולוגי
סרטן ריאות הוא סוג הסרטן המאובחן בשכיחות הגדולה ביותר (1.6 מיליון מקרים חדשים מדי שנה), והוא מהווה סיבה מובילה בתמותה מסרטן בעולם (Bishop וחב' ב-Hum Pathol משנת 2010, ו-Ueno וחב' ב-Br J Cancer משנת 2003). רוב המקרים של סרטן ריאות מתגלים לראשונה בשלב מתקדם של המחלה, עם שיעור הישרדות ל-5 שנים של 14 אחוז בלבד. ל-napsin A יש תפקיד בעיבוד של surfactant B הריאתי המיוצר על ידי פנאומוציטים אלבאולריים type II (Brasch וחב' ב-Biol Chem J משנת 2003, ו-Ueno וחב' באותו כתב עת משנת 2004), מה שהפך את napsin A לסמן פוטנציאלי של אדנוקרצינומה ראשונית של הריאות.
משנת 2004 דיווחו Rosai וחב' ב-9th Ed Ackerman's Surgical Pathology, על כך שגידולים פרימריים של מערכת הנשימה מתחלקים למספר סוגים היסטולוגיים, כאשר רובם מהווים שאתות ממאירות ממוצא אפיתליאלי. בקבוצת שאתות אלה, רוב המקרים מסווגים כ-non-small cell lung carcinomas (להלן NSCLCs) ומהווים כ-80 אחוז מכלל סרטני הריאות, או כ-small cell carcinomas (להלן SCCs), המהווים את שארית 20 אחוז של סרטן הריאות (Colby וחב' ב-Atlas Tumor of Pathology משנת 1994). ההערכה המקובלת היא שרוב המקרים של NSCLC מורכבים מ-adenocarcinoma (כ-40 אחוז) ומ- squamous cell carcinoma ו-large cell carcinoma.
בעבר, די היה באבחון קרצינומה ראשונית של הריאה כ-NSCLC או כ-SCC למטרות טיפוליות. אך עם הפיתוח של תרפיות חדשות ויעילות לטיפול ב-adenocarcinoma, חיוני במידת האפשר לסווג את תת-הסוג של NSCLC. טיפולים אלה כוללים א) תכשירים המכוונים כנגד מוטציות בקולטן של EGF, וכנגד גנים מוטנטים הגורמים לאיחוי של האנזים ALK או anaplastic lymphoma kinase המזרחן את טירוזין קינאזה בקולטני תאים, עם חלבונים אחרים דוגמת EML4, כאשר הצמד EML4-ALK הוא אונקוגני ואחראי ל-3–5 אחוז מכלל מקרי NSCLC. הגנים של איחוי ALK נמצאים כמעט באופן בלעדי ב-adenoacrcinoma (Soda וחב' ב-Nature משנת 2007, Sasaki וחב' ב-Eur J Cancer משנת 2010, ו-McDermott וחב' ב-Cancer Res משנת 2008); ב) התכשיר bevacizumab שהוא נוגדן חד-שבטי כנגד VEGF, המשמש כטיפול קו-ראשון באדנוקרצינומות רבות, אך עלול לגרום דימום חמור ואף מסכן חיים במטופלים עם קרצינומה של תאי קשקש; ג) תכשיר חדש יחסית כמו pemetrexed עשוי להיות יעיל באדנוקרצינומה אך לא בקרצינומה של תאי קשקש. לכן קריטי לסווג באופן מדויק ככול האפשר את סוג סרטן הריאה כדי להקל על שיקולי הטיפול האופטימאלי (Loo וחב' ב-J Thorac Oncol משנת 2010, וכן Rossi וחב' ב-Curr Med Chem משנת 2010, כמו גם Cagle ו-Dacic ב-Arch Pathol Lab Med משנת 2011 ו-Travis וחב' ב-J Thoacic Oncol משנת 2011).
הריאות הן גם יעד מקובל לגרורות של שאתות מאזורי גוף אחדים, כולל סרטני שד, סרטן מערכת העיכול, וסרטן מערכת השתן והרבייה. אדנוקרצינומה גרורתית ממקור ראשוני בלתי-ידוע מהווה 3–5 אחוז מכלל השאתות הממאירות, ובתור שכזו מהווה אחת מתוך 10 סוגי הסרטן השכיחים ביותר באדם (Pavlides וחב' ב-Eur J Cancer משנת 2003, ו-Varadhachary ב-Cancer משנת 2004). חתכים של רקמות סרטניות הצבועים בצביעת hematoxylin-eosin מהווה עדיין השיטה הנפוצה ביותר לפיה מסווגים סרטני ריאה, אך הסיווג של NSCLC ושל סוגי סרטן עם דרגת דיפרנציאציה נמוכה יותר קשה להשגה על ידי צביעת HE בלבד (Field וחב' ב-J Natl Cancer Inst משנת 2004 ו-Stang וחב' ב-Lung Cancer משנת 2006).
מאז סוף המאה ה-20 התבלטה הגישה של שיטות אימונו-היסטוכימיות כמכשיר עזר לאבחון מבדיל של קרצינומות של הריאה, בין אם הן שאתות ראשוניות של הריאה או שהם גרורות של שאתות שמקורם באיברים כגון מעי גס, שד, ערמונית, קיבה, כליות, שלפוחית השתן, שחלות ורחם. למרות שנכון לשנת 2013 לא קיים סמן מוסכם של שאת ריאתית, מאמצים לאתר סמן כזה היו בהחלט נמרצים. למרות שתאי-גזע פרוגניטוריים נחשבים כמועמדים הולמים לגישה אימונו-היסטוכימית לסיווג ומיון של קרצינומות של הריאה, לא נרשמה עדיין התקדמות מרשימה בתחום זה (Moreira וחב' ב-Mod Pathol משנת 2012).
תכונות napsin A כאנזים ממשפחת ה-aspartic proteinases
אנזימי aspartic proteinases שייכים למשפחת האנדו-פפטידאזות, והם מכילים 2 שיירי חומצה אספרטית באתר הפעיל שלהם, כל אחד מהשניים במקטע (domain) נפרד (Khan ו--James ב-Protein Sci משנת 1998). חברים אחרים במשפחת אנזימים זו הם ,cathepsin E cathepsin D, רנין, פפסין, gastricin ,chymosin של בקר. רבים מהאנזימים הללו נחקרו באופן מקיף, שכן תפקידם הפיזיולוגי מוגדר היטב, והם קשורים למצבים פתולוגיים כגון סרטן ( Rochefort ב-Acta Oncol משנת 1992) ומחלות אחרות (Kay וחב' ב-Protease Role in Health & Dis משנת 1988). בסוף שנות ה-90 תואר בבני-אדם ובעכברים האנזים A napsin שהואaspartic proteinase המופיע כשני איזופורמים napsin A ו-napsin B -ביניהם יש הומולוגיה של 85 אחוז ( Tatnell וחב' ב-FEBS lett משנת 1998). מייחסים ל-napsin A תפקיד בבשלות של surfactant הריאות הפעיל. העובדה שה-mRNA של napsin A ממוקם באופן ספציפי ברקמת הריאות והכליות, מצביעה על תפקיד ביולוגי שונה מזה של aspartic proteinases אחרים (Suzuki וחב' ב-Pathol Res Pract משנת 2005).
ל-napsin A שהוא חלבון מונומרי, משקל מולקולארי של 38,000 דלטון, והוא מכיל 420 חומצות אמינו. החלבון מקודד על ידי הגן NAPSA הממוקם בכרומוזום 19 בעמדה 19q13.33 והוא מכיל 10 אקסונים (Cook וחב' ב-Biochim Biophys Acta משנת 2002). הנקודה האיזואלקטרית של napsin A היא 5.29.
הערכה השוואתית של Napsin A, 5/6 cytokeratin, p63 ו- thyroid transcription factor 1 באבחון אדנוקרצינומה לעומת squamous cell carcinoma של הריאה
Whithaus וחב' ב- Arch Pathol Lab Med משנת 2012 דיווחו על כך שאבחנה מבדלת בין אדנוקרצינומה של הריאה לבין סוגי ממאירויות ראשוניים אחרים של הריאה חשובה קלינית. קלסיפיקציה מורפולוגית מדויקת נמנעת לרוב כיוון ש-70 אחוז מסרטני הריאה מאובחנים על בסיס של FNA או על בסיס דגימות המתקבלות על ידי ביופסיה טרנס-ברונכיאלית. למרות ש- thyroid transcription factor 1 (להלןTTF-1 ) נחשב היסטורית כסמן הספציפי ביותר של אדנוקרצינומה של הריאה, התברר ש-napsin A הוא סמן יותר רגיש ויותר ספציפי מ-TTF-1. במחקר המתואר בוצעה הערכה מורפולוגית של 291 דגימות משאתות ריאה (מתוכן 165 מקרי אדנוקצינומה, ו-66 מקרי squamous cell carcinomas). צביעות אימונו-היסטו-כימיות ל-4 הסמנים המוזכרים בוצעו על רקמות microarray של ביופסיה מקובעות בפורמלין.
תוצאות המחקר היו כדלקמן: ל-Napsin A נמצאה רגישות של 83 אחוז וספציפיות של 98 אחוז; ל-TTF-1 נמצאה רגישות של 60 אחוז וספציפיות של 98 אחוז לאדנוקרצינומה. ל- cytokeratin 5/6 נמצאה רגישות של 53 אחוז וספציפיות של 96 אחוז, ול-p63 נקבעה רגישות של 95 אחוז וספציפיות של 86 אחוז ל- squamous cell carcinoma. פאנל של Napsin A ו-p63 נמצא בעל רגישות של 96 אחוז וספציפיות של 94 אחוז לאבחנה מבדלת של אדנו-קרצינומה מ-squamous cell carcinoma. כלומר, שילוב של 2 סמנים,napsin A ו-p63, הוא האידיאלי לאבחנה מבדלת בין 2 שאתות הריאה האמורות. מחקרים אחדים תומכים ב-Napsin A כסמן בעל רגישות גבוהה של 59–100 אחוז לאדנוקרצינומה של הריאה (Kadivar ו-Boozari ב-Appl Immunohistochem Mol Morphol משנת 2013, Bishop וחב' ב-Hum Pathol משנת 2010, Terry וחב' ב-Am J Surg Pathol משנת 2010 ו-Mukhopadhyay ו-Katzenstein ב-Am J Clin Pathol משנת 2012), ספציפיות גבוהה של ,88-94 אחוז, ערך ניבוי חיובי (ppv) של 78–90 אחוז, וערך ניבוי שלילי של 72–96 אחוז (Turner וחב' ב-Arch Pathpol lab med משנת 2012).
השוואה בין napsin A ו-TTF-1 בספציפיות הביטוי באדנוקרצינומה ראתית ראשונית
אחד הסמנים בעלי ביטוי מוגבל, שניתן להיעזר בו כדי להפריד עם דרגת ביטחון סבירה בין שאת ראשונית של הריאה לבין גרורה ממקור מרוחק, הוא TTF-1 או thyroid transcription factor-1. סמן נוסף ספציפי לריאות הוא napsin-A, שמצטייר כסמן משלים ביחד עם TTF-1 בהגדרת קרצינומות של הריאה, וכן לסייע בתת-הסיווג של NSCLC כמו גם לסייע באבחנה מבדלת של NSCLC (בעיקר אדנוקרצינומות עם דרגת דיפרנציאציה נמוכה), מקרצינומת תאים קטנים (SCC) (Jagirdar ב-Arch Pathol Lab Med משנת 2008).
Turner וחב' דיווחו ב-Arch Pathol Lab med משנת 2012 על גישה אימונו-היסטו-כימית בביצוע השוואה בין napsin A לבין TTF-1, על microarrays רקמתיים של 1,674 מקרים של קרצינומה: 303 מקרי אדנוקרצינומה ראשונית (18.1 אחוז), 200 מקרים של squamous cell lung carcinomas ראשונית (11.9 אחוז), 52 מקרים של small cell lung carcinomas ראשונית (3.1 אחוז), קרצינומה של הכליה (320 מקרים, 19.1 אחוז), קרצינומה פפילואידית של התירואיד (96 מקרים, 5.7-48.3 אחוז), קרצינומה של כיס המרה (89 מקרים,5.3 אחוז ), קרצינומה של שלפוחית השתן (47 מקרים, 2.8 אחוז), קרצינומה של השד (93 מקרים, 5.6 אחוז), קרצינומה של המעי הגס (95 מקרים, 5.7 אחוז), קרצינומה של הכבד (96 מקרים, 5.7 אחוז), קרצינומה של השחלות (45 מקרים, 2.7 אחוז), קרצינומה של הלבלב (48 מקרים, 2.9 אחוז), קרצינומה של הערמונית (49 מקרים, 2.9 אחוז), קרצינומה של הקיבה (93 מקרים, 5.6 אחוז), וקרצינומה של האנדומטריום (48 מקרים, -2.9-16.2 אחוז).
תוצאות המחקר היו כדלקמן: Napsin A נמצא רגיש יותר מאשר TTF-1 במקרה של אדנו-קרצינומה ראשונית של הריאה, (87 אחוז לעומת 64 אחוז, p<0.001). Napsin A נמצא יותר ספציפי מאשר TTF-1 במקרים של אדנוקרצינומה ראשוני של הריאה, וכן מכל סוגי הקרצינומה המוזכרים פרט לקרצינומה של הכליות (p<0.001).
מסקנת בעלי מחקר זה היא ש-napsin A עדיף על TTF-1 באבחנה מבדלת של אדנוקרצינומה ראשונית של הריאות מקרצינומות אחרות (פרט לאלו של הכליה), ובפרט מ-SCC ראשונית של הריאות, ומקרצינומה ראשונית של התירואיד. שילוב של בדיקת Napsin A ושל TTF-1, שימושי להבדיל אדנוקרצינומה ראשונית של הריאות המתקבלת חיובית ל-napsin A ול-TTC-1, לבין קרצינומת תאי קשקש ראשונית של הריאות המתקבלת שלילית לשני סמנים אלה, או לבין small cell carcinoma ראשונית של הריאות המתקבלת שלילית ל-napsin A וחיובית ל-TTF-1.
ביטוי של Napsin A בממאירויות של הכליה
מחקרים אחדים זיהו ביטוי של Napsin A ברקמה נורמלית של הכליה (Chuman וחב' ב-FEBS lett משנת 1999) בעיקר באבוביות הכליה הפרוקסימליות והמְפֻתָּלות (convoluted) (Mori וחב' ב-Arch Histol Cytol משנת 2002). החברה הבינלאומית לפתולוגיה אורולוגית (ISUP), החליטה על מדרג Vancouver של ממאירות כלייתית וחלוקה לקטגוריות שונות כגון שאתות מטנפריות, גידולים נפרובלסטיים, גידולים מזנכימליים, גידולים מעורבים מזכימליים ואפיתליאליים, גידולים נוירואנדוקריניים, גידולים המטופויאתיים ולימפואידיים, גידולים של תאי נבט (germ cells) ועוד (Srigley וחב' ב-Am J Surg Pathol משנת 2013).
Zhu וחב' דיווחו ב-Diagn Pathol משנת 2015, על תוצאות מחקר אימונו-היסטוכימי בביופסיות מגידולי כליה שונים, תוך שימוש ב- microarray רקמתי (TMA). המחקר כלל 159 דגימות של סוגי סרטן כליה שונים, ותוצאות מחקרם כדלקמן: Napsin A התגלה ב-2 מתוך 2 מקרים של RCC או acquired cystic disease associated renal cell carcinoma, ב-5 מתוך 45 מקרים של chromophobe RCC (11.1 אחוז), ב-10 מתוך 23 מקרים של Clear cell RCC (43.5 אחוז), ב-9 מתוך 19 מקרים של cell papillary RCC Clear (47.4 אחוז), ב-3 מתוך 3 מקרים של metanephric adenoma (100 אחוז), ב-13 מתוך 23 מקרים של oncocytoma (56.5 אחוז), וב-31 מתוך 37 מקרים של papillary RCC (83.8 אחוז). לא נמצא ביטוי של Napsin A ב-mucinous tubular carcinoma, ב-spindle cell carcinoma, ב-TEE/MITF carcinoma, וב-urothelial carcinoma.
Napsin A הוא סמן ספציפי ב-Clear cell adenocarcinoma של השחלות
אדנוקרצינומה של תאי Clear בשחלות כרוכה לעיתים קרובות עם endometriosis (Kennedy וחב' ב-Gynecol Oncol משנת 1989, ו-Pearce וחב' ב-Lancet Oncol משנת 2012), וכן נמצא שעקה הנגרמת מעודף ברזל גורם לאמפליפיקציה של הגן Met וקרצינוגנזה בשחלות ( Yamaguchi וחב' ב-Clin Cancer Res משנת 2008, ו-Yamashita וחב' ב-PLos One משנת 2013). בהשוואה לאדנוקרצינומה סרוזית, תאי clear של אדנוקרצינומה עמידים לטיפול כימותרפי המבוסס על פלטינום (Sugiyama וחב' ב-Cancer משנת 2000, ו- Yamashita וחב' ב-Modern Pathol משנת 2015), כך ששיעורי ההישרדות של מטופלות עם אדנוקרצינומה של תאי clear גרועים יותר. לכן חיוני להבדיל בין הסוג האחרון של סרטן השחלות, מסוגי סרטן שחלות אחרים, לצורך החלטות טיפוליות.
המחקר של Yamashita וחב' בחן 195 מקרים של סרטן שחלות, לבחון את הביטוי של napsin A על פני תאי סרטן אפיתליאלי של השחלות, שלא נבחנו קודם לכן בהקשר זה. מחקר זה מצא בגישה של צביעה אימונו-היסטוכימית תוצאה חיובית של ביטוי napsin A ב-71 מתוך 86 מקרים של אדנוקרצינומה של תאי Clear (83 אחוז), ובכול 13 המקרים של אדנופיברומה של תאי Clear שלייתית. לא נמצא כל ביטוי של napsin A ב-30 מקרים של serous adenocarcinoma, ב-11 מקרים של serous adenoma, ב-10 מקרים של mucinous adenocarcinoma, ב-19 מקרים של endometrioid adenocarcinoma, ב-22 מקרים של mucinous adenoma, וב-3 מקרים של yolk sac tumor של השחלה. תוצאתnapsin A חיובית התקבלה בכל 5 הדגימות של אנדומטריוזיס עם אפיתל א-טיפי. יתרה מכך, לא נמצא כל ביטוי של napsin A על פני שטח הפנים של אפיתל תקין של השחלה, על פני האפיתל של החצוצרות, על פני אפיתל קשקשי, על פני האפיתל האנדו-סרביקאלי, או על פני האנדומטריום של הרחם. מסקנת בעלי המחקר היא שיש להתייחס ל-napsin A כאל סמן רגיש וספציפי להבדיל בין גידולי תאי Clear של השחלה (במיוחד אדנוקרצינומה אך גם אדנופיברומה), לבין גידולי שחלה אחרים.
הוראות לביצוע הבדיקה
הבדיקה שהיא חצי כמותית מתבצעת בצביעה אימונו-היסטו-כימית. לאחר ביצוע של הגידול הסרטני, מכינים "בלוק" על ידי קיבוע בפורמלין ו-embedding בפרפין, וזכוכית נושא אחת בה החומר שנלקח בביופסיה נצבע על ידי hematoxylin & eosin . פרוסות הרקמה לצורך הצביעה והמיקרוסקופיה הן בעובי של 4 מיקרון. הדגימה צריכה להישלח למעבדה בטמפרטורת החדר (מועדף), או בקירור. יש לפסול דגימות הנשלחות מוקפאות/רטובות, או כמשטחים ציטולוגיים, או כרקמות שלא עברו קיבוע בפורמלין, או embedding בפרפין.
ראו גם
המידע שבדף זה נכתב על ידי פרופ' בן-עמי סלע, המכון לכימיה פתולוגית, מרכז רפואי שיבא, תל-שומר;
החוג לגנטיקה מולקולארית וביוכימיה, פקולטה לרפואה, אוניברסיטת תל-אביב (יוצר הערך)


 כניסה
כניסה  עקבו אחרינו בפייסבוק
עקבו אחרינו בפייסבוק 