ProPSA
| מדריך בדיקות מעבדה | |
| ProPSA | |
|---|---|
| שמות אחרים | p2proPSA, [-2]proPSA |
| מעבדה | כימיה בדם |
| תחום | אבחון סרטן הערמונית |
| טווח ערכים תקין | פחות מ-15 פיקוגרם/מ"ל |
| יוצר הערך | פרופ' בן-עמי סלע |
הבדיקות המסורתיות לאבחון סרטן הערמונית
סרטן הערמונית הוא סוג סרטן שכיח, ובשנת 2008 נרשמו בארצות הברית כ-186,000 מקרים חדשים, עם תמותה של 28,600 מהמחלה באותה שנה. בשנת 2008 אובחנו באירופה 366,000 מקרים חדשים עם 55,000 פטירות מהמחלה (Schroder וחב' ב-N Eng J Med משנת 2009). פרט לסקירת על-שמע דרך החלחולת (TRUS), בדיקת מישוש דרך החלחולת, או נטילת ביופסיה מבלוטת הערמונית, רוב מקרי סרטן הבלוטה מאובחנים במסגרת בדיקות סקר של האנטיגן הספציפי PSA, שהוא אנזים פרוטאוליטי ממשפחת הסרין- פרוטאזות הנוצר בתאי האפיתל של הבלוטה כאשר קרצינומה של הערמונית, אך גם שגשוג טב שלה, מגבירים את הפרשתו לדם. מאז שזוהה PSA בשנת 1979 (Wang וחב' ב-Invest Urol) הוא המדד המקובל לגילוי סרטן הערמונית, אם כי כ-30% מהבדיקות מתבררות בדיעבד ככזובות-שליליות (false negative), ולמעלה מ-50% מבדיקות PSA מתבררות ככזובות-חיוביות (false positive), המחייבות בדיקות המשך ולעיתים אף לטיפולים מיותרים.
המגבלה העיקרית של מדד PSA נובעת מכך שחלבון זה נוצר בכלל תאי בלוטת הערמונית, ולאו דווקא של תאים סרטניים, לפיכך, רמה מוגברת של PSA בדם יכולה להתרחש בשגשוג טב של הבלוטה (BPH), במצבי דלקת שלה (prostatitis), כתוצאה משפיכת זרע יום לפני הבדיקה, מטראומה קלה לבלוטה בהחדרת צנתר, מביופסיה, מבדיקה ידנית דרך החלחולת או אפילו מאצירת שתן. לכן נוספו במרוצת השנים מדידות נוספות של מרכיבי PSA כפי שנראה להלן. PSA מופיע בדם בצורה חופשית (להלן fPSA) או בצורה של קומפלקס (להלן cPSA) עם מעכבי פרוטאזות כגון אלפא-1-כימוטריפסין ואלפא-2 מאקרוגלובולין (Lilja וחב' ב-Clin Chem משנת 1991). כ-70-90% מ-PSA מופיעים כ-cPSA, והשאר בצורת fPSA. קביעת היחס בין המקטע החופשי והקשור של PSA משפרת בהרבה את היכולת להבדיל בין סרטן הבלוטה לבין שגשוג טב שלה, בעיקר בנבדקים עם רמת PSA שבין 4–10 ננוגרם/מ"ל, הנחשבת רמה מוגברת.
ככל שאחוז fPSA גבוה יותר, לרוב 20-30%, הסיכון לסרטן הערמונית קטן יותר, אך כאשר שיעור fPSA נמוך מ-10%, גדל הסיכון לסרטן הערמונית, שכן הצורה החופשית של PSA מרוכזת בעיקר ב-transition zone בליבת הערמונית שגדלה בשגשוג טב של הבלוטה (Micolajxycyk וחב' ב-Urology משנת 2000), כאשר תאי הסרטן מרוכזים בעיקר בשכבת האפיתל ההיקפית של הבלוטה. הוכנסו מדדי הערכה נוספים באשר לנתוני PSA:
- מדד קצב ההשתנות של PSA או PSA velocity, העוזר בהערכה של הסיכון להתרחשות ממאירה בערמונית, כאשר רמת PSA הנמדדת עולה בשיעור של לפחות 0.75 ננוגרם/מ"ל מדי שנה בנבדקים עם רמת בסיס של סך-PSA גדולה מ-4 ננוגרם/מ"ל, מה שעשוי להצדיק ביצוע ביופסיה. לעומת זאת, עלייה שנתית מרבית של 0.35-0.4 ננוגרם/מ"ל בנבדקים עם ערכי סך-PSA הנמוכים מ-4 ננוגרם/מ"ל אינה מחייבת המשך בירור מידי (Loeb וחב' ב-J Urol משנת 2010)
- מדד נוסף הוא של צפיפות (density) של PSA, והוא מתייחס לרמת PSA בדם ביחס לגודל הבלוטה המתקבל בבדיקת על-שמע. מדד זה מתקבל על ידי חלוקת התוצאה של סך-PSA בנפח הערמונית, כאשר יחס המתקבל בין 0.1-0.15 נחשב תקין, ואילו יחס הגבוה מ-0.15 נחשב חשוד ומצדיק ביופסיה (Loeb וחב' ב-Urology משנת 2008).
במנגנון אחר שהוצע נלקחת בחשבון הגדלת נפח הערמונית עם הגיל, ומדד זה של age-specific PSA, מבוסס על הנתונים הבאים: בסקירה של כ-12,900 גברים, הוגדרו ערכי סף לסך-PSA של 2.5 ננוגרם/מ"ל לגברים בעשור החמישי; 3.5 ננוגרם/מ"ל בעשור השישי; 4.5 ננוגרם/מ"ל בעשור השביעי, ו-6.5 ננוגרם/מ"ל בעשור השמיני לחיים (Cheli וחב' ב-Urology משנת 2002). אך שיטה זו לא התקבלה בשל החשש שהיא עלולה להחמיץ מקרי סרטן הבלוטה ברבים מהנבדקים המבוגרים יותר. במסגרת בירור שמטרתו להבדיל בין תהליכים ממאירים לשגשוג טב של הבלוטה, ניתנה תשומת לב מוגברת למשמעות של fPSA, והיה בכך לכאורה מהלך מנוגד לממצא שככל שגדל מקטע fPSA קטנה סכנת האבחון של ממצא סרטני. כבר בשנת 1994 הועלתה הצעה, שתאים סרטניים המייצרים PSA הם גם מייצרים יותר אלפא-1-כימוטריפסין, בעוד שתאי ערמונית בריאים מייצרים חלבון הקושר-PSA בהיקף זעום, מה שיכול להסביר מדוע fPSA מזוהה יותר עם ממאירות הבלוטה.
מחקרים ראשונים על יעילות proPSA לאבחון סרטן הערמונית
במחקר משנת 2001 אפיינו Mikolajczyk וחב' ב-Cancer Res, את השיעורים היחסיים של צורות fPSA השונות בנסיוב של 157 גברים שאובחנו לוקים בסרטן הערמונית על פי ממצאי ביופסיה, אשר נמדדו בהם ערכי סך-PSA של 4–10 ננוגרם/מ"ל. נמצא, כי שיעור ה-fPSA מכלל ה-PSA היה 16% בממוצע. בנוסף, בפילוח המקטעים השונים המרכיבים את ה-fPSA, התברר שזה האחרון מכיל שלושה מרכיבים:
- 28% מכלל ה-fPSA מהווים מקטע של benign PSA, שהיא מולקולה הדומה למולקולת PSA, אך היא משוללת כל פעילות אנזימטית, כיוון שעברה ביקוע תוך-מולקולארי ליד השיירים Lys145 ו-Lys182 ברצף של חלבון זה. ה-benign-PSA נמצא בריכוז גבוה במיוחד בקשריות (nodules) טבות ומביא לשגשוג טב של הבלוטה; הוא נוצר בעקבות ביקוע פרוטאוליטי post translational בתוך רקמת הערמונית. במחקרים שונים נמצא שריכוז ה-benign PSA יכול לנוע בין שיעורים בודדים עד 50% מכלל ה-fPSA, והוא אופייני לשגשוג טב של הבלוטה.
- 33% מכלל ה-fPSA מהווה צורת ה-proPSA על שלושת תת-מרכיביה על פי החלוקה הבאה: 17% שמורים לשתי צורות של proPSA: זו השלמה [-7]proPSA המכילה 244 חומצות אמינו, וזו החסרה שתי חומצות אמינו [-2]proPSA; 10% מהווה הצורה הקטומה (truncated) של proPSA החסרה 3 חומצות אמינו- [-4]proPSA, ו-6% מהווה צורת ה-[-5]proPSA בה נבקעו 5 חומצות אמיניות.
- 39% מכלל ה-fPSA הם בצורת inPSA, שהיא צורה שלמה של מולקולת PSA המכילה 244 חומצות אמינו. צורה זו חסרה פעילות אנזימטית והיא מכונה intact, inactive PSA. צורה זו היא מולקולה שבה אין ביקוע פנימי ליד שיירי ליזין, אך היא משוללת כל פעילות אנזימטית ואף אינה יוצרת קומפלקס על חלבוני נסיוב כתוצאה משינוי מרחבי באזור הקצה ה-N טרמינאלי של מולקולה זו. אין הבדלים מובהקים ברמות inPSA בנסיוב של גברים עם או ללא סרטן הערמונית, אך היחס בין inPSA ל-fPSA נמצא גבוה משמעותית בדמם של אלה עם ממצא סרטני בבלוטה (Mikolajczyk ו-Rittenhouse ב-Keyo J Med משנת 2003, ו-Nurmikko וחב' ב-Clin Chem משנת 2001).
מחקרים להערכת proPSA כמדד חדש בנסיוב לגילוי מוקדם של סרטן הערמונית
המולקולה החופשית של PSA מופיעה בנסיוב ב-3 צורות לפחות של PSA חסר פעילות פרוטאליטית. אחת מהצורות הללו זוהתה כצורת קודמן (precursor) של PSA וכונתה proPSA, המכילה תוספת של 7 חומצות אמינו בקצה ה-N טרמינאלי של PSA, אשר מכונה Pro-leader או [-7]proPSA, ולראשונה נכרכה צורה זו באופן ספציפי יותר עם סרטן הערמונית כבר בשנת 1997 על ידי Mikolajczyk וחב' ב-Urology. הגליקופרוטאין PSA נמצא באופן סדיר בעיקר בנוזל הזרע בצורתו הבשלה והפעילה. בצורה זו הוא מבקע פרוטאוליטית מולקולות כמו פיברונקטין ו-semenogelin על מנת להפחית את צמיגות נוזל הזרע. צורה פעילה זו של PSA היא בעלת משקל מולקולארי של 28,400 דלטון, מכילה 237 חומצות אמינו, והיא חסרה את השייר הפפטידי הנוסף, המבוקע מחוץ לתא על ידי האנזים kallikrein 2 (hk2).
מתברר שצורת proPSA יכולה לעבור קיטום בתוך תאי הערמונית על ידי ביקוע פרוטאוליטי post translational, אשר במהלכו מורחקות שתיים, שלוש או חמש חומצות אמינו, ונוצרות הצורות 5]proPSA-], [-4]proPSA ו-[-2]proPSA, בהתאמה. מולקולות אלה מופרשות מהבלוטה וניתנות לגילוי בנסיוב, ואף הן צורות PSA שאינן פעילות אנזימטית. התברר, כי צורת [-2]proPSA היא היציבה ביותר בהשוואה לצורות הקטומות האחרות של proPSA, הן בדם והן in vitro, והיא משכה מיד תשומת-לב בהיותה המולקולה המיוצרת באופן מועדף על ידי תאי האפיתל הסרטנים של הערמונית, ואך מעט על ידי תאי הליבה הטבים של הבלוטה.
השלב המתבקש הבא היה להכין נוגדנים חד-שבטיים כנגד [-2]proPSA, ולהשתמש בהם בצביעות אימונו-היסטוכימיות של ביופסיות שנלקחו משאתות בערמונית או מרקמות טבות של הבלוטה. צביעות אלה הוכיחו מובהקות יותר גדולה של נוכחות [-2]proPSA בתאי ערמונית סרטניים (Kumar וחב' ב-Cancer Res משנת 1997, ו-Mikolajczyk וחב' ב-Clin Chem משנת 2004). Sokoll וחב' ב-J Urol משנת 2008, ביקשו להעריך במחקרם את רמת [-2]proPSA בדגימות נסיוב של 123 גברים שרמת PSA בדמם נמצאה בתחום שבין 2–10 ננוגרם/מ"ל. בדיעבד, כאשר נלקחו ביופסיות מהנכללים במחקר, אובחנו 51% מתוכם עם סרטן הערמונית, בעוד שב-49% נשללה אפשרות של סרטן הבלוטה. בעוד שלא נמצא במחקר זה הבדל משמעותי ברמת PSA בין 2 הקבוצות (6.80±5.20 ננוגרם/מ"ל באלה שלא אובחנו עם סרטן הערמונית לעומת 6.94±5.12 ננוגרם/מ"ל באלה שאובחנו עם סרטן הערמונית). במחקר זה נמצא מדד מנבא טוב יותר לנוכחות סרטן הערמונית: שיעור המקטע בדם של [-2]proPSA מכלל ה-fPSA, ששיעורו היה כ-1.53% בחולים עם סרטן הערמונית לעומת 1.10% בקרב הנקיים מהמחלה (p=0.0001).
במחקר זה השיגו 2 מדדים נוספים הקשורים ל-[-2]proPSA הבדלים בעלי מובהקות סטטיסטית, אם כי קלושים יותר, בהשוואת נתונים של נכללים שאובחנו עם סרטן הערמונית לאלה שנמצאו נקיים מהמחלה: הערך המוחלט של [-2]proPSA נקבע כ-11.97 פיקוגרם/מ"ל ו-9.31 פיקוגרם/מ"ל, בהתאמה (p=0.03). כמו כן נקבע היחס [-2]proPSA/benignPSA כ-0.069 ו-0.050, בין לוקים בסרטן לבין בריאים, בהתאמה (p=0.02). במחקר זה לא השיגו כל המדדים שיפורטו להלן מובהקות סטטיסטית, במסגרת השוואת רמתם בנסיוב בקרב נכללים שאובחנו עם סרטן הערמונית, לבין הנכללים הנקיים ממחלה: PSA, fPSA, benignPSA, (%)fPSA ו-(%)benignPSA.
במחקר של Catalona וחב' ב-J Urol משנת 2004, נבחנו בדיעבד 1,091 דגימות נסיוב, מתוכן 555 דגימות עם רמת PSA של 2–4 ננוגרם/מ"ל, ו-536 דגימות שרמת PSA בהן נמצאה בין 4–10 ננוגרם/מ"ל. קביעת רמתם של מדדים אחרים בנסיוב העלתה את הנתונים הבאים: בדגימות עם רמת PSA הנמוכה מ-4 ננוגרם/מ"ל, המדד המבטא את היחס בין proPSA ל-fPSA (או %proPSA) עם סף של 1.8% כהמלצה לביצוע ביופסיה, הביא לאיתור 90% מחולי סרטן הערמונית, כולל 16 מתוך 16 שאתות מחוץ לקפסולה, ו-28 מתוך 29 שאתות עם מדרג Gleason של 7 או יותר, תוך שניתן היה למנוע במדגם זה ביצוע של 19% מהביופסיות המיותרות. שיעור ה-fPSA בנסיוב עלה משמעותית בדגימות משאתות עם מדרג Gleason הגבוה מ-7, לעומת דגימות משאתות עם מדרג Gleason הנמוך מ-7 (p=0.0018). לעומת זאת, בדגימות עם ערכי PSA הגבוהים מ-4.0 ננוגרם/מ"ל, המדד של (%)proPSA נמצא עם הספציפיות הגבוהה ביותר; מנע ביצוע ביופסיות מיותרות, בשיעור של 31%, איפשר לאתר 34/35 שאתות עם מדרג Gleason של 7 ומעלה, ואיפשר לאתר 29/31 שאתות מחוץ לקפסולה. במדגם זה, לא שיפרו מדדים כמו(%)fPSA או רמת ה-PSA הקשור לחלבונים (cPSA) את האיתור של שאתות אגרסיביות בתחום של PSA מעל 4.0 ננוגרם/מ"ל.
אחד המדדים המקובלים באבחון המעבדתי של סרטן הערמונית הוא היחס בין fPSA לסך-PSA. אולם כמו בערכי מעבדה רבים המוגדרים כ"תחום האפור", כך גם התחום של שיעור ה-fPSA, הנע בין 10-15%. Khan וחב' (Urology משנת 2004) בחנו את היתרונות האפשריים במדידת proPSA ב-161 נבדקים עם שיעור PSA חופשי מתחת 15%, בנוסף למדידת ערכי סך-PSA ו-benignPSA . במדגם נבדקים זה בגיל הממוצע של 62 שנה, אובחן בדיעבד סרטן הערמונית ב-66 מתוכם (44%). בנוסף, בהשוואת מדדי המעבדה השונים בין המאובחנים עם המחלה לבין הנקיים ממנה, התקבלו נתונים אלה: סך-PSA בקבוצת החולים בסרטן הערמונית נמדד כ-6.0±4.0 ננוגרם/מ"ל, ובבריאים הוא נמדד כ-6.0±3.0 ננוגרם/מ"ל הממוצע (p לא משמעותי); שיעור PSA חופשי היה זהה בין 2 הקבוצות, 10.0±3.0 ננוגרם/מ"ל; רמת proPSA הממוצעת בקבוצת חולי הסרטן נקבעה כ-0.25±0.2 ננוגרם/מ"ל ובבריאים כ-0.3±0.2 (הבדל סטטיסטי לא משמעותי). שני המדדים היחידים שהשיגו הבדל סטטיסטי משמעותי בין 2 הקבוצות היו רמת benignPSA, שערכה הממוצע בקרב החולים בסרטן הערמונית נקבע כ-0.2±0.2 ננוגרם/מ"ל, ובבריאים נקבע כ-0.4±0.4 ננוגרם/מ"ל, (p<0.001), וכן היחס proPSA/benign PSA, שנקבע כ-1.33±0.7 בקבוצת המאובחנים עם סרטן וכ-0.9±0.7 בקבוצת הבריאים (p<0.001). זו הדגמה טובה נוספת לכך שמדידת proPSA כשלעצמה אינה משפרת את האבחון של סרטן הערמונית אלא אם היא באה בנוסף וביחס למדד אחר כמו benign/PSA.
במחקר שנערך ביפן נכללו 257 גברים יפניים שעברו בדיקות סקר ונמצאו עם ערכי PSA מוגברים שבין 4.1-20.0 ננוגרם/מ"ל. הם עברו בדיעבד בדיקות TRUS ונלקחה מהם ביופסיה של בלוטת הערמונית, ואף נמדדו בנסיוב מדדים אחרים ממשפחת ה-PSA (Miyakubo וחב' ב-Int J Urol משנת 2009). נמצא בדיעבד, כי 124 מתוך הנבדקים (48.2%) אובחנו עם סרטן הערמונית,. בהשוואה בין נבדקים הלוקים במחלה ונבדקים בריאים, נמצא כי מדדי proPSA ו-proPSA/totalPSA, היו 2 הפרמטרים הטובים ביותר, הן ברגישות הממצא והן ביכולת להימנע מנטילת ביופסיות מיותרות. למסקנות דומות באוכלוסייה היפנית הגיע גם Byori ב-Jap J Clin pathol משנת 2015).
במחקר רחב-היקף שנערך ב-2 מרפאות אורולוגיות בברלין, נבחנו דגימות נסיוב של 311 מאובחנים עם סרטן הערמונית, וכן 275 דגימות שנבדקים נקיים מהמחלה (Stephan וחב' ב-Prostate משנת 2009). במחקר זה נעשה שימוש במערכת Access של חברת Beckman Coulter בה נעשו הניסויים המוקדמים בהם התגלה היתרון של proPSA על PSA לגילוי מוקדם של סרטן הערמונית. במחקר באוכלוסייה הגרמנית נמדדו ערכי סך-PSA, (%) fPSA, רמת p2PSA, ו-(%) p2PSA, המהווה למעשה את היחס p2PSA/fPSA. סך-PSA במאובחני המחלה נקבע בממוצע כ-5.47 ננוגרם/מ"ל לעומת 4.9 ננוגרם/מ"ל בבריאים (p=0.0013). אולם ההבדל בין בריאים לחולים נמצא מובהק יותר במדידת (%) fPSA, עם ערכים של 13.2% לעומת 20.4%, בהתאמה, ובמדידת %) p2PSA ) שנקבע בממוצע כ-16.8% בחולים לעומת 11.6% בבריאים. בשני המדדים האחרונים נקבעה דרגת המובהקות כ-p=0.0001.
מחקר נוסף של Stephan וחב' ב-Anticancer Res 2007, בהשתתפות 376 חולים בסרטן הערמונית בתחום תוצאות סך-PSA של 1–25 ננוגרם/מ"ל, שעברו הסרת הבלוטה ונבחנו רמות proPSA ו-fPSA%. תוצאות המחקר הראו שרמת proPSA הייתה שונה משמעותית בין קרצינומה בשלבי pT2 ו-pT3 (עם מובהקות סטטיסטית של p=0.02) בתת-הקבוצה של החולים עם fPSA% נמוך מ-10%. היחס של proPSA/%fPSA היה שונה בין שלבי G2 ו-G3 של המחלה (p=0.004), בין Gleason קטן מ-7 לבין Gleason שווה או גבוה מ-7 (עם p=0.001), ובין שאתות בשלב pT2 ו-pT3 (עם 0.0001p<). עם זאת, רמת fPSA% שיפרה רק ההבדלה בין שאתות בשלב Gleason נמוך או גבוה מ-7, אך לא הייתה בעלת יתרון של הבדלה בין שאתות בשלבי pT2 ו-pT3 או בין שלבי G2 ו-G3. מסקנת מחקר זה הייתה שמדידת proPSA כשלעצמו לא הייתה בעלת יתרון גדול להבדיל בין קרצינומה מוגבלת לקפסולה לבין קרצינומה אגרסיבית, בה בשעה שהיחס proPSA/%fPSA היה בעל יתרון בהערכת ה-staging וה-grading ברמות השונות של סך-PSA.
מחקר עדכני רב-לאומי שהתנהל ב-4 מרכזים רפואיים באוסטריה, סרביה ואיטליה, בחן רמת proPSA ב-122 גברים בהם נקבעה על ידי ביופסיה קרצינומה של הערמונית בשלב 6 במדרג Gleason כאשר ל-19 מתוכם (17%) היו בני משפחה מדרגה ראשונה עם קרצינומה של הערמונית. בהערכה היסטולוגית של ביופסיה נמצא ש-75 מתוך משתתפי המחקר (66%) היו מוגדרים כ- Gleson >7. דם נלקח מהנבדקים ביום שלפני הניתוח להסרת הבלוטה, ונבדק לרמת סךproPSA, fPSA-, חופשיPSA, בשיטת sandwich immunoassay דואלי עם נוגדנים חד שבטיים. ממצאי המחקר הראו רמות proPSA מוגברות באופן משמעותי באלה עם שאת בשלב Gleason>7; בנוסף רמות גבוהות יותר של proPSA נבאו פריצת השאת מחוץ לקפסולה (pT3a<) עם שוליים נגועים (Heideegger וחב' ב-Prostate Cancer Prostate Dis משנת 2017, ו-Heidegger וחב' ב-PLos One משנת 2015).
- שני המדדים, [2-]proPSA% ו-PHI, מדויקים יותר מאשר סך-PSA ו-fPSA% בניבוי של תוצאה חיובית של בדיקת ביופסיה חוזרת
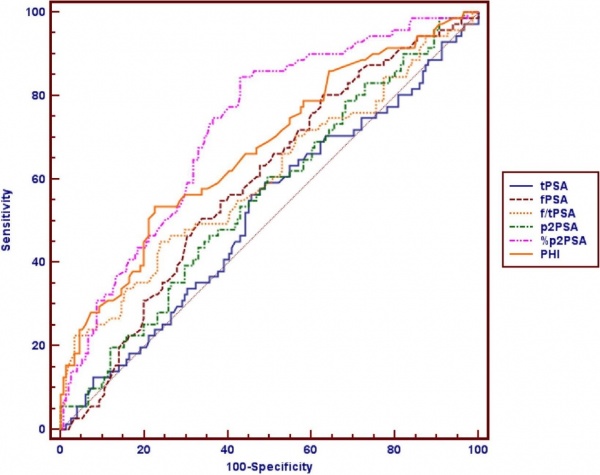
מחקר תצפיתי פרוספקטיבי התקיים בהשתתפות מטופלים עם בדיקת ביופסיה או 2 בדיקות ביופסיה קודמות שהתקבלו שליליות, ואשר קיים לגביהם חשד לסרטן הערמונית (Lazzeri וחב' ב-J Urol משנת 2012). במחקר זה נבחן הדיוק האיבחוני של p2PSA% לפי הנוסחה p2PSA/fPSA, וזה של המדד Prostate Health Index על פי הנוסחה: p2PSA/free PSA X square root of total PSA. תוצאות של 2 מדדים אלה הושוו עם רמות סך-fPSA, PSA ו-PSA%.
תוצאות מחקר זה היו כדלקמן: מתוך 222 נבדקים, סרטן הערמונית התגלה ב-71 מתוכם (31.9%). המנבאים הטובים ביותר לגילוי המחלה היו p2PSA% ו-PHI. מדד p2PSA% נמצא עדיף משמעותית על סך-PSA על fPSA, על PSA% ועל p2PSA בגילוי המחלה (0.01p<), אך לא נמצא עדיף על PHI (מובהקות גבולית של p=0.094). כמו כן נמצא ש-PHI היה עדיף משמעותית בגלוי המחלה על פני סך-PSA, וכן על פני p2PSA עם p<0.001, אך לא נמצא עדיף על פני fPSA עם מובהקות של p=0.109, וכן לא נמצא עדיף על פני fPSA/totalPSA עם מובהקות של p=0.136. בקביעת cutoff של 1.23 לגבי p2PSA% נמצא שניתן היה להימנע מביצוע של 153 ביופסיות חוזרות המהווה 68.9% מכלל הביופסיות שבוצעו, באופן שהיה מחמיץ רק 6 מקרים של סרטן הבלוטה (המהווים 2.7% מכלל הביופסיות). קביעת cutoff של 28.8 לגבי PHI, הייתה מונעת ביצוע מיותר של 116 ביופסיות (המהוות 52.25% מכלל בביופסיות שבוצעו).
תוצאות מחקר זה מסוכמות בטבלה:
| Cutoff | %sensitivity | %specificity | PPV | NPV |
|---|---|---|---|---|
| Total PSA (ng/ml) | ||||
| 17.2 | 93.0 | 8.6 | 32.4 | 72.3 |
| 7.45 | 56.3 | 54.3 | 36.7 | 72.5 |
| 3.23 | 12.7 | 92.0 | 42.8 | 69.1 |
| fPSA (ng/ml) | ||||
| 2.04 | 90.1 | 19.9 | 34.6 | 81.0 |
| 1.08 | 57.7 | 56.3 | 38.3 | 73.9 |
| 0.45 | 7.0 | 90.7 | 26.2 | 67.5 |
| %fPSA | ||||
| 0.24 | 91.6 | 13.9 | 33.4 | 77.9 |
| 0.15 | 54.9 | 56.3 | 38.3 | 73.9 |
| 0.09 | 23.9 | 91.4 | 56.7 | 71.8 |
| proPSA (pg/ml) | ||||
| 7.7 | 90.1 | 11.9 | 32.5 | 71.9 |
| 16.4 | 54.9 | 55.0 | 36.5 | 72.2 |
| 35.7 | 11.3 | 90.1 | 34.9 | 68.3 |
| %proPSA | ||||
| 1.23 | 90.1 | 40.4 | 41.6 | 89.7 |
| 1.68 | 67.6 | 66.9 | 49.0 | 81.4 |
| 2.31 | 31.0 | 91.4 | 62.9 | 73.8 |
| PHI | ||||
| 28.8 | 90.1 | 25.2 | 36.2 | 84.4 |
| 40.4 | 62.0 | 59.6 | 41.9 | 76.9 |
| 62.0 | 29.6 | 90.7 | 60.0 | 73.2 |
- PPV-positive predictive value
- NPV-negative predictive value
מחקר נוסף שנערך על ידי המחלקות לאורולוגיה ופתולוגיה במרכז הרפואי Johns Hopkins, בחן 167 חולים עם סרטן הערמונית שהיו במעקב במרכז זה כדי למצוא את המתאם בין רמות proPSA לתוצאות ביופסיה שבוצעו במעקב שנתי בחולים אלה. המדידה של המדדים השונים, נעשתה על ידי dual 3 monoclonal sandwich תוך שימוש בנוגדני Hybritech וערכת גלאי chemiluminiscence. במסגרת המחקר נמדדו גם רמות סך-PSA, רמת %fPSA, רמת היחס proPSA/%fPSA ונקבע הערך המחושב של PHI. נמצא שפרט לערך של סך-PSA, ארבעת המדדים האחרים שנמדדו או חושבו (%fPSA, ו-proPSA, ו-proPSA/%fPSA, ו-PHI היו במתאם טוב משמעותי ביחס לממצאים ההיסטולוגיים. עם זאת, proPSA ו-PHI סיפקו את דיוק הניבוי הגבוה ביותר לקרצינומצה בשלב המתקדם של המחלה (Tosoian וחב' ב-J Urol משנת 2012).
מחקר עדכני נוסף של Vukovic וחב' ב-Int Braz J Urol משנת 2017, בחן את הערך של proPSA ושל נגזריו בגילוי של סרטן הערמונית בנבדקים עם ערכי סך-PSA בתחום שבין 2–10 ננוגרם/מ"ל. במחקר השתתפו 129 גברים בני 50 שנה ומעלה, ללא היסטוריה קודמת של סרטן הערמונית, עם ממצאים תקינים בבדיקה דיגיטלית של החלחולת אך עם ערכי סך-PSA שבין 2–10 ננוגרם/מ"ל. כל משתתפי המחקר עברו ביופסיה של הבלוטה מכוונת על ידי על-שמע (TRUS) בפעם הראשונה. בכל משתתפי המחקר נמדדו ערכי סך-PSA, ו-fPSA, וכן proPSA, וחושבו ערכי proPSA% ו-PHI. ממצאי המחקר הראו שרמות proPSA% ו-PHI היו באופן משמעותי גבוהות יותר באלה עם קרצינומה של הערמונית בהשוואה לאלה ללא המחלה. אותם נתונים היו נכונים גם לגבי נבדקים עם מדרג Gleason מעל 7, לעומת אלה עם מדרג Gleason נמוך מ-7.
כאשר השוו במחקר זה את המדדים הללו בקרב מאובחנים עם המחלה שסווגו לכאלה עם מדרג Gleason נמוך מ-7 או גבוה מ-7, התקבלו בהתאמה התוצאות הבאות: סך-PSA נקבע בממוצע כ-5.2 לעומת 5.6 ננוגרם/מ"ל, כאשר מובהקות ההבדל היא p=0.08; מדד ה-fPSA נקבע כ-14.1% לעומת 11.9% כשמובהקות ההבדל p=0.004; מדד ה-p2PSA נקבע כ-15.4% לעומת 17.6% עם מובהקות הבדל של p=0.0008. מסקנת מחקר זה הייתה שמדידה אוטומטית של p2PSA מעניקה את המדד הרגיש ביותר לגילוי ממאירות בערמונית, ואף להערכת מידת האגרסיביות של השאת.
הדרך היעילה להערכת היתרונות של מדד ה-proPSA באבחון מוקדם וספציפי של סרטן הערמונית, היא הכנסת מדידה זו לשגרת המעבדות הקליניות. נמצא שכמעט 2 עשורים מופיעים מאמרים המדגישים את יתרונותיה, אך היא עדיין לא הפכה לבדיקה שגרתית. בשנת 2010 הכניסה חברת Beckman Coulter ערכה המבוססת על chemiluminiscence עם חלקיקים פרמגנטיים המצופים בנוגדנים חד שבטיים כנגד[-2]proPSA . הערך המחושב במערכת המתוארת מוגדר כ-prostate health index או PHI, שהוא ערך מתמטי מחושב, המכיל בנוסף לערך של [-2]proPSA גם ערכי סך-PSA ו-fPSA. בהיות הערך המשוקלל PHI ברמות בין 0 ל-21, הסבירות לסרטן הערמונית היא 8.4%, ובערכי PHI שבין 21 ל-40 ההסתברות לסרטן היא 21%. כאשר ערכי PHI נקבעים מעל 40, ההסתברות לסרטן הערמונית היא של 44%. כאשר רמת סך-PSA בדמם של נבדקים נמצאת בתחום של 2–10 ננוגרם/מ"ל, ערכי PHI הם בעלי ספציפיות הגבוהה פי 2.75 מזו של מדד כמו fPSA בהערכה האם לנבדק יש תהליך סרטני בערמונית.
מטה-אנליזה להערכת מדדי [-2] proPSA ו-Prostate Health Index (PHI) לגילוי סרטן הערמונית
מאמרים רלוונטיים זוהו והנתונים על הרגישות והספציפיות מוצו מתוך 12 מחקרים: 10 מחקרים על %[-2] proPSA כללו במקובץ 3,928 גברים מתוכם 1,762 עם סרטן ערמונית מוכח; 8 מחקרים על phi שכללו במקובץ 2,919 גברים מתוכם 1,515 עם סרטן ערמונית מוכח. הרגישות לזיהוי סרטן הערמונית נמצאה כ-90% למדידה המשולבת של %[-2]proPSA ו-phi, בעוד שהספציפיות הייתה רק 32.5% בבדיקת %[-2] proPSA ו-31.6% בבדיקה המשולבת של %[-2] proPSA ו-phi. המדידה של %[-2] proPSA משפרת את הדיוק של גילוי סרטן הערמונית בהשוואה למדידה של PSA או של %fPSA, במיוחד בקבוצת הנבדקים עם PSA של 2–10 ננוגרם/מ"ל. תוצאות דומות הושגו במדידת phi. תוצאות שהתפרסמו מראות גם ש-%[-2] proPSA ו-phi משקפות גם את האגרסיביות של השאת (Filella ו- Giménezב-Clin Chem Lab Med משנת 2013).
בשנת 2014 הופיעה ב-Korean J Urol מטה אנליזה של Abrate וחב' ובה ניתוח של 35 מחקרים שפורסמו בין השנים 1990 ו-2014 על proPSA ומשמעות מדד זה באבחון סרטן הערמונית. מסקנת סקירה נרחבת זו הייתה ש-proPSA ושני נגזריו, proPSA% ו-PHI, משפרים את הספציפיות של המדד המקובל של סך-PSA. מחקר של De Luca וחב' ב-BMC Urol משנת 2016 לגבי משמעות proPSA באוכלוסייה בסיכון גבוה לסרטן הערמונית. במחקר נכללו 106 מטופלים, שעברו הסרת ערמונית בשל קביעת שלב מחלה של pT3/pT4 ו/או שוליים חיוביים. אף לא אחד מהמטופלים טופל לפני או אחרי הניתוח על ידי אנדרוגנים, או על ידי הקרנות. סך-PSA ו-proPSA נמדדו 1, 3, 6, 9 ו-12 חודשים לאחר הניתוח. תוצאות מחקר זה על ההישנות של המחלה מבחינה ביוכימית שנה לאחר הסרת הבלוטה, קובעות שקיימות עליות וירידות ברמת proPSA באופן שלא מומלץ להשתמש במדד זה לאחר ניתוח להסרת הבלוטה במלואה לצורך ניבוי של הישנות המחלה.
הוראות לביצוע הבדיקה
אין צורך בצום או בהכנות מיוחדות. את דגימת הדם יש להקפיד ליטול בבוקר, במבחנה כימית (פקק אדום או צהוב) ולאחר המתנה של 10–15 דקות עד לקרישתו יש לסרכז בצנטריפוגה מקוררת, ואת הנסיוב המופרד יש להקפיא מיד בטמפרטורה של מינוס 70 מעלות. יש להימנע מהקפאות והפשרות מיותרות. המדידה מתבצעת ב-Access Immunoassay Analyzer של Beckman Coulter (על פי Igawa וחב' ב-J Clin Lab Anal משנת 2014).
ראו גם
המידע שבדף זה נכתב על ידי פרופ' בן-עמי סלע, המכון לכימיה פתולוגית, מרכז רפואי שיבא, תל-שומר;
החוג לגנטיקה מולקולארית וביוכימיה, פקולטה לרפואה, אוניברסיטת תל-אביב (יוצר הערך)


 כניסה
כניסה  עקבו אחרינו בפייסבוק
עקבו אחרינו בפייסבוק