הבדלים בין גרסאות בדף "שימור פוריות בחולות אונקולוגיות - Fertility preservation in oncologic patients"
| שורה 55: | שורה 55: | ||
|- | |- | ||
|Unknown risk* | |Unknown risk* | ||
| − | P[[Paclitaxel]], [[Taxotere]], [[Oxaliplatin]], [[Irinotecan]], [[Trastuzumab]], [[Avastin]] (Bevacizumab), [[Cetuximab]], [[Erlotinib]], [[Imatinib]] | + | |P[[Paclitaxel]], [[Taxotere]], [[Oxaliplatin]], [[Irinotecan]], [[Trastuzumab]], [[Avastin]] (Bevacizumab), [[Cetuximab]], [[Erlotinib]], [[Imatinib]] |
==השפעת רדיותרפיה על פריון האישה== | ==השפעת רדיותרפיה על פריון האישה== | ||
גרסה מ־15:22, 5 במאי 2014
ערך זה נמצא בבדיקה ועריכה על ידי מערכת ויקירפואה, וייתכן כי הוא לא ערוך ומוגה.
| שימור פוריות בחולות אונקולוגיות | ||
|---|---|---|
| Fertility preservation in oncologic patients | ||
| יוצר הערך | ד"ר הילה רענני וד"ר דרור מאירוב |
|
עם התפתחות הטיפולים האונקולוגיים ועלייה בשיעור ההחלמה בעקבות טיפולים כימותרפיים ורדיותרפיים, עלה באופן ברור הצורך לתת את הדעת על נושאי איכות החיים של המטופלות, ונושא הפריון בנשים צעירות הוא גורם ראשון במעלה. בזכרים, בשנות ה-50 של המאה הקודמת, החלו להקפיא זרע אנושי. על פי מידע הקיים כיום, נולדו יותר מ-250 אלף איש מזרע שהוקפא החל מ-1996.
מיצוי זרע הוא תהליך פשוט יחסית ועם התפתחות טכנולוגיות ההקפאה ושיטות ההפריה החוץ גופית ובעיקר החדרת תא זרע בודד לביצית (ICSI), הפך תהליך הקפאת זרע בגברים לפני טיפולים אונקולוגיים לתהליך מובן ושיעורי ההצלחה גבוהים[1].
כאשר מדובר בילדה, נערה או אישה העומדת בפני מצב רפואי העשוי לפגוע בפוריותה, תהליך השימור מורכב ועל כן יש צורך ״לתפור חליפה אישית״ לכל אחת, בהתאם למספר גורמים משפיעים שאותם ננסה להבהיר בסקירה זו.
השפעת מחלת הסרטן על הפוריות
פוריות האישה תלויה בתפקוד השחלתי, המהווה תנאי ליצירת הפריה, ומתפקוד הרחם, המהווה חֲמָמִית (Incubator) לגידול העובר. השחלה מתפקדת כל עוד קיים בה מאגר של ביציות השמורות בתוך הזקיקים הראשוניים (Primordial follicles). במשך חיי האישה חלק מהזקיקים מתפתחים לביציות בשלות, אך רוב מאגר הזקיקים מתנוון. ככל שחולפות השנים, מאגר הזקיקים מידלדל עד שמספרם מגיע לרמה קריטית קטנה, המחזור מפסיק והאישה נכנסת לגיל המעבר. מקובל להניח כי הביציות אינן יכולות להתחלק ולגדול במספרן, ועל כן אין תחליף לביציות שנהרסו. אם בגיל צעיר מאגר הביציות בשחלה נפגע עד לרמה קריטית נמוכה והמחזור ההורמונלי נפסק, האישה לא תוכל להרות. אולם, גם במקרים בהם הווסת ממשיכה ומופיעה באופן סדיר לאחר הטיפולים, קיימת שכיחות מוגברת של אי פריון מוקדם והפסקה של המחזור בגיל צעיר מהממוצע[2] עקב הידלדלות מאגר הזקיקים.
השפעת הטיפול האונקולוגי על הפריון
כשל שחלתי מוקדם מוכר כאחת מתופעות הלוואי ארוכות הטווח השכיחות, הפוגעות בנשים בגיל הפריון המטופלות בחומרים כימותרפיים או בקרינה ישירה לאגן.
עבודות היסטולוגיות בבעלי חיים ובשחלות הומאניות הדגימו שהתוצאה הסופית של נזקים מכימותרפיה היו ניוון שחלתי והרס הזקיקים הראשוניים[3] , [4]. ידוע כי מנגנון ההרס אינו ״הכל או לא כלום״[5] וכי מספר הזקיקים הנותר חיוני לאחר חשיפה לכימותרפיה נמצא ביחס הפוך למינון התרופות. מנגנון הפגיעה עדיין אינו מובן כל צורכו, אך נמצא נזק מושרה לתאי פרהגרנולוזה והודגמו תהליכי אפופטוזה במהלך הרס הביציות והזקיקים[6] , [7]. ברמת רקמת השחלה, הודגם נזק לכלי הדם ויצירת מוקדי הצטלקות בקליפת (Cortex) השחלה. מאזורים אלה, הזקיקים נעלמו. ירידה משמעותית במאגר הזקיקים הודגמה בחיות שבייצו, כביכול באופן ״נורמלי״[8].
הגורמים המשפיעים על כושר הפוריות הם הגיל בזמן החשיפה לטיפולים, פרוטוקול הטיפול ובעיקר שימוש בכימותרפיה ממשפחת האלקלואידים (Alkylating agents), מינון וחשיפה לטיפולים קודמים (תמונה1). כאמור, גם הישנות מחזורי וסת עם סיום הטיפולים אינה מבטיחה פוטנציאל פוריות נורמלי. בסקירה שפורסמה[9] הוסק כי הסיכוי להריון עצמוני (Spontaneous) מוערך בכ-28% בנשים שחלו לפני גיל 20, ורק ב-5% אם חלו אחרי גיל 25! במקרים של השתלת מח עצם, כשל שחלתי מופיע ביותר מ-80%, גם אם הטיפול בוצע בגיל הילדות. במידה ויש סכנה ממשית לפגיעה בפוריות, חשוב כי האישה תקבל ייעוץ לגבי האפשרויות השונות לשימור פריון לפני התחלת הטיפול.
תכשירים כימותרפיים
הנזקים הקשים ביותר נגרמים לרקמת השחלה על ידי אלקלואידים כמו Endoxan (Cyclophosphamid). חומרים אלה מאיצים את תהליך הרס הביציות, אחראיים לנזק המשמעותי ביותר למאגר הביציות ולפיכך גורמים להפסקת המחזור ולכשלון השחלה. אצל נשים שטופלו בעברן (למעלה משנה) בחומרים אלה, לא נמצאה עלייה בשיעור הפלות או עלייה בסיכון למומים מולדים[10]. גם לתרופות מקבוצת ה-Cisplatin ואנלוגים יכולת פגיעה משמעותית במאגר הביציות. לעומת זאת, לתרופות ממשפחת ה-Anti metabolics יכולת פגיעה נמוכה ביותר. למרות שאין עבודות אפידמיולוגיות נרחבות לגבי קבוצת ה-Taxol, עבודות בבעלי חיים ובחולות סרטן השד מעידות כי תכשירים אלה הם רעילים למאגר הזקיקים.
סיכום המידע לגבי מידת הפגיעה של תכשירים כימותרפיים בנשים בתלות בפרוטוקול ובגיל האישה, (מופיע במאמרים[11] , [12] , [13] ובטבלה 1).
| טבלה 1. הערכת הסיכון לכשלון שחלה בנשים | |||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| High risk | Stem cell transplant, external beam irradiation to fields including the ovaries, breast cancer adjuvant combination chemotherapy regimens containing Cyclophosphamide, Methotrexate, Fluorouracil, Doxorubicin, Epirubicin in women > 40 years | ||||||||||||||||||||||||||||||||||
| Intermediate risk | Breast cancer adjuvant chemotherapy regimens containing Cyclophosphamide in women 30-39 years, or Doxorubicin/ cyclophosphamide in women > 40 years | ||||||||||||||||||||||||||||||||||
| Low risk (<20%) | Combination chemotherapy regimens for NHL, ALL, AML, breast cancer adjuvant chemotherapy regimens containing Cyclophosphamide in women < 30 years or , or Doxorubicin/ Cyclophosphamide in women < 40 years | ||||||||||||||||||||||||||||||||||
| Very low risk or no risk | Vincristine, Methotrexate, Fluorouracil | ||||||||||||||||||||||||||||||||||
| Unknown risk* | PPaclitaxel, Taxotere, Oxaliplatin, Irinotecan, Trastuzumab, Avastin (Bevacizumab), Cetuximab, Erlotinib, Imatinib
השפעת רדיותרפיה על פריון האישהקרינה ישירה לאזור האגן פוגעת בתפקוד השחלות, דבר העלול להביא להפסקת הפרשת הורמוני המין, מצב הדומה לניתוח לכריתת שחלות. מידת הפגיעה תלויה במינון הקרינה הישירה ובמידת החשיפה לקרינה בסמוך לשדה הקרינה (50-4Gy LD). קרינה לבטן הקרנה כלל גופית (TBI, Total Body Irradiation) במינון של 20-30Gy גורמת ל-97 אחוז כשלון שחלה בנשים ועד 70 אחוז כשלון שחלה בילדות טרם בשלות מינית[13] , [14] , [15]. הרחם עלול להיפגע מקרינה לבטן לאגן או בקרינה, כתלות במינון ובגיל בעת ההקרנה. בילדות שהוקרנו טרם גדילת הרחם, עם ההתבגרות המינית נמצא נפח קטן של הרחם. פגיעה בתפקוד הרחמי עלולה להיגרם בחשיפה למנות קרינה של 14-30Gy כתוצאה מפגיעה הנגרמת לכלי הדם הפוגעת באלסטיות של שריר הרחם. אפילו במינוני קרינה נמוכים יותר, כמו בהקרנה כלל גופית, נראה פגיעה בגדילת הרחם ובזרימות הדם ברקמה. טיפול קרינתי אף לאחר ההתבגרות המינית גורם לפגיעה ברירית הרחם ועל כן קיימת הפרעה ביכולת ההשרשה של העובר. בהריונות שנקלטו מדווח על שיעור הפלות מוגבר, לידות מוקדמות ועל הפרעות בתפקוד השליה. נסיונות לשפר תפקוד הרחם לאחר הקרנה כלל גופית על ידי מתן טיפול הורמונאלי תחליפי הביאו לשיפור מסוים שהתבטא בהתעבות רירית הרחם ובמדידת זרימת הדם, אולם עבודתו של לרסן הדגימה כי הנזק הקרינתי שנגרם לרחם במינוני קרינה ישירה היה בדרך כלל בלתי הפיך[13] , [14] , [15], [16] , [17]. היריון עתידיההחלטה לגבי כניסה להיריון לאחר טיפול במחלת הסרטן היא מורכבת. יש להביא בחשבון מספר גורמים על מנת להגיע להחלטה. מבין השיקולים החשובים יש לציין: מהו פרק הזמן הנדרש על מנת להגיע לסבירות גבוהה של החלמה, מתי מתרחשות עיקר החזרות של המחלה, מהו המעקב הרפואי הנדרש אחרי הישנות מחלה ומתי והאם היריון יפריע לבדיקות מעקב אלו. מהו פרק הזמן שבו האישה פורייה ועדיין יכולה להרות וללדת. נתון חשוב זה קשור לגיל ולטיפולים כימותרפיים קודמים. אחד הגורמים החשובים המובאים בחשבון הוא הרצון להרות, ללדת ולקיים משפחה. אחת השאלות החוזרות הקשורה להיריון היא לגבי הסיכוי להצלחת ההיריון ותקינות העובר. עבודות רבות הדגישו שאין שכיחות מוגברת של הפלות או מומים מולדים בנשים שטופלו בעבר (למעלה משנה) בתרופות כימותרפיות[10] , [18]. אפשרויות לשימור פריון בחולות סרטןכיום קיימים ברשותנו מספר כלים לשימור פוריות. היכולת להשתמש בכלי זה או אחר או בשילוב מספר שיטות תלויה, כמובן, במספר גורמים שאותם עלינו להביא בחשבון כמו גיל החולה, המחלה הבסיסית ופרוטוקולי הטיפול המקובלים בה, התקדמות המחלה והאם קיימת אפשרות לדחיית התחלת הטיפול, מצב בריאותי בעת הייעוץ ורצון האישה והמשפחה[13] , [19] , [20] , [21]. הפריית ביציות ושימור עובריםשימור עוברים בחנקן נוזלי למשך תקופה ארוכה הוכח כיעיל ונמצא בשימוש שגרתי בטיפולי פוריות. במידה שניתן, מומלץ לנשים לעבור טיפולי הפריה חוץ גופית (IVF, In Vitro Fertilisation) והקפאת עוברים לפני מתן טיפול הפוגע בשחלות. לא ניתן ליישם טיפול זה בילדות ובנערות. בנשים לא נשואות, יש להשתמש בזרע תורם למטרות ההפריה. ניתן לשמור עוברים בהקפאה למשך שנים רבות, אף למשך יותר מעשר שנים. על מנת להשיג מספר רב של עוברים, יש צורך במתן טיפולים הורמונליים על מנת לגרות את השחלות. הטיפול גורם לעלייה ברמת האסטרוגן בדם, המהווה מצב היפרקואגולבילי. כמו כן, יש צורך בהתייחסות מיוחדת לנשים החולות בסרטן השד או בגידולים אחרים המושפעים מהורמונים. לשם כך קיימות תכניות טיפול מיוחדות לגירוי השחלות כמו מתן Tamoxifen החוסם את הקולטנים לאסטרוגן או פרוטוקול עם מעכבי ארומטז המונע עלייה ברמות אסטרוגן בזמן הגירוי השחלתי ויכול להתאים לנשים עם סרטן שד או גידול רגיש להורמוני מין. יתרונות השיטה: זוהי השיטה שצברה את הניסיון הרב ביותר עם אחוזי הצלחה ידועים התלויים בגיל האישה ובמשתנים מוכרים אחרים של פוריות הזוג. חסרונות השיטה:
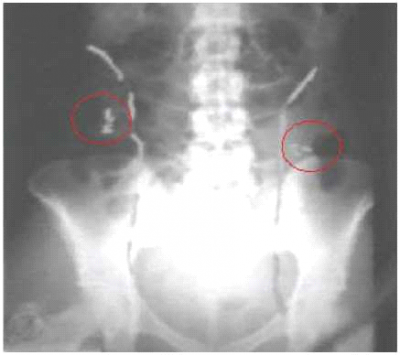
הקפאת ביציות בשלותניתן לשאוב ביציות בשלות מתוך השחלה במחזור הפריה חוץ גופית (IVF) ולהקפיאן ללא הפריה עם זרע. אין צורך בבן זוג ואין צורך להשתמש בבנק הזרע על מנת להקפיא ביציות. מבחינת הגירוי השחלתי, שאיבת הביציות, דחייה במתן הטיפול הכימותרפי והסכנות ההורמונליות, הטיפול זהה לטיפול המתואר בהקפאת עוברים. אולם, ההקפאה אינה יעילה באותה מידה, אם כי לאחרונה דווח על עלייה בשיעורי ההצלחה (כרבע לעומת הקפאת עוברים. שיעור ההריונות - ארבעה אחוזים לביצית מוקפאת שהופשרה) . הסטת שחלותבמידה שצפויה קרינה ישירה לאזור האגן, ניתן לבצע הסטת שחלות בניתוח לפרוסקופי. בשיטה זו מקבעים את שתי השחלות גבוה בגבול העליון של עצמות האגן על ידי תפר או מאחורי הרחם. חשוב לדעת לפני הפרוצדורה את שדה הקרינה המיועד על מנת להוציא את השחלות מחוץ לאזור זה. במהלך ההסטה נשמרת אספקת הדם לשחלות. במקרים רבים תיתכן נפילת השחלות חזרה למקומן המקורי. לכן, רצוי לבצע ניתוח בסמוך ככל האפשר למועד ההקרנה. חסרונות השיטה:
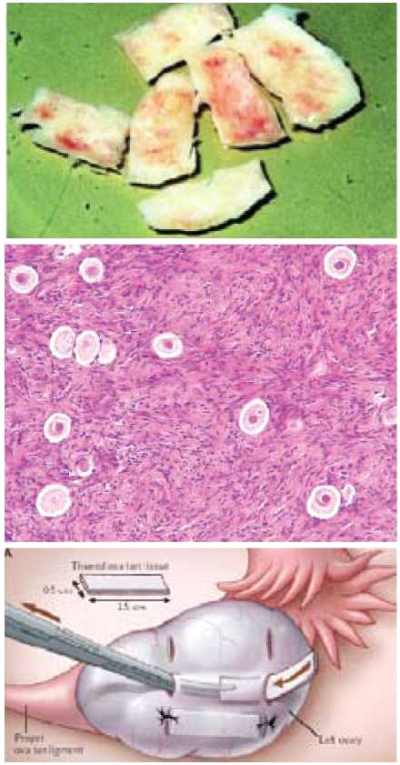
הקפאה והשתלת רקמת שחלהבמידה שצפויה פגיעה בסבירות משמעותית בפוריות האישה עקב הטיפולים הכימותרפיים, ניתן לבצע ניתוח לפרוסקופי שבו מוציאים מקטע ממעטפת שחלה לצורך הקפאה. בשיטה זו מונעים חשיפת הרקמה לגורמים הטוקסים. את מקטע השחלה חותכים לחתיכות קטנות, חלקן נשלח לבדיקה פתולוגית לשלילת הימצאות תאי סרטן. מקטעים אלה מכילים ביציות המוקפות בתאי גרנולוזה וטקה החיוניים לשמירה על איכות הביציות. את תהליך ההקפאה שורדות כ-70 אחוז מהביציות שהוקפאו. מרקמת השחלה ניתן למצות ביציות ולהבשילן במעבדה (IVM) לקראת תהליך הפריה חוץ גופית. את רקמת השחלה ניתן להשתיל חזרה לגוף במיטת השחלה, בסמוך לה בחלל הבטן, או במקום אחר מתחת לעור. הקפאת רקמת שחלה מבוצעת בעולם במרכזים רבים זה כעשר שנים והערכה היא כי מאות נשים עברו עד היום פרוצדורה זו. בארץ בוצעו הקפאות מאז 1996. שיטה זו נחשבת עדיין לנסיונית מאחר שההפשרות וההשתלות חזרה לגוף הנשים בוצעו רק במספר קטן של מקרים. עד היום דווח על חמש לידות (שתי לידות של הריונות ספונטניים ושלוש של הריונות IVF), מספר הריונות שעדיין לא ילדו וכן על מספר הריונות שהסתיימו בהפלות. דווח על מספר הריונות לאחר השתלת שחלה (ללא הקפאה) בין תאומות מונוזיגוטיות. הלידה הראשונה לאחר השתלת רקמת שחלה IVF-I דווחה בבית החולים שיבא. לא ידוע מהו מספר נסיונות ההשתלה שכשלו ולא דווחו[23] , [24] , [25] , [26] , [27]. יתרונות השיטה:
חסרונות השיטה:
על מנת להקטין את הסיכון בהחזרת תאים סרטניים לגוף האישה עם השתלת רקמה שלא עברה חשיפה לטיפול האונקולוגי, יש להקפיד על פרוטוקול בדיקות לפני הקפאת הרקמה ולבצע בדיקות מעמיקות טרם ההשתלה. בעבודה שפרסמנו לאחרונה, 58 חולות עם ממאירות המטולוגית שהופנו לביצוע הקפאת רקמת שחלה לפני טיפול אונקולוגי, עברו בדיקות הדמיה לפני הניתוח הלפרוסקופי וכן בדיקה היסטולוגית של קטעי שחלה לאחר הניתוח. לאחר הפשרת קטעי הרקמה, בוצעו בדיקות אימונוהיסטוכימיות לגילוי מרקרים אופייניים לשלילת שארית מחלה מינימלית. מתוך 58 נשים, אצל שתיים נתגלתה מעורבות שחלתית בהדמיה מקדימה. היסטולוגיה לפני ההקפאה לא הראתה סימני מחלה מינימלית אצל אף אחת מהנשים ולאחר ההפשרה נמצאה בדיקת PCR חיובית רק באישה אחת עם היסטוריה של CML. בדיקה זו מנעה השתלת קטעי רקמה חזרה בגוף האישה. מסקנות העבודה היו כי שילוב כל האמצעים הנ״ל ימנע הקפאת רקמת שחלה עם מעורבות אונקולוגית וכן יאפשר השתלת רקמה ללא שארית מחלה[28]. שיטה זו, על יתרונותיה וחסרונותיה, מוצעת כיום לנשים שהסיכון לאובדן פוריותן משמעותי, כמו לפני טיפולי השתלת מח עצם או פרוטוקולים אגרסיביים . דיכוי שחלתידיכוי שחלתי במנגנון היפותלמי היפופיזרי ניתן להשיג במתן זריקות תקופתיות של תכשירי דקהפפטיל. מטרת הטיפול להקטין חשיפת שחלה לא פעילה לטוקסיות של החומרים הכימותרפיים . יש עבודות בספרות המעידות כי דיכוי פעילות השחלה בזמן טיפולים כימותרפיים עשוי להגן על השחלות מפני הפגיעה השחלתית הנגרמת מטיפולים כימותרפיים. לעומתם, יש עבודות אחרות שלא הוכיחו הגנה על השחלות. טיפולים אלה מיועדים רק לנערות ולנשים לאחר ההתבגרות המינית ולא לילדות שטרם החלו לווסת[29] . הטיפול ניתן בזריקות של GNRH-a depo במרווחים של ארבעה שבועות. רצוי להתחיל את הטיפול לפני התחלת הטיפול הכימותרפי. יתרונות השיטה:
חסרונות השיטה:
לאחר סיום הטיפולים במחלת הסרטן, יש חשיבות רבה למעקב ספציפי אחרי התפקוד השחלתי. ידוע כי גם הישנות מחזורי הווסת אינה בהכרח מבטיחה יכולת פריון רגילה. מעקב זה יכלול בדיקות דם לפרופיל הורמונלי ומעקב סונוגרפי להדמיית נפח השחלות, פעילות הורמונלית ותגובת רירית הרחם. שיטות להערכת רזרבה שחלתית מופיעות בטבלה 2.
במידה שקיים רצון להרות לאחר סיום הטיפול האונקולוגי, יש צורך בהערכת פוטנציאל הפריון והערכת מצב בריאותה הכללי של האישה עקב חשיפה לחומרים כימותרפיים היכולים להשפיע על פעילות הלב, הכליות ומערכות גוף אחרות[10]. במידה שקיים כשל שחלתי מוקדם (היעלמות הווסת בנוכחות גונדוטרופינים גבוהים), ניתן להציע לאישה הפריה באמצעות תרומת ביצית. בהליך זה נלקחת ביצית מאישה תורמת, מבוצעת הפריה חוץ גופית בזרע בן הזוג והעוברים מוחזרים לרחם האישה המקבלת. במידה שקיים חשש לפגיעה ברירית הרחם (בעיקר עקב הקרנה ישירה לאגן), ניתן לבצע באישה הפריה חוץ גופית ולהחזיר את העוברים לאחר הפריה לרחם של פונדקאית. לסיכום, השפעת תהליך אונקולוגי על פוטנציאל הפריון העתידי של המטופלת הוא מולטיפקטוריאלי ותלוי בעיקר בגיל האישה בעת הטיפול, סוג הטיפול, פרוטוקול הטיפול ומשכו. יש חשיבות רבה לערב את האישה ומשפחתה בדיון מפורט לגבי סיכונים ואפשרויות לשימור פוריותה ורצוי מאוד לפני תחילת הטיפול האונקולוגי. בשנים האחרונות עלתה המודעות בעולם לתחום שימור הפוריות הן בקרב הרופאים ההמטולוגים והאונקולוגים המטפלים בחולים והן בקרב רופאי הפריון. סיכום השיטות השונות הזמינות כיום לשימור פוריות מוצג בטבלה 3. על מנת לקדם את התחום ולעזור למטופלות, יש צורך בשיתוף פעולה הדוק בין קבוצות רופאים בעלי התמחויות שונות. על כן הוקמו קבוצות עניין וארגונים העוסקים בתחום שימור הפוריות.
ביבליוגרפיה
קישורים חיצונייםהוקם ארגון בינלאומי ששם לו למטרה לקדם את התחום, וכן הוקם אתר אינטרנט המכיל את האינפורמציה העדכנית ביותר שנכתבה על ידי מומחים בתחום זה:
המידע שבדף זה נכתב על ידי ד״ר הילה רענני, ד״ר דרור מאירוב, שירות לשימור פוריות, שיבא תל השומר
|
||||||||||||||||||||||||||||||||||


 כניסה
כניסה  עקבו אחרינו בפייסבוק
עקבו אחרינו בפייסבוק