הבדלים בין גרסאות בדף "דיהידרוטסטוסטרון - Dihydrotestosterone"
| שורה 74: | שורה 74: | ||
==היסטוריה של הבנת הקשר בין רמת DHT לתרחישים קליניים== | ==היסטוריה של הבנת הקשר בין רמת DHT לתרחישים קליניים== | ||
בשנת 1942 הבחין James Hamilton שסירוס בגיל שלפני הבשלות המינית מונע בגיל מאוחר יותר את ההתפתחות של התקרחות במתווה זכרי (Hamilton ב-Am J Anatomy משנת 1942). בשנת 1974 פרסמו Imperato-McGinley וחב' ב-Science את הממצא לפיו בקבוצת ילדים באיים הקריביים שנולדו בהגדרה של intersex עם איברי מין שנראו כנקביים, אלא שבגיל הבשלות המינית הופיעו אצלם איברי מין זכריים ומאפיינים גבריים נוספים, נמצאה מוטציה שגרמה לחסר של האנזים 5α-reductase כמו גם לחסר של ההורמון DHT שעל פי סברת חוקרים אלה גרם לאי הסדירות בהתפתחות איברי המין הזכריים. בהמשך נמצא שבאותם מקרים התפתחה בלוטת ערמונית קטנה יותר, ולא הופיעה אצלם התקרחות "זכרית". | בשנת 1942 הבחין James Hamilton שסירוס בגיל שלפני הבשלות המינית מונע בגיל מאוחר יותר את ההתפתחות של התקרחות במתווה זכרי (Hamilton ב-Am J Anatomy משנת 1942). בשנת 1974 פרסמו Imperato-McGinley וחב' ב-Science את הממצא לפיו בקבוצת ילדים באיים הקריביים שנולדו בהגדרה של intersex עם איברי מין שנראו כנקביים, אלא שבגיל הבשלות המינית הופיעו אצלם איברי מין זכריים ומאפיינים גבריים נוספים, נמצאה מוטציה שגרמה לחסר של האנזים 5α-reductase כמו גם לחסר של ההורמון DHT שעל פי סברת חוקרים אלה גרם לאי הסדירות בהתפתחות איברי המין הזכריים. בהמשך נמצא שבאותם מקרים התפתחה בלוטת ערמונית קטנה יותר, ולא הופיעה אצלם התקרחות "זכרית". | ||
| + | |||
נתונים אלה הביאו את Roy Vagelos, ראש יחידת המחקר ב-Merck למחשבה על יצירת תכשיר שימלא את מקומו של DHT וימנע את תופעת BPH במבוגרים. בשנת 1992 אושר התכשיר finasteride 5 mg)) על ידי ה-FDA לטיפול ב-BPH תחת השם Proscar, ובשנת 1997 התקבל אישור ה-FDA ל-finasteride 1mg)) לטיפול בהתקרחות במתווה זכרי תחת השם Alopecia. הניסיון מוכיח שטיפול ב-Alopecia בגברים בלבד מאט את איבוד השיער (Habif ב-Clin Dermatol משנת 2015, ו-Varothai ו-Bergfeld ב-American journal of clinical dermatology משנת 2014). נמצא שיעילות הטיפות היא בתוקף רק כאשר נעשה שימוש בתכשיר. כאשר נבחן Alopecia למניעת איבוד שיער בנשים, יעילותו לא הייתה טובה מטיפול בפלצבו (Levy ו-Emer ב-Int J Women's Health משנת 2013). | נתונים אלה הביאו את Roy Vagelos, ראש יחידת המחקר ב-Merck למחשבה על יצירת תכשיר שימלא את מקומו של DHT וימנע את תופעת BPH במבוגרים. בשנת 1992 אושר התכשיר finasteride 5 mg)) על ידי ה-FDA לטיפול ב-BPH תחת השם Proscar, ובשנת 1997 התקבל אישור ה-FDA ל-finasteride 1mg)) לטיפול בהתקרחות במתווה זכרי תחת השם Alopecia. הניסיון מוכיח שטיפול ב-Alopecia בגברים בלבד מאט את איבוד השיער (Habif ב-Clin Dermatol משנת 2015, ו-Varothai ו-Bergfeld ב-American journal of clinical dermatology משנת 2014). נמצא שיעילות הטיפות היא בתוקף רק כאשר נעשה שימוש בתכשיר. כאשר נבחן Alopecia למניעת איבוד שיער בנשים, יעילותו לא הייתה טובה מטיפול בפלצבו (Levy ו-Emer ב-Int J Women's Health משנת 2013). | ||
==מנגנון הפעולה הקליני של Finasteride== | ==מנגנון הפעולה הקליני של Finasteride== | ||
גרסה מ־11:40, 21 במרץ 2017
| מדריך בדיקות מעבדה | |
| דיהידרוטסטוסטרון | |
|---|---|
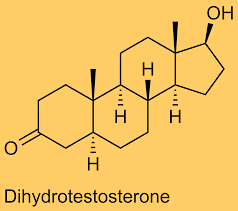
| Dihydrotestosterone | |
| שמות אחרים | DHT, stanolone, androstanolone, 5-α-dihydrotestosterone, allodihydrotestosterone, 5-α-dihydrotestosterone, 5α-androstan-17β-ol-3-ane. |
| |
משקל מולקולארי:290.44 דלטון
| |
| מעבדה | אנדוקרינולוגיה בדם או כימיה בדם |
| תחום | בירור בעיות פוריות ואי-סדירות במערכת הרבייה, וכן בהקשר למפגעי ערמונית והתקרחות אנדרוגנטית |
| טווח ערכים תקין | גברים-דם טבורי-פחות מ-100 פיקוגרם/מיליליטר; גיל עד 6 חודשים-פחות מ-1,200 פיקוגרם/מיליליטר; גיל מעל 6 חודשים ועד תחילת הבשלות המינית (גיל ממוצע של 7.1 שנים או Tanner stage I)-פחות מ-50 פיקוגרם/מיליליטר; (גיל 12.1 שנה או Tanner stage II)-פחות מ-200 פיקוגרם/מיליליטר; גיל 13.6 שנים או Tanner stage III)-בין 80-330 פיקוגרם/פיקוגרם/מיליליטר; גיל 15.1 שנה או Tanner stage IV-בין 220-520 פיקוגרם/מיליליטר; גיל 18 שנה או Tanner stage V- בין 240-650 פיקוגרם/מיליליטר. בגברים מעל גיל 19 שנה רמת DHT היא בתחום בין 112-955 פיקוגרם/מיליליטר. רמת DHT-חופשי בגברים 1.0-6.2 פיקוגרם/מיליליטר.
נשים-דם טבורי-פחות מ-50 פיקוגרם/מיליליטר; גיל עד 6 חודשים-פחות מ-1,200 פיקוגרם/מיליליטר; גיל מעל 6 חודשים ועד תחילת הבשלות המינית (גיל ממוצע של 7.1 שנים או Tanner stage I)-פחות מ-50 פיקוגרם/מיליליטר; גיל 10.5 שנים או Tanner stage II-פחות מ-300 פיקוגרם/מיליליטר; גיל 11.6 שנה או Tanner stage III-פחות מ-300 פיקוגרם/מיליליטר; גיל 12.3 שנה או Tanner stage IV-פחות מ-300 פיקוגרם/מיליליטר; גיל 14.5 שנה או Tanner stage V-פחות מ-300 פיקוגרם/מיליליטר. בנשים בגיל 20-55 שנה-50-460 פיקוגרם/ מיליליטר; בנשים מעל גיל 55 שנה פחות מ-128 פיקוגרם/מיליליטר. רמת DHT-חופשי בנשים 0.3-1.9 פיקוגרם/מיליליטר. |
| יוצר הערך | פרופ' בן-עמי סלע |
מטרת הבדיקה
הערכה של מטופלים הנחשדים לחסר האנזים 5α-reductase. ניטור של מטופלים המקבלים תרפיה עם מעכבי האנזים 5α-reductase או כימותרפיה. אבחון של היפר-אנדרגוניזם (Stanczyk ב-Best Pract Res Clin Endocrinol Metab משנת 2006). קביעת רמת DHT עשויה לסייע בקביעת הגיל בו מתחילה בשלות מינית בעיקר בנערות.
בסיס פיזיולוגי
דיהידרוטסטוסטרון (להלן DHT) הוא סטרואיד-מין אנדרוגני והורמון. האנזים 5α-reductase מקטלז את היצירה של DHT מטסטוסטרון במספר רקמות כולל בלוטת הערמונית, בלוטות הזרע, יותרת האשך (אפידידימיס), עור, זקיקי השיער, כבד ומוח. DHT הוא האנדרוגן הפרוסטתי העיקרי, ורמתו נותרת נורמאלית עם ההזדקנות למרות ירידה ברמת טסטוסטרון בדם. רמות DHT אינן מוגברות במקרים של שגשוג טב של הערמונית (BPH) על פי Pang וחב' ב-J Clin Endocrinol Metabol משנת 1979. רוב ה-DHT בדם קשור בזיקה גדולה ל-sex hormone binding globulin (או SHBG). מדידת DHT-חופשי משקפת את כמות ההורמון הזמין לרקמות היעד.
האנזים 5α-reductase מחזר את הקשר הכפול C4-5 בטבעת A של טסטוסטרון. בערך 5% עד 10%מהטסטוסטרון המיוצר במבוגר מדי יום עוברים תהליך של 5α-reduction ליצירת DHT. תהליך זה מתרחש בעיקר בבלוטת הערמונית ובשחלות, וכן בעור וברקמות אחרות. הסטרואיד DHT במבנהו הוא 5α-androstane המכיל 19 פחמנים, עם שייר ketone בעמדה 3 ושייר הידרוקסיל בעמדה C17β. כמות הטסטוסטרון המותמרת ל-DHT, גדולה בהרבה סביב גיל הבשלות המינית, ומכאן משמעותו הקריטית של DHT בתהליך זה. אכן, כהורמון DHT הוא בעל השפעה חזקה בהרבה מזו של טסטוסטרון.
יחסית לטסטוסטרון DHT הוא הרבה יותר פוטנטי כאגוניסט של הקולטן לאנדרוגן (AR). ל-DHT יש זיקה (Kd) של 0.25-0.5 ננומולר ל-AR באדם, שהיא בערך פי-2-3 גדולה יותר מהזיקה של טסטוסטרון לקולטן זה (0.4-1.0 ננומולר. הזיקה של DHT ל-AR גדולה פי-15-30 מזו של אנדרוגנים אדרנאליים לקולטן זה (Hemat ב-Urotext משנת 2004). קצב הדיסוסיאציה של DHT מהקולטן AR הוא פי-5 אטי יותר מזה של טסטוסטרון (Grino וחב' ב-Endocrinology משנת 1990). לאנזים 5α-reductase יש 2 איזואנזימים: Type I נמצא ברוב הרקמות בגוף והוא מהווה את הצורה הפעילה בבלוטות השומן. לעומתו type II הוא האיזואנזים הדומיננטי ברקמות הרבייה, כולל בלוטת הערמונית.
רמות DHT בגוף נקבעות על ידי הוויסות של יצירת טסטוסטרון, הנקבע על ידי ההיפותלמוס ובלוטת יותרת המוח (היפופיזה). בתגובה לרמות מופחתות של טסטוסטרון מפריש ההיפותלמוס LHRH או luteinizing hormone-releasing hormone, המגיע להיפופיזה ומגרה אותה לייצר ולהפריש LH או luteinizing hormone לזרם הדם. LH נודד בדם לתאי Leydig באשכים (וכן לשחלות בנשים) ומעודד אותם לייצר עוד טסטוסטרון, מה שמגדיל בהתאם גם את רמת DHT. כאשר רמות טסטוסטרון ו-DHT עולות, נוצר משוב שלילי המדכא הפרשת LHRH מההיפותלמוס, ובהתאם גם את הפרשת LH.
ה-EC50 של DHT לשפעול הקולטן AR הוא 0.13 ננומולר, שהוא בערך פי-5 גבוה יותר מה-EC50 של טסטוסטרון שהוא 0.66 ננומולר (Wilderer ב-Newnes משנת 2010). באופן עקבי, מוצאים ב-bioassays ש-DHT הוא פי-2.5-10 יותר פוטנטי מאשר טסטוסטרון. תקופת מחצית החיים של DHT בגוף היא בת 53 דקות, ארוכה משמעותית מזו של טסטוסטרון (34 דקות), מה שעשוי להסביר חלק מההבדל בפוטנטיות שלהם (Diamanti-Kandarakis ב-Current Pharmaceut Design משנת 1999). מחקר בו הושוותה השפעת הזרקה תוך-עורית, העלה תקופות מחצית חיים של DHT וטסטוסטרון שעמדו על 2.83 שעות לעומת 1.29 שעות, בהתאמה (von Deutsch וחב' ב-Handbook Drug Interactios משנת 2003).
DHT וההתפתחות המינית
במהלך ההתפתחות העוברית של הזכר, יש ל-DHT תפקיד חיוני ביצירת איברי המין החיצוניים בזכר, כאשר בגבר המבוגר DHT פועל כאנדרוגן העיקרי בבלוטת הערמונית, בבלוטות הזרע, בעור ובזקיקי השיער (Amory וחב' ב-J Urol משנת 2008). הדגמה למשמעות של DHT בהתפתחות של מאפייני מין משניים, ניתן למצוא במצבי חסר של 5α-reductase type II מוטציה גנטית זו עלולה לגרום ל-pseudohermaphroditism (על פי Imperato-McGinley וחב' ב-N Eng J Med משנת 1979). תרחיש זה מתבטא באופן אופייני עם איברי מין זכריים בלתי-מפותחים, כולל בלוטת הערמונית. בהגיע נערים אלה לגיל הבשלות המינית, רמת DHT נותרת נמוכה ביותר, ואף על פי כן רמות טסטוסטרון עולות באופן נורמאלי, והכוח השרירי שלהם מתפתח בדומה לזה של צעירים בריאים.
אחרי גיל הבשלות המינית, גברים בסטאטוס של pseudohermaphroditism נמצאים בחסר גדול של שעירות הגוף ושיער הבושת, אך אינם סובלים מהתקרחות אנדרוגנית (Marks ב-Rev Urol משנת 2004), וכן הם נהנים מאי הופעה של סרטן הערמונית (Jain וחב' ב-CABI משנת 2006). בניגוד לאנדרוגנים אחרים כגון טסטוסטרון, DHT אינו יכול להיות מותמר לאסטרוגן על ידי האנזים aromatase, כדוגמת estradiol, ולכן אין לו כל משמעות באשר לפעילות אסטרוגנית בגוף. לכן, DHT משמש לעתים קרובות במחקרים על מנת להבדיל בין ההשפעות של טסטוסטרון הנגרמות על ידי הקישור לקולטן AR, לבין אלו הנגרמות על ידי ההמרה של טסטוסטרון לאסטרדיול, מה שיביא בהמשך לקישור ולשפעול של הקולטנים של אסטרוגנים (Swerdloff ו-Wang ב-Bailliere's Clin Endocrinol Metabol משנת 1998).
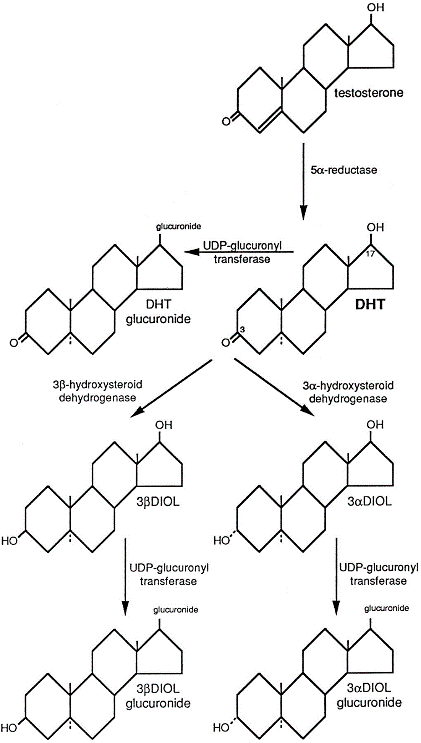
מטבוליזם של DHT
DHT עובר אינאקטיבציה בכבד וכן ברקמות מחוץ לכבד כמו העור, בהפיכתו ל-3α-androstandiol ול-3β-androstandiol על ידי האנזימים 3α-hydroxysteroid dehydrogenase ו-3β-hydroxysteroid dehydrogenase, בהתאמה. שני מטבוליטים אלה מומרים בהתאמה ל-androsterone ול-epiandrosterone, שעוברים בהמשך קוניוגציה דרך גלוקורונידציה וסולפציה, משתחררים לצירקולציה ומופרשים בשתן. רמות DHT בנסיוב מהוות רק כ-10% מאלו של טסטוסטרון, אך רמות DHT בבלוטת הערמונית הן פי-5-10 גבוהות מאלו של טסטוסטרון, שכן בבלוטה זו יש המרה של מעל 90% מהטסטוסטרון ל-DHT על ידי 5α-reductase המתרחשת בתוך הבלוטה. מסיבה זו, וכן בשל העובדה ש-DHT הוא הרבה יותר פוטנטי כאגוניסט של הקולטן AR, נחשב הורמון זה כאנדרוגן העיקרי של הערמונית.
נגזרות של DHT
מספר נגזרי קדם-תרופה (prodrugs) אסטריים של עמדה C17beta במולקולת DHT, פותחו והוכנסו לשימוש תרופתי כסטרואידים אנאבוליים אנדרוגניים (להלן AAS): ניתן להזכיר אחדים מהם כגון androstanolone benzoate, androstanolone valerate, androstanolone enanthate ו-androstanolone propionate (על פי Ian וחב' ב-John Wiley & Sons משנת 2009). נגזרות סינתטיות של DHT המשמשות כ-AAS כוללות את mesterolone שמבנהו 1alfa-methyl-DHT, וכן drostanolone שמבנהו 2alfa-methyl-DHT, כמו גם metenolone בעל מבנה 1beta-methyl-lamda1-DHT, ו-stenbolone שמבנהו 2-methyl-lamda1-DHT, ו-epitiostalol שמבנהו 2alfa,3alfa-epithio-3-deketo-DHT, וכן mepitiostane שהוא prodrug עם שייר אתרי בעמדה 17 של epitiostanol. נגזרים נוספים הם dihydroboldenone או Δ1-DHT, ו-mesabolone שהוא prodrug עם שייר אתרי בעמדה 17 של dihydroboldenone, ולפחות עוד 15 נגזרות נוספות.
הפורמולציות השונות של DHT כוללות טבליות למציצה בוקאלית או תת-לשונית (Anabolex ו-Stanolone), ג'ל למריחה מקומית (Ophtovital, Gelovit ו-Andractim), ואסטרים מומסים בשמן המוזרקים לשריר דוגמת dihydrotestosterone propionate (שם מותג Pesomax) ו-dihydrotestosterone valerate (שם מותג Apeton). אסטרים של DHT פועלים בגוף כ-prodrugs שלו ויש להם זמן תגובה ארוך. גם Dihydrotestosterone benzoate (שמות מותג Sarcosan, Hermalone ו-Ermalone-Amp), וכן dihydrotestosterone enenthate (שם מותג Anaboleen-Depot), הם אסטרים של DHT הזמינים לשימוש קליני.
מאפיינים של 2 האיזואנזימים של DHT
| איזואנזים type 1 | איזואנזים type 2 | |
|---|---|---|
| מקודד בכרומוזום | 5 | 2 |
| מצוי בבלוטת הערמונית | כן | כן |
| אופטימום pH לפעילות | ניטרלי עד בסיסי | חומצי |
| עיכוב ע"י finasteride | לא (Ki>300 nmol/L) | כן (Ki=5nmol/L) |
| עיכוב ע"י dutasteride | כן | כן |
| ביטוי mRNA גדל ב-BPH | כן | כן |
על פי McConnell ב-Isis Med Media Ltd משנת 1996, ו-Bartsch וחב' ב-Eur Urol משנת 2000.
היבטים פתולוגיים של DHT
DHT מיוצר באופן מקומי בזקיקי השיער על ידי 5α-reductase ולא מסופק על ידי DHT סיסטמי, הוא הגורם העיקרי להתקרחות (alopecia) אנדרוגנית, למרות שהמנגנון לתרחיש זה אינו מובהר לחלוטין (Nordqvist ב-Med News Today משנת 2012). במקרים של התקרחות אנדרוגנית בנשים המצב מורכב יותר, כאשר DHT הוא רק אחד ממספר גורמים מעורבים (McAnrews ב-Amer Hair Loss Assoc). נשים עם רמות מוגברות של DHT, עלולות לפתח תסמינים של היפר-אנדרוגניות, כגון שריריות בולטת, קול עמוק יותר ואף שעירות בפנים. בגברים, צמיחת בלוטת הערמונית ותהליכי התמיינות בבלוטה זו מושפעים מאוד מ-DHT, והורמון זה משחק תפקיד הן ב-BPH כמו גם בסרטן הבלוטה (Freedland וחב' ב-J Clin Oncol משנת 2005).
היסטוריה של הבנת הקשר בין רמת DHT לתרחישים קליניים
בשנת 1942 הבחין James Hamilton שסירוס בגיל שלפני הבשלות המינית מונע בגיל מאוחר יותר את ההתפתחות של התקרחות במתווה זכרי (Hamilton ב-Am J Anatomy משנת 1942). בשנת 1974 פרסמו Imperato-McGinley וחב' ב-Science את הממצא לפיו בקבוצת ילדים באיים הקריביים שנולדו בהגדרה של intersex עם איברי מין שנראו כנקביים, אלא שבגיל הבשלות המינית הופיעו אצלם איברי מין זכריים ומאפיינים גבריים נוספים, נמצאה מוטציה שגרמה לחסר של האנזים 5α-reductase כמו גם לחסר של ההורמון DHT שעל פי סברת חוקרים אלה גרם לאי הסדירות בהתפתחות איברי המין הזכריים. בהמשך נמצא שבאותם מקרים התפתחה בלוטת ערמונית קטנה יותר, ולא הופיעה אצלם התקרחות "זכרית".
נתונים אלה הביאו את Roy Vagelos, ראש יחידת המחקר ב-Merck למחשבה על יצירת תכשיר שימלא את מקומו של DHT וימנע את תופעת BPH במבוגרים. בשנת 1992 אושר התכשיר finasteride 5 mg)) על ידי ה-FDA לטיפול ב-BPH תחת השם Proscar, ובשנת 1997 התקבל אישור ה-FDA ל-finasteride 1mg)) לטיפול בהתקרחות במתווה זכרי תחת השם Alopecia. הניסיון מוכיח שטיפול ב-Alopecia בגברים בלבד מאט את איבוד השיער (Habif ב-Clin Dermatol משנת 2015, ו-Varothai ו-Bergfeld ב-American journal of clinical dermatology משנת 2014). נמצא שיעילות הטיפות היא בתוקף רק כאשר נעשה שימוש בתכשיר. כאשר נבחן Alopecia למניעת איבוד שיער בנשים, יעילותו לא הייתה טובה מטיפול בפלצבו (Levy ו-Emer ב-Int J Women's Health משנת 2013).


 כניסה
כניסה  עקבו אחרינו בפייסבוק
עקבו אחרינו בפייסבוק