הבדלים בין גרסאות בדף "תסמונת הכאב האזורית המורכבת - Complex regional pain syndrome"
| (159 גרסאות ביניים של 5 משתמשים אינן מוצגות) | |||
| שורה 1: | שורה 1: | ||
| − | |||
| − | |||
{{מחלה | {{מחלה | ||
| − | |תמונה= | + | |תמונה=[[קובץ:Complex regional pain syndrome.jpg|250px]] |
|כיתוב תמונה= | |כיתוב תמונה= | ||
|שם עברי= תסמונת הכאב האזורית המורכבת | |שם עברי= תסמונת הכאב האזורית המורכבת | ||
|שם לועזי= Complex regional pain syndrome | |שם לועזי= Complex regional pain syndrome | ||
| − | |שמות נוספים= | + | |שמות נוספים = Reflex sympathetic dystrophy |
|ICD-10= | |ICD-10= | ||
|ICD-9= | |ICD-9= | ||
|MeSH= | |MeSH= | ||
| − | |יוצר הערך= ד"ר סילביו בריל, ד"ר איתי גור-אריה {{ש}}[[קובץ:TopLogoR.jpg|80px]] | + | |יוצר הערך= [[משתמש:סילביו בריל|ד"ר סילביו בריל]], ד"ר איתי גור-אריה {{ש}}[[קובץ:TopLogoR.jpg|80px]] |
|אחראי הערך= | |אחראי הערך= | ||
}} | }} | ||
| − | {{הרחבה|כאב}} | + | {{הרחבה|כאב}} |
| − | + | '''תסמונת הכאב האזורית המורכבת''' (Complex Regional Pain Syndrome, CRPS) מוכרת מימי מלחמת האזרחים האמריקאית, עת נקראה קוזלגיה (Causalgia), שם שנבחר כדי לתאר שריפה וכאבים לאחר פציעה. מאז, שם התסמונת שונה מספר פעמים. Bonica טבע את המונח החזר סימפתטי דיסטרופי (Reflex Sympathetic Dystrophy, RSD) ב-1953. קבוצת מומחים קבעה את שינוי השם ב-1993 לתסמונת כאב אזורי מורכב. עם זאת רבים מהרופאים עדיין נוהגים להשתמש במונח החזר סימפתטי דיסטרופי. תסמונת הכאב האזורית המורכבת מאופיינת באירועי כאב מתפרץ בעצמה רבה, השונים באופיים מכאבים בעלי אופי קבוע. [[כאב נוירופתי]], נויראלגיה (נוירו=עצב, אלגיה=כאב), מהווה את אחת מבעיות הכאב הקשות שאיתן מתמודדת הרפואה בכלל, ורפואת הכאב בפרט. בין הגורמים לתסמונת הכאב האזורית המורכבת ניתן למנות מחלות [[סרטן]], [[טיפולים כימותרפיים]] ו[[הקרנות]], מחלות זיהומיות, מחלות של חילוף חומרים, חומרים רעילים, ניתוחים וכן פגיעות בשל חבלה או תאונות. הטיפול בתסמונת הוא ארוך טווח ומותאם לחולה, ומורכב מטיפול תרופתי, טיפולים גופניים ונפשיים, ולעתים כולל גם התערבות ניתוחית. | |
| − | הכאב | + | |
| + | == אפידמיולוגיה == | ||
| − | + | שכיחות תסמונת הכאב האזורית המורכבת עשויה להגיע לכדי 5%-7% מן האוכלוסייה הבוגרת. התסמונת מתפרצת בעיקר במבוגרים צעירים, מעט יותר בנשים. | |
| − | תסמונת הכאב | + | == אטיולוגיה == |
| − | + | תסמונת הכאב האזורית המורכבת יכולה להיגרם על-ידי מספר מצבי מחלה: | |
| + | * מחלות סרטן עשויות לגרום לפגיעה עצבית דרך מסת הגידול הלוחצת או חודרת לעצבים ולמוח, ואף דרך הטיפול במחלה על-ידי הקרנות וכימותרפיה, שיש ביכולתן לפגוע בעצב | ||
| + | * מחלות זיהומיות, כגון [[שלבקת חוגרת]] הרפטית (Herpes Zoster, Shingles) יכולות לפגוע בתאי העצב ולהורגם | ||
| + | * מחלות של חילוף חומרים, כגון [[סוכרת]] שגורמת לפגיעה בכלי הדם הקטנים המספקים דם לעצבים, ומשנית לכך נגרם מוות של תאי עצב | ||
| + | * חומרים רעילים, כגון [[הרעלת עופרת|עופרת]], אך גם [[אלכוהול]], גורמים לנזקים שונים ביניהם גם הרס של עצבי תחושה וכאב | ||
| + | * בנוסף, קיים כאב עצבי לאחר ניתוחים (ובמיוחד ניתוחי דופן בית החזה), וכן פגיעה בשל חבלה או תאונות או לאחר ניתוחים אחרים | ||
| + | לא נמצא קשר בין עוצמת התסמונת, מרגע שהתפתחה, לבין הגירוי הראשוני. עם זאת, קיימים גירויים מועדים, כגון [[שבר במפרק כף יד]] ו[[פגיעות מרפק|מרפק]], וכן אירועים כניתוחים של גידולים סרטניים ו[[התקף לב]], היכולים להוביל להתפתחות המחלה. | ||
| − | + | ייתכן ולגורמים גנטיים השפעה על הופעת תסמונת הכאב האזורית המורכבת. התסמונת שכיחה יותר בקרב חולים בעלי האללים HLA-A3 ,B7 ,DR2. נראה כי לשונות גנטית השפעה גם על התגובה לטיפול, שכן, לפי אחד המחקרים, חולים שהם בעלי הגנוטיפ HLA-DR2 היו עמידים יותר לטיפולים תרופתיים. | |
| − | |||
| − | + | ההיבט הנפשי כנראה שותף אף הוא להתפתחות התסמונת. 80% מהחולים שפיתחו את המחלה, סבלו מלחץ נפשי בחודשיים שקדמו להופעתה ובחודש לאחר שהתפתחה. עם זאת, יש לציין שלא נמצא מבנה נפשי משותף הקשור לתסמונת הכאב האזורית המורכבת. | |
| + | ;מנגנונים להתפתחות כאב עצבי | ||
| − | + | למרות שהתסמונת מוכרת כבר כמאה וחמישים שנים, עדיין אין מנגנון ברור המסביר את התסמונת. מספר מנגנונים אחראים להתפתחות הכאב העצבי. כל [[כאב כרוני]] מתאפיין בהתעצמות של הכאב לאורך זמן, וזאת בשל התפתחות של רגישות יתר לכאב. מצב הרגישות יתר מתפתח לאורכה של מערכת העצבים, וכל גירוי כאב מתמשך גורם לשינויים באזור קולטני הכאב ברקמה הפגועה, בגופי התא העצבי, בחוט השדרה ובמרכזי הכאב במוח. באופן תקין, לגוף יש מנגנוני תיקון ודיכוי שמעלימים את השינויים, אחרת, היה הגוף מוסיף לסבול מכל כאב שנחווה במהלך החיים. בפגיעות עצביות המנגנונים משמעותיים הרבה יותר והשינויים נמשכים לאורך זמן. מאחר שמערכת העצבים האחראית על ההעצמה של הכאב והפסקתו בהמשך, היא הנפגעת בתסמונת, התיקון קשה יותר ולפעמים כלל לא מתאפשר. | |
| − | + | מבחינה מכנית, ניתן לדמות את מערכת העצבים למערכת של חוטי טלפון מבודדים, הנעים יחדיו בצברים בתוך צינורות, אשר מוליכים אותם מהמוח לרקמות ומהרקמות חזרה אל המוח. בזמן פגיעה בעצב, יכולים להיווצר מספר מצבים שבהם יש הרס מוחלט או חלקי של כל אחד מחלקי המערכת. רקמת עצב יכולה לגדול שוב גם אם השלוחות והרקמות סביבה נפגעו, בתנאי שגוף תא העצב לא נפגע. קצב הגדילה של עצב עומד על כ-1-2 מ"מ ליממה, והגידול מחדש יכול, לכן, לקחת זמן רב. למשל, פגיעה בעצב באזור הישבן יכולה להתרפא במשך שלוש שנים, ולאפשר לשלוחות העצב לגדול חזרה לכף הרגל. הגדילה מחדש של עצב היא חלק מההחלמה, אך לעתים היא גם חלק מהבעיה. שלוחות העצב (Axons) הגדלות מחדש, לא תמיד גדלות בצורה סדירה. לחלק מן השלוחות אין רקמות בידוד, והן יוצרות מעין קצר עם שלוחות אחרות שאינן מבודדות. שלוחות אלה יכולות לגרום לכך שתחושה שאינה כאב, תעבור למסלול של כאב או להיפך. כאשר רקמות החיבור המובילות את שלוחות העצב נהרסות, השלוחות שגדלות מחדש ממשיכות לגדול ללא אבחנה, ויוצרות מבנה כדורי הנקרא [[נוירומה]], (Neuroma) הרגיש לכל מגע ולעתים מופעל באופן עצמוני וגורם לכאב עז. | |
| + | |||
| + | השינויים במערכת העצבית אינם מבניים בלבד, אלא מקורם בשינויים כימיים המתרחשים על מעטפות התאים ובגופי התא. השינויים הללו גורמים לתאים לפתח גריות יתר (Hyperexcitability) של העצב. משמעות הדבר היא כי גירוי שבדרך כלל לא היה מועבר דרך העצב, עתה יכול להיות מועבר וביתר עצמה. תעלות נתרן-סידן ותעלות אחרות ממלאות תפקיד מרכזי בהתהוותה של גריות היתר ההיקפית. המנגנונים חשובים להבנה של דרך פעילותן של תרופות הפועלות נגד כאב עצבי. נוסף על כך, מתפתחת גריות יתר של תאי עצב תחושתיים בחוט השדרה, וייתכן שגם באתרים גבוהים יותר במערכת העצבים המרכזית. שינויים אלו מושרים על ידי החומצה האמינית גלוטמאט (Glutamate) וכנראה שגם על-ידי חומרים אחרים. | ||
| − | + | [[קובץ: Regional_pain08.jpg|מרכז|400px]] | |
| − | + | מנגנון חשוב נוסף הנפגע בזמן פגיעה עצבית הוא המערכות המדכאות הולכה במערכת העצבית. באופן תקין, ישנם מסלולים עצביים במוח ומסלולים עצביים היורדים מהמוח אל חוט השדרה, אשר תפקידם לדכא את ההולכה של גירויים מהרקמות לכיוון המוח. דיכוי זה מונע מצב של גירויים בלתי פוסקים, כדוגמת תחושה של מגע הבגד על גופינו. בפגיעה עצבית יש ירידה בפעילותן של מערכות אלו, שחלקן מדכא הולכת כאב. מקצתן של התרופות מנסות לטפל דרך התערבות במנגנונים אלה, אף על פי שהמנגנונים טרם הובהרו די צורכם. | |
| − | + | מנגנון נוסף של תסמונת הכאב האזורית המורכבת קשור במערכת האוטונומית, בעיקר הסימפתטית, וזאת למרות שברוב המקרים, תרומתה לתסמונת ככל הנראה מוגבלת. על פי המנגנון המוצע, המערכת הסימפתטית מגיבה לפגיעה בפעילות יתר. תגובה זו לכאורה גורמת לעלייה בחום הגפה בשלב הראשון, המשולבת עם גידול מהיר של השיער והציפורניים - השלב של גדילת היתר (Hypertrophic). לאחר מכן, מתרחשת ירידת חום בגפה הפגועה, כלי הדם מתכווצים, והעור, השיעור והציפורנים עוברים ניוון - שלב הדלדול (Atrophic). אולם, ברוב המקרים אין כנראה עלייה בפעילות מערכת העצבים האוטונומית, ולכן ההגדרות החדשות שבשימוש הן תיאוריות ולא מנגנוניות. עם זאת, חלק מהמקרים אכן מבוססים על פגיעה אוטונומית תפקודית. פגיעה זאת נקראת SMP {{כ}} (Sympathetically Maintained Pain). | |
| − | + | ||
| − | + | [[קובץ: Regional_pain09.jpg|מרכז|400px]] | |
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | [[קובץ: | + | [[קובץ: Regional_pain10.jpg|מרכז|400px]] |
| − | + | ;תסמונת הכאב האזורית המורכבת חולקה לשני סוגים: | |
| + | #סוג 1, שבו הפגיעה היא כמתואר (90% ממקרים שייכים לסוג זה). | ||
| + | #סוג 2, שמלווה בפגיעה עצבית ברורה כמקור להתפתחות התסמונת. | ||
| − | + | == קליניקה == | |
| − | + | תסמונת הכאב האזורית המורכבת מאופיינת בכאבים אזוריים המלווים בדרך-כלל בשינויי צבע, הפרעות בהזעה, וחום ורגישות העור בגפה המעורבת. הכאבים מתוארים על פי רוב כ"שורפים", ולעתים אף מלווים בנפיחות מקומית או כללית של הגפה. הכאב בתסמונת חריג בעצמתו וללא יחס תואם לעוצמת הפגיעה שגרמה לו, והוא יכול להביא לחוסר תנועה של הגפה הפגועה. יכולות להופיע [[הפרעות תנועה]] שאינן קשורות לכאב, כגון התכווצויות, רעד וחוסר יכולת לתנועה מתואמת. מלבד עוצמת הכאב הגבוהה, תסמונת הכאב האזורית המורכבת מאופיינת בתגובת כאב לגירוי שבדרך כלל אינו מכאיב (Allodynia) וסף רגישות נמוך לכאב (Hyperalgesia). | |
| + | השלבים המתקדמים של המחלה יכולים להגיע עד שברים בעצמות עקב ניוון שלהן, התפתחות כיבים עקב חוסר תנועה ולחץ לא אחיד וקיצור שרירים, המובילים לשיתוק תפקודי. | ||
| + | תסמונת הכאב האזורית המורכבת יכולה להתפשט. ההתפשטות היא לרוב לאורך הגפה הפגועה, אם כי קיימים מקרים בהם הכאב קופץ לגפה השנייה המקבילה (ימין-שמאל) או לגפה השנייה באותו הצד (עליונה-תחתונה). | ||
| + | לאחר התפתחות התסמונת יש תסמינים נפשיים משניים לכאב, כגון פחד, [[חרדה]], כעס ו[[דיכאון]]. | ||
| + | [[קובץ: Regional_pain06.jpg|מרכז|400px]] | ||
| + | [[קובץ: Regional_pain07.jpg|מרכז|400px]] | ||
| + | [[קובץ: Regional_pain11.jpg|מרכז|400px]] | ||
| + | [[קובץ: Regional_pain12.jpg|מרכז|400px]] | ||
| − | + | == אבחנה == | |
| + | לאחר נטילת העבר הרפואי הקשור למחלה ובדיקה גופנית, קיימים מבחנים העוזרים להגיע לאבחנה. | ||
| + | * חסמים עצביים של המערכת הסימפתטית או של העצב החשוד כפגוע (בתסמונת הכאב האזורית המורכבת מסוג 2), וזאת על ידי הזרקות או עירויי [[Regitine]] {{כ}} (Phentolamine). | ||
| + | * בדיקות כגון [[אלקטרומיוגרפיה]] (Electromyography, EMG) ובדיקות של [[בדיקת הולכה עצבית|הולכה תחושתית]], היכולות לסייע באבחנה ובזיהוי רמת הפגיעה העצבית. | ||
| + | * [[הדמאה תרמית]] (Thermography) ובדיקת [[על-קול דופלר]] (Doppler ultrasound) משמשות לזיהוי הפגיעה בכלי הדם. | ||
| + | * צילומי [[רנטגן]] ו[[מיפוי עצמות]] עשויים להראות סימני ניוון אופייניים בעצמות, אך הם אינם נחשבים לחד-משמעיים בביסוס האבחנה. | ||
| − | + | נכון למועד כתיבת מאמר זה אין בדיקת עזר אשר יכולה לאשר או לשלול באופן מוחלט את קיום תסמונת הכאב האזורי המורכב. | |
| − | + | האגודה הבין-לאומית לחקר הכאב (International Association for the Study of Pain, IASP) קבעה את המדדים לאבחון של תסמונת כאב אזורי מורכב: | |
| − | + | * התסמין הראשון הוא עבר של פגיעה באיבר שפיתח את התסמונת, דוגמת מכה, נקע או שבר. עוצמת הפגיעה יכולה להיות קלה ביותר ולא קשורה לחומרת התסמונת. | |
| − | + | * התפתחות כאב באזור הפגיעה המאופיין בכאב בעצמה גבוהה, כאב המושרה על ידי גירוי שאינו מכאיב, וסף רגישות נמוך לכאב. הכאב הוא על פי רוב דמוי גרב או כפפה ואינו מתפזר לאורך מסלול עצבי ברור. | |
| + | * עדות לנפיחות בגפה הפגועה ועדות לפגיעה בתפקוד כלי הדם, כמו חום או קור של הגפה. | ||
| + | * שלילה של מחלות אחרות. | ||
| + | * סימנים של שינויים ברקמות, כמו ירידה במסת שריר, שינויים ניווניים בעור, גידול מהיר של שיער וציפורניים, מחזקים את האבחנה. | ||
| − | + | == טיפול == | |
| − | + | הטיפול בתסמונת הכאב האזורית המורכבת כולל מספר שיטות וגישות: תרופות, הזרקות וחסמים עצביים, [[פיזיותרפיה]] משמעותית ותמיכה נפשית. פעמים רבות יש לערב את מחלקות השיקום המתמחות בנושא. הטיפול מתבצע במספר שלבים שנכונים עבור כל טיפול: התחלה בטיפול שמידת הסיכון בו נמוכה, ועליה במידת הפולשניות במידת הצורך. הטיפול מתחיל בטיפול תרופתי, עובר להזרקות ולבסוף מגיע לניתוק עצבים ולהשתלת מוליכים חשמליים. | |
| − | + | בחירת הטיפול התרופתי ההתחלתי מתבססת על מספר גורמים: יעילות מוצעת ממחקרים וניסיון קודם לעומת מידת תופעות הלוואי הצפויות. פן נוסף הוא מידת החריפות של הבעיה, וכן חולה עם כאב עצבי חדש יטופל ביתר תוקפנות. בבחירת הטיפול התרופתי יש העדפה לתרופה אחת בלבד לטיפול בכאב, אך במקרים של כאב קשה לטיפול נישקל השימוש בשילוב של תרופות. לרוב קיימת העדפה לתרופות הניתנות דרך הפה, לעומת מתן תוך-ורידי. | |
| − | + | הטיפול התרופתי מבוסס על שימוש בתרופות לכאב עצבי, למשל: [[Lyrica]]{{כ}} (Pregabalin){{כ}}, [[Neurontin]]{{כ}} (Gabapentin){{כ}}, [[Duloxetine]]{{כ}}, {{כ}}[[Carbamazepine]]{{כ}}, ו-[[Anastrozole]]{{כ}}. קיימות גם תרופות ממשפחות אחרות, ובכלל זה תרופות החוסמות קולטנים אדרנרגיים, כגון: [[Clonidine]], וכן תרופות המונעות ספיגת עצם ממשפחת ה[[ביספוספונטים]] (Biphosphonates). כמו כן, קיימים דיווחים אודות יעילותן של תרופות במתן תוך-ורידי, אך חלק גדול מהן לא קיים בישראל. התרופות התוך-ורידיות יכולות לשפר את אספקת הדם לרקמות על-ידי הורדת פעילותה של המערכת הסימפתטית, והורדה של הכאב העצבי. העירויים המקובלים לטיפול הם של [[Lidocaine]], [[מגנזיום]], [[Phentolamine]]{{כ}}, [[Ketamine]] ו-[[Bretylium]]. | |
| − | |||
| − | |||
| − | + | חסמים עצביים וורידיים סימפתטיים כוללים את [[Dibenyline]] {{כ}}(Phenoxybenzamine), {{כ}}[[Prazosin]]{{כ}}, [[Doxazosin]]{{כ}} ו-[[Terazosin]], והם נמצאו יעילים בחסימה בררנית של קולטנים על כלי הדם, המכירים חומרים המופרשים על-ידי המערכת הסימפתטית. כתוצאה מהחסימה, חלה הרחבה של כלי הדם בגפה הפגועה, שיפור בזרימת הדם ושיכוך הכאב. ניתן להשתמש בחסמים של המערכת העצבית הסימפתטית בגובה הצוואר [חסם של גנגליון דמוי כוכב (Stellate ganglion)], אשר חוסמים את העצבוב לכיוון הגפה העליונה, וכן בחסמים של השרשרת העצבית הסימפתטית בגב התחתון, אשר מספקת את הרגל, וזאת כדי לסייע באבחנה ובטיפול בתסמונת. | |
| − | [[ | + | במקרים של תסמונת הכאב האזורית המורכבת מסוג 2 יש מקום גם לחסמים עצביים באזור העצב הפגוע, ואף לניסיון להזריק [[סטרואידים]] למקום. השימוש בפעולות פולשניות, כגון [[השתלת מוליכים חשמליים אפידורליים]] (Epidural electrodes) ו[[השתלת משאבות לעמוד השדרה|השתלת משאבות]] נמצא יעיל, אך נשמר לשלבים מאוחרים בטיפול עם הרס מכוון של שרשראות העצבים האוטונומיות. |
| − | + | שלוש קבוצות של תרופות מהוות את אבני היסוד בטיפול בכאב העצבי בכלל ובתסמונת כאב אזורי מורכב בפרט, והן תרופות [[נוגדות דיכאון]], [[נוגדות כפיון]] ו[[אופיואידים]]. | |
| − | + | === תרופות נוגדות דיכאון === | |
| − | |||
| − | + | מנגנון פעולתן המשוער של קבוצת התרופות נוגדות הדיכאון הוא הפעלת מערכות שיכוך כאב מוחיות וחיזוק פעולתם של המסלולים היורדים מהמוח לכיוון חוט השדרה, ודיכוי הולכה במסלולי כאב לכיוון המוח. הדבר נעשה באמצעות מניעת ספיגה חוזרת של סרוטונין ונוראדרנלין במצמדים מוחיים (Synapse, נקודות הקשר בין עצבים). ייתכן, כי לתרופה מנגנון שיכוך כאב נוסף באמצעות ייצוב מעטפות תא עצביות. השפעתן של התרופות נגד דיכאון על הכאב היא ישירה, ואינה תלויה בהשפעתן על דיכאון. לרוב השפעתן על הכאב היא במינונים נמוכים מהמינונים הנדרשים לטיפול בדיכאון, ומהירה יותר. | |
| + | חשוב לומר למטופל כי התרופה שבה הוא מטופל משמשת גם לטיפול בדיכאון, שכן אם ילמד על כך ממקורות אחרים, הוא עשוי לחשוב כי הרופאים אינם מאמינים לכאביו וחושבים שהם נפשיים, ובהמשך לכך יסרב ליטול את התרופה או להמשיך בטיפול. | ||
| − | + | פן הדיכאון עצמו הוא פן חשוב בכאב. כאב כרוני מוביל לדיכאון בחלק גדול מהמקרים ובמיוחד בקרב הסובלים מכאב עצבי, לכן יש תועלת כפולה בשימוש בתרופות נוגדות דיכאון לכאב. | |
| − | + | ;קבוצת התרופות נוגדות הדיכאון כוללת מספר תת-קבוצות: | |
| + | #הקבוצה הוותיקה של [[נוגדי דיכאון טריציקליים]] (Tricyclic Antidepressants, TCAs) נחקרה רבות ונמצאה יעילה בהפחתת סוגי כאב עצבי רבים ללא קשר להשפעתה על דיכאון. התרופות מתת-קבוצה זאת אינן בררניות ומשפיעות על חומרים מוחיים נוספים, ולכן תופעות הלוואי שלהן נרחבות יותר. [[Elatrol]]{{כ}} (Amitriptyline) היא נציגה של הקבוצה. התרופה ניתנת במינון התחלתי של 10-25 מ"ג. העלאת המינון חייבת להיות הדרגתית כדי להפחית תופעות לוואי. חלק מן המטופלים מדווחים על הקלת כאב במינוני ביניים (50-75 מ"ג), אם כי לעתים יש צורך להגיע ל-100-150 מ"ג ליממה ואף יותר במנה אחת בערב. הסיבה לכך היא שהתרופה גורמת ל[[ישנוניות]], וכך תופעת הלוואי מסייעת למטופל להירדם. קיימות תופעות לוואי רבות נוספות, הכוללות תופעות של [[יובש בפה]], [[עצירות]], ישנוניות יתר, [[סחרחורת]] ועוד. יש להימנע משימוש בתרופה אצל חולים הסובלים מ[[ברקית]] עם זווית חדה (Narrow angle glaucoma), [[הגדלת הערמונית]] (Prostatic hyperplasia), [[הפרעות במערכת ההולכה בלב]] ולאחר [[אוטם בשריר הלב]]. תרופות נוספות מקבוצה זאת הן [[Deprexan]] (Desipramine), וכן [[Clomipramine]]. | ||
| + | #[[מעכבי ספיגה חוזרת של סרוטונין ונוראפינפרין]]{{כ}} (Serotonin and Norepinephrin Reuptake Inhibitor, SNRI) היא תת-הקבוצה השניה והעדכנית של תרופות נוגדות דיכאון שנמצאה יעילה לטיפול בכאב עצבי. תרופות ממשפחה זו חוסמות את ספיגת נוראדרנלין וסרוטונין באופן בררני. מאחר שהחסימה בררנית יותר בהשוואה לפעולת נוגדי הדיכאון טריציקליים, תופעות הלוואי שלה פחותות. [[Duloxetine]] נרשמה בארץ ואף הוכנסה לסל התרופות לאחר שנמצאה לה יעילות גבוהה בהפחתת כאב ממקור [[נוירופתיה סוכרתית]], ירידה ב-50% ברמת הכאב ב-50% מהמטופלים. ניתן להתחיל טיפול במינון של 30 מ"ג לשבוע, ואז להעלות את המינון ל-60 מ"ג ליום במנה אחת בערב. תופעות הלוואי העיקריות שנצפו היו [[בחילה]], נמנום וסחרחורת, שחלפו לרוב עם הזמן. רוב תופעות הלוואי היו בדרגת חומרה קלה עד בינונית, נצפו בדרך כלל בתחילת הטיפול, וחלפו עם המשך הטיפול. נציגה נוספת ממשפחה זו היא ה-[[Venlafaxine]], אם כי לגביה ההוכחות ליעילות נמוכות יותר, והיא אינה רשומה לאבחנה של טיפול בכאב עצבי בישראל. | ||
| + | #[[מעכבי ספיגה חוזרת של סרוטונין]] {{כ}} (Selective Serotonin Reuptake Inhibitor, SSRI) תת-הקבוצה השלישית פועלת באופן בררני להעלאת מינון הסרוטונין במוח. תרופות אלה בטוחות יותר בשימוש בהשוואה לנוגדי הדיכאון הטריציקליים, אולם יעילותן כמשככי כאב עצבי ירודה בהתאם. מבין תרופות אלה ניתi לציין את ה-[[Paroxetine]] הניתנת במנה אחת בת 20-40 מ"ג מאחר שנמצאה יעילה בהפחתת כאב ממקור נוירופתיה סוכרתית במחקר בודד. נראה כי ההשפעה שלה על הכאב נובעת בעיקר מהשפעתה על הדיכאון הנלווה. | ||
| − | + | === תרופות נוגדות כפיון (Epilepsy) === | |
| + | ::השימוש בתרופות נוגדות [[כפיון]] לטיפול בכאב עצבי נראה מעט תמוה בתחילה, אך כאשר בוחנים את מנגנוני הפעולה של התרופות נוגדות הכפיון מחד, ומאידך את השינויים ומנגנוני הנזק בכאב עצבי, ניתן למצוא התאמה. התרופות פועלות על מנגנונים המונעים את ההתפרצויות העצמוניות של הכאב, ומעלות את סף ההפעלה של העצבים הפגועים. התרופות נוגדות הכפיון אינן יוצרות [[התרגלות]] או [[התמכרות]], הן בטוחות יחסית לשימוש, ותופעות הלוואי שלהן לרוב סבילות. התרופות ברובן בשימוש שנים רבות לטיפול בכפיון. | ||
| + | ::גם ביחס לתרופות נוגדות כפיון, יש לידע את החולה כי הוא מקבל תרופות מקבוצה זו, וכי אין סכנה שיפתח כפיון בשל כך. | ||
| + | ::'''בתוך נוגדי הכפיון יש מספר תת-משפחות הנבדלות במנגנונים אשר עליהן הן פועלות''' | ||
| + | ::* [[t:ליריקה - Lyrica|Lyrica]] היא תרופה חדשה אשר נבדקה ונמצאה יעילה ובטוחה במספר גדול של חולים עם כאב ממקור נוירופתיה סוכרתית או [[נוירלגיה בתר הרפטית]] (Post herpetic neuralgia). המינון הוא 300-600 מ"ג ליממה בשתי מנות מחולקות. יתרונה בהתאמת המינון המהיר המתבצעת תוך פרק זמן קצר (3-6 יממות). התרופה פועלת דרך חסימה של תעלות סידן מיוחדות המופיעות על גופי תאי העצב הפגועים. התרופה נקשרת ביעילות גבוהה פי 6 מאשר [[t:נאורונטין - Neurontin|Neurontin]] לתעלות הסידן, ולכן יותר בררנית וייתכן שאף בעלת תופעות לוואי פחותות. התרופה מופיעה במינונים של 25, 50, 75, 150 ו-300 מ"ג. עיקר תופעות הלוואי הן סחרחורת, עייפות, טשטוש ו[[בצקות]] היקפיות. זוהי התרופה היחידה הרשומה בישראל לכל סוגי הכאב העצבי ההיקפי ולאחרונה גם לכאב עצבי מרכזי. לאחרונה נכנסה לסל הבריאות. | ||
| + | ::* [[Neurontin]] הפועלת במנגנון זהה ל-Lyrica, נמצאה יעילה בשיכוך כאב עצבי מסוגים שונים במספר רב של מחקרים. בישראל רשומה רק לטיפול בכאב עצבי בתר-הרפטי וסוכרתי. מינון התרופה הוא בין 900 ל-3,600 מ"ג ליממה בשלוש מנות מחולקות. הקינטיקה של התרופה אינה קווית כך שלעתים שיכוך הכאב נראה רק במינוני תרופה גבוהים. העלאת המינון מתבצעת תוך ימים עד שבועות. תופעות הלוואי דומות לאלה של Lyrica. | ||
| + | ::* [[Carbamazepine]] יעילה במיוחד להפחתת התקפי [[תסמונת העצב המשולש]] (Trigeminal neuralgia), וייתכן שגם בכאבים עצביים נוספים. המינון התחלתי הינו 100 מ"ג פעמיים ביום, ויש לעלות במינון בהדרגה בשל ריבוי תופעות הלוואי. המינון המומלץ הוא זה שמביא להקלת כאב ללא תופעות לוואי בלתי נסבלות וללא קשר לרמת התרופה בפלזמה. תופעות הלוואי רבות וכוללות [[הפרעות בשווי משקל]], ישנוניות, [[תפרחת]] על פני העור, הפרעות ב[[תפקודי כבד]], רמה נמוכה של [[נתרן]], [[דיכוי מוח עצם]] ועוד. לפיכך, יש צורך לערוך בדיקת מלחים בדם, תפקודי כבד ו[[ספירת דם]] לפני תחילת הטיפול ואחת למספר חודשים בהמשך. | ||
| + | ::* [[Lamotrigine]] היא תרופה נוגדת כפיון נוספת אשר נמצאה יעילה במספר סוגי כאב עצבי דוגמת תסמונת העצב המשולש, כאב ממקור נוירופתיה סוכרתית, [[כאב סכיאטי]] (Sciatic nerve pain) ועוד. המינון היעיל הוא 200-400 מ"ג בשתי מנות מחולקות, אולם יש להעלות את מינון התרופה בהדרגה, פעם בשבוע, החל מ-25 מ"ג ליום כדי למנוע תופעות לוואי ובמיוחד תפרחת העלולה להתפתח כחלק מ[[תסמונת סטיבן ג'ונסון]] (Stevens–Johnson syndrome). | ||
| − | + | ===אופיואידים (Opioids) === | |
| + | :* [[אופיואידים]] הם מהתרופות הטובות והיעילות לשכוך כאב בכלל וכאב עצבי בפרט. בעבר נחשבו כלא יעילים לכאב העצבי, אך יעילותם בהפחתת כאב עצבי הוכחה במספר מחקרים קליניים. בשנים האחרונות גובר השימוש באופיואידים להקלת כאב כרוני שאינו ממקור ממאיר וזאת על סמך ניסיון מצטבר המראה כי הסיכון להתמכרות נמוך ביותר. התרופות משמשות בעיקר להתקפים קשים וכתרופות קו שני כאשר תרופות אחרות נכשלו. | ||
| − | + | ===סטרואידים=== | |
| + | :* במחקר של קולטין נמצא שיפור ניכר ב-83% מהחולים שטופלו ב-40 מ"ג [[Prednisolone]] ליממה למשך חודש, לעומת 17% שיפור בחולים שטופלו ב-[[Piroxicam]]. הטיפול ב[[סטרואידים]] הוא טיפול מקובל בשלבים הראשונים של המחלה. | ||
| − | [[ | + | ===קלציטונין - Calcitonin=== |
| + | :* יעילות הטיפול ב- [[Calcitonin Salmon|Calcitonin]] מוטלת בספק עם יתרון על אינבו עם תופעות לוואי משמעותיות. רוב הטיפולים האחרים נמצאו יעילים יותר. | ||
| − | + | ===ביספוספונטים=== | |
| + | :* במחקר של ורנה נמצאה [[Clodronate]] יעילה לעומת אינבו במתן דרך הווריד למשך 10 ימים במינון של 300 מ"ג ליממה. [[Aredia]] (Pamidronate Disodium) ו-[[Alendronate]] נמצאו גם הן יעילות עם השפעה משמעותית על רמת הכאב והתפקוד בחולים בתסמונת הכאב האזורית המורכבת. לסיכום, [[ביספוספונטים]] נמצאו יעילים כקבוצה בחולים הסובלים מתסמונת הכאב האזורית המורכבת. | ||
| − | == | + | === תרופות במתן תוך-ורידי === |
| − | + | # [[Lidocaine]] במתן תוך-ורידי במינון של עד 5 מ"ג לק"ג משקל גוף במהלך כשעה (בדרך כלל במסגרת מרפאות כאב). הטיפול עשוי להפחית כאב עצבי למשך ימים ואף שבועות. הטיפול מחייב ניטור קפדני עקב הסכנה לתופעות לבביות וכפיוניות. על פי רוב יש לבצע בדיקת [[אק"ג]] (אלקטרוקרדיוגרם) (Electrocardiogram, ECG) לפני העירוי הראשון. | |
| + | # [[Ketamine]] או [[Amantadine]] במתן תוך-ורידי משמשות כחסמים לקולטני גלוטמאט (חומרים המעלים את רגישות קולטני הכאב), והן נמצאו כטיפול יעיל לכאב עצבי. מתן עירויים מסוג זה מתבצע במרפאות כאב בניטור ולעתים תוך כדי אשפוז. מתן פומי או באמצעות משחות של תכשירים אלה לתקופות ממושכות מביא להפחתת כאב, אך מתונה הרבה יותר. | ||
| + | # [[מגנזיום]] במתן תוך-ורידי הוא טיפול מקובל במרפאות הכאב בישראל. יש מעט מאוד פרסומים בספרות הרפואית לגבי יעילות הטיפול, אך הניסיון הקליני בארץ תומך בשימוש בו. המגנזיום מוריד תחושת כאב, מרפה שרירים, מעלה סף הפעלה של עצבים, חוסם קולטני NMDA{{כ}} (N-Methyl-D-Aspartate), אשר מגרים כאב ומרחיבים כלי דם. יש לחזור על הטיפולים אחת למספר שבועות. ניתן להוסיף כדורי מגנזיום כתוסף מזון, אך יש לעקוב אחרי רמות המגנזיום בדם. | ||
| − | + | === טיפולים דרך העור === | |
| + | |||
| + | # משחת ה-[[Zostrix]] (Capsaicin) פועלת במנגנון ייחודי להפחתת הכאב. המשחה מכילה את החומר הפעיל מפלפל אדום. כאשר אנו אוכלים פלפל חריף לראשונה, אנו מרגישים צריבה חזקה. לאחר מכן, אם אנו ממשיכים לאכול פלפל חריף, הצריבה הולכת ופוחתת ותחושה של עמימות מופיעה במקומה. ה-Zostrix שנספגת דרך העור או הריריות ומגיעה לקצות העצבים גורמת לריקונם מחומר שנקרא Substance C, הגורם לצריבה בלשון. לאורך זמן ה-Zostrix מרוקנת את החומר מקצות העצבים, ולכן נמנעת תחושת הצריבה והשרפה המאפיינת את הכאב העצבי. הבעיה בשימוש במשחה היא שכדי לקבל את ההקלה בכאב יש לעבור תחילה דרך התקופה של הצריבה. על החולה למרוח את המשחה 2-4 פעמים ביום ולהתמיד בכך. | ||
| + | # מדבקות [[Lidoderm]] (Lidocaine Patch 5%) מצופות ב-Lidocaine שהוא [[חומר אלחוש מקומי]]. ה-Lidocaine נספג חלקית דרך העור אל סיבי העצב. המדבקה מוצמדת לעור פעם עד פעמיים ביממה למשך 12 שעות ועשויה להפחית כאב ורגישות יתר אצל חולים עם כאב עצבי ממוקם היטב. למרבה הצער, המדבקה אינה משווקת בארץ, אם כי ניתן להשיגה בבתי מרקחת מסוימים המייבאים אותה מחו"ל. | ||
| − | === | + | ===פיזיותרפיה=== |
| − | [[ | + | * [[פיזיותרפיה]] היא אבן פינה של הטיפול. הנחיות הטיפול צריכות לכלול שיפור תפקודי בעזרת [[פעילות גופנית]]. |
| − | + | === טיפולים פולשניים === | |
| − | + | * ישנו מגוון רחב של טיפולים פולשניים לטיפול בכאב עצבי. הטווח נע בין הזרקות של חומרי הרדמה מקומיים לבין הצורך באבחון של מקור הבעיה, ועד השפעה טיפולית של הפעולה הפולשנית. הזרקה של סטרואידים לעצב הפגוע, בייחוד בתקופה של התפתחות הפגיעה העצבית, ולבסוף פעולות לניתוק או הקטנת ההולכה בעצב על-ידי הזרקה של חומרים הורסי עצבים ([[Phenol]], אלכוהול ו-[[Glycerol]]). כיום מתבצעות חסימות עצב גם באמצעות [[גלי רדיו]], אשר יתרונם בכך שהם פוגעים באופן בררני בסיבי העצב מוליכי הכאב, תוך צמצום הפגיעה בתפקודים עצביים אחרים. במקרים מסוימים מבוצעים ניתוחים לשחרור [[הידבקויות צפקיות]], [[העתקת עצב]], [[ניתוק עצב]] או הרחקת נוירומה, אשר גם הם עשויים להקל או אף להעלים את הכאב. | |
| + | #[[גירוי חוט השדרה]] (Spinal cord stimulation): הטיפול מבוסס על החדרת מוליכים חשמליים לתעלת עמוד השדרה שדרכן מועבר גירוי חשמלי אל חוט השדרה במגמה לחסום את הולכת הכאב אל המוח. החדרת המוליכים החשמליים דרך העור ללא צורך בניתוח פתוח הופכת את הפעולה לפשוטה ומדויקת, וזאת במחיר של תחלואה נמוכה יחסית. הטיפול ניתן לחולים שבהם לא ניתן להשיג הקלת כאב בדרכים פשוטות יותר. יעילות השיטה נבדקה במספר עבודות רב, והיא כלולה מספר שנים בסל הבריאות בארץ. | ||
| + | #[[השתלת משאבות לעמוד השדרה|השתלת משאבות]] [[Morphine]] היא אמצעי נוסף לשיכוך כאב מכל סוג, וכאב עצבי בפרט, אשר יוצע רק לחולים שבהם כל האמצעים האחרים לא הועילו. הטיפול מבוסס על החדרת מינונים נמוכים ביותר של אופיואידים, חומרי אלחוש מקומי ותרופות נוספות ישירות אל החלל התת-עכבישי. השתלת המשאבה היא פעולה ניתוחית לכל דבר. מילוי המשאבה מתבצע אחת למספר שבועות תוך התאמת סוג התרופות ומינונן. יצוין שגם טיפול זה כלול בסל הטיפולים בארץ. | ||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | [[ | + | {| |
| + | |+ '''טבלה 1''' | ||
| + | |- | ||
| + | !valign="top"| חלוקה על פי מצב חולי{{רווח קשיח|40}} | ||
| + | !valign="top"| קו ראשון{{רווח קשיח|60}} | ||
| + | !valign="top"| קו שני{{רווח קשיח|60}} | ||
| + | !valign="top"| קו שלישי{{רווח קשיח|60}} | ||
| + | |- | ||
| + | | '''[[נוירופתיה סוכרתית]] (כואבת)'''{{ש}} | ||
| + | | [[נוגדי דיכאון טריציקליים]]{{ש}} | ||
| + | | [[Lyrica]]{{כ}}, [[Neurontin]]{{כ}}, [[Duloxetine]]{{כ}}{{ש}}*יש לנסות את כל התרופות לפני מעבר לקו השלישי | ||
| + | | [[Venlafaxine]]{{כ}}, [[Tramadol]]{{כ}},{{ש}}[[אופיואידים]] חזקים או שילובים בין התרופות | ||
| + | |- | ||
| + | | | ||
| + | |- | ||
| + | | '''[[תסמונת העצב המשולש]]''' | ||
| + | | [[Carbamazepine]]{{כ}}, [[Oxcarbazepine]]{{כ}} | ||
| + | | Neurontin{{כ}}, Lyrica{{כ}} | ||
| + | | | ||
| + | |- | ||
| + | | | ||
| + | |- | ||
| + | | '''כאב נוירופתי אצל חולי [[סרטן]]'''{{ש}}(לחולים עם מחלה ממארת פעילה) לא מומלץ{{ש}}שימוש בנוגדי דיכאון טריציקליים כקו ראשון{{ש}}מכיון שהטיטור שלהם איטי וממושך | ||
| + | | [[Opium]] עם Neurontin{{כ}} או Lyrica | ||
| + | | אופיואידים עם [[t:Venlafaxine|Venlafaxine]] או Duloxetine | ||
| + | | | ||
| + | |- | ||
| + | | | ||
| + | |- | ||
| + | | '''כאב נוירופתי מרכזי''' | ||
| + | | נוגדי דיכאון טריציקליים | ||
| + | | Lyrica,{{כ}} Neurontin{{כ}}, [[Lamotrigine]]{{ש}}*יש לנסות כל אחת מהתרופות במינון מרבי לפני{{ש}}מעבר לקו השלישי | ||
| + | | אופיואידים בלבד או בשילוב תרופות מקווים קודמים | ||
| + | |- | ||
| + | | | ||
| + | |- | ||
| + | | '''[[נוירלגיה בתר הרפטית]]''' | ||
| + | | נוגדי דיכאון טריציקליים, Neurontin{{כ}}, Lyrica{{כ}}{{ש}}ומדבקות [[Lidocaine]] | ||
| + | | [[Valproic acid]]{{כ}}, Tramadol, אופיואידים | ||
| + | | Duloxetine{{כ}}, [[t:Venlafaxine|Venlafaxine]] | ||
| + | |- | ||
| + | | | ||
| + | |- | ||
| + | | '''תסמונת הכאב האזורית המורכבת''' | ||
| + | | [[סטרואידים]], [[Calcitonin Salmon]], [[ביספוספונטים]], משככי כאב {{ש}}שאינם אופיואידים, אופיואידים על פי עוצמת הכאב | ||
| + | | Lyrica{{כ}}, Neurontin{{כ}}, Duloxetine{{כ}}, בטיטור מהיר{{ש}}למינונים מרביים (מומלץ טיפול בן מספר שבועות) | ||
| + | | | ||
| + | |- | ||
| + | | | ||
| + | |- | ||
| + | | '''נוירופתיות מפושטות'''{{ש}}(למעט סוכרת ומחלות ממאירות) | ||
| + | | נוגדי דיכאון טריציקליים, Neurontin{{כ}}, [[t:ליריקה - Lyrica|Lyrica]] {{כ}} | ||
| + | | Tramadol{{כ}}, Duloxetine{{כ}}, Venlafaxine{{כ}},{{ש}}Lamotrigine{{כ}}, Carbamazepine | ||
| + | | אופיואידים בלבד או בשילוב תרופות מקווים קודמים | ||
| + | |- | ||
| + | | | ||
| + | |- | ||
| + | | '''כאב נוירופתי משני לפגיעת עצב ממוקדת''' | ||
| + | | נוגדי דיכאון טריציקליים | ||
| + | | Lyrica{{כ}}, Neurontin{{כ}}, Duloxetine{{ש}}*יש לנסות את כל התרופות לפני מעבר לקו השלישי | ||
| + | | Venlafaxine{{כ}}, Tramadol{{כ}}, אופיואידים או שילובים | ||
| + | |} | ||
| − | == | + | == פרוגנוזה == |
| − | תסמונת הכאב האזורית המורכבת | + | תסמונת הכאב האזורית המורכבת ברובה אינה ניתנת לריפוי, ולכן הטיפול בה הוא ארוך טווח ופוגע באיכות החיים של הסובלים ממנו. |
==דגלים אדומים== | ==דגלים אדומים== | ||
==ביבליוגרפיה== | ==ביבליוגרפיה== | ||
| − | |||
<blockquote> | <blockquote> | ||
<div style="text-align: left; direction: ltr"> | <div style="text-align: left; direction: ltr"> | ||
| − | |||
{{הערות שוליים}} | {{הערות שוליים}} | ||
| − | |||
</div> | </div> | ||
</blockquote> | </blockquote> | ||
| שורה 171: | שורה 230: | ||
| − | {{ייחוס| ד"ר סילביו בריל - מנהל [http://www.pain.co.il/ יחידת לטיפול בכאב, המרכז הרפואי ת"א ע"ש סוראסקי, תל אביב]; מזכיר [http://www.pain.co.il/ האגודה הישראלית לכאב], ד"ר איתי גור-אריה- מנהל יחידת הכאב המרכז הרפואי ע"ש ח' שיבא, תל השומר; יו”ר האגודה הישראלית לכאב, }} | + | {{ייחוס| [[משתמש:סילביו בריל|ד"ר סילביו בריל]] - מנהל [http://www.pain.co.il/ יחידת לטיפול בכאב, המרכז הרפואי ת"א ע"ש סוראסקי, תל אביב]; מזכיר [http://www.pain.co.il/ האגודה הישראלית לכאב], ד"ר איתי גור-אריה- מנהל יחידת הכאב המרכז הרפואי ע"ש ח' שיבא, תל השומר; יו”ר האגודה הישראלית לכאב, }} |
| שורה 181: | שורה 240: | ||
[[קטגוריה: כאב]] | [[קטגוריה: כאב]] | ||
[[קטגוריה: נוירולוגיה]] | [[קטגוריה: נוירולוגיה]] | ||
| − | [[קטגוריה:מדיקל מדיה | + | [[קטגוריה:מדיקל מדיה]] |
גרסה אחרונה מ־10:43, 2 ביולי 2018
| תסמונת הכאב האזורית המורכבת | ||
|---|---|---|
| Complex regional pain syndrome | ||

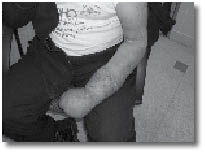
| ||
| שמות נוספים | Reflex sympathetic dystrophy | |
| יוצר הערך | ד"ר סילביו בריל, ד"ר איתי גור-אריה 
|
|
לערכים נוספים הקשורים לנושא זה, ראו את דף הפירושים – כאב
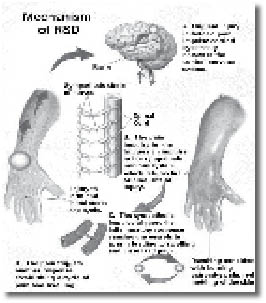
תסמונת הכאב האזורית המורכבת (Complex Regional Pain Syndrome, CRPS) מוכרת מימי מלחמת האזרחים האמריקאית, עת נקראה קוזלגיה (Causalgia), שם שנבחר כדי לתאר שריפה וכאבים לאחר פציעה. מאז, שם התסמונת שונה מספר פעמים. Bonica טבע את המונח החזר סימפתטי דיסטרופי (Reflex Sympathetic Dystrophy, RSD) ב-1953. קבוצת מומחים קבעה את שינוי השם ב-1993 לתסמונת כאב אזורי מורכב. עם זאת רבים מהרופאים עדיין נוהגים להשתמש במונח החזר סימפתטי דיסטרופי. תסמונת הכאב האזורית המורכבת מאופיינת באירועי כאב מתפרץ בעצמה רבה, השונים באופיים מכאבים בעלי אופי קבוע. כאב נוירופתי, נויראלגיה (נוירו=עצב, אלגיה=כאב), מהווה את אחת מבעיות הכאב הקשות שאיתן מתמודדת הרפואה בכלל, ורפואת הכאב בפרט. בין הגורמים לתסמונת הכאב האזורית המורכבת ניתן למנות מחלות סרטן, טיפולים כימותרפיים והקרנות, מחלות זיהומיות, מחלות של חילוף חומרים, חומרים רעילים, ניתוחים וכן פגיעות בשל חבלה או תאונות. הטיפול בתסמונת הוא ארוך טווח ומותאם לחולה, ומורכב מטיפול תרופתי, טיפולים גופניים ונפשיים, ולעתים כולל גם התערבות ניתוחית.
אפידמיולוגיה
שכיחות תסמונת הכאב האזורית המורכבת עשויה להגיע לכדי 5%-7% מן האוכלוסייה הבוגרת. התסמונת מתפרצת בעיקר במבוגרים צעירים, מעט יותר בנשים.
אטיולוגיה
תסמונת הכאב האזורית המורכבת יכולה להיגרם על-ידי מספר מצבי מחלה:
- מחלות סרטן עשויות לגרום לפגיעה עצבית דרך מסת הגידול הלוחצת או חודרת לעצבים ולמוח, ואף דרך הטיפול במחלה על-ידי הקרנות וכימותרפיה, שיש ביכולתן לפגוע בעצב
- מחלות זיהומיות, כגון שלבקת חוגרת הרפטית (Herpes Zoster, Shingles) יכולות לפגוע בתאי העצב ולהורגם
- מחלות של חילוף חומרים, כגון סוכרת שגורמת לפגיעה בכלי הדם הקטנים המספקים דם לעצבים, ומשנית לכך נגרם מוות של תאי עצב
- חומרים רעילים, כגון עופרת, אך גם אלכוהול, גורמים לנזקים שונים ביניהם גם הרס של עצבי תחושה וכאב
- בנוסף, קיים כאב עצבי לאחר ניתוחים (ובמיוחד ניתוחי דופן בית החזה), וכן פגיעה בשל חבלה או תאונות או לאחר ניתוחים אחרים
לא נמצא קשר בין עוצמת התסמונת, מרגע שהתפתחה, לבין הגירוי הראשוני. עם זאת, קיימים גירויים מועדים, כגון שבר במפרק כף יד ומרפק, וכן אירועים כניתוחים של גידולים סרטניים והתקף לב, היכולים להוביל להתפתחות המחלה.
ייתכן ולגורמים גנטיים השפעה על הופעת תסמונת הכאב האזורית המורכבת. התסמונת שכיחה יותר בקרב חולים בעלי האללים HLA-A3 ,B7 ,DR2. נראה כי לשונות גנטית השפעה גם על התגובה לטיפול, שכן, לפי אחד המחקרים, חולים שהם בעלי הגנוטיפ HLA-DR2 היו עמידים יותר לטיפולים תרופתיים.
ההיבט הנפשי כנראה שותף אף הוא להתפתחות התסמונת. 80% מהחולים שפיתחו את המחלה, סבלו מלחץ נפשי בחודשיים שקדמו להופעתה ובחודש לאחר שהתפתחה. עם זאת, יש לציין שלא נמצא מבנה נפשי משותף הקשור לתסמונת הכאב האזורית המורכבת.
- מנגנונים להתפתחות כאב עצבי
למרות שהתסמונת מוכרת כבר כמאה וחמישים שנים, עדיין אין מנגנון ברור המסביר את התסמונת. מספר מנגנונים אחראים להתפתחות הכאב העצבי. כל כאב כרוני מתאפיין בהתעצמות של הכאב לאורך זמן, וזאת בשל התפתחות של רגישות יתר לכאב. מצב הרגישות יתר מתפתח לאורכה של מערכת העצבים, וכל גירוי כאב מתמשך גורם לשינויים באזור קולטני הכאב ברקמה הפגועה, בגופי התא העצבי, בחוט השדרה ובמרכזי הכאב במוח. באופן תקין, לגוף יש מנגנוני תיקון ודיכוי שמעלימים את השינויים, אחרת, היה הגוף מוסיף לסבול מכל כאב שנחווה במהלך החיים. בפגיעות עצביות המנגנונים משמעותיים הרבה יותר והשינויים נמשכים לאורך זמן. מאחר שמערכת העצבים האחראית על ההעצמה של הכאב והפסקתו בהמשך, היא הנפגעת בתסמונת, התיקון קשה יותר ולפעמים כלל לא מתאפשר.
מבחינה מכנית, ניתן לדמות את מערכת העצבים למערכת של חוטי טלפון מבודדים, הנעים יחדיו בצברים בתוך צינורות, אשר מוליכים אותם מהמוח לרקמות ומהרקמות חזרה אל המוח. בזמן פגיעה בעצב, יכולים להיווצר מספר מצבים שבהם יש הרס מוחלט או חלקי של כל אחד מחלקי המערכת. רקמת עצב יכולה לגדול שוב גם אם השלוחות והרקמות סביבה נפגעו, בתנאי שגוף תא העצב לא נפגע. קצב הגדילה של עצב עומד על כ-1-2 מ"מ ליממה, והגידול מחדש יכול, לכן, לקחת זמן רב. למשל, פגיעה בעצב באזור הישבן יכולה להתרפא במשך שלוש שנים, ולאפשר לשלוחות העצב לגדול חזרה לכף הרגל. הגדילה מחדש של עצב היא חלק מההחלמה, אך לעתים היא גם חלק מהבעיה. שלוחות העצב (Axons) הגדלות מחדש, לא תמיד גדלות בצורה סדירה. לחלק מן השלוחות אין רקמות בידוד, והן יוצרות מעין קצר עם שלוחות אחרות שאינן מבודדות. שלוחות אלה יכולות לגרום לכך שתחושה שאינה כאב, תעבור למסלול של כאב או להיפך. כאשר רקמות החיבור המובילות את שלוחות העצב נהרסות, השלוחות שגדלות מחדש ממשיכות לגדול ללא אבחנה, ויוצרות מבנה כדורי הנקרא נוירומה, (Neuroma) הרגיש לכל מגע ולעתים מופעל באופן עצמוני וגורם לכאב עז.
השינויים במערכת העצבית אינם מבניים בלבד, אלא מקורם בשינויים כימיים המתרחשים על מעטפות התאים ובגופי התא. השינויים הללו גורמים לתאים לפתח גריות יתר (Hyperexcitability) של העצב. משמעות הדבר היא כי גירוי שבדרך כלל לא היה מועבר דרך העצב, עתה יכול להיות מועבר וביתר עצמה. תעלות נתרן-סידן ותעלות אחרות ממלאות תפקיד מרכזי בהתהוותה של גריות היתר ההיקפית. המנגנונים חשובים להבנה של דרך פעילותן של תרופות הפועלות נגד כאב עצבי. נוסף על כך, מתפתחת גריות יתר של תאי עצב תחושתיים בחוט השדרה, וייתכן שגם באתרים גבוהים יותר במערכת העצבים המרכזית. שינויים אלו מושרים על ידי החומצה האמינית גלוטמאט (Glutamate) וכנראה שגם על-ידי חומרים אחרים.
מנגנון חשוב נוסף הנפגע בזמן פגיעה עצבית הוא המערכות המדכאות הולכה במערכת העצבית. באופן תקין, ישנם מסלולים עצביים במוח ומסלולים עצביים היורדים מהמוח אל חוט השדרה, אשר תפקידם לדכא את ההולכה של גירויים מהרקמות לכיוון המוח. דיכוי זה מונע מצב של גירויים בלתי פוסקים, כדוגמת תחושה של מגע הבגד על גופינו. בפגיעה עצבית יש ירידה בפעילותן של מערכות אלו, שחלקן מדכא הולכת כאב. מקצתן של התרופות מנסות לטפל דרך התערבות במנגנונים אלה, אף על פי שהמנגנונים טרם הובהרו די צורכם.
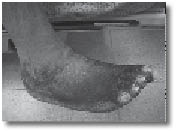
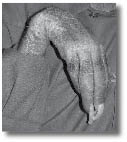
מנגנון נוסף של תסמונת הכאב האזורית המורכבת קשור במערכת האוטונומית, בעיקר הסימפתטית, וזאת למרות שברוב המקרים, תרומתה לתסמונת ככל הנראה מוגבלת. על פי המנגנון המוצע, המערכת הסימפתטית מגיבה לפגיעה בפעילות יתר. תגובה זו לכאורה גורמת לעלייה בחום הגפה בשלב הראשון, המשולבת עם גידול מהיר של השיער והציפורניים - השלב של גדילת היתר (Hypertrophic). לאחר מכן, מתרחשת ירידת חום בגפה הפגועה, כלי הדם מתכווצים, והעור, השיעור והציפורנים עוברים ניוון - שלב הדלדול (Atrophic). אולם, ברוב המקרים אין כנראה עלייה בפעילות מערכת העצבים האוטונומית, ולכן ההגדרות החדשות שבשימוש הן תיאוריות ולא מנגנוניות. עם זאת, חלק מהמקרים אכן מבוססים על פגיעה אוטונומית תפקודית. פגיעה זאת נקראת SMP (Sympathetically Maintained Pain).
- תסמונת הכאב האזורית המורכבת חולקה לשני סוגים
- סוג 1, שבו הפגיעה היא כמתואר (90% ממקרים שייכים לסוג זה).
- סוג 2, שמלווה בפגיעה עצבית ברורה כמקור להתפתחות התסמונת.
קליניקה
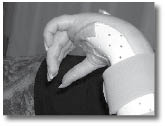
תסמונת הכאב האזורית המורכבת מאופיינת בכאבים אזוריים המלווים בדרך-כלל בשינויי צבע, הפרעות בהזעה, וחום ורגישות העור בגפה המעורבת. הכאבים מתוארים על פי רוב כ"שורפים", ולעתים אף מלווים בנפיחות מקומית או כללית של הגפה. הכאב בתסמונת חריג בעצמתו וללא יחס תואם לעוצמת הפגיעה שגרמה לו, והוא יכול להביא לחוסר תנועה של הגפה הפגועה. יכולות להופיע הפרעות תנועה שאינן קשורות לכאב, כגון התכווצויות, רעד וחוסר יכולת לתנועה מתואמת. מלבד עוצמת הכאב הגבוהה, תסמונת הכאב האזורית המורכבת מאופיינת בתגובת כאב לגירוי שבדרך כלל אינו מכאיב (Allodynia) וסף רגישות נמוך לכאב (Hyperalgesia). השלבים המתקדמים של המחלה יכולים להגיע עד שברים בעצמות עקב ניוון שלהן, התפתחות כיבים עקב חוסר תנועה ולחץ לא אחיד וקיצור שרירים, המובילים לשיתוק תפקודי. תסמונת הכאב האזורית המורכבת יכולה להתפשט. ההתפשטות היא לרוב לאורך הגפה הפגועה, אם כי קיימים מקרים בהם הכאב קופץ לגפה השנייה המקבילה (ימין-שמאל) או לגפה השנייה באותו הצד (עליונה-תחתונה). לאחר התפתחות התסמונת יש תסמינים נפשיים משניים לכאב, כגון פחד, חרדה, כעס ודיכאון.
אבחנה
לאחר נטילת העבר הרפואי הקשור למחלה ובדיקה גופנית, קיימים מבחנים העוזרים להגיע לאבחנה.
- חסמים עצביים של המערכת הסימפתטית או של העצב החשוד כפגוע (בתסמונת הכאב האזורית המורכבת מסוג 2), וזאת על ידי הזרקות או עירויי Regitine (Phentolamine).
- בדיקות כגון אלקטרומיוגרפיה (Electromyography, EMG) ובדיקות של הולכה תחושתית, היכולות לסייע באבחנה ובזיהוי רמת הפגיעה העצבית.
- הדמאה תרמית (Thermography) ובדיקת על-קול דופלר (Doppler ultrasound) משמשות לזיהוי הפגיעה בכלי הדם.
- צילומי רנטגן ומיפוי עצמות עשויים להראות סימני ניוון אופייניים בעצמות, אך הם אינם נחשבים לחד-משמעיים בביסוס האבחנה.
נכון למועד כתיבת מאמר זה אין בדיקת עזר אשר יכולה לאשר או לשלול באופן מוחלט את קיום תסמונת הכאב האזורי המורכב.
האגודה הבין-לאומית לחקר הכאב (International Association for the Study of Pain, IASP) קבעה את המדדים לאבחון של תסמונת כאב אזורי מורכב:
- התסמין הראשון הוא עבר של פגיעה באיבר שפיתח את התסמונת, דוגמת מכה, נקע או שבר. עוצמת הפגיעה יכולה להיות קלה ביותר ולא קשורה לחומרת התסמונת.
- התפתחות כאב באזור הפגיעה המאופיין בכאב בעצמה גבוהה, כאב המושרה על ידי גירוי שאינו מכאיב, וסף רגישות נמוך לכאב. הכאב הוא על פי רוב דמוי גרב או כפפה ואינו מתפזר לאורך מסלול עצבי ברור.
- עדות לנפיחות בגפה הפגועה ועדות לפגיעה בתפקוד כלי הדם, כמו חום או קור של הגפה.
- שלילה של מחלות אחרות.
- סימנים של שינויים ברקמות, כמו ירידה במסת שריר, שינויים ניווניים בעור, גידול מהיר של שיער וציפורניים, מחזקים את האבחנה.
טיפול
הטיפול בתסמונת הכאב האזורית המורכבת כולל מספר שיטות וגישות: תרופות, הזרקות וחסמים עצביים, פיזיותרפיה משמעותית ותמיכה נפשית. פעמים רבות יש לערב את מחלקות השיקום המתמחות בנושא. הטיפול מתבצע במספר שלבים שנכונים עבור כל טיפול: התחלה בטיפול שמידת הסיכון בו נמוכה, ועליה במידת הפולשניות במידת הצורך. הטיפול מתחיל בטיפול תרופתי, עובר להזרקות ולבסוף מגיע לניתוק עצבים ולהשתלת מוליכים חשמליים.
בחירת הטיפול התרופתי ההתחלתי מתבססת על מספר גורמים: יעילות מוצעת ממחקרים וניסיון קודם לעומת מידת תופעות הלוואי הצפויות. פן נוסף הוא מידת החריפות של הבעיה, וכן חולה עם כאב עצבי חדש יטופל ביתר תוקפנות. בבחירת הטיפול התרופתי יש העדפה לתרופה אחת בלבד לטיפול בכאב, אך במקרים של כאב קשה לטיפול נישקל השימוש בשילוב של תרופות. לרוב קיימת העדפה לתרופות הניתנות דרך הפה, לעומת מתן תוך-ורידי.
הטיפול התרופתי מבוסס על שימוש בתרופות לכאב עצבי, למשל: Lyrica (Pregabalin), Neurontin (Gabapentin), Duloxetine, Carbamazepine, ו-Anastrozole. קיימות גם תרופות ממשפחות אחרות, ובכלל זה תרופות החוסמות קולטנים אדרנרגיים, כגון: Clonidine, וכן תרופות המונעות ספיגת עצם ממשפחת הביספוספונטים (Biphosphonates). כמו כן, קיימים דיווחים אודות יעילותן של תרופות במתן תוך-ורידי, אך חלק גדול מהן לא קיים בישראל. התרופות התוך-ורידיות יכולות לשפר את אספקת הדם לרקמות על-ידי הורדת פעילותה של המערכת הסימפתטית, והורדה של הכאב העצבי. העירויים המקובלים לטיפול הם של Lidocaine, מגנזיום, Phentolamine, Ketamine ו-Bretylium.
חסמים עצביים וורידיים סימפתטיים כוללים את Dibenyline (Phenoxybenzamine), Prazosin, Doxazosin ו-Terazosin, והם נמצאו יעילים בחסימה בררנית של קולטנים על כלי הדם, המכירים חומרים המופרשים על-ידי המערכת הסימפתטית. כתוצאה מהחסימה, חלה הרחבה של כלי הדם בגפה הפגועה, שיפור בזרימת הדם ושיכוך הכאב. ניתן להשתמש בחסמים של המערכת העצבית הסימפתטית בגובה הצוואר [חסם של גנגליון דמוי כוכב (Stellate ganglion)], אשר חוסמים את העצבוב לכיוון הגפה העליונה, וכן בחסמים של השרשרת העצבית הסימפתטית בגב התחתון, אשר מספקת את הרגל, וזאת כדי לסייע באבחנה ובטיפול בתסמונת.
במקרים של תסמונת הכאב האזורית המורכבת מסוג 2 יש מקום גם לחסמים עצביים באזור העצב הפגוע, ואף לניסיון להזריק סטרואידים למקום. השימוש בפעולות פולשניות, כגון השתלת מוליכים חשמליים אפידורליים (Epidural electrodes) והשתלת משאבות נמצא יעיל, אך נשמר לשלבים מאוחרים בטיפול עם הרס מכוון של שרשראות העצבים האוטונומיות.
שלוש קבוצות של תרופות מהוות את אבני היסוד בטיפול בכאב העצבי בכלל ובתסמונת כאב אזורי מורכב בפרט, והן תרופות נוגדות דיכאון, נוגדות כפיון ואופיואידים.
תרופות נוגדות דיכאון
מנגנון פעולתן המשוער של קבוצת התרופות נוגדות הדיכאון הוא הפעלת מערכות שיכוך כאב מוחיות וחיזוק פעולתם של המסלולים היורדים מהמוח לכיוון חוט השדרה, ודיכוי הולכה במסלולי כאב לכיוון המוח. הדבר נעשה באמצעות מניעת ספיגה חוזרת של סרוטונין ונוראדרנלין במצמדים מוחיים (Synapse, נקודות הקשר בין עצבים). ייתכן, כי לתרופה מנגנון שיכוך כאב נוסף באמצעות ייצוב מעטפות תא עצביות. השפעתן של התרופות נגד דיכאון על הכאב היא ישירה, ואינה תלויה בהשפעתן על דיכאון. לרוב השפעתן על הכאב היא במינונים נמוכים מהמינונים הנדרשים לטיפול בדיכאון, ומהירה יותר. חשוב לומר למטופל כי התרופה שבה הוא מטופל משמשת גם לטיפול בדיכאון, שכן אם ילמד על כך ממקורות אחרים, הוא עשוי לחשוב כי הרופאים אינם מאמינים לכאביו וחושבים שהם נפשיים, ובהמשך לכך יסרב ליטול את התרופה או להמשיך בטיפול.
פן הדיכאון עצמו הוא פן חשוב בכאב. כאב כרוני מוביל לדיכאון בחלק גדול מהמקרים ובמיוחד בקרב הסובלים מכאב עצבי, לכן יש תועלת כפולה בשימוש בתרופות נוגדות דיכאון לכאב.
- קבוצת התרופות נוגדות הדיכאון כוללת מספר תת-קבוצות
- הקבוצה הוותיקה של נוגדי דיכאון טריציקליים (Tricyclic Antidepressants, TCAs) נחקרה רבות ונמצאה יעילה בהפחתת סוגי כאב עצבי רבים ללא קשר להשפעתה על דיכאון. התרופות מתת-קבוצה זאת אינן בררניות ומשפיעות על חומרים מוחיים נוספים, ולכן תופעות הלוואי שלהן נרחבות יותר. Elatrol (Amitriptyline) היא נציגה של הקבוצה. התרופה ניתנת במינון התחלתי של 10-25 מ"ג. העלאת המינון חייבת להיות הדרגתית כדי להפחית תופעות לוואי. חלק מן המטופלים מדווחים על הקלת כאב במינוני ביניים (50-75 מ"ג), אם כי לעתים יש צורך להגיע ל-100-150 מ"ג ליממה ואף יותר במנה אחת בערב. הסיבה לכך היא שהתרופה גורמת לישנוניות, וכך תופעת הלוואי מסייעת למטופל להירדם. קיימות תופעות לוואי רבות נוספות, הכוללות תופעות של יובש בפה, עצירות, ישנוניות יתר, סחרחורת ועוד. יש להימנע משימוש בתרופה אצל חולים הסובלים מברקית עם זווית חדה (Narrow angle glaucoma), הגדלת הערמונית (Prostatic hyperplasia), הפרעות במערכת ההולכה בלב ולאחר אוטם בשריר הלב. תרופות נוספות מקבוצה זאת הן Deprexan (Desipramine), וכן Clomipramine.
- מעכבי ספיגה חוזרת של סרוטונין ונוראפינפרין (Serotonin and Norepinephrin Reuptake Inhibitor, SNRI) היא תת-הקבוצה השניה והעדכנית של תרופות נוגדות דיכאון שנמצאה יעילה לטיפול בכאב עצבי. תרופות ממשפחה זו חוסמות את ספיגת נוראדרנלין וסרוטונין באופן בררני. מאחר שהחסימה בררנית יותר בהשוואה לפעולת נוגדי הדיכאון טריציקליים, תופעות הלוואי שלה פחותות. Duloxetine נרשמה בארץ ואף הוכנסה לסל התרופות לאחר שנמצאה לה יעילות גבוהה בהפחתת כאב ממקור נוירופתיה סוכרתית, ירידה ב-50% ברמת הכאב ב-50% מהמטופלים. ניתן להתחיל טיפול במינון של 30 מ"ג לשבוע, ואז להעלות את המינון ל-60 מ"ג ליום במנה אחת בערב. תופעות הלוואי העיקריות שנצפו היו בחילה, נמנום וסחרחורת, שחלפו לרוב עם הזמן. רוב תופעות הלוואי היו בדרגת חומרה קלה עד בינונית, נצפו בדרך כלל בתחילת הטיפול, וחלפו עם המשך הטיפול. נציגה נוספת ממשפחה זו היא ה-Venlafaxine, אם כי לגביה ההוכחות ליעילות נמוכות יותר, והיא אינה רשומה לאבחנה של טיפול בכאב עצבי בישראל.
- מעכבי ספיגה חוזרת של סרוטונין (Selective Serotonin Reuptake Inhibitor, SSRI) תת-הקבוצה השלישית פועלת באופן בררני להעלאת מינון הסרוטונין במוח. תרופות אלה בטוחות יותר בשימוש בהשוואה לנוגדי הדיכאון הטריציקליים, אולם יעילותן כמשככי כאב עצבי ירודה בהתאם. מבין תרופות אלה ניתi לציין את ה-Paroxetine הניתנת במנה אחת בת 20-40 מ"ג מאחר שנמצאה יעילה בהפחתת כאב ממקור נוירופתיה סוכרתית במחקר בודד. נראה כי ההשפעה שלה על הכאב נובעת בעיקר מהשפעתה על הדיכאון הנלווה.
תרופות נוגדות כפיון (Epilepsy)
- השימוש בתרופות נוגדות כפיון לטיפול בכאב עצבי נראה מעט תמוה בתחילה, אך כאשר בוחנים את מנגנוני הפעולה של התרופות נוגדות הכפיון מחד, ומאידך את השינויים ומנגנוני הנזק בכאב עצבי, ניתן למצוא התאמה. התרופות פועלות על מנגנונים המונעים את ההתפרצויות העצמוניות של הכאב, ומעלות את סף ההפעלה של העצבים הפגועים. התרופות נוגדות הכפיון אינן יוצרות התרגלות או התמכרות, הן בטוחות יחסית לשימוש, ותופעות הלוואי שלהן לרוב סבילות. התרופות ברובן בשימוש שנים רבות לטיפול בכפיון.
- גם ביחס לתרופות נוגדות כפיון, יש לידע את החולה כי הוא מקבל תרופות מקבוצה זו, וכי אין סכנה שיפתח כפיון בשל כך.
- בתוך נוגדי הכפיון יש מספר תת-משפחות הנבדלות במנגנונים אשר עליהן הן פועלות
- Lyrica היא תרופה חדשה אשר נבדקה ונמצאה יעילה ובטוחה במספר גדול של חולים עם כאב ממקור נוירופתיה סוכרתית או נוירלגיה בתר הרפטית (Post herpetic neuralgia). המינון הוא 300-600 מ"ג ליממה בשתי מנות מחולקות. יתרונה בהתאמת המינון המהיר המתבצעת תוך פרק זמן קצר (3-6 יממות). התרופה פועלת דרך חסימה של תעלות סידן מיוחדות המופיעות על גופי תאי העצב הפגועים. התרופה נקשרת ביעילות גבוהה פי 6 מאשר Neurontin לתעלות הסידן, ולכן יותר בררנית וייתכן שאף בעלת תופעות לוואי פחותות. התרופה מופיעה במינונים של 25, 50, 75, 150 ו-300 מ"ג. עיקר תופעות הלוואי הן סחרחורת, עייפות, טשטוש ובצקות היקפיות. זוהי התרופה היחידה הרשומה בישראל לכל סוגי הכאב העצבי ההיקפי ולאחרונה גם לכאב עצבי מרכזי. לאחרונה נכנסה לסל הבריאות.
- Neurontin הפועלת במנגנון זהה ל-Lyrica, נמצאה יעילה בשיכוך כאב עצבי מסוגים שונים במספר רב של מחקרים. בישראל רשומה רק לטיפול בכאב עצבי בתר-הרפטי וסוכרתי. מינון התרופה הוא בין 900 ל-3,600 מ"ג ליממה בשלוש מנות מחולקות. הקינטיקה של התרופה אינה קווית כך שלעתים שיכוך הכאב נראה רק במינוני תרופה גבוהים. העלאת המינון מתבצעת תוך ימים עד שבועות. תופעות הלוואי דומות לאלה של Lyrica.
- Carbamazepine יעילה במיוחד להפחתת התקפי תסמונת העצב המשולש (Trigeminal neuralgia), וייתכן שגם בכאבים עצביים נוספים. המינון התחלתי הינו 100 מ"ג פעמיים ביום, ויש לעלות במינון בהדרגה בשל ריבוי תופעות הלוואי. המינון המומלץ הוא זה שמביא להקלת כאב ללא תופעות לוואי בלתי נסבלות וללא קשר לרמת התרופה בפלזמה. תופעות הלוואי רבות וכוללות הפרעות בשווי משקל, ישנוניות, תפרחת על פני העור, הפרעות בתפקודי כבד, רמה נמוכה של נתרן, דיכוי מוח עצם ועוד. לפיכך, יש צורך לערוך בדיקת מלחים בדם, תפקודי כבד וספירת דם לפני תחילת הטיפול ואחת למספר חודשים בהמשך.
- Lamotrigine היא תרופה נוגדת כפיון נוספת אשר נמצאה יעילה במספר סוגי כאב עצבי דוגמת תסמונת העצב המשולש, כאב ממקור נוירופתיה סוכרתית, כאב סכיאטי (Sciatic nerve pain) ועוד. המינון היעיל הוא 200-400 מ"ג בשתי מנות מחולקות, אולם יש להעלות את מינון התרופה בהדרגה, פעם בשבוע, החל מ-25 מ"ג ליום כדי למנוע תופעות לוואי ובמיוחד תפרחת העלולה להתפתח כחלק מתסמונת סטיבן ג'ונסון (Stevens–Johnson syndrome).
אופיואידים (Opioids)
- אופיואידים הם מהתרופות הטובות והיעילות לשכוך כאב בכלל וכאב עצבי בפרט. בעבר נחשבו כלא יעילים לכאב העצבי, אך יעילותם בהפחתת כאב עצבי הוכחה במספר מחקרים קליניים. בשנים האחרונות גובר השימוש באופיואידים להקלת כאב כרוני שאינו ממקור ממאיר וזאת על סמך ניסיון מצטבר המראה כי הסיכון להתמכרות נמוך ביותר. התרופות משמשות בעיקר להתקפים קשים וכתרופות קו שני כאשר תרופות אחרות נכשלו.
סטרואידים
- במחקר של קולטין נמצא שיפור ניכר ב-83% מהחולים שטופלו ב-40 מ"ג Prednisolone ליממה למשך חודש, לעומת 17% שיפור בחולים שטופלו ב-Piroxicam. הטיפול בסטרואידים הוא טיפול מקובל בשלבים הראשונים של המחלה.
קלציטונין - Calcitonin
- יעילות הטיפול ב- Calcitonin מוטלת בספק עם יתרון על אינבו עם תופעות לוואי משמעותיות. רוב הטיפולים האחרים נמצאו יעילים יותר.
ביספוספונטים
- במחקר של ורנה נמצאה Clodronate יעילה לעומת אינבו במתן דרך הווריד למשך 10 ימים במינון של 300 מ"ג ליממה. Aredia (Pamidronate Disodium) ו-Alendronate נמצאו גם הן יעילות עם השפעה משמעותית על רמת הכאב והתפקוד בחולים בתסמונת הכאב האזורית המורכבת. לסיכום, ביספוספונטים נמצאו יעילים כקבוצה בחולים הסובלים מתסמונת הכאב האזורית המורכבת.
תרופות במתן תוך-ורידי
- Lidocaine במתן תוך-ורידי במינון של עד 5 מ"ג לק"ג משקל גוף במהלך כשעה (בדרך כלל במסגרת מרפאות כאב). הטיפול עשוי להפחית כאב עצבי למשך ימים ואף שבועות. הטיפול מחייב ניטור קפדני עקב הסכנה לתופעות לבביות וכפיוניות. על פי רוב יש לבצע בדיקת אק"ג (אלקטרוקרדיוגרם) (Electrocardiogram, ECG) לפני העירוי הראשון.
- Ketamine או Amantadine במתן תוך-ורידי משמשות כחסמים לקולטני גלוטמאט (חומרים המעלים את רגישות קולטני הכאב), והן נמצאו כטיפול יעיל לכאב עצבי. מתן עירויים מסוג זה מתבצע במרפאות כאב בניטור ולעתים תוך כדי אשפוז. מתן פומי או באמצעות משחות של תכשירים אלה לתקופות ממושכות מביא להפחתת כאב, אך מתונה הרבה יותר.
- מגנזיום במתן תוך-ורידי הוא טיפול מקובל במרפאות הכאב בישראל. יש מעט מאוד פרסומים בספרות הרפואית לגבי יעילות הטיפול, אך הניסיון הקליני בארץ תומך בשימוש בו. המגנזיום מוריד תחושת כאב, מרפה שרירים, מעלה סף הפעלה של עצבים, חוסם קולטני NMDA (N-Methyl-D-Aspartate), אשר מגרים כאב ומרחיבים כלי דם. יש לחזור על הטיפולים אחת למספר שבועות. ניתן להוסיף כדורי מגנזיום כתוסף מזון, אך יש לעקוב אחרי רמות המגנזיום בדם.
טיפולים דרך העור
- משחת ה-Zostrix (Capsaicin) פועלת במנגנון ייחודי להפחתת הכאב. המשחה מכילה את החומר הפעיל מפלפל אדום. כאשר אנו אוכלים פלפל חריף לראשונה, אנו מרגישים צריבה חזקה. לאחר מכן, אם אנו ממשיכים לאכול פלפל חריף, הצריבה הולכת ופוחתת ותחושה של עמימות מופיעה במקומה. ה-Zostrix שנספגת דרך העור או הריריות ומגיעה לקצות העצבים גורמת לריקונם מחומר שנקרא Substance C, הגורם לצריבה בלשון. לאורך זמן ה-Zostrix מרוקנת את החומר מקצות העצבים, ולכן נמנעת תחושת הצריבה והשרפה המאפיינת את הכאב העצבי. הבעיה בשימוש במשחה היא שכדי לקבל את ההקלה בכאב יש לעבור תחילה דרך התקופה של הצריבה. על החולה למרוח את המשחה 2-4 פעמים ביום ולהתמיד בכך.
- מדבקות Lidoderm (Lidocaine Patch 5%) מצופות ב-Lidocaine שהוא חומר אלחוש מקומי. ה-Lidocaine נספג חלקית דרך העור אל סיבי העצב. המדבקה מוצמדת לעור פעם עד פעמיים ביממה למשך 12 שעות ועשויה להפחית כאב ורגישות יתר אצל חולים עם כאב עצבי ממוקם היטב. למרבה הצער, המדבקה אינה משווקת בארץ, אם כי ניתן להשיגה בבתי מרקחת מסוימים המייבאים אותה מחו"ל.
פיזיותרפיה
- פיזיותרפיה היא אבן פינה של הטיפול. הנחיות הטיפול צריכות לכלול שיפור תפקודי בעזרת פעילות גופנית.
טיפולים פולשניים
- ישנו מגוון רחב של טיפולים פולשניים לטיפול בכאב עצבי. הטווח נע בין הזרקות של חומרי הרדמה מקומיים לבין הצורך באבחון של מקור הבעיה, ועד השפעה טיפולית של הפעולה הפולשנית. הזרקה של סטרואידים לעצב הפגוע, בייחוד בתקופה של התפתחות הפגיעה העצבית, ולבסוף פעולות לניתוק או הקטנת ההולכה בעצב על-ידי הזרקה של חומרים הורסי עצבים (Phenol, אלכוהול ו-Glycerol). כיום מתבצעות חסימות עצב גם באמצעות גלי רדיו, אשר יתרונם בכך שהם פוגעים באופן בררני בסיבי העצב מוליכי הכאב, תוך צמצום הפגיעה בתפקודים עצביים אחרים. במקרים מסוימים מבוצעים ניתוחים לשחרור הידבקויות צפקיות, העתקת עצב, ניתוק עצב או הרחקת נוירומה, אשר גם הם עשויים להקל או אף להעלים את הכאב.
- גירוי חוט השדרה (Spinal cord stimulation): הטיפול מבוסס על החדרת מוליכים חשמליים לתעלת עמוד השדרה שדרכן מועבר גירוי חשמלי אל חוט השדרה במגמה לחסום את הולכת הכאב אל המוח. החדרת המוליכים החשמליים דרך העור ללא צורך בניתוח פתוח הופכת את הפעולה לפשוטה ומדויקת, וזאת במחיר של תחלואה נמוכה יחסית. הטיפול ניתן לחולים שבהם לא ניתן להשיג הקלת כאב בדרכים פשוטות יותר. יעילות השיטה נבדקה במספר עבודות רב, והיא כלולה מספר שנים בסל הבריאות בארץ.
- השתלת משאבות Morphine היא אמצעי נוסף לשיכוך כאב מכל סוג, וכאב עצבי בפרט, אשר יוצע רק לחולים שבהם כל האמצעים האחרים לא הועילו. הטיפול מבוסס על החדרת מינונים נמוכים ביותר של אופיואידים, חומרי אלחוש מקומי ותרופות נוספות ישירות אל החלל התת-עכבישי. השתלת המשאבה היא פעולה ניתוחית לכל דבר. מילוי המשאבה מתבצע אחת למספר שבועות תוך התאמת סוג התרופות ומינונן. יצוין שגם טיפול זה כלול בסל הטיפולים בארץ.
| חלוקה על פי מצב חולי | קו ראשון | קו שני | קו שלישי |
|---|---|---|---|
| נוירופתיה סוכרתית (כואבת) |
נוגדי דיכאון טריציקליים |
Lyrica, Neurontin, Duloxetine *יש לנסות את כל התרופות לפני מעבר לקו השלישי |
Venlafaxine, Tramadol, אופיואידים חזקים או שילובים בין התרופות |
| תסמונת העצב המשולש | Carbamazepine, Oxcarbazepine | Neurontin, Lyrica | |
| כאב נוירופתי אצל חולי סרטן (לחולים עם מחלה ממארת פעילה) לא מומלץ שימוש בנוגדי דיכאון טריציקליים כקו ראשון מכיון שהטיטור שלהם איטי וממושך |
Opium עם Neurontin או Lyrica | אופיואידים עם Venlafaxine או Duloxetine | |
| כאב נוירופתי מרכזי | נוגדי דיכאון טריציקליים | Lyrica, Neurontin, Lamotrigine *יש לנסות כל אחת מהתרופות במינון מרבי לפני מעבר לקו השלישי |
אופיואידים בלבד או בשילוב תרופות מקווים קודמים |
| נוירלגיה בתר הרפטית | נוגדי דיכאון טריציקליים, Neurontin, Lyrica ומדבקות Lidocaine |
Valproic acid, Tramadol, אופיואידים | Duloxetine, Venlafaxine |
| תסמונת הכאב האזורית המורכבת | סטרואידים, Calcitonin Salmon, ביספוספונטים, משככי כאב שאינם אופיואידים, אופיואידים על פי עוצמת הכאב |
Lyrica, Neurontin, Duloxetine, בטיטור מהיר למינונים מרביים (מומלץ טיפול בן מספר שבועות) |
|
| נוירופתיות מפושטות (למעט סוכרת ומחלות ממאירות) |
נוגדי דיכאון טריציקליים, Neurontin, Lyrica | Tramadol, Duloxetine, Venlafaxine, Lamotrigine, Carbamazepine |
אופיואידים בלבד או בשילוב תרופות מקווים קודמים |
| כאב נוירופתי משני לפגיעת עצב ממוקדת | נוגדי דיכאון טריציקליים | Lyrica, Neurontin, Duloxetine *יש לנסות את כל התרופות לפני מעבר לקו השלישי |
Venlafaxine, Tramadol, אופיואידים או שילובים |
פרוגנוזה
תסמונת הכאב האזורית המורכבת ברובה אינה ניתנת לריפוי, ולכן הטיפול בה הוא ארוך טווח ופוגע באיכות החיים של הסובלים ממנו.
דגלים אדומים
ביבליוגרפיה
קישורים חיצוניים
המידע שבדף זה נכתב על ידי ד"ר סילביו בריל - מנהל יחידת לטיפול בכאב, המרכז הרפואי ת"א ע"ש סוראסקי, תל אביב; מזכיר האגודה הישראלית לכאב, ד"ר איתי גור-אריה- מנהל יחידת הכאב המרכז הרפואי ע"ש ח' שיבא, תל השומר; יו”ר האגודה הישראלית לכאב,


 כניסה
כניסה  עקבו אחרינו בפייסבוק
עקבו אחרינו בפייסבוק