הבדלים בין גרסאות בדף "מניעת שבץ מוחי בחולים עם פרפור פרוזדורים - Stroke prevention in atrial fibrillation patients"
| שורה 222: | שורה 222: | ||
<blockquote> | <blockquote> | ||
<div style="text-align: left; direction: ltr"> | <div style="text-align: left; direction: ltr"> | ||
| − | + | *Cannon CP, Kohli P. Danger ahead: Watch out for indirect comparisons. J Am Coll Cardiol 2012; 60:738-46. | |
{{הערות שוליים}} | {{הערות שוליים}} | ||
גרסה מ־07:36, 3 בפברואר 2013
ערך זה נמצא בבדיקה ועריכה על ידי מערכת ויקירפואה, וייתכן כי הוא לא ערוך ומוגה.
| מניעת שבץ מוח בחולים עם פרפור פרוזדורים | ||
|---|---|---|
| ' | ||
| יוצר הערך | ד"ר סיון בלוך, פרופ' נחן בורנשטיין | |
לערכים נוספים הקשורים לנושא זה, ראו את דף הפירושים – אירוע מוח
פרפור פרוזדורים הוא גורם סיכון בלחי תלוי לשבץ מוח איסכמי. מהן האפשרויות הטיפוליות בחולים עם פרפור פרוזדורים וכיצד ניחן להפחית אצלם את הסיכון להיארעות של שבץ מוח.
פרפור פרוזדורים הוא הפרעת קצב שכיחה וגורם שכיח לשבץ מוח במנגנון תסחיפי (קרדיואמבולי). היות ששכיחות פרפור פרוזדורים עולה עם הגיל, ולאור העובדה שתוחלת החיים באוכלוסיית העולם המערבי עולה, הרי ששכיחות הפרעת קצב זו הולכת וגוברת וצפויה להמשיך ולעלות אף יותר. שבץ מוח הוא גורם הנכות השכיח ביותר בעולם המערבי ואחד משלושת הגורמים השכיחים ביותר לתמותה. בכ-85 אחוז מהחולים הסובלים משבץ מוח חד, הגורם לשבץ הוא איסכמיה על רקע תרומבוטי או תרומבואמבולי. עוד ידוע כי כ-20 אחוז מתוך מקרי השבץ המוחי האיסכמי נגרמים על רקע פרפור פרוזדורים[1][2].
פרפור פרוזדורים הוא גורם סיכון בלתי תלוי לשבץ מוח איסכמי, ולחולים עם פרפור פרוזדורים סיכון מוגבר פי חמישה ללקות בשבץ מוח איסכמי בהשוואה לאוכלוסיה בעלת מאפיינים דומים אך ללא פרפור פרוזדורים[3].
יש מספר גורמי סיכון המעלים שכיחות פרפור פרוזדורים, כגון השמנת יתר, יתר לחץ דם וסוכרת. שכיחות גורמי סיכון אלה עולה גם כן באוכלוסיה בשנים האחרונות, ומכאן סיבה נוספת לעלייה עתידית בשכיחות של פרפור פרוזדורים[2]. מטרת הסקירה הנוכחית היא לסקור את האפשרויות הטיפוליות בחולים עם פרפור פרוזדורים, על מנת להפחית את הסיכון להיארעות של שבץ מוח.
הערכת חומרת הסיכון
לשם הערכת חומרת הסיכון לשבץ מוח בחולים עם פרפור פרוזדורים שלא על רקע מחלה של מסתמי הלב, קיימות שתי סקאלות שימושיות[4][5]:
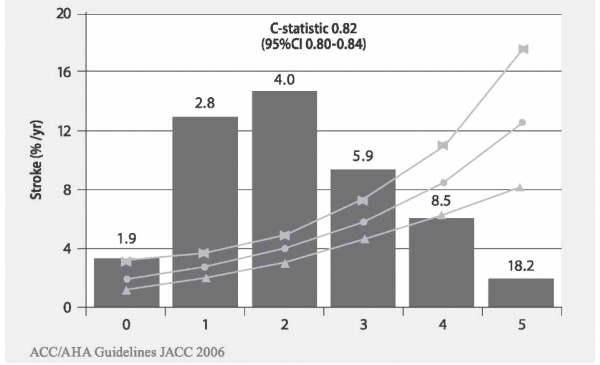
- CHADS2 SCORE - Congestive heart failure, Hypertension, Age over 75y, Diabetes mellitus, Stroke or TIA
(טבלה מסי 1, גרף מס' 1)- CHADS2-VASC SCORE - Congestive heart failure, Hypertension, Age over 75y, Diabetes mellitus, Stroke or TIA, Vascular Disease, Age65-74y, Sex-Female
(טבלה מסי 2, גרף מס' 2)
על פי ההנחיות, ניקוד מעל 1, באחת מהסקאלות הנ"ל, הוא הוריה לטיפול מניעתי בנוגדי קרישה (אנטיקואגולציה). ניקוד השווה ל-1 עדיין שנוי במחלוקת ותלוי בגורם הסיכון המסוים. ניקוד של 0 הוא הוריה לטיפול נוגד צימות טסיות (אנטיאגרגנטי) .
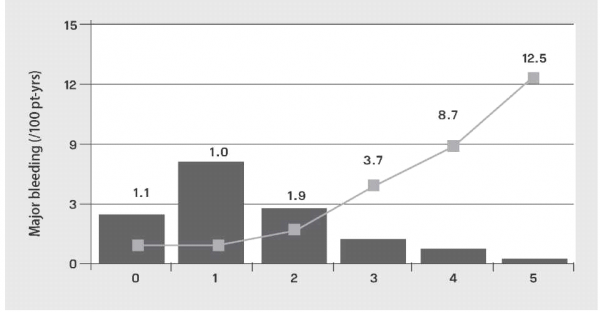
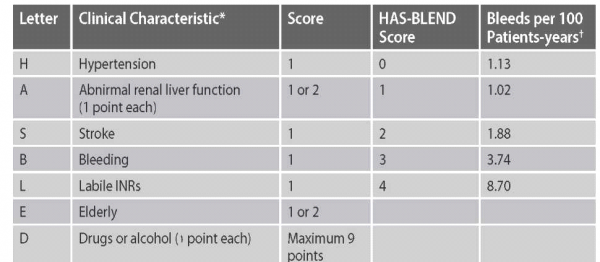
יש לציין כי אירוע איסכמי חולף (TIA) או שבץ מוח מביאים כבר לניקוד של שתי נקודות לפחות. כלומר, הוריה מלאה לטיפול אנטיקואגולנטי. היות שהטיפול בנוגדי קרישה טומן בחובו סיכון לדמם משמעותי, הרי בחישוב סיכון מול תועלת קיימת סקאלה להערכת הסיכון לדימום בחולים הסובלים מפרפור פרוזדורים[6]: HAS-BLED SCORE - Hypertension ,Abnormal liver or renal function, Stroke, Bleeding, Labile INRs, Elderly, Drugs or Alcohol (טבלה מסי 3, גרף מסי 2).
יש לציין כי הסקאלות המוזכרות עברו תיקוף מלא והוכחו כיעילות והן בעלות משמעות ורלבנטיות קלינית בבואנו להחליט על קו הטיפול המניעתי לשבץ מוח בחולים עם פרפור פרוזדורים[4][5][6][7].
| טבלה 1. הערכת הסיכון לשבץ מוח בחולי פרפור פרוזדורים שלא ממקור מסתמי |
|---|
| Stroke-Risk Stratification in non-valvular AF |
| The CHADS2 Score |
| Congestive heart failure (1 point) |
| Hypertension (1 point) |
| Age > 75 years (1 point) |
| Diabetes mellitus (1 point) |
| S2 Stroke or TIA (2 points) |
גרף 1. הסיכון לשבץ מוח כתלות בניקוד CHADS2
| טבלה 2. סקאלה נוספת להערכת הסיכון לשבץ מוח בחולי פרפור פרוזדורים שלא ממקור מסתמי | |
|---|---|
| The CHA2DS2-VASc Score | |
| Congestive heart failure/LV DysFx | 1 |
| Hypertension | 1 |
| Age > 75 years | 2 |
| Diabetes mellitus | 1 |
| Stroke/TIA/TE | 2 |
| Age 65-74 years 1 Vascular disease MI/PAD/aortic plaque 1 Sex female | 1 |
גרף 2. הסיכון לדימום כתלות בסקלת HAS-BLED
קו הטיפול המניעתי
לאור השכיחות העולה של פרפור פרוזדורים והסיכון המוגבר בחולים אלה לשבץ מוח איסכמי, נעשו עבודות מחקריות רבות שבדקו את הטיפולים השונים בהקשר של מניעת שבץ מוח בחולי פרפור פרוזדורים. עבודות אלו היוו את התשתית להנחיות טיפוליות בחולים הללו.
נכון להיום, קומאדין, אנטגוניסט של ויטמין K, הוא תכשיר נוגד הקרישה (אנטיקואגולנט) בעל השימוש הנרחב ביותר. זה מספר עשורים הצטבר ניסיון קליני רב בשימוש בקומאדין, תרופה זולה, עם אפשרות מעקב אחרי טווח הטיפולי של התרופה על ידי בדיקת המעבדה INR, שטווח הטיפולי שלו הוא בין 2.0 ל־3.0, וקיום פרוטוקול מתוקף לנרמול תפקודי הקרישה במידת הצורך בחולים הנוטלים קומאדין. בנוסף, בהסתמך על העבודות השונות, הוכחה יעילותה של תרופה זו במניעת שבץ מוח, עם הפחתת הסיכון היחסי לשבץ מוח בכ־2/3 בהשוואה לפלצבו והפחתת הסיכון היחסי לשבץ מוח בכ־40 אחוז בהשוואה לטיפול באספירין[8]. מספר עבודות גדולות הדגימו יעילות חד משמעית של קומאדין במניעת שבץ מוח איסכמי הן בהשוואה לטיפול באספירין והן בהשוואה לטיפול משולב של נוגדי צימות טסיות ־ אספירין עם קלופידוגרל, שאכן מוריד סיכון לשבץ מוח בהשוואה לטיפול באספירין בלבד, אך פחות יעיל מהטיפול בקומאדין[9].
עם זאת, לשימוש בקומאדין יש מספר מגבלות, ביניהן חלון טיפולי צר, עם אירועים איסכמיים מסכני חיים בטווח של תת פעילות (INR פחות מ־2.0) ודימומים משמעותיים כולל דימומים תוך־ מוחיים בטווח של יתר פעילות (INR מעל 3.0) . איזון חולה בחלון הטיפולי הוא בגדר אתגר, זאת על רקע אינטראקציות של התרופה עם מזון ועם תרופות אחרות (טבלה מסי 4).
| טבלה 4. אינטראקציות בין-תרופתיות של קומאדין |
|---|
| Drug interactions with warfarin |
|
Box 1: Five major mechanisms and examples of drug interactions with warfarin
|
| Juurlink DN. Drug interactions with warfarin: what clinicians need to know. |
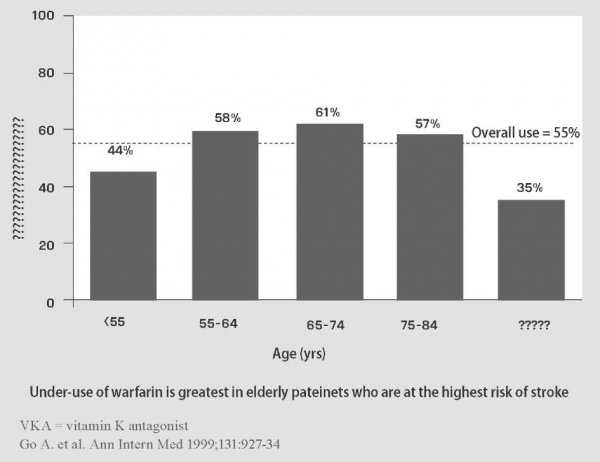
הניטור דורש בדיקות דם תכופות. אפילו במסגרת ניסויים קליניים שבהם קיים ניטור הדוק, זאת בחולים בעלי היענות גבוהה לטיפול ולניטור, הרי שאחוז החולים הנמצאים בטווח החלון הטיפולי של התרופה נע סביב 60 אחוז[10][11] (גרף מסי 3). בשל המגבלות הללו, לא מעט חולים ורופאים נמנעים מהשימוש בקומאדין.
גרף 3. אחוז החולים המטופלים בקומאדין הנמצאים בטווח החלון התרפואיטי לפי קבוצות גיל
בהסתמך על מספר מחקרי סקר ממספר מרכזים בעולם, עולה כי רק כ-50 אחוז מהחולים שיש להם הוריה מוחלטת לטיפול אנטיקואגולנטי אכן מטופלים בקומאדין. מתוך קבוצה זו, רק כ-55 אחוז מהחולים נמצאים בטווח החלון הטיפולי. באוכלוסיית החולים המבוגרים (מעל 80 שנה), שיעור המטופלים נמוך עוד יותר ועומד על כ-40
אחוז[12][13].
המשמעות היא שמספר לא קטן של חולים עם פרפור פרוזדורים לא מטופלים כיאות ונמצאים בסיכון מוגבר ללקות בשבץ מוח איסכמי. בגלל עובדה זו ניסו במשך שנים רבות למצוא תכשירים נוגדי קרישה שיהיו יעילים לפחות כמו הקומאדין ובעלי פרופיל בטיחותי כזה שיהווה חלופה לקומאדין ללא המגבלות שהוזכרו לעיל.
תרופות נוגדות קרישה חדשות
בשנים האחרונות פותחו מספר תרופות נוגדות קרישה (אנטיקואגולנטיות) שיכולות להוות חלופה טובה ויעילה לטיפול בקומאדין (גרף מסי 4).
להלן נסקור את התרופות החדשות, NOACS - New Anticoagulants:
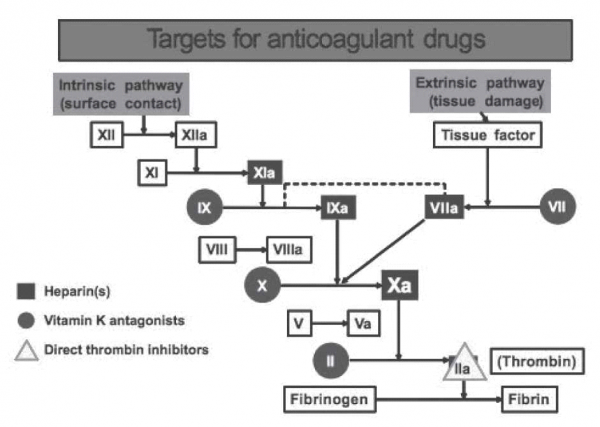
Pradaxa) Dabigatran) - האנטיקואגולנט הראשון שקיבל אישור ה-FDA, פועל במנגנון עיכוב ישיר של התרומבין (גרף מסי 5). התרופה מופרשת בעיקר על ידי הכליות, בעלת מספר אינטראקציות עם תרופות אחרות אך ללא אינטראקציות ידועות עם מזון.
זמן התחלת פעילות מהיר (2-1 שעות), זמן מחצית חיים קצר (17-12 שעות) והיא אינה דורשת ניטור מעבדתי.
מחקר לבדיקת טיפול אנטיקואגולנטי ארוך טווח בדביגטראן בהשוואה לקומאדין בחולים עם פרפור פרוזדורים (RE-LY) השתמש בשיטת מחקר פרוספקטיבי, אקראי, פתוח, סמוי —PROBE ובדק את התוצאים בחולים שקיבלו דביגטראן 110 מ״ג או 150 מ״ג פעמיים ביום אל מול חולים שטופלו בקומאדין[14]. המחקר כלל 18,113 חולים, זמן המעקב הממוצע היה שנתיים. גיל החולים הממוצע היה 71.5 שנים וניקוד ה-CHADAS הממוצע היה 2.1 נקודות. שבץ מוח (מכל סוג) ותסחיף סיסטמי היו תוצא סופי ראשוני. כל דימום משמעותי היה תוצא ראשוני בהקשר של בטיחות התרופה. דביגטראן, בשני המינונים הנבדקים, היה לא פחות יעיל מקומאדין למניעת שבץ מוח ותסחיפים סיסטמיים. המינון הגבוה יותר של דביגטראן נמצא יעיל יותר מקומאדין במניעת שבץ מוח ותסחיפים סיסטמיים. כלומר, דביגטראן בשני המינונים נמצא לא פחות יעיל מקומאדין במניעת שבץ מוח איסכמי, כשהמינון הגבוה יותר היה אף יעיל יותר מקומאדין. שיעור שבץ מוח דימומי היה משמעותית נמוך יותר בשני המינונים של דביגטראן יחסית לקומאדין. השיעור הכללי של דימומים משמעותיים היה נמוך יותר עם המינון הנמוך של דביגטראן, אך לא עם המינון הגבוה יותר.
יש לציין כי שיעור הדיספפסיה היה גבוה יותר בחולים שטופלו בשני המינונים של דביגטראן יחסית לקומאדין. שיעור התמותה לא היה שונה משמעותית באף מינון, בהשוואה לקומאדין, עם נטייה לתמותה פחותה בחולים שטופלו במינון הגבוה. נמצא קשר בין המינון הגבוה של דביגטראן לבין שיעורי התקפי הלב ודימומים משמעותיים ממערכת העיכול[14][15].
נערכה אנליזה נוספת בתת קבוצה של המחקר-חולים שנכנסו למחקר ושעברו בעבר TIA או שבץ מוח - והתוצאות היו דומות לשאר קבוצת המחקר. כלומר, דביגטראן יעיל גם למניעה שניונית של שבץ מוח תסחיפי בחולים עם פרפור פרוזדורים[14][16]. נמצא כי הפרעה בתפקודי כליה מעלה סיכון לדימומים בחולים הנוטלים דביגטראן (במחקר ה-RE-LY לא הכניסו חולים עם creatinine clearance פחות מ-30ml/min).
דביגטראן במינון 150 מ״ג פעמיים ביום (ובמינון של 75 מ״ג פעמיים ביום בחולים עם אי ספיקה כלייתית) אושר במדינות רבות וכן על ידי ה-FDA באוקטובר 2010, למניעה של שבץ מוח וקרישים עורקיים בחולים עם פרפור פרוזדורים[17].
לצורך התאמת מינון התרופה יש לבצע בדיקת תפקודי כליות לפני התחלת הטיפול התרופה. מומלץ לעקוב אחרי תפקודי כליות בזמן השימוש בדביגטראן.
Xareito) Rivaroxaban) - פועל במנגנון עיכוב ישיר של פקטור Xa (גרף מסי 5). התחלת פעולה תוך כשלוש שעות מהמתן, עם זמן מחצית חיים של 10-6 שעות. 1/3 מהתרופה מופרש בשתן ללא שינוי, 2/3 עוברים קודם פירוק בכבד דרך מספר איזו-אנזימים, ביניהם CYP3A4. על רקע הפירוק בכבד, יש מספר אינטראקציות בין-תרופתיות. בחולים עם ccr קטן ^30ml/min יש הוריית נגד לתרופה.
במחקר אקראי כפול סמיות בחולים עם פרפור פרוזדורים, ללא הפרעות במסתמים (ROCKET AF) בוצעה השוואה בין ריברוקסבאן במינון של 20 מ״ג ליום (או במינון של 15 מ״ג ליום, בחולים עם 30-49ml/min creatinine clearance) לבין קומאדין[18]. המחקר כלל 14,264 חולים, זמן המעקב הממוצע היה 1.94 שנים. הגיל הממוצע היה 73 שנים, CHADAS ממוצע היה גבוה יחסית למחקרים האחרים - 3.47. מחקר ה-ROCKET-AF נבדל משאר המחקרים בנושא כיוון שהדרישה במחקר הייתה ש-90 אחוז מהחולים יהיו בעלי יותר משלושה גורמי סיכון וסקולריים או אירוע תרומבואמבולי בעבר. התוצא הראשוני היה שבץ מוח או אירוע תסחיפי סיסטמי. התוצאות הדגימו כי ריברוקסבאן אינו פחות יעיל מקומאדין. בהפסקת התרופה נצפתה עלייה בשיעור אירועים תסחיפיים. מבחינת פרופיל בטיחות, שיעור הדימומים הכללי בשתי קבוצות המחקר היה דומה, אולם שיעור הדימומים שהביאו לתמותה היה מעט נמוך יותר בקבוצת החולים שטופלה בריברוקסבאן, בעיקר בשל הירידה בשיעור שבץ מוח דימומי ושיעור דימומים תוך מוחיים. שיעור דימומים ממערכת העיכול (עליונה, תחתונה, אזור רקטלי) היה גבוה יותר בקבוצת החולים שטופלה בריברוקסבאן, כולל דימומים שגרמו לירידת המוגלובין או/וצורך בטיפול במנות דם.
בגמר מחקר ROCKETS, שיעור שבץ מוח איסכמי ו/או תסחיף סיסטמי היה גבוה יותר בקרב החולים שהפסיקו את הריברוקסאן ועברו לטיפול בקומאדין. יש לציין כי בחולים אלה לקח יותר זמן מהממוצע להגיע 7-INR טיפולי, תחת טיפול בקומאדין. בנוסף, מדובר בחולים בעלי גורמי סיכון מרובים יותר יחסית לשאר המחקרים וכן הגיל הממוצע היה גבוה יותר במחקר זה[17][18].
Eiiquis) Apixaban) - תכשיר מעכב ישיר של פקטור Xa (גרף מסי 5) , בעל זמינות ביולוגית גבוהה, בעל זמן מחצית חיים 15-8 שעות ורק 1/4 ממנו מופרש דרך הכליות. נבדק מחקרית בשני ניסויים קליניים, הראשון AVERROES שבדק את האפיקסבאן כנגד אספירין למניעת שבץ מוח, מחקר כפול סמיות שכלל 5,599 חולים עם פרפור פרוזדורים כרוני שלא יכלו לקבל אנטיקואגולנטים ממשפחת אנטגוניסטים לויטמין K. החולים חולקו לשתי קבוצות, קבוצה אחת טופלה באפיקסבאן 5 מ״ג פעמיים ביום (ו-2.5 מ״ג פעמיים ביום במבוגרים, בבעלי מסת גוף ירודה או בחולים עם תפקודי כליה מופרעים) וקבוצה שנייה טופלה באספירין (81 או 324 מ״ג). הגיל הממוצע של החולים היה 70 שנה. המחקר הופסק לאחר מעקב של 1.1 שנים, בשל עליונות ברורה של האפיקסבאן במניעת שבץ מוח או תסחיפים סיסטמיים[19].
שיעור הדימומים היה דומה בין שתי הקבוצות. בקבוצת החולים שטופלו באפיקסבאן סבלו פחות מתופעות לוואי ופחות הפסיקו טיפול. למעשה, מחקר זה הדגים את בטיחות ויעילות השימוש בטיפול באפיקסבאן[17][19].
מחקר שני השווה אפיקסבאן כנגד קומאדין בחולים עם פרפור פרוזדורים (ARISTOTLE). מחקר זה היה אקראי, כפול סמיות והשווה מתן אפיקסבאן 5 מ״ג פעמיים ביום כנגד קומאדין[20].
המחקר כלל 18,201 חולים עם פרפור פרוזדורים. CHADAS ממוצע היה 2.1 וזמן המעקב הממוצע היה 1.8 שנים. גיל ממוצע 70 שנה. מתוצאות מחקר ARISTOTLE עולה כי הטיפול באפיקסבאן בהשוואה לקומאדין בחולים עם פרפור פרוזדורים ולפחות גורם סיכון אחד נוסף לשבץ מוח יעיל יותר במניעת שבץ מוח איסכמי. בקבוצת החולים שנטלה אפיקסבאן נמצאה ירידה משמעותית בשיעור שבץ מוח או תסחיף סיסטמי ב-21 אחוז, ירידה משמעותית בשיעור דימומים (עם דגש על ירידה משמעותית במספר הדימומים התוך-מוחיים) ב-31 אחוז, וירידה בשיעור התמותה ב-11 אחוז, בהשוואה לקבוצת החולים שנטלו קומאדין. נתונים אלה אומתו בכל תת אוכלוסיות המחקר.
השוואה בין התכשירים
כל שלוש התרופות הנ״ל שנחקרו הראו פחות דימומים תוך מוחיים ופחות שבץ מוח דימומי, בהשוואה לקומאדין[17][21].
דביגטראן במינון 150 מ״ג פעמיים ביום הייתה התרופה היחידה שהדגימה שיעור נמוך יותר של שבץ מוח איסכמי, בהשוואה לקומאדין, והראתה עליונות על קומאדין במניעת שבץ מוח איסכמי. בנוסף, שלוש התרופות האנטיקואגולנטיות בעלות מספר יתרונות על פני הקומאדין:
- שלושתן בעלות פרופיל פרקמקוקינטי יציב.
- לשלושתן פחות אינטראקציות בין-תרופתיות.
- שלושתן נטולות אינטראקציות עם מרכיבי מזון.
- בשלושתן לא נדרש ניטור מעבדתי.
- שלוש התרופות הדגימו יעילות לא פחותה מזו של הקומאדין אך לעומת זאת הדגימו פרופיל בטיחות טוב יותר.
כמו בכל התרופות האנטיקואגולנטיות, דימומים עדיין מהווים בעיה, אך שיעור הדימום התוך-מוחי יורד משמעותית. שימוש בדביגטראן ואפיקסבאן דורש מתן פעמיים ביום, בעוד ריברוקסבאן ניתן לקחת פעם ביום. במחקר ה-RE-LY הודגם שיעור גבוה יותר של דימומים בדרכי העיכול במינון הגבוה ושיעור גבוה של דיספפסיה בשני המינונים של דביגטראן.
הנחיות קליניות
ה-FDA אישר דביגטראן במינון 150 מ״ג פעמיים ביום ובמינון של 75 מ״ג פעמיים ביום לחולים עם הפרעה משמעותית בתפקודי הכליות (מינון שלא נבדק במחקר ה-RE-LY).
האיגוד האירופאי לקרדיולוגיה ממליץ על דגיבטראן במינון 150 מ״ג פעמיים ביום לחולים עם HAS-BLED score בין 0 ל-2 ועל מינון של 110 מ״ג פעמיים ביום בחולים עם HAS-BLED score שווה/ גדול מ-3.
ריברוקסבאן קיבל לאחרונה אישור ה-FDA עם אזהרה לעלייה בסיכון לשבץ מוח בהפסקת התרופה. אפיקסבאן נמצא בשלבי אישור סופיים.
בסקירה עדכנית שפורסמה ב-16 באוגוסט 2012 בוצעה השוואה בלתי ישירה בין שלוש התרופות האנטיקואגונטיות החדשות, זאת בהסתמך על תוצאות שלושת המחקרים (,RE-LY , ARISTOTLE ROCKET-AF). בהשוואה המתייחסת להפחתת הסיכון לשבץ מוח ולתסחיף סיסטמי עלו ההמצאים הבאים:
- לא נמצא הבדל בין אפיקסבאן לדביגטראן בשני המינונים שנבדקו.
- לא נמצא הבדל בין אפיקסבאן לריברוקסבאן.
- דביגטראן 150 מ״ג נמצא יעיל יותר מריברוקסבאן ב-26 אחוז. כמו כן, דביגטראן בהשוואה לריברוקסבאן, הפחית סיכון לשבץ דימומי ב-56 אחוז ולשבץ שאינו גורם נכות ב-40 אחוז.
בהשוואה שמתייחסת להפחתת הסיכון לדימומים:
- אפיקסבאן מפחית את הסיכון ב-26 אחוז בהשוואה לדביגטראן 150 מ״ג, וב-34 אחוז בהשוואה לריבורוקסבאן.
- דביגטראן 110 מ״ג מפחית את הסיכון ב-23 אחוז בהשוואה לריבורוקסבאן.
- לא נמצא הבדל משמעותי בסיכון לדימומים בהשוואה בין אפיקסבאן לדביגטראן 110 מ״ג כמו גם בין דביגטראן 150 מ״ג לבין ריבורוקסבאן.
בהשוואה בין התרופות החדשות כקבוצה אחת לבין קומאדין, התרופות החדשות נמצאו מפחיתות הסיכון לשבץ מוח או לתסחיף סיסטמי ב-21 אחוז, לשבץ מוח ב-23 אחוז, לשבץ דימומי ב-53 אחוז ולדימומים משמעותיים ב-13 אחוז. כמו כן, תרופות אלו נמצאו כמפחיתות הסיכון לתמותה ב-12 אחוז, זאת בהשוואה לקומאדין.
תוצאות ההשוואה הבלתי ישירה זו תומכות בעדיפות לשימוש באנטיקואגולנטים חדשים על פני קומאדין, אך חשוב להדגיש את המגבלות של שיטת השוואה בלתי ישירה[22].
ניתן אפוא לסכם ולומר כי כיום יש בידינו תרופות אנטיקואגולנטיות חדשות שיכולות להוות חלופה לטיפול בקומאדין. עבור החולה הספציפי, יש לעשות המרב על מנת להתאים את התרופה המתאימה ביותר עבורו תוך התחשבות במכלול גורמי הסיכון הקרדיווסקולריים כמו גם את הסיכון לדימום.
סגירת האוזנית של העלייה השמאלית (Percutaneus Left Atria; Appenage Obliteration)
מבין החולים עם פרפור פרוזדורים שיפתחו שבץ מוח, ביותר מ-90 אחוז מהמקרים השבץ המוחי הוא תוצאה של תסחיף שמקורו מהאוזנית של העלייה השמאלית (LAA).
קיימת אפשרות של סגירת האוזנית על ידי device מיוחד שהוא מעין ״כלוב״ הבנוי מ-nitinol ומכוסה בממברנה מיוחדת, מוחדר על ידי קטטר לאוזנית העלייה השמאלית, מתרחב לגודל האוזנית וחוסם אותה ובכך מונע היווצרות קריש דם באוזנית. יש שני devices בשימוש: Amplatzer-I Watchman occlude plug.
שתי עבודות מרכזיות הדגימו יעילות הפרוצדורה. במחקר PLAATO הפרוצדורה בוצעה ב-73 חולים עם פרפור פרוזדורים שלא יכלו ליטול קומאדין ובמעקב של חמש שנים נמצא שיעור היארעות שבץ מוח פחות מהצפוי, בהסתמך על CHADS2 score.[23] מחקר נוסף היה ה-PROTECT AF שכלל 707 חולים, מתוכם 1/3 טופלו בקומאדין ו-2/3 עברו את הפרוצדורה של הכנסת device לעלייה. התוצאות הדגימו יותר סיבוכים סביב הפרוצדורה, אך מבחינת יעילות מניעת שבץ מוח ^device נמצא כבעל יעילות דומה לזו של הקומאדין[24].
כיום מצטבר ניסיון בטיפול בסגירת האוזנית באמצעות טיפול צנתורי באותם חולים שמסיבות שונות אינם יכולים או קיימת הוריית נגד למתן נוגדי קרישה. זוהי חלופה אפשרית בחולים אלה שאין להם הגנה תרופתית כנגד היארעות שבץ מוח תסחיפי מהלב בנוכחות פרפור פרוזדורים.
לסיכום, קבוצת התרופות האנטיקואגולנטיות החדשות יעילות לפחות כמו קומאדין במניעת אירועים תסחיפיים למוח וגרימת שבץ מוח
ביבליוגרפיה
- Cannon CP, Kohli P. Danger ahead: Watch out for indirect comparisons. J Am Coll Cardiol 2012; 60:738-46.
- ↑ Miasaka Y, Barnes ME, Gersh BJ, Cha SS, Bailey KR, Abhayaratna WP, et al. Secular trends in incidence of atrial fibrillation in Olmsted Country, Minnesota, 1980 to 2000, and implication on the projection for future prevalence. Circulation.2006;114:119-125.
- ↑ 2.0 2.1 Go A.S. The epidemiology of atrial fibrillation in eldery persons; the tip of the iceberg. Am J Geriatr Cardiol.2005;14:56-61.
- ↑ Wolf PA, Abbott RD, Kannel WB. Atrial fibrillation as an independent risk factor for stroke;the Framingham study. Stroke.1991;22:983-988.
- ↑ 4.0 4.1 Wann L. S, Curtis A.B, January C.T, Ellenbogen K.A, Lowe J.E., Mark Estes M et al. 2011 ACCF/AHA/HRS Focused Update on the Management of Patients With Atrial Fibrillation (Updating the 2006 Guideline): Title and subTitle Break. A Report of the American College of Cardiology Foundation/American Heart Association Task Force on Practice Guidelines. J Am Coll Cardiol. 2011;57(2):223-242.
- ↑ 5.0 5.1 Lip GY, Frison L, Halperin JL, Lane DA. Identifying patients at high risk for stroke despite anticoagulation: a comparison of contemporary stroke risk stratification schemes in an anticoagulated atrial fibrillation cohort. Stroke. 2010;41(12):2731-8.
- ↑ 6.0 6.1 Pisters R, Lane DA, Nieuwlaat R, de Vos CB, Crijns HJ, Lip GY. A novel user-friendly score (HAS-BLED) to assess 1-year risk of major bleeding in patients with atrial fibrillation: the Euro Heart Survey. Chest. 2010 ; 138(5): 1093-100.
- ↑ Wrigley BJ, Shantsila E, Lip GY. Percutaneous coronary intervention in anticoagulated patients and balancing the risk of stroke and bleeding: to interrupt or not to interrupt? Chest. 2010;138(4):771-4.
- ↑ Hart RG, Pearce LA, Aguilar MI. Meta-analysis; Anthitrombotic therapy to prevent stroke in patients who have nonvalvular atrial fibrillation. Ann Intern Med. 2007;146:857-867.
- ↑ Connolly SJ, Pogue J, Hart RG, Hohnloser SH, Pfeffer M, Chrolavicius S, Yusuf S. Effect of clopidogrel added to aspirin in patients with atrial fibrillation. N Engl J Med. 2009;360(20):2066-2078.
- ↑ van Walraven C, Jennings A, Oake N, Fergusson D, Forster AJ. The effect of study setting on anticoagulation control: a systematic review and metaregression. Chest. 2006;129;1155-1166.
- ↑ Baker WL, Cios DA, Sander SD, Coleman CI. Meta-analysis to assess the quality of warfarin control in atrial fibrillation patients in the United States. J Manag Care Pharm. 2009;15(3):244-52.
- ↑ Go A.S., Hylek E.M., Borowsky L.H, Phillips K.A., Selby J.V., Singer D.E. Warfarin Use among Ambulatory Patients with Nonvalvular Atrial Fibrillation: The AnTicoagulation and Risk Factors in Atrial Fibrillation (ATRIA) Study. Ann Intern Med. 1999;131(12):927-934. Ann Inten Med.1999;131:927-934.
- ↑ Birman-Deych E, Radford MJ, Nilasena DS, Gage BF. Use and effectiveness of warfarin in Medicare beneficiaries with atrial fibrillation. Stroke. 2006;37(4):1070-1074.
- ↑ 14.0 14.1 14.2 Connolly S.J, Ezekowitz M.D, Yusuf S, Eikelboom J, Oldgren J, Parekh A et al. Dabigatran Versus Warfarin in Paitents with Atrial Fibrillation. N Engl J Med. 2009;361(12):1139-1151.
- ↑ Uchino K, Hernandez AV. Dabigatran association with higher risk of acute coronary events: meta-analysis of noninferiority randomized controlled trials. Arch Intern Med. 2012;172(5):397-402.
- ↑ Gage B.F. Can We Rely on RE-LY. N Engl J Med. 2009;361(12):1200-1202.
- ↑ 17.0 17.1 17.2 17.3 Katsnelson M, Sacco R.L., Moscucci M. Progress for stroke prevention with Atrial Fibrillation. Emerge of Alternative Oral Anticoagulats. Stroke 2012;43:1189-1185.
- ↑ 18.0 18.1 Manesh R. Patel et al (ROCKET AF investigators). Rivaroxaban Versus Warfarin in Nonvalvular Atrial Fibrillation. N Engl J Med. 2011;365(10):;883-891.
- ↑ 19.0 19.1 Connolly SJ, Eikelboom J, Joyner C, Diener HC, Hart R, Golitsyn S et al. AVERROES Steering Committee and Investigators. ,Apixaban in patients with atrial fibrillation. N Engl J Med.2011;;364(9):806-17.
- ↑ Granger C.B, Alexander J, McMurray J.J.V , Lopes R.D, Hylek E.M, Hanna M et al. (ARISTOTLE investigators) . Apixaban versus Warfarin in Patients with atrial fibrillation. N Engl J Med 2011;361(11):981-992.
- ↑ Del Zoppo G.J., Eliasziw M. New Options in Anticoagulation for Atrial Fibrillation. N Engl J Med.2011;365(10):952-952.
- ↑ Lip GY, Larsen TB, Skj0th F, Rasmussen LH. Indirect comparisons of new oral anticoagulant drugs for efficacy and safety when used for stroke prevention in atrial fibrillation. J Am Coll Cardiol 2012; 60:738-46.
- ↑ Nakai T, Lesh MD, Gerstenfeld EP, Virmani R, Jones R, Lee RJ. Percutaneous Left Atrial Appendage Occlusion (PLAATO) for Preventing Cardioembolism. Circulation. 2002; 105: 2217-2222.
- ↑ Holmes DR, Reddy VY, Turi ZG, Doshi SK, Sievert H, Buchbinder M et al. Percutaneous closure of the left atrial appendage versus warfarin therapy for prevention of stroke in patients with atrial fibrillation: a randomised non-inferiority trial. Lancet. 2009;374(9689):534-42.
קישורים חיצוניים
המידע שבדף זה נכתב על ידי ד"ר סיון בלוך, פרופ' נחן בורנשטיין


 כניסה
כניסה  עקבו אחרינו בפייסבוק
עקבו אחרינו בפייסבוק