פורין - Furin
| מדריך בדיקות מעבדה | |
| פורין | |
|---|---|
| Furin | |
| שמות אחרים | PACE (Paired basic Amino acid Cleaving Enzyme) , FUR (FES Upstream Region) ,PCSK3 ,SPC1. |
| מעבדה | כימיה בדם |
| תחום | הפיכת פרו-הורמונים וחלבונים ממצב לא פעיל למצב פעיל. |
| טווח ערכים תקין | ממוצע במבוגרים בריאים - 0.04 ננוגרם/מ"ל. |
| יוצר הערך | פרופ' בן-עמי סלע |
מטרת הבדיקה
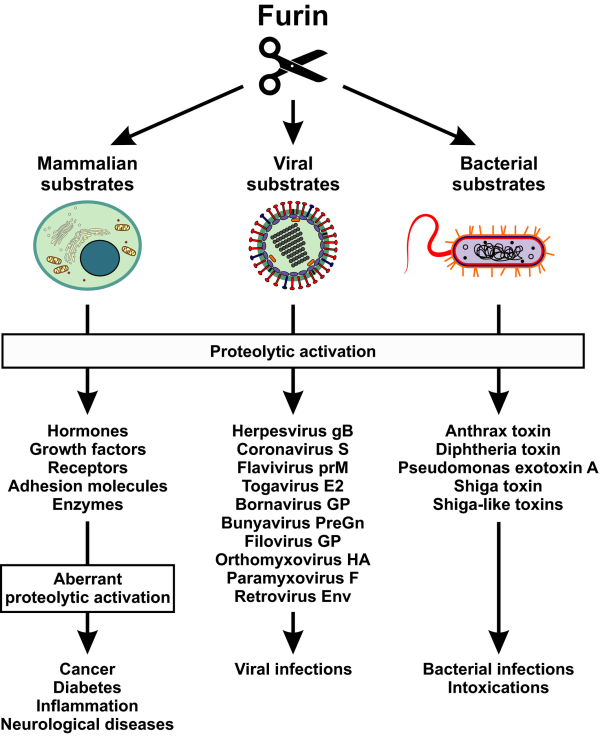
בחינת השפעול של הורמונים ופפטידים בממברנה של חיידקים ונגיפים פתוגניים למולקולות פעילות.
כללי
פורין הוא פרוטאז המקודד על ידי הגן FURIN המשופעל על ידי מצע. מספר חלבונים הם בלתי פעילים כאשר הם מסונתזים, וחייבים להיות מבוקעים ולאד מספר מקטעים כדי להפוך לפעילים. פורין מבקע מקטעים אלה ומשפעל את החלבונים (Kiefer וחב' ב-DNA and Cell Biol משנת 1991, Roebroek וחב' ב-EMBO J משנת 1986, ו-Lin וחב' ב-Blood Cells, Mol & Dis משנת 2008). השם furin נקבע כיוון שהוא היה באזור של אונקוגן הידוע כ-FES. הגן היה היה ידוע כ-FUR (או FES Upstream Region), ומכאן השם furin. אנזים זה ידוע גם כ-PACE (או Paired basic Amino acid Cleaving Enzyme). כחבר במשפחת S8, פורין הוא פפטידאז דמוי-subtilisin.
הגילוי של פורין
בשנת 1990 הזיהוי של furin כ-proprotein convertase (או PC) הראשון ביונקים הביא לסיום של מחקר שנמשך 25 שנה אחר אנזימים ביונקים המקטלזים את הבשלות הפרוטאליטית של פרו-הורמונים ושל פרו-חלבונים (Zhou וחב' בJ Biol Chem משנת 1999, ו-Seidah ו-Chrétien ב-Brain Res משנת 1999). החיפוש אחר PCs החל לאחר מחלקיו הסמינליים של Donald Steiner בשנת 1967 (Steiner וחב' ב-Science משנת 1967, ו-Seiner וחב' ב-Recent Prog Horm Res משנת 1969), שהראה לראשונה שהורמונים פפטידיים מבוקעים מפרו-הורמונים באתרים של חומצות אמינו בסיסיות (לדוגמה, Lys–Arg↓– ו- –Arg–Arg↓). מחקרים אלה היו מהפכניים ממש כמו אלה של Krebs ו-Fisher, שהראו שזרחון של חלבון הוא שינוי אוניברסלי בהעברת איתותים. מחקרים באותה תקופה של Chrétien ו-Choh Hoh Li ב-Canad J Biochem משנת 1967 על הקשרים המבניים בין β-melanocyte stimulating hormone (להלן β-MSH), γ-lipotropin (γ-LPH), תת-קבוצות של פפטידים הנובעים מפרו-הורמון בבלוטת ההיפופיזה הידוע כ-proopiomelanocortin (להלן POMC), סיפקו את המפתחות הראשונים לרעיון עיבוד הפרו-חלבונים. יחדיו, מחקרים אלה יצרו את הבסיס למחקרים מאוחרים יותר ב-20 השנים הבאות, שהראו שלמעשה כל ההורמונים הפפטידיים כגון growth hormone ומולקולות הספיחה הבינתאית, כמו גם רבים מהטוקסינים הבקטריאליים וכן גליקופרוטאינים של מעטפת הנגיפים, עוברים תהליך דומה ליצירת מולקולות פעילות ביולוגית. אך האנזימים המקטלזים ריאקציות אלו זוהו רק בשנת 1984, כאשר האנדו-פרוטאז של שמרים הידוע כ-kexin או Kex2 בודד (Julius וחב' ב-Cell משנת 1984).
תפקוד
החלבון המקודד על ידי גן זה שייך למשפחת subtilisin-like proprotein convertase. החברים במשפחה זו הם proprotein convertases ההופכים קודמנים בלתי פעילים של חלבונים לתוצרים פעילים ביולוגית. אנזים זה הוא serine endoprotease התלוי בסידן שיכול לבקע ביעילות חלבונים קודמנים באתרים של חומצות אמינו בסיסיים. חלק מהמצעים הם: proparathyroid hormone, הקודמן של transforming growth factor beta 1, פרו-אלבומין, pro-beta-secretase, תת-יחידה בטא של pro-nerve growth factor, גורם von Willebrand ו-membrane type-1 matrix metalloproteinase. פרו-פרוטאין קונברטאז דמוי-פורין פועל בעיבוד של RGMc (הידוע גם כ-homojuvelin), שהוא גן הכרוך במפגע של יתר-ברזל חמור הידוע כ-juvenile hemochromatosis. קבוצות המחקר של Ganz ושל Rotwein הראו ש-proprotein convertases (PPC) דמויי-פורין אחראיים להיפוך של HJV שמשקלו המולקולרי 50 קילו-דלטון לחלבון שמשקלו המולקולרי 40 קילו-דלטון עם קצה C-טרמינלי קטום, תוך ביקוע ליד RNRR בסיסי משומר. זה מרמז על מנגנון פוטנציאלי ליצור HJV/hemojuvelin (או s-hemojuvelin)שמוצאים בדם של מכרסמים ושל האדם (Kuninger וחב' ב-BMC Biochemistry משנת 2008, ו-Duckert וחב' ב-Protein Engineer Design Select משנת 2004). המצעים של פורין, ואתרי הביקוע על ידי פורין, יכולים להיות צפויים על ידי שתי שיטות ביו-אינפורמטיביות: ProP (לTian וחב' ב-Scient Rep משנת 2012,) ו-PiTou (Hellenberger וחב' ב-Nature Rev Mol Cell Biol משנת 1992).
התכונות הביוכימיות של מבנה המקטע של פורין
פורין הוא חלבו טרנס-ממברנלי type 1 נפוץ בעל 794 חומצןת אמינו הנמצא בכל בעלי החוליות ואף בחסרי חוליות (Seidah וחב' ב-Ann NY Acad Sci משנת 1998, ו-Thacker ו-Rose ב-Bioessays משנת 2000). המקטע הגדול הלומנלי/חוץ תאי שלו הוא בעל הומולוגיה עם אזורים דומים של חברים אחרים של משפחת ה-proprotein convertase, השייכת לתת-משפחת ה-subtilisine של serine endoproteases. הדמיון הגדול ביותר של הרצף נמצא במקטע הקטליטי דמוי-subtiisine, שיירי האספרטאט, ההיסטידין והסרין היוצרים את הטריאדה הקטליטית משומרים באופן ניכר, והמקטעים הקטליטיים של PCs אחרים זהים ב-54-70% לפורין. בנוסף לפפטיד הסיגנל מכוון את הטרנסלוקציה של הפרו-אנזים לתוך הרטיקולום האנדופלזמטי, פורין וה-PCs האחרים מכילים פרו-מקטעים המאוגפים על ידי ביקוע הפפטידאז הסיגנלי בצד הטרמינל האמיני ועל ידי חומצות האמינו הבסיסיים המשומרים המכילים את אתר הביקוע האוטו-פרוטאוליטי בצד הקרבוקסי-טרמינלי. הפרו-מקטע החיוני הוא בעל תפקיד קריטי בקיפול, בשפעול ובטרנספורט של PCs, וכן בוויסות של פעילות PC. פורין ו-PCs אחרים מכילים גם מקטע P משומר, החיוני לפעילות האנזים, למודולציה של ה-pH וכן לדרישות לסידן (Zhou וחב' ב-J Biol Chem משנת 1998). מקטע P זה חסר באנזימים דומים בחיידקים. פורין אינו ה-PC היחיד הכרוך בפרוגנוזה גרועה בסוגי סרטן רבים. ההומולוג PACE4 של פורין, מוגבר בסרטן השד (Cheng וחב' ב-Int J Cancer משנת 1997), והביטוי של PC זה מגביר בעכברים את החודרנות של קרצינומת תאי קשקש, על ידי הפיכתם ליותר אגרסיביים, עם התמיינות פחותה (Mahloogi וחב' ב-Carcinogenesis משנת 2002). המשקל המולקולרי של פורין -104 קילו-דלטון.
משמעות קלינית
פורין הוא אחד הפרוטאזות האחראיות לביקוע הפרוטאליטי של הרב-חלבונים הקודמנים של מעטפת HIV ללgp160 ל-gp120 ול-gp41 לפני ההתכנסות של נגיף (Thomas ב-Protein traffic embryogen dis משנת 2002). פרוטאז זה משחק גם תפקיד בהתפתחות התהליך הסרטני. השימוש ב-polyadenylation חלופי מיוחס אף הוא לגן FURIN. פורין מועשר ב-Golgi apparatus, שם הוא פועל לבקע חלבונים אחרים לצורתם הבשלה והפעילה (Coutard וחב' ב-Antiviral Res משנת 2020). פורין מבקע חלבונים ליד רצף של חומצות אמינו בסיסיות (Arg-X-(Arg/Lys)). בנוסף לעיבוד של חלבונים תאיים קודמנים, פורין גם משמש למספר פתוגנים. לדוגמה, חלבוני המעטפת של נגיפים כגון HIV, שפעת ו-dengue, מספר פילו-נגיפים כולל ebola ונגיף marburg, וחלבון ה-spike של SARS-CoV-2 (לHoffmann וחב' ב-Mol Cell משנת 2020, ו-Shiryaev וחב' ב-J Biol Chem משנת 2007). הטוקסין של anthrax, האקסו-טוקסין של pseudomonas ונגיף פפילומה חייבים להיות מטופלים על ידי פורין במהלך חדירתם לתוך תאי הפונדקאי. מעכבים של פורין נחשבים מועמדים תרפויטיים לטיפול בהדבקה על ידי anthrax (Wang וחב' ב-J Biol Chem משנת 2023). פורין מווסת על ידי כולסטרול ועל ידי המצע. כאשר רמת כולסטרול גבוהה, פורין מופנה לכיוון הגנגליוזיד GM1. כאשר רמת כולסטרול נמוכה, פורין יכול לפעול על מצעים רבים (Pesu וחב' ב-Nature משנת 2008). הביטוי של פורין בתאי-T נדרש לשמירה של עמידות לחיסון היקפי (Wan וחב' ב-Cell משנת 2008).
וירולנטייות
התפקיד הרחב של פורין בשפעול של טוקסינים בקריאליים דומה לתפקידו בשפעול של מספר נגיפים פתוגניים, שרבים מתוכם כולל נגיף שפעת העופות, HIV-1, נגיף החצבת ו-RSV, מבטאים גליקופרוטאינים ממברנליים החייבים להיבקע על מנת ליצור גליקופרוטאינים בשלים במעטפת הנגיף (Molloy וחב' ב- Trends Cell Biol משנת 1999). לדוגמה, עיבוד של gp160 של הנגיף HIV-1 חושף את הקצה האמיני gp41 של פפטיד האיחוי הנכלל בתוך הקומפלקס המעטפתי הטרימרי gp120/g41. לא ברור אם furin או אחד מה-PCs האחרים הוא ה-gp160 convertase בתנאי in vivo (לMoulard ו-Decroly ב-Biochim Biophys Acta משנת 2000). תאי lovo שחסרים פורין, מעבדים את HIV-1 gp160 (Ohnishi וחב' ב-J Virol משנת 1994). אף-על-פי-כן מעכבי פורין חוסמים את העיבוד של HIV-1 gp160, ובתגובה את הייצור של HIV-1 אינפקטיבי. פורין מבקע HIV-1 gp160 בקצה הקרבוקסי טרמינלי ברצף Arg–Glu–Lys–Arg–↓. שייר ה-P3 glutamate בנקודת ביקוע זו מפחיתה את היעילות של העיבוד על ידי פורין. מוטציה באתר הביקוע שהופכת אותו לרצף חומצות אמינו בסיסיות (–Arg–Arg–Lys–Arg–↓), מגבירה את תהליך הביקוע על ידי פורין (Binley וחב' ב-J Virol משנת 2002).
החשיבות של פורין בווירולנטיות הפתוגנית באה לביטוי בנגיפים אחרים, כולל נגיף Ebola. לדוגמה, נגיף Ebola Zaire הפתוגני מאוד, וגזעי Ivory Coast הגורמים לחום ולדימום מאוד מסיביים, ההורגים 90% מהנדבקים על ידיהם, מכילים אתר קונצנזוס של פורין בגליקופרוטאין המעטפת שלהם (Volchkov וחב' ב-Proc Natl Acad Sci USA משנת 1998), אך בניגוד לכך, הגליקופרוטאין של הנגיף המתון יותר יחסית, Ebola Reston, אינו מכיל את אתר הקונצנזוס של פורין,ואינו פתוגני באדם.
הוראות לביצוע הבדיקה
הדם נלקח במבחנה כימית (פקק אדום או צהוב) אך ניתן לקחתו במבחנת ספירת דם (EDTA, פקק בצבע סגלגל). לאחר הסרכוז יש להקפיא את הדם בשליחתו למעבדה. הבדיקה מתבצעת בשיטת ELISA או ב-immunoassay.
ראו גם
המידע שבדף זה נכתב על ידי פרופ' בן-עמי סלע, המכון לכימיה פתולוגית, מרכז רפואי שיבא, תל-שומר;
החוג לגנטיקה מולקולארית וביוכימיה, פקולטה לרפואה, אוניברסיטת תל-אביב (יוצר הערך)


 כניסה
כניסה  עקבו אחרינו בפייסבוק
עקבו אחרינו בפייסבוק