בדיקת חומצה טריכלורואצטית בשתן
| מדריך בדיקות מעבדה | |
| בדיקת חומצה טריכלורואצטית בשתן | |
|---|---|
| trichloroethanoic acid | |
| 250 פיקסלים | |
| מעבדה | כימיה בשתן |
| תחום | בדיקות טוקסיות |
| טווח ערכים תקין | תוצאה שלילית – מעידה על היעדר חשיפה לכימיקל ושוללת בסבירות גבוהה אבחנה של הרעלה. תוצאות מעל לנורמה: חשיפה לטריכלורואתן: >10mg/L, חשיפה לטריכלורואתילן: >100mg/L1; חשיפה לטטרה-כלורואתילן: >ליטר/7mg. הערכים הנ"ל מתייחסים לתוצאות בדיקות שבוצעו בסיום שבוע עבודה, ומעידים על חשיפה לכימיקלים המצוינים. |
| יוצר הערך | פרופ' בן-עמי סלע |
חומצה טרילורואצטית (TCA, וכן TCAA או trichloroethanoic acid) היא אנלוג של חומצה אצטית בו שלושת אטומי המימן של קבוצת המתיל הותמרו על ידי אטומי כלור. מלחים ואסטרים של TCA קרויים trichloroacetates.
הפיזיולוגיה של TCA
חומצה זו קיימת בצורת גבישים היגרוסקופיים רומבו-הדראליים בטמפרטורה ובלחץ סטנדרטיים ויש לה ריח חריף. היא מאוד מסיסה במים ובסולבנטים אורגניים שונים. תכונותיה הפיזיקליות כוללות: משקל מולקולרי של 163.4 גרם/מול, נקודת המסה בטמפרטורה של 59.2 מעלות צלסיוס, נקודת רתיחה בטמפרטורה של 197.6 מעלות צלסיוס, וצמיגות של 1.63 גרם/סמ"ק בטמפרטורה של 60 מעלות צלסיוס.
תכונות כימיות של TCA: יש לחומצה זו חומציות חזקה (pKa = 0.7) בגין התמרה מוחלטת של מימני ה-methyl עם אטומים של כלור, מה שהופך אותה ליותר יציבה מאשר חומצה כלורואצטית ומאשר חומצה דיכלורואצטית, ופחות רגישה לריאקציות התמרה של אטומי הכלור. בתנאים מימיים טמפרטורות מוגברות משרות את פירוק TCA לכלורופורם ולדו-תחמוצת הפחמן. תהליך זה מוחש בנוכחות של בסיסים אורגניים או אינאורגניים, בעוד ש-aniline, רזורצינול ופחמן משופעל משמשים כקטליסטים בתנאים שהם anhydrous. פירוק תרמי טהור מתרחש רק מעל נקודת הרתיחה, ומניב הידרו-קרבונים שעברו כלורינציה, CO, דו-תחמוצת הפחמן ו-phosgene. חומצת TCA יוצרת מלחים עם בסיסים אורגניים ואינאורגניים מגוונים, ומלחים אלה מתפרקים בחימום בסביבה מימית תוך שחרור של כלורופורם.
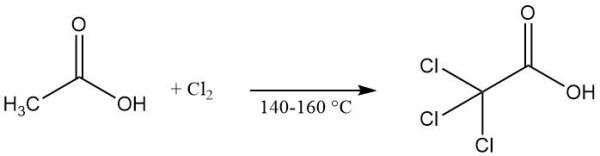
TCA מיוצר מסחרית על ידי כלורינציה של חומצה אצטית, חומצה כלורואצטית או בטמפרטורות מוגברות (140–160 מעלות צלסיוס). Calcium hypochlorite יכול לשמש קטליסט בהחשת הריאקציה. גישות חלופיות שנבחנו, כוללות 2% חומצה פוספורית או שילוב של קטליסטים עם הארת UV. פותחו גם שיטות ללא קטליסטים. התוצר המכיל לרוב 95% TCA, עובר טיהור על ידי גיבוש בהתכה. שיטה זו מרחיקה חומרים מזהמים הנמצאים בנוזל "האם". שיפור נוסף בניקיון התוצר יכול להיות מושג על ידי סרכוז או על ידי שלב גיבוש נוסף. כאשר חומצה גפריתנית משמשת כקטליסט בטמפרטורות גבוהות (עד 180 מעלות צלסיוס), אין צורך בטיהור שלאחר הייצור של TCA. המלח נתרן-TCA מיוצר מסחרית על ידי נטרול של TCA עם NaOH או ביקרבונאט.
trichloroacetate (Cl3CCOONa). הוא המלח התעשייתי היחיד בעל משמעות של TCA. הוא מוצק חסר צבע המתפרק מתחת לנקודת ההמסה שלו. הוא מסיס מאוד במים ובמתנול, ומסיס באופן מתון בסולבנטים פולריים אחרים. המסיסות במים גדלה עם הטמפרטורה. תכונות כימיות: הוא יציב בהיותו יבש, אך עובר הידרוליזה בתמיסה מימית, תוך יצירת סודיום ביקרבונאט וחומצה דיכלורואצטית. התפרקות תרמית בטמפרטורות מוגברות (125–170 מעלות צלסיוס), מייצרת NaCl, טריכלורואצטיל כלוריד ודו-תחמוצת הפחמן. הוא מגיב עם אולפינים תוך שימוש בקטליסטים שהם phase transfer. סודיום-טריכלורו אצטאט מיוצר תעשייתית על ידי ניטרול של TCA עם NaOH או עם קרבונאט. בנייר דיאזו המיוצר בחום, הוא משמש לשחרר בסיס בטמפרטורות מוגברות. סודיום-טריכלורו אצטאט שימש בעבר כהרביציד לווסת דשאים עם תקופת מחצית חיים בקרקע של 1-2 חודשים, אך החשש מאקו-טוקסיות הביא להחרמתו בארה"ב, קנדה, דרום אפריקה והאיחוד האירופי. נתונים in vitro שוללים פוטנציאל מוטגני של החומר.
אסטרים של TCA: Ethyl trichloroacetate משמש גם כקו-קטליסט בפולימריזציות מסוג Ziegler. להלן מספר תכונות פיזיקליות של שני אסטרים בעלי רלוונטיות תעשייתית: א) Methyl trichloroacetate (נוסחה - Cl3CCOOCH3), משקל מולקולרי 177.43 גרם/מול, נקודת רתיחה - 153 מעלות צלסיוס, צמיגות - 1.486 גרם/סמ"ק. ב) Ethyl trichloroacetate (נוסחה - Cl3CCOOCH2CH3, משקל מולקולרי - 191.45 גרם/מול, נקודת רתיחה - 167.5 מעלות צלסיוס, צמיגות - 1.382 גרם/סמ"ק.
הסינתזה של TCA בוצעה על ידי ריאקציה של כלור עם חומצה אצטית בנוכחות קטליסט דוגמת זרחן אדום, במה שקרוי הלוגניזציה על שם Hell–Volhard–Zelinsky. דרך נוספת לקבלת TCA היא על ידי חמצון של trichloroacetaldehyde. השימוש ל-TCA בביוכימיה הוא לשקע חלבונים, DNA ו-RNA ומאקרו-מולקולות נוספות. TCA ו-DCA משמשים בטיפולים קוסמטיים לקילוף נגעי עור והרחקת tattoo, וכן כתרופה מקומית לטיפול ביבלות. הטיפולים הללו נחשבים בטיחותיים בנשים הרות (Jones ו-Kirby ב-TCA or Bichloroacetic Acid Genit Warts משנת 2012). מלח הנתרן sodium trichloroacetate שימש כהרביציד כבר בשנות ה-50 אך הוסר מהמדפים בסוף שנות ה-80 של המאה ה-20 (Rai ו-Hamner ב-Weeds משנת 1953, ו-Heier ב-EPA משנת 1991). על פי סוכנות הכימיקלים האירופית, TCA עלול לגרום לכוויות עור חמורות ונזק לעיניים.
היסטוריה: TCA התגלה בשנת 1839 על ידי Jean-Baptiste Dumas (ב-Annalen der Pharmacie) והיווה מחלוקת קשה לתיאוריה של Jöns Berzelius שהתנגד לתיאוריה של רדיקלים אורגניים וערכויות.
יצירה של TCA
השימושים ב-TCA
לפני שנות ה-90 של המאה ה-20, השימוש העיקרי ב-TCA היה הייצור של מלח הנתרן שלו, ששימש כהרביציד סלקטיבי בשליטה על טבק ומריחואנה. אלא שבגלל החשש להשפעה אקו-טוקסיקולוגית שימוש זה פחת משמעותית. בנוסף לשימוש כהרביציד יש ל-TCA שימושים רבים כטיפול בשטחי מתכות, וגם כחומר צריבה וחריטה. הוא משמש גם כסולבנט בתעשיה הפלסטית, ובביוכימיה הוא משמש להשקעת חלבונים, אלבומין DNA ו-RNA.
נגזרות של TCA
לטריכלורילאצטיל כלוריד בעל הנוסחה הכימית Cl3CCOCl משקל מולקולרי של 197.9 גרם/מול, והוא בעל תכונות פיזיקליות הדומות לאלה של dichloroacetyl chloride. אסטרים של TCA מקיפים קבוצה רחבה של תרכובות, אך רק נגזרות ה-methyl וה-ethyl הן בעלות עניין תעשייתי. שני אסטרים אלה ניתנים לאפליקציה כסולבנטים, והם יכולים לשמש כחומרי מוצא לסינתזה של אמידים ושל אסטר רב-אלכוהולי.
טוקסיקולוגיה של TCA ושל טריכלורואצטאט
TCA הוא בעל סיכונים בריאותיים אחדים בגלל האופי המאכל שלו ויכולת השקעת החלבונים שלו. הוא עלול לגרום במגע לגירוי בעור ובעיניים ויש לו גם השפעות גסטרואנטרליות.
נתוני מפתח של טוקסיות: LD50 פומי בחולדות 3320–5060 מיליגרם/ק"ג. השפעה טוקסית כרונית בדרכי הנשימה העליונות. באדם TCA נסבל בנטילה יומית של 0.075 מיליגרם/ק"ג משקל. תופעות לוואי של נטילת TCA הן איבוד משקל, חולשה, נזק רקמתי לחניכיים ולחך, שינויים בספירת התאים הלבנים, ממצאים אנומליים בשתן, נגעים בכבד ובלב, אטרופיה בשריר, ופגיעה ביצירת תאי-זרע. פירוק תרמי בטמפרטורות מוגברות (125–170 °C) מייצר NaCl, trichloroacetyl chloride, CO ו-דו-תחמוצת הפחמן. חומצה טריכלורואצטית היא חומצה גבישית בטמפרטורת החדר המשמשת כמומס בתמיסות נוזליות שונות, והיא בעלת תכונות רעילות ומאכלות. עיקר החשיפה לחומצת TCA ולחומרים אחרים הקשורים אליה, מתרחשת במסגרת תעסוקתית, במיוחד בייצור תרופות וחמרי הדברה. דרכי החשיפה העיקריות הן נשימה של החומצה ושאיפתה אל דרכי הנשימה והריאות, ומגע עורי - שתיהן עלולות להוביל לגירוי הרקמות ולכוויות כימיות. לאחר חשיפה לחומר וכניסתו לדם, הוא מסונן בכליות ומופרש בשתן. בבדיקה זו ניתן לזהות את החומצה בשתן כעדות לחשיפה לכימיקלים מסוימים ולהרעלה.
מחלות ומצבים בריאותיים שהבדיקה יכולה לזהות: הרעלת חומצה טריכלורואצטית – חשיפה לחומר בכמות מספקת עלולה לגרום לנזק לרקמות שונות, בהתאם לדרך החשיפה. בכל אחת מהדרכים, המנגנון הראשוני של הנזק הוא קרישה של חלבונים ודה-נטורציה של התאים החיצוניים, ובהמשך גם של תאים עמוקים יותר.
התסמינים הנפוצים בחשיפה חריפה לחומצה טריכלורואצטית כוללים: גירוי ושריפה בעיניים, גירוי וכוויות בעור, גירוי של ריריות האף והגרון, שיעול, קוצר נשימה ואף בצקת ריאות. חשיפה כרונית לחומצה טריכלורואצטית עלולה לגרום לדלקת סימפונות (ברונכיטיס) הגורמת לשיעול, ייצור מוגבר של ליחה ולקוצר נשימה, וכן לנזק מצטבר בכבד.
אוכלוסיות בסיכון
מומלץ לבצע את הבדיקה בהוראת רופא בעובדים בסביבת כימיקלים בתעשייה או במטופל לאחר חשיפה ידועה לחומצה טריכלורואצטית או לחומצות אחרות כגון טריכלורואתילן, טטרה-כלורואתילן ועוד. חומצות אלו מביאות לייצור של חומצה טריכלורואצטית במהלך חילוף החומרים בגוף.
הוראות לביצוע הבדיקה
יש לבצע את הבדיקה לאחר שהייה במוקד חשיפה חשוד, בסוף יום עבודה או בסוף שבוע עבודה. לא נדרשות הכנות מוקדמות. הבדיקה אינה פולשנית ואינה חושפת את הנבדק לסיכונים.
ביצוע הבדיקה: הבדיקה כוללת איסוף שתן לכלי קיבול שיינתן במעבדה.


 כניסה
כניסה  עקבו אחרינו בפייסבוק
עקבו אחרינו בפייסבוק