כאב עצבי בתר הרפטי - Post herpetic neuralgia
ערך זה נמצא בבדיקה ועריכה על ידי מערכת ויקירפואה, וייתכן כי הוא לא ערוך ומוגה.
| נוירלגיה בתר הרפטית | ||
|---|---|---|
| Post herpetic neuralgia | ||
| יוצר הערך | ד"ר ולנטינה סמיונוב
|
|
נגיף הווריצלה זוסטר שייך למשפחת ההרפס (Herpesvirus), והוא גורם לשתי תסמונות עיקריות שונות.
ההדבקה הראשונית Primary Infection)) בנגיף השלבקת (HZV) מתבטא באבעבועות רוח (Varicella, Chickenpox), מחלה מידבקת ולרוב בלתי מזיקה, המתרחשת במגפות בקרב ילדים רגישים. נגיף הווריצלה מידבק מאוד, ולפני כניסת החיסון נגד אבעבועות רוח יותר מ-99.6% מאוכלוסיית ארצות הברית מעל גיל 40 נחשפה לזיהום וריצלה קודם.[1]
נגיף השלבקת נותר סמוי בעיקר בשורשי עצבים במשך שנים, אך שומר על יכולת שכפול וזיהום בהינתן לו תנאים מתאימים (גיל מתקדם, דיכוי מערכת החיסון, תרופות מסוימות).[2] וכך, מעל 90% מהמבוגרים בארצות הברית נמצאים בסיכון לפתח שלבקת חוגרת בעתיד.[3]
שלבקת חוגרת היא מחלה שנגרמת משפעול (Reactivation) של נגיף הווריצלה זוסטר (Varicella Zoster Virus) שקיים בצורה סמויה בעצבים תחושתיים. בקרב 20% מבני האדם שנדבקו, בהדבקה הראשונית מתרחש שפעול של הנגיף במהלך חייהם.[4]
גיל הוא גורם סיכון עיקרי להתפתחות שלבקת חוגרת; שכיחותה בקרב אנשים מעל גיל 75 שנים היא מעל 10 מקרים לכל 1,000 שנות אדם.[5]
הגורם השני להתפתחות של שלבקת חוגרת הוא כשל במערכת החיסון (Altered Cell-Mediated Immunity). חולים עם מחלות דם פרוליפרטיביות, חולים שמקבלים תרופות מדכאות מערכת החיסון, כגון סטרואידים, וחולים מושתלי איברים מעלים משמעותית את הסיכון לפתח זיהום של הרפס זוסטר. הרפס זוסטר מתרחשת בתדירות גבוהה יותר גם בקרב בני אדם שהם חיובים (Seropositive) לווירוס HIV (איידס).[2]
תמונה קלינית של שלבקת חוגרת מתאפיינת בדרך כלל בפריחה ובדלקת עצבית חריפה (ניריטיס). הפריחה בשלבים ההתחלתיים היא פפולות אריטמטוטיות. שעות עד ימים לאחר מכן היא מתפתחת לשלפוחיות ולבולות, וחולפת במשך 4-3 השבועות הבאים. בדרך כלל הפריחה מוגבלת בדרמטום אחד אצל אנשים בריאים, אך לפעמים היא יכולה לכלול שניים או יותר דרמטומים. דרמטום טורקלי ומותני הם דרמטומים המעורבים יותר בזיהום של הרפס זוסטר.[6]
רוב המקרים של הרפס זוסטר הם קלים וחולפים מעצמם, אך במקרים מסוימים המחלה יכולה לגרום לסבל משמעותי, במיוחד אצל קשישים.
סיבוכים של שלבקת חוגרת אצל חולים ללא דיכוי מערכת החיסון (Immunocompetent) הן תסמונת כאב עצבי Postherpetic Neuralgia) PHN), אנצפליטיס, מיאליטיס, שיתוק עצבים היקפים ומרכזיים.[1] היום גם הופיעו עדויות על כך שהרפס זוסטר מעלה את הסיכון לשבץ מוחי איסכמי וגם המורגי ב-30%, במיוחד זוסטר אופטלמיקוס (מאמר בפרסום בעיתון Stroke).
נוירגליה פוסט-הרפטית (PHN)
הסיבוך השכיח ביותר הוא תסמונת כאב עצבי כרוני, הנקראת נוירלגיה פוסט-הרפטית. במחקר אחד אחוז החולים עם הרפס זוסטר שפיתחו Neuralgia Post Herpetic (המוגדרים לפחות 90 ימים של כאב מתועדים) עלה מ-5 אחוזים, באותם צעירים מעל גיל 60, ועד 40-20 אחוזים אצל בני 80 ומעלה.[7]
PHN קשורה לעתים קרובות לתחלואה משמעותית, ויכולה לגרום נוסף על כאב קשה גם לנדודי שינה, עייפות, דיכאון עם הפרעה בפעילות היום-יומית.
מחקרים הראו כי יש שלושה שלבים של PHN: שלב חריף, תת-חריף ושלב כרוני.[8] השלב החריף מתרחש עם תחילת הפריחה ונמשך כ-30 יום, השלב התת-חריף נמשך 3-1 חודשים לאחר הופעת הפריחה, והשלב הכרוני או נוירלגיה פוסט-הרפטית (PHN), נמשך 3 חודשים או יותר לאחר תחילת הפריחה.[9]
גורמי סיכון ל-PHN כוללים תסמינים קליניים בשלב טרום-קליני והחמרת כאב בתחילת הפריחה. הגורם המשמעותי ביותר לפיתוח תסמונת כאב עצבי כרוני (PHN) הוא הגיל. לפי המחקרים, טווח ההיארעות הכוללת הוא 10% עד 27%, השכיחות עבור אנשים מבוגרים מגיל 50 היא 40%, ו-75% עבור אלה שגילם 75.[10][11][12]
פתוגנזה
בשלב של שלבקת חוגרת חריפה ברמת התאים נמצאו עדויות של דלקת המרורג‘י בעצבים פריפריים, שורשים דורזליים וגנגליון, ובהמשך יכול להתפתח תהליך של פיברוזיס, איבוד של מיאלין מהמעטפת של העצבים, ותהליכים אטרופיים.[13][14][15]
מחקרים רבים לא הצליחו לזהות נוירו-מדיאטורים ספציפיים ב-PHN, וייתכן שאותן נוירומדיאטורים של כאב נוירופתי, כגון סובסטנס P (Substance P), סרוטונין ואפינפרין משתתפים בהעברת סיגנל כאב גם באותם המקרים של PHN.[16]
תמונה קלינית
הכאב הקשור להרפס זוסטר חריף, בדרך כלל מתואר בכאב חד ודוקר או בתחושת שריפה. כאב “בוער“ הוא ציטוט הכי שכח מפי חולי PHN.[17] ליותר מ-90 אחוז מהחולים עם PHN תהיה גם אלודיניה, המוגדרת ככאב מעורר בדרך כלל על ידי גירויים לא מכאיבים (כגון: מגע מלטף בעור). בד“כ נפגעים דרמטומים טורקליים (במיוחד T4 עד T6), צווארי ועצב הקרניאלי החמישי (Trigeminal Nerve).[18] כתוצאה מכך לעתים קרובות פוגע כאב קשה באיכות החיים של המטופל, בתפקוד היום-יומי שלו, שכן הוא עלול לגרום לחולשה, נדודי שינה, חרדה ודיכאון. יש לציין שכאב עצבי לא נעלם עם היעלמות הפריחה, ונוירגליה יכולה להימשך חודשים עד שנים לאחר אפיזודה חריפה של שלבקת חוגרת. לעתים רחוקות יותר מתרחשים מקרים שנוירלגיה מופיעה זמן מסוים אחרי זיהום זוסטר חריף באותו אזור של פריחה, לאחר גורם מסוים (כגון: פעולה כירורגית, דלקת מוגלתית בשן.[19]
טיפול
- טיפול מניעתי ל-Postherpetic Neuralgia
חיסון: ב-2005 בעיתון אמריקאי NEJM פורסם מחקר גדול כפול-סמיות רנדומלי שבדק השפעת חיסון חדשני חי מוחלש לשלבקת חוגרת. המחקר כלל כמעט 40,000 אנשים מעל גיל 60. שכיחות הנוירלגיה הפוסט-הרפטית ירדה ב-67% בקבוצת האנשים שקיבלה חיסון. נוגדנים נגד הרפס זוסטר וחסינות תאים (Cell-Mediated Immunity) מופיעים ב-6 שבועות נוספים לאחר מתן החיסון.[20][21] משנת 2008, לפי המלצות אמריקאיות, חיסון נגד הרפס זוסטר מומלץ לכל האוכלוסייה מעל גיל 60 במנה אחת ללא קשר אם המטופל חלה בזוסטר בעברו או לא.[22]
טיפול אנטי וירלי: תרופות אנטי-וירליות (,Acyclovir ,Valcyclovir Famcyclovir) ניתנות לשימוש בהרפס זוסטר חריפה במטרה להפחית את חומרת הסימפטומים ומשך שכפול הנגיף, וכך להקטין את חומרת הנגעים בעור. מחקרים קודמים לא הצליחו להראות יעילות של תרופות אלו בהורדת השכיחות והחומרה של נוירלגיה.
עם זאת, מטה-אנליזה אחרונה של מחקרים רנדומליים (Placebo-Controlled Studies) כן הצליחה להוכיח שטיפול באציקלוביר מוריד כאב עצבי באופן משמעותי.[23][24] הסקירה האחרונה בקוקריין (Cochrane), שפורסמה באפריל 2009, מסכמת שוב, על סמך אנליזה של 12 מחקרים באיכות גבוהה, שאין הוכחות ברורות שטיפול באציקלוביר מוריד משמעותית את הסיכוי ל-PHN, בניגוד לזאת, יש השפעה לטובה לפמציקלוביר (Famcyclovir) במינון של 500 עד 750 מ“ג למנה להוריד שכיחות של נוירלגיה אחרי הרפס זוסטר באופן משמעותי סטטיסטית.[25]
טיפול בסטרואידים: בניגוד לכך, טיפול בסטרואידים סיסטמיים (במתן פומי, תוך-שרירי או תוך-ורידי) לא מוריד שכיחות של נוירגליה בהשוואה לאינבו.[26]
טיפול מוקדם במשככי כאב: שיטה אחרת היא התחלת טיפול מוקדם בכאבים במטרה למנוע התפתחות של נוירלגיה עוד בשלבים אקוטיים של הרפס זוסטר. יש תוצאות חיוביות ממחקר כפול-סמיות רנדומלי של Bowsher, שכלל 72 מטופלים מעל גיל 69 עם שלבקת חוגרת, שבו הם קיבלו 25 מ“ג אמיטריפטילין או אינבו במשך 90 יום.[27] הטיפול החל ב-48 שעות ראשונות של הפריחה. שכיחות של הכאבים ב-6 חודשים הבאים הייתה כמעט ב-50% פחות בקבוצה שקיבלה אמיטריפטילין. בסקירה האחרונה של Uptodate מ-2009, המחברים ממליצים על טיפול מוקדם של אמיטריפטילין 25 מ“ג ליום או נורטריפטילין 25 מ“ג ליום כטיפול מונע למטופלים עם שלבקת חוגרת חריפה ב-48 שעות הראשונות של הופעת פריחה. משך הטיפול עד 90 יום. במקרים של תופעות לוואי לטריציקליים, במיוחד אצל אנשים קשישים, מומלץ גם מתן גבפנטין 1,800 מ"ג ליום למשך 90 יום (יש לציין שאין עבודות של טיפול בגבפנטין לטיפול מונע על בני אדם אלא רק ב-Animal Model, אך פרופיל בטיחותי מאפשר את שקילת האופציה הזאת).
אופציות טיפוליות ל-PHN
טיפול בנוירלגיה אחרי שלבקת חוגרת נותר קשה. קיימות מספר אופציות טיפוליות.
טיפול מקומי
טיפול מקומי הוא בשימוש רחב לטיפול בנוירלגיה במיוחד לזמן קצר. קרם קפסאיצין (Capsaicin) שניתן למריחה עד 4-3 פעמים ביום, מוריד כאבים על ידי עיקוב של Substance P דרך הרחבה של כלי דם (וזודילטציה). תופעת לוואי היא כאב שורף בלתי נסבל.[28] עדיין לא הסתיים המחקר שבא לבדוק שימוש במדבקת קפסאיצין בריכוז גבוה (8%) חד-יומית. במחקר שכלל 402 חולים, הוריד טיפול במדבקת קפסאיצין בריכוז גבוה ל-12 שבועות כאבים בצורה משמעותית, לעומת מדבקה עם ריכוז נמוך (0.4%).[29]
תפקידו של לידוקאין מקומי בטיפול ב-PHN לא מבוסס מחקרית עד הסוף. מטה-אנליזה שפורסה ב-2007 כוללת רק שני מחקרים קטנים. אף שבמחקרים אלו טיפול בלידוקאין טופיקלי מוריד כאב בצורה בינונית, מערכי מטה-אנליזה קובעים שאין מספיק הוכחות להמליץ על לידוקאין כטיפול קו ראשון.[30]
טיפול סיסטמי
א. נוגדי דיכאון: תרופות נוגדות דיכאון מקבוצה הטריציקלייםTricyclic Antidepressant) TCA) נחקרו יותר מכל התרופות בנושא של נוירלגיה פוסט-הרפטית. הן הוכיחו את עצמן כיעילות ומהוות טיפול קו ראשון. לפחות בחמישה מחקרים נחקרו תרופות טריציקליות לטיפול ב-PHN, והשפעתן נקבעה מבינונית עד מצוינת להקלת כאבים.[31] טיפול בנוירלגיה פוסט-הרפטית על ידי תרופות טריציקליות NNT שווה בין 2.1 עד 3.1.[32] המינון הממוצע הוא 65 מ“ג. בד“כ כדי לקבוע כישלון טיפולי בתרופות טריציקליות צריך להגיע למינון של 100 מ“ג לפחות, ולטפל לפחות 3 שבועות.[33][34] למרות הטיפול הנרחב בהן, קיימות תופעות לוואי נפוצות, ולעתים קרובות נדרש שיקול דעת לפני שמתחילים טיפול ב-TCA, במיוחד אצל חולים מבוגרים. יובש בפה, אצירת שתן, הפרעות ראייה, החמרה של גלאוקומה, עלייה במשקל, תופעות קשורות למערכת כלי דם ולב - ירידה בל“ד אורתוסטטית, הפרעות קצב, שינויים ב-אק“ג. NNH (Number Needed to Harm) של תרופות טריציקליות הוא 4.1 עד 9.9.[35]
תרופות נוגדות דיכאון אחרות לא היו יעילות כמו TCAs. כך לפי סיכום של מספר מחקרים שבדק השפעת נוגדי דיכאון מקבוצות אחרות, כגון: SNRI ,SSRI. ל-SNRI בטיפול בנוירופתיה כואבת היה NNT 5.1 (3.9-7.4), ל-SSRI היה ה-NNT סביב 7.0.
ב. נוגדי פרכוס: נוגדי פרסוכים, עוד קבוצת תרופות לטיפול בכאב עצבי. 3 תרופות נחקרו בעבודות רנדומליות - גבפנטין (Gabapentin), פרגבלין (Pregabalin) וכן ולפורט (Valproic Acid).
היעילות של גבפנטין הוכחה במספר מחקרים. אם כי אין מינון סטנדרטי, ממליצים להתחיל ממינון של 900 מ“ג ליום, ולעלות באופן הדרגתי עד 1,800 מ“ג. חלק מהחולים יצטרכו מינון המגיע ל-3,600 מ“ג ליום. התרופה נסבלת בד“כ היטב. תופעות לוואי שכיחות הן ישנוניות, סחרחורות, הפרעות בהליכה - אטקסיה.[36][37]
פרגבלין, תרופה דומה במבנה לגבפנטין ול-GABA. לפחות שני מחקרים חקרו את התרופה בטיפול ל-PHN. התרופה משפרת שינה וכאבים אצל חולים עם נוירגליה אחרי שלבקת חוגרת. המינון המומלץ הוא 150 עד 600 מ“ג ליום.[38][39]
ג. אופיאטים: משככי כאבים אופיודיים נמצאים היום בשימוש רחב לטיפול בכאב עצבי כולל PHN. טרמדול (Tramadol), מורפין (Morphine), אוקסיקודון (Oxycodon) נחקרו לטיפול ב-PHN.[35] יש לקחת בחשבון תופעות לוואי של אופיאטים ולהעריך את ההיסטוריה של המטופל להתמכרויות לפני החלטה על טיפול. במחקר של Boureau וחב‘ שפורסם ב-2003 בעיתון Pain, נבדקו יעילות ובטיחות של טרמדול בטיפול ב-PHN. במחקר כפול-סמיות רנדומלי נכללו 127 חולים שסבלו מ-PHN בגילים 35 עד 85, קיבלו טרמדול במינון של 100 מ“ג עד 400 מ“ג ליום (אנשים מבוגרים מגיל 75 קיבלו עד 300 מ“ג) לפחות 6 שבועות. בקבוצה שטופלה בטרמדול אחוז הקלה של כאב במהלך השבוע 6 היה גבוה באופן משמעותי מאשר בקבוצת האינבו, החולים הצטרכו פחות משככי כאבים לצורך מנות הצלה, ולא היה הבדל משמעותי בתופעות לוואי (29.7% בקבוצת טרמדול ו-31.8% בקבוצת אינבו.[40]
ב-2005 בעיתון NEJM פורסם מחקר שבדק יעילות מורפין, גבפנטין ושילוב ביניהם לטיפול בכאב עצבי (נוירופתיה סוכרתית נוירלגיה פוסט-הרפטית). מסקנות המחקר: בשילוב של שתי התרופות הכאב הממוצע היה פחות בקבוצה שקיבלה שילוב מורפין וגבפנטין, ומצד שני, בקבוצה הזאת חולים הצטרכו מינונים קטנים יותר של התרופות.[41]
ד. סטרואידים: במקרים שבהם חולים סובלים ממעורבות עצבית אחרת מעצב טריגמינלי, אופציה לטיפול בכאב עקשני היא סטרואידים במתן אינטרה-טקלי. ב-2000 ב-NEJM פורסמה עבודה על 277 חולים עם כאב עצבי עקשני על רקע שלבקת חוגרת. החולים חולקו ל-3 קבוצות: הראשונה קיבלה מטילפרדניזולון ולידוקאין, השנייה קיבלה רק לידוקאין, והשלישית לא קיבלה טיפול כלל. יותר מ-90% מהחולים בקבוצת פרדניזולון דיווחו על הקלה מצוינת בכאבים לתקופה של 4 שבעות עד שנתיים. יש לציין שלא היו תופעות לוואי משמעותיות קשורות להזרקות של התרופה.[42]
ה. לידוקאין סיסטמי: במקרים עקשניים שטיפול קודם לא הביא להקלת כאבים, ניתן לשקול עירוי לידוקאין תוך-ורידי. עם זאת, יש רק מחקרים קטנים, אך לא משכנעים על עדיפויות בטיפול לעומת אינבו.[43][44]
ו. טיפולים אחרים: אנטגוניסטים לקולטני NMDA - רק קטמין במתן תוך-ורידי הוכיח את עצמו בהורדת כאב עצבי אחרי הרפס זוסטר, אך הוא כרוך בהרבה תופעות לוואי (ישנוניות, דיספוריה, הזיות ארוטיות).[45] דקרומטורפן (Dextromethorphan) לא הראה אפקט מול אינבו.[46]
יש מספר עבודות קטנות על קריאותרפיה וכירורגיה של העצבים הפגועים ב-PHN, אך עדיין אין הוכחות ברורות ליעילות של הטיפולים.
סיכום
טיפול בתסמונת כאב עצבי לאחר שלבקת חוגרת הוא אתגר לא קטן. מסקירה סיסטמטית בספרות ניתן להמציא מסקנות שטיפול בנוגדי דיכאון מקבוצה של טריציקליים, גבפנטין או פרגבלין, אופיאטים, טיפול מקומי בקפסיצין או לידוקאין יעילים יותר לעומת אינבו בטיפול ב-PHN.
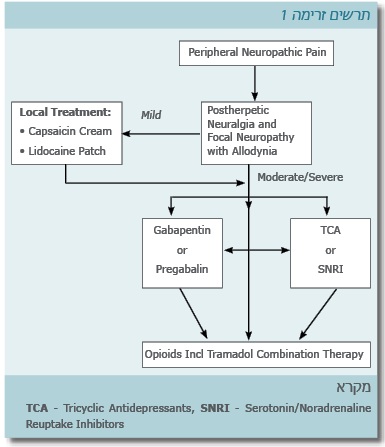
אנו מציעים אלגוריתם טיפולי (תרשים זרימה 1): תרופות טריציקליות ואופיאטיות הן תרופות הכי יעילות, ומומלץ להשתמש בהן כקו ראשון. גבפנטין היא אלטרנטיבה טובה לטריציקליים, וגם ניתן להוסיף אותה לאופיאטים, ניתן גם להשתמש בפרגבלין.
אם טיפול שהוצג באלגוריתם לא הועיל, ניתן לשקול טיפול בלידקאין תוך-ורידי, והזרקת Intrathecal Glucocorticoid יכול להיחשב כטיפול טוב עבור מטופלים אשר ממשיכים לסבול מכאב עקשני למרות הצעדים המוזכרים לעיל.
ביבליוגרפיה
- ↑ 1.0 1.1 Kimberlin DW, Whitley RJ. Varicella–Zoster Vaccine for the Prevention of Herpes Zoster. NEJM 2007;356:1338-1343
- ↑ 2.0 2.1 Gnann JW, Whitley RJ. Herpes Zoster. NEJM 2002;347:340-346
- ↑ Choo PW, Donahue JG, Manson JE, et al. The epidemiology of varicella and its complications. J Infect Dis 1995;172:706-712
- ↑ ורמן מ‘, הלפרין ד‘. שלבקת חוגרת המערבת את הסעיף השני (המקסילרי) של עצב הגולגולת החמישי. הרפואה, 2007, 146, ב: 89-91
- ↑ Donahue JG, Choo PW, Manson JE, et al. The incidence of herpes zoster. Arch Intern Med 1995;155:1605-1609
- ↑ Yawn BP, Saddier P, Wollan PC, et al. A population-based study of the incidence and complication rates of herpes zoster before zoster vaccine introduction. Mayo Clin Proc 2007;82:134
- ↑ Bowsher D. Postherpetic neuralgia and its treatment: A retrospective survey of 191 patients. J Pain Symptom Manage 1996;12:290
- ↑ Arani RB, Soong SJ, Weiss HL, et al. Phase specific analysis of herpes zoster associated pain data: a new statistical approach. Stat Med 2001;20(16):2429-2439
- ↑ Dworkin RH, Portenoy RK. Proposed classification of herpes zoster pain. Lancet 1994;343(8913):1648
- ↑ Scott FT, Leedham-Green ME, Barrett-Muir WY, et al. A study of shingles and the development of postherpetic neuralgia in East London. J Med Virol 2003;70(Suppl 1):24-30
- ↑ Lancaster T, Silagy C, Gray S. Primary care management of acute herpes zoster: systematic review of evidence from randomized controlled trials. Br J Gen Pract 1995;45(390):39-45
- ↑ Portenoy RK, Duma C, Foley KM. Acute herpetic and postherpetic neuralgia: clinical review and current management. Ann Neurol 1986;20(6):651-664
- ↑ Denny-Brown D, Adams RD, Fitzgerald PF. Pathologic features of herpes zoster: A note on ‘geniculate herpes‘. Schweiz Arch Neurol Psychiatr 1944;57:216
- ↑ Head H, Campbell AW. The pathology of herpes zoster and its bearing on sensory localization. Brain 1900; 23:353
- ↑ Zacks SI, Elliott FA, Langfitt TW. Herpetic neuritis: A light and electron microscopic study. Neurology 1964;14:744
- ↑ Watson CP, Morshead C, Van der Kooy D. Postherpetic neuralgia: Post-mortem analysis of a case. Pain 1988;34:129
- ↑ Lydick E, Epstein RS, Himmelberger D, et al. Herpes zoster and quality of life: a self-limited disease with severe impact. Neurology 1995;45:52
- ↑ Watson CP, Evans RJ, Watt VR, et al. Post-herpetic neuralgia: 208 cases. Pain 1988;35:289
- ↑ Schott GD. Triggering of delayed-onset postherpetic neuralgia. Lancet 1998;351:419
- ↑ Oxman MN, Levin MJ, Johnson GR, et al. A vaccine to prevent herpes zoster and postherpetic neuralgia in older adults. NEJM 2005;352:2271
- ↑ Levin MJ, Oxman MN, Zhang JH, et al. Varicella-zoster virus-specific immune responses in elderly recipients of a herpes zoster vaccine. J Infect Dis 2008;197:825
- ↑ Recommended Adult Immunization Schedule: United States, 2010. Annals of Internal Medicine 2010;152:36-39
- ↑ Wood MJ, Kay R, Dworkin RH, et al. Oral acyclovir therapy accelerates pain resolution in patients with herpes zoster: a meta-analysis of placebo-controlled trials. Clin Infect Dis 1996;22(2):341-347
- ↑ Jackson JL, Gibbons R, Meyer G, et al. The effect of treating herpes zoster with oral acyclovir in preventing postherpetic neuralgia. A meta-analysis. Arch Intern Med 1997;157(8):909-912
- ↑ Li Q, Chen N, Yang J, et al. Antiviral treatment for preventing postherpetic neuralgia. Cochrane Database Syst Rev 2009;(2):CD006866
- ↑ He L, Zhang D, Zhou M, et al. Corticosteroids for preventing postherpetic neuralgia. Cochrane Database Syst Rev 2008;CD005582
- ↑ Bowsher D. The effects of pre-emptive treatment of postherpetic neuralgia with amitriptyline: a randomized, double-blind, placebo-controlled trial. J Pain Symptom Manage 1997;13:3
- ↑ Kost RG, Straus SE. Postherpetic neuralgia--pathogenesis, treatment, and prevention. NEJM 1996;335(1):32-42
- ↑ Backonja M, Wallace MS, Blonsky ER, et al. NGX-4010, a high-concentration capsaicin patch, for the treatment of postherpetic neuralgia: a randomised, double-blind study. Lancet Neurol 2008;7:1106
- ↑ Khaliq W, Alam S, Puri N. Topical lidocaine for the treatment of postherpetic neuralgia. Cochrane Database Syst Rev 2007;CD004846
- ↑ Kost RG, Straus SE. Postherpetic neuralgia--pathogenesis, treatment, and prevention. NJM 1196;335(1):32-42
- ↑ McCleane G. Pharmacological management of neuropathic pain. CNS Drugs 2003;17:1031-1043
- ↑ Watson CP, Evans RJ, Reed K, et al. Amitriptyline versus placebo in postherpetic neuralgia. Neurology 1982;32:671
- ↑ Max MB, Schafer SC, Culnane M, et al. Amitriptyline, but not lorazepam, relieves postherpetic neuralgia. Neurology 1988;38:1427
- ↑ 35.0 35.1 Finnerup NB, Otto M, McQuay HJ, et al. Algorithm for neuropathic pain treatment: An evidence based proposal. Pain 2005;118:289–305
- ↑ Rice AS, Maton S. Postherpetic Neuralgia Study Group. Gabapentin in postherpetic neuralgia: a randomised, double blind, placebo controlled study. Pain 2001;94(2):215-224
- ↑ Backonja M, Glanzman RL. Gabapentin dosing for neuropathic pain: evidence from randomized, placebo-controlled clinical trials. Clin Ther 2003;25(1):81-104
- ↑ Dworkin RH, Corbin AE, Young JP, et al. Pregabalin for the treatment of postherpetic neuralgia: a randomized, placebo-controlled trial. Neurology 2003;60:1274
- ↑ Sabatowski R, Galvez R, Cherry DA, et al. Pregabalin reduces pain and improves sleep and mood disturbances in patients with post-herpetic neuralgia: results of a randomised, placebo-controlled clinical trial. Pain 2004;109:26
- ↑ Boureau F, Legallicier P, Kabir-Ahmadi M. Tramadol in post-herpetic neuralgia: a randomized, double-blind, placebo-controlled trial. Pain 2003;104(1-2):323-331
- ↑ Gilron I, Bailey JM, Dongsheng Tu, et al. Morphine, Gabapentin, or Their Combination for Neuropathic Pain. NEJM 2005;352:1324-1334
- ↑ Kotani N, Kushikata T, Hashimoto H, et al. Intrathecal methylprednisolone for intractable postherpetic neuralgia. NEJM 2000;343:1514
- ↑ Baranowski AP, De Courcey J, Bonello E. A trial of intravenous lidocaine on the pain and allodynia of postherpetic neuralgia. J Pain Symptom Manage 1999;17:429
- ↑ Hempenstall K, Nurmikko TJ, Johnson RW, et al. Analgesic therapy in postherpetic neuralgia: a quantitative systematic review. PLoS Med 2005;2:164
- ↑ Eide P, Jorum E, Stubhaug A, et al. Relief of postherpetic neuralgia with the N-methyl-D-aspartic acid receptor antagonist ketamine: A double-blind, crossover comparison with morphine and placebo. Pain 1994;58:347
- ↑ Nelson KA, Park KM, Robinovitz E, et al. High-dose oral dextromethorphan versus placebo in painful diabetic neuropathy and postherpetic neuralgia. Neurology 1997;48:1212
קישורים חיצוניים
המידע שבדף זה נכתב על ידי ד"ר ולנטינה סמיונוב


 כניסה
כניסה  עקבו אחרינו בפייסבוק
עקבו אחרינו בפייסבוק