כולין - Choline
| מדריך בדיקות מעבדה | |
| כולין | |
|---|---|
| Choline | |
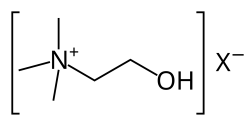
המבנה הכימי של כולין. X מציין את היון השלילי הקשור בדרך כלל לכולין
| |
| מעבדה | כימיה בדם |
| תחום | מולקולה הקשורה לתפקוד מערכת העצבים ומרכות גוף נוספות. |
| יוצר הערך | פרופ' בן-עמי סלע |
מטרת הבדיקה
הערכת רמת כולין במפגעים עצביים, מחלות כבד ושרירים וסינתזת DNA ברקמות גוף אחרות.
כללי
כולין הוא קטיון שמשקלו המולקולרי 104.2 דלטון, עם הנוסחה +CH3)3NCH2CH2OH) היוצר מלחים שונים כגון choline chloride ו-choline bitartrate. כולין הוא תוצר מזון חיוני לבעלי חיים, והוא מרכיב מבני של פוספוליפידים בממברנת התא. כולין משמש לסינתזה של הנוירוטרנסמיטר אצטילכולין, הכרוך בפעולת השרירים ובמספר תפקודים של מערכת העצבים, בהיותו כרוך בהתפתחות המוקדמת של המוח, של הביטוי הגני, של האיתות הבינתאי, ושל המטבוליזם המוחי. אף על פי שהאדם מסנתז כולין בכבד, כמות זו אינה מספיקה לתפקודים התאיים, ולכן יש דרישה לכולין המגיע מהמזון. סוגי מזון העשירים בכולין הם בשרים, עוף, חלמון ביצים, ירקות ממשפחת המצליבים, אפונה, אגוזים ודגנים מלאים. כולין נמצא בחלב-אם.
גילוי כולין
בשנת 1849, Adolph Strecker היה הראשון לבודד כולין ממרה של חזירים (Baeyer ב-Justus Liebigs Ann Chem משנת 1867). בשנת 1852, היו אלה Babo ו־Hirschbrunn שמיצו כולין מזרעים של חרדל, ובשנת 1862 היה זה Strecker שכינה את החומר כולין וקבע את נוסחתו כ-C5H13NO (Dybkowsky ב-J Prakt Chem משנת 1867). בשנת 1850, Theodore Gobley מיצה ממוחות את החומר לציטין והראה ב-1874 שמדובר בתערובת של phosphatidylcholines (Gobley ב-J Pharm Chim, ו-Sourkes ב־Bull Hist Chem משנת 2004). בשנת 1867 היה זה Adolf von Baeyer שפתר לראשונה את ההרכב של כולין (Sebrell וחב' ב-The Vitamins משנת 1971).
הכולין נחשב ויטמין, וסומן בעבר כוויטמין B4 (סימון זהה לבסיס החנקני אדנין, שבעבר נחשב אף הוא לוויטמין).
הכימיה של כולין
כולין הוא קטיון רביעוני של אמוניום, המסיס במים. הוא מהווה את תרכובת האב של משפחת הכולינים, המורכבת מאתנולאמין המכיל שלושה שיירי מתיל הקשורים לאותו אטום חנקן. כולין הידרוקסיד ידוע כבסיס כוליני. הוא מופיע כסירופ היגרוסקופי, חסר צבע וצמיג, עם ריח דגים הנובע מטרימתילאמין (TMA). תמיסות מימיות של כולין יציבות אך החומר מתפרק לאט לאתילן גליקול, לפולי-אתילן-גליקולים ול-TMA. היסטורית, כולין מיוצר ממקורות טבעיים, כגון דרך ההידרוליזה של לציטין. ברוב בעלי החיים, פוספוליפידים המכילים כולין הם חומרים חיוניים בממברנות תאים, כמו גם בליפופרוטאינים בעלי צפיפות נמוכה.
כולין כתוצר תזונתי
האדם מסוגל לסנתז de novo כמות מסוימת של כולין, אך נזקק לתוספת כולין בדיאטה לשמור על בריאותו. הדרישה לכולין יכולה להיות בצורת פוספוליפידים המכילים כולין, כגון פוספטידילכולין. כולין אינו מסווג כוויטמין למרות היותו תוצר תזונה חיוני עם מבנה ומטבוליזם של חומצת אמינו (Rucker וחב' ב-Handbook of vitamins משנת 2007). כולין נדרש ליצירה של אצטילכולין ושל S-adenosylmethionine (להלן SAM) שהוא תורם מתיל אוניברסלי. כתוצאה מהמתילציה, SAM מותמר ל-S-adenosyl homocysteine. חסר סימפטומטי של כולין גורם למחלת כבד שומני לא-אלכוהולי ולנזק לשריר (Kenny וחב' ב-Nature Metab משנת 2025). צריכה מוגברת של כולין שהיא מעל 7.5 גרם ליום, עלולה לגרום ללחץ-דם נמוך, להזעה, לשלשולים, ולריח גוף דמוי-דגים כתוצאה מהצטברות של טרימתילאמין, הנוצר במטבוליזם של כולין. ירקות עם פסטה ואורז גם כן מוסיפים לצריכת כולין בדיאטה האמריקנית.
כמות הכולין היומית הנדרשת במזון
- גיל 0–6 חודשים - 125 מיליגרם ליום
- גיל 7–12 חודשים - 150 מיליגרם ליום
- גיל 1–3 שנה - 200 מיליגרם ליום
- גיל 4–8 שנה - 250 מיליגרם ליום
- 9-13 שנה - 375 מיליגרם ליום
- 14-18 שנה:
- נערות - 400 מיליגרם ליום
- נערים - 550 מיליגרם ליום
- נשים מבוגרות - 325 מיליגרם ליום
- גברים מבוגרים - 50 מיליגרם ליום
- נשים מניקות -550 מיליגרם ליום;
- נשים הרות - 430 מיליגרם ליום
מטבוליזם
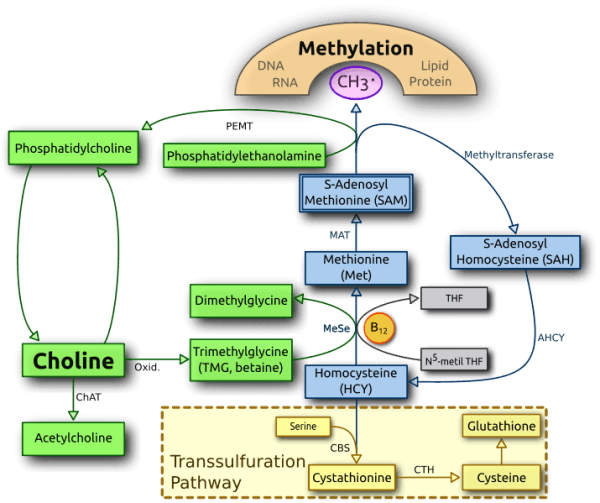
בצמחים, הצעד הראשון בביו-סינתזה de novo של כולין הוא הדה-קרבוקסילציה של של serine לאתנולאמין, המקוטלז על ידי האנזים serine decarboxylase (Rontein וחב' ב-J Biol Chem משנת 2003). הסינתזה של כולין מאתנולאמין יכולה להתרחש ב-3 מסלולים מקבילים, בהם שלושה שלבים רציפים של N-מתילציה מקוטלזים על ידי methyl transferase ומתרחשים או על בסיס חופשי (Prud'homme ו-Moore), או על בסיס של בסיסים פוספטיים (Nuccio וחב' ב-J Biol Chem משנת 2000), או על בסיסים פוספטידיליים (McNeil וחב' ב־Proc Natl Acad Sci USA משנת 2001). המקור של קבוצת המתיל הוא ה-S-adenosyl-L-methionine, כאשר S-adenosyl-L-homocysteine נוצר כתוצר צדדי. באדם וברוב בעלי החיים, הסינתזה de novo של כולין מתקדמת דרך מסלול ה-phosphatidylethanolamine N-Imethyltransferase (להלן PEMT), אך ביוסינתזה זו אינה מספיקה לספק את דרישות האדם (Zeisel וחב' ב-Ann Nutr Metab משנת 2012). במסלול הכבדי של PEMT, 3phosphoglycerate (להלן 3PG) מקבל 2 קבוצות אציל מ-acyl-CoA ליצירה של חומצה פוספטידית, ומגיב עם cytidineIn triphosphate ליצור cytidine diphosphate-diacylglycerol. אנזים PEMT נוטל 3 קבוצות מתיל משלושה תורמי S-adenosyl methionines ומעבירם לקבוצת אתנולאמין של phosphatidylethanolamine ליצירה של כולין בצורת phosphatidylcholine. בתהליך זה שלושה S-adenosylhomocysteines (להלן SAHs) נוצרים כתוצרים צדדיים. כולין יכול גם להשתחרר מקודמנים יותר מורכבים. לדוגמה, פוספטידילכולינים יכולים לעבור הידרוליזה לולין ברוב סוגי התאים, והוא יכול גם להיווצר במסלול CDP-choline, וכן על ידי choline kinases ציטוזולי המזרחן כולין עם ATP ליצירת phosphocholine. התהליך האחרון מתרחש בתאי הכבד והכליות. Choline-phosphate cytidylyltransferases (להלן CPCT) מתמיר PChol ל-CDP-choline עם cytidine triphosphate (להלן CTP). באדם, מספר מוטציות באנזים PEMT וחסר אסטרוגן (לרוב בתקופת חידלון הווסת), מגבירים את הצורך לכולין. במכרסמים, 70% מה-phosphatidylcholines מיוצרים דרך מסלול ה-PEMT, ורק 30% דרך מסלול CDP-choline. בעכברי knockout, אינאקטיבציה של PEMT הופכת אותם לחלוטין תלויים בכולין דיאטתי.
ספיגת כולין
באדם, כולין נספג מהמעיים על ידי החלבון הממברנלי SLC44A1 (CTL1) בתהליך של דיפוזיה המנוהלת על ידי גרדיאנט של ריכוז כולין והפוטנציאל החשמלי החוצה את הממברנות של אנטרוציטים. ל-SLC44A1 יש יכולת מוגבלת לשמש לטרנספורט של של כולין, כאשר בריכוז גבוה של האחרון חלק ממנו לא נספג. הכולין הנספג עוזב את האנטרוציטים דרך הווריד השערי של הכבד, עובר את הכבד ונכנס לצירקולציה הסיסטמית. חיידקי המעי מפרקים את הכולין שלא נספג ליצירת TMA, המחומצן בכבד ל-trimethylamine N-oxide. פוספוכולין ו-glycerophosphocholines, עוברים הידרוליזה דרך פוספוליפאזות ליצירת כולין, הנכנס לווריד השער. תרכובות המכילות כולין מסיס בשומן כגון phosphatidylcholines וספינגומיאלינים, עוברות הידרוליזה על ידי פוספוליפאזות או שהן נכנסות ללימפה שם הן מותמרות לכילומיקרונים.
הובלה
באדם, כולין עובר טרנספורט דם כיון (ion) חופשי. פוספוליפידים המכילים כולין ותרכובות אחרות כגון glycerophosphocholines מועברים בליפופרוטאינים בדם. רמות של כולין בפלזמת הדם של מבוגרים בריאים בצום הן 7–20 מיקרומולר לליטר (μmol/L), ו-10 מיקרומולר בממוצע. רמות אלו מוגברות בערך 3 שעות לאחר צריכת כולין. רמות פוספטידילכולין בפלזמה של מבוגרים בצום הן 1.5-2.5 מיקרומולר. צריכת כולין מעלה את רמות כולין חופשי לפרק זמן של 8–12 שעות, אך אינה משפיעה על רמות פוספטידילכולין באופן משמעותי. כיוון שכולין מסיס במים הוא נזקק לטרנספורטרים לסייע לו לחצות את ממברנת התאים המסיסה בשומן. ידועים שלושה טרנספורטרים של כולין (Inazu ב-Nutrients משנת 2019):
- SLC5A7 הוא טרנספורטר התלוי ב-sodium- (Na+) וב-ATP. יש לטרנספוטר זה זיקה גבוהה לכולין, והוא מעביר אותו לראשונה לנוירונים שם הוא מסייע ליצירה של אצטילכולין. חסר של טרנספורטר זה גורם לחולשה מולדת במערכת הריאות ובשרירים אחרים (Barwick וחב' ב-Am J Human Genet משנת 2012). עכברי knockout עם חסר זה בדרך כלל מתים כתוצאה מ-cyanosis ושיתוק. לטרנספורטרים מסוג CTL1s יש זיקה ממוצעת לכולין וטרנספורט כמעט בכל הרקמות כולל המעיים, הכבד, הכליות, השלייה והמיטוכונדריה.
- CTL1s מספקים כולין עבור יצירת פוספטידילכולין וטרימתילגליצין.
- טרנספורטרים מסוג CTL2s מופיעים בעיקר במיטוכונדריה של הלשון, הכליות, השרירים והלב. הם קשורים בחמצון המיטוכונדריה של כולין ל-טרימתילגליצין.
CTL1s ו-CTL2s אינם קשורים ליצירת אצטילכולין, אך מסוגלים לבצע טרנספורט של כולין דרך מחסום-דם-מוח (BBB). רק CTL2s נמצא בצד המוחי של המחסום. טרנספורטרים אלה מרחיקים עודף כולין מהנוירונים בחזרה לדם. לעומת זאת, CTL1s נמצא רק בצד הדמי של המחסום, אך גם על הממברנות של אסטרוציטים ונוירונים. CTL1s ו-CTL2s אינם קשורים ליצירה של אצטילכולין. הם מבצעים טרנספורט של כולין בזיקה נמוכה. CTL1s מבצע טרנספורט של כולין בעיקר בכבד ובכליות, בעוד ש-CTL2s מבצע טרנספורט של כולין בכליות ובמוח.
כולין במזון
כולין מופיע במזון כקטיון חופשי ובצורת פוספוליפידים בעיקר כ-phosphatidylcholines. הוא שכיח במיוחד בבשרים ובחלמון ביצה, אך הוא מופיע בריכוז נמוך יותר בדגנים, בירקות, פירות, ומוצרי חלב. שומני בישול מכילים כולין בריכוז של 5 מיליגרם/100 גרם של סך כולין. בארצות הברית ההמלצה היא על צריכה יומית של כולין של 550 מיליגרם (zeisel וחב' ב-J Nutr משנת 2003). חלב-אם עשיר בכולין והנקה מספקים לתינוק 120 מיליגרם כולין ליום. פורמולות לתינוקות חייבות להכיל לפחות 7 מיליגרם לכל 10 קילו-קלוריות של הפורמולה. באירופה, רמות של מעל 50 מיליגרם/100 קילוקלוריות אינן מותרות. להלן תכולת כולין בסוגי מזון שונים כאשר המספרים מבטאים תכולה של מיליגרם/100 גרם פריט מזון: Bacon-125; בשר אדום מבושל-78.2; כבד בקר-418.2; בשר עוף-78.4; כבד עוף-290.3; בשר חזיר-102.7; שרימפס-70.6; חמאה-18.8; גבינה-23.6; חלב-15.7; יוגורט-15.2; סובין של חיטה או שיבולת שועל-58.6; אורז לבן-2.1; נבטי חיטה-152.1; ביצים-251; פולי סויה-115.9; אגוזי אדמה (בוטנים)-52.5; טופו-27.4; ברוקולי-40.1; כרוב-15.4; תירס מתוק-21.95; אפונה-13; כרובית-39.1; גזר-8.8; מלפפון-5.9; חסה-8.1; ,תרד-22.1; תפוחי אדמה-13.1; עגבנייה-6.74; תפוחי עץ-3.44; אבוקדו-14.2; בננה-9.8; ענבים-7.53; תפוזים-8.4; תות שדה-5.6; אפרסק-6.1; אגס-5.1; אוכמנית-6.04; שזיף-9.7; אשכולית-5.63; אבטיח-6.3.
שנים עשר סקרים שבוצעו ב-9 מדינות של האיחוד האירופי בין השנים 2000 ו-2011, ביצעו הערכה של צריכת כולין על ידי מבוגרים במדינות אלו, ומצאו ערכים של 269-468 מיליגרם ליום. הצריכה הייתה 269-444 מיליגרם/יום בנשים מבוגרות, ו-332-468 מיליגרם/יום בגברים מבוגרים. בתינוקות/ילדים/נערים הצריכה היומית של כולין הייתה 75-127 מיליגרם בתינוקות, 151-210 מיליגרם/יום בילדים בני 1-3 שנה, 177-304 מיליגרם/יום בבני 3-10 שנה, ו-244-373 מיליגרם/יום בבני 10-18 שנה. הצריכה היומית הממוצעת של כולין, הייתה 336 מיליגרם בנערות הרות, ו-356 מיליגרם בנשים הרות. מחקר המבוסס על סקר NHANES בשנים 2009-2012 העריך שצריכת כולין הייתה נמוכה מדי במספר תת-אוכלוסיות. בקרב בני שנתיים ומעלה, רק 15.6±0.8% מבין הזכרים ו-6.1±0.6% מבין הנקבות צרכו יותר מהצריכה המומלצת. מדובר ב־62.9±3.1% מבין אלה בני שנתיים עד שלוש שנה שצרכו יותר כולין ממה מומלץ, 45.4±1.6% בני 4-8 שנה שצרכו יותר כולין מהמומלץ, 9.0±1.0% בני 9–13 שנה צורכי כולין מעל המומלץ, 1.8±0.4% בני 14–18 המרבים בצריכת כולין, ו- 6.6±0.5% בני 19 שנה ומעלה שהירבו בצריכת כולין (Imbard וחב' ב־Int J Environmental Research and Public Health משנת 2013).
סימנים ותסמינים
חסר סימפטומטי באדם נדיר. רוב האנשים מקבלים די כולין מהמזון או מסוגלים לסנתז כמויות מוגבלות של כולין דרך PEMT. חסר חמור של כולין גורם נזק לשרירים כמו גם מחלת כבד שומני לא-אלכוהולי, העלול להתפתח לשחמת הכבד. פרט לאדם, כבד שומני הוא סימן אופייני לחסר כולין בחיות אחרות. דימום בכליות עלול להופיע במספר סוגי חיות, כתוצאה מחסר של טרימתילגליצין שמקורו בכולין, שכו טרימתילגליצין מתפקד כווסת אוסמוטי.
צריכת יתר
נטילת יתר של כולין עלולה לגרום לתופעות לוואי. צריכה יומית של 8–20 גרם כולין יכולה לגרום ללחץ-דם נמוך, הזעות, בחילה, הקאות, שלשולים וריח גוף דמוי זה של דגים. הכבד מחמצן TMA ל-trimethylamine N-oxide (להלן TMAO). רמות גבוהות של TMA ו-TMAO בגוף נכרכו בטרשת עורקים ובתמותה. עם זאת, צריכה מוגברת של כולין לא נמצאה גורמת לתמותת-יתר מחלות קרדיו-וסקולריות (Wiedeman וחב' ב-Nutrients משנת 2018).
התפתחות העובר וסגירת הצינור העצבי
צריכה מועטה של כולין על ידי אישה הרה כרוכה בסיכון למפגעים של הצינור הנוירלי בעובר. לעומת זאת, צריכת כולין גבוהה של האם ההרה כרוכה בהתפתחות נוירו-קוגניטיבית טובה יותר של העובר. כולין וחומצה פולית המגיבים עם ויטמין B12, משמשים כתורמים של קבוצת מיל להומוציסטאין ליצירת מתיונין המתפתח ל־S-adenosylmethionine (להלן SAM), שהוא המצע של כמעט כל ריאקציות המתילציה ביונקים. מוטציות אחדות הפוגעות במטבוליזם של כולין מגבירות את השכיחות של פגמים בצינור העצבי בעובר. היריון והנקה מגבירים דרמטית את הדרישה לכולין. דרישה זו מולאה על ידי רגולציה מוגברת של PEMT, על ידי הגברת רמות אסטרוגן ליצירה מוגברת של כולין de novo. נתון זה מודגם על ידי הממצא שבעכברים -/-PEMT החסרים PEMT מתפקד, העובר ימות ביום ההיריון 9–10 אלא אם כן יזינו את העכברות בכולין (Caudill ב-J Am Dietetic Assoc משנת 2010). בה בשעה שמאגרי כולין מתרוקנים במהלך הריון והנקה, השלייה צוברת כולין כאשר נוזל השלייה יכול להיות פי-10 עשיר יותר בכולין בהשוואה לדם האם. החיוניות של כולין במהלך היריון היא בגין היותו כרוך לבניית ממברנות תאים המהירה מאוד בעובר. כולין חיוני גם בצורך המוגבר למולקולות חד-פחמניות הנחוצות למתילציה של DNA, לצורך של הגברת מאגרי כולין בשלייה, ולצורך של יצירה מוגברת של ליפופרוטאינים (King ב-Am J Clin Nutrit משנת 2000). במיוחד יש עניין בהשפעה של יצירת כולין על המוח. גדילת המוח מהירה ביותר בשליש השלישי של ההיריון, וצמיחת מוח זו ממשיכה להיות בולטת עד גיל 5 שנה. בפרק זמן זה של היריון יש דרישה מוגברת לספינגומייאלין המיוצר מפוספטידילכולין הנחוץ למיאלינציה של שלוחות תא העצב (Oshida וחב' ב-Pediatr Res משנת 2003). כולין נדרש במהלך ההיריון ליצירה של הנוירוטרנמיטר אצטילכולין, שמשפיע על המבנה של אזורי מוח, לנוירוגנזה, וליצירת סינפסות. אצטילכולין נמצא גם בשלייה ועשוי לסייע בבקרה של שגשוג תאים והתמיינותם (Sastry וחב' ב-Biochem Pharmacol משנת 1997).
מחלות קרדיו-וסקולריות וסרטן
חסר כולין עלול לגרום לכבד שומני, המגביר את סיכון לסרטן ולמחלות קרדיו-וסקולריות. חסר בכולין מפחית את יצירת SAM הכרוך במתילציה של DNA מה שעלול להגביר קרצינוגניות.
שימושי כולין
כולין כלוריד ו-choline bitartrate משמשים כתוספי מזון. Bitartrate משמש לעיתים יותר תכופות בגלל ההיגרוסקופיות הנמוכה שלו. מספר מלחי כולין משמשים כתוספים לתרנגולות, תרנגולי הודו ומספר חיות אחרות. Choline theophyllinate ו-choline salicylate משמשים כתרופות כגון methacholine ו-carbachol. כולין מסומן רדיו-אקטיבית כגון 11C-choline משמש להדמיה רפואית. מלחי כולין זמינים מסחרית כגון tricholine citrate ו-choline bicarbonate.
הוראות לביצוע הבדיקה
את הדם יש להכניס למבחנה כימית (פקק אדום) או למבחנת ספירת-דם (מכילה EDTA פקק סגלגל). לאחר הסרכוז יש לקחת נוזל עליון (נסיוב או פלזמה) ולהעביר למבחנת פלסטיק לצורך העברה למעבדה.
הבדיקה מתבצעת בשיטת ELISA או בשיטת LC-MS/MS.
ראו גם
המידע שבדף זה נכתב על ידי פרופ' בן-עמי סלע, המכון לכימיה פתולוגית, מרכז רפואי שיבא, תל-שומר;
החוג לגנטיקה מולקולארית וביוכימיה, פקולטה לרפואה, אוניברסיטת תל-אביב (יוצר הערך)


 כניסה
כניסה  עקבו אחרינו בפייסבוק
עקבו אחרינו בפייסבוק