ריקוורין - Recoverin
| מדריך בדיקות מעבדה | |
| ריקוורין | |
|---|---|
| Recoverin | |
| שמות אחרים | RCVRN ,RCV1. |
| מעבדה | כימיה בדם |
| תחום | חלבון המשחק תפקיד חשוב במערכת הראייה |
| טווח ערכים תקין | שלילי |
| יוצר הערך | פרופ' בן-עמי סלע |
מטרת הבדיקה
הערכה של מטופלים עם חשד לרטינופתיה פארא-נאופלסטית (תסמונת פארא-נאופלסטית) בעקבות קרצינומה של תאים קטנים (Small cell carcinoma).
כללי
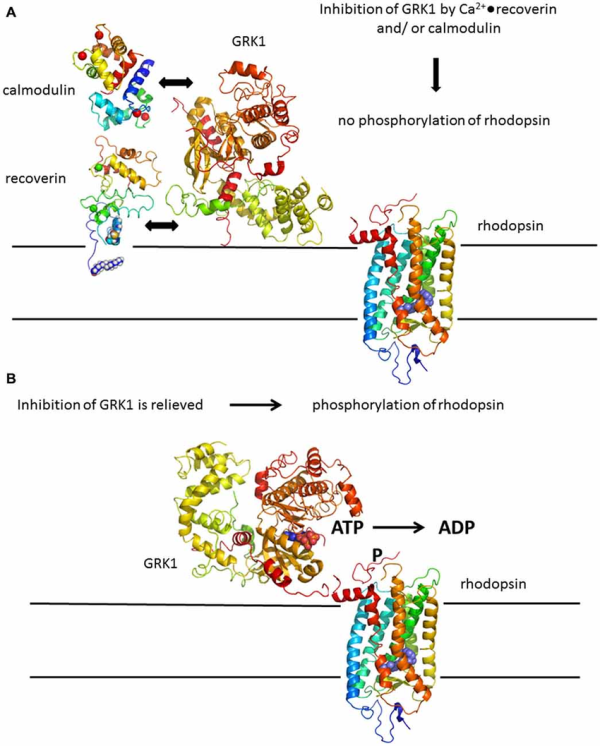
Recoverin הוא חלבון נוירונלי הקושר סידן שמשקלו 23 קילו-דלטון שהוא לרוב מתגלה בתאים הפוטו-רצפטוריים בעין (Murakami וחב' ב-Biochem Biophys Res Commun משנת 1992). חלבון זה משחק תפקיד מפתח בעיכוב של rhodopsin kinase, אנזים המווסת את הזרחון של rhodopsin (Chen וחב' ב-J Biol Chem משנת 1995). הפחתה של עיכוב זה מווסתת התאמה סנסורת של הרשתית, כיוון שסגירת התעלות התלויה באור בפוטו-רצפטורים גורמת לרמות הסידן לרדת, מה שמקל על עיכוב rhodopsin kinase על ידי recoverin הקשור לסידן, מה שמוליך לאינאקטיבציה מהירה יותר של metarhodopsin שהיא הצורה המשופעלת של rhodopsin.
המבנה
ה-recoverin מורכב מ-4 EF-hand motifs המאורגנים בצורה קומפקטית, המנוגדת לצורה המִשְׁקוֹלִית של חלבונים קושרי-סידן אחרים כגון calmodulin ו-troponin C (Flaherty וחב' ב-Cell משנת 1993). Recoverin עובר שינוי קונפורמציה באופן התלוי ב-Ca+2. חלבון זה עובר מיריסטולציה בקצה האמינו-טרמינלי שלו (Ray וחב' ב-Proc Natl Acad Sci USA משנת 1992). קבוצת המיריסטויל עוברת הפרדה בבְּקִיעַ ההידרופובי של החלבון בצורתו שאינה קשורה ל-Ca+2. כאשר recoverin נקשר ל-Ca+2, קבוצת המיריסטויל מסולקת ומוחדרת לתוך הממברנות של ה-rod (קָנֶה, אחד מקבוצת תאים ברשתית העין) (Ames וחב' ב-Nature משנת 1997), ובכך כנראה מקילה על האינטראקציה עם ה-GRK1 (או ה-rhodopsin kinase) הקשור לממברנה. שיירי חומצות אמינו ספציפיים נחשפים ל-recoverin ובכך יוצרים אתר המעכב את GRK1 (Valentine וחב' ב-Biochemistry משנת 2003, ו-Tachibanaki וחב' ב-J Biol Chem משנת 2000). דווח על מבנים של מיריסטויל ו-recoverin עם או בלי Ca+2 קשור (Tanaka וחב' ב-Nature משנת 1995). הרשתית של בעלי חוליות מכילה 2 סוגים של פוטו-רצפטורים: rods ו-cones (או קנים ומדוכים). הקנים נלמדו בצורה יותר אינטנסיבית מאשר המדוכים בגלל הכנתם היותר פשוטה. הקנים מגיבים לאור על ידי יצירת תגובה חשמלית מקוטבת יותר דרך קסקדה של פוטו-רדוקציה הממוקמת במקטע החיצוני יותר של הקנה המותאם למצבי אור שונים, על ידי הפחתת רגישותם למנוע ריוויון, ובכך יש הגברה של פעילותם במגוון עוצמות אור בטמפרטורת החדר. תהליך זה של הסתגלות לאור, כרוך בשינויים בקסקדה של הפוטו-רדוקציה המתרחשת ברמות נמוכות יותר של Ca+2 בקנים במהלך חשיפה לאור (Nakatani ו-Yau ב-Nature משנת 1988). הצעד הראשון בקסקדה הוא ספיגת אור על ידי פיגמנטים ויזואליים. רודופסין משופעל מגרה בערך 100 מולקולות של transducin בשנייה, לאתחול הקסקדה. צורה זו של רודופסין משפעלת חלבון G שמעביר את הסיגנל. חלבון ה-G שמגיב עם רודופסין נקרא טרנסדוצין. קנה של רודופסין 2 מפעיל את השחלוף של GDP ב-GTP בתת-יחידה α של טרנסדוצין. לאחר השפעול של הפוטו-רדוקציה, רודופסין עובר אינאקטיבציה. אף על פי שרודופסין דועך לאחר זמן, rhodopsin kinase פוחת מהר יותר במהלך זרחון. Recoverin משחק תפקיד בתהליך זה על ידי עיכוב הזרחון של רודופסין ברמות גבוהות של Ca+2 (Kawamura וחב' ב-J Biol Chem משנת 1993), על ידי קישור ל-rhodopsin kinase ופחות לרודופסין (Chen וחב' ב-J Biol Chem משנת 1995), ובכך מאריך את משך החיים של רודופסין. הבנת התפקיד של recoverin בהסתגלות לאור, דורשת הבנה ש-Ca+2 גבוה בחשכה ונמוך בתנאי אור (Yau ו-Nakatani ב-Nature משנת 1985). לפיכך, הבזק אור בחשכה מגרה תגובה מתמשכת כיוון ש-recoverin בתנאי Ca+2 גבוהים מעכב את rhodopsin kinase, הגורם תקופת חיים ממושכת יותר של רודופסין. מיקום הגן המקודד ל-recoverin הוא Chr 17: 9.9 – 9.91.
מחקרים פיזיולוגיים גילו שהזרקת recoverin לתוך קנים של Gecko האריכו את משך התגובה לאור (Gray-Keller וחב' ב-Neuron משנת 1993), בעוד שהחסר ב-recoverin בקנים של עכברים, הפחית משך זה (Makino וחב' ב-J General Physiol משנת 2004) המתאים לציפיות. עם זאת, המחקר בעכברים גילה שחסר של recoverin אינו משפיע על התגובה לאור או על שיא התגובה, ומסייעת להתאוששות משך התגובה. תוצאות אלו ניתנות להסבר כאשר הזרחון של רודופסין מתרחש מיד לאחר שיא התגובה בקנים (Kawamura ו-Tachibanaki ב-Prog Retinal Eye Res משנת 2022). הזרחון של הקנים מתרחש לפני שהתגובה מגיעה לשיאה. כיוון שאמפליטודת התגובה קובעת את הרגישות לאור של הפוטו-רצפטורים, recoverin משפיע באופן מינימלי על הרגישות של הבזק-אור בודד של עכברי-בר. עם זאת, תחת אור מתמשך, אמפליטודת התגובה ורגישותה, נמוכה יותר בעכברים החסרים recoverin בהשוואה לעכברי-בר (Sampath וחב' ב-Neuron משנת 2005). כתוצאה מכך, recoverin מרגש את הקנים באירוע של אור יציב בעכברי-בר, מה שמאפשר להם לזהות אור מתמשך חלש, שהיה קשה לזהות ללא חלבון זה. בחשכה, בערך 10% מסך ה-recoverin ברשתית עין העכבר ממוקם בקנים, ושאר החלבון ממוקם בתאי הקנים (Polans וחב' ב-J Cell Biol משנת 1991). תחת אור הקנים עוברים טרנסלוקציה לקראת הטרמינלים הסינפטיים, מה שמציע של-recoverin יש תפקידים בנוסף לשליטה באורך החיים של רודופסין, כגון הגברה של העברת סיגנל מהקנים לתאי הקנים הדו-קוטביים (Dizhoor וחב' ב-Science משנת 1991). ה-recoverin הוא גם אנטיגן במקרי רטינופתיה הכרוכה בסרטן (Kawamura ו-Murakami ב-Nature משנת 1991). שני חלבונים, recoverin בבקר, והאורטולוג שלו בצפרדע, S-modulin, דווחו בשנת 1991 כחלבונים הכרוכים בהסתגלות לאור בפוטו-רצפטורים של הקנים.
יוני סידן (2+Ca) הם למעשה messenger שני המווסתים מגוון גדול של מסלולי איתות בכל סוגי התאים, כולל אלה במוח וברשתית. חלבונים קושרי יוני סידן, השייכים למשפחת הסנסורים הנוירונליים לסידן, מזהים 2+Ca נוירונלי (Burgoyne וחב' ב-Trends Neurosci משנת 2004, ו-Weiss וחב' ב-Cell Mol Neurobiol משנת 2010). בדומה לחברי משפחה אחרים, recoverin מכיל ארבעה EF hand motifs, ושרשרת מיריסטויל בקצה ה-N-טרמינלי. רק שניים מה-EF hands (EF2 ו-EF3) קושרים 2+Ca של species אחרים (Senin וחב' ב-J Biol Chem משנת 2002, ו-Lamb ו-Hunt ב-Open Biol משנת 2018). Recoverin עובר שינוי קונפורמציה בעת הקישור ל-2+Ca בחשכה, ובהתאם נקשר למקטע החיצוני של ממברנת הפוטו-רצפטור (Tanaka וחב' ב-Nature משנת 1995, ו-Ames וחב' ב-J Biol Chem משנת 1995). הדבר, מאפשר קישור של G protein-coupled receptor kinases (או GRK). קישור של recoverin ל-2+Ca מעכב את GRK ועל ידי כך מונע את זרחון הפיגמנט הוויזואלי. בתנאים של אור בהיר, 2+Ca עובר דיסוסיאציה מ-recoverin והחלבון עובר טרנסלוקציה למקטע הפנימי. ה-GRK המשתחרר מסוגל כעת לזרחן ולגרום לרה-שפעול באור של הפיגמנט הוויזואלי (Strissel וחב' ב-J Biol Chem משנת 2005). מנגנון זה מותנה כחלק מהמשוב השלילי של 2+Ca במהלך האדפטציה לאור. מחקרים עדכניים מדגימים את התפקידים הנוספים של recoverin בוויסות של משך PDE והטרנסמיסיה הסינפטית (Sampath וחב' ב-J Gen Physiol משנת 1999, ו-Chen וחב' ב-J Gen Physiol משנת 2010, ו-Chen וחב' ב-J Gen Physiol משנת 2015).
הוראות לביצוע הבדיקה
יש ליטול דם למבחנה כימית (פקק אדום או צהוב) או למבחנת ג'ל, ולאחר סרכוז יש להעביר את הנסיוב למבחנת פלסטיק.
מידע על יציבות הדגימה: דגימה מקוררת (מועדפת) - 28 יום, דגימה קפואה - 28 יום, דגימה בטמפרטורת החדר - 72 שעות.
שיטת המדידה: Immunoblot.
ראו גם
המידע שבדף זה נכתב על ידי פרופ' בן-עמי סלע, המכון לכימיה פתולוגית, מרכז רפואי שיבא, תל-שומר;
החוג לגנטיקה מולקולארית וביוכימיה, פקולטה לרפואה, אוניברסיטת תל-אביב (יוצר הערך)


 כניסה
כניסה  עקבו אחרינו בפייסבוק
עקבו אחרינו בפייסבוק