אבחון מולקולרי של מחלות מונוגניות בילדים ובמבוגרים - נייר עמדה
ערך זה נמצא בבדיקה ועריכה על ידי מערכת ויקירפואה, וייתכן כי הוא לא ערוך ומוגה.
|
| |
|---|---|
| אבחון מולקולרי של מחלות מונוגניות בילדים ובמבוגרים | |
| תחום | גנטיקה |
| 250px | |
| האיגוד המפרסם | איגוד הגנטיקאים הרפואיים בישראל |
| סימוכין | באתר הר"י נייר קודם מ-2016 |
| קישור | באתר הר"י |
| תאריך פרסום | אפריל 2025 |
| יוצר הערך | ד"ר קארין ויס; ד"ר דפנה מרום; ד"ר אהוד בן; ד"ר אמיר פלג; ד"ר תמר פפרנה; רותם גרינברג |
| ניירות עמדה מתפרסמים ככלי עזר לרופא/ה ואינם באים במקום שיקול דעתו/ה בכל מצב נתון. כל הכתוב בלשון זכר מתייחס לשני המגדרים. | |
מושגים
- מחלה מונוגנית (מנדליאנית) - Monogenic / Mendelian disorder -מחלה הנגרמת עקב פגיעה בגן בודד ובעלת תבנית הורשה מנדלית מוכרת
- הורשה רב-גורמית - Multifactorial inheritance - מצב קליני על רקע שאינו מונוגני אלא שילוב של מספר גורמים גנטיים וסביבתיים
- הורשה פוליגנית - Polygenic inheritance - מצב קליני על רקע שילוב של מספר שינויים גנטיים בגנים שונים
- שיטות ריצוף מתקדמות - ריצוף מקבילי, ריצוף מהדור הבא next generation sequencing / massive parallel sequencing/ - שיטה המאפשרת ריצוף של מספר רב של מקטעי דנ"א במקביל
- בדיקות ריצוף כלל גנומיות - ריצוף אקסום, ריצוף גנום exome sequencing / genome sequencing - ריצוף הכולל את מרבית האזורים המקודדים )אקסום (או מרבית רצף הדנ"א בכללותו (גנום)
- ממצאים אקראיים - incidental findings - ממצא אבחנתי שמאותר בבדיקה כלל גנומית ואינו קשור לסיבת הבדיקה
- ממצאים שניוניים - secondary findings - ממצא אבחנתי אקראי בגן המופיע ברשימה מקובלת של גנים (actionable genes), ששינויים גורמי מחלה בהם, מומלצים לדיווח עקב משמעות קלינית במניעה וטיפול. הדיווח הוא בכפוף להסכמה מדעת שניתנת בכתב על ידי הנבדק (או הוריו במקרה של קטין)
רקע ומבוא
מטרת מסמך זה לפרט ולעדכן את עמדת איגוד הגנטיקאים הרפואיים בישראל לגבי אבחון מולקולארי קליני בילדים ומבוגרים חשודים כחולים במחלה מונוגנית. מאז פרסום נייר העמדה הקודם (2016), התבססה ונקבעה עליונותן של בדיקות ריצוף כלל-גנומיות באבחון מהיר ומדויק של מחלות מונוגניות בכללותן, בהשוואה לאבחנה על בסיס קריטריונים קליניים, בדיקות הדמיה ומעבדה אחרות. במקביל להוזלת עלויות, חל שיפור משמעותי בזמינות ובנגישות לשימוש בטכנולוגיות ריצוף מתקדמות, וקיצור משמעותי של משך הבדיקה וקבלת התוצאות (ממספר חודשים לשבועות ספורים ואף ימים). בנוסף, הצטבר ידע רב לגבי תרומתן באבחון ובטיפול בחולים במחלות מונוגניות בכל תחומי הרפואה, וכן בתכנון משפחה. גישה של בירור גנטי כקו ראשון בבירור חשד למחלה מונוגנית היא בעלת יתרון כלכלי משמעותי בשל חיסכון וייעול הוצאות רפואיות נלוות, לרבות בדיקות מעבדה והדמיה, הליכים פולשניים, משך אשפוז וטיפול מותאם ברשימה הולכת ומתארכת של מחלות מונוגניות, ובחולים קריטיים. לפיכך, מצאנו לנכון לעדכן את נייר העמדה כפי שמפורט במסמך זה. נייר עמדה זה אינו דן באבחון הגנטי הטרום לידתי, בשימוש בטכנולוגיות ריצוף מתקדמות כבדיקת סקר לאוכלוסייה בריאה בילודים/ילדים/מבוגרים כולל סקר לאיתור זוגות בסיכון ללידת ילד חולה במחלה גנטית חמורה, או בבדיקות המתבצעות במסגרת מחקר. סוגיות מורכבות אלו הן מעבר לתחום עיסוקו של נייר עמדה זה.
מחלות מונוגניות מוגדרות כמחלות שנגרמות על ידי שינוי בגן בודד, לרוב גורמות למחלות כרוניות קשות, מלוות תחלואה גבוהה ולעיתים קיצור תוחלת חיים. רובן מוגדר כמחלות נדירות, אך שכיחותן המצטברת באוכלוסייה לפחות 5%-10% [1]. מרביתן מסתמנות בגיל הילדות, אך שיעורן במבוגרים מגיע לפחות ל-1%-2%[2]. ההסתמנות הפנוטיפית של מחלות מונוגניות היא רחבה ביותר וכוללת את כל תחומי הרפואה: מומים מולדים ועיכוב התפתחותי/לקות שכלית, מחלות נוירולוגיות, מחלות לב ורקמת חיבור, מחלות כליה מבודדות, לקויות ראייה ולקויות שמיעה, מחלות אנדוקריניות ובמערכת העיכול, מחלות דלקתיות, חסר חיסוני ועוד.
בתלות בפנוטיפ הקליני, יעילות האבחון של בדיקות גנטיות נע בין 20%-70% בילדים ומבוגרים. שיעור יעילות זה גבוה לעין ערוך בהשוואה ליעילות אבחון בירור סטנדרטי המוערך באחוזים בודדים בלבד. בסקירה סטטיסטית שפורסמה על ידי הקולג' האמריקאי לגנטיקה רפואית (American College of Medical Genetics) ACMG (כללה 25 מחקרים שהקיפו למעלה מ-2100 ילדים עם איחור התפתחותי ו/או מומים מולדים), נמצא כי לבדיקות ריצוף כלל-גנומיות הייתה השפעה קלינית משמעותית. בדיקה אבחנתית או לא אבחנתית הובילה להשפעה על המלצות טיפוליות כולל פולשניות ועל מעקבים והפנייה למומחים ב-8% וב-10% מהמקרים, בהתאמה. בנוסף על פי אותה סקירה נמצאה השפעה על תכנון ילודה ב-9% מהמשפחות[3]. בתינוקות עד גיל שנה המאושפזים ביחידות טיפול נמרץ ומתייצגים עם פנוטיפים לא מוסברים שביצעו ריצוף גנום, הודגם שיעור אבחון ממוצע של 37% (טווח 30%-46%) והשפעה מיטבית על ניהול המקרה בכ-35% מהמקרים[4]. ברוב המחלות המונוגניות (אך לא בכולן) היעילות האבחנתית של ריצוף כלל גנומי גבוהה יותר בהשוואה לבדיקות גנטיות ממוקדות כגון ריצוף גן בודד וריצוף או פענוח ממוקד לרשימת גנים (פאנל).
מידע זה הביא לעדכון ההנחיות לשימוש בבדיקות ריצוף מתקדמות בחולים על ידי מספר איגודים מקצועיים בעולם. ה-ACMG ממליץ משנת 2021 על ריצוף אקסום או גנום כבדיקת הבחירה הראשונה (או השנייה במקרים של חשד לאטיולוגיה גנטית ספציפית) באבחון של כל ילד צעיר מגיל שנה עם לפחות מום מבני אחד ובכל ילד צעיר מגיל 18 שנים עם עיכוב התפתחותי או לקות שכלית (ללא ציון דרגת חומרה)[5]. הקולג' הקנדי לגנטיקה קלינית הרחיב כבר ב-2015 את ההמלצה לריצוף אקסום או גנום כבדיקה אבחנתית ראשונה לכל חולה ללא הגבלת גיל, עם חשד קליני למחלה מונוגנית[6].
שיטות לביצוע בדיקות רצף דנ"א לצורך אבחון מחלות מונוגניות
בדיקת רצף דנ"א בשיטת סנגר (Sanger)
שיטה זו מאפשרת ריצוף של מקטעי דנ"א ארוכים יחסית של מאות בסיסים תוך שימוש בתחלים (פריימרים) סגוליים למקטע אותו מעוניינים לבדוק. השיטה נחשבת לאמינה ומדויקת. שיטה זו ממוקדת לריצוף גן בודד או שינוי יחיד החשוד כגורם למחלה או לזיהוי שינויים באזורים קשים לריצוף בשיטות ריצוף מתקדמות.
בדיקת רצף בשיטות ריצוף מתקדמות (NGS)
השיטה מאפשרת ריצוף במקביל של כמות גדולה מאוד של מקטעי דנ"א. השיטה השכיחה בקליניקה היא short read sequencing בה מרוצפים מקטעים באורך ממוצע של כ-150 בסיסים. בשיטה זו מתקבלים תוצרי ריצוף רבים (עשרות עד אלפי תוצרים) של כל מקטע גנומי.
"עומק קריאה" (read depth) - מבטא את מספר העותקים שרוצפו במיקום גנומי מסוים. לדוגמה עומק קריאה ממוצע 30X בריצוף אקסום מבטא 30 עותקים בממוצע של תוצרי ריצוף לאורך הגנום.
"כיסוי בדיקה" (coverage) - מספר המבטא את שיעור האזור הגנומי שאכן רוצף בבדיקה. לדוגמה, שיעור כסוי של 97% של האזור המקודד, מבטא מצב בו 97% מכלל האקסונים בגנום אכן עברו ריצוף.
שני הפרמטרים הנ"ל ניתנים לשליטה על ידי יישומים שונים של השיטה, ועשויים להיות שונים בין מעבדות שונות. לאחר הריצוף, בעזרת תוכנות ביואינפורמטיות, מתבצעת התאמה (alignment) של המקטעים שרוצפו לרצף ייחוס (reference), הערכת איכות (quality), איתור שינויים ברצף הנבדק בהשוואה לרצף הייחוס, ופירוט המאפיינים שלהם (variant calling and annotation). בשלב הבא מתבצע פענוח (analysis) של תוצאות הריצוף על מנת לאתר שינויים גנטיים שיכולים להסביר את הפנוטיפ.
- לשיטה זו מספר יישומים
- ריצוף גן בודד או פאנל (קבוצת גנים הקשורים לאבחנה מסוימת). בדיקת פאנל ייעודית כוללת לרוב עומק קריאה גבוה וכיסוי מלא של הגנים בפאנל שמאפשר זיהוי של כל השינויים הנקודתיים באזורים מקודדים, חסרים / עודפים של שני אקסונים ויותר, ואף יכולה לעיתים לכלול אזורים אינטרונים שבהם דווח בעבר על שינוי פתוגני
- ריצוף אקסום (Exome sequencing) - כולל ריצוף של כל האזורים המקודדים לחלבון. בפועל שיעור הכיסוי הוא לרוב 95%-98% מכלל האזורים המקודדים, כתלות בשיטה בה מתבצעת לכידת הרצפים הרלוונטיים (capture kit). ריצוף אקסום ניתן לבצע לנבדק החולה בלבד (אקסום יחיד, singleton) או לנבדק החולה ולהוריו (אקסום טריו, trio WES). לרוב קיימת עדיפות לריצוף אקסום טריו בשל שיעור אבחון גבוה יותר ובשל חיסכון זמן בבדיקת הורים לשינויים בעלי משמעות לא ידועה או אישור הורשה רצסיבית מורכבת[5]. ניתן להשתמש בפלטפורמת האקסום לביצוע פענוח ממוקד לרשימת (פאנל) גנים virtual gene panel. היתרון בדרך זו הוא שניתן לעדכן את רשימת הגנים הנבדקים בקלות. החיסרון הוא שהכיסוי ועומק הריצוף עשוי להיות תת-מיטבי בהשוואה לבדיקת פאנל ייעודית
- ריצוף גנום (Genome sequencing) - ריצוף כל הדנ"א בגנום, כולל אזורים שאינם מקודדים לחלבון. לריצוף גנום יש יתרון בכך שהוא מאפשר זיהוי חסרים ועודפים בצורה מדויקת יותר בהשוואה לריצוף אקסום, ומאפשר זיהוי שינויים באזורים שאינם מקודדים כגון אינטרונים. בסדרות שונות בילדים ומבוגרים, שעברו בירור על ידי ריצוף אקסום, ולא נמצא גורם גנטי למחלתם, יעילות ריצוף הגנום המלא הייתה נמוכה יחסית - 5%-8% תוספת לגילוי הגורם בבסיס מחלתם[7]
- Long read sequencing - טכנולוגיות אלו כוללות ריצוף מקטעי דנ"א ארוכים - פי 100 ועד פי 10,000 באורכם ביחס למקטעי short read. שיטה זו מאפשרת ריצוף של אזורים חזרתיים, פסאודוגנים, וזיהוי שינויים מבניים וכמותיים מורכבים באמינות גבוהה יותר. נכון לכתיבת נייר עמדה זה, טכנולוגיות אלו מיושמות במסגרת מחקרית.
שיטות נוספות
במקרים של חשד לאטיולוגיות גנטיות ספציפיות קיים לעיתים צורך בשיטות אבחון ייחודיות כגון בדיקת דפוס מתילציה, בדיקה לשינויים חזרתיים repeat disorders, בדיקת MLPA לחסרים ועודפים, בדיקת רנ"א, בדיקות ממוקדות לדנ"א מיטוכונדריאלי, בדיקה ממוקדת לרקמה חולה. בדיקות הריצוף אינן מזהות שינויים אפיגנטיים. בתוצרים של ריצוף גנום ניתן לזהות חלק מהשינויים מסוג triple repeats כתלות באלגוריתם הביואינפורמטי האנליטי של הבדיקה. כמו כן, ניתן לאתר שינויים נקודתיים בגנום מיטוכונדריאלי ברוב ריצופי האקסום, כולל שינויים הטרופלזמיים. הסבר ודיון מעמיק בטכנולוגיות הבדיקות הנ"ל אינו חלק מנייר עמדה זה.
התוויות לבירור גנטי מולקולרי
ההחלטה לגבי הצורך בבירור מולקולרי צריכה להתבסס על הערכה קלינית הקובעת כי:
- קיים חשד משמעותי לאטיולוגיה מונוגנית המסבירה את התסמינים בנבדק
- לאבחנה יש משמעות קלינית מבחינת המעקב והטיפול בחולה או בני משפחתו, כולל מניעה של הישנות במשפחה
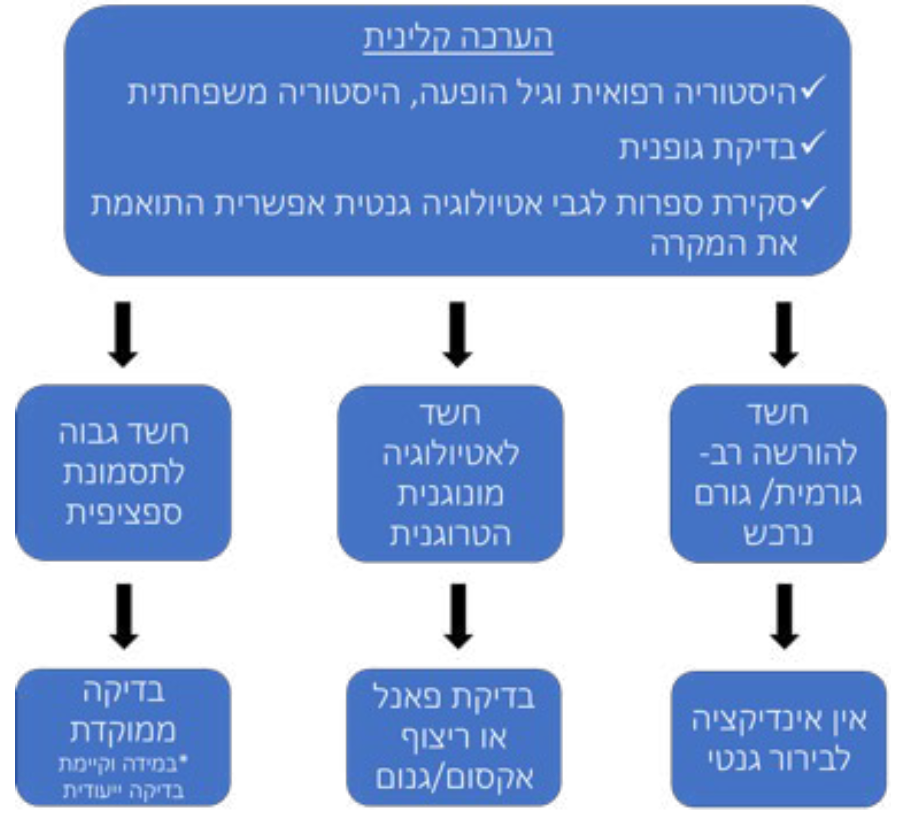
ההמלצה על בירור גנטי צריכה להיות מותאמת לכל מקרה באופן ספציפי ולכלול התייחסות לספרות המקצועית והערכה קלינית של הגורם המפנה לגבי הסבירות לאטיולוגיה מונוגנית על-פי הקליניקה וגיל ההופעה (ראו דיאגרמה)[8]. בפנוטיפים בהם ידוע על שכיחות גבוהה של אטיולוגיה רב-גורמית או פוליגנית כגון - אוטיזם מבודד ללא לקות קוגניטיבית, מחלות אוטואימוניות, מחלות שכיחות של גיל מבוגר או כאשר יש גורם נרכש ברור, לרוב אין הוריה רפואית לביצוע בדיקות ריצוף.
במקרים שאין חשד לאבחנה ספציפית והאבחנה המבדלת רחבה יש יתרון לבדיקות ריצוף נרחבות כגון פאנל, ריצוף אקסום/ גנום כקו ראשון[3][9]. לעומת זאת, במקרים שיש חשד לאבחנה גנטית ספציפית שיש לה בדיקה ייעודית קיימת עדיפות לבדיקה ייעודית לאותה אטיולוגיה (למשל מתילציה, איקס שביר)[6].
הערכה קלינית
ייעוץ גנטי והסכמה מדעת
תהליך האבחון המולקולרי ומסירת התוצאה יבוצעו בהתאם לחוק מידע גנטי התשס"א. טרם הבדיקה ייערך דיון לגבי היקף, סוג הבדיקה ומגבלותיה, תוצאות הבדיקה המצופות, והאפשרות לקבל תוצאות שמשמעותן אינה ידועה. אם מדובר בבדיקה כלל גנומית יוסבר על האפשרות לזיהוי של ממצאים שניוניים ב-actionable genes לפי הנחיות ACMG{הערה|שם=הערה11|Miller DT, Lee K, Chung WK, Gordon AS, Herman GE, Klein TE, et al. ACMG SF v3.0 list for reporting of secondary findings in clinical exome and genome sequencing: a policy statement of the American College of Medical Genetics and Genomics (ACMG). Genet Med. 2021;23(8):1381-90.}} או שינויים אקראיים בגנים נוספים בעלי משמעות רפואית שאינם קשורים לסיבת הבדיקה. על פי חוק מידע גנטי כל רופא/ה מומחה/ית בתחום מומחיותו מוסמך להפנות את מטופליו לבדיקות גנטיות. רופא/ה מומחה/ית שמפנה לבדיקות גנטיות מחויב למסור את מכלול התוצאות למטופל במסגרת מפגש מסכם על פי חוק מידע גנטי. התייעצות עוקבת עם רופא/ה מומחה/ית לגנטיקה או יועץ/צת גנטי היא באחריות הרופא/ה המפנה. בנספח א' מצורף טופס הסכמה לבדיקת ריצוף פאנל/אקסום/גנום המומלץ לשימוש על ידי איגוד הגנטיקאים הרפואיים בישראל. ככלל בדיקות ריצוף קליניות לאבחון מחלות מונוגניות הן בדיקות אבחנתיות לחולה ואינן מיועדות לאיתור נשאות למחלות רצסיביות לצורך תכנון היריון או כבדיקות סקר אחרות לנבדקים.
סיווג ממצאים המתגלים בבדיקות ריצוף
השימוש בבדיקות ריצוף מתקדמות בקליניקה הוביל לגילוי כמות גדולה של שינויים גנטיים נדירים שלא תוארו בעבר בחולים. חלקם עשויים להסביר את הפנוטיפ הקליני של החולה וחלקם לא.
קיימות 5 קטגוריות של סיווג[10]:
- פתוגני - שינוי גורם מחלה בוודאות גבוהה
- פתוגני בסבירות גבוהה - שינוי, ככל הנראה, גורם מחלה בסבירות של כ-90%
- שינוי בעל משמעות לא ידועה - לא ניתן לקבוע אם שפיר או גורם מחלה
- שפיר בסבירות גבוהה - שינוי, ככל הנראה, שפיר בסבירות של כ-90%
- שפיר - שינוי שפיר בוודאות גבוהה
באופן כללי אין לתת המלצות לטיפול, או לבצע אבחון טרום לידתי במקרים שמדובר בשינוי בעל משמעות לא ידועה או שפיר בסבירות גבוהה, ולכן קיימת חשיבות גבוהה לסיווג מדויק ככל הניתן. קיימות הנחיות בספרות לגבי סיווג וריאנטים כגון הנחיות ה-ACMG[10] ו־Clingen. תשובת הבדיקה צריכה לכלול את הסיווג באופן ברור. כמו כן, הגורם הרפואי המוסר את התשובה הגנטית למטופל יתייחס להקשר הקליני של הממצא.
יצירת מאגר מידע גנטי ישראלי
מאגר מידע משותף של הממצאים הגנטיים באוכלוסייה המקומית משפר מאוד את יכולת הפענוח וסיווג השינויים, במיוחד במקרים של איתור ממצאים שמשמעותם הקלינית אינה ברורה. לכן, אנו ממליצים כי המעבדות שמבצעות בדיקות מולקולריות אבחוניות בארץ תשתתפנה במאגר מידע גנומי לאומי בחסות משרד הבריאות.
מקרים לא פתורים
לכל בדיקה גנטית יש מגבלות ובדיקה תקינה לא שוללת לחלוטין גורם גנטי לתחלואה בנבדק. הסיבות האפשריות להיעדר אבחון גנטי בבדיקת ריצוף כוללות: מגבלות טכניות של הבדיקה, מגבלות בכלים הביואינפורמטיים, קושי בסיווג שינויים נדירים, היעדר מידע על קשר בין גן מסוים למחלה באדם, אטיולוגיה רב- גורמית / פוליגנית או אטיולוגיה שאינה גנטית. במקרה שדווח על שינוי בעל משמעות לא ידועה, באחריות המטופל להתעדכן מעת לעת לגבי הסיווג במסגרת ייעוץ גנטי שכן הסיווג עשוי להשתנות עם הזמן. פרט לכך, במקרים לא פתורים עם חשד גבוה למחלה מונוגנית, יש לשקול אנליזה מחודשת לנתונים הגולמיים לאחר שנה או יותר בתשלום נוסף[11]. במחקר מטאנליזה שפורסם נמצא כי אנליזה חוזרת הובילה לאבחנה ב-10% מהמקרים בממוצע[12]. ההחלטה הרפואית לגבי יעילות/רגישות/צורך בפענוח חוזר של תוצאות ריצוף קודם, צורך בהרחבת בירור גנטי על ידי שימוש בטכנולוגיות חדשות (ריצוף גנום או long read sequencing) תתקבל במסגרת ייעוץ גנטי חוזר[13].
סיכום
ההחלטה על בדיקות גנטיות לאבחון מחלות מונוגניות היא מותאמת למקרה ודורשת הערכה קלינית טרם ההפנייה לביצוע הבירור וכן לאחר קבלת תוצאותיו. לאבחנה של מחלות מונוגניות יש חשיבות גדולה בטיפול והמעקב הרפואי והאיגוד לגנטיקה רפואית ממליץ על ביצוע בדיקות מולקולאריות אבחנתיות בכל המקרים שעונים לקריטריונים הקליניים המפורטים, כולל בדיקות כלל גנומיות כקו ראשון בהתאם לאבחנה המבדלת וללא מגבלת גיל.
נייר עמדה זה משקף ותואם את המקובל במקומות אחרים בעולם. נייר העמדה יעבור הערכה מחדש מעת לעת בהתאם להתקדמות המחקר בתחום המחלות המונוגניות/הנדירות.
ביבליוגרפיה
- ↑ Nguengang Wakap S, Lambert DM, Olry A, Rodwell C, Gueydan C, Lanneau V, et al. Estimating cumulative point prevalence of rare diseases: analysis of the Orphanet database. Eur J Hum Genet [Internet]. 2020;28)2(:165-73. Available from: http://dx.doi.org/10.1038/s41431-019-0508-0
- ↑ Giampietro PF, Greenlee RT, McPherson E, Benetti LL, Berg RL, Wagner SF. Acute health events in adult patients with genetic disorders: The Marshfield Epidemiologic Study Area. Genet Med [Internet]. 2006;8(8):474-90. Available from: https://doi.org/10.1097/01 .gim.0000232479.90268.40
- ↑ 3.0 3.1 Srivastava S, Love-Nichols JA, Dies KA, Ledbetter DH, Martin CL, Chung WK, et al. Meta-analysis and multidisciplinary consensus statement: exome sequencing is a first-tier clinical diagnostic test for individuals with neurodevelopmental disorders. Genet Med [Internet]. 2019;21(11):2413-21. Available from: http://dx.doi.org/10.1038/s41436-019-0554-6
- ↑ Krantz ID, Medne L, Weatherly JM, Wild KT, Biswas S, Devkota B, et al. Effect of Whole-Genome Sequencing on the Clinical Management of Acutely Ill Infants with Suspected Genetic Disease: A Randomized Clinical Trial. JAMA Pediatr. 2021;92122(12):1218-26.
- ↑ 5.0 5.1 Manickam K, McClain MR, Demmer LA, Biswas S, Kearney HM, Malinowski J, et al. Exome and genome sequencing for pediatric patients with congenital anomalies or intellectual disability: an evidence¬based clinical guideline of the American College of Medical Genetics and Genomics (ACMG). Genet Med [Internet]. 2021;23(11):2029-37. Available from: https://doi.org/10.1038/s41436-021-01242-6
- ↑ 6.0 6.1 Boycott K, Hartley T, Adam S, Bernier F, Chong K, Fernandez BA, et al. The clinical application of genome-wide sequencing for monogenic diseases in Canada: Position statement of the Canadian College of medical geneticists. J Med Genet. 2015;52(7):431-7.
- ↑ Clark MM, Stark Z, Farnaes L, Tan TY, White SM, Dimmock D, et al. Meta-analysis of the diagnostic and clinical utility of genome and exome sequencing and chromosomal microarray in children with suspected genetic diseases. npj Genomic Med [Internet]. 2018;3(1):1-10. Available from: http://dx.doi. org/10.1038/s41525-018-0053-8
- ↑ Gonzaludo N, Belmont JW, Gainullin VG, Taft RJ. Estimating the burden and economic impact of pediatric genetic disease. Genet Med [Internet]. 2019;21(8):1781-9. Available from: http://dx.doi. org/10.1038/s41436-018-0398-5
- ↑ Fernandez IS, Loddenkemper T, Ga^nza-Lein M, Sheidley BR, Poduri A. Diagnostic yield of genetic tests in epilepsy: A meta-analysis and cost-effectiveness study. Neurology. 2019;92(5):E418-28.
- ↑ 10.0 10.1 Richards S, Aziz N, Bale S, Bick D, Das S. ACMG Standards and Guidelines Standards and guidelines for the interpretation of sequence variants : a joint consensus recommendation of the American College of Medical Genetics and Genomics and the Association for Molecular Pathology. 2015;(March):1-20.
- ↑ Deignan JL, Chung WK, Kearney HM, Monaghan KG, Rehder CW, Chao EC. Points to consider in the reevaluation and reanalysis of genomic test results: a statement of the American College of Medical Genetics and Genomics )ACMG(. Genet Med [Internet]. 2019;21)6(:1267-70. Available from: http://dx.doi.org/10.1038/s41436-019-0478-1
- ↑ Dai P, Honda A, Ewans L, McGaughran J, Burnett L, Law M, et al. Recommendations for next generation sequencing data reanalysis of unsolved cases with suspected Mendelian disorders: A systematic review and meta-analysis. Genet Med [Internet]. 2022;24(8):1618-29. Available from: https://doi .org/10.1016/j .gim .2022.04.021
- ↑ Marwaha S, Knowles JW, Ashley EA. A guide for the diagnosis of rare and undiagnosed disease: beyond the exome. Genome Med [Internet]. 2022;14(1):1-22. Available from: https://doi. org/10.1186/s13073-022-01026-w
המידע שבדף זה נכתב על ידי ד"ר קארין ויס, מנהלת מכון גנטי, רמב"ם; ד"ר דפנה מרום, סגנית מנהלת מכון גנטי, איכילוב; ד"ר אהוד בן, מנהל מכון גנטי, וולפסון; ד"ר אמיר פלג, מנהל מכון גנטי, כרמל; ד"ר תמר פפרנה, מנהלת מעבדה גנטית, מכון גנטי רמב"ם; גב׳ רותם גרינברג, יועצת גנטית, מנהלת תחום גנטיקה קלינית, מרכז גנומי כללית


 כניסה
כניסה  עקבו אחרינו בפייסבוק
עקבו אחרינו בפייסבוק