איברוטיניב לטיפול בלויקמיה לימפוציטית כרונית - Ibrutinib for the treatment of chronic lymphocytic leukemia - CLL
ערך זה נמצא בבדיקה ועריכה על ידי מערכת ויקירפואה, וייתכן כי הוא לא ערוך ומוגה.
| איברוטיניב לטיפול בלויקמיה לימפוציטית כרונית - CLL | ||
|---|---|---|
| Ibrutinib for the treatment of chronic lymphocytic leukemia | ||
| שמות נוספים | צעד חשוב בטיפול ב - CLL | |
| ICD-10 | Chapter C 91.1 | |
| ICD-9 | V10.60 204.1 V10.60 | |
| MeSH | D015451 | |
| יוצר הערך | ד״ר אוהד בנימיני | |
לערכים נוספים הקשורים לנושא זה, ראו את דפי הפירושים: – איברוטיניב, לוקמיה לימפוציטית כרונית
לויקמיה לימפוציטית כרונית (CLL, Chronic Lymphocytic Leukemia) היא הלוקמיה השכיחה ביותר בעולם המערבי. מהלך המחלה לרוב איטי אך יחד עם זאת שונה מאוד מחולה לחולה. ההישרדות יכולה להיות רבת שנים אך בחלק מהחולים תוחלת החיים קצרה עם מהלך של חודשים. המחלה נחשבת לחשוכת מרפא עם פוטנציאל ריפוי על ידי השתלה אלוגנאית בקבוצה מצומצמת של חולים[1]. חלה התקדמות ממשית בטיפול בלוקמיה לימפטית כרונית על ידי כימואימונותרפיה הכוללת שילוב של כימותרפיה עם נוגדן מונוקלונלי ל-CD20, שהביא לתגובה ממושכת ללא מחלה ולהארכת חיים בחולים צעירים. הטיפול הסטנדרטי בחולים צעירים עד גיל 65 הוא משלב FCR [Fludarabine, Cyclophosphamide (Endoxan) ו-Rituximab (Mabthera)][2].
חולים מבוגרים יותר שיכולים לעמוד בטיפול אינטנסיבי משיגים תוצאות דומות במשלב BR [Bendamustine (Ribomustin) ו-Rituximab][3]. חולים עם מחלות נלוות או חולים מבוגרים יותר לרוב אינם יכולים לעמוד בכימואימונותרפיה אינטנסיבית והם מטופלים בכימותרפיה קלה יותר, Chlorambucil בשילוב נוגדנים מונוקלונלים חדשים ל-CD20[4],[5]. שילוב Chlorambucil עם Gazyva (Obinutuzumab) הביא להארכת חיים לעומת טיפול עם Chlorambucil בלבד והאריך בכשנה את משך הזמן ללא מחלה (PFS, Progression-free Survival) לעומת חולים שטופלו ב-Chlorambucil עם הנוגדן Rituximab[5].
על אף התוצאות המרשימות, במרבית החולים המחלה תתקדם תוך חודשים או שנים לאחר הטיפול הראשון והתגובה לטיפול חוזר קצרה ומוגבלת. מדדים פרוגנוסטים חדשים שיפרו את היכולת לנבא עמידות לטיפול ולזהות חולים שמחלתם תתקדם מוקדם יותר. מדדים אלו כוללים זיהוי שינויים ידועים בכרומוזומים על ידי בדיקת FISH (Fluorescence In Situ Hybridization), סטטוס המוטציה ב-IGVH ZAP70, CD38, CD49d ו-microglobulin-β2[6].
פיתוח טיפולים חדשים מתמקד במציאת מענה טוב יותר לשתי אוכלוסיות חולים בעיקר:
- חולים מבוגרים או חולים עם מחלות נלוות אשר אינם יכולים לעמוד בטיפול כימואימונותרפי סטנדרטי.
- חולים עם גורמים פרוגנוסטים רעים וסמנים גנטים וביולוגים המנבאים עמידות או חזרה מוקדמת של המחלה לאחר כימואימונותרפיה. תת הקבוצה של חולים עם חסר הזרוע הקצרה של כרומוזום 17 (de117p) או מוטציה ב-TP53{{כ]} (tumor suppressor gene) מתאפיינת בהתקדמות המחלה עם עמידות לכימותרפיה. קבוצה זו מהווה פחות מ-10% מחולי CLL באבחנה אך כשליש מהחולים שמחלתם נשנית[7].
תהליכים ביולוגים שהביאו לפיתוח תרופות
הבנה טובה יותר של תהליכים בביולוגיה של המחלה הביאה לגילויים ולפיתוח מולקולות ממוקדות מטרה לתהליכים ספציפיים המעורבים בפהגונזה של המחלה. חלק מהמולקולות הגיעו לכדי פיתוח תרופות המיושמות בקליניקה ומתמקדות בעיכוב אנזימים המעבירים אותות מהרצפטור לתאי B (BCR). שתי תרופות עם יעדים שונים בעיכוב האותות מהרצפטור לתאי B הן איברוטיניב (Ibrutinib), מעכב של BTK (Bruton thyrosin kinase) ואידלליסיב (Idelalisib), מעכב PI3Kδ (phosphatidylinositol-3-kinaseδ). מנגנון נוסף הוא השראת אפופטוזיס על ידי עיכוב החלבון 2-Bci עם מולקולה קטנה וסלקטיבית, ונטוקלקס (Venetoclax) . היעילות המרשימה ומיעוט תופעות הלוואי של התרופות הללו הביאו לאישורן לשימוש בקליניקה על ידי הרשויות בארצות הברית ובאירופה.
הרפצטור לתאי B - מנגנון פעולה
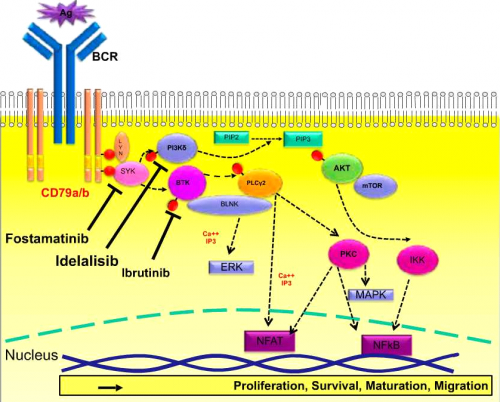
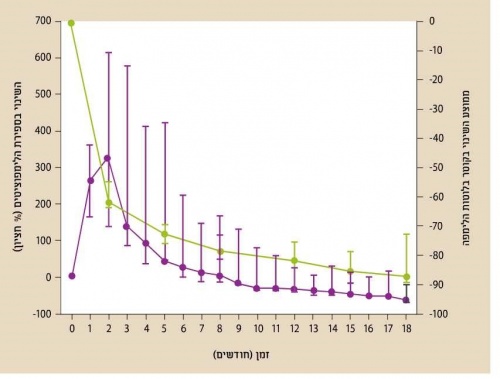
הרצפטור לתאי B cell receptor, BCR) B) הוא קומפלקס טרנסממברנלי מורכב הכולל שרשרת אימונוגלובולין. קישור ליגנד לרצפטור תאי B גורם להפעלה של מספר תהליכים החיוניים להתפתחות תאי B המשפיעים על פרוליפרציה, התמיינות, הבשלה, אפופטוזיס ונדידה של התאים. הקשר בין הפעלת הרצפטור על ידי אנטיגן וקבלת תגובה התוך תאית תלוי במעבר אותות והפעלת קסקדה של חלבונים ומולקולות מתאמות[8], [9]. האנזימים PI3Kδ , SYK (Spleen tyrosin kinases) ו-BTK (Bruton's tyrosin kinase) חיונים להעברת האותות ב-BCR ועיכוב שלהם מביא לפגיעה בהבשלה ושגשוג התאים, לאחר מפגש האנטיגן עם תא B המתרחש בעיקר בבלוטות לימפה[10], [11]. ידוע שלגורמים בסביבת תא CLL שמקורם בתאי משתית ומונוציטים, בהם "Nurse like cells" חיוניים ומשפיעים על השרדותו דרך אותות המועברים על ידי הרצפטור[12], [13]. עד היום פותחו מספר מולקולות קטנות שנמצאו יעילות בעיכוב BTK PI3K SYK - קינזות חיוניות למעבר האותות ב-BCR - שהביאו לפגיעה בהפעלתו ופגיעה בפרוליפרציה של תאי המחלה. (תרשים 1) בחולים, התגובה שנצפית בטיפול בכל אחת ואחת מהמולקולות הללו (Class effect) היא שיפור בסימפטומים של המחלה והצטמקות מהירה של בלוטות הלימפה בד בבד עם עלייה בספירה האבסולוטית של לימפוציטים בדם פריפרי. העלייה בספירת הלימפוציטים בדם היא זמנית ומתרחשת תוך כדי שיפור במדדים הקליניים של המחלה. לאחר שיא בספירת הלימפוציטים שמופיע תוך שבוע-שבועיים מתהילה הטיפול חלה ירידה הדרגתית שמתחילה לאחר כחודשיים. (תרשים 2) אף שהעלייה בספירה הלימפוציטים משתנה בין החולים ויכולה להמשך חודשים רבים, היא אינה מבשרת על כשלון טיפולי. הלימפוציטוזיס נובע מיציאה של לימפוציטים ממדורי מח העצם ובלוטות הלימפה לדם כתוצאה מהשפעה של מעכבי הקינזות על נדידה ואינטרקציה של תאי CLL וללא גדילה בכמות הלימפוציטים. נמצא שבשלב זה מתרחשת ירידה בפרוליפרציה של הלימפוציטים[14].
עיכוב הרפצטור לתאי B על ידי איברוטיניב (ibrutinib)
איברוטיניב (ibrutinib, imbruvica) היא מולקולה קטנה הנקשרת כקשר קובלנטי בלתי הפיך לציסטאין (Cys481) שבאחר הפעיל של האנזים BTK וחוך שעות נורמת לעיכוב מוחלט של פעילוהו בריכוזים נמוכים. האנזים הציטופלסמטי BTK הוא tyrosin kinase, שלוקח חלק חשוב במעבר אותות דרך רצפטורי תאי B וגורם להפעלה של מסלול NFkB, MAP kinase ומסלולים נוספים[11]. מוטציה גנטית ב-BTK מבטלת אח פעילותו חוסמת את הכשלת תאי B בשלב pre-B וגורמת ל-X-linked agamaglobulinemia. המחלה נקראה גם Bruton's agammaglobulinemia, גורמת לחסר מוחלט של האי B בשלים וחסר באימונוגלובולינים ומהבטאה בזיהומים חיידקיים חוזרים[15]. איברוטיניב, מעכב BTK ופוגע במעבר האותות ב- BCR לפקטורי שיעהוק בגרעין התא ובתוצאה מכך גורם לפגיעה בשגשוג תאי המחלה.
איברוטיניב ניחנה כטיפול פומי, ויתרון נוסף של החרופה הוא הפרופיל הבטיחוחי. בניגוד לכימותרפיה, התרופה אינה גורמת לדיכוי מח העצם ואינה מדכאת יצור אימונוגלובולינים. ציטופניות מדרגה 3-5 קיימוה בכ-15% מהחולים לעומה 85% בטיפול כימואימונותרפי סטנדרטי. מרבית תופעות הלוואי שאינן המטולוגיות הן מדרגה 1-2. קיים סיכון מוגבר לאירועי דמם בעיקר קלים המתבטאים כהמטומות או אכימוזות בעור. התרופה אינה ניתנת בשלוב עם אנטיקואגולציה מסוג וורפרין בשל הסיבון לאירועי דמם קשים. איברוטיניב הוגדרה בתרופה פורצת דרך ועברה אישור על ידי ה-FDA בפברואר 2014 לטיפול בלוקמיה לימפטית ברונית עמידה או במחלה חוזרת ולאחר מכן גם בטיפול קו ראשון בחולים עם del17p.
מחקרים עם איברוטיניב כטיפול יחיד בלוקמיה לימפטית כרונית
במחקרים הראשונים בשלב I נמצאה תפוסה מלאה של איברוטיניב לאתרי הקישור לאנזים כבר במינון 2.5mg/kg ללא הגעה למינון מירבי בלתי נסבל (MTD maximal tolerated dose). המינון המקובל עם מיעוט תופעוה לראי בלוקמיה לימפטית כרונית הוא 420 מ"ג ליום. שיעור תגובה כוללת (0RR) ב־70% מהחולים ובעוד 20% מהחולים הגובה חלקיה ולימפוציטוזיס[16]. כבר במחקרים הראשובים ניתן היה לראות שיעילוח הטיפול באיברוטיביב לא תלויה בגורמים פרוגנוסטים קלינים או ביולוגיים כמו שלב מחלה מתקדם, מספר קווי טיפול קודמים ונוכחות 17p) del). סיכום של 132 חולים במשך מעקב חציוני של 3 שנים הראה שהתגובה לטיפול ממושכת. רק ב-25 חולים בתקופת המעקב המחלה התקדמה[17]. על בסיס נתונים אלה אושר בפברואר 2014 הטיפול באיברוטיניב על ידי ה-FDA לטיפול בחולי לוקמיה לימפטית כרונית עם השנות המחלה. יעילות ובטיחות איברוטיניב נבדקה ונמצאה זהה במחקר פאזה Ib גם כקו טיפול ראשון בחולים מבוגרים (מגיל 65 ומעלה)[18].
התפרסמו תוצאות מחקר אקראי שלב III (RESONATE) שהשווה טיפול באיברוטיניב לנוגדן מונוקלונלי ל-CD20 אופטומומב (ofatumumab) ב-391 חולים עם מחלה עמידה או חוזרת[19]. החולים שbכללו לא היו מהאימים לטיפול בכימו,רפיה עם purine analogues בשל חזרת מחלתם זמן קצר לאחר כימואימונותרפיה. נכללו גם חולים עם מחלות נלוות, חולים מבוגרים (גיל 70 ויותר) או חולים עם 17p) del). התגובה הכוללת הייתה טובה יותר משמעותית בקבוצת החולים שטופלו באיברוטיביב 42.6% ועוד 20% עם תגובה חלקית ולימפוציטוזיס לעומת 4.1% בקבוצת אופטומומב. לאחר מעקב של 9.4 חודשים החולים שטופלו באיברוטיביב לא הגיעו למשך הזמן החציוני ללא מחלה (PFS) לעומת 8.4 חודשים בחולים שטופלו באופטומומב. הטיפול באיברוטיניב השפיע באופן חיובי גם על השררות החולים. אפקט בסדר גודל דומה נצפה גם בתת קבוצת חולים עם 17p) del) וחולים עם מחלה עמידה לאנלוגים של פורינים[19]. יעילות איברוטיניב בחולים עם 17p) del) נבדקה במחקר פאזה II על 51 חולים עם 17p) del) כקו ראשון או בחזרת מחלה. אחרי שנהיים מעקב תגובה נצפתה ב-97% מהחולים וב-80% מהחולים במחלה עמידה או חוזרת[20]. בעקבות מחקר זה, הרחיב ה-FDA את הההתוויה לטיפול באיברוטיניב לחולים עם 17p) del) גם כקו טיפול ראשוני.
טיפול באיברוטיניב במשלבים
במטרה לבטל את הלימפוציטוזיס בעקבות טיפול כאיברוטיניב ולשפר עוד יותר את התגובה לטיפול נבדק איברוטינב במשלבים. במחקר פאזה II על 40 חולים עם מחלה בסיכון גבוה החולים טופלו באיברוטיניב ונוגדן מונוקלונלי ל-CD20, ריטוקסימב. החולים שהוגדרו בסיכון גבוה כללו del( 17p)/TP53 mutation, התקדמות מחלה תוך פחות מ-36 חודשים לאחר כימואימונוהרפיה בקו ראשון או חולים עם deliiq שמחלתם נשתנה. שיעור התגובה הכוללת (0RR) היה 95% עם 8% הגובה מלאה (CR) ו-90% תגובה ב-20 החולים עם del(17p)/TP53mutation[21].
השילוב האולטימטיבי של איברוטיניב עם כימואימונותרפיה נבדק תחילה על 33 חולים במחקר פאזה lb וניתן עם BR (bendamustin-rituximab) או FCR (fludarabuine-bendamustin-rituximab). שיעור התגובה הכוללת (ORR) של BR-ibrutinib היה 93.3% עם 16.7% תגובה מלאה (CR) שהשתפרה במהלך המעקב ל-40%. לאחר 36 חודשים 70% מהחולים המשיכו טיפול ללא התקדמות המחלה. תופעוה הלוואי שנצפו במחקר זה היו דומות לאלו שבצפו בחולים המטופלים באיברוטיניב או BR בנפרד. תוצאות מחקר זה הראו שאיברוטיניב מגבירה יעילות כימואימונותרפיה ללא תוספת רעילות[22].
מחקר HELIOS המחקיים כעת הוא מחקר רב מרכזי אקראי כפול םמיות שלב III בעל פוטנציאל לשינוי היסטורי בטיפול בלוקמיה לימפטית כרונית. תוצאוח ביניים של מחקר זה פורסמו במפגש החברה האמריקראית לאונקולוגיה (ASCO 2015) והציגו שיפור של 80% במשך התגובה ללא מחלה (PFS) כאשר איברוטיניב שולב עם כימואימונתרפיה. המחקר כולל 578 חולי CLL/SLL שטופלו ב-BR בשילוב אינבו (289=n) או 420 מג' ליום איברוטיניב (289=n). אה 6 מחזורי הטיפול המתוכנן עם BR השלימו 83% ו-78% מהחולים בזרוע אינבו והאיברוטיניב, בהתאמה. בשלב תוצאות הביניים 31% (90=n) מהחולים בקבוצת ה-BR ואינבו התקדמו והועברו לזרוע איברוטיניב. שיעור התגובה הכולל (0RR) היה 82.7% בזרוע איברוטיניב לעומת 67.8% בקבוצת הביקורת (0.0001=p), עם תגובה מלאה CR/CRO) ב-10.4% לעומת 2.8% בקבוצה איברוטיביב ואינבו, בהתאמה. לאחר מעקב חציוני של 17.2 חודשים, בזרוע BR עם איברוטיניב לא הגיע להתקדמות ללא מחלה (PFS) לעומת 13.3 חודשים בחולים שקיבלו BR בלבד. (.HR=0.203;95%CI 0.0001>0150-0.276;p) תועלה זו נצפתה גם בתת קבוצת החולים בסיכון גבוה[23].
סיכום
הטיפול בלוקמיה לימפטית כרונית עובר שינויים דרמטיים. מגוון הטיפולים החדשים יאפשר בעתיד הקרוב טיפול אינדיבידואלי ומהאים לפי רמה סיכון ההלויה בגורמים פרוגנוסטים והחלואה נלוית.
איברוטיניב, הראשונה מבין התרופות החדשוה להכנס לארסנל הטיפול בלוקמיה לימפטית כרונית. איברוטיניב הפכה בחמש שנים מתרופת מחקר לטיפול םטנדטי בחולים בסיכון גבוה ולחולים עם מחלה חוזרת או עמידה. התרופה מאושרת בארץ בהתוויה מצומצמה למתן בחולים עם מדד פרוגנוסטי גרוע - de117p ומיועדת להרחבה בסל התרופות הקרוב לחולי CLL שמחלתם נשנית לאחר טיפולים קודמים. תוצאות הטיפולים החדשים מבשרות כי בשנים הקרובות המחקר הקליני ב-CLL יתמקד בטיפולים ללא כימותרפיה ושילוב תרופות עם מנגנונים סינרגיסטים עם מיעוט תופעות לוואי במטרה לשפר השרדוה ואיכות החיים בדרך לריפוי המחלה.
דגלים אדומים
ביבליוגרפיה
- ↑ Chiorazzi N, Rai KR, Ferrarini M, Chronic lymphocytic leukemia. N Engl J Med 2005352:804-15.
- ↑ Keating MJ, O'Brien S, Albitar M, etal. Early results of a chemoimmunotherapy reg¬imen of fludarabine, cyclophosphamide, and rituximab as initial therapy for chronic lymphocytic leukemia. J Clin Oncol 2005;23:4079-88.
- ↑ Eichhorst B, Fink AM, Busch R, et al. Frontline Chemoimmunotherapy with Fluda-rabine (F), Cyclophosphamide (C], and Rituximab (R) (FCR) Shows Superior Efficacy in Comparison to Bendamustine (B) and Rituximab (BR) in Previously Untreated and Physically Fit Patients (pts) with Advanced Chronic .2014.
- ↑ Goede V, Fischer K, Engelke A, etal. Obinutuzumabas frontline treatment of chron¬ic lymphocytic leukemia: updated results of the CLL11 study. Leukemia 2015:29:1602¬4.
- ↑ 5.0 5.1 Hillmen P, RobakT,Janssens A, etal. Chlorambucil plus ofatumumab versus chlo-rambucil alone in previously untreated patients with chronic lymphocytic leukae¬mia (COMPLEMENT l):a randomised, multicentre, open-label phase 3 trial. Lancet 2015;385:1873-83.
- ↑ Wierda WG, O'Brien S, Wang X, etal. Multivariate model for time to first treatment in patients with chronic lymphocytic leukemia. J Clin Oncol 2011;29:4088-95.
- ↑ ZenzT, Gribben JG, Hallek M, Dohner H, Keating MJ, Stilgenbauer 5. Risk categories and refractory CLL in the era of chemoimmunotherapy. Blood 2012;119:4101-7.
- ↑ Pleyer L, Egle A, Hartmann TN, Greil R. Molecular and cellular mechanisms of CLL: novel therapeutic approaches. Nat Rev Clin Oncol 2009;6:405-18,
- ↑ Burger JA, Chiorazzi N. B cell receptor signaling in chronic lymphocytic leukemia. Trends Immunol 2013;34:592-601.
- ↑ Herishanu Y, Perez-Galan P, Liu D, et al.The lymph node microenvironment promotes B-cell receptor signaling, NF-kappaB activation, and tumor proliferation in chronic lymphocytic leukemia. Blood 2011;117:563-74.
- ↑ 11.0 11.1 Cheng S, Ma J, Guo A, etal. BTK inhibition targets in vivo CLL proliferation through its effects on B-cell receptor signaling activity. Leukemia 2014;28:649-57.
- ↑ Burger JA. The CLL cell microenvironment. Adv Exp Med Biol 2013;792:25-45.
- ↑ Burger JA, Ghia P, Rosenwald A, Caligaris-Cappio F. The microenvironment in ma¬ture B-cell malignancies: a target for new treatment strategies. Blood 2009:114:3367¬75.
- ↑ Herman SE, Niemann CU, Farooqui M, et al. Ibrutinib-induced lymphocytosis in patients with chronic lymphocytic leukemia: correlative analyses from a phase II study. Leukemia 2014;28:2188-96.
- ↑ Bruton OC. Agammaglobulinemia. Pediatrics 1952;9:722-8.
- ↑ Advani RH, Buggy JJ, Sharman JP, et al. Bruton tyrosine kinase inhibitor ibrutinib (PCI-32765) has significant activity in patients with relapsed/relractory B-cell malig¬nancies. J Clin Oncol 2013;31:88-94.
- ↑ Byrd JC, Furman RR, Coutre SE, et al. Three-year follow-up of treatment-naive and previously treated patients with CLL and SLL receiving single-agent ibrutinib. Blood 2015;125:2497-506.
- ↑ O'Brien S, Furman RR, Coutre SE, etal. Ibrutinib as initial therapy for elderly patients with chronic lymphocytic leukaemia or small lymphocytic lymphoma: an open-label, multicentre, phase 1b/2 trial. Lancet Oncol 204,15:48-58.
- ↑ 19.0 19.1 Byrd JC, Brown JR, O'Brien S, et al. Ibrutinib versus ofatumumab in previously treated chronic lymphoid leukemia. N Engl J Med 2014;371:213-23.
- ↑ Farooqui MZ, Valdez J, Martyr S, etal. Ibrutinib for previously untreated and relapsed or refractory chronic lymphocytic leukaemia with TP53 aberrations: a phase 2, single-arm trial. Lancet Oncol 2015:16:169-76.
- ↑ Burger J A, Keating MJ, Wierda WG, et al. Safety and activity of ibrutinib plus ritux-imabfor patients with high-risk chronic lymphocytic leukaemia: a single-arm, phase 2 study. Lancet Oncol 2014;15:1090-9.
- ↑ Brown JR, Barrientos JC, Barr PM, etal. Ibrutinib In Combination With Bendamus-tine and Rituximab Is Active and Tolerable In Patients With Relapsed/Refractory CLL/ SLL: Final Results Of a Phase lb Study2013.
- ↑ Chanan-Khan AAA, Cramer P, Demirkan F, et al. Ibrutinib combined with benda-mustine and rituximab (BR) in previously treated chronic lymphocytic leukemia/small lymphocytic lymphoma (CLL/SLL): First results from a randomized, double-blind, placebo-controlled, phase III study. ASCO Meeting Abstracts 2015;33:LBA7005.
קישורים חיצוניים
- צעד חשוב בטיפול ב - CLL, TheMEDICAL
המידע שבדף זה נכתב על ידי ד"ר אוהד בנימיני, רופא בכיר, מכון המטואונקולוגי, המרכז הרפואי ע״ש שיבא, תל השומר


 כניסה
כניסה  עקבו אחרינו בפייסבוק
עקבו אחרינו בפייסבוק