הבדלים בין גרסאות בדף "אינווגה - Invega"
ביאנקה סטרלצין (שיחה | תרומות) |
ביאנקה סטרלצין (שיחה | תרומות) |
||
| שורה 1: | שורה 1: | ||
| − | |||
{{תרופה | {{תרופה | ||
|שמות נוספים= | |שמות נוספים= | ||
גרסה מ־17:11, 6 בנובמבר 2012
| אינווגה - Invega | ||
|---|---|---|
| מרכיב פעיל | PALIPERIDONE | |
| קבוצה פרמקולוגית (ATC) | "OTHER ANTIPSYCHOTICS" | |
| שם התרופה | "אינווגה®" (קישור לדף התרופה במאגר משרד הבריאות) |
|
| סל הבריאות | כלול | |
| מסגרת הכללה בסל | תרופה מוגבלת לרישום ע"י רופא מומחה או הגבלה אחרת.
1. הטיפול בתרופה האמורה יינתן לאחד מאלה: א. למבוטח בגיר שהוא חולה סכיזופרניה, ובהתקיים אחד מהתנאים האלה: 1. המטופל מוגדר כבעל קווי התנהגות תוקפניים, וכטיפול ראשון; 2. המטופל לא הגיב לטיפול ב-Risperidone או פיתח תופעות לוואי קשות לטיפול כאמור; ב. למבוטח קטין הסובל מסכיזופרניה או מפסיכוזה אחרת, כטיפול ראשון; 2. התחלת הטיפול בתרופה תהיה על פי הוראתו של מנהל מחלקה בבית חולים או של מנהל מרפאה שהינם רופאים מומחים בפסיכיאטריה או בפסיכיאטריה של הילד והמתבגר או בנוירולוגיה, לפי העניין; 3. לא יינתנו לחולה בו בזמן שתי תרופות או יותר ממשפחת התרופות האנטיפסיכוטיות האטיפיות. |
|
התוויות |
Invega is indicated for : - treatment of schizophrenia . - acute treatment of schizoaffective disorder as monotherapy. - acute treatment of schizoaffective disorder as an adjunct to mood stabilizers and/or antidepressants
| |
| שם יצרן | ALZA CORPORATION, USA | |
| שם בעל הרישום | J-C HEALTH CARE LTD | |
דרך מתן
מינונים
התוויות נגד
תופעות לוואי
פרמקוקינטיקה
פרמקודינמיקה
חומרים בלתי פעילים
הנחיות בטיחות
תגובות בין-תרופתיות
שימוש בהריון
זמינות בארץ
זמינות בעולם
מאמרים עדכניים
מידע ברשת
רקע
Paliperidone ER (Invega) היא תרופה אנטי פסיכוטית אטיפית חדשה במתן דרך הפה שפותחה לטיפול בסכיזופרניה. Invega היא התרופה האנטי פסיכוטית האטיפית היחידה שעושה שימוש במערכת שחרור אוסמוטית - טכנולוגיית OROS® - לשחרור תרופה פעילה בקצב מדויק ומבוקר.
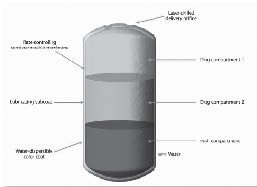
טכנולוגיית OROS®
כאמור, ב-Paliperidone ER נעשה שימוש בטכנלוגיית OROS® (Osmotic Release Oral Delivery System) לשחרור פליפרידון בקצב מבוקר במשך 24 שעות לאחר לקיחת מנה יומית אחת. הטכנולוגיה מבטיחה עלייה הדרגתית בריכוז הפליפרידון בדם, וכך ניתן להתחיל את הטיפול במינון תרפויטי אפקטיבי כבר ביום הראשון, ללא צורך בטיטרציה ראשונית של המינון. הטכנולוגיה נועדה גם למזער את התנודות בריכוזי הפליפרידון בפלסמה בפרק זמן של 24 שעות (1).
פרמקוקינטיקה
שיא ריכוז פליפרידון בפלסמה מושג כ-24 שעות לאחר לקיחת מנה אחת. הפרמקוקינטיקה היא תלויית-מינון (Dose-Proportional). זמן מחצית החיים לסילוק סופי של פליפרידון הוא כ-23 שעות. ריכוזי פליפרידון במצב יציב מושגים במרבית המטופלים תוך 5-4 ימים מתחילת השימוש בפליפרידון בשחרור מושהה.
מרבית התרופה (כ-70%) מופרשת בשתן ללא שינוי (2).
פרמקודינמיקה
Paliperidone ER הוא חוסם סלקטיבי של אפקט המונואמין ותכונותיו שונות מתרופות נוירולפטיות קודמות. Paliperidone ER נקשר בחוזקה לקולטנים הסרוטונרגיים 5-HT2 וכן לקולטנים הדופאמינרגיים D2.
פליפרידון פעיל גם כאנטגוניסט לקולטנים האדרנרגיים אלפא 1 ואלפא 2 ולקולטנים היסטמינרגיים מסוג H1, אולם אין לו זיקה לקולטנים כולינרגיים, מוסקריניים או לקולטנים בטא 1 ובטא 2 אדרנרגיים (3).
יעילות התכשיר ובטיחותו
.Kane et al (7002) במחקר שכלל 628 חולי סכיזופרניה בוגרים (4) הראה כי בהשוואה לפלצבו, כל המינונים של Paliperidone ER הראו שיפור משמעותי בניקוד PANSS כללי, בניקוד כל הרכיבים של PANSS (p<0.001) בניקוד CGI ובתפקוד אישי וחברתי (p<0.001).
אחוזים גבוהים יותר משמעותית של מטופלים שקיבלו Paliperidone ER הראו ירידה ≥ 30% בניקוד PANSS כללי בהשוואה לפלצבו (p<0.001).
מרבית תופעות הלוואי שנצפו במחקר היו קלות או בינוניות בחומרתן. היארעות EPS והיפרקינזיה הייתה דומה בקבוצת האינבו והמטופלים במינון 6 מ"ג. אם כי דווחו לעתים קרובות יותר בקבוצות של 9 ו-12 מ"ג, בהשוואה לפלצבו דווחו טכיקרדיה, הפרעה חוץ-פירמידלית והיפרקינזיה.
לא נצפו במשתתפים במחקר תופעות לוואי הקשורות לרמת הסוכר או שינויים משמעותיים בערכי מעבדה כלשהם מנקודת ההתחלה לנקודת הסיום, לרבות רמת סוכר ממוצעת בצום, אינסולין או ליפידים בסרום. השינוי הממוצע במשקל הגוף היה נמוך מ-1 ק"ג בכל הקבוצות של Paliperidone ER.
.Kramer et al (7002) דיווח על תוצאות מחקר שבדק את היעילות של מינון גמיש של פליפרידון בשחרור מושהה בעיכוב הישנות התסמינים ב-113 חולי סכיזופרניה בוגרים (5).
בשל תוצאות יעילות חיוביות מובהקות הופסק המחקר לאחר ניתוח הביניים.
הזמן להישנות המחלה היה משמעותית ארוך יותר בקבוצה של Paliperidone ER (מינון ממוצע 10.8 מ"ג ליום) בהשוואה לפלצבו (p=0.005). 92 מטופלים שקיבלו פלצבו (53%) סבלו מאירוע הישנות לעומת 14 מטופלים שקיבלו Paliperidone ER (25%). נקודת הזמן בה סבלו 25% מהמטופלים מהישנות הייתה 23 יום בקבוצת הפלצבו לעומת 83 יום בקבוצת Paliperidone ER. גם מדדים אחרים של חומרת התסמינים (QOL, תפקוד המטופל) הראו עלייה משמעותית.
תדירות תופעות הלוואי בעקבות הטיפול הייתה דומה בקבוצות של Paliperidone ER ופלצבו. תופעות הלוואי הנפוצות ביותר שדווחו בעקבות הטיפול בשלב הפתוח כללו רעד (16%), כאב ראש (%14), היפרקינזיה(12%) ונדודי שינה (10%). בשלב כפול-הסמיות דווח רק על פסיכוזה, תגובה תוקפנית ונדודי שינה
≥5% מהמטופלים בכל אחת מקבוצות הטיפול. העלייה הממוצעת במשקל הייתה 1.8 ק"ג בקבוצה של Paliperidone ER לעומת 0.2 ק"ג בקבוצת הפלצבו.
במחקר מעניין אחר .Canuso et al מסן-דייגו (6) הישוו בניסוי כפול-סמיות את הטיפול ב-Paliperidone ER, לטיפול ב-Quetiapine.
399 חולי סכיזופרניה שסבלו מהחמרה אקוטית ונזקקו לאשפוז שובצו באקראי לטיפול ב-Paliperidone ER, Quetiapine או פלצבו.
התוצאות הראו שיפור משמעותי עם Paliperidone ER לעומת Quetiapine מבחינת ממוצע (SE) השינוי בניקוד PANSS כבר מיום 5 -11.4 (1.1)] לעומת (1.1) -8.2; p=0.011)] ועד לסיום המונותרפיה כעבור שבועיים [(1.8) -23.4 לעומת (1.8) -17.1; p<0.001].
כמו כן, נמצאו שיפורים משמעותיים עם פליפרידון בשחרור מושהה, לעומת קווטיאפין בניקוד הפקטורים החיוביים, השליליים, מחשבות לא מאורגנות ועוינות/התרגשות בלתי נשלטת ב- SSNAP (p≤0.008).
המסקנות היו כי פליפרידון בשחרור מושהה (9-12 מ"ג) יעילה יותר מקווטיאפין (600-800 מ"ג ליום) בטווח הקצר כטיפול חד-תרופתי להחמרה אקוטית של סכיזופרניה שאירעה לאחרונה וחייבה אשפוז.
סיכום
לרופא המטפל בחולי סכיזופרניה הזקוק לתרופות אפקטיביות וחדשניות Paliperidone ER היא תרופה אטיפית חדשה המפחיתה את רמת תופעות הלוואי, תוך שמירה על יעילות טיפולית ושיפור משמעותי אף בתפקודים האישיים והחברתיים של החולים. לשיפור במדדים אלה משמעות רבה בקרב חולי הסכיזופרניה הנוטים להחליף את הטיפול התרופתי מספר פעמים בשנה מסיבות שונות (כישלון בטיפול, תופעות לוואי, היעדר דבקות בטיפול). התרופה רשומה בארץ מאוגוסט 2008 והוגשה בקשה לכלול אותה בסל התרופות לשנת 2009.
מידע ברשת
ביבליוגרפיה
- Vermeir M, Boom S, Naessens I, Talluri K, Eerdekens M. Metabolism and excretion of a single oral dose of 14C-paliperidone 1 mg in healthy subjects (poster). 18th Annual Meeting of the European College of Neuropsychopharmacology; October 22-26, 2005; Amsterdam, Netherlands.
- Conley R, Gupta, SK, Sathyan G. Clinical spectrum of
the osmotic-controlled release oral delivery system (oros), an advanced oral delivery form. Current medical research and opinion 2006;22(10):1879-1892
- עלון לרופא כפי שאושר על ידי משרד הבריאות, אוגוסט 2008
- Kane, J et al. Treatment of schizophrenia with paliperidone extended-release tablets: a 6-week placebo-controlled trial. Schizophrenia Research 2007;90 (1-3):147-161
- Kramer, M, et al. Paliperidone extended-release tablets for prevention of symptom recurrence in patients with schizophrenia. A randomized, double-blind, placebo-controlled study. Journal Clinical Psychopharmacology 2007;27 (1):6-14
- Canuso C, et al. A comparative analysis of paliperidone ER and quetiapine in patients with a recent, acute exacerbation of schizophrenia, presented at the 20th Annual U.S. Psychiatric and Mental Health Congress in Orlando, Florida 2007
המידע שבדף זה נכתב על ידי ד"ר רוני מאור (MD), חברת יאנסן סילג; ד"ר שילה גלרשטיין (PhD), מנהלת מדעית ומנהלת מחקרים קליניים, חברת יאנסן סילג


 כניסה
כניסה  עקבו אחרינו בפייסבוק
עקבו אחרינו בפייסבוק