אנטיגן NS1 של נגיף דנגי - NS1 antigen test
| מדריך בדיקות מעבדה | |
| אנטיגן NS1 של נגיף דנגי | |
|---|---|
| NS1 antigen test | |
| מעבדה | נגיפים, כימיה בדם |
| תחום | זיהוי הדבקה בנגיף דנגי (Dengue) |
| יוצר הערך | פרופ' בן-עמי סלע |
לערכים נוספים הקשורים לנושא זה, ראו את דף הפירושים – דנגי
מטרת הבדיקה
סיוע באבחון הדבקה בנגף Dengue.
זיהוי של החלבון הלא-מבני NS1 של Dengue מצביע על חשיפה עדכנית ו/או הדבקה אקוטית עם הנגיף.
הפיזיולוגיה של הנגיף
נגיף דנגי (Dengue) (להלן DV) הוא נגיף flavi המפוזר בכל העולם והוא מכיל 4 serotypes:
- DV-1
- DV-2
- DV-3
- DV-4
הנגיף מועבר בעיקר על ידי היתוש Aedes aegypti, השכיח באזורים הטרופיים והתת-טרופיים של מעל 100 מדינות, ולכן נגיף זה מהווה בעיה בריאותית ציבורית עבור בערך 2.3 עד 3.0 מיליארד אנשים המתגוררים באזורים אנדמיים, מתוכם 50–100 מיליון אנשים יידבקו על ידי הנגיף, ו-30,000 איש ימותו בגינו מדי שנה (Bhatt וחב' ב-Nature משנת 2013). הדבקות אלו תגרומנה לחצי מיליון אשפוזים בשנה בעולם כולו בגין דימומים וחום גבוה, כאשר התמותה מהנגיף עלולה להיגרם ל-5-10% מהנדבקים בנגיף. כאמור, DV אנדמי במדינות באסיה, אפריקה, מדינות בפסיפיק, באמריקה ובאיים הקריביים (Kyle ו-Harris ב-Ann Rev Microbiol משנת 2008, Guzman וחב' ב-Nature Rev Microbiol משנת 2010, Alves וחב' ב-Revista da Sociedade Brasliera de Medicina Tropical משנת 2011, Amarasinghe וחב' ב-Emerging Infectious Diseases משנת 2011, Blaylock וחב' ב-Travel Med & Infect Dis משנת 2011, Brown וחב' ב-West Indian Med J משנת 2011, Chaaithanya וחב' ב-India Epidemiol Infect משנת 2001, Cuong וחב' ב- PLos Neglect Trop Dis משנת 2011, Franco וחב' באותו כתב-עת מאותה שנה, Gutierrez וחב' באותו כתב-עת משנת 2011, Hayden וחב' ב-New South Wales Pub Health Bull משנת 2011, Rai ב-Nature משנת 2011, Tissera וחב' ב-Emerging Infectious Diseases משנת 2011, Whitehorn וחב' ב-Clin Med משנת 2011, Hynes ב-Cleve Clin J Med משנת 2012, ו-Simmons וחב' ב-N Eng J Med משנת 2012).
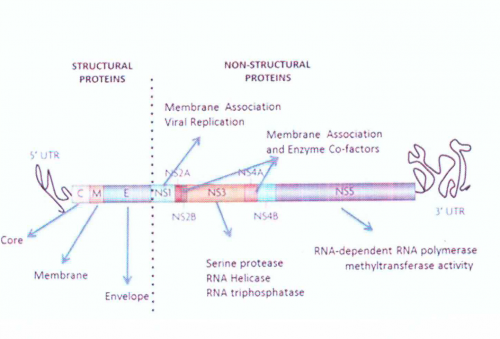
אזורי ההתפשטות של DV ממשיכים להתרחב כתוצאה מגורמים כגון עיוּר מוגבר, נסיעות וטיולים מוגברים בעולם, וכן ההתחממות הגלובלית (McMichael וחב' ב-Lancet משנת 2006, Natiello וחב' ב-Emerging Infectious Diseases משנת 2008, Banu וחב' ב-Tropical Med Int Health משנת 2011, Chen ו-Vasilakis ב-Viruses משנת 2011, Luz וחב' ב-Lancet משנת 2011, Bouri וחב' ב-Pub Health Rep משנת 2012, ו-Amarasinghe וחב' ב-Emerging Infectious Diseases משנת 2012). תקופת ההדגרה של הנגיף לאחר ההדבקה היא 3–10 ימים, ובה בשעה שחלק מההדבקות תיוותרנה א-תסמיניות, רוב הנדבקים ייפתחו את קדחת Dengue הקלאסית. הגנום של הנגיף מקודד לשלושה גליקו-חלבונים מבניים: ה-capsid (להלן C), חלבון הממברנה (להלן M) וחלבון המעטפת (להלן E). כמו כן מקודד הגנום ל-7 חלבונים לא-מבניים (NS4B ,NS4A ,NS3 ,NS2B ,NS2A ,NS1 ו-NS5).כל סוג של הנגיף הוא בעל הומולוגיה של 65% ברצף הגנום, ולמרות השוני הגנומי, כל serotype של DV גורם לתסמינים כמעט זהים באנשים הנדבקים בנגיף. הדבקה עם serotype מסוים משרה חסינות לכל החיים כנגד הדבקה מחודשת עם אותו serotype בלבד, אך רק הגנה זמנית וחלקית מהדבקה על ידי ה-serotypes האחרים (Gubler ו-Kuno ב-CAB Int משנת 1997, Gordon וחב' ב-PLoS Neglect Trop Dis Trop PLos Neglect משנת 2013, ו-Guzman ו-Vasquez ב-Viruses משנת 2010).
תסמינים קליניים
קלינית, הדבקה עם DV יכולה לחלוף ללא תסמינים, אך עלולה גם לגרום מוות (Guzman וחב' ב-PLoS Neglect Tropical Dis משנת 2010, Giraldo וחב' ב-Trans Royal Soc Tropic Med Hygien משנת 2011, Kalayanarooj ב- J Med Assoc Thailand משנת 2011). אנשים בשלב מוקדם של ההדבקה יכולים לסבול מהופעה פתאומית של חום, וכן כאבים לא ספציפיים ככאבים באזורי גוף שונים, כאבי שרירים, אדמומיות עור, סומק בפנים, כאבי ראש ופרקים. ייתכן גם כאב רטרו-אורביטלי הדומה למיגרנה או לכאב ראש צרור. פריחה מקולרית זמנית מופיעה בעיקר בילדים. זו מוגדרת כפאזה האקוטית של ההדבקה, שיכולה להימשך בין 2–7 ימים. לאחר פאזה התחלתית זו, המחלה מתקדמת בדרך כלל דרך פאזה קריטית המתאפיינת על ידי חום בתחום שבין 37.5-38.0 צלזיוס ועל ידי דרגות שונות של דליפת פלזמה לתוך חללי הפלאורה והבטן שנמשכת 24–48 שעות. בשלב זה, תסריטים שונים של התקדמות המחלה יכולים להתרחש, כאשר בכמה נדבקים מוצאים שיפור, ואילו באחרים תחול הידרדרות עם סימני אזהרה. האנשים האחרונים עשויים להתאושש על ידי עירוי נוזלים לווריד, אך אחרים עלול להידרדר אף למוות, אם הטיפול אינו נאות. לסיכום, תסמיני dengue החמורים מתבטאים בדליפת פלזמה עד כדי הלם, בהצטברות של נוזל סרוזי הדומה לנסיוב אך מכיל מעט חלבון, שעלול לגרום למצוקה נשימתית. כמו כן עלול להופיע דימום ופגיעה באיברים שונים (Gregory וחב' ב-Am J Trop Med Hygiene משנת 2010, Alexander וחב' ב-Trop Med Int Health משנת 2011, Chitra ו-Panicker ב-J Vector Borne Dis משנת 2011, Kalayanrooj וחב' ב-Trop Med Health משנת 2011, Kulkarni וחב' ב-Indian J Med Microbiol משנת 2011, Narvaez וחב' ב-PLoS Neglect trop Dis משנת 2011, ו-Akbar וחב' ב-Clin Infect Dis משנת 2012).
מנגנון המחלה
המנגנון האחראי למחלת Dengue חמורה אינו ברור במלואו, אם כי ישנן מספר השערות. גורמי סיכון למחלה חמורה כוללים הדבקה קודמת עם serotype הטרוטיפי (Kliks וחב' ב-Am J Trop Med Hygiene משנת 1989, Dejnirattisai וחב' ב-Science משנת 2010, ו-Tricou וחב' ב-BMC Infect Dis משנת 2010), הזן של הנגיף המדביק (Vaughn וחב' ב-J Infect Dis משנת 2000, Wang וחב' ב-Virology משנת 2003, de Araujo וחב' ב-Trans Royal Soc Trop Med Hygiene משנת 2009, Costa וחב' ב-Infect Genet Evolution משנת 2012, ו-Maciel-de-Freitas ב-Trans Royal Soc Trop Med Hygiene משנת 2011) בגיל ובמגדר (Anders וחב' ב-Am J Trop Med Hygiene משנת 2011 ו-Balasubramanian וחב' ב-Arch Dis Child משנת 2012), סטאטוס התזונה (Thisyakorn ו-Nimmannitya ב-Clin Infect Dis משנת 1993, Kalayanarooj וחב' ב-Southeast J Trop Med Pub Health משנת 2005), והרקע הגנטי של הנדבק (Nguyen וחב' ב-PLoS Neglect Trop Dis משנת 2008, ו-Appanna וחב' ב-PLoS One משנת 2010). גיל הנדבק והסטאטוס החיסוני שלו הם גורמי מפתח בחומרת המחלה והתקדמותה (Guzman וחב' ב-PLoS Neglect Trop Dis משנת 2010). הדליפה מכלי הדם חמורה ביותר בקרב ילדים והיא קשורה כנראה בפגיעה בשלמות הקפּילרות (Gamble וחב' ב-Clin Scu משנת 2000).
מחקרים אפידמיולוגיים הראו שמחלה חמורה שכיחה יותר לאחר הדבקה שניונית אפילו אם מדובר ב-serotype אחר של הנגיף (graham וחב' ב-Am J Trop Med Hygiene משנת 1999 ו-Halstead ב-Adv Virus Res משנת 2003). הדבקה עם DV-1 שאחריה יש הדבקה עם DV-2 או DV-3, או הדבקה ראשונה עם DV-3 שאחריה יש הדבקה עם DV-2, כרוכות בתסמונת הלם Dengue (על פי Guzman וחב' ב-Am J Trop Med Hygiene משנת 1990, ו-Alvarez וחב' באותו כתב-עת משנת 2006). אף על פי שלא קיים טיפול אנטי-נגיפי ספציפי בהדבקות DV, הדבקה לא חמורה יכולה להיות מטופלת על ידי נוזלים פומיים ו-paracetamol בהצלחה משמעותית. מחלה חמורה צריכה להיות מטופלת על ידי עירוי נוזלים לווריד (Nimmannitya ב-Southwest J Trop Med Pub Health משנת 1987). קריטי לבצע אבחון מבדיל בין של Dengue ותחלואות אחרות עם חום גבוה, אם כי בשלבים מוקדמים של קדחת Dengue קשה מאוד לאבחנה כיוון שהתסמינים המוקדמים של הדבקה בנגיף זה אינם ספציפיים (Potts ו-Rothman ב-Trop Med Int Health משנת 2008).
בידוד הנגיף
תהליך בידוד הנגיף מייגע ועלול להימשך בין 7–14 יום לקבלת תוצאות. לפיכך, זו אינה שיטה מתאימה לזיהוי מוקדם של הדבקה עם נגיף זה. תרבית תאים היא השיטה הנפוצה ביותר לבידוד נגיפים. שורות תאים המתאימות ליתוש הרלוונטי הן Ae. albopictus C6/36 ו-Ae. pseudoscutllaris AP61 (על פי Race וחב' ב-Lancet משנת 1978, Tesh ב-Am J Trop Med Hygiene משנת 1979, Kuno וחב' ב-Bull WHO משנת 1985, ו-Nawa וחב' ב-Jap J Med Sci Biol משנת 1987). זיהוי הנגיף מתבצע בשיטה אימונו-פלואורוסצנטית עם נוגדנים חד-שבטיים ספציפיים לנגיף (Henchal וחב' ב-Am J Trop Med Hygiene משנת 1983, ו-Gubler וחב' באותו כתב-עת משנת 1984). ה-WHO ממליץ שדגימת הנדבקים לצורך בדיקת זיהוי הנגיף תתבצע במהלך 5 הימים הראשונים מהופעת החום.
זיהוי RNA נגיפי על ידי RT-PCR
שיטה זו מהירה יחסית עם תוצאות תוך 24–48 שעות, אך היא יקרה יחסית ולא תמיד זמינה במדינות האנדמיות. לאבחון שגרתי של הדבקה עם DV השיטה הנפוצה ביותר היא אמפליפיקציה של חומצת גרעין (להלן NAAT) המבוססת על ריאקציית שרשרת של האנזים reverse transcriptase polymerase בזמן אמת (RT-PCR) (על פי Morita וחב' ב-J Clin Microbiol משנת 1991, ו-Lanciotti וחב' באותו כתב-עת משנת 1992, ו-Harris וחב' באותו כתב-עת משנת 1998). הרגישות של מבחני RT-PCR בהשוואה לבידוד הנגיף בתרבית תאים נעה בין 25-79% (Raengsakulrach וחב' ב-J Virol Methods משנת 2002, ו-Tesh ב-J Trop Med Hygiene משנת 1979). בגישה עכשווית הרגישות המדווחת היא מעל 90% בשיטות NAAT בהשוואה לבידוד הנגיף תוך שימוש בשורת התאים C6/36 (על פי Wu וחב' ב-J Clin Microbiol משנת 2001, Hapugoda וחב' ב-Trans Royal Soc Trop Med Hygiene משנת 2010, Callahan וחב' ב-J Clin Microbiol משנת 2001, ו-Houng וחב' ב-J Virol Methods משנת 2001).
זמן דגימת החומר לבדיקות NAAT קריטי ומומלץ שיהיה בתחום של 5 ימים מהופעת החום. לאבחון שגרתי של הדבקה עם DV השיטה הנפוצה ביותר היא אמפליפיקציה של חומצת גרעין (להלן NAAT) המבוססת על ריאקציית שרשרת של האנזים reverse transcriptase polymerase בזמן אמת (RT-PCR) (על פי Morita וחב' ב-J Clin Microbiol משנת 1991, ו-Lanciotti וחב' באותו כתב-עת משנת 1992, ו-Harris וחב' באותו כתב-עת משנת 1998). הרגישות של מבחני RT-PCR בהשוואה לבידוד הנגיף בתרבית תאים נעה בין 25-79% (Raengsakulrach וחב' ב-J Virol Methods משנת 2002).
בדיקות סרולוגיות המבוססות על גילוי נוגדנים מסוג IgM ו-IgG כנגד הנגיף
בדיקות אלה הן השימושיות ביותר לזיהוי הדבקה ב-DV. מציאות נוגדנים מסוג IgM ו-IgG היא במתאם עם התקדמות המחלה ועם סוג ההדבקה (ראשונית או חוזרת) והיא נחקרה רבות (Gubler ב-Dengue Bull משנת 1996, Innis וחב' ב-Am J Trop Med Hygiene משנת 1989, Chanama וחב' ב-J Clin Virol משנת 2004, ו-Wahala וחב' ב-Viruses משנת 2011). אף על פי שמציאת נוגדנים כנגד הנגיף שיטה זולה יותר וקלה יותר לביצוע מאשר RT-PCR, שיטה זו מחייבת בחינה של דגימה כפולה, האחת הנלקחת בשלב האקוטי של המחלה, והשנייה בשלב ההחלמה כאשר הדגימה השנייה נלקחת למעלה מ-7 ימים מהופעת החום, על מנת לספק אבחון מוחלט. לכן גישה זו אינה מתאימה לצורך החלטות קליניות בזמן אמת. שיטות סרולוגיות אחרות הנמצאות בשימוש הן IgM antibody capture ELISA (הידועה כ-MAC-ELISA), כמו גם E/M -specific capture IgM & IgG ELISA (על פי Burke וחב' ב-J Clin Microbiol משנת 1982, ו-Bundo ו-Igarashi ב-J virol Methods משנת 1985). שיטה נוספת היא של עיכוב המאגלוטינציה (HI) (על פי Clarke ו-Casals ב-Am J Trop Med Hygiene משנת 1958), שעדיין נחשבת לשיטה מקובלת (Shu וחב' ב-Clin Diagn Lab Immunol משנת 2004). באופן מסורתי, בדיקת HI שימשה לגלות ולהבדיל בין הדבקות ראשוניות וחוזרות של DV, בשל רגישותה הגבוהה וקלות ביצועה. אך שיטה זו פחות פופולרית והיא הוחלפה בהדרגה על ידי שיטות MAC-ELISA ו-E/M specific capture IgM & IgG ELISA (על פי Shu ו-Huang ב-Lab Immunol משנת 2004). למעלה מ-50 ערכות מסחריות זמינות עם דרגות רגישות וספציפיות שונות (Blacksell וחב' ב-Clin Vaccine Immunol משנת 2007, Dussart וחב' באותו כתב-עת משנת 2006, Blacksell וחב' ב-Diagn Microbiol Infect Dis משנת 2008, Bessoff וחב' ב-Clin Vaccine Immunol משנת 2008, Dussart וחב' ב-PLoS Neglect Trop Dis משנת 2008, Wang ו-Sekaran ב-J Clin Microbiol משנת 2010, Blacksell וחב' ב-Clin Vaccine Immunol משנת 2012).
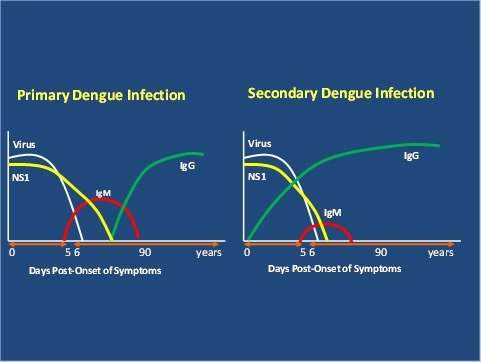
אף על פי ש-MAC-ELISA המגלה נוגדני IgM קלה יותר לביצוע וזולה יותר מבידוד הנגיף DV או משיטות NAAT, יש לה מספר מגבלות חשובות. שיטה זו אינה מאפשרת זיהוי מוקדם של הדבקה ב-DV, שכן במהלך הדבקות ראשוניות נוגדנים מסוג IgM ניתנים לגילוי רק ב-50% מהנבדקים בין הימים 3–5 מהופעת החום, ב-80% ביום החמישי, וב-99% ביום העשירי. לכן WHO ממליץ שבשיטה זו דגימות תילקחנה רק לאחר 5 ימים מהופעת החום.
במטופלים עם הדבקה חוזרת ב-DV, הקינטיקה של יצירת IgM יותר מגוונת ורמות IgM משמעותית נמוכות יותר מאשר במהלך הדבקה ראשונה. תוצאות false negative לגבי נוגדני IgM כנגד DV עלולות להתקבל במהלך הדבקה חוזרת. בנוסף, בדיקות אחדות נותנות ריאקטיביות לא-ספציפית בדגימות נסיוב של מטופלים עם מלריה או עם leptospirosis. מבחן IgG ELISA יכול לשמש לאשרור של הדבקה עם DV אם 2 דגימות בהפרש מספר ימים נלקחות לצורך הבדלה בין הדבקה ראשונית והדבקה חוזרת (Vaughn וחב' ב-Am J Trop Med Hygiene משנת 1999). בהדבקה ראשונית של DV, מתגלהIgG בדרך כלל בטיטר נמוך בסוף השבוע הראשון של המחלה, והטיטר עולה באיטיות לאחר מכן כאשר נוגדני IgG כנגד הנגיף ניתנים לגילוי אף לאחר מספר חודשים (וייתכן אפילו לשארית החיים). במהלך הדבקה חוזרת, רמות גבוהות של נוגדני IgG ניתנות לזיהוי בפאזה האקוטית של הדבקה חוזרת זו. עלייה של פי-4, או אף גבוהה יותר של נוגדני IgG בדגימות נסיוב של הפאזה האקוטית או של שלב ההחלמה, יכולה לשמש לצורך תיעוד של ההדבקות בתקופה הסמוכה לביצוע הבדיקה, עם זאת בדיקת -IgG ELISA חסרה בדרך כלל ספציפיות בין קבוצות שונות של מודבקים עם נגיפי flavi (על פי Makino וחב' ב-Microbiol Immunol משנת 1994).
היחס בין DV E/M protein-specific IgM לבין DV E/M protein-specific IgG, יכול לשמש לצורך הבדלה בין הדבקה ראשונית והדבקה חוזרת של הנגיף, כאשר IgM capture ELISA ו-IgG capture ELISA, הן הבדיקות השכיחות ביותר למטרה זו (Prince וחב' ב-Clin Vaccine Immunol משנת 2011). לפי שיטה זו, הדבקה עם DV מוגדרת ראשונית אם יחס ה-optical density של IgM לעומת IgG גדול מ-1.2 (כאשר משתמשים בדגימות נסיוב מהולות 1:100), או גדול מ-1.4 (כאשר דגימות הנסיוב מהולות 1:20). ההדבקה שניונית כאשר היחס קטן מ-1.2 עם דגימות נסיוב מהולות 1:100, או קטן מ-1.4 עם דגימות נסיוב מהולות 1:20 (על פי Kuno וחב' ב-J Virol Methods משנת 1991). עם זאת, יחסים אלה עלולים להיות שונים במעבדות שונות, מה שמצביע על צורך לסטנדרטיזציה טובה יותר בין המעבדות (Falconer וחב' ב-Clin Vaccine Immunol משנת 2006).
השימוש ב-NS1 לזיהוי הדבקה ב-DV
זיהוי של NS1: מבחן האנטיגן הלא-מבני NSI הוכנס בשנת 2006 Dussart) וחב' ב-Clin Vaccine Immunol משנת 2006), וחשיבותו ביכולתו לזהות הדבקה ב-DV כבר לאחר יום אחד, כ-5 ימים לפני הופעת נוגדנים לנגיף. זיהוי NS1 אפשרי עד 9 ימים מההדבקה. הוא מאושר לשימוש בלמעלה מ-80 מדינות (Narayan וחב' ב-Indian J Med Res משנת 2016, ו-Amorim וחב' ב-Virus Res משנת 2016). אנטיגן NS1 יכול להיות מזוהה גם במהלך הדבקה חוזרת עם DV, אלא שבמקרה זה זיהויו בתוקף לפרק זמן קצר יותר של 1–4 ימים ממועד ההדבקה החוזרת. תוצאה שלילית בבדיקה לזיהוי NS1, פירושה אי הדבקה על ידי הנגיף (Chumansumrit וחב' ב-Pediatr Infect Dis J משנת 2008, ו-Chaiyaratana וחב' ב-Diagn Microbiol Infect Dis משנת 2009).
מספר מחקרים הציעו שזיהוי החלבון הלא-מבני NS1 של נגיף dengue, יכול להוות שיטה יעילה לאבחון מוקדם של הדבקה בנגיף (Young וחב' ב-J Clin Microbiol משנת 2000, Huang וחב' ב-J Med Virol משנת 2001, Koraka וחב' ב-J Clin Microbiol משנת 2006, Alcon וחב' באותו כתב-עת משנת 2002, ו-Xu וחב' באותו כתב-עת משנת 2006). החלבון NS1 הוא גליקו-פרוטאין לא-מבני בעל משקל מולקולרי של 46,000 דלטון, המשומר היטב בנגיפי flavi, כולל Dengue כמו גם Tick-borne encephalitis ו-Japanese encephalitis yellow fever (על פי Winkler וחב' ב-Virology משנת 1989, ו-Chuansumrit וחב' ב- Diagn Microbiol Infect Dis משנת 2011). האנטיגן NS1 התגלה בנסיוב של חולים בשלב האקוטי של ההדבקה (Hu וחב' ב-Virol J משנת 2011) כבר ביום הראשון לאחר הופעת החום ב-80-87.5% מהדגימות, והוא נותר מזוהה בנסיוב של מחלימים עד 14 יום לאחר הופעת החום. אף על פי ששיעור החיוביות של הבדיקה דועך בהדרגה בדגימות שנלקחו בין הימים 8–14 מהופעת החום, בסך הכול אנטיגן NS1 המופיע בדם של נדבקים בנגיף מתגלה לתקופות ארוכות יותר מאשר RNA נגיפי (Kumarasamy וחב' ב-Singapore Med J משנת 2007, Singh וחב' ב-Diagn Microbiol Infect Dis משנת 2010 ו-Huhtamo וחב' ב-J Clin Virol משנת 2010). לא ברור האם עודף אנטיגן NS1 עשוי לשמש כסמן אבחוני של הדבקה חוזרת (Duong וחב' ב-PLoS Neglect Trop Dis משנת 2011). מספר מחקרים מדווחים על הבדלים משמעותיים בזיהוי NS1 בדגימות נסיוב של נדבקים בפעם הראשונה או השנייה. מחקרים אחרים מדווחים על ירידה משמעותית ברגישות של בדיקות המבוססות על NS1 בהדבקות חוזרות (Hang וחב' ב-PLoS Neglect Trop Dis משנת 2009). אם לוקחים בחשבון את הרמות הגבוהות יותר של נוגדנים אנטי-NS1 האופייניות להדבקה החוזרת, הרגישות הנמוכה יותר בדיקות מבוססות על NS1, יכולות לנבוע משיעור גבוה של אנטיגן NS1, הקשור לקומפלקסים אימוניים, מה שגורם לרמה נמוכה יותר של NS1 חופשי בנסיוב של אנשים מודבקים ב-Dengue.
בדיקות מעבדה
המשמעות של בדיקות מעבדה לזיהוי הדבקה ב-DV, תלויה בשלב המחלה כאשר נדגם החולה לביצוע הבדיקות (Guzman ו-Kouri ב-Int J Trop Dis משנת 2004).
כיוון שהסימנים והתסמינים של קדחת Dengue אינם ספציפיים, קריטריונים מעבדתיים לאפיון המחלה כוללים את הממצאים הבאים: הדגמה של אנטיגן נגיפי ברקמת אוטופסיה בשיטת אימונו-היסטוכימיה או אימונו-פלואורסצנציה, או בדגימות נסיוב בשיטות enzyme-immunoassay כגוןMAC-ELISA, IgG ELISA ,NS1 או EIA. כמו כן זיהוי של רצפי גנום נגיפי ברקמת אוטופסיה, בנסיוב או ב-CSF על ידי RT-PCR. באופן פחות שכיח, בידוד של DV מנסיוב, מפלזמה, מלויקוציטים או מרקמת אוטופסיה. RT-PCR מייצר אבחון סרוטיפי-ספציפי במהירות רבה (Warrilow ב-J Med Virol משנת 2002, ו-Kong וחב' ב-J Virol Methods משנת 2006). שיטה זו מאוד שימושית בשלבי המחלה המוקדמים, ואינו חשוף להצלבה עם נגיפי flavi אחרים, כפי שמוצאים בבדיקות סרולוגיות.
בדיקות המעבדה הבאות צריכות להתבצע כדי לספק נתוני עזר לאבחון:
- ספירת דם מלאה (CBC) בה צפויים למצוא המטוקריט מוגבר בלמעלה מ-20% בגין ריכוז-יתר של הפלזמה כתוצאה של דליפת דם מכלי הדם לרקמה המקיפה אותם. ההמטוקריט צריך להימדד אחת ל-24 שעות כדי לזהות מוקדם תרחיש של hemorrhagic fever, ואחת ל-3–4 שעות במקרים חמורים של התרחיש האחרון, או במקרים של תסמונת הלם על ידי DV. ממצאים אופייניים של קדחת dengue הם תרומבוציטופניה (ספירת טסיות דם הנמוכה מ-100,000 למ"ל), שהודגמה בעד-50% מהמקרים של קדחת dengue, והיא מזוהה עוד לפני ירידת החום בקדחת זו או התחלת ההלם. ממצא אחר הוא מִעוּט כַּדּוּרִיּוֹת לְבָנוֹת (leukopenia) המופיע בדרך כלל ביחד עם לימפופניה נצפה בדרך כלל סמוך לסיום השלב החום הגבוה של המחלה. לעומת זאת, לימפוציטוזיס עם לימפוציטים לא-אופייניים, מתפתחת בדרך כלל לפני ירידת החום או ההלם. סקירה סיסטמטית מצאה שבמטופלים עם DV יש ירדה משמעותית במספר כדוריות הדם הלבנות, בנויטרפילים, ובטסיות הדם, בהשוואה למחלות חום אחרות באוכלוסיות אנדמיות ל-DV (על פי Potts ו-Rothman ב-Trop Med Int Health משנת 2008). בדיקות המעבדה יכולות לגלות גם עלייה קלה עד ממוצעת של שני אנזימי הכבד, sGPT ו-sGOT, אם כי לא מגלים כשל כבד חמור או צהבת. אנזימי הכבד מתחילים לעלות בשלב מוקדם, ומגיעים לשיאם בשבוע השני. מדידת רמת חלבונים ואלבומין בדם מצביעה באופן כללי על היפו-פרוטאינמיה.
פנל מטבולי ואנזימי כבד: היפונתרמיה היא האנומליה הבולטת ביותר של אלקטרוליטים באנשים עם Dengue hemorrhagic fever, או עם תסמונת הלם על ידי Dengue. חמצת מטבולית מזוהה באנשים עם הלם ויש לתקנה במהירות. רמות urea מוגברות מזוהות במצבי הלם. לעומת זאת, נזק אקוטי לכליות אינו שכיח במצב זה (Lima ו-Nogueira ב-Semin Nephrol משנת 2011, ו-Lombardi וחב' באותו כתב עת מאותה שנה.
מבחני קרישה: בנדבקים עם הנגיף ותסמיני hemorrhagic fever ניתן לגלות זמן פרותרומבין מוארך, APTT (או (activated partial thromboplastin time מוארך, רמת פיברינוגן נמוכה, וכמות מוגברת של פיברין ושל תוצרי הביקוע שלו (כאשר האחרונים הם סממן של DIC או disseminated intravascular coagulation). כל אלה עם חשד להדבקה עם DV צריכים לעבור בדיקת guaiac לזיהוי דם סמוי בצואה.
בדיקת שתן (urinalysis) מזהה המטוריה. מדידת גז עורקי חיונית באלה עם מחלה אקוטית להערכת ה-pH בדם, רמת החמצון שלו ודרגת האוורור. ביופסיה של נגעי עור בנדבקים עם מחלה לא מורכבת עשויה לגלות אנומליה בנימי דם. התנפחות אנדותליאלית, בצקת סב-וסקולרית, והסננה של תאים חד-גרעיניים הם ממצאים היסטולוגיים ראשיים. מומלץ גם לבצע הדמיית חזה לבחינת אפשרות של תפליטים פלאורליים, ודלקת ריאות. תפליט פלאורלי של צד ימין אופייני, ואילו תפליטים פלאורליים דו-צדדיים שכיחים באלה עם תסמונת הלם dengue. ביצוע CT של הראש ללא חומר ניגוד מומלץ במטופלים הנמצאים בדרגות הכרה משתנות, כדי לזהות דימום תוך-גולגולתי, או בצקת מוחית במצב של dengue hemorrhagic fever.
אולטרה-סאונד (US): ביצוע סריקות US הוא הליך עם עלות-יעילות טובה וקל לביצוע בהערכה של dengue hemorrhagic fever פוטנציאלי. ממצאים חיוביים ואמינים של US כוללים נוזל בחזה ובחלל הבטן, תפליט פריקרדיאלי ודופן מעובה של כיס המרה (Statler וחב' ב-J Clin Ultrasound משנת 2008, Santhosh וחב' ב-J Clin Imaging Sci משנת 2014, ו-Srikiatkhachorn וחב' ב-Pediatr Infect Dis משנת 2007). התּוֹעַלְתִּיּוּת של מחקרים קודמים הייתה מוגבלת כיוון שהמטופלים עברו בדיקת US בודדת. אך מחקרם של Srikiatkhachorn וחב' הראה שבדיקות US יומיות של בית החזה והבטן, היו יעילות בהערכת נבדקים עם חשד ל-dengue hemorrhagic fever. גם מחקרם של Santhosh וחב' הראה שממצאי US של דופן מעובה של כיס המרה היו נכונים ב-66.7% מהנבדקים החיוביים סרולוגית להדבקה עם DV, ב-64.5% מאלה עם מיימת, וב-50.3% מאלה עם תפליט פלאורלי.
קריטריוני-עזר לאבחון מחלת DV חמורה כוללים דימום מרקמות ריריות בעיקר במערכת העיכול, הקאת-דם (hematemesis), צואה שחורה (melena), דמם תת-עורי או תוך-עורי זעיר (petechiae), פורפורה או אכימוזות (שטפי דם תת-עוריים המופיעים ככתמים כחולים-סגולים). ראיות לדליפת פלזמה כתוצאה מחודרנות וסקולרית. קריטריוני-עזר במקרים של הלם מקדחת dengue כוללים דופק מהיר אך חלש, לחץ-דם נמוך, עור קריר, הפרש מועט בין לחצי הדם הסיסטולי והדיאסטולי (נמוך מ-20 מ"מ כספית) שמוגדר כ-narrow pulse pressure, והגברה של התנגודת הווסקולרית ההיקפית (PVR). כמו כן יש שינויים בסטאטוס הנפשי.
הוראות לביצוע הבדיקה
יש לדגום דם במבחנה כימית (פקק אדום או צהוב או במבחנת ג'ל). את הנסיוב המבודד לאחר הסרכוז יש להקפיא או לשמור בקור. יש לפסול דגימות נסיוב מאוד, המוליטיות, ליפמיות או איקטריות. דגימות הנסיוב מועדפות כמקוררות או קפואות, ובשתי צורות אלה יציבות הדגימה עד 14 יום.
שיטת הבדיקה: Enzyme-Linked Immunosorbent Assay (ELISA).
ראו גם
המידע שבדף זה נכתב על ידי פרופ' בן-עמי סלע, המכון לכימיה פתולוגית, מרכז רפואי שיבא, תל-שומר;
החוג לגנטיקה מולקולארית וביוכימיה, פקולטה לרפואה, אוניברסיטת תל-אביב (יוצר הערך)


 כניסה
כניסה  עקבו אחרינו בפייסבוק
עקבו אחרינו בפייסבוק