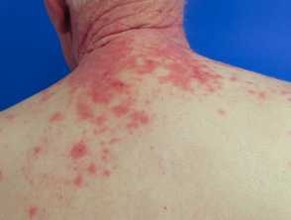
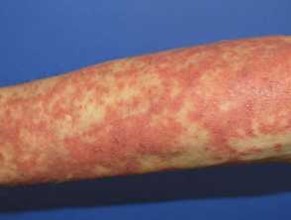
בדיקת נוגדנים כנגד פמפיגוס פאראנאופלסטי - Antibody test for paraneoplastic pemphigus
| מדריך בדיקות מעבדה | |
| בדיקת נוגדנים כנגד פמפיגוס פאראנאופלסטי | |
|---|---|
| Antibody test for paraneoplastic pemphigus" | |
| מעבדה | המטולוגיה בדם |
| תחום | תחלואת עור |
| יוצר הערך | פרופ' בן-עמי סלע |
מטרת הבדיקה: אבחון של paraneoplastic pemphigus תרחיש של מחלה רירית-עורית ליכנואידיים.
Paraneoplastic Pemphigus (PNP)
מדובר ב-PNP שהיא מחלה אוטו-אימונית שלפוחיתית המשפיעה על מבוגרים או באופן נדיר על ילדים, המצביעה על נוכחות של ממאירות נסתרת. PNP יכולה להיות מוגדרת כשילוב של המאפיינים הבאים:
- סטומטיטיס מכאיבה והתלקחות עורית פולימורפית, עם נגעים שיכולים להיות שלפוחייתיים, ליכנואידים, בעלי תצורה אריתמית או מורביליפורמיים.
- שינויים היסטו-פתולוגיים הכוללים acantholysis (או היפרפלזיה של השכבה הספינוטית באפידרמיס, לרוב בתגובה לתהליך בדרמיס (זיהום פטרייתי, דלקת קשה, גידול).
- ראייה ישירה אימונו-פלואורסצנטית מביופסיה של הנגע המדגימה משקעים של IgG ושל משלים בחללים האפידרמליים הבינתאיים, לאורך ממברנת הבסיס האפידרמלית, או ריאקציה ברקמה הליכנואידית.
- ראייה אימונו-פלואורסצנטית בלתי-ישירה של משקעים על פני תאי ושט של פרימטים או על האפיתל של שלפוחית השתן של חולדות (Liu וח' ב-J Am Acad Dermatol משנת 1993).
- ראייה בשיטת ELISA של נוגדנים עצמיים בנסיוב כנגד desmoglein 1 ו-desmoglein 3, וכן כנראה כנגד האנטיגנים 180 ו-230 של bullus pemphigoid
שכיחות המחלה אינה ידועה אך היא פחות שכיחה מאשר pemphigus vulgaris. המאפיינים הקליניים של המחלה יכולים לדמות לריאקציה לתרופות מסוימות, ל-erythema multiformis, לתסמונת Stevens-Johnson, ל-lichen-planus, או לנקרוליזיס אפידרמלית טוקסית. ברוב המקרים PNP כרוכה עם לימפומה non-Hodgkin, עם לויקמיה לימפוציטית כרונית, עם thymoma, או עם מחלת Castelman. סיבוך חמור של PNP יכול לכלול bronchiolitis obliterans שעלול לגרום לכשל נשימתי.
PNP היא מחלה אוטו-אימונית נדירה שכמעט תמיד כרוכה עם ממאירות מוכחת סמויה. מטופלים עם PNP סובלים אופיינית עם מעורבות עורית ורירית, עם פרוגנוזה גרועה. עדיין אין פרוטוקולים לאבחון ולטיפול בנגע. פמפיגוס מהווה קבוצת מחלות אוטואימוניות הנגרמות מתגובת IgG בהן נוגדנים עצמיים מגיבים עם הדסמוזומים, שהם מבני הספיחה הבינתאית בין קרטינוציטים, מה שגורם לנגעי עור מכאיבים ושלפוחיות.
נמצאו שלוש צורות משמעותית של פמפיגוס:
- Pemphigus faliaceus
- pemphigus vulgaris (הסוג השכיח ביותר)
- paraneoplastic pemphigus (Kasperkiewicz וחב' ב-Nat Rev Dis Primers משנת 2017, ו-Vassileva וחב' ב-Clin Dermatol משנת 2017).
PNP מתאפיין על ידי שחיקה רירית מכאיבה וכתמים כהים על העור שבשלב מאוחר יותר משיר קשקשים. מגוון של נגעים שונים במורפולוגיה שלהם, הנעים בין שלפוחיות שטוחות לאזורים ליכנואידיים מפושטים (Seghalו-Srivastra ב-Int J Dermatology משנת 2009, ו-Kelly וחב' ב-J Dermatol משנת 2015). אובדן ניכר של האפידרמיס גורם ליובש ניכר, לחסר של חלבונים ולסכנה מוגברת של דלקות בעור. מטופלים עם PNP לעתים קרובות דורשים טיפול אינטנסיבי מקובל בסובלים מכוויות. מבוגרים בגיל 45 עד 70 שנה הם הסובלים העיקריים מ-PNP, אם כי גם ילדים עלולים לפתח PNP (Czernik וחב' ב-Int J Dermatology משנת 2011). PNP זוהה לראשונה על ידי Anhalt בשנת 1990 (Anhalt וחב' ב- N Eng J Med משנת 1990) והוגדר כ- “paraneoplastic ,autoimmune multiorgan syndrome” ובהמשך זכה לביטוי bronchiolitis obliterans (Nguyen וחב' ב-Arch Dermatol משנת 2001).
אטיולוגיה
ממאירויות לימפו-משגשגות משתתפות בהתפתחות של התחלואות השכיחות ביותר בהתפתחות של PNP והן מופיעות ב-84% מהמקרים (Kaplan וחב' ב-Oral Oncol משנת 2004). בערך 1/3 ממקרי PNP מקורם בלימפומה non-Hodgkin (38.6%) ובלויקמיה כרונית לימפוציטית (18.4%) (Kartan וחב' ב-Am J Clin Dermatol משנת 2017, ו-Pollman וחב' ב-Clin Rev Allergic Immunol משנת 2018), וכן במחלת Castelman עם 18.4%. עם זאת, גם גידולים נוספים כרוכים ב-PNP, כגון סרקומות, ובעיקר follicular dendritic cell sarcomas (Akel וחב' ב-Case Rep Oncol משנת 2018, ו-Su וחב' ב-Int J Clin Exp Patol משנת 2015), טימומות (Lim וחב' ב-Ann Dermatol משנת 2017), וכן squamous cell carcinomas של העור, הלשון והנרתיק, וקרצינומות של הריאות, הקיבה והמעי הגס (Wong ו-Ho ב-Australia J Dermatol משנת 2000, ו-Hayanga וחב' ב-J Burn Care Res משנת 2010). זוהתה רגישות מוגברת להתפתחות במטופלים עם PNP במטופלים עם HLA Class II Drb1*03 allele (Martel וחב' ב-J Autoimmun בשנת 2003), ועם אלל HLA-Cw*14 (Liu וחב' באותו כתב עת משנת 2008). אללים אלו שכיחים יותר באוכלוסיות לבנות וסיניות, בהתאמה. לשם שינוי HLA-DR4 ו-HLA-DR1-14 מגבירים את בסיכון ל- pemphigus vulgaris ול- pemphigus foliaceus אך לא הראו כל קשר להתפתחות PNP.
אפידמיולוגיה
השכיחות המדויקת של PNP אינה ידועה, והיא שכיחה הרבה פחות מאשר pemphigus vulgaris ומ-pemphigus foliaceus, כשהיא מהווה רק 1-3% מכל מקרי pemphigus. הנגע מופיע בגברים ובנשים באופן שווה. מחקר שכלל 496 מטופלים עם ממאירות פנימית, מצא ש-25 מתוכם פיתחו פמפיגוס (25%). הגיל הממוצע של המטופלים עם PNP, היה 64.7 שנים, והתפתחות נגע זה עלתה עם הגיל (Ogawa וחב' ב-J Dermatol Scipemphigus משנת 1995).
פתופיזיולוגיה: החלבונים דלהלן בנוסף לאחרים מהווים יעד לנוגדנים עצמיים ב- PNP (Paolino וחב' ב- Int J Mol Sci משנת 2017, ו-Tsuchisaka וחב' ב- J Invest Dermatol משנת 2016):
- Desmoglein type 1 ו-type 3
- desmosome חוץ-תאי
- desmoplakin-1 ו-2
- desmoplakin תוך תאי
- envoplakin תוך-תאי
- epiplakin תוך תאי
- periplakin תוך תאי
- α-2-macroglobulin-like-1 antigen (להלן (A2ML1 המעכב פרוטאזות (Numata וחב' ב-J Invesr Drmatol משנת 2013, ו- Schepens וחב' ב-PLoS One משנת 2010).
נוגדנים כנגד חלבוני plakin אופייניים ל-PNP ולא מצויים בצורות אחרות של pemphigus (Amber וחב' ב-Autoimmun Rev משנת 2018, ו-Chin Med J משנת 2009).
היסטופתולוגיה
מאפיינים היסטולוגיים של PNP כוללים acantholysis של האפידרמיס והתבקעותו, קרטינוציטים נקרוטיים, ווקואוליזציה של השכבה הבזלית, ואקסוציטוזיס של לימפוציטים (Horn ו-Anhalt ב-Arch Dermatol משנת 1992, Zhu ו-Zhang ב-J Dermatol משנת 2007, ו-Joly וחב' ב-J Am Acad Dermatol משנת 2000). דיס-קרטוזיס עם acantholysys סופרה-בזלי, היא תכונה אופיינית של PNP. עם זאת, המאפיינים ההיסטופתולוגיים של PNP ישתנו עם המורפולוגיה הספציפית של הנגעים שיכולים להיות לא דלקתיים אך להיות גם הסננות ליכנואידיות דלקתיות דחוסות. דרמטיטיס שהיא שניונית לריאקציה אוטו-אימונית של תאי T והסננה לתוך האפידרמיס מצביעה על ציטוטוקסיות על ידי תאים שהיא מרכיב ציטוטוקסי של PNP (Solimani וחב' ב-Front Immunol משנת 2019). PNP יכול לחקות תרחיש של erythema multiforme קלינית והיסטולוגית, בפרט אם הנגעים מאופיינים על ידי דרמטיטיס עם קרטינוציטים נקרוטיים. לפיכך, בדיקה אימונופלואורסצנטית ישירה חיונית לאבחון נכון של PNP. בדומה, acantholysis סופרה-בזלית, ויצירת שלפוחיות שמוצאים ב-PNP, הם זהים למה שמוצאים ב-pemphigus vulgaris , אם כי מאפיינים אחרים של vulgaris חסרים ב-PNP. נגעים דמויי lichen planum ב- PNP מאופיינים על ידי הסננות של לימפו-היסטיוציטים בדרמיס הפפילארי, מלוות על ידי וקואולות.
פרוגנוזה
אפילו עם טיפול, תוצאי PNP אינם משופרים, עם שיעורי תמותה של עד 90% (Yong ב-Oral Oncol משנת 2004, ו-Nousari וחב' ב- N Eng J Med משנת 1999). הדבקות עור הנובעות מאיבוד רקמת עורית, תרפיה אימונו-סופרסיבית, והתקדמות הממאירות הנלווית, תוך התפתחות של bronchiolitis obliterans, הן סיבות שכיחות לתמותה. גידולים פחות אגרסיביים או כאלה הניתנים להסרה כרוכים בפרוגנוזה משופרת (Zhang וחב' ב- J Cancer Res Clin Oncolמשנת 2011). המציאות של נמק של קרטינוציטים ונגעים עוריים הדומים ל-erythema multiforme, בעיקר כאשר הם מלווים על ידי נגעים ריריים נמרצים בשלב המוקדם, הם גורמים הכרוכים בפרוגנוזה גרועה (Leger וחב' ב-Arch Dermatol משנת 2012). במחקר של 144 מטופלים עם PNP והיסטולוגיה של ממאירות, הנוכחות של נוגדנים עצמיים כנגד envoplakin ו-bronchiolitis obliterans כרוכים בסיכון מוגבר של תמותה. מצג קליני טוקסי דמוי נקרוליזיס אפידרמלי, או דמוי בועתיות פמפיגואידית כרוך בהישרדות נמוכה (Ouedraogo וחב' ב- J Am Acad Dermatolמשנת 2019). הריכוזים בנסיוב של נוגדנים עצמיים מסוג IgG כנגד Dsg 1 וכנגד Dsg3 יכולים להיות מקבילים לתסמינים הקליניים, ולכן Dsg-ELISA יכולה לשמש סמן סרולוגי של פעילות המחלה בפמפיגוס.
המנגנון המוביל לתסמינים מרכזיים
בערך שליש ממקרי המוות הנגרמים מ-PNP הם בגלל אי-ספיקה פולמונרית המתרחשת כתוצאה מפעולת PNP על רירית הריאות. היא באה לביטוי כקוצר נשימה המתקדם ל-bronchiolitis obliterans שהיא פגיעה חסימתית בלתי הפיכה של הריאות. PNP נגרמת על ידי גידול, ואינה מדבקת. למרות ש-PNP נמצאה בבני גילים שונים, היא פוגעת יותר בבני גיל הביניים ומעלה (Frew ו-Morrell ב- ב-Dermatol Clin משנת 2011).
הגידול הסמוי גורם להופעת נוגדנים בצירקולציה וכאלה הקשורים לרקמה, באופן שהם מגיבים כנגד אנטיגנים ממשפחת ה-plakins, המעורבים במבנים של ספיחה בין-תאית השומרת את רקמת העור בגוף כולו. דרך immunoprecipitation התגלו אנטיגני-יעד הכוללים desmoglein-3, desmoglein-1, envoplakin, periplakin, desmoplakin 1, desmoplakin 2 ו- bullous pemphigoid antigen I. המנגנון המדויק דרכו גידולים מסוגלים להשרות נוגדנים עצמיים כנגד חלבוני plakin אינו ידוע (Poot וחב' ב-Br J Dermatol משנת 2013, ו-Proby וחב' ב-J Invest Dermatol משנת 1999).
האבחון
במטרה לאבחן PNP מספר בדיקות חייבות להתבצע. בתחילה, דגימות המתקבלות מביופסיה של העור עוברות מיקרוסקופיה ו- immunofluorescence ישיר (להלן DIF). דגימות הביופסיעה צריכות להילקח מאזורי עור הסמוכים לנגע (Camisa ב-Arch Dermatol משנת 1993).
בדיקות מרכזיות: ברור נוכחות של גידול תת-עורי, התפרצות רירית-עורית פולימורפית, מציאות נוגדנים בנסיוב עם מתווה ספציפי של immunoprecipitation.
בדיקות מינוריות: ראיות היסטולוגיות של acantholysis (אובדן של קישורים בינתאיים הגורם לשבירת העור ולנגע); DIF המראה צביעה תוך תאית וצביעת הממברנה הבסיסית; צביעת DIF עם האפיתל של שלפוחית השתן של חולדה.
מיקרוסקופיה: בתהליך זה עם דגימה שהושגה בביופסיה משתמשים לגלות נוכחות של ביקוע בתוך הדרמיס, epidermal acantholysis, וכן exocytosis אפידרמלי (פליטה תאית שהיא תהליך של הפרשת חומר אל מחוץ לתא על ידי הכוונת שלפוחית אל קרום התא). תוצאות חיוביות של בדיקות אלו מצביעות על סבירות גבוהה של PNP.
בדיקת DIF: הנוכחות של IgG, IgM ו-IgA באפידרמיס נורמלית, אך כאשר נוגדנים אלה מופיעים במיקומים אחרים כגון נוכחות תוך-תאית, או באזורים תת-אפידרמיים, וכן לאורך הצמתות הדרמו-אפידרמיות (אזורים המחברים את האידרמיס והדרמיס), מרמזים על PNP.
בדיקת Indirect immunofluorescence (IIF): מטופלים עם רמה נמוכה של נוגדנים המופיעים כתוך-תאיים.
מחקר עדכני
הפיתוח של ELISA לאבחון ספציפי של PNP הושלם בשנת 2009. המחקר התמקד בקביעה ספציפית של נוגדנים עצמיים הקשורים להופעת PNP. ספציפית, נוגדנים כנגד envoplakin ו-periplakin נחקרו, והוכח שנוגדנים כנגד שני חלבונים אלה משחקים תפקיד ב- PNP (Probst Kasperkiewicz ב-Clin Chim Acta משנת 2009, ו-Huang וחב' ב-Arch Dermatol Res מאותה שנה). מחקר נוסף משנת 2013 קבע שנוגדנים כנגד plakins ו-desmogleins, כמו גם כנגד α2-macroglobulin-like-1 (להלן A2ML1) כרוכים בממאירות הסמויה. מחקר משנת 2010 עסק בהרחקה הכירורגית של הגידול על מנת לטפל ב-PNP. בעוד ש-7 מתוך 2 המנותחים נפטרו בגלל אי היכולת של הגוף להתמודד עם הניתוח, 15 המנותחים האחרים שרדו (Zhang וחב' ב-. J Cancer Res Clin Oncol משנת 2011).
בשנת 2011, מחקר באישה עם כיבים מאחורי הרגליים, אבחן אותה כחולת PNP. נמצאה אצלה באופן אקסקלוסיבי מעורבות של תאי B. עם זאת, תאי T ותאי NK CD56+, גם כן נכרכו עם PNP. מקרה זה הצביע על הקשר הנדיר בין תאי NK lymphoma לבין PNP, מה שמציע שתאי NK יכולים להיות קשורים לפתוגנזה של PNP ומוסיף נדבך לתהליך הפתוגני הבלתי מובן לחלוטין של PNP (Gil וחב' ב-Br J Hematol משנת 2011). באוניברסיטת טורונטו מנסים לפתח טיפול לשיפור איכות החיים בחולי PNP, והם מאמינים שניתן להשיג זאת דרך מתן מינון קבוע של rituximab, אם כי תהליך מתן התכשיר אינו מוגדר סופית. תוצאות טיפול זה הדגימו דרגות שונות של רמיסיה (Heelan וחב' ב-JAMA Dermatol משנת 2014).
סיבוכים
מעורבות עיינית ב-PNP שכיחה וחייבת להיות מנוטרת בזהיות על ידי אופטלמולוג על מנת למנוע איבוד מתקדם של הראייה עד כדי עיוורון. תרפיה עיינית יכולה לכלול שימוש בטיפות קורטיקוסטרואידים, תמיסת דמעות מלאכותיות, ו-10% N-acetylcysteine, אך לעתים יש אפילו להזדקק למעורבות ניתוחית במקרים של הצטלקות ניכרת (Broussard וחב' ב-Clin Dermatol משנת 2016). Bronchiolitis obliterans, המופיע כשיעול יבש, קוצר נשימה והיפוקסמיה, פוגע ב-30-90 אחוזים ממטופלי PNP (Nicolskaia וחב' ב-Br J Dermatol משנת 2003). כשל נשימתי בגין התפתחות של bronchiolitis obliterans היה מזוהה כסיבה השכיחה ביותר למוות במקר של חולי PNP עם מחלת Castleman. ביופסיה של הריאות עשויה לגלות bronchiole fibrosis, הסננה חמורה של תאים ברונכיהיסטוציטים, ומשקעים של נוגדנים עצמיים באפיתל הברונכיאלי. להסרת גידולים, אינפוזיה תוך ורידית של מינון גבוה של אימונוגלובולינים לפני ואחרי הניתוח עשויה להפחית את הסיכון של bronchiolitis obliterans על ידי חסימת השחרור של נוגדנים עצמיים מהגידול לצירקולציה. תוצאות מחקר שנערך ביפן בחולי PNP, מציעות ש- bronchiolitis obliterans כרוך בנוגדנים עצמיים ל-epiplakin, שכן חולי PNP שליליים ל-epiplakin לא מפתחים bronchiolitis obliterans.
שחיקה אפידרמלית וקרע בשלפוחיות עלול לגרום איבוד ניכר של נוזלים, חלבונים ואלקטרוליטים ולהביא ליצירת דה-הידרציה וחוסר איזון של אלקטרוליטים. איבוד של מחסום עורי עלול לגרום לזיהומים ולספסיס. נגעים ריריים עמידים לרוב לטיפול אינטנסיבי. הזנה חסרה שניונית לשחיקה מכאיבה בחלל הפה והגרון עלולה להופיע, מה שמחייב הזנה דרך צינורית נזו-גסטרית במטופלים אחדים.
הוראות לביצוע הבדיקה
את הדם יש לקחת במבחנה כימית (פקק אדום או צהוב), ולאחר הסרכוז יש להכניס את הנסיוב לקירור. יש לפסול דגימות מאוד המוליטיות, ליפמיות או איקטריות, או דגימות פלזמה. הדגימות יציבות למשך שבוע בטמפרטורת החדר, למשך 14 או בקירור ועד 30 יום בהקפאה. שיטת המדידה היא על ידי בדיקה חצי-כמותית של indirect Immunofluorescence (או IIF). כיוון שהבדיקה אינה רגישה ביותר, תשובה שלילית אינה שוללת אפשרות של PNP.
ראו גם
המידע שבדף זה נכתב על ידי פרופ' בן-עמי סלע, המכון לכימיה פתולוגית, מרכז רפואי שיבא, תל-שומר;
החוג לגנטיקה מולקולארית וביוכימיה, פקולטה לרפואה, אוניברסיטת תל-אביב (יוצר הערך)


 כניסה
כניסה  עקבו אחרינו בפייסבוק
עקבו אחרינו בפייסבוק