דלקת חוליות מקשחת - סיבוכים קרדיווסקולרים - Ankylosing spondylitis - cardiovascular complications
ערך זה נמצא בבדיקה ועריכה על ידי מערכת ויקירפואה, וייתכן כי הוא לא ערוך ומוגה.
| דלקת חוליות מקשחת - סיבוכים קרדיווסקולרים | ||
|---|---|---|
| Ankylosing spondylitis - cardiovascular complications | ||
| יוצר הערך | ד"ר אלכסנדרה בלביר-גורמן
|
|
לערכים נוספים הקשורים לנושא זה, ראו את דף הפירושים – דלקת חוליות מקשחת
דלקת חוליות מקשחת (דח"מ) היא מחלה דלקתית כרונית שמערבת מפרקים ורקמות רכות של שלד ואגן ולעתים גם מפרקים גדולים. עם זאת, לדלקת חוליות מקשחת יש ביטויים מחוץ לפגיעה במפרקים ובשלד. תסמיני לב כלי דם הם ביטויים מערכתיים ידועים במחלת דלקת החוליות המקשחת. הפגיעה במערכת הלב וכלי הדם יכולה להיות כפולה: פגיעה ישירה במסתמי הלב, אבי העורקים ומערכת ההולכה על ידי התהליך הדלקתי, או לחילופין אירועי לב וכלי דם בשל טרשת עורקים מוקדמת בעקבות תהליך דלקתי מתמשך. הפגיעה במסתמי הלב, אבי העורקים ומערכת ההולכה נמצאת בהקשר לאנגד (Antigen) הייחודי למחלת דלקת חוליות מקשחת- HLA B27. למרות ההתקדמות בטיפול בדלקת חוליות מקשחת מבחינת מערכת המפרקים והשלד על ידי שימוש בתרופות לא סטרואידליות או תרופות ביולוגיות מסוג נוגדי α-TNF, השפעתן על הפרעות לב וכלי דם טרם הובהרה.
מבוא
מחלת דח"מ היא מחלה כרונית דלקתית המתאפיינת בעיקר במעורבות מפרקים ורקמות חיבור של השלד והאגן (Sacroileitis ,Spondylitis). בחלק מהחולים קיימת גם מעורבות של מספר מפרקים, לרוב המפרקים הגדולים הקרובים לשלד, כגון כתפיים וירכיים. המעורבות של המפרקים הרחוקים מהשלד (ברכיים, מרפקים, שורשי ידיים, קרסוליים) פחות שכיחה במחלה זו. אופיינית לדח"מ גם דלקת שמערבת אזורי חיבור גידים או רצועות לעצם - Enthesitis. למחלה מגוון ביטויים חוץ-מפרקיים, כמו דלקת של העיניים או תפרחות בעור. דלקת בקרום הריאות תוארה בדח"מ, אך זה ביטוי נדיר. הפגיעה במערכת הקרדיו-וסקולרית מזוהה עם המחלה הזו ומופיעה ב-0.5% עד 3% מהחולים עם דח"מ. רוב החולים עם דח"מ (מעל 90%) נושאים אנטיגן גנטי ייחודי -27HLA B. בסקירה זו נדון בתסמינים קרדיו-וסקולריים הקשורים למחלת דח"מ, כמו כן נדון בקשר בין הגורם הגנטי 27HLA B לבעיות הלב, והקשר בין מחלת דח"מ לטרשת העורקים.
תסמינים קרדיו-וסקולריים ייחודיים למחלת דח"מ
הסיבוכים הקרדיו-וסקולריים האופייניים למחלת דח"מ קשורים בעיקר לפגיעה במסתם האאורטלי, שורש וקשת האאורטה, ומערכת ההולכה. בחלק מהחולים הפגיעה היא בודדת, למשל אי ספיקה של המסתם האאורטלי. הקרבה האנטומית בין מוצא האאורטה למסתם האאורטלי היא בסיס לפגיעה משולבת של האאורטה, המסתם האאורטלי ומערכת ההולכה. פגיעה לבבית יכולה להיות סמויה שנים רבות. שימוש בבדיקות אקו-קרדיוגרפיות (אקו לב) מאפשר לאבחן שינויים במסתם האאורטלי וקשת האאורטה גם בחולים א-סימפטומטים.
סוקניק וחב' מצאו בבדיקת אקו לב רגילה אי ספיקה של המסתם האאורטלי ב-5 מתוך 40 (12.5%) חולים עם דח"מ. באקו לב דרך הוושט נמצאה פגיעה במסתם האאורטלי ב-27.5% מתוך 44 חולי דח"מ (2). יש לציין, שבשליש מהחולים נמצאה גם התעבות משמעותית של עלי המסתם המיטרלי. עשרים וחמישה חולים היו במעקב של אקו לב דרך הוושט במשך שנתיים לפחות. במשך המעקב חלו שינויים במצב החולים: ב-24% מהם הופיעו שינויים חדשים בשורש האאורטה, ב-12% חלה החמרה באי ספיקה של המסתם האאורטלי, אך עם זאת ב-20% השינויים במסתם האאורטלי נסוגו. בתקופת המעקב, 20% מהחולים פיתחו אי ספיקת לב, אירוע מוח או מוות או נזקקו להחלפת המסתם, בהשוואה ל-3% בקבוצת הביקורת. בסקירה על 210 חולי דח"מ פיתחו 21 סיבוכים קרדיו-וסקולריים: אי ספיקה של המסתם האאורטלי (חמישה חולים), דלקת קרום הלב (חולה אחד). אחד החולים פיתח דלקת של כלי הדם הגדולים - Takayasu's Arteritis(3). השכיחות של הבעיות הקרדיו-וסקולריות עלתה ככל שמשך מחלה היה ארוך יותר.
אקו לב רגיל או דרך הוושט הוא כלי רגיש ואמין לזיהוי בעיות מסתמים בקרב חולי דח"מ, והוא מאפשר להעריך הרחבה של האאורטה, שינוי בעובי של דופנותיה, עיבוי של השורש וכדומה. כדאי לציין, שקשר בין דח"מ לפגיעה במסתם האאורטלי מוכר זה שנים רבות.
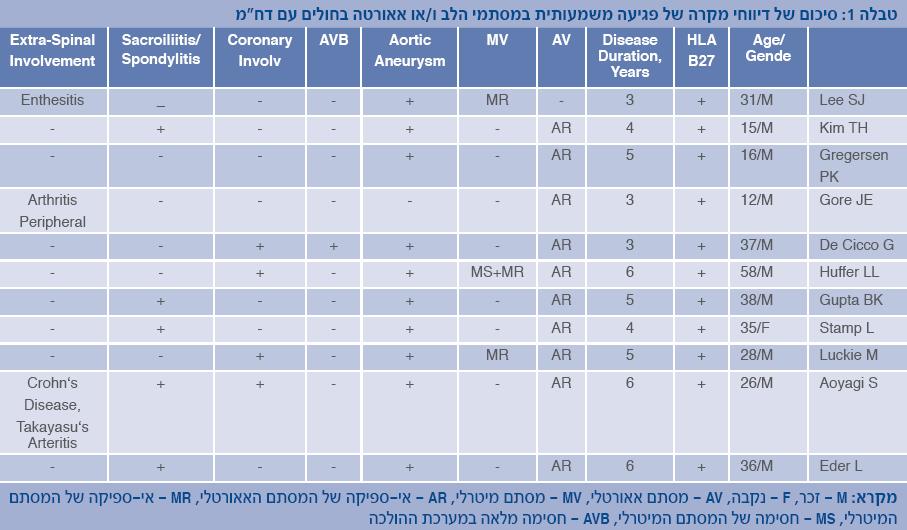
בעבודות המבוססות על תוצאות של אקו לב מסתמן שבחלק מחולי דח"מ לא נדיר למצוא פגיעה במסתם המיטרלי. דווח על פגיעה משמעותית במסתם המיטרלי (ב-7% מהחולים): אי ספיקה של המסתם, התעבות של עלי המסתם, ואפילו היצרות של המסתם (4,2). בחלק מהחולים הפגיעה במסתמים מלווה גם בפגיעה באאורטה עצמה: הרחבה ולעתים התפתחות של מפרצת. נמצאו בספרות דיווחים על 11 חולים (טבלה 1) שפיתחו פגיעה קשה במסתמים (Valvulitis) ו\או באאורטה (Aortitis) שהייתה קשורה באופן ישיר לדח"מ. במחצית מהמקרים האלו Valvulitis ו-Aortitis הקדימו את ההופעה של Sacroileitis או Spondylitis. בחלק מהחולים הביטויים במערכת המפרקים והשלד היו בעיקר דלקת מפרקים היקפית או Enthesitis. רוב החולים שבהם דווח על מהלך אגרסיבי של דלקת במסתמים ו'או אאורטה היו גברים (10 מתוך 11) צעירים (הגיל הממוצע היה 30.2 שנים), עם משך מחלה קצר (בממוצע 4.5 שנים), ב-90% מהם הייתה פגיעה במסתם האאורטלי, ב-27% הייתה פגיעה במסתם המיטרלי. מעורבות של אאורטה (90%) ועורקים כליליים (37%) הייתה שכיחה. חסימה במערכת ההולכה נמצאה רק אצל חולה אחד. כולם ללא יוצא מהכלל היו נשאים של אנטיגן 27HLA B.
הופרץ וחב' (5) בדקו את שכיחות מעורבות הלב בקרב 40 חולים צעירים עם דלקת מפרקים היקפיים JCA(Juvenile Chronic Arthritis) הנושאים אנטיגן 27HLA B, ומצאו סימני דלקת במסתם האאורטלי ב-4 מהם (10%). באף חולה עם JCA ללא אנטיגן 27HLA B (קבוצת ביקורת שכללה 40 חולים) לא נמצאו סימני מעורבות הלב (5). הקשר בין אנטיגן 27HLA B לפגיעה במסתמים או באאורטה נבדק בקרב 20 חולים שאצלם הופיע דח"מ בגיל צעיר (פחות מגיל 20 שנים, Juvenile Ankylosing Sponsylitis). יותר מ-90% מהם נשאו אנטיגן 27HLA B לעומת 51% בקרב חולים מבוגרים. בשליש מהם הייתה מעורבות של המסתם האאורטלי ו'או האאורטה. רבע מחולים אלו פיתחו פגיעה במסתם המיטרלי. הפגיעה במסתם האאורטלי ובאאורטה הייתה שכיחה יותר (58%) דווקא בחולים שאצלם הופיע דח"מ בגיל מבוגר מ-20 שנה (6).
קווסוג'י (7) בדק את הסיבות לאי ספיקה קשה של המסתם האאורטלי בקרב 887 חולים שעברו החלפת מסתם אאורטלי בבית חולים בהנובר בשנים 1981-1976, ביניהם נמצאו 3 חולים עם דח"מ; אצל אחד החולים הייתה גם מפרצת של האאורטה שדרשה השתלת תותב אאורטלי. ביופסיה מרקמת המסתם והאאורטה הראתה סימנים ברורים של דלקת ופיברוזיס.
יואן (8) סיכם ניסיון של החלפת המסתם האאורטלי עם ובלי הכנסת תותב לאאורטה ב-3 חולים עם דח"מ בתל השומר. כל 3 החולים נשאו אנטיגן 27HLA B. הניתוחים עברו בהצלחה. העובדות בספרות מצביעות על מהלך פתוגנטי זהה בין פגיעה במסתמים ופגיעה באאורטה, וייתכן שמהלך דלקתי באאורטה גם הוא קשור לנוכחות אנטיגן 27HLA B. בקרב חולי דח"מ הפגיעה באאורטה יכולה להיות גם מסוג אחר, סוג שאיננו קשור לאנטיגן 27HLA B.
תוארו מקרים של Aortitis על רקע דלקת כלי הדם (Vasculitis) בחולים עם דח"מ שהיו ביטוי למחלה נוספת – Takayasu's Arteritis. עד כה תוארו 4 מקרים של Takayasu's Arteritis בחולי דח"מ (11-9,2).
האבחנה של דלקת באאורטה ובעורקים הגדולים, בעיקר בשלב פעילות הדלקת, תמיד הייתה אתגרית. כיום בדיקות PET FDG או תהודה מגנטית עם הזרקת גדוליניום (MRA) יכולים לתת פתרון לגילוי מוקדם של הדלקת באבי העורקים וענפיו. לגילוי מוקדם של דלקת בעורקים משמעות קלינית חיונית בשל השלכות קשות אפשריות, כגון הופעת היצרויות, מפרצות, קרישים, פגיעה באספקת דם לאיברים חיוניים או לגפיים (11,10).
באופן טבעי, התהליך הדלקתי במסתמי הלב ובשורש האאורטה מסתיים ביצירת רקמה צלקתית. בדומה לפגיעה במסתמים ובאאורטה, דלקת ופיברוזיס הם גם האחראים לפגיעה במערכת ההולכה בחולים עם דח"מ.
ניטר-האוגה וחב' (12) פרסמו עבודה על הפרעות קצב והולכה בקרב 30 חולים עם דח"מ. הם מצאו הפרעות הולכה ב-14 חולים (48%), ב-5 מהם היו הפרעות קשות שדרשו הכנסת קוצב לב זמני (אצל שני חולים - במהלך ניתוח להחלפת המסתם האאורטלי) או קוצב קבוע (4 חולים). אצל חולה אחד נרשם פרפור פרוזדורים. כל החולים עברו בדיקה אלקטרו-פיזיולוגית. הפגיעה שהתגלתה בכל החולים הייתה במבנים מעל המערכת על-שם היס.
תומסן וחב' (13) בדקו תוצאות של מעקב בעזרת אק"ג במשך 24 שעות (Holter) אצל 54 חולים עם דח"מ. 48 מהם נשאו אנטיגן 27HLA B, ומצאו הפרעות הולכה בדרגות שונות אצל 12 (22%) מהם. הפרעות הולכה נמצאו רק בחולים הנושאים אנטיגן 27HLA B.
ברגפלד (14) בדק את הקשר בין הופעת חסימה מלאה במערכת ההולכה, הצורך בהכנסת קוצב לב קבוע, מחלת דח"מ ואנטיגן 27HLA B. מבין 223 חולים שהגיעו לבית חולים בשל חסימה מלאה במערכת ההולכה ונזקקו להכנסת קוצב לב קבוע, 28 חולים ענו על הקריטריונים של מחלת מפרקים כל שהיא, אצל 15 חולים נמצאו סימנים מובהקים של דח"מ. רק מחצית החולים אובחנו עם מחלה ראומטית לפני שהגיעו להשתלת קוצב לב. מתוך 28 חולים, 26 עברו בדיקה לאנטיגן 27HLA B והוא נמצא אצל 22 חולים (85% מכלל אלה שנזקקו להכנסת קוצב לב).
בעבודה אחרת, בבדיקה של 74 חולים שעברו השתלת קוצב לב קבוע ונשאו אנטיגן 27 HLA B, אצל 82% מהם נמצאו סימנים של מחלת מפרקים או שלד, ואילו בשאר החולים (18%) הפרעה במערכת ההולכה בדרגת חומרה גבוהה הייתה הביטוי הראשון והיחיד של מחלה הקשורה בנשאות אנטיגן 27HLA B(14). אותו חוקר מצא ששכיחות השתלות קוצב לב באוכלוסייה רגילה היא 8%-6%, ואילו בחולים עם 27HLA B היא מגיעה ל-20%-15%. אצל חולים הנושאים אנטיגן 27HLA B שנזקקו להשתלת קוצב לב קבוע, נמצאה שכיחות גבוהה מאוד (88%-67%) של פגיעה נלווית במסתם האאורטלי. בבדיקות פתולוגיות נמצאו סימני פרוליפרציה של אינטימה בכלי הדם ופיברוזיס שהיו זהים באאורטה ובמסתמים. פגיעה במערכת ההולכה ובמסתמים בחולים אלו הייתה מלווה גם בשכיחות גבוהה של ביטויים נוספים מחוץ למפרקי השלד, כגון נגעים בעור או דלקת עיניים או דלקת במפרקים ההיקפיים (14).
דלקת קרום הלב תוארה בקרב חולי דח"מ, אך תופעה זו היא נדירה מאוד (2).
הטיפול השגרתי בחולים עם דח"מ הוא בתרופות לא סטרואידליות (NSAIDs) או בתרופות שמעכבות Cycloxygenase 2 (2COX). חולים שלא מגיבים לטיפול בתרופות מסוג NSAIDs או 2COX מטופלים בתרופות מסוג נוגדי TNF-α (Tumor Necrosis Factor-α). אין נתונים בספרות על השפעת טיפול נוגד דלקת על ביטויים קרדיו-וסקולריים. בתיאור מקרה של Valvulitis המערבת את המסתם האאורטלי אצל חולה עם דלקת מפרקים היקפיים שנשא אנטיגן 27HLA B, מתן טיפול בסטרואידים, NSAIDs, ו-Salasopyrin הביא לבקרה של מחלת המפרקים וגם לבקרה ולהתייצבות של מצב המסתם במשך שנתיים של מעקב(15).
תחלואה קרדיו-וסקולרית כללית (טרשת העורקים והשלכותיה) בדח"מ
בעשור האחרון נמשכה תשומת לבם של החוקרים לעלייה בתחלואה ותמותה מאירועים קרדיו-וסקולריים בקרב חולים עם מחלות ראומטיות. שימוש מוצלח בטיפולים המעכבים תהליכי דלקת (סטרואידים, תרופות מדרג שני - DMARDs, תרופות ביולוגיות) בחולים עם מחלות ראומטיות דלקתיות, כמו דלקת מפרקים ראומטואידית (Rheumatoid Arthritis) RA או זאבת SLE (Systemic Lupus Erythematosus) הביאו להארכת החיים של החולים. עם הזמן התרבו דיווחים על שכיחות גבוהה של אירועים קרדיו-וסקולריים (אוטם שריר הלב או אירוע מוח) בקרב חולים עם RA או SLE על רקע טרשת עורקים מוקדמת. נמצא שהסיכוי לחלות באירוע קרדיו-וסקולרי עולה פי 3 בקרב חולי RA ועד פי 6 בקרב חולי SLE בהשוואה לאנשים בריאים בגיל ומין זהה. סיכוי לחלות באירוע קרדיו-וסקולרי אצל חולים הלוקים בדח"מ גם הוא גבוה פי 1.6 בהשוואה לאוכלוסייה בריאה באותו גיל ומין. ההערכה של טרשת העורקים מתבססת כיום על מספר מדדים אפידמיולוגיים א. גורמי סיכון לחלות במחלה קרדיו-וסקולרית - השמנה, עודף שומנים בדם, הפרעה באיזון שומנים בדם, יתר לחץ דם, סוכרת, עודף חומצת שתן בדם ועוד. בחלק מהחולים קיים שילוב של גורמי סיכון שונים והמצב הזה מוגדר כ"תסמונת מטבולית". ב. שכיחות אירועים קרדיו-וסקולריים בקרב חולים. ג. מקרי מוות בעקבות אירועים קרדיו-וסקולריים בקרב חולים. ניתן לבצע הערכה כמותית של מצב העורקים מבחינת הטרשת גם בשיטות שונות א. בדיקה על-קולית של עורקי התרדמה. בבדיקה זו ניתן למצוא רבדים טרשתיים או לחלופין למדוד את עובי השכבה הפנימית של עורק התרדמה IMT (Intimal Media Thickness). ב. בדיקת טומוגרפיה ממוחשבת של העורקים הכלילייםElectron Beam Computed) Tomography), שבודקת באופן כמותי הסתיידויות של העורקים הכליליים CCA (Coronary Artery Calcification). גורמי סיכון מקובלים הם סימן פרוגנוסטי חיוני בקרב חולים עם מחלות מזוהות עם טרשת כלי הדם, כמו אירוע מוחי או אירוע לב. גם במחלות מפרקים דלקתיות כמו RA או SLE לגורמי סיכון סטנדרטיים השפעה רבה. עם זאת, מחלה דלקתית כשלעצמה מקדמת תהליך טרשתי בעורקים. גורמי סיכון שונים נבדקו בקרב חולי דח"מ. בחלק מהפרסומים נמצאה עלייה בגורמי סיכון לתחלואה קרדיו-וסקולרית כמו יתר לחץ דם, עודף שומנים בדם, ירידה בפעילות גופנית, סימני תסמונת מטבולית, ירידה ברמת HDL. הפרעות אלו בחולי דח"מ תאמו רמות גבוהות של מדדי דלקת CRP (C-Reactive Protein) ושקיעת דם (ESR) ומדדי פעילות וחומרת המחלה (מדד BASDAI) (18-16). בדיקות IMT ו-CCA נמצאו רגישות ואמינות בקרב חולים עם מחלות מפרקים דלקתיות, כמו RA או SLE. תוצאות של בדיקות IMT ו-CCA נמצאו בהתאמה עם חומרת המחלה הדלקתית, רמות מדדי דלקת (ESR או (CRP, רמות גבוהות של ציטוקינים מקדמים דלקת, כמו α-TNF ו-6Interleukin . אצל חולים עם דח"מ נמצאה עלייה משמעותית במדדים של IMS, אך ההפרעה הזו תאמה בעיקר גורמי סיכון שגרתיים, כמו יתר לחץ דם, השמנה ועודף שומנים בדם (20,19). ממצא זה לא תאם רמות מדדי דלקת ESR או CRP או מדד פעילות או חומרה של דח"מ. במחקר אחר כן נמצאה התאמה בין תוצאות מדידות IMS לחומרה של דח"מ מעבר להשפעה של גורמי סיכון שגרתיים בקרב 64 חולים (21). כפי שצוין קודם, רוב החולים עם דח"מ מטופלים במשך תקופות ארוכות בתרופות מסוג NSAIDs או 2COX שהן טיפול הבחירה. ידוע שתרופות מסוג זה מעלות את הסיכוי לאירוע לבבי או אירוע מוחי. פורסמה מטה-אנליזה של מחקרים קליניים מבוקרים בשלב IIb/III עם שימוש באחת התרופות מסוג 2-COX - Etoricoxib (Arcoxia) כנגד תרופת ביקורת (NSAIDs) או אינבו בקרב חולים עם דלקות מפרקים שונות (RA, SLE, דח"מ ואחרות) או כאבי גב כרוניים במשך 4 שבועות או יותר (6,500 מטופלים'שנים). סך הכל 69 מטופלים ב-Etoricoxib פיתחו 74 אירועים קרדיו-וסקולריים. שיעור זה היה גבוה באופן משמעותי מזה שבקבוצת אינבו, אך לא נמצאו הבדלים משמעותיים בין חולים מטופלים ב-NSAIDs שגרתיים לחולים המטופלים ב-Etoricoxib. גם במחקר על שימוש ב-Etoricoxib לטיפול בדח"מ לא נרשמה שכיחות גבוהה יותר של אירועים קרדיו-וסקולריים בהשוואה ל-Naproxen (22). תוצאות זהות פורסמו גם עם שימוש בקוקסיבים (חוסמי 2COX) אחרים. בעשור האחרון נמצא שתרופות מסוג נוגדי α-TNF מועילות מאוד לחולים עם מחלות מפרקים שונות, כולל דח"מ. כיום, חולים עם דח"מ שאינם מגיבים, או אלו שבשל תופעות לוואי לא מסוגלים לקבל טיפול ב- NSAIDs או חוסמי 2COX מטופלים בהצלחה רבה בתרופות נוגדות α-TNF. ספנקיס וחב' (23) פרסמו נתונים על ההשפעה החיובית של טיפול בנוגדי α-TNF על פרופיל השומנים, בעיקר על רמות של HDL ב-26 חולים עם דח"מ. ואן אייק וחב' (24) דיווחו על הטבה בכל מדדי הדלקת בחולים עם דח"מ שטופלו באחת מהתרופות נוגדות α-TNF - Etanercept (Enbrel). אצל חולים אלו במקביל לשיפור במחלה הדלקתית, נצפה שיפור במדדי הטרשת. עד כה לא פורסמו נתונים על ההשפעה של תרופות מסוג DMARDs ונוגדי α-TNF על תחלואה או על תמותה קרדיו-וסקולרית בקרב חולי דח"מ.
סיכום
- מעורבות קרדיו-וסקולרית שכיחה בקרב חולים עם דח"מ. הפגיעה במערכת הקרדיו-וסקולרית בדח"מ היא תוצאה ישירה של התהליך הדלקתי ברקמות חיבור של הלב ושל האאורטה. בשל הדלקת יכולים להיפגע המסתמים (בעיקר המסתם האאורטלי, אך גם המסתם המיטרלי), האאורטה וענפיה ומערכת ההולכה. לתהליך זה השלכות קשות, כגון: הרס של המסתמים (אי ספיקה של המסתם האאורטלי, אי ספיקה של המסתם המיטרלי), הופעת הרחבה או מפרצות של האאורטה, התפתחות ברדיקרדיה קיצונית בעקבות חסימה במערכת ההולכה. פגיעה בלב בעקבות דח"מ מוכרת בקרב מבוגרים, אך גם בקרב חולים צעירים. חולים עם מחלה ממושכת נוטים יותר לסיבוכים קרדיו-וסקולריים. במקרים מסוימים מעורבות קרדיו-וסקולרית יכולה להיות ביטוי ראשון של מחלה ולהקדים הופעה של Sacroileitis או Spondylitis. קיים קשר הדוק בין הופעות של פגיעה במסתמים, באאורטה ובמערכת ההולכה וממצא של אנטיגן רקמתי 27HLA B האופייני לדח"מ. בחולים צעירים עם סימני אי ספיקה של המסתם האאורטלי, סימני Aortitis או הפרעות הולכה, יש מקום לבדיקה של ראומטולוג ובדיקת סיווג רקמות לאנטיגן 27HLA B. במקרים של מעורבות האאורטה או ענפיה, בדיקות PET FDG או MRA עם גדוליניום יכולות לעזור לגילוי או שלילה של Vasculitis. ההשפעה של טיפול בנוגדי דלקת על מעורבות של מסתמים, אאורטה ומערכת ההולכה אינה ידועה.
- בחולים עם דח"מ, תחלואה ותמותה מאירועים קרדיו-ולסקולריים גבוהים מאלו שבקרב אנשים בריאים. לגורמי סיכון שגרתיים השפעה רבה על פרוגנוזה של דח"מ. טיפול בנוגדי α-TNF משפר את איזון השומנים בדם בקרב חולי דח"מ. תועלת של מדדי טרשת כמו IMS או CCA בקרב חולי דח"מ טרם הובהרה.
- תרופות מסוג NSAIDs וחוסמי 2COX יכולות להביא לעלייה בשיעור אירועים קרדיו-וסקולריים ודורשות מעקב קפדני אחרי חולים שזקוקים לטיפול זה. ההשפעה של תרופות נוגדות α-TNF על תחלואה ותמותה קרדיו-וסקולרית אצל חולי דח"מ לטווח ארוך אינה ידועה. יצירת רשימות סדירות (Registries) של חולים המטופלים בתרופות ביולוגיות מסוג נוגדי α-TNF תאפשר לענות על שאלות שטרם הובהרו.
ביבליוגרפיה
- Sukenik S, Pras A, Buskila D, et al. Cardiovascular manifestations of ankylosing spondylitis. Clin Rheumatol 1987;6(4):588-592
- Roldan CA, Chavez J, Wiest PW, et al. Aortic root disease and valve disease associated with ankylosing spondylitis. J Am Coll Cardiol 1998;32(5):1397-1404
- Ben Taarit Ch, Kaffel D, Ben Maiz H, et al. Cardiovascular manifestations in ankylosing spondylitis. Concerning 210 cases Tunis Med 2008;86(6):546-549
- Yildirir A, Aksoyek S, Calguneri M, et al. Echocardiographic evidence of cardiac involvement in ankylosing spondylitis. Clin Rheumatol 2002;21(2):129-134
- Huppertz H, Voigt I, Müller-Scholden J, et al. Cardiac manifestations in patients with HLA B27-associated juvenile arthritis. Pediatr Cardiol 2000;21(2):141-147
- Jiménez-Balderas FJ, García-Rubi D, Pérez-Hinojosa S, et al. Two-dimensional echo Doppler findings in juvenile and adult onset ankylosing spondylitis with long-term disease. Angiology 2001;52(8):543-548
- Kawasuji M, Hetzer R, Oelert H, et al. Aortic valve replacement and ascending aorta replacement in ankylosing spondylitis: report of three surgical cases and review of the literature. Thorac Cardiovasc Surg 1982;30(5):310-348
- Yuan SM. Cardiovascular involvement of ankylosing spondylitis: report of three cases. Vascular 2009;17(6):342-354
- Aoyagi S, Akashi H, Kawara T, et al. Aortic root replacement for Takayasu arteritis associated with ulcerative colitis and ankylosing spondylitis-report of a case. Jpn Circ J 1998;62(1):64-68
- Soomro H, Armstrong M, Graham EM, et al. Sudden loss of vision caused by a vasculitic ophthalmic artery occlusion in a patient with ankylosing spondylitis and Crohn's disease. Br J Ophthalmol 2006;90(11):1438
- Hilàrio MO, Terreri MT, Prismich G, et al. Association of ankylosing spondylitis, Crohn's disease and Takayasu's arteritis in a child. Clin Exp Rheumatol 1998;16(1):92-94
- Nitter-Hauge S, Otterstad JE. Characteristics of atrioventricular conduction disturbances in ankylosing spondylitis (Mb Bechterew). Acta Med Scand 1981;210(3):197-200
- Thomsen NH, Hørslev-Petersen K, Beyer JM. Ambulatory 24-hour continuous electrocardiographic monitoring in 54 patients with ankylosing spondylitis. Eur Heart J 1986;7(3):240-246
- Bergfeldt L. HLA-B27-associated cardiac disease. Ann Intern Med 1997 15;127(8 Pt 1):621-629
- Lee SJ, Im HY, Schueller WC. HLA-B27 positive juvenile arthritis with cardiac involvement preceding sacroiliac joint changes. Heart 2001;86(6):19
- Peters MJ, van der Horst-Bruinsma IE, Dijkmans BA. Nurmohamed MT. Cardiovascular risk profile of patients with spondylarthropathies, particularly ankylosing spondylitis and psoriatic arthritis. Semin Arthritis Rheum 2004;34(3):585-592
- van Halm VP, van Denderen JC, Peters MJ, et al. Increased disease activity is associated with a deteriorated lipid profile in patients with ankylosing spondylitis. Ann Rheum Dis 2006;65(11):1473-1477
- Papadakis JA, Sidiropoulos PI, Karvounaris SA, et al. High prevalence of metabolic syndrome and cardiovascular risk factors in men with ankylosing spondylitis on anti-TNF-alpha treatment: correlation with disease activity. Clin Exp Rheumatol 2009;27(2):292-298
- Mathieu S, Joly H, Baron G, et al. Trend towards increased arterial stiffness or intima-media thickness in ankylosing spondylitis patients without clinically evident cardiovascular disease. Rheumatology (Oxford) 2008;47(8):1203-1207
- Peters MJ, van Eijk IC, Smulders YM, et al. Signs of accelerated preclinical atherosclerosis in patients with ankylosing spondylitis. J Rheumatol 2010;37(1):161-166
- Gonzalez-Juanatey C, Vazquez-Rodriguez TR, Miranda-Filloy JA, et al. The high prevalence of subclinical atherosclerosis in patients with ankylosing spondylitis without clinically evident cardiovascular disease. Medicine (Baltimore) 2009;88(6):358-365
- van der Heijde D, Baraf HS, Ramos-Remus C, et al. Evaluation of the efficacy of etoricoxib in ankylosing spondylitis: results of a fifty-two-week, randomized, controlled study. Arthritis Rheum 2005;52(4):1205-1215
- Spanakis E, Sidiropoulos P, Papadakis J, et al. Modest but sustained increase of serum high density lipoprotein cholesterol levels in patients with inflammatory arthritides treated with infliximab. J Rheumatol 2006;33(12):2440-2446
- van Eijk IC, de Vries MK, Levels JH, et al. Improvement of lipid profile is accompanied by atheroprotective alterations in high-density lipoprotein composition upon tumor necrosis factor blockade: a prospective cohort study in ankylosing spondylitis. Arthritis Rheum 2009;60(5):1324-1330
קישורים חיצוניים
- סיבוכים קרדיו-וסקולריים ב-Ankylosing Spondylitis, מדיקל מדיה
המידע שבדף זה נכתב על ידי ד"ר אלכסנדרה בלביר-גורמן, יחידה ראומטולוגית על שם ב' שיין, מרכז רפואי רמב"ם, הקריה הרפואית לבריאות האדם, חיפה


 כניסה
כניסה  עקבו אחרינו בפייסבוק
עקבו אחרינו בפייסבוק