הכללת טכנולוגיות רפואיות חדשות שאינן תרופות בסל הבריאות - סוגיות ואתגרים
| הכללת טכנולוגיות רפואיות חדשות שאינן תרופות בסל הבריאות - סוגיות ואתגרים. | ||
|---|---|---|
| יוצר הערך | ד"ר אתי סממה וד"ר עינב הורוביץ | |
לערכים נוספים הקשורים לנושא זה, ראו את דף הפירושים – סל תרופות 2016
לקראת תהליך הרחבת סל שירותי הבריאות לשנת 2012, הוצע לראשונה להכליל בסל התקן לתיקון מילעורי של דלף במסתם המיטרלי של הלב. האביזר המושתל באמצעות צנתור מצמיד את עלי המסתם בלב תוך כדי שהוא פועם מבלי להזדקק לפתיחת בית החזה ולהעברת החולה למכונת לב-ריאה. הפעולה נעשית תחת שיקוף והנחיה אקו-קרדיוגרפית. הטכנולוגיה נועדה לטפל באי ספיקה של המסתם המיטרלי בלב, מחלה המהווה את ההפרעה המסתמית הנפוצה ביותר בעולם המערבי. הטיפול הוצע עבור חולים הנמצאים בסיכון גבוה לניתוח לב פתוח. ועדת הסל דנה בטכנולוגיה ודירגה אותה בדירוג 8A, שמשמעו במקרה זה טכנולוגיה שאין לגביה די עדויות מדעיות (לחלופין, בהקשר אחר יינתן הדירוג לטכנולוגיות שיש להן תועלת מסוימת אך היא מועטה בלבד ביחס לחלופות או שעניינן תוספת איכות חיים שאינה משמעותית במיוחד). בשל הדירוג שאינו גבוה דיו, לא כללה הוועדה את הטכנולוגיה בהמלצותיה להכללת טכנולוגיות חדשות בסל באותה שנה. כך אירע גם בשנה שלאחר מכן בדיוני סל 2013. עיקר ההסתייגויות של חברי הוועדה בדיון היו ביחס להיקפה ואיכותה של הספרות המדעית והיעדר הלימה בין קבוצות הנחקרים המוצגות במאמרים לבין ההתוויות המבוקשות להכללת הטכנולוגיה בסל.
בשנת 2014 הוצעה ונדונה הטכנולוגיה פעם נוספת. באותה שנה דווח על ניסיון מצטבר בשימוש בטכנולוגיה בישראל ונוספו מספר מאמרים מחקריים חדשים. בנוסף ניתן אישור FDA (Food and Drug Administration) לשימוש בה. למרות שההסתייגויות של חברי הוועדה נותרו בעינן ואף הועלו היבטים נוספים לגבי סייגים שהכתיב ה-FDA בנוגע למיומנות המטפלים הנדרשת והשיפורים המצופים באביזר, תועדפה הטכנולוגיה בדירוג 8/9A, מעט גבוה בהשוואה לשנים הקודמות והוכללה בסופו של דבר בסל באותה שנה.
בשל מורכבות השימוש התקבלה המלצת המועצה הלאומית לטיפול במחלות לב וכלי דם להגבלת השימוש בטכנולוגיה למספר מרכזים רפואיים מובילים ולחייב את בתי החולים בקבלת אישור שנתי לביצוע הפעולה, אישור שיינתן רק לאחר הוכחת הצלחה ב-5 פעולות המבוצעות בהדרכת פרוקטור (מלווה מטעם החברה) מקצועי. כתולדה מכך החל תהליך מעקב ואיסוף נתונים בשלב Post marketing ולאחר הכללת השירות בסל.
תהליך הכללת טכנולוגיה זו בסל מדגים היטב את הסוגיות והאתגרים הכרוכים בהערכת טכנולוגיות שאינן תרופות והבאתן לדיון במסגרת ועדת הסל, תוך השוואתן לתרופות חדשות ולעדויות המדעיות אודותיהן.
מבוא
המשרד להערכת שירותי בריאות (OTA, Office of Technology Assessment) בארצות הברית טבע בשנת 1976 את הגדרת המושג "טכנולוגיה רפואית" הכוללת: תרופות, מכשירים, גישות אבחנתיות וטיפוליות - כלליות וכירורגיות, וכן מסגרות ארגוניות שבהן ניתן הטיפול[1]. באופן רחב יותר נכללים תחת הגדרה זו פרוצדורות אבחוניות וטיפוליות (לרבות בדיקות מעבדה), מכשירים רפואיים (Devices), אביזרים רפואיים (גם אלה המושתלים בתוך גוף החולה או המסייעים בביצוע פרוצדורות) וגם אביזרים ממוזערים (Nanotechnology) וציוד מתכלה. להגדרה נוספו במקור גם מסגרות ארגוניות (כולל שיטות התחשבנות) ומסגרות מבניות (יחידות מקצועיות) שבהן ניתן שירות רפואי. משנת 2000 יש הכוללים בהגדרת "טכנולוגיה רפואית" גם מערכות מידע ותקשורת לשימושו של החולה, לרבות תיק רפואי מקוון (EHR, Electronic Health Record), רובוטיקה בשימוש הרפואה וטלרפואה (Telemedicine).
בעוד שתרופות מהוות טכנולוגיה מוגדרת ואחידה מבחינת מאפיינים, טווח ומגוון הטכנולוגיות שאינן תרופות הוא נרחב מאוד עם שונות רבה בין סוגי הטכנולוגיות ומאפייניהם. הבדלים מהותיים בין מכשירים, מושתלים או חיצוניים, בדיקות, פרוצדורות ושירותים הופכים את תהליך ההערכה של טכנולוגיות שאינן תרופות למורכב יותר. שוני זה הביא לכך שבחלק מהמסגרות העוסקות בהערכת טכנולוגיות רפואיות (HTA, Health Technology Assessment) בעולם, ההערכה של טכנולוגיות שאינן תרופות נעשית בנפרד מתרופות, על ידי גוף ייעודי או אנשי מקצוע אחרים באותו גוף, כפי שהוא נעשה גם במשרד הבריאות[2],[3],[4]. חלק מהיבטים אלה יוצרים אתגר נוסף ושונה, לא רק לתהליך ההערכה אלא גם בעת גיבוש המלצות ועדת הסל בכל שנה לגבי הכללה של טכנולוגיות שאינן תרופות ואספקתן במימון ציבורי.
תהליך הרחבת הסל במסגרת ועדה ציבורית, כפי שהוא מתקיים משנת 1999, מתפתח ומתעצב לאורך השנים. האתגרים העומדים בפני חברי הוועדה, הצריכים לאזן בין שיקולים מקצועיים, חברתיים, אתיים וכלכליים, הם רבים. בתוכם משולב אתגר ההתמודדות עם טכנולוגיות רפואיות שאינן תרופות ומורכבות קבלת ההחלטות על אימוצן והטמעת השימוש בהן במערכת בריאות בכלל ובציבורית בפרט. למרות המורכבות בביצוע הערכות של טכנולוגיות רפואיות שאינן תרופות, הבעייתיות במחקרים בתחום והקושי בהערכת היקפי שימוש צפויים, מעניין היה לגלות כי בשנים האחרונות, היחס בין אחוז כלל הטכנולוגיות העולות לדיון בוועדת הסל (תרופות ושאינן תרופות) לבין אלו שמוכללות בו בסופו של דבר עומד על כ־20%, בדיוק אותו שיעור ממוצע כפי שנמצא לגבי טכנולוגיות שאינן תרופות. כך נמצא גם כי היקף התקציב המיועד להן עומד אף הוא על כחמישית מסך התקציב, למרות שבהיבט זה קיימת תנודתיות משמעותית בין השנים (לפחות בחמש השנים האחרונות.ייתכן כי בשנים שקדמו להן המגמות היו שונות).
הדבר מעיד כי ועדת הסל מצליחה להתגבר בדיוניה על המגבלות באיכות העדויות המדעיות ועל הקושי בהערכת היקפי שימוש צפויים ועלויות עתידיות של טכנולוגיות שאינן תרופות המיועדות להכללה בסל, ומודעת למגבלות כפי שעולה מתוך הפרוטוקולים. יחד עם זאת היא מתמודדת עם האתגר תוך שהיא מכירה בחשיבותן של הטכנולוגיות ומוצאת את הדרך להכליל בסל את הראויות והחיוניות מביניהן.
ניכר כי דווקא הראייה הכוללת של כלל הטכנולוגיות, תרופות ושאינן תרופות, ושל התקציב המיועד להכללת טכנולוגיות חדשות בסל בכל שנה מאפשרת לוועדת הסל, הכוללת נציגים מתחומי ידע ותפקידים מגוונים, ליצור תוצאה המשקללת את כלל הנתונים וההיבטים והשומרת על איזון ראוי בהכללה בסל של תרופות וטכנולוגיות אחרות. איזון זה בא לידי ביטוי במספר הטכנולוגיות החדשות המוכללות בסל בכל שנה, באחוז שלהן מתוך אלו שעולות לדיון ובנתח תקציב משמעותי מתוך התקציב המיועד להוספת טכנולוגיות רפואיות חדשות לסל.
אתגרים בהערכת טכנולוגיות רפואיות שאינן תרופות
הבדלים מתודולוגיים
ההבדלים בין טכנולוגיות שאינן תרופות לתרופות מתחיל כבר בשלב הרגולציה. ניתן למצוא הבדלים ופערים ברמת מחקרים כבר בשלב הרישום של מכשירים. נקודה ראשונה שעליה ניתן להצביע היא שקיימות טכנולוגיות, כגון פרוצדורות, שירותים ואף חלק מהמכשירים או האביזרים, שאינם עוברים תהליך של רגולציה כטכנולוגיה רפואית, וחלקם לא עובר רגולציה בכלל. גם בטכנולוגיות שכן עוברות מסלול של רגולציה כטכנולוגיה רפואית קיימים הבדלים בין דרישות הרגולציה של הרשויות העיקריות, בעיקר האירופאית (CE mark) ושל ארצות הברית (FDA), וזאת בניגוד לתרופות, עבורן המסלולים והדרישות דומים יחסית. ה-CE mark מהווה אישור רגולטורי על בסיס הוכחת יעילות טכנית ובטיחות, עם התייחסות פחותה לצורך בהוכחה לגבי תועלת קלינית. ה-FDA מתייחס בצורה שונה לטכנולוגיות המוגדרות טכנולוגיות ראשונות מסוגן, לעומת מכשירים שאותם הוא רואה כדומים באופן עקרוני למכשירים קיימים. במסלול הראשון (PMA, Pre-Market Approval), ה-FDA דורש עדויות קליניות לגבי היעילות והבטיחות אך הוא לא מגדיר דרישת מינימום למחקרים אלה. חלק לא מבוטל מהטכנולוגיות המאושרות במסלול של PMA מאושר על סמך מחקר בודד, ומרבית המחקרים הם ברמה מתודולוגית נמוכה יותר - מחקרים לא אקראיים או לא סמויים, לא משווים לחלופה טיפולית פעילה ומשתמשים בתוצאים משמעותיים פחות מבחינה רפואית (לדוגמה, תוצא של שיעור הצלחה טכנית בהשתלת המכשיר ולא שיפור במדד הקליני)[5]. מחקר אחד הראה שפחות מ-80% מטכנולוגיות Class III - טכנולוגיות בסיכון גבוה - עוברות במסלול של PMA. טכנולוגיות המוגדרות כדומות לטכנולוגיות קיימות נבחנות במסלול המכונה 510(k), בו הדרישות מבחינת הוכחות הן נמוכות אף יותר ולרוב אין צורך במחקר קליני להוכיח את היעילות או הבטיחות.
במחקר אחד רק 10-15 אחוזים מההגשות ל-510(k) כללו נתונים קליניים ומחקר אחר הראה שלמעלה ממחצית לא כללו מידע חיוני כגון תיאור הטכנולוגיה או ההתוויה המבוקשת[5]. נושא הדמיון בין טכנולוגיות עלול להיות בעייתי. על אף שלעתים ניתן להמשיל את זה לתרופות גנריות, מדובר במצב שונה לחלוטין. תרופה גנרית היא חומר זהה לחלוטין לחומר של התרופה המקורית אך טכנולוגיות המאושרות במסלול 510(k) אינן זהות, וההבדלים ביניהן יכולים להיות משמעותיים בהשפעתם.
ההבדלים בדרישות הרגולטוריות משפיעים גם על רמת העדויות הקיימות כאשר מבצעים הערכה של טכנולוגיות שאינן תרופות. בעוד שכאשר מדובר בתרופות באופן קלאסי (אם כי לא תמיד) יש לפחות מחקר אחר שנחשב Pivotal - מחקר שהוא לרוב אקראי מבוקר, בעל רמה מתודולוגית גבוהה שהיווה את מחקר ה-Phase III, בטכנולוגיות שאינן תרופות לא קיימים השלבים המוסדרים הללו, ועבור טכנולוגיות רבות קיימים בעיקר רק מחקרי עוקבה או מחקרים אקראיים מבוקרים בגודל קטן או בינוני. נושא הסמיות (Blind) במחקרים שבודקים טכנולוגיות שאינן תרופות הוא אתגר בפני עצמו. לדוגמה, כאשר מדובר בטיפול באמצעות מכשיר מושתל שמושווה לאי טיפול או טיפול שאינו פולשני. שימוש בניתוחי Sham, דבר שיכול לאפשר סמיות מסוג זה, עלול להיות בעייתי מבחינה אתית. גם כשמדובר בטכנולוגיות של שירותים, כגון סדנאות שבהן האדם צריך להשתתף, אין יכולת ליצור סמיות, לפחות לא של הנבדק. במצבים שבהם מהלך המחלה עשוי להיות תנודתי, או במצבים שבהם הערכת התועלת מתבססת בעיקר על מדדים סובייקטיביים, העדר מחקרים אקראיים מבוקרים בכלל, וכפולי-סמיות בפרט, גורמים לכך שהתוצאות של המחקרים עשויים להיתפש כמהימנים פחות[6],[7].
בעיה נוספת הקשורה למחקרים ולתוצאותיהם היא שלעתים התועלת של טכנולוגיות שאינן תרופות עשויה להיות תלויה במיומנות של הגורם המבצע אותה. אמנם גם בתרופות הגורמים המטפלים צריכים להכיר את התרופה, לדעת לנהל את שינויי המינון או את תופעות הלוואי, אך עצם דרך השימוש בתרופה לרוב אינו מצריך מיומנות מסוימת. לעומת זאת, בטכנולוגיות שאינן תרופות, בעיקר מכשירים, פרוצדורות וחלק מהשירותים, קיום עקומת למידה יכול להביא לתוצאות שונות אצל מטפלים או מבצעים שונים[4],[6]. מיקום המטפל על גבי עקומה זו עשוי להשפיע למשל על משך זמן ביצוע פרוצדורה, סיבוכים אפשריים, משך האשפוז וההצדקה לבחירת גישה או טכנולוגיה מסוימת כתולדה מכך[8].
חלק מהחברות המייצרות מכשירים מושתלים, לדוגמה, שולחות נציג של החברה (פרוקטור) להיות נוכח בעת השתלה על מנת לסייע לצוות ולקצר את עקומת הלמידה. לדבר זה עשויות להיות השלכות חוקיות-אתיות משמעותיות.
כך, הן בשלב ביצוע ההערכה והן בשלב קבלת ההחלטות על בסיס ההערכה, טכנולוגיות שאינן תרופות צריכות להישען לעתים קרובות על בסיס ראייתי בדרגה נמוכה יותר מאשר תרופות, עם דרגת חוסר ודאות רבה יותר.
פערים במסגרות טיפוליות - שירותי בריאות
שירותים רפואיים, הן שירותים קליניים (סדנאות, טיפולים וכדומה) והן שירותים מנהלתיים, מהווים אתגר מיוחד. שירותים כאלה מתחילים במקרים רבים In house על ידי קבוצת אנשים "משוגעים לדבר", והמחקרים משקפים לרוב את נסיונם ולא מתודולוגיה מחקרית מסודרת. כתולדה מכך, מטבע הדברים, שירותים אלה הם בעלי שונות מובנית. כאשר קיימות מספר קבוצות כאלו, שפיתחו שירותים דומים, השונות בין השירותים הספציפיים עלולה להשפיע על התוצאים ועל התועלת. כך לדוגמה, האם ניתן להשוות את התועלת של שירות שיקום שניתן פעמיים בשבוע לזה שניתן חמישה ימים בשבוע? בין כזה שניתן במרפאה, בבית המטופל או בבית החולים? מה משכו של כל טיפול ומהו נסיונו ומקצועו של המטפל וכיצד זה משפיע? מסיבה זו, גם כאשר יוחלט לאמץ שירות כזה, לא בטוח שהמתאר שבו הוא יינתן, במסגרת מבנה מערכת הבריאות הישראלית, יביא לתוצאות דומות לאלו שבמקומות אחרים בעולם כפי שמצופה על פי המחקרים. דוגמה לכך היא הטיפול בפצע קשה, ריפוי המשלב בכל מרפאה או מחלקה טכנולוגיות שונות (למשל, טיפול בוואקום, ברימות, במקרופאגים, בתא לחץ, באוזון מקומי או סיסטמי) ושילוב טיפולים (למשל, חבישות מתקדמות, משחות, הפחתת לחץ על הפצע וכדומה) העשויים להשפיע על התוצאים.
מאפייני טכנולוגיות אבחנתיות
ההערכה של טכנולוגיות אבחנתיות מצריכה הסתכלות שונה לחלוטין מאשר זו על טכנולוגיות רפואיות אחרות (כולל תרופות). בניגוד לתרופות או לטכנולוגיות שאינן תרופתיות שמטרתן טיפולית ובהן ההערכה מתבססת על מחקרים הבודקים את השפעתן על מדדים ישירים או עקיפים הרלוונטיים לתועלת הבריאותית, כאשר מדובר בטכנולוגיות אבחנתיות, ההערכה צריכה לכלול לפחות שני מרכיבים:
- המרכיב הראשון הוא היכולת האבחנתית של הבדיקה לזהות את המצב הרפואי הרלוונטי
- המרכיב השני הוא מידת השפעתו של האבחון הזה על אפשרויות הטיפול והתוצאות הקליניות
כך התועלת של בדיקה שיכולה לאבחן, אפילו בצורה מצוינת, מצב שאין לתוצאת הבדיקה השלכה קלינית על ההחלטות הטיפוליות בו היא מוגבלת ביותר. תועלת זו גם תלויה בנכונות של האדם לבצע את הטיפול הנדרש בעקבות האבחנה, דבר המסבך עוד יותר את התרגום של התוצאות להשפעה קלינית[9],[10],[11].
היכולת האבחנתית כוללת התייחסויות למאפיינים שונים כגון רגישות וסגוליות, Negative predictive value, Positive predictive value, Positive likelihood ratio, ו-Negative likelihood ratio, שהבנתם ותרגומם למשמעות מעשית אינם תמיד פשוטים. בנוסף, חלק מהיעילות של הבדיקה באבחון תלוי בשכיחות של המצב שאותו מבקשים לאבחן ולכן התועלת המערכתית יכולה להיות שונה באוכלוסיות שונות[10],[12]. דוגמה למצב שבו השכיחות השונה בישראל אל מול המקומות בעולם שבהם נבדקה הטכנולוגיה היוותה שיקול משמעותי בדיוני ועדת הסל, היא בדיקת הסקר באמצעות CT במינון קרינה נמוך לגילוי מוקדם של סרטן הריאה. שכיחות סרטן הריאה בישראל נמוכה ביחס לשכיחותה בארצות הברית ולכן התועלת צפויה להיות פחותה.
כך התבטאו חברי ועדת הסל בדיון אודות בדיקה זו:
- "הנתונים בישראל בכל זאת חשובים, כי שכיחות סרטן הריאה בישראל הרבה יותר נמוכה...
- בקרב יהודים, לא בקרב גברים ערבים... זה לא מוכר לי, אבל עדיין זה יותר נמוך מאשר האוכלוסייה שנסקרה פה...
- אני רוצה להוסיף עוד... קודם כל שיעור המעשנים בארץ יורד, זאת אומרת ש-10-20 שנה מהיום שיעור סרטן הריאה ירד. לוקח בערך 20 שנה מהשינוי באחוזים באוכלוסיה ועד שרואים את זה בסרטני ריאה וסרטנים שקשורים לעישון. אבל כיוון שהמספרים יורדים, ויורדים מהר, דווקא בשנים האחרונות מאז שהכנסנו את הטכנולוגיות להפסקת עישון לסל, רואים ירידה משמעותית..."[13].
דוגמה נוספת היא בדיקת סקר היילודים לאבחון מוקדם של סיסטיק פיברוזיס (CF, Cystic Fibrosis). כיוון שבישראל קיים סקר לגילוי נשאות למחלה, מספר היילודים שנולדים עם סיסטיק פיברוזיס לא מאובחן הוא נמוך ביחס למקומות אחרים בעולם שבהם אין סקר כזה, גם אם שכיחות המחלה בישראל אמורה להיות גבוהה יותר.
בעניין זה, ציינו חברי הוועדה:
- "אבל השאלה היא כמה מהמדינות עושות גם סקר [לסיסטיק פיברוזיס - א.ס.] בזמן ההיריון, כי יש מדינות שבוחרות לעשות סקר יילודים במקום סקר היריון.... יש דבר שקיים בסל ואנשים לא עושים, זה בגלל שהמודעות שלהם לא טובה... צריך מישהו שידחף אותם, להשקיע מאמצים של יידוע... אולי צריך לשים את הכסף למה שקיים כבר וצריכים מודעות במקום להכניס טכנולוגיה חדשה, שגם אליה לא תהיה מודעות"[14].
סוגיה נוספת המצריכה התייחסות כאשר מדובר בטכנולוגיות אבחנתיות היא בטיחות הבדיקה (או בדיקות נלוות). בניגוד לטכנולוגיות טיפוליות, שבהן נעשה שימוש כאשר האדם כבר חולה ולכן יש הגיון בלקיחת סיכון רב יותר בהתערבות, בדיקה אבחנתית יכולה להתבצע באדם בריא שעבורו הנכונות לקחת סיכון היא שונה. במידת מה הדבר דומה למתן חיסונים אשר גם בהם נלקח סיכון מסוים באנשים בריאים על מנת להיטיב עם המצב הבריאותי של חלק מהם. הדבר בעייתי במיוחד כאשר מדובר בבדיקות סקר לאוכלוסיה הכללית, ולא בדיקות לאבחנה באדם חשוד למחלה, ששם יש דרישה ליותר בטיחות ופחות פולשנות.
סוגיה נוספת היא נושא התוצאות המוטעות. כיוון שלא קיימת בדיקה מושלמת יכולים להיות מקרים שבהם הבדיקה מזהה אדם בריא כחולה (False positive) או אדם חולה כבריא (False negative), ויש צורך להביא בחשבון את ההשלכות הבריאותיות של טעויות אלו: מתן טיפול מיותר, או ביצוע בדיקות אבחון פולשניות (עם תופעות לוואי) באדם בריא ואי מתן טיפול (או מתן באיחור) באדם חולה, וזאת מעבר להשלכות הפסיכולוגיות של אבחון מוטעה[10],[12].
היכולת האבחנתית של בדיקה יכולה גם להיות שונה אם היא מבוצעת באופן חד פעמי או כבדיקה חוזרת. ההבדלים ביכולת האבחנתית תלויים בתדירות שבה מבוצעת הבדיקה ובקצב ההופעה או השינוי של המצב שאותו רוצים לאבחן ולכן חשוב לבדוק בקפדנות את מידת ההתאמה ביניהם כאשר מדובר בבדיקות מעקב או בבדיקות סקר.
בדיקות סקר מעלות מספר סוגיות נוספות האופייניות להן. אחת הבעיות המשמעותיות בבדיקות סקר, במיוחד של סרטן, היא בעיית האבחון יתר (Over-diagnosis) - אבחון באמצעות בדיקת הסקר דווקא של גידולים פחות אלימים הגדלים בקצב איטי ושהשפעת הגילוי המוקדם שלהם משמעותית פחות, בעוד שהגידולים האלימים מתגלים יותר בצורה קלינית בין הבדיקות עקב קצב הגידול המהיר שלהם. בעיה נוספת של בדיקות סקר היא Lead time, שהוא מצב שבו תוצאות מחקרים מראות השפעה של הבדיקה על ההישרדות, אך השפעה זו נובעת מפערי זמן בין הגילוי המוקדם יותר באמצעות הסקר לבין הגילוי הקליני המאוחר יותר למוות שהיה מתרחש ממילא באותו מועד. קיימות שיטות להעריך את מידת ההשפעה של עיוותים אלה על התועלת הקלינית האמיתית אך הטיות אלו עדיין מהוות מקור משמעותי לחוסר ודאות בעת ההערכה וקבלת ההחלטה לגבי אימוץ והטמעת השימוש בבדיקות אלו ומימון ציבורי שלהן.
סוגיה נוספת בתחום הבדיקות, בעיקר בדיקות סקר, היא השפעתן על ההוצאות הרפואיות. מעבר לעלויות של הבדיקה עצמה והנלווים לה, שעשויות להיות מאוד משמעותיות בבדיקות סקר לאוכלוסיות נרחבות, עצם הגילוי של מספר גדול יותר של חולים (או חולים פוטנציאליים) שצריך לטפל בהם עלול להביא לעלייה משמעותית בהוצאות בעקבות הכללת הבדיקה. בחלק מבדיקות הסקר השאיפה היא שהגילוי המוקדם יביא לזיהוי חולים במצב קל יותר וכך תיחסכנה עלויות של טיפול במצבים הקשים יותר, שהן לרוב גדולות יותר, אך לעתים לא כך הדבר. נושא העלויות הנלוות היווה שיקול משמעותי הן בהחלטה והן בתמחור של בדיקת הסקר לגילוי מוקדם של מפרצת אאורטלית בטנית (Abdominal aortic aneurysm), טכנולוגיה שהוצעה להכללה בסל בשנת 2015. גילוי של יותר מקרי מפרצת יצריך יותר תיקונים של המפרצות בניתוח או בצנתור, פרוצדורות הכרוכות בהשתלת תומכן שעלותו משמעותית, בעוד שגילוי מאוחר תוך כדי דימום מהמפרצת מסתיים בשיעור פטירה גבוה של החולים. הדבר בא לידי ביטוי בדברי חברי הוועדה בדיון:
- "לא דיברתי על כסף, אמרתי רק שיובהר לחברי הועדה שזו טכנולוגיית סיקור שיש לה משמעויות טיפוליות... זה מעלה פי שניים את מספר המטופלים... נדמה לי 120,000 שקל DRG... זה לא יחומש, זה יעושר. אבל עם Cost-effectiveness ... אבל אנחנו רוצים להציל אנשים" (הציטוטים מכמה דוברים אוחדו)[15].
חוק ביטוח בריאות ממלכתי וטכנולוגיות רפואיות (כולל טכנולוגיות בתי חולים)
התייחסות הסל - באופן כללי בישראל, חלק משמעותי בהערכת טכנולוגיות רפואיות נעשה בהקשר למימון שלהן במסגרת סל שירותי הבריאות. תרופות וטכנולוגיות שאינן תרופות נבדלות גם בדרך שבו חוק ביטוח בריאות ממלכתי מתייחס אליהן בנוגע לזכאות למימון ציבורי. בעוד שתרופות מזוהות מבחינת החוק בשם גנרי המאפשר בכמעט כל המקרים זיהוי ברור אם מדובר בתרופה הנדונה והאם ניתן לראותה ככלולה בסל בהתוויה הרשומה או זו שהוגדרה בסל, טכנולוגיות שאינן תרופות מוגדרות באופן תיאורי יותר. התיאור יכול להגדיר קבוצה מוגדרת פחות או יותר של טכנולוגיות דומות או להגדיר את הטכנולוגיה על בסיס מטרתה בלבד, כאשר במקרים רבים ההגדרה מלווה במילים כגון "כגון", "לדוגמה" או "וכו'" המאפשרות להכליל תחתיה מספר טכנולוגיות. כך לדוגמה כלולה בסל בדיקת MRI ללא פירוט התוויות המשתנות בהתאם לפרקטיקה הרפואית הנוהגת או למשל "טיפול בעקרות" או "הפריה חוץ גופית", תחום שבו חלים כל העת פיתוחים של טכנולוגיות מתקדמות חדשות. מאחורי צורת הגדרה זו עומדת החשיבה שעולם הטכנולוגיות הוא עולם דינאמי, הן כאשר מדובר בטכנולוגיות דומות (כפי שדובר לגבי הרגולציה) והן מבחינת שינויים לאורך הזמן בטכנולוגיה עצמה, והגדרה פרטנית מדי תביא לכך שעלול להיות צורך לדון מחדש בכל שכלול או פיתוח של טכנולוגיה קיימת. עם זאת, יש לציין שלאורך השנים של עדכוני הסל יש נטייה לתת הגדרות מוגדרות יותר מתוך הבנה שהגדרה רחבה מדי עלולה להיות בעייתית באותה מידה.
כך לדוגמה, בשנת 1999 הוכלל בסל שתל השבלול (Cochlear Implant) לטיפול בחירשות בילדים ללא השתתפות עצמית. מסגרת הסל הוגדרה בחוזר מנכ"ל: "מבוטחים בגילאי 2-18 עם חירשות דו צדדית אשר איננה ניתנת לשיקום באמצעות מכשיר שמיעה - לא יידרשו להשתתף בעלות השתל"[16]. בעוד שבעת הכללת השירות בסל נהוג היה להתקין שתל יחיד באוזן אחת, במהלך השנים השתנתה הפרקטיקה הטיפולית והורחבו ההתוויות המצדיקות התקנת שתל השבלול לילדים כולל השתלה באוזן השנייה או השתלה דו צידית סימולטנית. לנוכח הניסוח הרחב והכוללני בחוק, נמצא כי השתל השני כלול אף הוא בסל. בשנת 2006 הוכלל בסל השתל גם עבור מבוגרים. בחוזר מנכ"ל משרד הבריאות ומינהל רפואה באותה שנה הוכללו שישה סעיפים שונים המגדירים באופן מדויק את ההתוויות לשתל השבלול במבוגרים וביניהם סף רמת דציבלים אותם שומע המטופל, מיצוי טיפולים קודמים וקיומה של שפה דבורה[17].
לאור זאת, הערכה של טכנולוגיות שאינן תרופות מחייבת הסתכלות על הטכנולוגיה ובחינה משפטית שלה מול הזכאויות הקיימות, והיא נעשית עוד בטרם דיוני ועדת הסל ויכולה להשפיע על השאלה אם הטכנולוגיה בכלל תעלה לדיון.
טכנולוגיות אשפוז - נקודה נוספת הקשורה לחוק ומשפיעה יותר, אם לא כמעט אך ורק, על טכנולוגיות שאינן תרופות היא הנושא של טכנולוגיות בתי חולים (אשפוז).
שירותי הבריאות הניתנים בבתי החולים אינם מפורטים בסל שירותים מוגדר ובתי החולים יכולים לאמץ ולהטמיע שימוש טכנולוגיות רפואיות חדשות על פי שיקול דעתם בכפוף לאישורים הרגולטוריים המחייבים. קופות החולים מספקות התחייבות למבוטחיהן לפעולות המבוצעות בבתי החולים בהתאם למסגרת הסל. הנחת המחוקק הייתה כי שירות אשפוזי הניתן במסגרת הרפואה הציבורית, המשקף שכלול או פיתוח של פתרונות רפואיים מוכרים, ייחשב גם הוא ככלול בסל ללא צורך בפירוט ספציפי שלו בתוספת השנייה או בהוספה מפורשת שלו לסל. באופן זה, חלק מהטכנולוגיות המוצעות להכללה בסל נמצאות לא מתאימות להיות מובאות לדיון בוועדת הסל ומועברות לדיון בצוות שמונה לכך על ידי מנכ"ל משרד הבריאות ופועל באחריות האגף למדיניות טכנולוגיות רפואיות, הרכב הצוות מפורט בחוזר מינהל הרפואה בנושא[18].
מטרת הצוות היא להעריך את הטכנולוגיה הרפואית החדשה המוצעת ולהתאים את הפתרונות הנדרשים כדי שניתן יהיה להטמיע את השימוש בטכנולוגיות אלו בבתי החולים, לגבי כל טכנולוגיה לפי נתוניה, תוך בחינה של ההיבט המדעי-רפואי, הכלכלי והמשפטי. אם הצוות מצא כי הטכנולוגיה בשלה ומוצדקת מבחינה רפואית ויש לראותה ככלולה בסל, ואין הצדקה לשימוש באמצעים רגולטוריים משלימים כגון תמחור נפרד שלה, הוא מודיע על כך למנהלי בתי החולים. במקרים נבחרים מוגדרות אמות מידה והתוויות לאספקת הטכנולוגיה בהתאם לקווים מנחים מקצועיים שמנסחים האיגודים המקצועיים. במקרה שנדרש תמחור ייעודי, ממשיך התהליך במסגרת תת ועדת המחירים. במקרים שבהם נדרש תקצוב ייעודי, בעיקר לטכנולוגיות תשתיתיות יקרות, מועברת הסוגיה למנכ"ל המשרד לבחינת פתרונות מתאימים ככל שניתן[18].
תמחור טכנולוגיות
תמחור של טכנולוגיות שאינן תרופות מצריך הסתכלות על היבטים שלרוב לא משחקים תפקיד בתמחור של תרופות. מעבר לעלות הטכנולוגיה עצמה, במקרים רבים יש צורך להביא בחשבון עלויות כוח אדם ועלויות של ציוד נלווה שאינו ספציפי לטכנולוגיה. קיימים מצבים דומים בתרופות, כגון בתרופות הניתנות בהזרקה על ידי גורם רפואי, אך אלה מהווים את יוצא הדופן. לעומת זאת, בתמחור טכנולוגיות מושתלות לדוגמה, יש להביא בחשבון את שעות העבודה של צוות חדר הניתוח, את זמן השימוש בחדר עצמו (תשתיות) ועלויות ציוד ניתוחי נלווה. תמחור שירותים מבוסס כולו, או כמעט כולו, על תמחור כזה.
עלויות נוספות שצריכות לבוא בחשבון הן עלויות השקעה ברכישת ציוד קבוע או תשתית אחרת וכן בלאי וצורך בהחלפה של ציוד. בנוסף, כאשר מדובר בציוד קבוע, התמחור לצורך הסל פורס את עלות הרכישה על פני צפי כמות המטופלים שעתידה להשתמש במכשיר לאורך השנים, ולכן תמחור הטכנולוגיה עצמה עשוי להיות תלוי בהיקף האוכלוסיה, בעוד שבתרופות הוא אינו משפיע על מחיר התרופה אלא רק על הנטל התקציבי הכולל.
בעיה משמעותית נוספת בתמחור של טכנולוגיות שאינן תרופות נובעת מכך שקופות החולים, המקבלות את התקציב מהסל עבור מתן הטכנולוגיה, אינן תמיד הספקיות בפועל של הטכנולוגיה והן צריכות לרכוש חלק מהשירותים הקשורים במתן זה מגורם שלישי. חלק מהתמחור של טכנולוגיות מושתלות מתייחס להשתלה של המכשיר, שירות הניתן בבית חולים, והיעדר תמחור ייעודי הולם של הטכנולוגיה (מנקודת המבט של בית החולים) יכול להביא לכך שהוא לא יהיה מעוניין לספק את הטכנולוגיה ויעדיף שירותים אחרים רווחיים יותר. תופעה דומה עשויה להתרחש לגבי שירותים שיכולים להינתן על ידי גורמים פרטיים חיצוניים, והתמחור של בניית ומתן שירותים כאלו In house בתוך הקופה יכול להיות שונה מהתמחור של התקשרות עם ספק כזה.
דוגמה נוספת היא אביזרים שיכולים להירכש בשוק החופשי ללא פיקוח על המחיר, ואז תמחור הטכנולוגיה עבור הסל (שיכול להינתן לעתים באמצעות החזר למטופל על ידי הקופה ולא נרכש על ידה עבורו) יכול להביא לכך שהמחיר שהספקים ידרשו יעלה והתמחור (ולכן ההחזר) לא יכסה את ההוצאה בפועל.
הקשר בין תמחור לביצוע בפועל מכניס משתנים נוספים לתהליך התמחור מעבר לעלויות הנקיות הכרוכות בתמחור הטכנולוגיה, דבר שלרוב לא קורה בתרופות שמחירן ידוע מראש ועלותן יורדת ככל שחולף הזמן.
נתונים מספריים
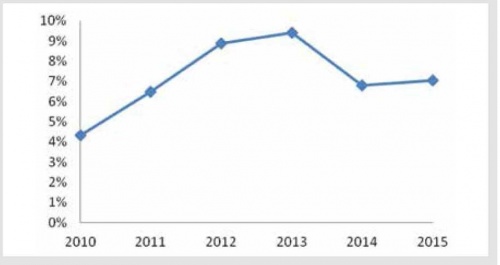
לאורך השנים חלה עלייה במספר הכולל של ההגשות של טכנולוגיות חדשות לסל. הדבר נכון גם לגבי טכנולוגיות שאינן תרופות, כאשר מספר ההגשות של טכנולוגיות אלו מגיע ליותר מ־100 בכל שנה. עם זאת, מרבית הטכנולוגיות הללו אינן מגיעות לדיוני ועדת הסל מהסיבות שצוינו לעיל או מסיבות אחרות, ובארבע השנים האחרונות מספר הטכנולוגיות שאינן תרופות שעלו לדיון עמד על כ־35 בשנה. בסקירה של כל התרופות והטכנולוגיות שעלו לדיון בין השנים 2010 ל־2015 נמצא כי טכנולוגיות שאינן תרופות מהוות כ־7% מכלל הטכנולוגיות שעולות לדיונים (תרשים מספר 1)[19].
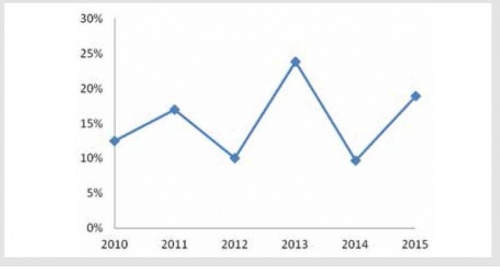
מתוך ניתוח מספרי הטכנולוגיות שאינן תרופות שהוכללו בסופו של דבר בסל, לא ניתן להגדיר מגמה קבועה לגבי טכנולוגיות אלו והן היוו בין 10% לכמעט רבע מהטכנולוגיות שהוכללו בסל בין השנים 2010 ל־2015 (תרשים מספר 2)[19].
כיוון שבמהלך עבודת ועדת הסל חלים שינויים בהתוויות עבור התרופות והטכנולוגיות הנדונות, כולל פיצולים או איחודים של התוויות וטכנולוגיות (לדוגמה, איחוד של טכנולוגיות שתכליתן הטיפולית זהה, כמו סוגים שונים של סנסורים לניטור סוכר או הפרדה של טכנולוגיה להתוויות שונות, כמו מכשיר לקיצוב סרעפת לחולי ALS ולנפגעי עמוד שידרה), לא ניתן להשוות בין מספר התרופות והטכנולוגיות הנדונות והנכללות. לעתים גם נכללות בסל טכנולוגיות שכלל לא הוגשו להכללה לאחר שהוועדה החליטה שהן נחוצות בהקשר להכללה של תרופה או טכנולוגיה אחרת. דוגמאות לכך הן הסדנאות לגמילה מעישון שנכללו כחבילה אחת יחד עם שתי תרופות לגמילה, והבדיקות לדרגת הפיברוזיס של הכבד שנכללו כיוון שהן שימשו ככלי להחלטה אילו חולים עם דלקת כבד כרונית על רקע נגיף ההפטיטיס C מתאימים לטיפול בתרופות שנכללו באותה שנה. דוגמה נוספת היא הבדיקות הגנטיות למוטציות שונות בתאי הגידול כדי שניתן יהיה להחליט על התאמה לטיפול תרופתי ביולוגי בחולי סרטן.
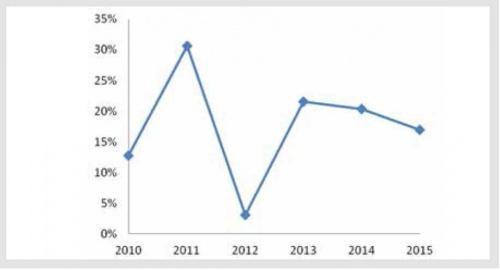
חשוב לציין שבשנים האחרונות מספר גדול יחסית של תרופות מוכללות בסל "ללא תוספת עלות", דבר שכמעט אינו מתרחש בטכנולוגיות שאינן תרופות. מבין 388 התרופות שנכללו בסל בין השנים 2010 ל־2015 כמעט 31% היו ללא תוספת עלות לעומת רק 1.4% (אחת מתוך 70) בטכנולוגיות שאינן תרופות. מתוך תקציב עדכון הסל בין השנים 2010 ל־2015 טכנולוגיות שאינן תרופות תומחרו בכ־20% מתוך כלל התקציב שיועד להרחבת הסל באותן שנים, פרט לסל 2012 שבה טכנולוגיות שאינן תרופות תומחרו רק בכ־3% (תרשים מספר 3)[19]. לעומת זאת, בסל 2011 ניתן לראות כי האחוז מהתקציב שניתן להכללת טכנולוגיות שאינן תרופות היה גדול באופן חריג (כ־30%). בשנה זו הוכללו בסל שתי טכנולוגיות עתירות תקציב המיועדות לאוכלוסיות רחבות היקף (עשרות אלפי מטופלים). הכללתן בסל של טכנולוגיות אלו נועדה להסדיר תחומים חדשים ובעלי השלכות רוחב וקליניות משמעותיות כגון: מימון מכשירי שמיעה לבני 65 ומעלה וסל טכנולוגיות לטיפול בפצע קשה ריפוי.
התייחסות ועדת הסל - נתונים איכותניים
במטרה להדגים את ההתבטאויות שנאמרות בוועדת הסל במסגרת דיוניה, אודות טכנולוגיות רפואיות שאינן תרופות והעדויות המדעיות המוצגות לגביהן, מובאים להלן ציטוטים מתוך פרוטוקולים של ועדת הסל מחמש השנים האחרונות (2010-2015) לגבי טכנולוגיות נבחרות המובאות כדוגמאות. הפרוטוקולים מוצגים בשקיפות מלאה לטובת הציבור, באתר ועדת הסל בתוך אתר משרד הבריאות (ניתן למצאם באתר משרד הבריאות)[19].
לדוגמה, לגבי טכנולוגיה שאינה תרופה שנדונה בוועדה לאחר שהוצעה להכללה בסל במשך מספר שנים, נאמר:
- "אני רוצה להתייחס שנייה לפרסומים. אני לא ראיתי פרסומים בעיתונים איכותיים כאן בנושא הזה. יש עבודות בעיתונים טובים, אולי מישהו מכיר? מי יכול להתייחס לתחום...? מבחינתי, ה-Level of evidence פחות או יותר יישאר ב-Level הזה. זה לא החברות האלה שעושים מחקר על טכנולוגיה אולי בקרדיולוגיה אבל בתחומים אחרים המחקרים הם קטנים, מוגבלים, על קבוצות קטנות של חולים, הם עושים את זה בגלל שה-Cycle time של הטכנולוגיה הוא קצר, הם מכניסים שיפור בטכנולוגיה ופעם הבאה... יש מכשיר עם סוויצ' טיפה שונה. לכן הם עושים מחקרים קצרים מאוד, מוגבלים מאוד. זה פחות או יותר מה שיהיה. לכן הסטנדרט שאנחנו צריכים לשפוט את זה הוא לא בסטנדרט הרגיל של כל הטכנולוגיות האחרות... מה שאני מנסה לומר. לכן, אם יש ניסיון מצטבר במרכזים רפואיים גדולים שיש איזה ערך חיובי דהיינו... שהמנתחים עוקבים אחרי חולים ואומרים שזה עובד וזה עובד טוב, שיש אוכלוסיה שנהנית כי הם נכשלו על החלופה שקיימת, אנחנו צריכים לתת יותר, ללכת יותר לכיוון הטכנולוגיה... אני רוצה להזכיר לחברנו הלא רופאים, ש-X מדבר על Level of evidence. הוא צודק שתרופות שהן טכנולוגיה תרופתית אנחנו דורשים בדרך כלל Level מאוד גבוה. כשאנחנו אומרים שבטכנולוגיה שאיננה תרופתית הרבה פעמים אין את ה-Level הזה, זה נכון אבל שיהיה משהו... מי שעשה 45 מקרים ופרסם אותם..." (מתוך פרוטוקול הוועדה מיום 26/10/2010).
הדיונים אודות הטכנולוגיה שהוצגה בהקדמה, התקן לתיקון דלף מיטרלי, כללו לאורך השנים התבטאויות מייצגות המדגימות היטב את המורכבות בהערכת טכנולוגיות שאינן תרופות, הכרוכה בין השאר בחדשנות הטכנולוגיה, מיעוט מידע, איכות ירודה של מחקרים בהיבט של היקף מטופלים ומיומנות משתנה של המטפלים. כתוצאה מכך בא לידי ביטוי קושי רב של חברי ועדת הסל לגבש החלטה על אימוץ הטכנולוגיה והכללתה בסל, לאורך מספר שנים. כפי שהוזכר, הטכנולוגיה הוצעה לראשונה לקראת הרחבת הסל לשנת 2012. באותה עת במאמר המחקרי המוביל נכללו מספר תת קבוצות של חולים, ביניהם כאלה היכולים לעבור ניתוח לב פתוח ושמצבם קל יותר יחד עם חולים קשים שאינם מועמדים לניתוח ושעבורם יועדה הטכנולוגיה בהצעה לסל. בשל הפער בין קבוצות החולים שבמחקר לאלה שיטופלו בטכנולוגיה, התקשו חברי הוועדה לגבש עמדה על הכללתה בסל.
- "המחקר העיקרי שמתייחס לחולים האלה הוא מחקר האוורסט 5 עם תת קבוצה שנקראת High risk. האוורסט 5 השווה את הפרוצדורה הזאת לניתוח בחולים שכן יכולים לעבור ניתוח ולכן הוא פחות רלוונטי אם כי הוא מופיע אצלכם גם במחקרים. בתת קבוצת High risk היה למעשה מחקר פרוספקטיבי עם השוואה רטרוספקטיבית לחולים שלא עברו טיפול ובסיכון גבוה... עם ההשוואה לניתוח שזה לא אוכלוסיה רלוונטית" (מתוך פרוטוקול הוועדה מיום 11/11/2013).
באותה שנה דורגה הטכנולוגיה עבור חולים הנמצאים בסיכון גבוה לביצוע ניתוח לב פתוח A8/9. בשנה קודם לכן, נאספו נתונים על 47 הפעולות שבוצעו תוך שימוש בטכנולוגיה בישראל ותוצאותיהם דווחו לוועדה. היקף הנתונים הזעום וחוסר הבהירות ביחס ליכולת ההכללה על פיהם מנעו מחברי הוועדה לדרג את הטכנולוגיה בדירוג גבוה.
- "העובדה שנעשו 47 מקרים להגיד שהטכנולוגיה עוד לא בשלה, או לפחות לא בשלה במדינת ישראל... אמנם הנתונים, כפי שמודדים אותם באקו, הם מרשימים, אבל לא מצורף פה [נתונים על... - א.ס.] תמותה" (מתוך פרוטוקול הוועדה מיום 11/12/12). :
שנתיים אחר כך, בדיוני ועדת הסל לשנת 2014 ולאחר שהתקבל אישור FDA, נדונה הטכנולוגיה בפעם נוספת. חברי הוועדה הדגישו בדיוניהם בעיקר את החידושים בנושא מעבר למה שהוצג בשנים הקודמות.
- ה-FDA אישר אותו רק לחולים עם MR (Mitral Regurgitation) דגנרטיבי כיון שהאוורסט נעשה על MR דגנרטיבי, אם כי רוב הניסיון בעולם וכל המחקרים ה-High risk שהצגתי לכם מדברים בעיקר על חולים עם MR פונקציונאלי. אלה בעצם החולים שנמצאים בסיכון לניתוח" (מתוך פרוטוקול הוועדה מיום 11/11/2013).
חבר ועדה אחר הדגיש כי "מתייחסים לזה כאל טיפול אפשרי לחולים שאינם מיועדים לניתוח אבל אין המלצה רשמית כיון שמבחינתם הראיות עוד לא מספקות".
אחר הוסיף: "עוד שתי הערות לגבי הספרות שהוצגה פה. לדעתי, רובה מציגה שיפור באיכות חיים ולא בהישרדות. עדיין החולים האלה אחוזי התמותה שלהם גבוהים חרף המיטראקליפ, מכיוון שאפריורי אלה חולים קשים. זאת אומרת, זה טיפול שהוא ברובו משפר איכות חיים ואני לא מזלזל בכך" (מתוך פרוטוקול הוועדה מיום 11/11/2013).
באותו הדיון נאמרו הערות נוספות המתייחסות בין השאר לשלב בו נמצא פיתוח האביזר והיכולת לבחור את החולים המתאימים: "הטכנולוגיה... קשה מבחינה טכנית ודורשת צוות רב משתתפים... המכשירים האלה עוד יעברו שדרוגים... אני חושב שהמכשירים האלה הם עדיין לא במיטבם... אני חושב שזה התקדם באווידנס... יש כאלה שאומרים שזה פשוט עניין של בחירת חולים ועדיין לא יודעים לבחור את החולים הנכונים".
התלבטות חברי הוועדה, באותו הדיון, הובילה להצעה להגביל בשלב הראשון את השימוש בטכנולוגיה למרכזים נבחרים במטרה לאפשר רכישת מיומנות, ניסיון ומעקב אחרי ביצועים: "בוא ניתן את זה לכמה מרכזים שמתמחים. לא לפרוץ את זה יותר מדי".
באותה שנה הוכללה הטכנולוגיה בסל והצעה זו של חברי הוועדה הובילה בסופו של דבר להמלצת המועצה הלאומית לטיפול במחלות לב וכלי דם למתן רישוי למספר קצוב של מרכזים רפואיים לביצוע הפעולה.
ביבליוגרפיה
- ↑ Office of Technology Assessment. Assessing the Efficacy and Safety of Medical Technologies. Sept 1978.
- ↑ Ciani O, Wilcher B, Blankart CR et al. Health Technology Assessment Of Medical Devices: A Survey Of Non-European Union Agencies. Int J Technol Assess Health Care. 2015 Jan;31(3):154-65.
- ↑ Green W, Hutton J. Health technology assessments in England: an analysis of the NICE Medical Technologies Evaluation Programme. Eur J Health Econ. 2014 ;15(5):449-52
- ↑ 4.0 4.1 NICE. Medical Technologies Evaluation Programme I methods guide. April 2011. https://www.nice.org.uk/ Media/Defaul^About/what-we-do/NICE-guidance/NICE-medical-technologies/Medical-technologies-evaluation-programme-methods-guide.pdf
- ↑ 5.0 5.1 Sorenson C, Drummond M. Improving medical device regulation: the United States and Europe in perspective. Milbank Q. 2014 Mar;92(1):114-50.
- ↑ 6.0 6.1 Sorenson C, Tarricone R, Siebert M, Drummond M. Applying health economics for policy decision making: do devices differ from drugs? Europace. 2011;13 Suppl 2:ii54-8
- ↑ Ferguson M. Medical devices are different to '. pharmaceuticals in the Health Technology Assessment process. J Comp Eff Res. 2014 May;3(3):217-9.
- ↑ Lenihan JP Jr, Kovanda C, Seshadri-Kreaden U. What ; is the learning curve for robotic assisted gynecologic surgery? J Minim Invasive Gynecol. 2008 Sep-Oct;15(5):589-94.
- ↑ Siontis KC, Siontis GC, Contopoulos-Ioannidis DG et al. Diagnostic tests often fail to lead to changes in patient outcomes. J Clin Epidemiol. 2014 Jun;67(6):612-21.
- ↑ 10.0 10.1 10.2 NICE. Diagnostics Assessment Programme manual. December 2011. https://www.nice.org.uk/Media/Default/ About/what-we-do/NICE-guidance/NICE-diagnostics-guidance/Diagnostics-assessment-programme-manual.pdf
- ↑ Bossuyt PM, Reitsma JB, Linnet K et al. Beyond diagnostic accuracy: the clinical utility of diagnostic tests. Clin Chem. 2012 Dec;58(12):1636-43.
- ↑ 12.0 12.1 EUnetHTA. HTA Core Model for Diagnostic Technologies 1.0r http://www.eunethta.eu/outputs/hta-core-model-diagnostic-technologies-10r
- ↑ משרד הבריאות. ישיבת הועדה הציבורית להרחבת שירותי סל הבריאות לשנת 2015. ישיבה מתאריך 2.11.2014
- ↑ משרד הבריאות. ישיבת הועדה הציבורית להרחבת שירותי סל הבריאות לשנת 2015. ישיבה מתאריך 29.10.2014
- ↑ משרד הבריאות. ישיבת הועדה הציבורית להרחבת שירותי סל הבריאות לשנת 2015. ישיבה מתאריך 30.10.2014
- ↑ משרד הבריאות. חוזר המנהל הכללי 7/99 הרחבת של שירותי הבריאות. http://www.health.gov.il/hozer/mk07_1999.pdf
- ↑ משרד הבריאות. חוזר המנהל הכללי 26/06 הרחבת של שירותי הבריאות ספטמבר 2006. .http://www.health.gov.il/hozer/mk26_2006.pdf
- ↑ 18.0 18.1 משרד הבריאות. חוזר מנהל רפואה 25/2011. טכנולוגיות אשפוז. http://www.health.gov.il/hozer/mr25_2011.pdf
- ↑ 19.0 19.1 19.2 19.3 משרד הבריאות. ועדה ציבורית להרחבת סל שירותי http://www.health.gov.il/Services/ הבריאות Committee/vsal/Pages/default.aspx
קישורים חיצוניים
המידע שבדף זה נכתב על ידי ד"ר אתי סממה משרד הבריאות, ד"ר עינב הורוביץ מכון גרטנר, עריכה: הדס לבמור, משרד הבריאות


 כניסה
כניסה  עקבו אחרינו בפייסבוק
עקבו אחרינו בפייסבוק