טיפול בכאב בקשישים - נייר עמדה - Pain management in the elderly
הופניתם מהדף טיפול בכאב בקשישים - Pain management in the elderly לדף הנוכחי.
|
| |
|---|---|
| הטיפול בכאב בקשישים | |
| 250px | |
| האיגוד המפרסם | אגודה ישראלית לכאב האיגוד לרפואה גריאטרית האיגוד הישראלי לפרמקולוגיה קלינית |
| תאריך פרסום | יוני 2025 |
| יוצר הערך | ד"ר נטלי שליט ד"ר מריה פרידמן ד"ר יעל אוריון ד"ר ורד חרמוש ד"ר נביל גרה ד"ר נועה שטרן ד"ר איתי גואטה ד"ר דנה ברחל עטר |
| ניירות עמדה מתפרסמים ככלי עזר לרופא/ה ואינם באים במקום שיקול דעתו/ה בכל מצב נתון. כל הכתוב בלשון זכר מתייחס לשני המגדרים. | |
מסמך זה נועד לשימושם של רופאים גריאטריים, פנימאים, רופאי משפחה, אורתופדים, רופאי כאב, רופאים פליאטיביים ורופאים נוספים המטפלים באוכלוסיית הגיל השלישי.
נייר העמדה דן בעיקרו בטיפול בכאב כרוני, אך עקרונות האבחון והטיפול רלוונטיים גם בכאב אקוטי באוכלוסייה הקשישה.
מטרותיו:
- להעלות את המודעות לקיומו של כאב במטופלים בני הגיל השלישי ולנזקים שלו
- להוות כלי עזר שימושי לאבחון כאב במטופלים בגיל השלישי
- להנגיש את הידע ולסייע בבחירה מושכלת בטיפול בכאב בבני הגיל השלישי
- להפחית את החשש וההימנעות ממתן טיפול נוגד כאב באוכלוסייה זו
במסמך זה ריכזנו את המידע הקיים בנושא הטיפול בכאב באוכלוסייה הקשישה, וכן חלקנו מניסיוננו הקליני כמטפלים באוכלוסייה זו. עם זאת, המידע הקיים בספרות בנוגע לטיפול באוכלוסייה הספציפית הזו הוא דל באופן יחסי, ויש מקום להמשיך לחקור ולהרחיב את גוף הידע בנושא חשוב זה.
רקע
תסמונות הכאב השכיחות
12 אחוזים מהאוכלוסייה היא מעל גיל 65, וההשערה היא שעד שנת 2030, 20 אחוזים מהאוכלוסייה הכללית יהיו קשישים. עם הזדקנות האוכלוסייה, ישנה עלייה בשכיחות המצבים הקשורים בכאב כרוני[1][2][3].
כ-66 אחוזים מהאנשים מעל גיל 65 מדווחים על כאב כרוני, ובקרב דיירי בתי אבות ומוסדות סיעודיים השכיחות של כאב כרוני אף גבוהה יותר[1][2][3].
הסיבות השכיחות לכאב בקשישים הן כאב כתוצאה משינויים ניווניים, כגון כאבי גב תחתון וכאבי צוואר (כ-65 אחוזים מהמטופלים עם כאב כרוני), כאבים כרוניים במפרקים (15–25 אחוזים) משנית לאוסטאוארטריטיס או שברים אוסטאופורוטיים, כאב מוסקולוסקלטלי (כ-40 אחוזים), כאב נוירופתי פריפרי (בדרך כלל על רקע סוכרת או נוירלגיה פוסט-הרפטית, כ-35 אחוזים)[1][4][5][6][7][8], וכן כאב על רקע מחלה אונקולוגית או מחלות דלקתיות כגון טמפורל ארתריטיס/polymyalgia rheumatica.
הערכת כאב
משמעות הכאב במטופל הגריאטרי[9][10][11]
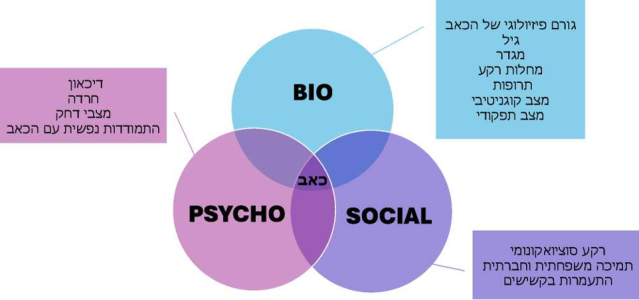
בגיל המבוגר ישנה השפעה משמעותית ביותר של הגורמים הביופסיכוסוציאליים על ההתמודדות עם כאב כרוני: גורמים ביולוגיים כוללים גיל, מגדר, מחלות רקע (כולל דמנציה ודיכאון) ותסמונות גריאטריות (כמו הפרעות שינה ושבריריות - FRAILTY).
גורמים פסיכולוגיים כוללים דיכאון, חרדה, שימוש באלכוהול וסמים והפרעות פסיכולוגיות הקשורות לכאב.
גורמים סוציאליים כוללים מוצא אתני ותרבותי, מצב סוציו-אקונומי, גילנות, התעמרות, תמיכה סוציאלית ובידוד חברתי.
השלכות הכאב על הקשיש:
עקב ירידה ברזרבה התפקודית בקשיש, לכאב ישנן השלכות רבות הכוללות:
- פגיעה ב-Basic activities of daily living - BADL. כאב כרוני כרוך בפגיעה בתפקודים יומיומיים כגון הליכה, מעברים, רחצה, שימוש בשירותים ועוד
- פגיעה ב-Instrumental activities of daily living - IADL - כאב כרוני כרוך בפגיעה בתפקודים מתקדמים כמו קניות, בישול, נהיגה וכן בפעילויות פנאי
- הפרעות במצב רוח, קוגניציה והתנהגות - כאב כרוני גורם לעלייה בסיכון לדיכאון, חרדה והפרעות שינה. גורמים אלה יכולים לפגוע בתפקוד הקוגניטיבי של הקשיש. בקשישים הסובלים מדמנציה, כאב כרוני יכול לגרום להפרעות התנהגות כולל אי שקט, תוקפנות, שוטטות ומצד שני לאפאטיה
- פגיעה תזונתית - כאב כרוני בקשישים כרוך בסיכון לתת-תזונה
- שבריריות (Frailty) - השילוב של ירידה בתפקוד ותת-תזונה מעלה סיכון לשבריריות, שהיא גורם סיכון משמעותי לתוצאים שליליים כולל אשפוזים, פגיעה תפקודית ומוות
- נפילות - השילוב של כאב כרוני, הפרעה בהליכה ושבריריות מעלה סיכון לנפילות
- איכות חיים - הכאב הכרוני עם כל התוצאים שלו פוגעים באופן משמעותי באיכות חייו של הקשיש
לסיכום - קשישים הסובלים מכאב סובלים משכיחות מוגברת של תסמונות גריאטריות רבות. הקשיש הכאוב נזקק לשימוש מוגבר במשאבי בריאות. בקשישים עם כאב כרוני יש עלייה בסיכון לאשפוזים והפחתה ביעילות תהליכים שיקומיים, מצב שמביא לפגיעה תפקודית, נכות ומיסוד. לטווח ארוך נצפית באנשים אלה עלייה בתחלואה ובתמותה. כל אלה מעלים את העומס הרגשי על בני המשפחה המטפלים.
המודל הביופסיכוסוציאלי של הכאב
| סוג כאב אפיון | נוסיספטיבי | נוירופתי | נוסיפלסטי |
|---|---|---|---|
| מקור | msk, דלקתי, ויסרלי | פריפרי או מרכזי | |
| דוגמאות | אוסתאוארטריטיס, כתף קפואה, שברים | TN ,PHN, נוירופתיה סוכרתית,
PSCP |
פיברומיאלגיה |
| מאפיינים | כאב הנובע מפגיעה ברקמה. כאב לוחץ, מושפע מתנועה, מנח ועומס | כאב הנובע מפגיעה עצבית. כאב שורף, חשמלי, מעקצץ | הכאב אינו נובע מפגיעה ברקמה. מלווה לרוב בהפרעות שינה, הפרעות מצב רוח והפרעות קוגניטיביות |
*MSK- musculoskeletal, PHN- post herpetic neuralgia, TN- trigeminal neuralgia, PSCP- post stroke central pain
אנמנזה
| אות | משמעות | הסבר |
| P | Provocative/Palliative | מה מקל או מחמיר את הכאב |
| Q | Quality | איכות הכאב |
| R | Region/ Radiation | מיקום והקרנה |
| S | Severity | חומרה |
| T | Timing | מתי התחיל הכאב, משכו, זמנים ביום שהוא מופיע |
דגשים לאנמנזה בקשישים[9][10][11]
- האנמנזה צריכה לכלול רקע רפואי מלא ותרופות
- הערכה תפקודית - תפקודים יומיומיים בסיסיים (BADL) ואינסטרומנטליים (IADL) המשקפים את יכולת המטופל לתפקד באופן עצמאי
- השפעת הכאב על גורמים אחרים - תפקוד, מצב רוח, שינה, תיאבון
- הערכה פסיכוסוציאלית להערכת גורמי תמך, קשר עם המטפל העיקרי ועם המשפחה, מצב כלכלי. למטופלים עם מערכת תמיכה יציבה וקשרים משפחתיים טובים פחות התמקדות בכאב ולפיכך טיפול יעיל יותר. נידוי חברתי וחוסר במערכת תמיכה תוביל לכאב עמיד יותר
- הערכת חומרת הכאב בכלים מתאימים (NRS לקשיש שמור קוגניטיבית, PAIN-AD לחולה דמנציה). צריך לזכור שבקשישים יש מרכיב תרבותי משמעותי שיכול לגרום להעצמה של הדיווח או לתת-דיווח
- חשוב לברר באופן מכוון אירועים של נפילות (כגורם לשברים סמויים)
- דגש לאנמנזה מחולים הסובלים מדמנציה לפי יכולתם והשלמה ממטפל עיקרי
- חלק מהקשישים לא משתמשים בביטוי "כואב", חשוב להבין את המושגים בהם המטופל משתמש ("לוחץ", "דוקר", "לא נעים") ולהשתמש בהם בעתיד
- צריך לזכור שתלונות של כאב יכולות לבטא בעיה אחרת כגון דיכאון או התעמרות בקשישים
אומדני כאב באוכלוסייה ירודה קוגניטיבית
זיהוי והערכת כאב במטופלים עם ירידה קוגניטיבית עלולה להיות קשה מאחר שרוב סולמות הכאב מסתמכים על דיווח עצמי[12][13][14]. כדאי להיעזר במטפליו של הקשיש לבירור שינויים במצב הרוח, שינויים בתפקוד, שינויים ביכולת המוטורית.
סרגל PAIN ASSESMENT IN ADVANCED DEMENTIA) PAINAD): מטופלים עם ירידה קוגניטיבית לעיתים אינם מסוגלים להביע את מצוקתם בצורה מילולית אלא על ידי התנהגות לא נורמטיבית וחריגה, אי-שקט פסיכומוטורי, צעקות, בכי, הבעת פנים, שפת גוף, בלבול, התנגדות לטיפול, ירידה בניידות. PAINAD הוא אומדן כאב במטופלים מבוגרים הלוקים בדמנציה על ידי התבוננות חיצונית של המטפל, ומתן ציון בקטגוריות קבועות לפי שפת הגוף של המטופל[15][16].
| ציון | 2 | 1 | 0 | התנהגות |
| נשימות כבדות ומהירות באופן קבוע/ | נשימה כבדות לסירוגין/ נשימות מהירות לסירוגין | רגילה | נשימה | |
| צעקות כאב ממושכות/בכי/אנחות בקול רם | נאנח לסירוגין/דיבור רפה | ללא | קולות | |
| עווית פנים | עצוב, מדוכא, מקמט את מצחו | מחייך או ללא הבעה | הבעת פנים | |
| נוקשה/אגרופים קמוצים/תנוחה עוברית/מתנגד למטפל | מתוח/חסר מנוחה/תנועות מונוטונית | רגוע | שפת גוף | |
| לא ניתן לנחם, להסיח או להרגיע | נרגע על ידי קול או מגע של המטפל | אין צורך/רגוע | הרגעת המטופל |
*הציון הכולל נע בין 0–10 נקודות. פרשנות אפשרית לציונים היא: 3-1 = כאב קל; 7-4 = כאב בינוני; 10-8 = כאבים עזים. יש אפליקציות המעריכות חומרת כאב של אנשים עם דמנציה על פי הבעות פנים בעזרת בינה מלאכותית.
https://www.painchek.com/improving-lives/
בדיקה גופנית
הבדיקה הגופנית מבוססת על מודל ARTNS[9][10][11]
| אות | משמעות | הסבר |
| A | Appearance | שינויים מקומיים, אסימטריה, סימני דלקת |
| R | Range of motion | תנועה אקטיבית ופאסיבית של האזור הכואב |
| T | Tissue texture /
Tenderness |
רגישות מקומית, בצקת, שינויי טמפרטורה |
| N | Neurological | חסרים נוירולוגיים מוטוריים, דיסאסטזיה ואלודיניה |
| S | Special tests | בדיקות מותאמות למקור הכאב |
תוספת לבדיקה גופנית בקשישים
- בדיקת יציבות הליכה
- הגבלות בטווחי תנועה שיכולות להשפיע על תפקוד יומיומי
בדיקות עזר - דגלים אדומים
פעמים רבות בקשישים ישנם מספר מקורות כאב במקביל, כך שלא בהכרח ניתן יהיה לאתר סיבה בודדת כמחוללת הכאב המרכזית.
מנגד, בירור מקיף מדי בגילאים האלו עלול להדגים ממצאים מקריים בהדמיה אשר גוררים בירורים נוספים ולרוב מיותרים שמהווים בפני עצמם מקור לקושי נוסף.
לכן ההמלצה שלנו היא לשלוח לאמצעי הדמיה רק במקרים של דגלים אדומים (לדוגמה כאב לאחר נפילה או טראומה, חסר נוירולוגי, הפרעה בשליטה על סוגרים, סימני B, רקע אונקולוגי או דיכוי חיסוני). באשר לבדיקות דם, בכל מטופל הסובל מכאב מומלץ להשלים בירור בסיסי של תפקודי כליות וכבד על מנת להתאים באופן מיטבי את המינון של הטיפול התרופתי.
האתגר בטיפול באוכלוסייה הקשישה
הטיפול בכאב בקשישים עלול להיות מאתגר, ממספר בחינות:
- קושי בהערכת כאב מדויקת במיוחד במטופלים ירודים קוגניטיבית (מבחינת מיקום, עוצמה ומאפיינים)
- קושי בהתאמת טיפול תרופתי עקב אינטראקציות בין-תרופתיות, שינויים פרמקודינמיים ופרמקוקינטיים במטבוליזם של תרופות אצל קשישים[17][18][19][20][21][22][23], שינויים תלויי-גיל במערכת העצבים המרכזית והפריפרית ושינויים בעיבוד הכאב. ידע במנגנוני כאב בקרב מטפלים יכול להוביל לשיפור איכות הטיפול ואיכות החיים של האוכלוסייה הגריאטרית
בהתאמת הטיפול התרופתי לכאב יש לקחת בחשבון גורמים רבים המשפיעים על הפרמקודינמיקה והפרמקוקינטיקה של התרופות, משנית לירידה הטבעית בתפקוד איברי הגוף ביחד עם קו-מורבידיות רבה.
- כחלק מהזדקנות תקינה ישנה ירידה ב-LEAN MASS וב-TOTAL BODY WATER ועלייה ברקמת השומן, המשפיעים על פיזור התרופה, רמות התרופה בדם ועל פינוי התרופה
- תפקוד כלייתי: מעל גיל 70 ישנה ירידה של כ-40–50 אחוזים מהתפקוד הכלייתי גם בהיעדר מחלת כליות ברקע[24][25]. שינויים אלה יכולים להוביל לעיכוב בפינוי תרופות ולהצטברות מטבוליטים[26]
- המערכת הגסטרואינטסטינלית: שינויים בספיגה ובמטבוליזם של תרופות, בין היתר עקב אטרופיה של רירית הקיבה וירידה במהירות מעבר התרופה בוושט, מעי דק ומעי גס[27]
- תפקוד כבדי: עיכוב הפינוי הכבדי יכול להיגרם עקב סיבות פרה-הפטיות (לדוגמה ירידה בזרימת דם פורטאלית), אינטרה-הפטיות (לדוגמה בשחמת או עקב ירידה בתפקוד ציטוכרום 450P) ופוסט-הפטיות (משנית לפתולוגיה בדרכי מרה במערכת האנטרו-הפטית)[28]
עקרונות לטיפול באוכלוסייה הקשישה[29]
- שילוב טיפול לא תרופתי
- מתן אנלגטיקה "סביב השעון"
- במידת האפשר, העדפת טיפול מקומי טופיקלי
- לטיפול סיסטמי יש להעדיף מתן פומי או טרנסדרמלי
- שימוש ב"סולם כאב" הכולל:
- כאב קל - הבחירה הראשונה היא Paracetamol או Dipyrone
- כאב קל עד בינוני או כאב שלא התאזן תחת טיפול קו ראשון - NSAIDs בתנאי שאין התוויות נגד; ראה בהמשך ערך על NSAIDs
- לכאב עמיד לתוכנית הקודמת, או כאב חמור - אופיואידים
- ניתן לשלב תרופות אדג'ובנטיות (תכשירים נוגדי כאב נוירופתי) ליצירת סינרגיזם עם התרופות הקודמות
- בכאב עמיד או צורך בטיפול תרופתי ממושך - יש לשקול התערבות פולשנית אם ניתן
- ברוב המקרים, ישנה עדיפות לתרופות לא אופיואידיות לטיפול בכאב שאינו ממקור סרטני, עקב סבירות גבוהה לתופעות לוואי בחולים מבוגרים
- יש להתחיל במשככי כאבים במינון היעיל הנמוך ביותר, ולבצע טיטרציה כדי להשיג שליטה בכאב עם מינימום השפעות שליליות; הדבר מצריך הערכה תכופה של המטופלים עם התאמה של המינונים באופן תדיר
- שימוש מקומי בתרופות (כגון זריקות למפרקים או לשרירים) עשוי להיות עדיף על פני תרופות סיסטמיות (למשל משככי כאבים פומיים) כאשר הדבר אפשרי
- התכנית הטיפולית תמיד צריכה לכלול במקביל טיפולים לא פרמקולוגיים כדי לשפר את המצב התפקודי ולהפחית כאב, וכן על מנת למזער את מינוני התרופות
הגדרת מטרות הטיפול ותיאום ציפיות
לפני התחלת הטיפול חובה לתאם ציפיות ולהגדיר את מטרות הטיפול ביחד עם המטופל ובני משפחתו. חשוב להסביר כי כאב כרוני הוא מחלה כרונית לכל דבר, ניתן להפחית כאב כרוני אך לרוב לא ניתן להכחידו באופן מלא.
מטרת הטיפול המרכזית היא שיפור התפקוד, שיפור איכות השינה ומצב הרוח, ושיפור איכות החיים הכוללת.
טיפולים לא פרמקולוגים
אין להפחית בחשיבות הטיפול הלא פרמקולוגי בטיפול בכאב כרוני בקשישים, בעיקר כאשר מקור הכאב הוא MSK. הטיפול הלא פרמקולוגי כולל קשת רחבה של טיפולים כאשר שילוב של מספר התערבויות יעיל יותר מאשר גישה טיפולית אחת. הבחירה בטיפול היא אינדיבידואלית ותלויית מטופל, סוג הכאב, הגישה לטיפול, עלות והעדפות המטופל[30].
פעילות גופנית
בקווים המנחים קלינית של ארגון הרופאים האמריקאי AMERICAN COLLEGE OF PHYSICIANS לשנת 2017 יש המלצות על פעילות גופנית מובנית, יוגה, טאי צ'י, פעילות מוטורית מבוקרת, הרפייה ממושכת וכן ביופידבק[31]. גם פילאטיס והתעמלות במים הוכחו כמועילים. פעילות גופנית לא רק משפרת תפקוד אלא גם מפחיתה התנהגויות כאב כגון הימנעות ופחד מתנועה[32][33].
פעילות גופנית יכולה להתקיים במרכזים קהילתיים, בבית המטופל ואף באמצעות הנחיה מרחוק.
מתיחות- תרגילי מתיחות הוכחו כמשפרים תפקוד ומפחיתי כאב במטופלים הסובלים מכאבי גב כרוניים[34][35]. מתיחות מסייעות לשמור על טווחי התנועה. התרגילים יכולים להתחיל באופן סביל ולהתקדם בהמשך לאופן פעיל.
פיזיותרפיה וריפוי בעיסוק
טיפול פרטני פיזיותרפי או טיפול בריפוי בעיסוק צריך להיות מותאם למגבלות התפקודיות של המטופל, הסובל מכאב כרוני.
יש להתאים את הטיפול לרמת הכושר של המטופל באופן מדורג, על מנת למנוע החמרה בכאב, החמרה בתפקוד והפחתת נכונות המטופל להשתתף. הטיפול משפר את תפקוד המטופל וכן מפחית הימנעות ופחד מתנועה[36][37][38][39][40]. הוכח כבעל השפעה קלה עד בינונית מבחינת הכאב והמוגבלות, ובנוסף ישנו יתרון מסוים באיכות החיים, דיכאון וחרדה[41].
הטיפול הפיזיקלי ובכללו התאמת אביזרי עזר כגון הליכונים, סדים וכדומה חשוב גם כן לצורך שימור תפקודי.
פסיכולוגי
משלבים טיפול פסיכולוגי כאשר הכאב משפיע על מצב הרוח, השינה, איכות החיים, קשרים עם אחרים. הספרות תומכת במספר שיטות פסיכולוגיות לטיפול בכאב כרוני[42][43][44].
טיפול קוגניטיבי התנהגותי CBT COGNITIVE BEHAVIORAL THERAPY - הטיפול המומלץ והנחקר ביותר, נמצא יעיל כחלק מהגישה המולטידיסיפלינרית לטיפול בכאב[45][46].
בטיפול ה-CBT, המטופלים לומדים כיצד עלייה במודעות למחשבות יכולה להפחית את עוצמת הכאב תוך שימוש במספר גישות התנהגותיות לשינוי האינטראקציה עם הסביבה. ב-CBT ישנו שימוש בטכניקות הירגעות, pacing ותקשורת[47].
טיפולי גוף נפש - MIND BODY THERAPY MBT מגוון טיפולים להקלת כאב המשלבות מחשבה, רגשות, התנהגויות, תנועה ומודעות גופנית.MBT משלב CBT יחד עם גישות של MINDFULNESS להפחתת מתחים, לעיתים יש חפיפה בין השיטות, לדוגמה הרפייה, נשימות עמוקות ומדיטאציה[41].
רפואה משלימה
רפואה משלימה ואינטגרטיבית - COMPLEMENTARY AND INTEGRATIVE HEALTH THERAPIES CIH
יש ספרות התומכת ביעילות ובבטיחות. דוגמאות ל־CIH כוללות שילוב של MBT (לדוגמה שיטת MINDFULNESS להפחתת מתח, שיטות הרפייה, דמיון מודרך ביופידבק, מדיטציה) ושילוב של עיסוי. שיטות נוספות של CIH שפחות נחקרו הן REIKI, מגע טיפולי ושיטות הילינג וכן הומאופתיה. מרבית שיטות הרפואה המשלימה הן בטוחות ואינן גורמות לנזק.
טיפול בעל פוטנציאל מזיק הוא שימוש בצמחי מרפא עם פוטנציאל לרעילות, או אינטראקציות עם טיפולים אחרים, על כן יש להימנע משימוש בטיפול זה.
התערבויות תזונתיות - תזונה היא מרכיב עיקרי בהפחתת כאב ובשמירה על הבריאות והכושר, וכבר בביקור הראשון יש לתת המלצות לשינוי תזונתי בריא[48][49].
דיקור - אקופונקטורה - בשימוש נרחב מזה שנים. המלצת ארגון הרופאים האמריקאים AMERICAN COLLEGE OF PHYSICIANS היא שאקופונקטורה צריכה להיות בין האפשרויות הטיפוליות הלא תרופתיות הראשונות למטופלים עם כאב גב תחתון כרוני[34].
שימוש ב־TENS
TRANSCUTANEOUS ELECTRICAL NERVE STIMULATION שימוש באנרגיה חשמלית המועברת דרך העור, תוך אפשרות לשליטה על הגל, תדירות ועצמה. מדובר בטיפול נפוץ היכול להינתן ללא פיקוח רפואי. הספרות התומכת מאוד דלה, והעדויות אינן חד-משמעיות[50][51][52][53].
טיפולים פרמקולוגים
ישנו מיעוט מידע בספרות המקצועית באשר ליעילות ובטיחות הטיפול התרופתי נוגד כאב בקשישים. נוסף על כך בגיל המבוגר מתן טיפול תרופתי נוגד כאב אינו חף מסיכונים. תרופות לשיכוך כאב עשויות להשפיע על מצבו הקוגניטיבי, הפיזיולוגי והתפקודי של המטופל.
לאור הנזכר למעלה קשישים רבים אינם מטופלים כראוי כנגד כאב. ההשלכות הגופניות והנפשיות המשמעותיות של היעדר טיפול נדונו בתחילת מסמך זה.
בבואנו להחליט על הטיפול הטוב ביותר עבור המטופל הקשיש, מה שעומד בבסיס ההחלטה הטיפולית הם שיקולי סיכון-תועלת, תוך התחשבות בפרופיל הבטיחות של כל תכשיר והבנה מעמיקה אודות תופעות הלוואי האפשריות, כאשר הנקודה העיקרית היא קודם כל לא להסב נזק.
אי לכך, מפורטות כאן המלצותינו באשר לטיפול התרופתי נוגד כאב בקשישים, בהתבסס על הספרות הקיימת וניסיונם הקליני של כותבי מסמך זה.
האיגוד הגריאטרי האמריקאי וארגון הבריאות העולמי (WHO - World Health Organization) גיבשו הסכמה לגבי הגישה הטובה לטיפול בכאב כרוני בקשישים[54] והנחיות מפורטות הופצו על ידי האיגוד הגריאטרי האמריקאי (AGS), ועודכנו בשנת 2023[55].
משככי כאב לא אופיואידים
Paracetamol
Paracetamol הוא קו ראשון לכאב כרוני קל-בינוני במבוגרים בשל פרופיל הבטיחות הגבוה שלו בהשוואה למשככי כאבים אחרים. יעיל במיוחד בכאבי שריר שלד[54]. המינון המומלץ הוא פחות מ-4 גרם ליום. יש להפחית מינון ב-50–75 אחוזים למטופלים עם הפרעה בתפקוד כבדי ואלה הצורכים אלכוהול על בסיס קבוע, או בתת-תזונה כאשר המטופל שוקל פחות מ-50 קילוגרם[56].
- התוויות נגד מוחלטות: אי-ספיקת כבד מתקדמת
- התוויות נגד ואזהרות יחסית: אי-ספיקת כבד, שימוש כרוני באלכוהול או תלות
- אין לחרוג מהמינון היומי המומלץ המקסימלי ויש לכלול "מקורות נסתרים" כגון תרופות המשלבות בתוכן Zaldiar, Percocet, Paracetamol וכדומה
(Optalgin) Dipyrone
Optalgin המכילה את החומר הפעיל Dipyrone (אשר קרוי גם metamizole) מהווה את אחת התרופות הפופולריות לשיכוך כאבים בישראל. התרופה משפיעה גם על הורדת חום והפחתת פעילות דלקתית.
הוכחה כיעילה למגוון הפרעות כאב, לרבות כאב לאחר ניתוח, והפחתת פעילות דלקתית מוגברת.
כאשר התכשיר נרשם לטיפול קצר מועד, אין צורך בהתאמת מינון. המינון המקובל הוא עד 4 גרם ביממה, ובקשישים ייתכן שמומלץ לא לחרוג מ-3 גרם ביממה. בטיפול הנועד לטווח ארוך, בקשישים הסובלים מירידה ב-GFR וכן במצבי שחמת, מומלץ להפחית מינון, מאחר שבאוכלוסיות אלה קצב פינוי התרופה עלול להתארך במידה מסוימת[57]. אין מספיק מידע/המלצות לגבי המינון המומלץ ולגבי מה נחשב טיפול ממושך ב-Dipyrone.
ישנם מחקרים שהראו כי Dipyrone עשוי להיות הפטוטוקסי[58]. כאשר ניתן ביחד עם אספירין או NSAIDs ובמינונים גבוהים ולאורך זמן, עלול במקרים נדירים לגרום לאי ספיקת כליות או לדימומי GI. נוסף על כך, Dipyrone עלולה לגרום לאגרנולוציטוזיס באופן אידיוסינקרטי.
מבחינה פרמקוקינטית, מצטברות ראיות המעידות שהתכשיר בעל אפקט משפעל של חלק מאנזמי ה-CYP, ובפרט CYP3A4. בעוד שהמשמעות הקלינית של אינטראקציה פרמקוקינטית זו אינה ידועה דיה, מומלץ להתייעץ עם פרמקולוג קליני במקרים בהם מתוכנן טיפול ממושך[59][60].
NSAIDs
NSAIDs יעילים בטיפול בכאב כרוני קל עד בינוני, במיוחד במצבים עם מרכיב דלקתי.
האיגוד הגריאטרי האמריקאי ממליץ לנקוט משנה זהירות בעת שימוש בטיפול ב-NSAIDs בקשישים בשל תופעות הלוואי הפוטנציאליות על מערכת העיכול, הכליות והמערכת הקרדיווסקולרית. נמצא כי כ-24 אחוזים מהקשישים שאושפזו כתוצאה מתופעות לוואי תרופתיות אושפזו כתוצאה מנטילת NSAIDs.
במטופלים נבחרים ניתן לתת NSAIDs, רצוי לפרקי זמן קצרים בלבד במהלך התלקחויות אפיזודיות.
NSAIDs לא סלקטיביים ומעכבי COX-2 (cyclooxygenase) סלקטיביים יכולים להוות קו טיפולי באוכלוסיות נבחרות[54].
- בחירת מטופל: כאשר טיפולים אחרים (בטוחים יותר) נכשלו, ולאחר שבוצעה הערכה מקיפה של תועלת מול פוטנציאל נזק. ההחלטה הכוללת בעניין מתן NSAIDs לכאב כרוני אצל קשישים חייבת להיות מותאמת אישית על בסיס מחלות נלוות וגורמי סיכון אחרים
- התוויות נגד מוחלטות: כיב פפטי פעיל, מחלת כליות כרונית, אי-ספיקת לב
- התוויות נגד ואזהרות יחסיות: יתר לחץ דם, הליקובקטר פילורי, היסטוריה של כיב פפטי, שימוש מקביל בקורטיקוסטרואידים, אנטיאגרגנטים או אנטיקואגולציה, או SSRIs
- הנחיות לטיפול[54]
- אנשים מבוגרים הנוטלים NSAIDs לא סלקטיביים צריכים להשתמש במעכב משאבת פרוטון או ב-Misoprostol להגנה על מערכת העיכול
- חולים הנוטלים מעכב סלקטיבי COX-2 עם Aspirin צריכים להשתמש במעכב משאבת פרוטון או ב-Misoprostol להגנה על מערכת העיכול
- אין לצרוך יותר מ-NSAID אחד במקביל לשליטה בכאב
- מתן בו-זמנית של כל אחד מהסוגים של NSAIDs עם Aspirin, ובמיוחד Ibuprofen, עלול לשלול את ההשפעות המגנות על הלב של Aspirin במינון נמוך
- חולים הנוטלים NSAIDs צריכים להיבדק באופן שגרתי לגבי רעילות במערכת העיכול והכליות, יתר לחץ דם, אי-ספיקת לב ואינטראקציות אחרות בין תרופתיות
- מבחינת פרופיל בטיחות קרדיווסקולרי - ייתכן ש-Naproxen בטוח יותר בהשוואה ל-NSAIDs אחרים. Diclofenac נחשב כבעל סיכון גבוה
לפי ה-BEERS CRITERIA יש להימנע משימוש ב-Ketorolac וב-Indomethacin בקשישים[55].
טיפולים טופיקליים
NSAIDs
טיפול מקומי ב-NSAIDs מהווה חלופה חשובה ל-NSAIDs דרך הפה[54].
תכשירים אלו עשויים לשמש עבור חולים עם דלקת מפרקים מקומית של מפרקים שטחיים (כגון יד ושורש כף היד, כף הרגל והקרסול, או הברך), עם פוטנציאל להשגת רמות טיפוליות של תרופה ברקמה הסינוביאלית, עם ספיגה סיסטמית נמוכה יותר לעומת טיפול פומי. טיפול מקומי עשוי להתאים גם במצבי כאב שרירי ממוקד.
קיימים מספר תכשירים של NSAIDs עבור אוסטאוארתריטיס: לדוגמה, 1 אחוז Diclofenac sodium ג'ל (1 אחוז Voltaren emulgel), או במדבקה Dicloplast. עם זאת, גם במתן טופיקלי, Diclofenac נספג ברמה מסוימת לזרם הדם ובשימוש חוזר/מרובה יכול לגרום לאי-ספיקת כליות חריפה.
Capsaicin
Capsaicin הוא נגזרת אלקלואידית פעילה ממשפחת הפלפלים (capsicum) הפועלת על ידי הפחתת החומר P, אשר מפעיל סיבים נוציספטיביים עוריים. טיפול זה עשוי לשמש עבור כאבים נוירופתיים וכאבי שרירים ושלד, אך בעיקר כמשכך כאב אדג'ובנטי. החיסרון הגדול של טיפול זה הוא תחושת צריבה מקומית בעת מריחת התכשיר בימים הראשונים לטיפול. ניתן להתגבר על כך על ידי שימוש בריכוז נמוך של Capsaicin מספר פעמים ביום או בריכוז גבוה פעם אחת כדי לבטל את הרגישות של אזור המריחה.
בישראל זמינים רק שני ריכוזים: 0.075 אחוזים עבור כאב נוירופתי ו-0.025 אחוזים עבור כאבי פרקים, הניתנים עד ארבע פעמים ביום. בארצות הברית, מנהל המזון והתרופות (FDA) אישר מדבקת Qutenza (Capsaicin) בריכוז גבוה של 8 אחוזים לכאב נוירופתי, שיכול לספק הקלה בכאב עד 12 שבועות לאחר שימוש בודד של 60 דקות. יש להיזהר מתופעות "דמויות כווייה" במריחות חוזרות[29][61]. תכשיר זה אינו זמין בישראל נכון למועד כתיבת נייר עמדה זה.
טופיקלי Lidocaine
Lidocaine זמין בפורמולציות שונות של קרם, תרסיס וכמדבקות. השימוש היחיד המאושר על ידי ה-FDA הוא 5 אחוזים Lidocaine שנועד לנוירלגיה פוסט-הרפטית. השימוש הוא למשך 12 שעות באופן יום-יומי. תופעת לוואי אפשרית היא רק גירוי קל בעור. טיפול זה יכול לשמש עבור מצבי כאב נוירופתיים אחרים (כגון diabetic polyneuropathy)[29].
אופיואידים
הנחיות כלליות:
- הנחיות ה-CDC שפורסמו ב-2016, כמו גם נייר העמדה של ההסתדרות הרפואית הישראלית "טיפול באופיואידים בכאב כרוני ממקור לא סרטני" שפורסם ב-2016, קובעות שאין להשתמש באופיואידים לטיפול קו ראשון או שגרתי בכאב כרוני, מלבד במקרים של סרטן פעיל, טיפול פליאטיבי וסוף החיים, ויש להשתמש בו רק כאשר התועלת עולה על הסיכונים[62]
- מומלץ לבצע טיטרציה של מינון באיטיות ובזהירות במבוגרים[63]. יש להשתמש במינון האפקטיבי הנמוך ביותר, עם הערכה מחודשת מעת לעת של תועלת אל מול סיכון
- בעת מתן אופיואידים בקשישים יש לנקוט בגישת "start low, go slow"[64]. יש להתחיל במינון של 25-50 אחוזים מהמינון המומלץ למבוגרים צעירים. לדוגמה, מינון התחלתי פומי טיפוסי של Morphine או Oxycodone באדם צעיר הוא 5-10 מיליגרם, ואילו בקשישים המינון ההתחלתי המומלץ הוא 2.5-5 מיליגרם. הזמן להשגת רמת שיא בפלזמה של תכשירים פומיים בשחרור מהיר הוא כ-30 דקות ונמשך כ-3-4 שעות. בקשישים מומלץ מרווח של 6-8 שעות בין המנות בתחילת הטיפול. רק לאחר השגת steady state (סביב 4–5 מחציות חיים של התכשיר) יש לשקול עליית מינון
- בתחילת הטיפול יש להשתמש בתכשירים בשחרור מיידי ורק בהמשך לעבור לתכשירים בשחרור מושהה או לטווח ארוך
- תופעות הלוואי של אופיואידים כגון בחילות, נמנום וסחרחורת, סיכון מוגבר לנפילות, דיכוי נשימתי, הן תופעות קצרות טווח אשר צפויות לחלוף תוך מספר ימים מהתחלת השימוש בתרופה. סיכון לאצירת שתן ועצירות - תופעות שקיימות לאורך זמן. כמו כן, עלייה ב-All cause mortality בשימוש ממושך באופיואידים. בעת התחלת שימוש באופיואידים יש לשקול טיפול מניעתי לעצירות
- דיכוי נשימתי נובע בדר"כ כתוצאה מעלייה מהירה מדי במינון, או משימוש מקביל בתרופות המדכאות CNS כגון בנזודיאזפינים ואלכוהול. יש לנקוט משנה זהירות בעת שימוש באופיואידים במקביל לתרופות מדכאות CNS
- יש לטפל באופיואיד מסוג אחד לפי מאפייני המטופל בדגש על תפקוד כלייתי וכבדי. אין יתרון במתן משלב של סוגי אופיואידים שונים
- במטופלים עם כאב רציף יש לתת טיפול "סביב השעון", באמצעות אופיואידים בשחרור מושהה כטיפול "בזאלי" ולהוסיף טיפול בשחרור מהיר כמנות הצלה "בולוס" למקרי כאב מתפרץ
- יש לבצע הערכה רפואית וניטור הדוק במטופלים הנוטלים משככי כאבים אופיואידים לצורך השגה מתמשכת של מטרות טיפוליות (בדגש על יעדים תפקודיים ומדדי שיפור איכות חיים), ניטור תופעות לוואי ושימוש בטוח ואחראי בתרופות
אופיואידים חלשים
Tramadol[65][66]
Tramadol מאושר לטיפול בכאב בינוני עד חמור במבוגרים. יעיל למספר סוגי כאב, כולל כאב לאחר ניתוח, דלקת מפרקים ניוונית, פיברומיאלגיה וסרטן. כמו כן, ישנה ראיה מדעית ליעילותו בטיפול בכאב נוירופתי.
משכך כאבים אופיואידי סינתטי ו-SNRI (מעכב ספיגה חוזרת של סרוטונין/נוראפינפרין). בשל פרופיל הסבילות הטוב שלה ומנגנון הפעולה הרב-מודאלי שלה, Tramadol נחשבת בדרך כלל כאופציה אופיואידית בעלת סיכון נמוך יותר לטיפול בכאב בינוני עד חמור.
עם זאת, במטופלים בני 75 שנים ויותר: ישנה ירידה בקצב פינוי התרופה. יתר על כן, מדובר בתכשיר העובר מטבוליזם על ידי CYP2D6 הנתון לשונות אינדיבידואלית משמעותית, כך שחלק מהמטופלים עשויים להדגים ריכוזי מטבוליט פעיל נמוכים, ואחרים גבוהים מהצפוי. על כן, ייתכן ותהיינה תופעות לוואי רבות יותר מאשר במטופלים צעירים. במקביל, ייתכן שתהיה אפקטיביות במינונים נמוכים מהרגיל[67]. אם בוחרים להשתמש בה, יש לתת מינון התחלתי נמוך ולעקוב קלינית.
יש להבדיל בין התכשירים בעלי השחרור המיידי (IR) לבין השחרור המושהה (ER): באופן עקרוני מומלץ לרשום תכשירים בעלי שחרור מיידי. במטופלים עם GFR מתחת ל-30, מומלץ לתת תכשיר בעל שחרור מיידי ובטווחים של מינימום 12 שעות ולהימנע ממתן פורמולציית ה-ER. ניתן לשקול מתן Zaldiar, תכשיר משולב עם Paracetamol המכיל מינון מופחת של Tramadol. ב-GFR מתחת ל-10 קונטרהאינדיקציה מוחלטת לטיפול ב-Tramadol.
בדומה לתרופות אופיואידיות אחרות, Tramadol מהווה סיכון להתפתחות סבילות ותלות. תופעות לוואי ייחודיות ונדירות לתכשיר זה הן התפתחות תסמונת סרוטונין, היפונתרמיה וכן פרכוסים, כאשר במרבית המקרים שדווחו החולים נטלו מינון גבוה מהמומלץ או נטלו שילוב של תרופות[68].
אינטראקציות בין תרופתיות במנגנון פרמקוקינטי: מדובר ב-Prodrug כך שהתכשיר חייב שפעול על ידי CYP2D6. לפיכך, תכשירים המעכבים את אותו CYP יובילו לריכוזים נמוכים יותר של המטבוליט הפעיל, כדוגמת Paroxetine ו-Fluoxetine. מאידך, תכשירים המעכבים את CYP3A4 עלולים להוביל לריכוזי מטבוליט פעיל גבוהים מהצפוי (Clarithromycin, Ketoconazole).
Codeine
Codeine הוא תכשיר העובר מטבוליזם על ידי CYP2D6 הנתון לשונות אינדיבידואלית משמעותית, כך שחלק מהמטופלים עשויים להדגים ריכוזי מטבוליט פעיל נמוכים, ואחרים גבוהים מהצפוי.
אי לכך, יש להיזהר עם השימוש בתכשיר זה בקשישים, במיוחד מעל גיל 85, ובייחוד במשלב של תרופות נוספות כגון בנזודיאזפינים. אם בכל זאת הוחלט על טיפול זה, יש לתת במינונים נמוכים ולא בשילוב עם תרופות סדטיביות אחרות ככל האפשר[69].
בשל הנזכר למעלה, בניגוד להמלצות מעלית הכאב של ה-WHO לטיפול באופיואידים חלשים בכאב בינוני, כותבי נייר עמדה זה ממליצים להשתמש באופיואידים חזקים יותר (במינון נמוך) גם בכאב בינוני, באם קווי הטיפול הקודמים נכשלו, היות שבקשישים אופיואידים חזקים במינונים נמוכים יספקו שיכוך כאב יותר הולם ועם פחות תופעות לוואי לעומת אופיואידים חלשים. כאמור, יש להתחיל במינון הנמוך בכ-50 אחוזים מהמינון ההתחלתי בצעירים, עם אינטרוולים גדולים יותר ותוך מעקב הדוק.
אופיואידים חזקים
Oxycodone
בעת התחלת טיפול, שימוש בתמיסה הוא עדיף מבין צורות המתן הן בשל היכולת לבצע טיטרציה במינונים קטנים והן בחולים עם קשיי בליעה. במצבי אי ספיקת כליות דרושה התאמת מינון[70]. בנוסף ישנם תכשירים בשחרור מושהה Oxycontin ו-Targin (המכיל גם Naloxone) לצורך טיפול בכאב רציף.
Morphine
תמיסת Oramorph עדיפה הן בשל היכולת לבצע טיטרציה במינונים קטנים והן בחולים עם קשיי בליעה. במטופלי אי-ספיקת כליות יש צורך בהפחתת המינון וריווח תדירות המתן שכן לתכשיר מטבוליט פעיל, פוטנטי, המתפנה כלייתית. להימנע ממתן במטופלים הסובלים מאי ספיקת כליות מתקדמת. יש להתאים מינון במחלה כבדית[70]. ישנם תכשירים בשחרור מושהה MCR, MST לצורך טיפול בכאב רציף.
Transdermal Buprenorphine - Butrans
Buprenorphine טרנס-דרמלי הוא בעל משך פעולה ארוך (תחילת השפעה בחלוף 12–24 שעות, משך פעולה של 7 ימים), וכן הוא אופיואיד ייחודי במנגנון הפעולה שלו. Buprenorphine הוא אגוניסט חלקי של רצפטור μ וכן אנטגוניסט של רצפטורי k ו-δ. לאור זאת הוא בעל פרופיל בטיחות טוב יותר לעומת אופיואידים שהם אגוניסטים מלאים של רצפטור μ, מכיוון שישנו אפקט תקרה לתופעת הלוואי של דיכוי נשימתי וכן פחות שימוש לרעה. Buprenorphine[71] הוא מועדף במיוחד בקשישים מאחר שבהשוואה לאופיואידים אחרים, הוא גורם פחות לפגיעה קוגניטיבית, לנפילות ולסרקופניה, וכן הוא בטוח לשימוש באי-ספיקת כליות ובאי-ספיקה כבדית. נוסף על כך תכשיר זה מייצר פחות אינטראקציות עם תרופות אחרות וגם בכך מהווה יתרון בשימוש בגיל המבוגר[72][73][74][75].
Fentanyl
Fentanyl הוא אופיואיד סינתטי הנחשב פוטנטי פי 100 מ-Morphine[76], אינו מתאים לשימוש בחולים נאיבים לאופיואידים. מותר באי ספיקת כליות. התכשירים קצרי הטווח (כגון Abstral, Fentora) רשומים בארץ לחולים אונקולוגים בלבד ולא לכאב כרוני.
Methadone
Methadone היא תרופה אפשרית לשימוש בחולים שאינם נאיבים לאופיואידים, אך בשל תופעות הלוואי הפוטנציאליות בעת תחילת הטיפול תינתן רק על ידי מומחה כאב עם ניסיון בטיפול ב־Methadone. מותר באי ספיקת כליות.
סיכון מוגבר להארכת מקטע QTC והפרעות קצב חדריות מסכנות חיים[70][56]; לפיכך יש צורך בביצוע אקילוגרם טרם תחילת הטיפול ומעקב לאחר הטיפול (למשל: ביצוע אקילוגרם כשבוע לאחר התחלתו, אחת לחודש במהלך הטיפול ולאחר הוספת תכשירים המאריכים מקטע QT).
עקב זמן מחצית חיים ארוך מאוד יש לשקול עלייה במינון לאחר 5 ימי טיפול לפחות ולא מוקדם יותר מסיכון למנת יתר ודיכוי נשימתי.
(Meperidine) Pethidine
בשל סיכון מוגבר לדליריום ולנוירוטוקסיסיטי Pethidine אינה מתאימה לשימוש בקשישים לפי ה-BEERS CRITERIA[55]
תרופות לכאב נוירופתי
הנחיות כלליות:
בדומה לטיפול באופיואידים, גם בקבוצת תרופות זו יש לבצע טיטרציה של מינון באיטיות ובזהירות במבוגרים תוך מתן מינון התחלתי הנמוך בכ-50 אחוזים מהמינון ההתחלתי בצעירים. להתחיל בכל פעם תרופה אחת בלבד, להשתמש במינון האפקטיבי הנמוך ביותר, ולבצע הערכה מחודשת מעת לעת של תועלת אל מול סיכון.
נוגדי פרכוס[29]
Pregabalin ו-Gabapentin
הקו הראשון לטיפול בכאב נוירופתי בקשישים. מומלץ לקחת Gabapentin ו-Pregabalin בקורסים קצרים (שניים עד ארבעה חודשים) עבור סוגים מסוימים של כאב נוירופתי כולל נוירופתיה סוכרתית. יש לבצע טיטרציה קפדנית של מינון Gabapentin החל מ-100–300 מיליגרם מדי יום, ושל Pregabalin החל מ־25 מיליגרם ליום.
מדובר בתכשירים שברובם מתפנים כלייתית כך שיש צורך בהתאמת המינון במבוגרים עם אי-ספיקת כליות. תופעות הלוואי השכיחות ביותר של gabapentinoids הן סחרחורת, נמנום, עייפות ושינויים במשקל. נתונים חדשים מ־FDA Adverse Event Reporting System מצביעים על כך שלתרופות אלו עלולות להיות השפעות נוספות של דיכוי נשימתי בשימוש עם תרופות אחרות שמדכאות את מערכת העצבים המרכזית, כולל אופיואידים. כמו כן תרופות אלה עשויות לגרום להתמכרות באנשים עם נטייה להתמכרות ולהחמרת תסמיני פרקינסוניזם במטופלי פרקינסון שאינם מאוזנים.
Carbamazepine/ Oxcarbazepine - חסמי תעלות נתרן
Carbamazepine היא חסם תעלות נתרן המוכח בטיפול בכאב עצבי, ההתוויה המרכזית שלו היא נוירלגיה טריגמינלית. לאור פעילותה המשפעלת על קבוצת אנזימי הכבד CYP היא עלולה לגרום למגוון אינטראקציות בין תרופתיות, ומכאן שבקשישים ובמיוחד במצבי פוליפרמסי יש לנקוט משנה זהירות. נוסף על כך הנזכרת למעלה משפיעה על התפקוד הכבדי, על התפקוד הכלייתי וגם עלולה לגרום לרעילות המטולוגית משמעותית. כמו כן עשויה לגרום להיפונתרמיה ובשימוש ממושך לאוסתאופורוזיס. Trileptin) Oxcarbazepine) גורמת לפחות תופעות לוואי ונסבלת טוב יותר באוכלוסייה הקשישה. יש לבצע טיטרציה זהירה, להתחיל במינון של 150 מיליגרם פעמיים ביום ולעלות באיטיות.
אינטראקציות בין תרופתיות: מדובר בתכשיר הנחשב משפעל חזק של CYP3A4 ומשפעל בינוני של CYP2B6. לפיכך, תכשירים העוברים מטבוליזם על ידי אנזימים אלו חשופים לאינטראקציה משמעותיות. במרבית המקרים התוצאה תהייה ריכוזים נמוכים של התכשיר המושפע, כך שצפויה ירידה ביעילותו (פרט ל־prodrugs). בהקשר זה יובהר כי מתן Carbamazepine יחד עם Apixaban, Rivaroxaban) DOACs או Dabigatran) נחשב כהתווית נגד מוחלטת[77].
Lamotrigine
Lamotrigine היא תרופה בטוחה יותר לשימוש בקשישים, אך עם יעילות מופחתת. קצב פינוי התכשיר במבוגרים איטי בכ-20 אחוזים. תופעת הלוואי הנפוצה היא עורית עם הופעת פריחה אשר במקרים נדירים יכולה להגיע לכדי Stevens-Johnson syndrome. ניתן להפחית את הסיכון על ידי ביצוע טיטרציה איטית וזהירה במינוני התרופה. מתחילים במינון 25 מיליגרם פעם ביום[70][78][79].
נוגדי דיכאון
(Serotonin-Norepinephrine Reuptake Inhibitors) SNRI
SNRIs כגון Duloxetine, Venlafaxine ו-Milnacipran יכולות לשמש לכאב נוירופתי אצל קשישים. SNRIs בדרך כלל נסבלים היטב אבל תופעות הלוואי כוללות היפונתרמיה, סחרחורת, בחילות וכאבי בטן. עשויות להגביר לחץ תוך-עיני במטופלים עם גלאוקומה מסוג זווית סגורה.
השימוש ב-Venlafaxine בקשישים שנוי במחלוקת, מאחר שמספר מחקרים הראו כי עלול לגרום לעלייה משמעותית של לחץ הדם.
קשישים רבים מטופלים באופן קבוע ב-SSRI (Selective Serotonin Reuptake Inhibitor). במקרים אלה, ניתן לשקול להמיר את הטיפול ל־SNRI כדי להשיג השפעות משככות כאב ואנטי-דיכאוניות באמצעות תרופה בודדת, ובכך לפשט את הטיפול התרופתי באוכלוסייה הקשישה ולהמעיט את הסיכון הכרוך בפוליפרמסי[29][26].
תרופות נוגדות דיכאון טריציקליות (TCA)
תרופות נוגדות דיכאון טריציקליות כגון Amitriptyline, Desipramine, ו-Nortriptylin, הן בעלות השפעות אנטיכולינרגיות, נוראדרנרגיות ואף עשויות לגרום להארכת QTc, על כן הן לא מומלצות לשימוש בקשישים[29].
| משפחה | שם גנרי | שמות מסחריים | מינון יומי התחלתי (מיליגרם) | מינון יומי מקובל (מיליגרם) | מספר מנות מקסימלי ליום | אינטראקציות | התאמת מינון |
|---|---|---|---|---|---|---|---|
| Paracetamol | 3 גרם | 3 | להיזהר ממתן עם Warfarin | שחמת, תת-משקל | |||
| Dipyrone | 3 גרם | 3 | NSAIDS
Aspirin |
ייתכן שיש להפחית מינון במצבי אי ספיקת כליות או כבד | |||
| NSAIDS | COX NON
SELECTIVE |
ישנן התוויות נגד, ראה מעלה. המינון היעיל הנמוך ביותר לפרק הזמן הקצר ביותר | |||||
| COX 2 SELECTIVE | Celcox
Arcoxia |
100 מיליגרם
30 מיליגרם |
עד 200 מיליגרם עד 120 מיליגרם | 2
1 |
|||
| נוגדי פרכוס, חסמי תעלות סידן | Gabapentin ,Pregabalin | 100 מיליגרם 25 מיליגרם | עד 3600 מיליגרם עד 600 מיליגרם | 3 2 | זהירות בעת שימוש במקביל בתרופות סדטיביות- BNZ, אופיואידים | אי ספיקת כליות אי ספיקת כליות | |
| נוגדי דיכאון SNRI | Duloxetine Venlafaxine, Milnacipran | 30 מיליגרם
37.5 מיליגרם 12.5 מיליגרם |
60 מיליגרם
225 מיליגרם 200 מיליגרם |
1
1 2 |
תסמונת סרוטונין | אי ספיקה כבדית
אי ספיקת כליות אי ספיקת כליות | |
| נוגדי דיכאון טריציקלים | ,Amitriptyline ,Desipramine Nortriptylin | להימנע משימוש. | |||||
| חסמי תעלות נתרן | Carbamazepine, Oxcarbazepine | 150 מיליגרם פעמיים ביום
25 מיליגרם פעם ביום |
1200-1800 מיליגרם ליממה 400 מיליגרם ביממה | 2
2 |
אסורה לשימוש במקביל לתכשירים אנטיקוא-גולנטים | ||
| אופיואידים | Tramadol | 25 מיליגרם
1-3 פעמים ביום |
300 מיליגרם ביממה | 3 | עדיף שימוש בפורמולה קצרת טווח, מינון נמוך. לדוגמה להעדיף
.Zaldiar |
||
| Codeine | 15-30 מיליגרם | 180 מיליגרם ביממה | 3 | עדיף להימנע משימוש. | אי ספיקת כליות אי ספיקה כבדית | ||
| Buprenorphine | Butrans | 5 מיקרוגרם לשעה | 20 מיקרוגרם לשעה | מדבקה אחת ל-7 ימים | אי ספיקה כבדית | ||
| Oxycodone | 2.5 מיליגרם IR 5 מיליגרם ER | 4 2 | אי ספיקת כליות וכבד | ||||
| Morphine | 5 מיליגרם IR 10 מיליגרם ER | 4 2 | אי ספיקת כליות וכבד | ||||
| Fentanyl | טרנסדרמלי | 12.5 מיקרוגרם לשעה | לא במטופל נאיבי. | ||||
| Methadone | יינתן על ידי מומחה בלבד | ||||||
| Pethidine | להימנע משימוש. |
IR- immediate release, ER- extended release
קלציטונין וביספוספונטים
קלציטונין עשוי להקל על כאבים הנובעים משברי דחיסת חוליות אוסתאופורוטיות ושברים באגן וכן ובחולי סרטן עם גרורות בעצמות[29]. המנגנון שבו קלציטונין מקל על כאב אינו ידוע. השימוש בו הולם במקרים של כאב אקוטי לאחר שבר, לתקופה קצרה של עד 6 שבועות בלבד.
תופעות הלוואי העיקריות של קלציטונין הן תגובת רגישות יתר, בחילות ושינוי ברמות הסידן והזרחן בסרום, לכן מומלץ להעריך את רמות הסידן והזרחן.
ביספוספונטים כגון Pamidronate ו-Clodronate[29] עשויים גם כן לספק שיכוך כאב בחולים עם סרטן גרורתי לשלד, במיוחד בסרטן השד, הערמונית או מיאלומה נפוצה. תופעות הלוואי של ביספוספונטים קשורות בדרך כלל לבחילות, דלקת בוושט או היפוקלצמיה.
קנאביס
כאב כרוני הוא האינדיקציה השכיחה ביותר לרישום קנאביס רפואי, אולם יעילות הקנאביס כתרופה לכאב כרוני עדיין שנוייה במחלוקת[80][81]. ישנן ראיות התומכות בשימוש בקנאביס רפואי כתוספת או כתחליף לטיפול אנלגטי קונבנציונלי בטיפול בכאב כרוני, כדי להפחית מצב של ריבוי תרופות או כדי להימנע מתופעות לוואי של טיפול אנלגטי[1][82][83][84][85][86]. עם זאת בכל המחקרים הגדולים שבוצעו להערכת טיפול בקנאביס לאיזון כאב, כמות הקשישים אשר נכללו בקריטריוני ההכללה הייתה קטנה או שהם לא נבחנו בנפרד מבחינת בטיחות ויעילות[87][81] ויש להמשיך לחקור וללמוד את הנושא.
במחקר שבוצע על ידי י. אבירם וד. מאירי הודגמו שיפור באיכות החיים והפחתה בשיעורי צריכת תרופות לשיכוך כאב הודות לטיפול בקנאביס רפואי[85]. מספר עבודות הוכיחו כי השילוב בין אופיואידים לבין קנבינואידים תורם להעצמת ההשפעה האנטי-נוציספטיבית[88]. קנבינואידים ואופיואידים חולקים מספר תכונות פרמקולוגיות ועשויים לפעול באופן סינרגיסטי[89][90][91], אשר יביאו להקלה מצטברת בכאב, הפחתה בצריכת תרופות אופיואידיות, הפחתה בשיעור תופעות הלוואי שלהן, הפחתה בסבילות לטיפול (TOLERANCE) ושיפור בשיעורי גמילה מאופיואידים[92][93].
במחקר נוסף שבוצע על ידי אברמס וחבר' נצפה כי קנאביס באידוי מגביר את ההשפעות משככות הכאב של אופיואידים מבלי לשנות משמעותית את רמתם בפלזמה. השילוב עשוי לאפשר טיפול באופיואידים במינונים נמוכים יותר עם פחות תופעות לוואי[89].
ההתוויות לשימוש בקנאביס רפואי על פי נוהל 106 של משרד הבריאות, בהקשר של כאב כרוני, הן[94]
- כאב ממקור אונקולוגי (במטופלים עם מחלה אונקולוגית פעילה/בעת טיפול אנטינאופלסטי פעיל לצורך הקלה בתסמיני המחלה הפעילה או בתופעות הלוואי של הטיפול הפעיל)
- כאב ממקור גסטרואינטסטינלי במטופלים עם IBD
- כאב נוירופתי
- כאב ממקור נוירולוגי (למטופלים המאובחנים בטרשת נפוצה במצבים ספסטיים, או למטופלים המאובחנים בפרקינסון הסובלים מכאב כרוני או כאב הנגרם מהריגידיות)
- כאב בחולים סופניים
אינדיקציה נוספת לטיפול בקנאביס רפואי בקשישים היא דמנציה המלווה בהפרעות התנהגות[95].
תופעות הלוואי של קנאביס
יש לקחת בחשבון כי בזקנה יש שינויים משמעותיים מבחינה פרמקודינמית ופרמקוקינטית, הגורמים לעליית זמן מחצית החיים של הקנבינואידים ולעלייה בנפח הפיזור של קנבינואידים[96][97].
- תופעות לוואי פיזיולוגיות כגון סחרחורות, ירידה בלחץ הדם, טכיקרדיה, פלפיטציות, ירידה בערכי סוכר, עייפות, חוסר יציבות, וכן תופעות קוגניטיביות כגון בלבול, חשובות במיוחד בקשישים הסובלים מדמנציה, מהפרעות תנועה, מנפילות חוזרות, או מלקויות ראייה או שמיעה[98][99][93]. תופעות אלו חולפות בדרך כלל זמן קצר לאחר הסתגלות למוצר. במתן אוראלי תופעות הלוואי עלולות להימשך עד 72 שעות לאחר נטילת המוצר
- השפעה ארוכת-טווח על הקוגניציה בקשישים אינה ברורה. בוצעו שתי עבודות אשר הדגימו קשר בין שימוש ארוך-טווח בקנאביס רפואי לבין השפעה שלילית על תפקודים קוגניטיביים מסוימים, אך השפעה חלשה לטווח הרחוק. ייתכן ושימוש קבוע בכמויות גבוהות עלול להוביל לפגיעה ביכולות הקוגניטיביות[100][99][101][102][103], ובמקרים מסוימים, אצל אנשים בעלי נטייה מוקדמת, לגרום להתפרצות זמנית של מצבים פסיכוטיים או חרדות[94][104]
- בקשישים נתאים את אופן, ריכוז ותדירות השימוש למצב התפקודי והקוגניטיבי של המטופלים[105]
בחינת הטיפול בקנאביס רפואי תהיה בהתאם למחלות הרקע:
- הימצאות מחלת כבד או כליות חמורה
- תחלואה לבבית כגון אי-ספיקת לב, מחלת לב לא יציבה, הפרעות קצב - מחייב הסכמה ומעקב קרדיולוגי
- מטופלים עם תחלואה נפשית (PTSD, דיכאון, חרדה, הפרעה דו קוטבית) - מחייב הסכמה ומעקב פסיכיאטרי[100][105]
במטופלים שבריריים או עם מחלות רקע משמעותיות, ההמלצה היא מתן טיפול בתכשיר קנאביס בשמן מבוסס CBD, תוך ניטור תופעות לוואי שכיחות[105].
מטופלים עם פוליפרמסי - אין הרבה מידע בנוגע לאינטראקציות בין תוצרי קנאביס לבין תרופות אחרות[106]. מתן קנאביס יחד עם תרופות אחרות אשר משפיעות על קבוצת אנזימי הכבד CYP עלולים לשנות את המטבוליזם של הקנבינואידים[107][108][109][110][111][112].
התוויות נגד לטיפול בקנביס
- יש להיזהר ממתן קנביס עם תרופות היפוגליקמיות, תרופות להורדת לחץ דם, תרופות בעלות אפקט סימפתומימטי, מדכאי מערכת CNS (למשל תרופות הרגעה, תרופות להפרעות שינה) ותרופות עם אפקט מרפה שרירים עקב סיכון מוגבר לנפילות. יש להיזהר בעת מתן יחד עם אופיאטים (עקב חשש מהגברת תחושות סדציה, סחרחורות, אטקסיה, חוסר שיווי משקל), ומתרופות עם אפקט אנטיכולינרגי (לדוגמה נוגדי דיכאון, אנטיהיסטמינים)[100][105]
- יש להפסיק את הטיפול בחשד לתגובה אלרגית, בכל מצב היפומאני/מאני/פסיכוטי חדש, באם ישנה עלייה במינון אנלגטיקה או תרופות נוירופסיכיאטריות - ללא הסבר אורגני מזוהה, באם ישנה חוסר יעילות לאורך זמן למרות ניסיונות חוזרים ותחת מעקב רפואי סדיר, או אם ישנן תופעות לוואי משמעותיות[105]
- מבחינה פסיכיאטרית - מצבים כגון פסיכוזה פעילה, מצב פסיכוטי בעבר, הפרעה חרדתית, תורשה פסיכיאטרית משמעותית בקרוב משפחה מדרגה ראשונה, היסטוריה של התמכרות או שימוש לרעה בסמים מהווים קונטרהאינדיקציה לטיפול[100]
נקודות חשובות בטיפול[105]
- התחלת טיפול בקנאביס רפואי – לשקול בזהירות, תוך התחשבות ביתרונות מול חסרונות, והתאמת הטיפול למטופל באופן פרטני
- START LOW GO SLOW – התחלת טיפול ממינון נמוך וטיטרציה איטית על מנת להימנע מתופעות לוואי כגון נפילות ואורטוסטטיזם
- צורות השימוש המומלצות הן מתן תת-לשוני של מיצוי שמן קנאביס עבור כאב מתמשך, ובאידוי עבור כאב מתפרץ. ככלל, השימוש בקנאביס בעישון אינו מומלץ באופן גורף[100][105]
- בטיפול בכאב כרוני בקשישים מומלץ להיעזר במיצוי קנאביס רפואי עם ריכוזי CBD גבוהים וריכוזי THC נמוכים. במקרים בהם יש צורך בטיפול לכאב מתפרץ, יש לשקול קנאביס בשאיפה – בשימוש במכשיר אידוי. לפי הצורך, ניתן לשקול עלייה הדרגתית במינון הקנאביס, מספר הטיפות או השאיפות וכן שינוי בריכוזים. יש לבצע שינויים אלו בצורה איטית והדרגתית ככל הניתן במטופל הקשיש, על מנת להימנע מתופעות לוואי
- ביצוע מעקב תקופתי לבחינת יעילות ותופעות לוואי, בעיקר בהקשר של פוליפרמסי. קיימת חובה של מעקב רפואי רציף אצל רופא מוסמך לטיפול בקנאביס רפואי. אם החסרונות עולים על התועלת, יש לשקול להפסיק את הטיפול
- המינון הנכון הוא המינון האפקטיבי הנמוך ביותר שלא גורם לתופעות לוואי
מרפי שרירים
Baclofen - תכשיר מרפה שרירים שבמרביתו מתפנה כלייתית. גישת הטיפול בכל קבוצות האוכלוסייה מאופיינת בטיטרציה איטית לאורך שבועות כתלות ביעילות במקרה הפרטני מחד, ובסבילות מאידך. במטופלים עם אי-ספיקת כליות מומלץ להפחית את מינון התכשיר ולרווח את תדירות הטיטרציה[113].
Orphenadrine - תכשיר מרפה שרירים בעל פעילות אנטיהיסטמינרגית, אנטיכולינרגית ואנטי - NDMA. מאחר שמדובר בתכשיר עם פעילות שאינה סלקטיבית הכוללת גם מרכיבים אנטי-היסטמינרגים ואנטיכולינרגיים, הסיכון לתופעות לוואי (כודגמת ישנוניות, נפילות) בקרב מטופלים מבוגרים גבוה ולכן במרבית המקרים התועלת הפוטונציאלית אינה עולה על הסיכון. לאור האמור, מומלץ להימנע ממתן תכשיר זה במבוגרים[114].
עירויי Lidocaine
Lidocaine הוא מאלחש מקומי הניתן סיסטמית בהתווית כאב פריאופרטיבי וכאב נוירופתי כרוני. במינונים נמוכים מעכב התכשיר את הפעילות החשמלית הפתולוגית בעצבים המעורבים בכאב הנוירופתי מבלי לפגוע במערכת ההולכה הלבבית או בעצבים בריאים. משטרי הטיפול משתנים בין המוסדות השונים אך לרוב מדובר במינונים של 3-5 מיליגרם/קילוגרם הניתנים במשך כ-30-60 דק. לתכשיר זמן מחצית חיים קצר (1–2 שעות במתן סיסטמי) ועם זאת, בחלק מהמטופלים השפעתו נמשכת לתקופה ממושכת יותר. מדובר בתכשיר שבמרביתו מתפנה על ידי הכבד ולכן מאפייניו הפרמקוקינטים מושפעים משינויים בפעילות הכבד ובזרימת הדם אליו.
- על כן מומלץ לשקול להפחית את המינון ואת קצב המתן במטופלים עם אי-ספיקת לב ו/או עם הפרעה סינתטית בפעילות הכבד. במשטרי טיפול יומיומיים מומלץ אף לשקול את ריווח הטיפול
- אי- ספיקת כליות (30 > eGFR מיליליטר/דקה/1.73 מטר מרובע) עלולה להפחית את קצב פינוי המטבולוטים הפעילים ולכן במקרים בהם משטר הטיפול הוא יומיומי, מומלץ לרווח את תדירותו
- יש להיזהר במטופלים הסובלים מחסם הולכה לבבי (AV block) או במטופלים הנוטלים תרופות המאטות את ההולכה החשמלית כגון חסמי בטא
- אינטראקציות בין תרופתיות במנגנון פרמקוקינטי: מדובר בתכשיר העובר מטבוליזם על ידי CYP1A2, כך שתכשירים עלולים להוביל לקצב פינוי איטי מהצפוי ולפיכך לחשיפה גבוהה (ciprofloxacin, fluvoxamine) המעכבים אותו מהצפוי[115][116][117][118]
טיפולים פולשניים
זריקות
האוכלוסייה הקשישה רגישה יותר לתופעות לוואי סיסטמיות של טיפול תרופתי נוגד כאב, לפיכך ייתכן וישנו יתרון לטיפול פולשני נוגד כאב הפועל באופן נקודתי וגורם לפחות תופעות לוואי סיסטמיות.
הפעולות אותן ניתן לבצע במסגרת מרפאות הכאב הן הזרקות אפידורליות, הזרקות למפרקים, חסמים עצביים, הזרקות לשרירים ואף שימוש בהשתלת קוצב ספינלי.
במרבית הפעולות הנזכרות למעלה מוזרקים חומרי אלחוש מקומיים כגון Lidocaine, Marcaine, בשילוב עם סטרואיד כגון Dexamethasone, Depomedrol או Celestone.
סטרואידים בהזרקה מקומית
סטרואידים בהזרקה מקומית עשויים לגרום לתופעות לוואי סיסטמיות היות שהם נספגים במידה חלקית אל מחזור הדם. מטופלים הנמצאים בקבוצת סיכון לסבול מתופעות לוואי אלו הם במיוחד חולי סוכרת וחולי אוסתאופורוזיס.
מטופלים הסובלים מסוכרת - הזרקת סטרואידים עלולה לגרום להיפרגליקמיה ולהימשך עד שבועיים ממועד ההזרקה, כאשר ערכי הסוכר עלולים לעלות אף ב-120 מיליגרם/דציליטר ב-3 הימים שלאחר הזריקה[119][120][121]. אי-לכך במטופלים עם סוכרת לא מאוזנת עם ערכי סוכר של מעל 200 מיליגרם/דציליטר בצום או עם ערכי המוגלובין מסוכרר מעל 9 אחוזים, מומלץ להימנע מהזרקת סטרואידים מחשש לגרימת DKA (Diabetic Ketoacidosis)[122].
מטופלים עם אוסתאופורוזיס - סטרואידים מעלים את הפעילות של אוסטאוקלסטים ומפחיתים פעילות אוסטאובלסטים. בנוסף מעלים את הפרשת הסידן בשתן ומפחיתים את הספיגה שלו במעי, על ידי כך גורמים לירידה במינרליזציה ובצפיפות העצם. מספר מחקרים בדקו את השפעתן של זריקות סטרואידים בנשים פוסטמנופאוזליות. נמצא שהזרקות אפידורליות מפחיתות צפיפות עצם באופן תלוי מינון, כאשר כל זריקה מעלה ב-20 אחוזים את הסיכון לשבר ורטברלי[123]. זאת למעט בנשים שטופלו במקביל בתרופות לאוסתאופורוזיס, בהן מתן סטרואידים בזריקה לא העלה את הסיכון לשברים אוסתאופורוטים[123][124][125][126][127][128][129][130]. מחקר הראה כי שימוש במינון מצטבר של 160 מיליגרם מתילפרדניזולון אקוויוולנטי לא נמצא כמעלה סיכון להתפתחות שבר אוסתאופורוטי[131]. לאור המידע הקיים, בגברים ובנשים מעל גיל 50 יש לשקול להגביל את המינון המקסימלי של מתילפרדניזולון ל-200 מיליגרם בשנה, ול-400 מיליגרם ב-3 שנים. בחולי אוסתאופורוזיס ובייחוד בחולים עם שברים, יש לשקול טיפול בביספוספונטים בטרם טיפול בהזרקות סטרואידים[122].
נוסף על כך, ישנם מספר דיווחים בספרות על תסמינים פסיכיאטרים לאחר הזרקה חד-פעמית של סטרואידים לרבות התקפים מאנים, פסיכוזה ודליריום, באופן תלוי מינון[132][133][134].
נראה כי שימוש במינון של 40 מיליגרם מתילפרדניזולון (או מינון אקוויוולנטי של סטרואיד אחר) פר זריקה הןא בטוח יותר לשימוש באוכלוסייה הקשישה, ובעל יעילות דומה למינונים גבוהים יותר[135].
בנוסף, מטופלים הסובלים מאי-ספיקת לב קשה ולא מאוזנת, מיתר לחץ דם לא מאוזן, מדיכוי חיסוני או מטופלים לפני ניתוח, יש לשקול האם התועלת עולה על הסיכון ולהתאים את הטיפול באופן אינדיבידואלי.
הזרקה מקומית באנשים הנוטלים טיפול נוגד קרישה או אגרגציית טסיות
קשישים רבים מטופלים בנוגדי קרישה או במעכבי אגרגציית טסיות באופן קבוע. ישנן הנחיות של האיגוד האמריקאי להרדמה אזורית ורפואת כאב - American Society of Regional Anesthesia and Pain Medicine לגבי הפסקת השימוש בתרופות אלו לפני זריקה פולשנית. ההנחיות נגזרות מהסיכון לדמם בסוגי הפעולות השונות.
פעולות בסיכון גבוה כוללות פעולות בהן הסיכון לדמם גבוה או שדימום באזור המוזרק עלול לגרום להשלכות מסכנות חיים/תפקוד. למשל הזרקות אפידורליות, השתלת אלקטרודות בחלל האפידורלי או באזור של עצבים פריפריים, חסמים למקלעות סימפתטיות.
פעולות בסיכון בינוני כוללות בין היתר את ההזרקות למפרקים הפצטריים והזרקות לשורשי עצבים בעמוד השדרה המותני. פעולות בסיכון נמוך כוללות את ההזרקות לשרירים ונקודות הדק, הזרקה למפרקים פריפריים, חסמים עצביים פריפריים, הזרקות קאודליות.
מטופלים עם הפרעות בתפקודי קרישה או תחת טיפול במדללי דם הם בסיכון מוגבר לדמם לאחר פעולה לכן קיימות הנחיות לגבי הפסקת הטיפול לפני פעולות לטיפול בכאב.
ככלל אין צורך בהפסקה של מרבית התרופות לדילול הדם לפני פעולות בעלות סיכון נמוך. כמו כן אין צורך בהפסקת אספירין לפני מרבית הפעולות.
לפני פעולות בסיכון בינוני וגבוה יש להפסיק טיפול בנוגדי קרישה ומעכבי אגריגציית טסיות לפי זמן מחצית החיים שלהן. לקביעת משך ההפסקה ניתן להיעזר בהמלצות של האיגודים המוכרים - דוגמת ASRA, ASIPP, הנחיות של איגוד המרדימים הישראלים ודומיהם. ניתן להמיר את הטיפול לזריקות קלקסן ולהפסיקן 12-24 שעות לפני הפעולה כתלות במינון ובתפקוד הכלייתי של המטופל. יש לחדש את הטיפול בנוגדי קרישה ומעכבי אגריגציית טסיות בטווח שבין 8–24 שעות לאחר הפעולה.
קיפופלסטיה/ורטברופלסטיה
מדובר בטיפולים המבוצעים בשברים אוסתאופורוטיים בחוליות, בהן מוזרק צמנט באופן מלעורי תחת שיקוף לתוך גוף החוליה השבורה.
המידע בספרות אינו חד-משמעי באשר לאינדיקציות והתזמון של פעולות אלה בחולים עם שבר בחוליה משנית לאוסתאופורוזיס, אולם נראה כי ישנה יעילות בשימוש בפרוצדורות אלה בחולים עם שבר אקוטי - סאב אקוטי (6–12 שבועות) אשר סובלים מכאב חזק תחת טיפול שמרני. שימוש בפרוצדורות הנזכרות למעלה בקשישים המאושפזים עקב שבר אוסתאופורוטי כואב, מפחית משך אשפוז ואחוזי אשפוז חוזר. קיים מידע סותר באשר להפחתת תמותה[136]. עם זאת ישנם מחקרים שהראו כי ייתכן וישנה עלייה בסיכון לשברים אוסתאופורוטים בחוליות הסמוכות לאחר הפעולה[137][138].
לדעת כותבי נייר עמדה זה, לאור היעדר הנחיות חד משמעיות נכון למועד כתיבת המסמך, נראה כי במצב של כאב חריף משנית לשבר חוליה, בשלב הראשון יש לנסות ולאזן את המטופל תרופתית, אם הנזכר למעלה נכשל לנסות טיפול על ידי זריקה בודדת במסגרת מרפאת כאב, ואם לאחר מכן עדיין ישנו כאב משמעותי לנסות טיפול של קיפופלסטיה/ורטברופלסטיה לאחר שחלפו כ- 6–12 שבועות ממועד השבר.
באשר לבטיחות של הזרקת סטרואידים בשלב האקוטי לאחר שבר, מהמידע המועט שקיים בספרות, נראה כי מתן חד-פעמי של סטרואידים אינו פוגע באיחוי השבר או בהחלמת הרקמה הרכה[139][140].
יש לשקול טיפול בביספוספונטים בטרם טיפול בהזרקות סטרואידים[122].
ביבליוגרפיה
- ↑ 1.0 1.1 1.2 1.3 Molton IR, Terrill AL. Overview of persistent pain in older adults. Am Psychol. 2014;69:197-207.
- ↑ 2.0 2.1 Centers for Disease Control and Prevention. The State of Aging and Health in America 2013. Atlanta, GA: Centers for Disease Control and Prevention, US Dept of Health and Human Services; 2013 .
- ↑ 3.0 3.1 sang A, Von Korff M, Lee S, Alonso J, Karam E, Angermeyer MC, et countries: gender and age differences and comorbidity with depression-anxiety disorders. J Pain. 2008;9:883-91. doi:10.1016/j.jpain.2008.05.005
- ↑ Kaye AD, Baluch A, Scott JT. Pain management in the elderly population: a review. Ochsner J. 2010;10)3(:179-87
- ↑ Mark C. Bicket, Jianren Mao, Chronic pain in older adults, Anesthesiology Clinics, Volume 33, Issue 3, September 2015, Pages 577-590, ISSN 1932-2275.
- ↑ Sauver JLS, Warner DO, Yawn BP, et al. Why patients visit their doctors: assessing the most prevalent conditions in a defined American population. Mayo Clin Proc. 2013;88:56-67.
- ↑ Thielke S, Sale J, Reid MC. Aging: are these 4 pain myths complicating care? J Fam Pract. 2012;61:666-70.
- ↑ Dunn KM et al. Low back pain across the life course. Best Pract Res Clin Rheumatol. 2013;27)5(:591-600.
- ↑ 9.0 9.1 9.2 9.3 Hazzard’s Geriatric Medicine and Gerontology, 8th edition, 2022
- ↑ 10.0 10.1 10.2 10.3 Malec M. Shega JW - Pain Management in the Elderly; Med Clin N Am 99 )2015( 337-350
- ↑ 11.0 11.1 11.2 11.3 Vulfsons S, Orion Y - Approach to a Geriatric Patient in Pain Clinic in G. Slobodin, Y. Shoenfeld )eds.(, Rheumatic Disease in Geriatrics, 2020
- ↑ BA Ferrell, Pain management in elderly people’ J Am Geriatr Soc, 39 )1991(, pp. 64-73
- ↑ FM Gloth, AA Scheve, CV Stober, J Prosser, The functional pain scale: Reliability, validity, and responsiveness in an elderly population, J Am Med Dir Assoc, 2 )2001(, pp. 110-114
- ↑ KA Herr, PR Mobily, Complexities of pain assessment in the elderly: Clinical considerations, J Gerontol Nurs, 17 )1991(, pp. 12-19
- ↑ Kaye AD, Baluch A, Kaye R, Niaz RS, Kaye A, Liu H, et al. Geriatric pain management, pharmacological and nonpharmacological considerations. Psychol Neurosci. 2014;7)1(:15-26.
- ↑ American Geriatrics Panel on chronic pain in older persons. The management of chronic pain in older persons. J Am Geriatr Soc. 1998;46:635-51
- ↑ Hadjistavropoulos T. Assessing pain in older persons with severe limitations in ability to communicate. In: Gibson S.J., Weiner D., editors. Pain in the Elderly. IASP Press; Seattle, WA, USA: 2005. pp. 135-157. [Google Scholar]
- ↑ Marcum Z.A., Duncan N.A., Makris U.E. Pharmacotherapies in Geriatric Chronic Pain Management. Clin. Geriatr. Med. 2016;32:705-724. doi: 10.1016/j.cger.2016.06.007. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- ↑ Gazelka H.M., Leal J.C., Lapid M.I., Rummans T.A. Opioids in Older Adults: Indications, Prescribing, Complications, and Alternative Therapies for Primary Care. Mayo Clin. Proc. 2020;95:793-800. doi: 10.1016/j.mayocp.2020.02.002. [PubMed] [CrossRef] [Google Scholar]
- ↑ Papaleontiou M., Henderson C.R., Turner B.J., Moore A.A., Olkhovskaya Y., Amanfo L., Reid M.C. Outcomes Associated with Opioid Use in the Treatment of Chronic Noncancer Pain in Older Adults: A Systematic Review and Meta-Analysis. J. Am. Geriatr. Soc. 2010;58:1353- 1369. doi: 10.1111/j.1532-5415.2010.02920.x. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- ↑ Prostran M., Vujovic K.S., Vuckovic S., Medic B., Srebro D., Divac N., Stojanovic R., Vujovic A., Jovanovic L., Jotic A., et al. Pharmacotherapy of Pain in the Older Population: The Place of Opioids. Front. Aging Neurosci. 2016;8:144. doi: 10.3389/fnagi.2016.00144. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- ↑ Jourdan D., Pickering G., Marchand F., Gaulier J.-M., Alliot J., Eschalier A. Impact of ageing on the antinociceptive effect of reference analgesics in the Lou/c rat. Br. J. Pharmacol. 2002;137:813-820. doi: 10.1038/sj.bjp.0704944. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- ↑ Naples J.G., Gellad W.F., Hanlon J.T. The Role of Opioid Analgesics in Geriatric Pain Management. Clin. Geriatr. Med. 2016;32:725-735. doi: 10.1016/j.cger.2016.06.006. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- ↑ umer N, Scarpace PJ, Lowenthal DT. Geriatric pharmacology: basic and clinical considerations. Annu Rev Pharmacol Toxicol. 1992;32:271-302.
- ↑ Davies DF, Shock NW. Age changes in glomerular filtration rate, effect of venal plasma flow, and tubular excretory capacity in adult males. J Clin Invest. 1950;29)5(:496-507.
- ↑ 26.0 26.1 Malec M, Shega JW. Pain management in the elderly. Med Clin N Am. 2015;99)2(:337-50
- ↑ Tracy B, Sean MR. Pain management in older adults. Clin Ther. 2013;35)11(:1659-68.
- ↑ Avorn J, Gurwitz JH, Rochon P. Principles of pharmacology. In: Cassel CK, Leipzig RM, Cohen HJ, Larson EB, Meier DE, Capello CF, editors. Geriatric medicine: an evidence-based approach. 4th ed. New York: Springer; 2003. p. 65-77.
- ↑ 29.0 29.1 29.2 29.3 29.4 29.5 29.6 29.7 Ali A, Arif A, Bhan C, et al. )September 13, 2018( Managing Chronic Pain in the Elderly: An Overview of the Recent Therapeutic Advancements. Cureus 10)9(: e3293. DOI 10.7759/ cureus.3293
- ↑ Scascighini L, Toma V, Dober-Spielmann S, Sprott H. Multidisciplinary treatment for chronic pain: a systematic review of interventions and outcomes.Rheumatology (Oxford). 2008;47)5(:670
- ↑ Chou R, Deyo R, Friedly J, Skelly A, Hashimoto R, Weimer M, Fu R, Dana T, Kraegel P, Griffin J, Grusing S, Brodt ED Nonpharmacologic Therapies for Low Back Pain: A Systematic Review for an American College of Physicians Clinical Practice Guideline.Ann Intern Med. 2017;166)7(:493. Epub 2017 Feb 14.
- ↑ Wertli MM, Rasmussen-Barr E, Held U, Weiser S, Bachmann LM, Brunner F Fear-avoidance beliefs-a moderator of treatment efficacy in patients with low back pain: a systematic review.Spine J. 2014;14)11(:2658. Epub 2014 Mar 12.
- ↑ Bartels EM, Juhl CB, Christensen R, Hagen KB, Danneskiold-Sams0e B, Dagfinrud H, Lund H Aquatic exercise for the treatment of knee and hip osteoarthritis.Cochrane Database Syst Rev. 2016;3:CD005523
- ↑ 34.0 34.1 Qaseem A, Wilt TJ, McLean RM, Forciea MA, Noninvasive Treatments for Acute, Subacute, and Chronic Low Back Pain: A Clinical Practice Guideline From the American College of Physicians. Clinical Guidelines Committee of the American College of Physicians Ann Intern Med. 2017;166)7(:514. Epub 2017 Feb 14
- ↑ Sherman KJ, Cherkin DC, Wellman RD, Cook AJ, Hawkes RJ, Delaney K, Deyo RA A randomized trial comparing yoga, stretching, and a self-care book for chronic low back pain. Arch Intern Med. 2011;171)22(:2019. Epub 2011 Oct 24.
- ↑ Cherkin DC, Sherman KJ, Balderson BH, Cook AJ, Anderson ML, Hawkes RJ, Hansen KE, Turner JA Effect of Mindfulness-Based Stress Reduction vs Cognitive Behavioral Therapy or Usual Care on Back Pain and Functional Limitations in Adults With Chronic Low Back Pain: A Randomized Clinical Trial.JAMA. 2016 Mar;315)12(:1240-9.
- ↑ Siddall B, Ram A, Jones MD, Booth J, Perriman D, Summers SJ Short-term impact of combining pain neuroscience education with exercise for chronic musculoskeletal pain: a systematic review and meta-analysis.. Pain. 2022;163)1(:e20.
- ↑ Louw A, Diener I, Butler DS, Puentedura EJ The effect of neuroscience education on pain, disability, anxiety, and stress in chronic musculoskeletal pain. Arch Phys Med Rehabil. 2011;92)12(:2041
- ↑ Saracoglu I, Akin E, Aydin Dincer GB Efficacy of adding pain neuroscience education to a multimodal treatment in fibromyalgia: A systematic review and meta-analysis.. Int J Rheum Dis. 2022;25)4(:394. Epub 2022 Jan 21.
- ↑ Ordonez-Mora LT, Morales-Osorio MA, Rosero ID. Effectiveness of Interventions Based on Pain Neuroscience Education on Pain and Psychosocial Variables for Osteoarthritis: A Systematic Review. Int J Environ Res Public Health. 2022;19)5( Epub 2022 Feb 23.
- ↑ 41.0 41.1 Skelly AC, Chou R, Dettori JR, Turner JA, Friedly JL, Rundell SD, Fu R, Brodt ED, Wasson N, Winter C, Ferguson Noninvasive Nonpharmacological Treatment for Chronic Pain: A Systematic Review, AJR. )Eds(, Agency for Healthcare Research and Quality )US(, Rockville )MD( 2018
- ↑ Stanos SP, McLean J, Rader Physical medicine rehabilitation approach to pain.Med Clin North Am. 2007;91)1(:57
- ↑ Skelly AC, Chou R, Dettori JR, Turner JA, Friedly JL, Rundell SD, Fu R, Brodt ED, Wasson N, Kantner S, Ferguson Noninvasive Nonpharmacological Treatment for Chronic Pain: A Systematic Review Update, AJR. )Eds(, Agency for Healthcare Research and Quality )US(, Rockville )MD( 2020.
- ↑ Williams ACC, Fisher E, Hearn L, Eccleston C Psychological therapies for the management of chronic pain )excluding headache( in adults.Cochrane Database Syst Rev. 2020;8:CD007407. Epub 2020 Aug 12.
- ↑ Gatchel RJ, McGeary DD, McGeary CA, Lippe B. Interdisciplinary chronic pain management: past, present, and future. Am Psychol. 2014;69)2(:119.
- ↑ Debar LL, Kindler L, Keefe FJ, Green CA, Smith DH, Deyo RA, Ames K, Feldstein A A primary care-based interdisciplinary team approach to the treatment of chronic pain utilizing a pragmatic clinical trials framework. Transl Behav Med. 2012;2)4(:523. Epub 2012 Aug 30.
- ↑ Sturgeon JA Psychological therapies for the management of chronic pain. Psychol Res Behav Manag. 2014;7:115. Epub 2014 Apr 10.
- ↑ ElmaO, Yilmaz ST, Deliens T, Clarys P, Nijs J, Coppieters I, Polli A, Malfliet A Chronic Musculoskeletal Pain and Nutrition: Where Are We and Where Are We Heading? PM R. 2020;12)12(:1268. Epub 2020 Mar 20
- ↑ Tick H . Nutrition and pain.Phys Med Rehabil Clin N Am. 2015;26)2(:309.
- ↑ Johnson MI, Claydon LS, Herbison GP, Jones G, Paley CA Transcutaneous electrical nerve stimulation )TENS( for fibromyalgia in adults. Cochrane Database Syst Rev. 2017;10:CD012172. Epub 2017 Oct 9.
- ↑ Gibson W, Wand BM, Meads C, Catley MJ, O’Connell NE. Transcutaneous electrical nerve stimulation )TENS( for chronic pain - an overview of Cochrane Reviews.Cochrane Database Syst Rev. 2019;2:CD011890. Epub 2019 Feb 19.
- ↑ Johnson MI. Resolving Long-Standing Uncertainty about the Clinical Efficacy of Transcutaneous Electrical Nerve Stimulation )TENS( to Relieve Pain: A Comprehensive Review of Factors Influencing Outcome.Medicina )Kaunas(. 2021;57)4( Epub 2021 Apr 14.
- ↑ Binny J, Joshua Wong NL, Garga S, Lin CC, Maher CG, McLachlan AJ, Traeger AC, Machado GC, Shaheed CA. Transcutaneous electric nerve stimulation )TENS( for acute low back pain: systematic review. Scand J Pain. 2019;19)2(:225.
- ↑ 54.0 54.1 54.2 54.3 54.4 Kaye AD, Baluch A, Scott JT. Pain management in the elderly population: a review. Ochsner J. 2010 Fall;10)3(:179-87. PMID: 21603375; PMCID: PMC3096211.
- ↑ 55.0 55.1 55.2 By the 2023 American Geriatrics Society Beers Criteria® Update Expert Panel. American Geriatrics Society 2023 updated AGS Beers Criteria® for potentially inappropriate medication use in older adults. J Am Geriatr Soc. 2023 Jul;71)7(:2052-2081. doi: 10.1111/jgs.18372. Epub 2023 May 4. PMID: 37139824.
- ↑ 56.0 56.1 Pickering, G., Kotlihska-Lemieszek, A., Krcevski Skvarc, N. et al. Pharmacological Pain Treatment in Older Persons. Drugs Aging )2024(. https://doi.org/10.1007/s40266-024-01151-8
- ↑ עלון התרופה Optalgin® Teva
- ↑ Lutz M. Metamizole )Dipyrone( and the Liver: A Review of the Literature. J Clin Pharmacol. 2019 Nov;59)11(:1433-1442. doi: 10.1002/jcph.1512. Epub 2019 Aug 21. PMID: 31433499.
- ↑ Time course of CYP3A activity during and after metamizole )dipyrone( in healthy volunteers. Br J Clin Pharmacol. 2023;89:2458-2464
- ↑ Metamizole is a Moderate Cytochrome P450 Inducer Via the Constitutive Androstane Receptor and a Weak Inhibitor of CYP1A2. 2020. doi:10.1002/cpt.2141
- ↑ Pharmacological Management of Persistent Pain in Older Persons. Journal of the American Geriatrics Society, 57: 1331-1346. https://doi-org.ezlibrary.technion.ac.il/10.1111/j.1532- 5415.2009.02376.x
- ↑ Dowell D, Haegerich TM, Chou R. CDC Guideline for Prescribing Opioids for Chronic Pain — United States, 2016. MMWR Recomm Rep 2016;65)No. RR-1(:1-49. DOI: http://dx.doi.org/10.15585/ mmwr.rr6501e1external icon
- ↑ Josianna Schwan, MD, Joseph Sclafani, MD, Vivianne L. Tawfik, MD PhD*, Chronic Pain Management in the Elderly; Anesthesiol Clin. 2019 September ; 37)3(: 547-560. doi:10.1016/j. anclin.2019.04.012
- ↑ G. Slobodin, Y. Shoenfeld )eds.(, Rheumatic Disease in Geriatrics chapter 5: Pharmacokinetics of Anti-Rheumatic in Geriatric Patients, p.55.; , https://doi.org/10.1007/978-3-030-44234-7_5;
- ↑ Grond S, Sablotzki A: Clinical pharmacology of tramadol. Clin Pharmacokinet. 2004;43)13(:879- 923. )PubMed ID 15509185(
- ↑ Duehmke RM, Derry S, Wien PJ, Bell RF, Aldington D, Moore RA. Tramadol for neuropathic pain in adults. Cochrane Database of Systematic Reviews 2017, Issue 6. Art. No.: CD003726. DOI: 10.1002/14651858.CD003726.pub4.
- ↑ מתוך העלון לרופא של משרד הבריאות Tramadol
- ↑ Murray BP, Carpenter JE, Dunkley CA, Moran TP, Alfaifi M, Alsukaiti WS, Kazzi Z: Seizures in tramadol overdoses reported in the ToxIC registry: predisposing factors and the role of naloxone. Clin Toxicol )Phila(. 2019 Aug;57)8(:692-696. doi: 10.1080/15563650.2018.1547826. Epub 2019 Jan 24. )PubMed ID 30676832(
- ↑ Tchoe HJ, Jeong S, Won DY, Nam JH, Joung KI, Shin JY. Increased risk of death with codeine use in the elderly over 85 years old and patients with respiratory disease: A case-control study using retrospective insurance claims database. Medicine )Baltimore(. 2020 Sep 18;99)38(:e22155. doi: 10.1097/MD.0000000000022155. PMID: 32957338; PMCID: PMC7505312
- ↑ 70.0 70.1 70.2 70.3 Micromedex website
- ↑ Pergolizzi JV Jr. And R.B. Raffa, safety and efficacy of the unique opioid buprenorphine for the treatment of chronic pain. J Pain Res. 2019;12:3299-317.
- ↑ Case AA, Kullgren J, Anwar S, Pedraza S, Davis MP. Treating Chronic Pain with Buprenorphine- The Practical Guide. Curr Treat Options Oncol. 2021 Nov 18;2 2)12(:116. doi: 10.1007/s11864-021-00910-8. PMID: 34791564.
- ↑ Rekatsina, M., Paladini, A., Viswanath, O. et al. Opioids in the Elderly Patients with Cognitive Impairment: A Narrative Review. Pain Ther 11, 381-394 )2022(.
- ↑ Dufort, Alexander, and Zainab Samaan. “Problematic opioid use among older adults: epidemiology, adverse outcomes and treatment considerations.” Drugs & Aging 38.12 (2021): 1043-1053.
- ↑ Dufort, Alexander, and Zainab Samaan. “Problematic opioid use among older adults: epidemiology, adverse outcomes and treatment considerations.” Drugs & Aging 38.12 (2021): 1043-1053.
- ↑ Han, Ying, et al. “The rising crisis of illicit fentanyl use, overdose, and potential therapeutic strategies." Translational psychiatry 9.1 (2019): 282.
- ↑ Galgani, Alessandro, et al. “Pharmacokinetic interactions of clinical interest between direct oral anticoagulants and antiepileptic drugs.” Frontiers in neurology 9 )2018(: 1067.
- ↑ Sajatovic, Martha, et al. “Lamotrigine therapy in elderly patients with epilepsy, bipolar disorder or dementia.” International Journal of Geriatric Psychiatry: A journal of the psychiatry of late life and allied sciences 22.10 )2007(: 945-950.
- ↑ Arif, Hiba, et al. “The effect of age and comedication on lamotrigine clearance, tolerability, and efficacy.” Epilepsia 52.10 )2011(: 1905-1913.
- ↑ National Academies of Sciences, Engineering, and Medicine. Health and Medicine Division. Board on Population Health and Public Health Practice. Committee on the Health Effects of Marijuana: An Evidence Review and Research Agenda . The Health Effects of Cannabis and Cannabinoids: The Current State of Evidence and Recommendations for Research. National Academies Press )US(; Washington, DC, USA: 2017. [)accessed on 7 October 2019(]. Available online:
- ↑ 81.0 81.1 Freeman M., Low A., Kondo K., Elven C., Zakher B., Motu’Apuaka M., Paynter R., Kansagara D., Nugent S.M., Morasco B.J., et al. The Effects of Cannabis among Adults with Chronic Pain and an Overview of General Harms. Ann. Intern. Med
- ↑ Abuhasira R., Shbiro L., Landschaft Y. Medical use of cannabis and cannabinoids containing products—Regulations in Europe and North America. Eur. J. Intern. Med. 2018;49:2-6. doi: 10.1016/j.ejim.2018.01.001.
- ↑ . Schleider L.B.-L., Abuhasira R., Novack V. Medical cannabis: Aligning use to evidence-based medicine approach. Br. J. Clin. Pharmacol. 2018;84:2458-2462. doi: 10.1111/bcp.13657
- ↑ Reynolds I.R., Fixen D.R., Parnes B.L., Lum H.D., Shanbhag P., Church S., Linnebur S.A., Orosz G. Characteristics and Patterns of Marijuana Use in Community-Dwelling Older Adults. J. Am. Geriatr. Soc. 2018;66:2167-2171. doi: 10.1111/jgs.15507
- ↑ 85.0 85.1 Aviram J, Lewitus GM, Vysotski Y, Yellin B, Berman P, Shapira A, Meiri D. Prolonged Medical Cannabis Treatment is Associated With Quality of Life Improvement and Reduction of Analgesic Medication Consumption in Chronic Pain Patients. Front Pharmacol. 2021 May 19;12:613805. doi: 10.3389/fphar.2021.613805. PMID: 34093173; PMCID: PMC8172141.
- ↑ O’Neil C.K., Hanlon J.T., Marcum Z.A. Adverse effects of analgesics commonly used by older adults with osteoarthritis: Focus on non-opioid and opioid analgesics. Am. J. Geriatr. Pharmacother. 2012;10:331-342. doi: 10.1016/j.amjopharm.2012.09.004.
- ↑ Ware M.A., Wang T., Shapiro S., Collet J.-P., Boulanger A., Esdaile J.M., Gordon A., Lynch M., Moulin D.E., O’Connell C. Cannabis for the Management of Pain: Assessment of Safety Study )COMPASS( J. Pain. 2015;16:1233-1242. doi: 10.1016/j.jpain.2015.07.014
- ↑ Desroches J, Beaulieu P. Opioids and cannabinoids interactions: involvement in pain management. Curr Drug Targets. 2010 Apr;11)4(:462-73. doi: 10.2174/138945010790980303. PMID: 20017728.
- ↑ 89.0 89.1 Abrams DI, Couey P, Shade SB, Kelly ME, Benowitz NL. Cannabinoid-opioid interaction in chronic pain. Clin Pharmacol Ther. 2011 Dec;90)6(:844-51. doi: 10.1038/clpt.2011.188. Epub 2011 Nov 2. PMID: 22048225.
- ↑ Cooper ZD, Bedi G, Ramesh D, Balter R, Comer SD, Haney M. Impact of co-administration of oxycodone and smoked cannabis on analgesia and abuse liability. Neuropsychopharmacology. 2018 Sep;43)10(:2046-2055. doi: 10.1038/s41386-018-0011-2. Epub 2018 Feb 5. PMID: 29463913; PMCID: PMC6098090.
- ↑ Cichewicz DL. Synergistic interactions between cannabinoid and opioid analgesics. Life Sci. 2004 Jan 30;74)11(:1317-24. doi: 10.1016/j.lfs.2003.09.038. PMID: 14706563.
- ↑ Lucas MA. Cannabis as an Adjunct to or Substitute for Opiates in the Treatment of Chronic Pain. Journal of Psychoactive, Drugs 2012; 125-33
- ↑ 93.0 93.1 Scavone JL, Sterling RC, Van Bockstaele EJ. Cannabinoid and opioid interactions: implications for opiate dependence and withdrawal. Neuroscience. 2013 Sep 17;248:637-54. doi: 10.1016/j. neuroscience.2013.04.034. Epub 2013 Apr 24. PMID: 23624062; PMCID: PMC3742578.
- ↑ 94.0 94.1 נוהל 106, חוזר היחידה לקנאביס רפואי )יק"ר(, משרד הבריאות, תאריך עדכון )7(: ינואר 2024, עמ' 3–8 .
- ↑ Hermush V, Ore L, Stern N, Mizrahi N, Fried M, Krivoshey M, Staghon E, Lederman VE, Bar-Lev Schleider L. Effects of rich cannabidiol oil on behavioral disturbances in patients with dementia: A placebo controlled randomized clinical trial. Front Med )Lausanne(. 2022 Sep 6;9:951889. doi: 10.3389/fmed.2022.951889. PMID: 36148467; PMCID: PMC9486160.
- ↑ Mangoni A.A., Jackson S.H.D. Age-related changes in pharmacokinetics and pharmacodynamics: Basic principles and practical applications. Br. J. Clin. Pharmacol. 2003;57:6-14. doi: 10.1046/j.1365-2125.2003.02007.x
- ↑ Lucas CJ, Galettis P, Schneider J. The pharmacokinetics and the pharmacodynamics of cannabinoids. Br J Clin Pharmacol. 2018 Nov;84)11(:2477-2482. doi: 10.1111/bcp.13710. Epub 2018 Aug 7. PMID: 30001569; PMCID: PMC6177698.
- ↑ Singh-Manoux A., Kivimaki M., Glymour M.M., Elbaz A., Berr C., Ebmeier K.P., Ferrie J.E., Dugravot A. Timing of onset of cognitive decline: Results from Whitehall II prospective cohort study. BMJ. 2012;344:d7622. doi: 10.1136/bmj.d7622.
- ↑ 99.0 99.1 Elsen G.V.D., Ahmed A., Lammers M., Kramers C., Verkes R., Van Der Marck M., Rikkert M.O. Efficacy and safety of medical cannabinoids in older subjects: A systematic review. Ageing Res. Rev. 2014;14:56-64. doi: 10.1016/j.arr.2014.01.007
- ↑ 100.0 100.1 100.2 100.3 100.4 חוזר משנה למנהל הכללי, משרד הבריאות ,IMC-GCP -קנביס לשימוש רפואי- חוברת מידע ומדריך רפואי .
- ↑ Ganzer F., Broning S., Kraft S., Sack P.-M., Thomasius R. Weighing the Evidence: A Systematic Review on Long-Term Neurocognitive Effects of Cannabis Use in Abstinent Adolescents and Adults. Neuropsychol. Rev. 2016;26:186-222. doi: 10.1007/s11065-016-9316-2
- ↑ Schreiner A.M., Dunn M.E. Residual effects of cannabis use on neurocognitive performance after prolonged abstinence: A meta-analysis. Exp. Clin. Psychopharmacol. 2012;20:420-429. doi: 10.1037/a0029117.
- ↑ Rezkalla S., Stankowski R., Kloner R.A. Cardiovascular effects of marijuana. Trends Cardiovasc. Med. 2018;21:452-455.
- ↑ T. Wang, J.P. Collet, S. Shapiro, M.A. Ware Adverse effects of medical cannabinoids: a systematic review CMAJ, 178 )2008(, pp. 1669-1678
- ↑ 105.0 105.1 105.2 105.3 105.4 105.5 105.6 הנחיות קליניות - שימוש בקנאביס לטיפול בכאב, ההסתדרות הרפואית בישראל, ינואר 2023 .
- ↑ Alsherbiny M.A., Li C.G. Medicinal Cannabis—Potential Drug Interactions. Medicines. 2018;6:3. doi: 10.3390/medicines6010003.
- ↑ Stout S.M., Cimino N.M. Exogenous cannabinoids as substrates, inhibitors, and inducers of human drug metabolizing enzymes: A systematic review. Drug Metab. Rev. 2014;46:86-95. doi: 10.3109/03602532.2013.849268.
- ↑ Mahvan T.D., Hilaire M.L., Mann A., Brown A., Linn B., Gardner T., Lai B. Marijuana Use in the Elderly: Implications and Considerations. Consult. Pharm. 2017;32:341-351. doi: 10.4140/ TCP.n.2017.341.
- ↑ Ware M.A., Wang T., Shapiro S., Collet J.-P., Boulanger A., Esdaile J.M., Gordon A., Lynch M., Moulin D.E., O’Connell C. Cannabis for the Management of Pain: Assessment of Safety Study )COMPASS( J. Pain. 2015;16:1233-1242. doi: 10.1016/j.jpain.2015.07.014
- ↑ Mangoni A.A., Jackson S.H.D. Age-related changes in pharmacokinetics and pharmacodynamics: Basic principles and practical applications. Br. J. Clin. Pharmacol. 2003;57:6-14. doi: 10.1046/j.1365-2125.2003.02007.x
- ↑ Freeman M., Low A., Kondo K., Elven C., Zakher B., Motu’Apuaka M., Paynter R., Kansagara D., Nugent S.M., Morasco B.J., et al. The Effects of Cannabis among Adults with Chronic Pain and an Overview of General Harms. Ann. Intern. Med. 2017;167:319.
- ↑ National Academies of Sciences, Engineering, and Medicine. Health and Medicine Division. Board on Population Health and Public Health Practice. Committee on the Health Effects of Marijuana: An Evidence Review and Research Agenda . The Health Effects of Cannabis and Cannabinoids: The Current State of Evidence and Recommendations for Research. National Academies Press )US(; Washington, DC, USA: 2017. [)accessed on 7 October 2019(]. 2017;167:319.
- ↑ Pelter, Megan, Samantha RS Bagsic, and Laura Nicholson. “Oral baclofen toxicity in older patients with chronic kidney disease.” Journal of the American Geriatrics Society 69.8 )2021(: 2352-
- ↑ Abd-Elsalam, Sherief, et al. “Orphenadrine in treatment of muscle cramps in cirrhotic patients: a randomized study.” European journal of gastroenterology & hepatology 32.8 )2020(: 1042-1045.
- ↑ Abernethy, Darrell R., and David J. Greenblatt. “Impairment of lidocaine clearance in elderly male subjects.” Journal of cardiovascular pharmacology 5.6 )1983(: 1093-1096.
- ↑ THOMSON, PATE D., et al. “Lidocaine pharmacokinetics in advanced heart failure, liver disease, and renal failure in humans.” Annals of Internal Medicine 78.4 )1973(: 499-508.
- ↑ Zhu, Bo, et al. “Intra-venous lidocaine to relieve neuropathic pain: a systematic review and metaanalysis.” Frontiers in neurology 10 )2019(: 954.
- ↑ Waller, Elaine S. “Pharmacokinetic principles of lidocaine dosing in relation to disease state.” The Journal of Clinical Pharmacology 21.4 )1981(: 181-194.
- ↑ Younes M, Neffati F, Touzi M, et al. Systemic effects of epidural and intra-articular glucocorticoid injections in diabetic and nondiabetic patients. Joint Bone Spine. 2007;74:472-476.
- ↑ Gonzalez P, Laker SR, Sullivan W, Harwood JE, Akuthota V. The effects of epidural betamethasone on blood glucose in patients with diabetes mellitus. PM R. 2009;1:340-345.
- ↑ Even JL, Crosby CG, Song Y, McGirt MJ, Devin CJ. Effects of epidural steroid injections on blood glucose levels in patients with diabetes mellitus. Spine. 2012;37:E46-E50.
- ↑ 122.0 122.1 122.2 Stout A, Friedly J, Standaert CJ. Systemic absorption and side effects of locally injected glucocorticoids. PM R 2019; 11: 409-19.
- ↑ 123.0 123.1 Mandel S, Schilling J, Peterson E, Rao DS, SandersW. A retrospective analysis of vertebral body fractures following epidural steroid injections. J Bone Joint Surg Am. 2013;95:961-964.
- ↑ Emkey RD, Lindsay R, Lyssy J, Weisberg JS, Dempster DW, Shen V. The systemic effect of intraarticular administration of corticosteroid on markers of bone formation and bone resorption in patients with rheumatoid arthritis. Arthritis Rheum. 1996;39:277-282.
- ↑ Kerezoudis P, Rinaldo L, Alvi MA, et al. The effect of epidural steroid injections on bone mineral density and vertebral fracture risk: a systematic review and critical appraisal of current literature. Pain Med. 2018;19:569-579.
- ↑ Nah SY, Lee JH, Lee JH. Effects of epidural steroid injections on bone mineral density and bone turnover markers in patients taking anti-osteoporotic medications. Pain Physician. 2018;21:E435-E447.
- ↑ Al-Shoha A, Rao DS, Schilling J, Peterson E, Mandel S. Effect of epidural steroid injection on bone mineral density and markers of bone turnover in postmenopausal women. Spine. 2012;37:E1567-E1571.
- ↑ KimS, Hwang B. Relationship between bone mineral density and the frequent administration of epidural steroid injections in postmenopausal women with low back pain. Pain Res Manag. 2014;19:30-34.
- ↑ Kang SS, Hwang BM, Son H, Cheong IY, Lee SJ, Chung TY. Changes in bone mineral density in postmenopausal women treated with epidural steroid injections for lower back pain. Pain Physician. 2012;15: 229-236.
- ↑ Kim YU, Karm MH, Cheong Y, et al. Effect of epidural steroid injection on bone mineral density in postmenopausal women according to antiosteoporotic medication use. Pain Physician. 2016;19: 389-396.
- ↑ Sytsma, Terin T., et al. “Corticosteroid injections and risk of fracture.” JAMA network open 7.5 )2024(: e2414316-e2414316.
- ↑ Fischer, Matt, and Peggy Y. Kim. “Corticosteroid-induced psychosis after a single transforaminal epidural steroid injection.” WMJ 118.2 )2019(: 91-94.
- ↑ Benyamin, Ramsin M., et al. “Corticosteroid induced psychosis in the pain management setting.” Pain Physician 11.6 )2008(: 917-920.
- ↑ Malladi, Arundathi S., et al. “Recurrent adverse psychiatric effects following intra-articular corticosteroid injection.” JCR: Journal of Clinical Rheumatology 17.5 )2011(: 284-285.
- ↑ Deer, Timothy & Ranson, Matthew & Kapural, Leonardo & Diwan, Sudhir. )2009(. Guidelines for the proper use of epidural steroid injections for the chronic pain. Techniques in Regional Anesthesia and Pain Management. 13. 288-295. 10.1053/j.trap.2009.06.010.
- ↑ Chandra, Ronil V., et al. "Vertebroplasty and kyphoplasty for osteoporotic vertebral fractures: what are the latest data?." American Journal of Neuroradiology 39.5 )2018(: 798-806.
- ↑ G.C. Anselmetti et al. Pain relief following percutaneous vertebroplasty: Results of a series of 283 consecutive patients treated in a single institution Cardiovasc Intervent Radiol )2007(
- ↑ K. Ha et al. Causes of late revision surgery after bone cement augmentation in osteoporotic vertebral compression fractures Asian Spine J )2013(
- ↑ Pountos, Ippokratis, et al. “Pharmacological agents and impairment of fracture healing: what is the evidence?.” Injury 39.4 )2008(: 384-394.
- ↑ H0gevold, Hans E., Bjarne Gr0gaard, and Olav Reikeras. “Effects of short-term treatment with corticosteroids and indomethacin on bone healing: a mechanical study of osteotomies in rats.” Acta Orthopaedica Scandinavica 63.6 )1992(: 607-611.


 כניסה
כניסה  עקבו אחרינו בפייסבוק
עקבו אחרינו בפייסבוק